-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Přednemocniční aplikace transfuzních přípravků a krevních derivátů
Prehospital blood and blood products administration
The history of blood administration in injured patients in the prehospital care started early after the discovery of blood groups in the first decade of the 20th century. The first practical experiences were gained by army during World War I. During the 20th century blood products were not administered in the civilian prehospital care due to the risk of infectious disease transmission, transfusion reactions and donor deficiency. A rebirth of this method was seen at the beginning of the 21st century when the concept of remote damage control resuscitation was defined and blood became a part of hemostatic resuscitation. Different countries may use different blood products (whole blood, erythrocytes, plasma, fibrinogen, etc.) in prehospital treatment of a severely bleeding patient. Prehospital blood administration is feasible and safe. However, what is the most beneficial blood product for a patient with severe hemorrhagic-traumatic shock during the prehospital phase? This question is now explored in ongoing studies. This paper provides an overview of current policies for pre-hospital blood products administration.
Keywords:
prehospital blood transfusion – hemorrhagic-traumatic shock – damage control resuscitation
Autoři: J. Berková
Působiště autorů: Oddělení urgentní medicíny, Fakultní nemocnice Hradec Králové
Vyšlo v časopise: Rozhl. Chir., 2019, roč. 98, č. 12, s. 481-487.
Kategorie: Souhrnné sdělení
doi: https://doi.org/10.33699/PIS.2019.98.12.481–487Souhrn
Historie podání krve u poraněných pacientů v přednemocniční fázi začíná časně po objevu krevních skupin v prvním desetiletí 20. století. První praktické zkušenosti získávala armáda během 1. světové války. Díky riziku přenosu infekcí, transfuzním reakcím a nedostatku dárců nebyla krev v přednemocniční péči v civilním prostředí v průběhu 20. století rutinně využívána. Renesanci této metody přináší začátkem 21. století definovaný koncept remote damage control resuscitation, kdy se krev stává součástí hemostatické resuscitace. Různé státy mají k dispozici různé produkty (plnou krev, erytrocyty, plazmu, fibrinogen atd.), které využívají k léčbě závažně krvácejícího pacienta v přednemocniční péči. Podání krevní transfuze v přednemocniční fázi je proveditelné a bezpečné. Jaký produkt je však v přednemocniční fázi pro pacienta se závažným hemoragicko-traumatickým šokem ten nejvýhodnější, je otázkou nyní probíhajících studií. Toto sdělení přináší přehled současných možností aplikace krve a krevních derivátů v přednemocniční péči.
Klíčová slova:
přednemocniční transfuze – traumaticko-hemoragický šok – damage control resuscitation
Krvácení následkem závažného úrazu je nejčastější preventabilní příčina traumatického úmrtí, které typicky nastává v prvních třech hodinách od vzniku úrazu [1]. Efektivní léčba takového krvácení v přednemocniční fázi je závislá na rychlé identifikaci a kontrole zdroje závažného krvácení (použití přímého tlaku, turniketu, hemostatického obvazu, pánevního pásu, dlah), adekvátní oxygenaci pacienta, zajištění vstupu do cévního řečiště, hemostatické resuscitaci s cílem zabránit rozvoji traumatem indukované koagulopatie a rychlém transportu do adekvátního zdravotnického zařízení.
Použití krve v přednemocniční fázi péče o závažně poraněné pacienty má vliv na snížení rizika úmrtí na hemoragický šok ještě před přijetím takového pacienta do nemocnice. Koncepce tohoto použití v civilním prostředí vychází z historického vývoje aplikace plné krve nebo složek krve v prostředí vojenském. Aplikace transfuzních přípravků v přednemocniční fázi je součástí konceptu „Remote Damage Control Resuscitation“ (RDCR), tj. zahájení aplikace těchto přípravků ještě před branou nemocnice (traumacentra) [2].
Historie aplikace krve u traumat
Dokumentovaná historie prvních krevních převodů sahá do 15. století, pokusy však nekončily úspěšně. K velkému rozvoji krevní transfuze dochází v průběhu 20. století v návaznosti na objev krevních skupin a využití citrátu jako antikoagulans [3].
Karl Landsteiner publikoval v roce 1901 práci, ve které rozdělil lidskou krev do 3 skupin podle aglutinačních vlastností. V roce 1907 Jan Jánský publikoval práci, ve které rozdělil krevní skupiny do 4 skupin, které označil I, II, III a IV [3]. Až ve 30. letech 20. století byly krevní skupiny všeobecně označeny tak, jak je známe dnes – písmeny A, B, AB a 0. První krevní transfuze podle těchto poznatků byla podána v roce 1911. Následně byly objeveny další antigenní vlastnosti erytrocytů – systém MN v roce 1927, Rh faktor v roce 1941, po roce 1946 další označené jako Kell, Duffy, Kidd, Lutheran.
Již během 1. světové války se zkoušela podávat plná krev jako součást život zachraňujících postupů u zraněných vojáků se závažnou krevní ztrátou. Po vstupu USA do této války v roce 1917 bylo dokumentováno podání plné chlazené krve skupiny 0 na praporních obvazištích [4]. To byl impulz pro britské, kanadské a americké jednotky k zahájení zásobování polních zdravotnických pracovišť plnou krví skupiny 0.
Po zkušenostech z 1. světové války plánovaly americké jednotky využít k léčbě život ohrožujícího traumatického krvácení sušenou plazmu a albumin i během 2. světové války, bohužel se v prevenci traumaticko-hemoragického šoku tento postup neosvědčil. Britské jednotky zvolily k léčbě traumaticko-hemoragického šoku aplikaci plné krve s výrazně větším úspěchem. Proto je americká armáda následovala a byl ustanoven koncept bezprostředně dostupných dárců, tzv. „field blood banks“, s možností provést krevní převod okamžitě nebo krev odebrat a podat ji na vzdálenějším místě. Během 2. světové války byla využívána i lyofilizovaná plazma nebo plazma sušená sprejováním [5].
Podobné postupy přenesla americká armáda i do dalších konfliktů v Koreji a Vietnamu; navíc zde se začal uplatňovat koncept univerzálního dárce a podání plné krve skupiny 0 s nízkým titrem protilátek všem příjemcům, kteří neměli krevní skupinu 0.
V druhé polovině 70. let 20. století dochází k nahrazení krve v přednemocniční fázi náhradními roztoky krystaloidů (fyziologický roztok, Ringer-laktát) a koloidů (hydroxyetyl-škrob). K využívání krystaloidů a koloidů došlo částečně díky riziku přenosu infekčních nemocí a zčásti kvůli průkazu nutnosti zajištění perfuze tkání, která byla možná za použití krystaloidů [4].
V civilním přednemocničním prostředí v této době nebyla plná krev ani jiné transfuzní přípravky dostupné. K léčbě traumaticko-hemoragického šoku se používaly jednotlivé složky krve, zejména erytrocyty a trombocyty, ale až v nemocniční fázi ošetření poraněného pacienta. Koncept ATLS (Advanced Trauma Life Support) představený začátkem 80. let 20. století doporučoval zahájit resuscitaci krvácejícího pacienta bolusem 2000 ml krystaloidů. První podání transfuzní jednotky erytrocytů v přednemocniční péči bylo publikováno v roce 1985 [6].
Koncept použití krve v časné nemocniční fázi byl restituován během válečných konfliktů v Iráku a Afghánistánu v prvním desetiletí 21. století. To souviselo s uveřejněním konceptu Damage Control Resuscitation (DCR) v roce 2007 [7]. Tento koncept zahrnuje časné podávání transfuzních přípravků a současnou minimalizaci podávání krystaloidů, s cílem zabránit rozvoji traumatem indukované koagulopatie. V roce 2013 Holcomb et al. publikovali studii PROMMT (The Prospective, Observational, Multicenter, Major Trauma Transfusion Study: Comparative Effectiveness of a Time-varying Treatment with Competing Risks), která ukázala, že podání vyššího poměru plazmy a trombocytů při podání nejméně 3 jednotek erytrocytů v prvních 24 hod. od úrazu je spojeno se snížením mortality [8]. Následně publikovali studii PROPPR (Pragmatic, Randomized Optimal Platelet and Plazma Ratio), kde byl zkoumán adekvátní poměr podávaných jednotek erytrocytů, plazmy a trombocytů [9]. V této práci nebyl zjištěn signifikantní rozdíl v 24hodinové ani 30denní mortalitě při podání jednotlivých komponent v poměru 1 : 1:1 nebo 1 : 1:2, nicméně ve skupině s poměrem 1 : 1:1 v prvních 24 hod. dosáhlo více pacientů hemostázy a méně jich zemřelo v důsledku vykrvácení.
Se začátkem 21. století se začíná aplikace plné krve či transfuzních přípravků a krevních derivátů v přednemocniční fázi péče o pacienta se závažným krvácením přesouvat i do civilního sektoru jako součást RDCR.
Transfuzní přípravky
Transfuzní přípravek je individuálně vyrobený léčivý přípravek připravovaný v zařízení transfuzní služby odběrem krve od maximálně 10 dárců. Separací plné krve se vyrábějí jednotlivé transfuzní přípravky – koncentrát erytrocytů, koncentrát trombocytů, plazma a kryoprotein, který obsahuje fibrinogen a další koagulační faktory (faktor VIII, XIII a von Willebrandův faktor). Všechny tyto přípravky se využívají v léčbě život ohrožujícího krvácení vč. traumatického. Obecnými komplikacemi podání plné krve a transfuzních přípravků jsou posttransfuzní reakce vč. anafylaxe, přenos infekčních nemocí, riziko přetížení oběhu podanými transfuzními přípravky, hypokalcemie (v závislosti na počtu a druhu podaných transfuzních jednotek obsahujících citrát jako konzervant) a potransfuzní akutní poškození plic (TRALI). Použitelnost erytrocytů je 42 dnů. Čerstvě odebranou plazmu je možno hluboce zmrazit a uchovat několik let, po rozmražení je její použitelnost až 5 dnů. Trombocyty mají použitelnost 5–7 dnů při uskladnění v teplotách 20–24 °C, lze je také uchovávat zmrazené.
Aplikace plné krve vychází z jednoduchého konceptu: krvácející pacient ztrácí plnou krev, ne její jednotlivé složky; proto by tato ztráta měla být hrazena také plnou krví. Plná krev skladovaná při teplotách 2–6 °C ztrácí v průběhu několika dnů aktivitu koagulačních faktorů (hlavně F V a F VIII) a zhoršuje se v ní funkce trombocytů. Plná krev má vyvážený poměr erytrocytů, plazmy a trombocytů a menší poměr konzervantu ve srovnání s podáním jednotlivých složek krve v poměru 1 : 1:1 nebo 1 : 1:2 [4]. Její podání je lepší než podání krystaloidů [10]. Použití plné krve má kromě medicínských hlavně logistické výhody zejména pro přednemocniční složku a vojenské použití. Tato logistická výhoda spočívá v transportu a aplikaci jedné konzervy obsahující plnou krev místo dvou a více v případě podávání transfuzních přípravků a odpadá nutnost ředění a rozpouštění v případě aplikace fibrinogenu. Další výhodou oproti podání jednotlivých krevních složek je potřeba jednoho vstupu do cévního řečiště, na rozdíl od nutnosti zajištění 2 a více vstupů do cévního řečiště, pokud je potřeba podávat jednotlivé transfuzní přípravky současně. Vzhledem k ekonomické náročnosti využití plné krve se nyní jeví výhodnější separace darované krve na další transfuzní přípravky a krevní deriváty a jejich následná aplikace.
Podáním erytrocytů dochází ke zvýšení kapacity přenosu kyslíku, což krystaloidy neumějí. Pilotní studie prokázaly použitelnost podání erytrocytů a plazmy v přednemocniční fázi s nízkým rizikem znehodnocení nepoužitých jednotek [11]. Zlepšení přežití v prvních 24 hod. a závažnosti šoku při přijetí do traumacentra u pacientů, kterým v rámci přednemocniční fáze byly podány erytrocyty, ukazuje studie Browna et al. [12]. Recentně publikovaná studie z Velké Británie deklaruje snížení mortality, i když nesignifikantní, při přednemocničním podání erytrocytů ve srovnání s podáním krystaloidů [13]. Rehn et al. analyzují vliv zavedení přednemocniční aplikace erytrocytů do rutinní praxe londýnské letecké záchranné služby [14]. Výsledkem této práce je průkaz snížení celkového množství jednotek erytrocytů a snížení počtu dále podávaných jednotek čerstvě zmražené plazmy i trombocytů. Za bezpečnou považují přednemocniční aplikaci erytrocytů cestou letecké záchranné služby (LZS) i v Nizozemí. Ve studii nizozemských autorů nebylo prokázáno zlepšení přežití ani snížení výskytu šoku, ale podle závěrů práce je potřeba dalších studií k prokázání časného efektu podaných erytrocytů na přežití [15].
Aplikace plazmy zmírňuje traumatem indukovanou koagulopatii tím, že obsahuje fibrinogen a další koagulační faktory; chrání endoteliální glykokalyx, čímž snižuje cévní permeabilitu [16]. K dispozici je čerstvě zmražená plazma (ČZP), kterou je před použitím nutné rozmrazit. V případě masivního krvácení se ČZP podává v dávce 10–20 ml/kg. Chlazená plazma se používá výjimečně a jen v několika zemích, její doba použitelnosti je obvykle 14 dnů. K dispozici je také lyofilizovaná plazma, případně sprejově sušená plazma. Lyofilizovaná plazma je na civilním trhu velmi obtížně dostupná, využívají ji např. francouzská armáda, letecká záchranná služba v Norsku a dále je k dispozici v Německu, Izraeli, Jihoafrické republice [17]. Její použitelnost je až 2 roky a skladuje se při pokojové teplotě, což je její největší výhodou oproti výše uvedeným preparátům. Její příprava k aplikaci trvá 3–6 min. Lyofilizovaná plazma má stejné riziko přenosu infekce jako ČZP. Ve studii Sperryho et al. PAMPer, která srovnávala přednostní použití rozmražené plazmy v přednemocniční fázi u pacientů s traumatickým hemoragickým šokem proti podání krystaloidů samotných nebo v kombinaci s erytrocyty, bylo prokázáno, že aplikace ČZP signifikantně neprodlužuje přednemocniční čas a snižuje 30denní mortalitu [16]. Studie izraelských autorů potvrzuje použitelnost lyofilizované plazmy na místě úrazu v přednemocniční fázi [18]. V další studii lokalizované do městské aglomerace oproti tomu bylo prokázáno, že pokud transportní čas do nejbližšího traumacentra je kratší než 19 minut, nemá přednemocniční aplikace plazmy vliv na přežití [19]. Pro možnost využití přednemocničního podání transfuzních přípravků (erytrocytů a plazmy) hovoří velká multicentrická studie Holcomba et al. PROHS (Prehospital Resuscitation on Helicopter Study), medián trvání aplikace transfuzních přípravků při leteckém transportu je 18 min. a nezvyšuje mortalitu pacientů [20]. Nguyen et al. porovnávali možnost použití francouzské lyofilizované plazmy a ČZP v rámci zahájení masivního transfuzního protokolu, dle jejich výsledků je lyofilizovaná plazma vhodnou alternativou ČZP, a nabízí se tedy možnost jejího užití v přednemocniční fázi [17].
Trombocyty se v přednemocniční fázi managementu závažného traumatického krvácení kvůli náročné logistice jejich skladování a trvanlivosti využívají málo (např. v oblasti Mayo Clinic) [21]. Své místo mají v časné nemocniční fázi.
Krevní deriváty
Krevní deriváty jsou hromadně vyráběné léčebné přípravky vzniklé zpracováním plazmy tisíců dárců ve frakcionačních centrech, nebo se vyrábějí za použití biotechnologických postupů (rekombinantní přípravky). Mezi krevní deriváty se řadí albumin, fibrinogen, koncentrát protrombinového komplexu (PCC), rekombinantní faktor VIIa, VIII, IX a faktor XIII. Výhodou všech těchto derivátů je prakticky okamžitá dostupnost v rámci nemocnice a dlouhá doba použitelnosti. Výraznou nevýhodou je jejich finanční náročnost, částečnou limitací relativně pomalé zahájení aplikace (musejí se rozpouštět několik minut). PCC, rekombinantní faktor VIIa a XIII se využívají pro pokračující na míru šitou léčbu život ohrožujícího krvácení podle aktuálních výsledků viskoelastických metod krevního srážení.
Z těchto důvodů se jako jediný pro možné použití v přednemocniční fázi jeví fibrinogen. Fibrinogen se vyrábí derivací plazmy jako koncentrát. Proč používat zrovna fibrinogen v rámci přednemocniční fáze, ukazuje studie Inaby, která detekovala, že do traumacentra přijíždí až 65 % pacientů s nízkou nebo kritickou hladinou fibrinogenu [22]. Pacienti s kritickou hodnotou fibrinogenu mají signifikantně vyšší mortalitu v průběhu hospitalizace. Podle současných evropských doporučení pro léčbu život ohrožujícího traumatického krvácení by každý závažně krvácející pacient měl dostat 3–4 g fibrinogenu nebo 50 mg/kg kryoprecipitátu [23]. Recentně byla v Evropě (Rakousko, Německo, ČR – Zdravotnická záchranná služba Libereckého kraje) ukončena multicentrická randomizovaná dvojitě slepá studie FIinTIC (Fibrinogen in Trauma Induced Coagulopathy), jejímž cílem je zhodnocení vlivu v přednemocniční fázi podaného koncentrátu fibrinogenu v dávce 50 mg/kg na změny koagulačních parametrů (hodnocení MCF pomocí viskoelastické metody FIBTEM), množství podaných transfuzních přípravků a tromboembolické komplikace [24]. Její výsledky nebyly zatím publikovány.
V současné době není v databázi dostupná žádná studie zabývající se vlivem fibrinogenu podaného v přednemocniční fázi. Studie prováděné v rámci časné nemocniční fáze doporučují podání fibrinogenu při jeho nízké hladině co nejdříve od přijetí pacienta do nemocnice a nejlépe za předpokladu vyšetření hladiny pomocí viskoelastických metod [25]. Britská studie E-FIT 1 udává, že ne vždy lze dodržet co nejčasnější čas aplikace fibrinogenu při příjmu do nemocnice [26]. Problém se zdá být v rychlosti rozpouštění, který nebyl většinou udávaných 10 min., ale medián rychlosti rozpuštění byl 23 min. Ve studii nezaznamenali trombofilní komplikace při podání fibrinogenu.
Kyselina tranexamová
Kyselina tranexamová (TXA) je syntetický analog aminokyseliny lyzin, který má schopnost inhibovat fibrinolýzu díky blokování vazby plazminogenu na fibrin.
Ve srovnání s ostatním produkty se jedná o velmi levný preparát. Finanční hledisko a snadnost aplikace (stačí 2 ampule naředit do 100 ml fyziologického roztoku a podávat 10 min.) z něj dělá vhodný preparát pro přednemocniční péči v porovnání např. s fibrinogenem. Při podání TXA v přednemocniční nebo časné nemocniční fázi je nutné opakovat podání 1 g intravenózně za 8 hod.
Podle současného evropského doporučení pro život ohrožující traumatické krvácení v civilním prostředí, které vychází ze závěrů studie CRASH-2, se doporučuje podání TXA v množství 1 g do 3 hod. od vzniku úrazu [27]. Ovšem ve vyspělých civilních traumasystémech není její podání asociováno se snížením mortality během hospitalizace [28]. Na základě studií CRASH-2 a MATTERs je TXA součástí managementu život ohrožujícího krvácení v konceptu RDCR také ve vojenském prostředí. V současnosti se i zde diskutuje o přehodnocení pokynů k použití TXA pro riziko tromboembolické nemoci [29].
Současná praxe přednemocničního podávání transfuzních přípravků a krevních derivátů
V současné době není v přednemocniční péči použití transfuzních přípravků běžné. V civilním sektoru je plná krev k dispozici v traumacentrech nemocnic na několika různých místech po celém světě, nicméně v přednemocniční péči je využívána výrazně méně (vybrané lokality v USA, Kanadě, Austrálii, Norsku, Francii a Izraeli). Mnohem rozšířenější je využití jednotlivých složek krve v rámci časné nemocniční péče o závažně poraněného pacienta. V rámci přednemocniční péče je jejich využití nižší, spíše výjimečně je aplikují pozemní, častěji letecké složky zdravotnické záchranné služby (ZZS).
Ve spádové oblasti traumacentra Mayo Clinic v USA využívá LZS již několik let transfuzní přípravky v přednemocniční fázi, v poslední době také plnou krev [21]. Transportní box obsahuje jednu jednotku chlazené plné krve skupiny 0, jednu jednotku chlazených trombocytů, dvě jednotky erytrocytů 0 negativní a dvě jednotky rozmražené plazmy skupiny A. Cílem jejich výzkumu bylo zjistit, který transfuzní přípravek podat jako první.
Od roku 2017 používají plnou krev s nízkým titrem protilátek pozemní přednemocniční složky v okolí Houstonu a od roku 2018 v oblasti San Antonio, Texas, USA, kde funguje celý strategický program zahrnující indikaci aplikace krve, rotaci přípravků a nábor dárců [30].
V Pensylvánii byla v listopadu 2018 zahájena prospektivní randomizovaná studie Pragmatic Prehospital Group O Whole Blood Early Resuscitation Trial (PPOWER), jejímž cílem je porovnání mortality a morbidity při přednemocničním podání 2 jednotek plné krve s nízkým titrem protilátek a standardní léčby transfuzními přípravky v poměru 1 : 1:1 [31].
V Austrálii podávají erytrocyty a čerstvě zmraženou plazmu. Po schválení lékařem mohou erytrocyty 0 Rh negativní podat i záchranáři LZS [32].
Ve Velké Británii byla zahájena aplikace erytrocytů v roce 2012 prostřednictvím LZS v Londýně [14], dále v roce 2013 na LZS v oblasti jihovýchodní Anglie. Indikací k podání byl těžký hemoragický šok v důsledku traumatu, u tupých traumat nehmatný pulz na a. radialis u ventilovaných pacientů, u penetrujících traumat trupu nutnost udržení hmatného pulzu centrálně [33]. Toto podání mělo za výsledek signifikantní snížení času podání první jednotky erytrocytů a potvrdilo proveditelnost aplikace erytrocytů v přednemocniční fázi v civilním prostředí. V současnosti probíhá ve Velké Británii multicentrická randomizovaná studie ReFILL (Resuscitation with Pre-Hospital Blood Products) [34], jejímž cílem je srovnání přednemocniční aplikace 2 jednotek erytrocytů a 2 jednotek lyofilizované plazmy vs. standardní péče o závažně poraněného pacienta a vlivu na zlepšení tkáňové perfuze a snížení mortality. Studie byla zahájena v roce 2016 a její ukončení je naplánováno v roce 2020.
V Norsku používá LZS od roku 2013 lyofilizovanou plazmu [35], v roce 2014 byly přidány erytrocyty a od roku 2015 mají možnost aplikovat plnou krev s nízkým titrem protilátek. Nyní zde probíhá studie PRoHEMS [36].
V roce 2018 byla publikována proveditelnost a bezpečnost podání erytrocytů a lyofilizované plazmy v přednemocniční fázi péče o závažně krvácející pacienty ve Švédsku, tyto produkty podává LZS od roku 2016 [37]. Stejné zkušenosti s podáváním erytrocytů a lyofilizované plazmy mají v Nizozemí [38].
Použití transfuzních přípravků ve Francii v civilním sektoru kopíruje jejich použití v sektoru vojenském. V civilním sektoru se používají výhradně pro vzdálené destinace (např. polární základny) a prolongované transporty. Z dostupných preparátů se využívá lyofilizovaná plazma vlastní provenience. Od roku 2016 probíhá ve Francii studie PREHO-PLYO, která chce zhodnotit vliv podání lyofilizované plazmy na prevenci a léčbu hemoragickým šokem asociované koagulopatie [39].
Také ve Španělsku se pilotně zkouší podávat erytrocyty a fibrinogen, nyní zde probíhá studie s cílem porovnat vliv přednemocničního podání erytrocytů, TXA a fibrinogenu proti standardnímu podávání krystaloidů a TXA na traumatem indukovanou koagulopatii – studie PRETIC (Transfusion of Red Blood Cells, Tranexamic Acid and Fibrinogen Concentrate for Severe Trauma Hemorrhage at Pre-hospital Phase of Care).
V Izraeli začala být používána od roku 2011 v civilní ZZS lyofilizovaná plazma, do té doby nebyly používány žádné transfuzní přípravky [19]. Izraelská armáda využívá plnou krev od civilních dárců.
Zajímavou lokalitou, která má možnost aplikace plné krve od roku 2009, jsou zaoceánské lodi [21]. Lékařský personál na těchto lodích pracuje s „dárci“, kteří se plaví na téže lodi a jsou v případě potřeby požádáni o darování krve. Jedná se o koncept „Walking blood bank“ používaný hlavně ve válečných konfliktech, ale i na odlehlých místech nezasažených válkou. Jde o odběr plné krve předem vyšetřenému dárci nacházejícímu se v blízkosti postiženého a její bezprostřední podání jako součást život zachraňující léčby. Od zahájení používání tohoto principu byla plná krev podána 73 pacientům. Většinou se jednalo o netraumatické krvácení jako komplikaci antiagregační nebo antikoagulační léčby.
V ČR v současnosti probíhají pilotní programy v aplikaci transfuzních přípravků nebo krevních derivátů v přednemocniční fázi. Letecká výjezdová skupina ZZS hlavního města Prahy poraněným pacientům se známkami hemoragického šoku III. a/nebo IV. stupně aplikuje 2 g fibrinogenu, pacienti jsou následně transportováni do některého z pražských traumacenter.
Na aplikaci fibrinogenu se zaměřila také ZZS Kraje Vysočina, aplikují 4 g fibrinogenu, pacienty pak předávají do traumacentra Fakultní nemocnice Brno Bohunice, kde následně hodnotí vliv podaného fibrinogenu v přednemocniční fázi na traumatem indukovanou koagulopatii (studie TICAF – Incidence of Trauma Induced Coagulopathy in Patient with Prehospital Administration of Fibrinogen).
Studie RABBIT (Rapid Administration of Blood by HEMS in Trauma) probíhající nyní za spolupráce letecké výjezdové skupiny ZZS Královéhradeckého kraje a traumacentra Fakultní nemocnice Hradec Králové (FN HK) pracuje v konceptu RDCR, závažně poraněným pacientům je v přednemocniční fázi aplikována jedna jednotka rozmražené plazmy, následovaná podáním jedné jednotky erytrocytů. Transfuzní přípravky jsou LZS vydávány na základě schválení Státního ústavu pro kontrolu léčiv a Etické komise FN HK v souladu s gescí zákona č. 378/2007 Sb., o léčivech v platném znění (§ 67, odst. 4k a 5c). Pacient je transportován do traumacentra FN HK, kde se při potvrzení život ohrožujícího krvácení pokračuje v podávání masivního transfuzního protokolu. V současnosti nejsou k dispozici ani předběžné výsledky žádného z výše uvedených probíhajících projektů.
Plnou krev v ČR zatím nepodává žádná ZZS ani traumacentrum. Nejdál v přípravě civilního sektoru k aplikaci plné krve, zatím v nemocničním prostředí, je Ústřední vojenská nemocnice – Vojenská fakultní nemocnice Praha, hlavně díky zkušenostem s aplikací plné krve u traumat ze zahraničních válečných misí [40].
V Tab. 1 je uveden přehled v současné době recentně ukončených nebo probíhajících studií zabývajících se přednemocniční aplikací transfuzních přípravků či krevních derivátů s termíny jejich ukončení.
Tab. 1. Přehled vybraných studií s tématem přednemocniční aplikace transfuzních přípravků a krevních derivátů
Tab. 1. Overview of selected studies concerning pre-hospital blood or blood products administration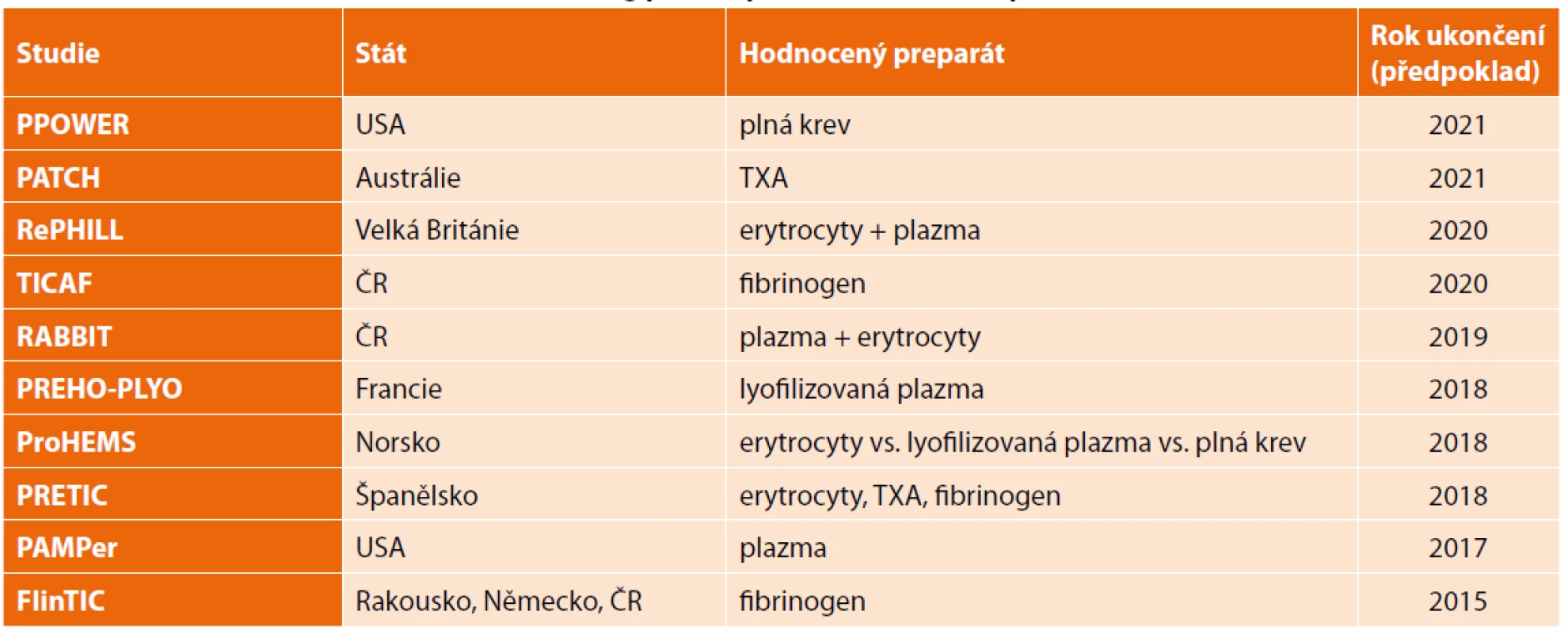
Závěr
Léčba závažně krvácejícího pacienta zahrnuje v přednemocniční fázi zástavu masivního zevního krvácení pomocí přímého tlaku, hemostatického obvazu nebo turniketu, zmírnění vnitřního krvácení pomocí pánevního pásu a dlahování zlomenin dlouhých kostí a přednostní transport do adekvátního zdravotnického zařízení. Součástí hemostatické resuscitace závažně traumaticky krvácejícího pacienta je také minimalizace podávání krystaloidů a aplikace transfuzních přípravků a krevních derivátů. V současné době probíhá několik studií v různých zemích včetně České republiky, které se zabývají možností přednemocničního podávání transfuzních přípravků nebo krevních derivátů. Zatím dostupné výsledky ukazují, že podání plné krve a/nebo plazmy a erytrocytů je v přednemocniční fázi proveditelné a bezpečné. Jaký transfuzní přípravek nebo krevní derivát bude za daných okolností v přednemocniční fázi ten nejvhodnější, ukážou postupně výsledky probíhajících studií.
Seznam zkratek
ATLS – Advanced Trauma Life Support
DCR – Damage Control Resuscitation
ČZP – čerstvě zmražená plazma
FIBTEM – fibrinogen tromboelastometrie
FN HK – Fakultní nemocnice Hradec Králové
LZS – letecká záchranná služba
MCF – maximum clot firmness (maximálního hodnota pevnosti koagula)
PCC – prothrombin complex concentrate (koncentrát protrombinového komplexu)
RDCR – Remote Damage Control Resuscitation
TRALI – transfusion-related acute lung injury
TXA – kyselina tranexamová
ZZS – zdravotnická záchranná služba
Podpořeno MZ ČR – RVO (FNHK, 00179906)
Konflikt zájmů
Autoři článku prohlašují, že nejsou v souvislosti se vznikem tohoto článku ve střetu zájmů a že tento článek nebyl publikován v žádném jiném časopise.
MUDr. Jana Berková
Oddělení urgentní medicíny
Fakultní nemocnice Hradec Králové
Sokolská 581
500 05 Hradec Králové
e-mail: jana.berkova@fnhk.cz
Zdroje
- Davenport R. Haemorrhage control of the pre-hospital trauma patient. Scan J Trauma Resus. 2014;22(S1). doi: 10.1186/1757-7241-22-S1-A4.
- Naumann DN, Khan MA, Smith JE, et al. Future strategies for remote damage control resuscitation after traumatic hemorrhage. J Trauma Acute Care Surg. 2019;86 : 163–6. doi: 10.1097/TA.0000000000002080.
- Marešová J. Historie a současnost transfuze krve (v intencích vývoje transfuzního oddělení Fakultní nemocnice v Hradci Králové). Bakalářská práce. Univerzita Karlova v Praze, Farmaceutická fakulta v Hradci Králové 2014.
- Spinella PC, Pidcoke HF, Strandenes G, et al. Whole blood for hemostatic resuscitation of major bleeding. Transfusion 2016;56 : 190–202. doi: 10.1111/trf.13491.
- Inaba K. Freeze-Dried Plasma. J Trauma 2011;70 : 57–8. doi: 10.1097/TA.0b013e31821a6057.
- Smith IM, James RH, Dretzke J, et al. Prehospital blood product resuscitation for trauma. Shock 2016;46 : 3–16. doi: 10.1097/SHK.0000000000000569.
- Holcom JB. Damage control resuscitation. J Trauma 2007;62(Suppl):36–7. doi: 10.1097/TA.0b013e3180654134.
- Holcom JB, Del Junco DJ, Fox EE, et al. The prospective, observational, multicenter, major trauma transfusion (PROMMTT) study. JAMA Surg. 2013;148 : 127–36. doi: 10.1001/2013.jamasurg.387.
- Holcomb JB, Tilley BC, Baraniuk S, et al. Transfusion of plasma, platelets, and red blood cells in a 1 : 1. JAMA 2015;313 : 471–82. doi: 10.1001/jama.2015.12.
- Woolley T, Thompson P, Kirkman E, et al. Trauma hemostasis and oxygenation research network position paper on the role of hypotensive resuscitation as part of remote damage control resuscitation. J Trauma Acute Care Surg. 2018;84 : 3–13. doi: 10.1097/TA.0000000000001856.
- Dretzke J, Smith IM, James RH, et al. Protocol for a systematic review of the clinical effectiveness of pre-hospital blood components compared to other resuscitative fluids in patients with major traumatic haemorrhage. Systematic Reviews 2014;3 : 123. doi: 10.1186/2046-4053-3-123.
- Brown JB, Sperry JL, Fombona A, et al. Pre-trauma center red blood cell transfusion is associated with improved early outcomes in air medical trauma patients. J Am Coll Surg. 2015;220 : 797–808. doi: 10.1016/j.jamcollsurg.2015.01.006.
- Griggs JE, Jeyanathan J, Joy M, et al. Mortality of civilian patients with suspected traumatic haemorrhage receiving pre-hospital transfusion of packed red blood cells compared to pre-hospital crystalloid. Scan J Trauma Resus. 2018;26 : 100. doi: 10.1186/s13049-018-0567-1.
- Rehn M, Weaver AE, Eshelby S, et al. Pre-hospital transfusion of red blood cells in civilian trauma patients. Transfusion Med. 2018;28 : 27–83. doi: 10.1111/tme.12483.
- Peters JH, Smulders PSH, Moors XRJ, et al. Are on-scene blood transfusions by a helicopter emergency medical service useful and safe? A multicentre case–control study. Eur J Trauma Emerg Surg. 2019;26 : 128–32. doi: 10.1097/MEJ.0000000000000516.
- Sperry JL, Guyette FX, Brown JB, et al. Prehospital plasma during air medical transport in trauma patients at risk for hemorrhagic shock. New Eng J Med. 2018;379 : 315–26. doi: 10.1056/NEJMoa1802345.
- Nguyen C, Bordes J, Cungi PJ, et al. Use of French lyophilized plasma transfusion in severe trauma patients is associated with an early plasma transfusion and early transfusion ratio improvement. J Trauma Acute Care Surg. 2018;84 : 780–5. doi: 10.1097/TA.0000000000001801.
- Shlaifer A, Siman-Tov M, Radomislensky I, et al. Prehospital administration of freeze-dried plasma, is it the solution for trauma casualties? J Trauma Acute Care Surg. 2017;83 : 675–82. doi: 10.1097/TA.0000000000001569.
- Moore HB, Moore EE, Chapman MP, et al. Plasma-first resuscitation to treat haemorrhagic shock during emergency ground transportation in an urban area: a randomised trial. Lancet 2018;392 : 283–91. doi: 10.1016/S0140-6736(18)31553-8.
- Holcomb JB, Swartz MD, Desantis SM, et al. Multicenter observational prehospital resuscitation on helicopter study. J Trauma Acute Care Surg. 2017;83 : 83–91. doi: 10.1097/TA.0000000000001484.
- Zielinski MD, Stubbs JR, Berns KS, et al. Prehospital blood transfusion programs. J Trauma Acute Care Surg. 2017;82 : 70–78. doi: 10.1097/TA.0000000000001427.
- Inaba K, Karamanos E, Lustenberger T, et al. Impact of fibrinogen levels on outcomes after acute injury in patients requiring a massive transfusion. J Am Coll Surg. 2013;216 : 290–7. doi: 10.1016/j.jamcollsurg.2012.10.017.
- Rossaint R, Bouillon B, Cerny V, et al. The European guideline on management of major bleeding and coagulopathy following trauma: fourth edition. Crit Care 2016;20 : 98. doi: 10.1186/s13054-016-1265-x.
- Maegele M, Zinser M, Schlimp C, et al. Injectable hemostatic adjuncts in trauma. J Trauma Acute Care Surg. 2015;78 : 76–82. doi: 10.1097/TA.0000000000000632.
- Yamamoto K, Yamaguchi A, Sawano M, et al. Pre-emptive administration of fibrinogen concentrate contributes to improved prognosis in patients with severe trauma. Trauma Surg Acute Care Open 2016;1: e000037. doi: 10.1136/tsaco-2016-000037.
- Curry N, Foley C, Wong H, et al. Early fibrinogen concentrate therapy for major haemorrhage in trauma (E-FIT 1): results from a UK multi-centre, randomised, double blind, placebo-controlled pilot trial. Crit Care 2018;22 : 164. doi: 10.1186/s13054-018-2086-x.
- Spahn DR, Bouillon B, Cerny V, et al. The European guideline on management of major bleeding and coagulopathy following trauma: fifth edition. Crit Care 2019;23 : 98. doi: 10.1186/s13054-019-2347-3.
- Boutonnet M, Abback P, Le Saché F, et al. Tranexamic acid in severe trauma patients managed in a mature trauma care system. J Trauma Acute Care Surg. 2018;84 : 54–62. doi: 10.1097/TA.0000000000001880.
- Johnston LR, Rodrigues CJ, Elster EA, et al. Evaluation of military use of tranexamic acid and associated thromboembolic events. JAMA Surg. 2018;153 : 169–75. [On line]. doi:10.1001/jamasurg.2017.3821. https://www.strac.org/blood.
- Sperry J. Pragmatic Prehospital Group 0 Whole Blood Early Resuscitation Trial (PPOWER). Clinicaltrials.gov [online]. Bethesda: NIH NLM, 2018 [cit. 2019-05-04]. Available from https://clinicaltrials.gov/ct2/show/NCT03477006.
- Heschl S, Andrew E, De Wit A, et al. Prehospital transfusion of red cell concentrates in a paramedic-staffed helicopter emergency medical service. Emerg Med Australas 2018;30 : 236–41. doi: 10.1111/1742-6723.12910.
- Lyon RM, De Sausmarez E, McWhirter E, et al. Pre-hospital transfusion of packed red blood cells in 147 patients from a UK helicopter emergency medical service. Scan J Trauma Resus. 2017;25. doi: 10.1186/s13049-017-0356-2.
- Smith IM, Crombie N, Bishop JR, et al. RePHILL: protocol for a randomised controlled trial of pre-hospital blood product resuscitation for trauma. Transfusion Med. 2018;28 : 346–56. doi: 10.1111/tme.12486.
- Sunde GA, Vikenes B, Strandenes G, et al. Freeze dried plasma and fresh red blood cells for civilian prehospital hemorrhagic shock resuscitation. J Trauma Acute Care Surg. 2015;78 : 26–30. doi: 10.1097/TA.0000000000000633.
- Sunde GA. Norway – update on blood products pre-hospital. In: The THOR network [online]. Available from: https://rdcr.org/wp-content/uploads/2016/07/08-SUNDE-Norway-update-on-blood-products-pre-hospital-Geir-Arne-Sunde.pdf.
- Sato Folatre JG, Arnell P, Henning M. Introduction of prehospital blood transfusion programme in Sweden: experiences from a physician staffed helicopter emergency medical service. [In Swedish], Läkartidningen 2018 : 115.
- Peters JH, Smulders PSH, Moors XRJ, et al. Are on-scene blood transfusions by a helicopter emergency medical service useful and safe? A multicentre case–control study. Eur J Trauma Emerg Surg. 2019;26 : 128–32. doi: 10.1097/MEJ.0000000000000516.
- Martinaud C. French Dried Plasma Program – update on prehospital and emergency unit use for massive hemorrhage management. In: The THOR network [online] 2017. Available from: https://rdcr.org/wp-content/uploads/2017/07/08-Martinaud-THOR-2017.compressed.pdf.
- Bohoněk M. RCDR a koncept „Blood far forward“ jako aktuální výzva. [přednáška]. Praha 12. Střešovický transfuzní den – „Plná krev se vrací“ 15.11.2018.
Štítky
Chirurgie všeobecná Ortopedie Urgentní medicína
Článek vyšel v časopiseRozhledy v chirurgii
Nejčtenější tento týden
2019 Číslo 12- U pacientů s traumatem je častěji dosaženo adekvátních hladin anti-Xa při dávkování enoxaparinu podle hmotnosti
- Spolehlivý systém skórování jizev k hodnocení fotografií popálenin
- Nedostatečné dávkování enoxaparinu je u pacientů po ortopedickém výkonu časté a zvyšuje riziko tromboembolické nemoci
- Spasmolytický účinek metamizolu
-
Všechny články tohoto čísla
- Odběr tukové tkáně při dárcovské nefrektomii; chirurgický model pro výzkum aterosklerózy
- Přednemocniční aplikace transfuzních přípravků a krevních derivátů
- Léčba poranění jater v traumacentru Fakultní nemocnice Plzeň
- Načasování cholecystektomie v terapii akutní kalkulózní cholecystitidy
- Dva typy autologních buněk v prevenci vytvoření striktury po kompletní cirkulární endoskopické disekci u miniprasete
- Extraperitoneální fixace sleziny je vhodné řešení pro bloudivou slezinu u dětí a adolescentů – kazuistika
- Cholangioskopie a intraduktální sonografie v diagnostice karcinomu žlučových cest
- United European Gastroenterology Week – UEGW 2019
- Zápis z jednání schůze Redakční rady časopisu Rozhledy v chirurgii, konané dne 6. 11. 2019
- Rozhledy v chirurgii
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Načasování cholecystektomie v terapii akutní kalkulózní cholecystitidy
- Přednemocniční aplikace transfuzních přípravků a krevních derivátů
- Léčba poranění jater v traumacentru Fakultní nemocnice Plzeň
- Cholangioskopie a intraduktální sonografie v diagnostice karcinomu žlučových cest
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: MUDr. Petr Výborný, CSc., FEBO
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



