-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Klostridiová flegmóna břišní stěny u obézní pacientky s Crohnovou chorobou
Clostridial phlegmona of the abdominal wall in an obese patient with Crohn’s disease
Clostridial infection represents a serious chapter in the field of surgery. Infections of soft tissue caused by clostridial infection often end in death despite the early diagnosis and appropriate treatment. Authors present a case history of a young overweight patient, immunologically compromised, after a recent biological treatment for Crohn’s disease. The patient developed extensive clostridial cellulitis of the abdominal wall as well as of the proximal part of her lower limb following a banal skin wound. Despite resuscitation and surgical care, the patient died. When treating soft tissue infections, it is particularly important to consider the possibility of an anaerobe infection.
Keywords:
clostridial cellulitis – gas gangrene – Clostridium ramosum – Clostridium tertium
Autoři: K. Chrz; R. Fraško
Působiště autorů: 1. chirurgická klinika hrudní, břišní a úrazové chirurgie VFN ; Přednosta: prof. MUDr. Zdeněk Krška, DrSc. ; 1. lékařská fakulta Univerzity Karlovy
Vyšlo v časopise: Prakt. Lék. 2015; 95(1): 36-41
Kategorie: Kazuistika
Souhrn
Klostridiové infekce představují vážnou kapitolu v chirurgii. Přes včasnou diagnostiku a adekvátní terapii jimi způsobeného postižení měkkých tkání končí často infaustně. Autoři předkládají kazuistiku mladé obézní nemocné, imunologicky kompromitované, po recentně nasazené biologické léčbě pro Crohnovu chorobu. U nemocné se rozvinula rozsáhlá klostridiová epifasciální flegmóna břišní stěny a proximální části pravé dolní končetiny. I přes intenzivní resuscitační a chirurgickou péči vedla ke smrti nemocné. Důležité v diagnostice a léčbě infekcí měkkých tkání je především myslet na možnost anaerobní infekce.
Klíčová slova:
plynatá sněť – klostridiová celulitida – Clostridium ramosum – Clostridium tertiumÚVOD
Klostridia způsobují, vedle prosté kontaminace měkkých tkání, závažná onemocnění. Od klostridiové kontaminace, epifasciální klostridiovou flegmónu měkkých tkání přes fulminantně probíhající tkáňovou myonekrózu až po toxémii a multiorgánové selhání. Epifasciální klostridiová flegmóna, která probíhá obvykle perakutně, bez náležité terapie vykazuje 100% letalitu.
Klostridia jsou obecně gram-pozitivní bakterie se schopností tvorby spor. Jsou vysoce citlivé na přítomný kyslík. Vegetativní buňky mají tvar tyčky, spory jsou oválné. V přírodě jsou hojně rozšířeny (v rybnících, v říčních i mořských březích, v půdě). Řadu druhů klostridií lze nalézt v tlustém střevě obratlovců, včetně člověka. Klidové, sporulující formy se nemnoží a jsou vysoce odolné. Jejich jaderná hmota je kryta více obaly, které jim zajišťují odolnost vůči teplu, vyschnutí i dezinfekčním prostředkům.
Vegetativní formy klostridií jsou naopak schopny rychlého množení a jsou vysoce citlivé na kyslík díky absenci kataláz, cytochromů a peroxidáz. Vzniklé peroxidy a superoxidy nemohou být bakterií rozloženy a bakteriální buňku zničí (1). Povrch klostridií obsahuje velké množství antigenů, jež lze využít pro jejich identifikaci například pomocí imunofluorescenčního testu.
Klostridiové buňky produkují toxiny (2), které můžeme rozdělit na endotoxiny a exotoxiny. Endotoxiny se uvolňují až po rozpadu buňky a jsou svojí stavbou lipopolysacharidy. Exotoxiny jsou difuzibilní polypeptidy, které buňka kontinuálně produkuje. Exotoxiny jsou termolabilnější než endotoxiny, ale zároveň jsou toxičtější. Na jejich přítomnost reaguje tělo tvorbou protilátek (antitoxinů). Tyto antitoxiny lze též využít k identifikaci. Některé toxiny se po částečné denaturaci (např. formaldehydem) mění v toxoidy, které již nemají toxický účinek a v určitých případech (toxoid Clostridium tetani) je lze využít k léčbě a profylaxi onemocnění. Klostridie vyvolávají tři typy infekcí (3):
- Neuroinfekce jsou nejčastěji způsobeny C. tetani a C. botulinum.
- Nekrotizující fascitidu a myositidu a infekci nitrobřišních orgánů obsahujících svalovinu nejčastěji způsobují (histotoxické klostridie) C. perfringens, C. septikum a C. novyi.
- Klostridové infekce lokalizované ve střevě jsou nejčastěji způsobeny C. perfringens a C. difficile.
Klostridiová plynatá sněť je rychle se šířící proces primárně lokalizovaný v podkoží, eventuálně v prostoru mezi svaly, které primárně napadeny nejsou. K jejich nekróze může dojít po narušení aponeurózy. Produkovaný plyn se tedy typicky objevuje pouze v postižených kompartmentech. Zde také může být klinicky a rentgenologicky verifikován. Zánětlivý proces však může postupovat zpočátku bez výraznějších změn na kožním krytu, a to velkou rychlostí – až 2 cm za hodinu, septický šok může nastat už během prvních 12 hodin od počátku infekce (4).
Léčba musí být vždy rychlá, komplexní. Základem úspěšné terapie jsou po stanovení včasné diagnózy (do 2 hodin) tři opatření:
- Chirurgický výkon, který musí být radikální. Je nutné odstranit veškeré nekrotické tkáně a otevřít případné choboty. Radikalita je nutná i za cenu značných ztrát tkání, nezřídka je nutné přistoupit k amputacím.
- Antibiotická terapie jednak vychází z empirických zkušeností, kdy je doporučován krystalický penicilin v dávce 5 mil. j. i.v. ve 100 ml fyziologického roztoku každé 4 hodiny a současně Klindamycin 600–900 mg v 250 ml F1/1 i.v. každých 6 hodin (5). Je nutné odebírat histologické a bakteriologické vzorky a promptně reagovat na změny citlivosti, případně na přítomnost dalších bakterií.
- Celková intenzivní léčba spočívá v uložení nemocného na monitorované lůžko charakteru JIP, péči o vnitřní prostředí, zajištění oběhové podpory, oxygenoterapie apod.
Podání antigangrenózního séra je již obsoletní metodou pro jeho nedostatečnou účinnost a těžké alergické reakce (5). Celosvětově byl postupně vyřazen z doporučených postupů. Jeho výroba byla ukončena a nyní již není v České republice ani v okolních zemích k dispozici. Antigangrenózní sérum se připravovalo imunizací koní přípravky obsahujícími toxiny pěti nejvýznamnějších druhů klostridií.
VLASTNÍ POZOROVÁNÍ
Nemocná, stáří 26 let, obézní s BMI 32,6, léčená cca 2 roky pro Crohnovu chorobu s postižením tlustého střeva a terminálního ilea. Morbus Crohn diagnostikován před 3 lety, nasazena léčba Salofalk 500 mg 2-2-2, Imuran 50 mg 1-1-1, Prednison 20 mg 1-0-0. Pacientka užívala hormonální antikoncepcí AK Minisiston. Recentně byla nasazena biologická léčba Infliximabem v dávce 400 mg 0., 2. a 6. týden. Pacientka byla bez dalších interních komorbidit, bez anamnestického údaje předchozích chirurgických výkonů.
Nemocná byla prvotně ošetřena v jiném zdravotnickém zařízení pro bolesti zad a pravého bedra, klinicky zjištěno nevelké zarudnutí v této oblasti. Nález byl uzavřen jako incipientní infekce herpes zoster a doporučena medikace Herpesin 800 mg tbl á 4 hod. s osmihodinovou přestávkou v průběhu noci. Anamnestický údaj drobného poranění o ventilek gumového člunu, ke kterému došlo přibližně týden před první návštěvou lékaře, nebyl hodnocen jako významný pro etiologii infekce.
Přes vysoké dávky analgetik (Tramal 100 mg á 12 hod. tbl, Novalgin 1 tbl á 4 hod.) si stěžovala na velké bolesti zad, pro něž byla zhruba po týdnu přivezena RZP do Všeobecné fakultní nemocnice. Byla vyšetřena na dermatologické ambulanci a přijata k hospitalizaci na dermatologickou kliniku s diagnostickým závěrem Erysipel (obr. 1).
Obr. 1. Vstupní klinický obraz hodnocený jako Erysipel 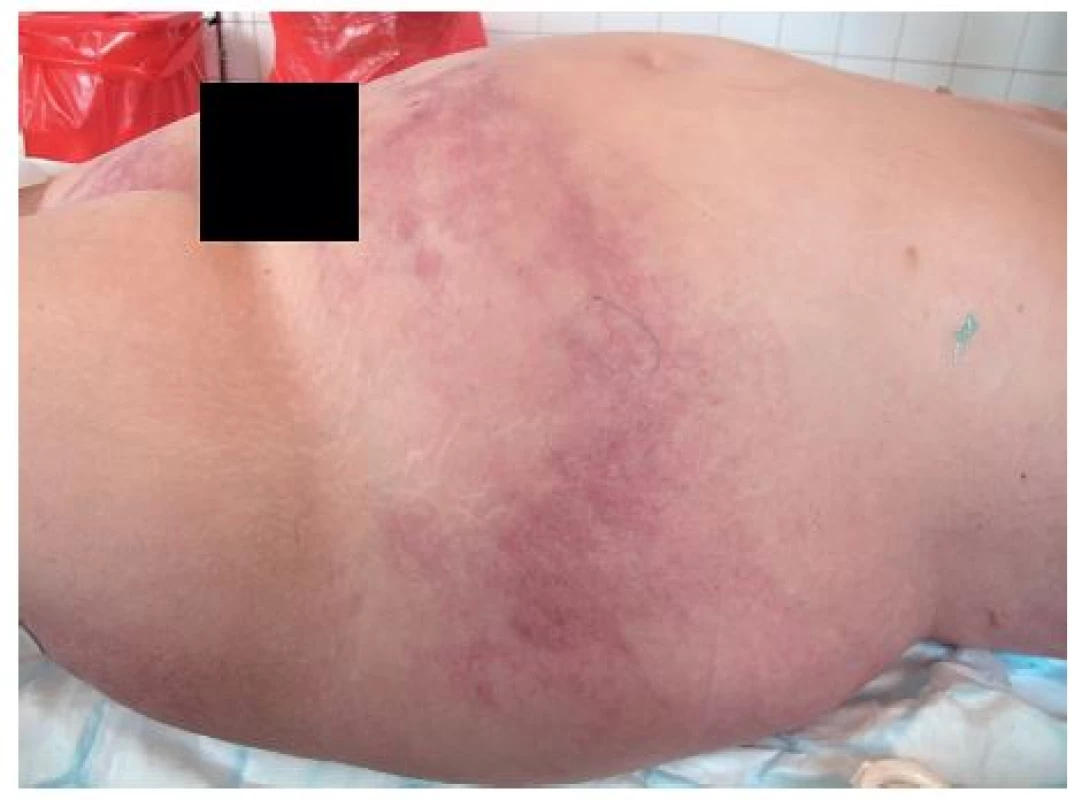
Laboratorní parametry při přijetí: CRP 400 mg/l, leu 17,109/l, laktát 1,3 mmol/l; prokalcitonin 5 mg/l. Po dohodě s ATB centrem nasazena léčba Klacid 1 g i.v. á 12 hod., Zyvoxid 600 mg á 8 hod.
Příjem na oddělení ve 12 hodin. Ve 3 hodiny ráno dalšího dne, tedy zhruba po 15 hodinách, byla nalezena středním zdravotním personálem dermatologické kliniky na lůžku bez kontaktu, v bezvědomí, s lapavými dechy. Přivolán resuscitační tým, GCS 3, areaktivní zornice, zaintubována a převezena na resuscitační oddělení.
S odstupem dalších cca 5 hodin proběhlo chirurgické konsilium. Chirurg na základě lokálního i celkového nálezu indikoval urgentně CT vyšetření. U pacientky byl klinicky patrný rozvoj rozsáhlé nekrózy břišní stěny (obr. 2), epidermolýza a putridní zápach. Laboratoř po překladu na resuscitační oddělení: CRP 260 mg/l, leu 14,109/l, laktát 1,3 mmol/l; prokalcitonin 5 mg/l.
Obr. 2. Klinický obraz s odstupem cca 16–20 hodin 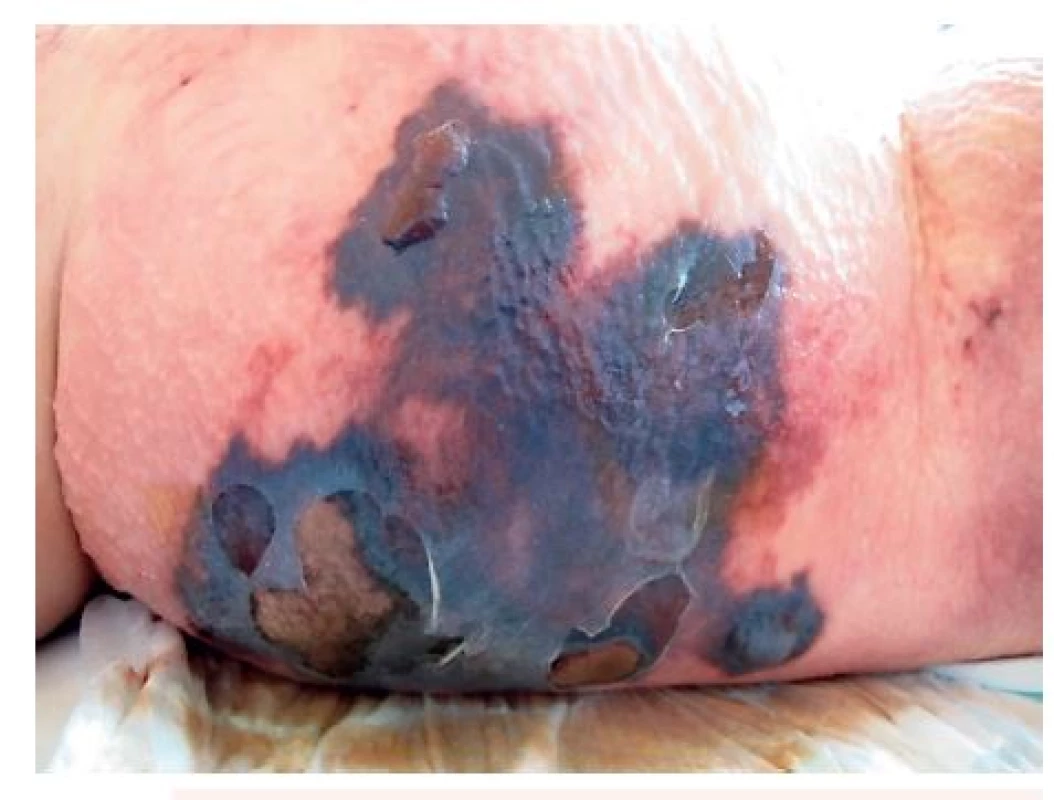
Před neodkladnou operační revizí bylo provedeno CT hrudníku, břicha a dolních končetin s nálezem rozsáhlé flegmóny břišní stěny a pravého stehna s nálezem plynu v podkoží (obr. 3). Z CT snímku bylo podezření na komunikaci zánětlivě změněného terminálního ilea přitaženého ke stěně břišní s podkožím (obr. 4). Chirurg neodkladně provedl důkladnou revizi kůže a podkoží, drenáž břišní stěny a pravého stehna, masivní výplachy H2O2. Zánět makroskopicky postihoval jen kůži a podkoží, subfasciální pronikání nebylo peroperačně potvrzeno. Komunikace s GIT popisovaná na CT se neprokázala, stěna břišní byla bez nálezu perforace. Součástí výkonu bylo i odebrání avitální tkáně k mikroskopickému a kultivačnímu vyšetření na aeroby i anaeroby. Histologické vyšetření potvrdilo přítomnost Clostridium ramosum, Clostridium tertium a Bacteroides ovatus. Po dohodě s ATB centrem byla nasazena kombinace antibiotik Tienam 1 g i.v. á 4 hod. + Tygacil 100 ml i.v. á 12 hod. + Zyvoxid 600 mg i.v. á 8 hod. + Metronidazol 1g i.v. á 8 hod. + Gentamycin 400 mg i.v. á 24 hod. (tab. 1, graf 1 až 6).
Tab. 1. Antibiotika podaná během hospitalizace 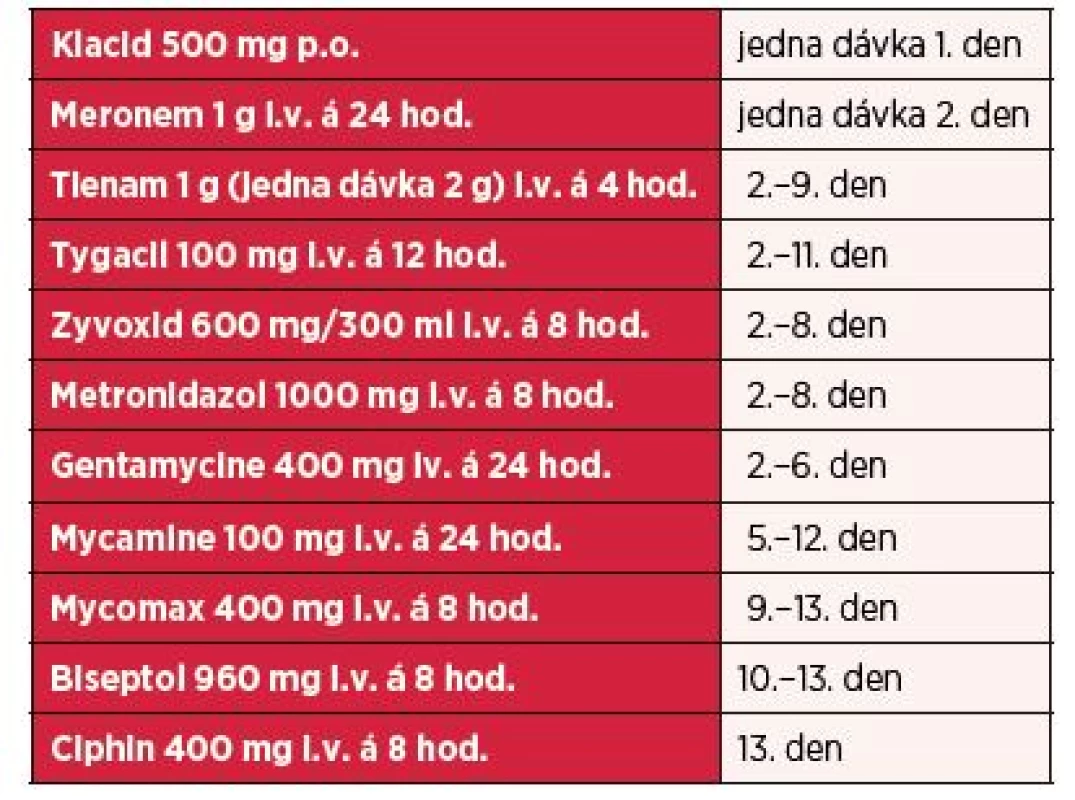
Obr. 3. CT snímek s nálezem plynu ve stěně břišní 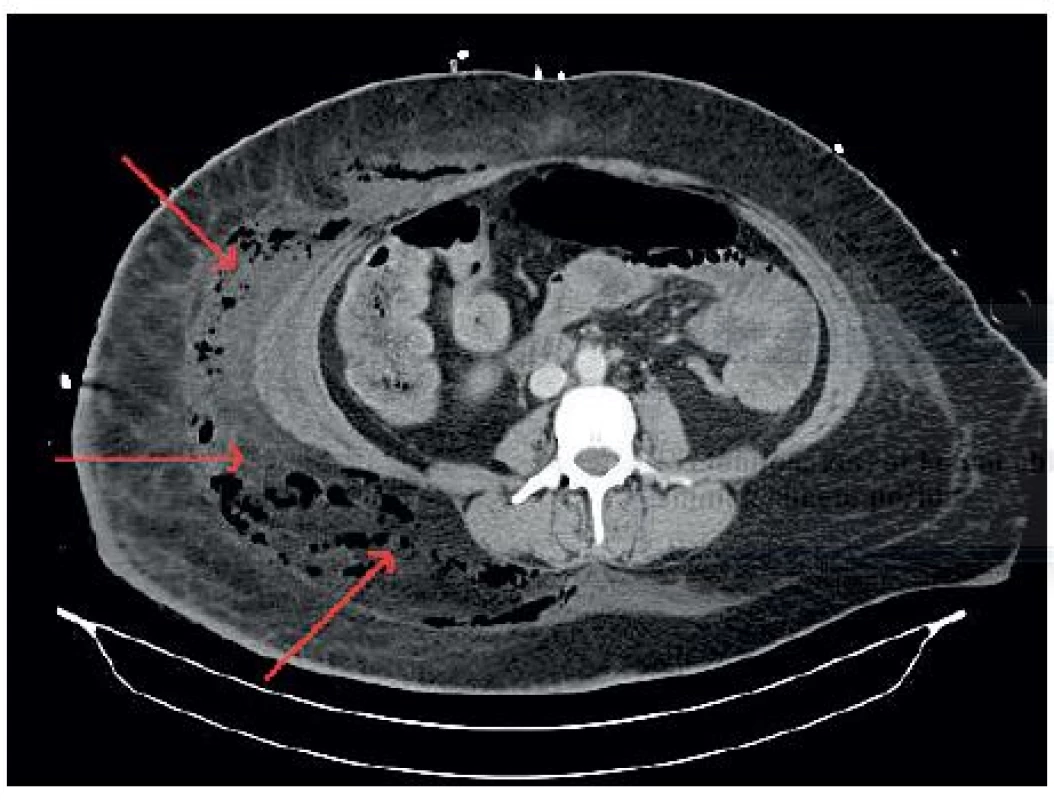
Obr. 4. Podezření na komunikaci terminálního ilea s podkožím 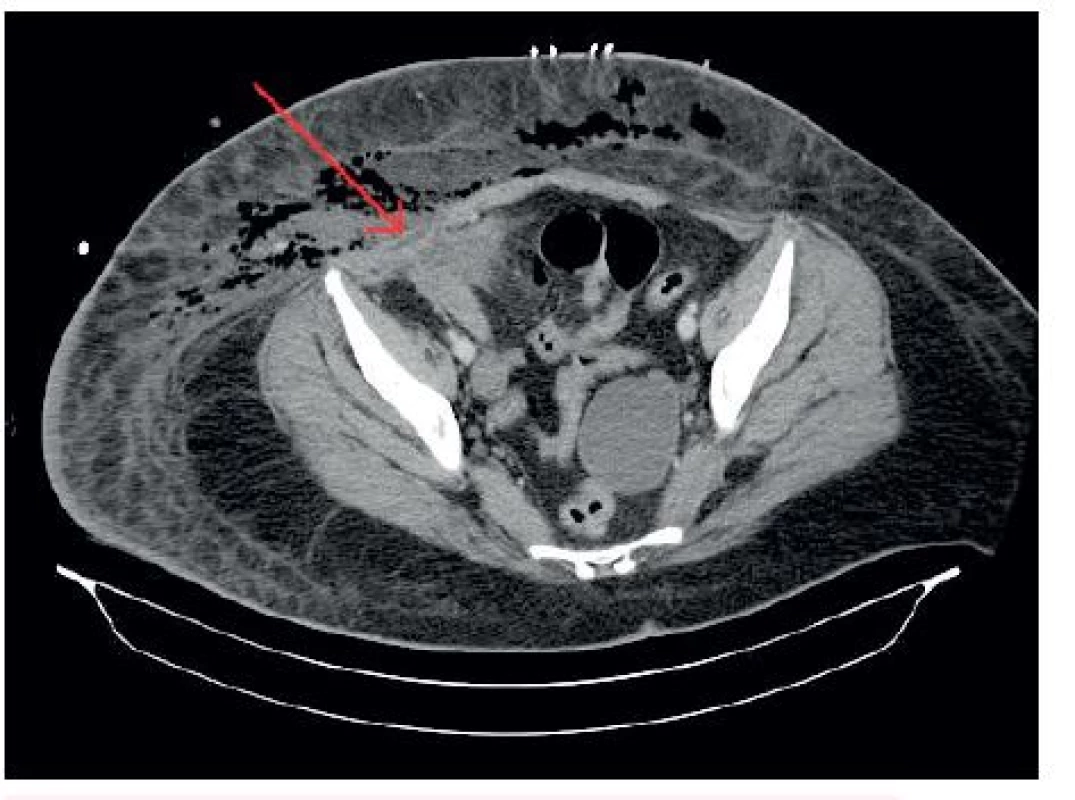
Graf 1. Hladina CRP během hospitalizace 
Graf 2. Hladina leukocytů během hospitalizace 
Graf 3. Hladina trombocytů během hospitalizace 
Graf 4. Hladina prokalcitoninu během hospitalizace 
Graf 5. Hladina laktátu během hospitalizace 
Graf 6. Hladina myoglobinu během hospitalizace 
Laboratoř po operaci: CRP 260 mg/l, leu 14,109/l, laktát v rozmezí 7–17 mmol/l!!!, prokalcitonin 290 mg/l!!!
U pacientky se postupně rozvíjí multiorgánové selhání, známky těžkého septického šoku, hypovolémie a hypotenze s nutností vazopresorické podpory, renální selhání. Řízená ventilace velmi obtížná, pacientka tolerovala jen nízké dechové objemy. Při angioCT hrudníku vyloučena plicní embolie, ale zjištěna masivní intraparenchymová nevzdušnost plic postihující přibližně polovinu plicní kapacity. Dochází k rozvoji hepatální insuficience a disseminované intravaskulární koagulopatie, které vedou k recidivujícím těžkým atakám enteroragie. Krvácení bylo úspěšně zvládnuto konzervativní léčbou, opakovanými krevními převody a úpravou koagulačních parametrů.
V dalším průběhu onemocnění progredovala centralizace oběhu, počáteční akrocyanóza (obr. 5) postoupila do obrazu suché gangrény prstů rukou (obr. 6) a nohou.
Obr. 5. Počáteční akrocyanóza jako následek centralizace oběhu 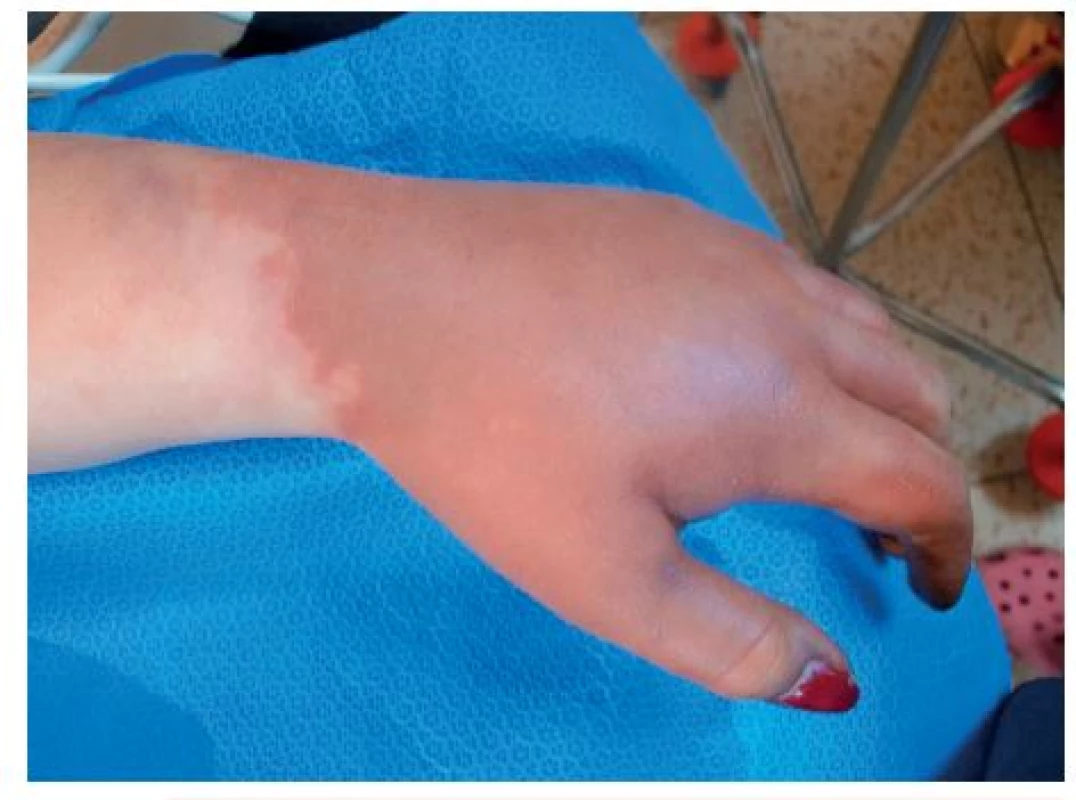
Obr. 6. Progrese akrocyanózy do suché gangraeny prstů 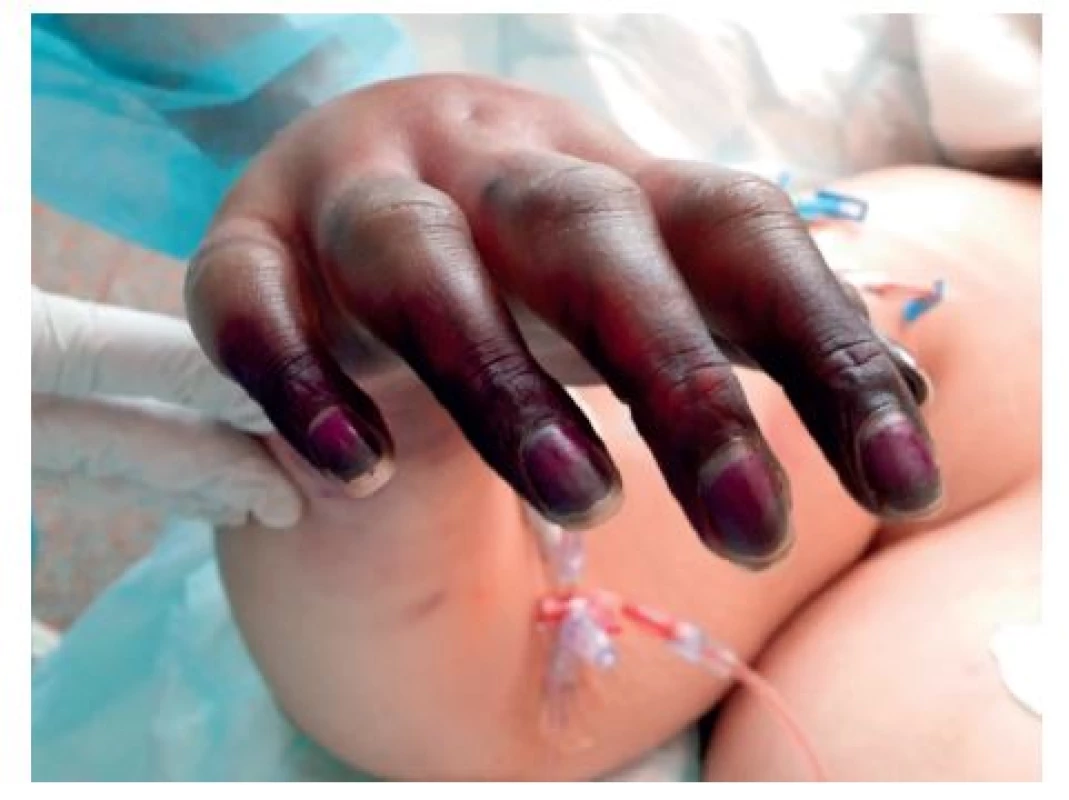
Pacientka celkem 3krát operována na operačním sále. Nejprve rozsáhlé incize a drenáže s odebráním vzorků na mikroskopické a kultivační vyšetření. Druhý pooperační den provedena již rozsáhlá nekrektomie do zdravé tkáně. Výsledkem byla nekrektomie v rozsahu podkoží a kůže téměř poloviny břišní stěny a pravého stehna (obr. 7, 8). Při těchto rozsáhlých ztrátách kožního krytu docházelo k masivním tekutinovým ztrátám ranou plochou, 6. pooperační den provedeny již jen menší nekrektomie. Mimo operační dny denně převazy a výplachy peroxidem na lůžku.
Obr. 7. Rozsah prvních nekrektomií na operačním sále 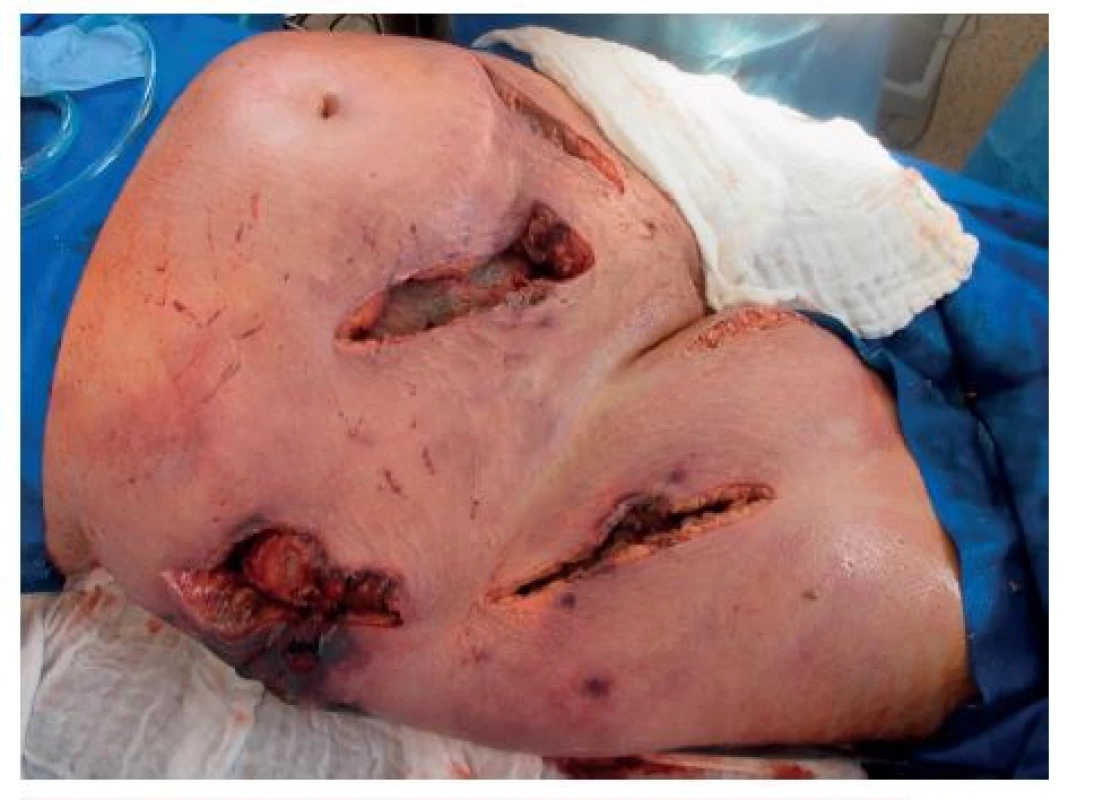
Obr. 8. Rozsah definitivní nekrektomie břišní stěny a pravého stehna provedený 2. pooperační den 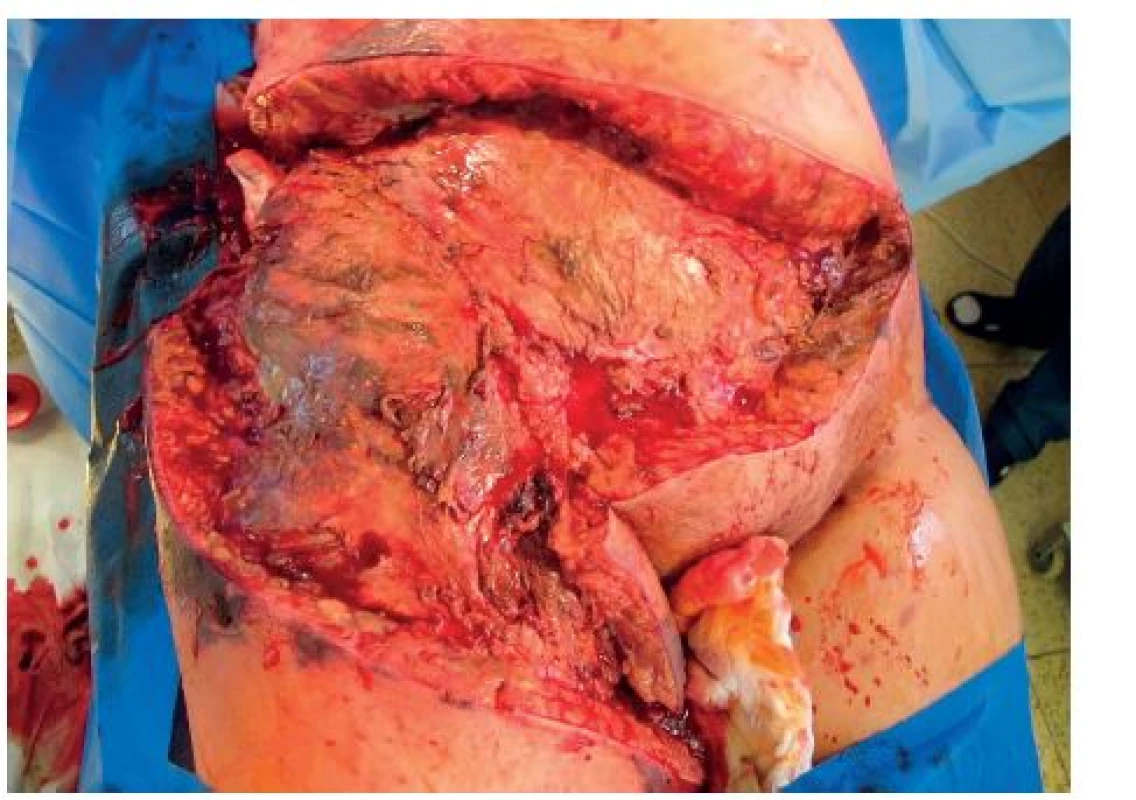
Osmý den hospitalizace (6. pooperační den) cestou z operačního sálu oběhové selhání, náhlý pokles krevního tlaku, fibrilace komor, bradykardie, zástava oběhu. Celkem 8krát defibrilace, proběhla standardní kardiopulmonální resuscitace. Po obnovení vitálních funkcí bylo provedeno CT mozku, na kterém byla zjištěna rozvinutá ischémie v povodí a. cerebri media mírně expanzivního charakteru způsobující přesun středových struktur, dále hypodenzní ložiska v dalších lalocích, uložená subkortikálně, rovněž charakteru rozvinuté ischémie mozkové tkáně (obr. 9). Neurochirurg hodnotí stav jako kontraindikovaný k jakékoliv neurochirurgické intervenci, zaveden status DNR (do not resuscitate). Exitus letalis 14. den hospitalizace.
Obr. 9. Rozvinutá ischémie mozkové tkáně s maximem v průběhu a. cerebri media 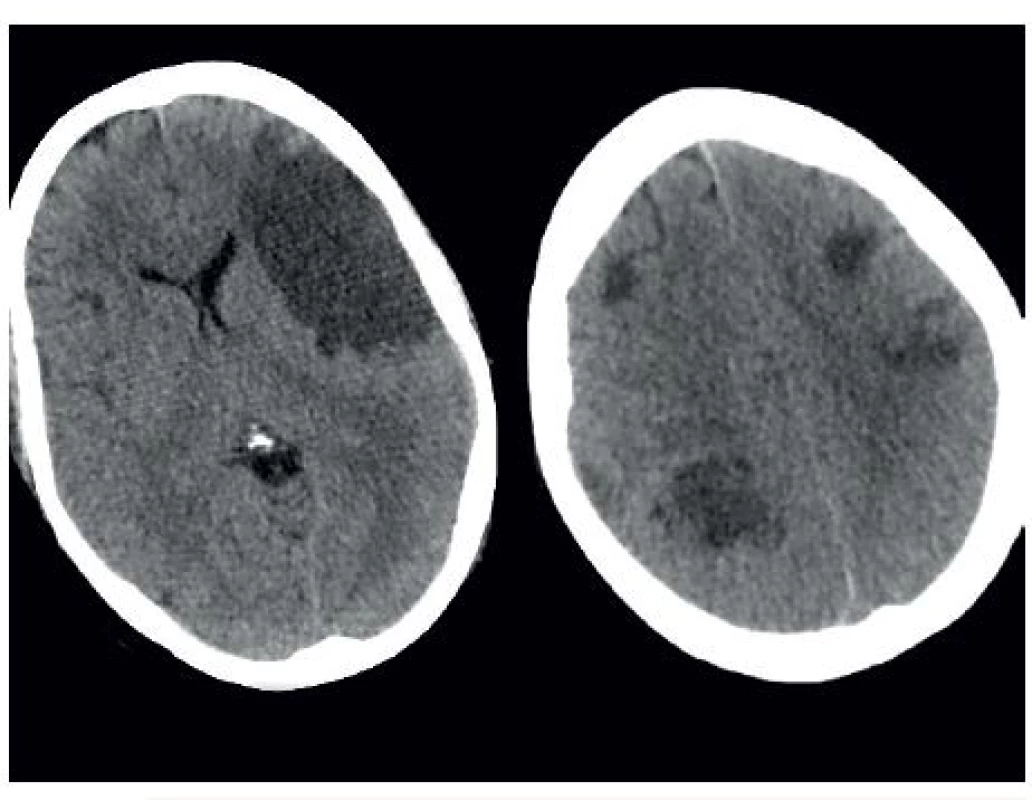
DISKUZE
Klostridiové bakterie objevil roku 1877 francouzský biolog, chemik a lékař Louis Pasteur. Odebíral krev uhynulých zvířat a pátral po bakteriích způsobujících Antrax, které již však ve tkáních přítomny nebyly. Později došel k závěru, že aerobní bakterie Bacillus anthracis po smrti zvířete zhynou v důsledku nedostatku kyslíku, ale vytvoří podmínky pro anaerobní bakterie. Tuto anaerobní bakterii nazval Vibrion septique, dnes známou jako Clostridium septicum (6).
Clostridium tertium je exotoxin neprodukující anaerobní bakterie, poprvé izolovaná Herbertem Henrym roku 1917 v rá-nách po válečných zraněních (7). Rozpoznáno jako lidský patogen však bylo až roku 1963 (8). Miller poukazuje na důležitou roli neutropenie u pacientů s Clostridium tertium bakteriémií (9). Naopak bakteriémie Clostridium tertium u non-neutropenických pacientů jsou popisovány jen velmi raritně (10).
Clostridum ramosum poprvé izoloval roku 1898 z hnisu pacienta s plicní gangrénou a appendicitidou Veillon a Zuber. Bylo pojmenováno Bacillus ramosum (11). Clostridium ramosum se vyskytuje v infekčních ránách po intraabdominálních traumatech, akutních střevních perforacích a kolorektálních abscesech. Zřídka může být Clostridium ramosum izolováno i z proleženin. V těchto případech může způsobit osteomyelitidu, metastaticky i přímým přístupem. Mohadas popisuje případ starší nemocné diabetičky s dekubity sakra a kyčle IV. stupně s osteomyelitidou stehenní kosti, kde bylo vykultivováno Clostridium ramosum (12).
V německém Institute of Human Nutrition Potsdam-Rehbruecke probíhá výzkum Clostridium ramosum (13). Prvotní výzkumy ukazují přímou souvislost mezi Clostridium ramosum ve střevech obézních lidí a myší a metabolickým syndromem (arteriální hypertenze, hyperglykémie, inzulinorezistence, dyslipidémie). Výzkum na gnotobiotických myších (gnotobionti jsou získána prenatálním vybavením z dělohy a chovem ve speciálních podmínkách) prokázal, že Clostridium ramosum podporuje vznik dietou indukované obezity, pravděpodobně zvýšením absorpce živin.
Vezmeme-li u naší pacientky v potaz vstupní CT břicha (viz obr. 4) popisující velmi intimní vztah zánětlivě změněného terminálního ilea s břišní stěnou v místě, kde byl klinicky počátek patologických změn, nelze zcela vyloučit ani přestup Clostridium ramosum ze střevní flóry. A to přesto, že stěna břišní byla bez nálezu perforace. Předpokládáme proto průnik klostridií per diapedesim poškozenou stěnou střevní při základním onemocnění. Crohnova choroba se vyznačuje, mimo jiné i tvorbou zánětu a píštělí.
Z tabulky (tab. 2) vyplývá, že bakteriální spektrum infekce nalezené v prvotním období se nemění v průběhu léčení. Předpokládáme, že anaerobní infekce potlačuje všechna další možná aerobní agens.
Tab. 2. Bakterie prokázané ve tkáních břišní stěny a stehna 
ZÁVĚR
I přes všechny pokroky v antibiotické terapii, možnostech urgentní mikroskopické detekce klostridií a určení jejich druhu, přes současné možnosti intenzivní resuscitační léčby, zůstává nejdůležitější včasná správná diagnostika těchto život ohrožujících infekcí a adekvátní agresivní chirurgická léčba. Rozhodujícím faktorem v diagnostice těchto infekcí je, aby lékař první linie na možnost anaerobní infekce myslel. Velká obezřetnost je nutná zejména u obézních, diabetiků a imunokompromitovaných jedinců s netypickou lokalizací a průběhem zánětu měkkých tkání. Takový pacient pak musí být primárně pod dohledem chirurga, nejlépe na lůžkovém chirurgickém oddělení po přijetí adekvátních bariérových opatření.
Střet zájmů: žádný.
ADRESA PRO KORESPONDENCI:
MUDr. Kristian Chrz
1. chirurgická klinika hrudní, břišní a úrazové chirurgie 1. LF UK a VFN
U Nemocnice 2, 128 08 Praha 2
e-mail: kchrz@seznam.cz
Zdroje
1. Bednář M. Lékařská mikrobiologie. Praha: Triton 1996.
2. Kašpárková V. Toxiny bakterií rodu Clostridium. Bakalářská práce. Zlín: Univerzita Tomáše Bati 2009. Dostupný z: http://dspace.k.utb.cz/bitstream/handle/10563/10081/kašpárková_2009_bp.pdf.
3. Zeman M, Krška Z, et al. Chirurgická propedeutika. 3., doplněné a přepracované vydání. Praha: Grada Publishing 2011.
4. Revis D. Clostridial gas gangrene. Medscape 2014. Dostupný z: http://emedicine.medscape.com/article/214992-overview
5. Vyhnánek F. Plynatá sněť – standardy postupu. Dostupný z: http://www.infekce.cz/Standardy/PlynataSnetDP.pdf
6. Brabencová S. Diagnostika Clostridium difficile a jeho výskyt ve FN Brno. Bakalářská práce. Oddělení klinické mikrobiologie Fakultní nemocnice Brno Bohunice 2011. Dostupný z: http://is.muni.cz/th/258751/lf_b/diagnostika_clostridium_difficile_a_jeho_vyskyt_ve_fn_brno.pdf
7. Henry H. An investigation of the cultural reactions of certain anaerobes found in wounds. J Pathol Bacteriol 1918; 21(3): 344–385.
8. King BM. Clostridium tertium septicemia. N Engl J Med 1963; 269 : 467–469.
9. Miller DL, Brazer S, Murdoch D, et al. Significance of Clostridium tertium bacteremia in neutropenic and nonneutropenic patients: review of 32 cases. Clin Infect Dis 2001; 32(32): 975–978.
10. Ray P, Das A, Singh K, et al. Clostridium tertium in necrotizing fasciitis and gangraene. Emerg Infect Dis 2003; 9(10): 1347–1348.
11. Veillon A, Zuber A. Recherches sur quelques microbes strictement anaerobies et leur role en pathologie. Arch Med Exp Anat Pathol 1898; 10 : 517–545.
12. Mohadas R, Poduval RD, Unnikrishnan D, Corpuz M. Clostridium ramosum bacteremia and osteomyelitis in a patient with infected pressure sores. Infect Dis Clin Pract 2001; 10(2): 123–124.
13. Woting A, Pfeiffer N, Loh G, et al. Clostridium ramosum promotes high-fat diet-induced obesity in gnotobiotic mouse models. mBio 2014; 5(5): e01530–14. doi: 10.1128/mBio.01530-14.
Štítky
Praktické lékařství pro děti a dorost Praktické lékařství pro dospělé
Článek vyšel v časopisePraktický lékař
Nejčtenější tento týden
2015 Číslo 1- Naděje budí časná diagnostika Parkinsonovy choroby založená na pachu kůže
- Na inkontinenční pomůcky nově dosáhne více pacientů
- Efektivita kartáčku Sonicare For Kids u dětí předškolního věku
- Trombóza portální žíly jako komplikace infekce COVID-19 – kazuistika
-
Všechny články tohoto čísla
- Současná léčba pyogenního abscesu jater – zkušenosti Chirurgické kliniky FN Plzeň
- Dopady holokaustu na zdraví přeživších
- Intervence v prevenci pádů seniorů v institucích: přehledová studie
- Změny v hladinách prolinu v moči mohou korelovat s úspěšností operační léčby karcinomu prostaty
- Klostridiová flegmóna břišní stěny u obézní pacientky s Crohnovou chorobou
- Virové hemoragické horečky
-
Josef Štorek, Petr Herle
Urgentní medicína pro všeobecné lékaře -
Křeslo pro Fausta
Rozhovory vedla a k vydání připravila Marie Retková - Jubilanti
- Praktický lékař
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Současná léčba pyogenního abscesu jater – zkušenosti Chirurgické kliniky FN Plzeň
- Klostridiová flegmóna břišní stěny u obézní pacientky s Crohnovou chorobou
- Virové hemoragické horečky
- Jubilanti
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Revma Focus: Spondyloartritidy
nový kurz
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Autoři: prof. MUDr. Pavel Horák, CSc., doc. MUDr. Ludmila Brunerová, Ph.D., doc. MUDr. Václav Vyskočil, Ph.D., prim. MUDr. Richard Pikner, Ph.D., MUDr. Olga Růžičková, MUDr. Jan Rosa, prof. MUDr. Vladimír Palička, CSc., Dr.h.c.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



