-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Třicet let od popsání prvních případů AIDS: historie a současnost Část II.
30 Years since the First AIDS Cases Were Reported: History and the Present Part II
HIV taxonomy, morphology, biophysical properties, and replication cycle as well as modes of HIV transmission in humans are described. State of the art laboratory diagnosis of HIV/AIDS, core clinical diagnostic criteria for AIDS, and AIDS treatment guidelines are summarized. Global HIV/AIDS epidemic and relevant prevention activities are discussed.
Key words:
HIV-1 – viral genome – AIDS – antiretroviral therapy – global epidemic – prevention
Autoři: Brůčková Marie
Působiště autorů: Emeritní vedoucí NRL pro AIDS
Vyšlo v časopise: Epidemiol. Mikrobiol. Imunol. 61, 2012, č. 3, s. 72-78
Souhrn
V článku je popisována taxonomie, morfologické a biofyzikální vlastnosti viru HIV, jeho replikační cyklus a způsob šíření HIV infekce v lidské populaci. Jsou uvedeny současné možnosti laboratorní diagnostiky HIV/AIDS, základní klinická ktitéria pro stanovení diagnózy AIDS a terapeutické postupy. Je diskutován současný stav globální epidemie HIV/AIDS a základní preventivní opatření.
Klíčová slova:
HIV-1 – virový genom – AIDS – antiretrovirová terapie – globální epidemie – prevenceÚVOD
V I. části sdělení jsme krátce popsali výskyt prvních případů nového infekčního onemocnění – AIDS, objev jeho virového původce – HIV a základní charakteristiky šíření AIDS v lidské populaci. V této části se budeme podrobněji věnovat popisu některých taxonomických a biofyzikálních vlastností viru HIV, mechanismu jeho množení v cílových buňkách napadeného organismu, způsobech přenosu a důvodech jeho globálního epidemického šíření, zejména v některých regionech a specifických populačních skupinách. Uvedeme některé charakteristické klinické projevy onemocnění AIDS podle definice užívané pro surveillance HIV/AIDS. Zmíníme též možnosti léčby a prevence šíření HIV/AIDS.
VIRUS HIV
Taxonomie HIV je uvedena v tabulce 1. HIV patří do skupiny retrovirů, kam se řadí jedny z nejdéle známých virů. Jejich společnou vlastností je schopnost přepisovat vlastní genetickou informaci, nesenou RNA, do DNA napadené buňky. V přírodě je tento proces velmi neobvyklý, obvyklý je postup opačný – přepis DNA na RNA. Retrovirům umožňuje tuto nezvyklou dráhu enzym reverzní transkriptáza, který je integrální součástí virového genomu.
Tab. 1. Taxonomie HIV-retroviry Table 1. HIV taxonomy – retroviruses 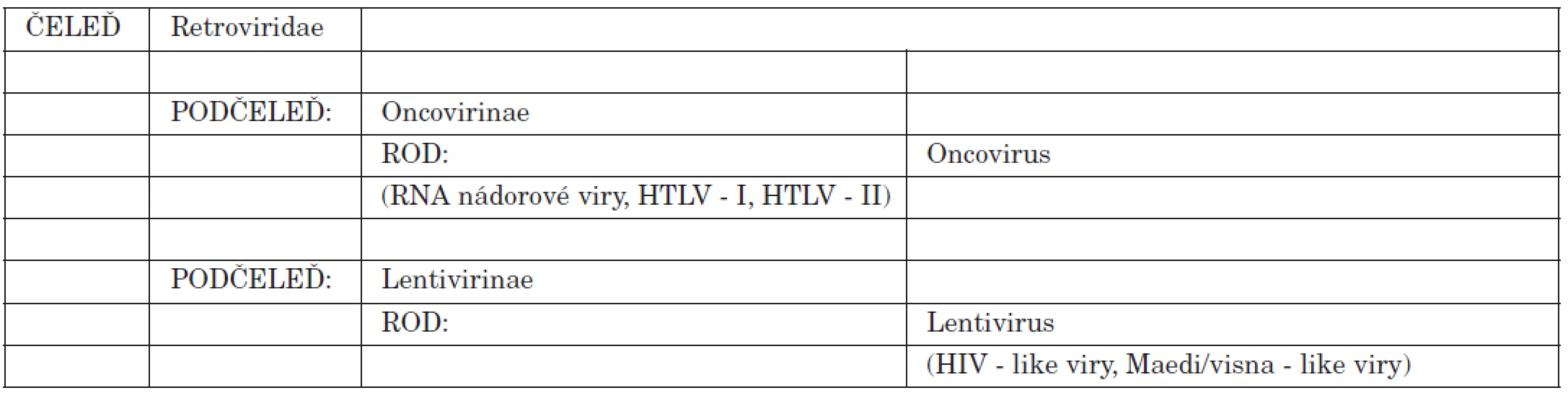
Další společnou charakteristikou retrovirů je dlouhé období latence, kdy virová genetická informace je sice zabudovaná do chromozomálního aparátu napadené buňky, společně s ní se množí, ale po dlouhou dobu infikované buňky přežívají bez zásadního funkčního poškození. Infekce se neprojevuje v tomto období klinickými příznaky a je rozpoznatelná pouze laboratorními testy. Do skupiny retrovirů proto spadají také tzv. pomalé viry, „zabijáci“, vyznačující se dlouhou perzistencí v organismu bez známek jeho poškození. Většinou mají afinitu k CNS, vyskytují se hlavně u zvířat. Dlouhodobý infekční proces končí smrtí (Visna, Maedi viry vyskytující se u ovcí a aleutských minků). Někteří sebekritičtí virologové humorně tvrdí, že neexistují pomalé viry, pomalí jsou jen virologové.
Velkou podskupinou retrovirů jsou lidské onkogenní viry způsobující některé druhy leukémií. Mezi ně také američtí autoři HIV původně řadili pod názvem HTLV-III (viz Část I. publikace). Stejně tak do skupiny retrovirů patří viry vyvolávající nádorová onemocnění u zvířat, zejména drůbeže.
Při dalších studiích bylo zjištěno, že virus HIV se vyskytuje ve dvou typech, označovaných jako HIV-1 a HIV-2. Rozdíly v genetické skladbě virů HIV-1 a HIV - 2 jsou velmi malé (obr. 1). Podrobně charakterizované kmeny HIV-1 se pak řadí do 3 velkých skupin – podtypů HIV-1 značených M, N a O. Skupina M (Major) je největší a dělí se dále na různé kmenové varianty označované alfabeticky (dosud A–L, CRF – cirkulující rekombinantní formy). U viru HIV-2 nebyly rozpoznány žádné subtypy (obr. 2).
Obr. 1. Genetická skladba HIV-1 a HIV-2 Fig. 1. Genome structure of HIV-1 and HIV-2 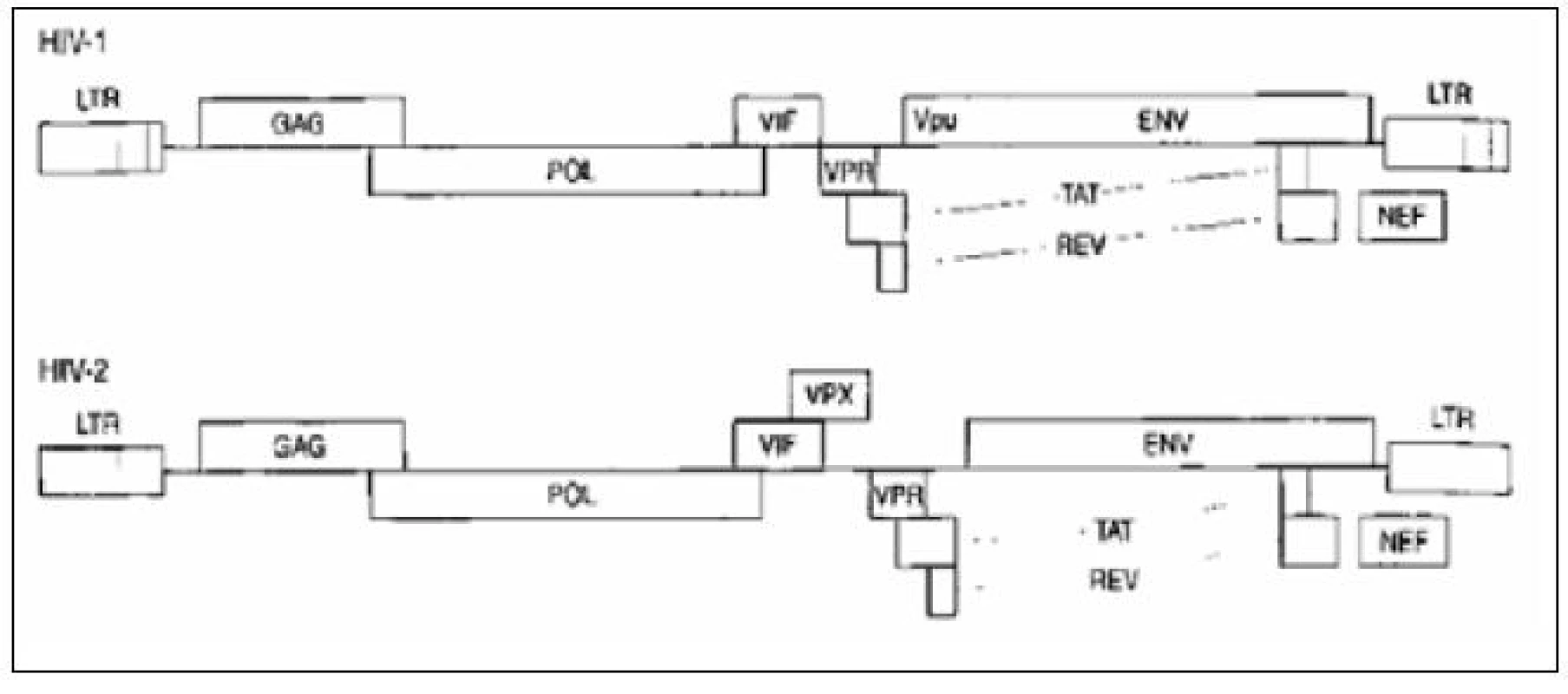
Obr. 2. Subtypy HIV-1 a HIV-2 Fig. 2. Subtypes HIV-1 and HIV-2 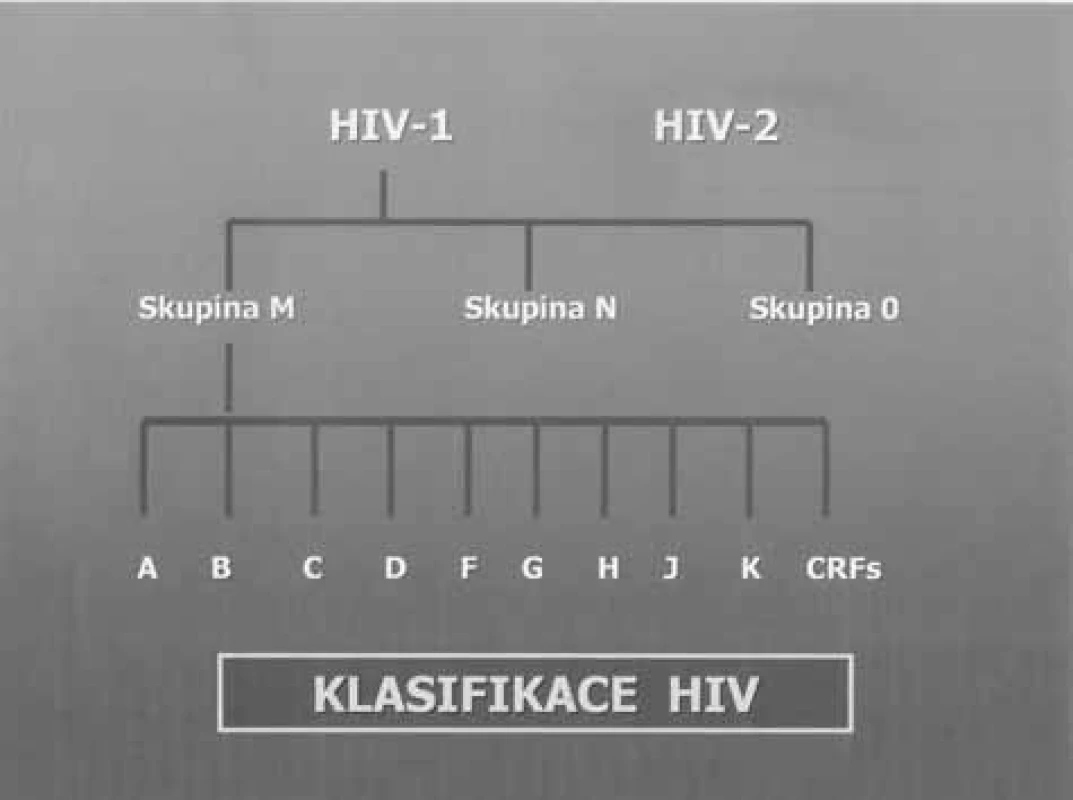
Virus HIV patří mezi malé až středně velké viry (30–100 nm) – obrázek 3. Jeho partikule mají sférický tvar s jasně vyznačenými povrchovými strukturami (spikes) a denzním jádrem v podobě malého oříšku (snad čínského), jak morfologicky výstižně popsala jedna z nejznámějších elektronových mikroskopiček June Almeida.
Obr. 3. Elektronmikroskopický snímek HIV Fig. 3. Electron microscopy image of HIV 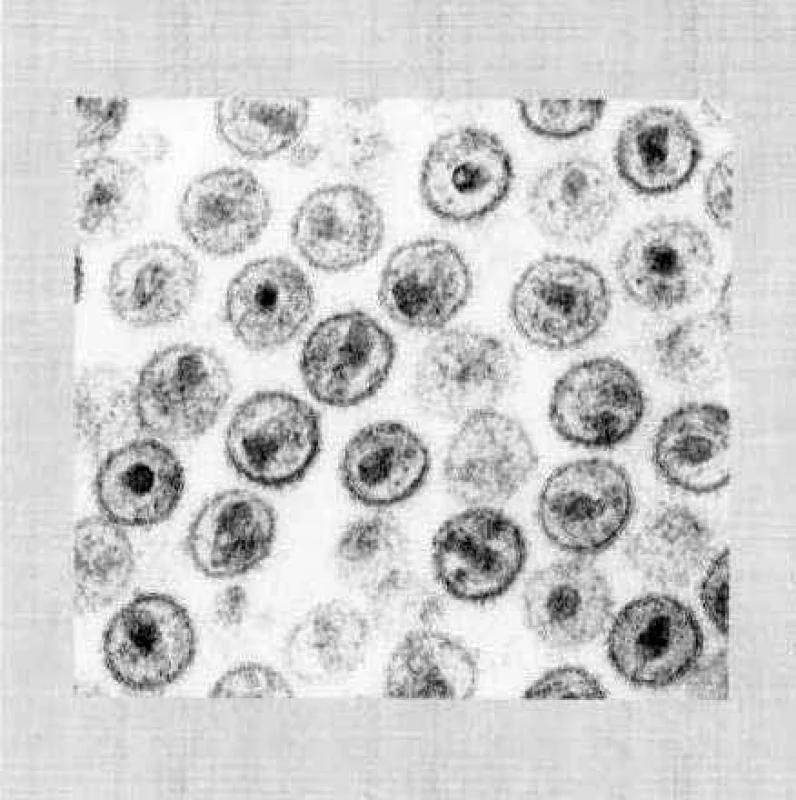
Morfologií, velikostí, strukturálním uspořádáním, biofyzikálním složením i některými vlastnostmi je HIV podobný virům chřipky. Patří mezi tzv. obalené viry či viry s obálkou (envelope) tvořenou lipoproteiny. Z obalu vyčnívají výběžky (spikes), morfologií podobné houbičkám na tenké nožce – glykoproteiny o molekulové hmotnosti 40 a 120 kilodaltonů (GP 40 a GP 120). Tyto povrchové struktury jsou immunogenní (tvoří se proti nim protilátky) a velmi mutagenní – stejně jako podobné struktury u chřipkových virů. Udává se však, že viry HIV jsou až 100krát mutagennější než viry chřipky. Vlastní jádro viru tvoří proteinový obal p24 a p17, který kryje virový genetický materiál, to je dvoušroubovici RNA a enzymové vybavení viru (jak znázorňuje schematický obrázek 4). Podrobné molekulární studie genetické skladby viru HIV prokázaly přítomnost tří genů strukturálních, označených jako env, gag, pol, které kódují různé virové struktury a řadu genů regulačních, které kódují různé virové funkce (funkce některých z nich není dosud přesně známa) – tabulky 2 a 3.
Obr. 4. Schematický obrázek HIV Fig. 4. Schematic representation of HIV 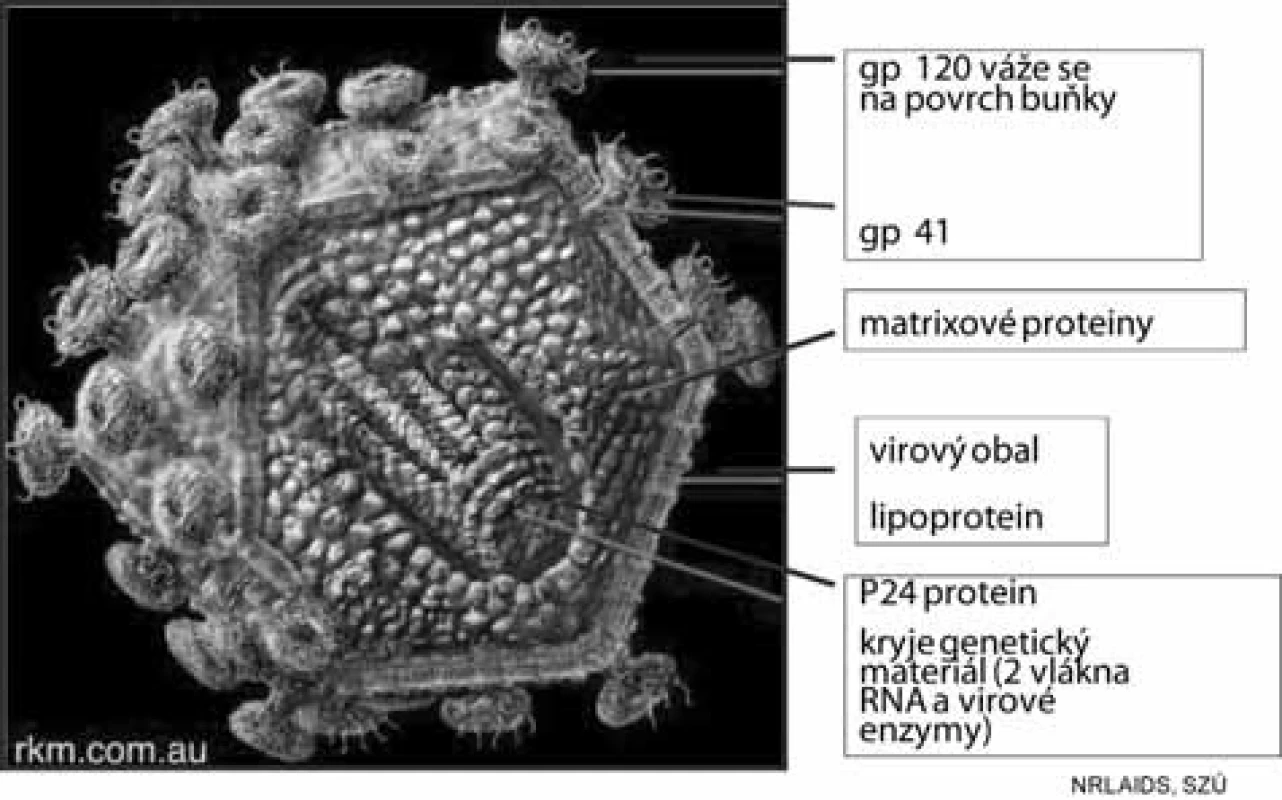
Tab. 2. Strukturální geny HIV Table 2. HIV structural genes 
Tab. 3. Regulační geny HIV Table 3. HIV regulatory genes 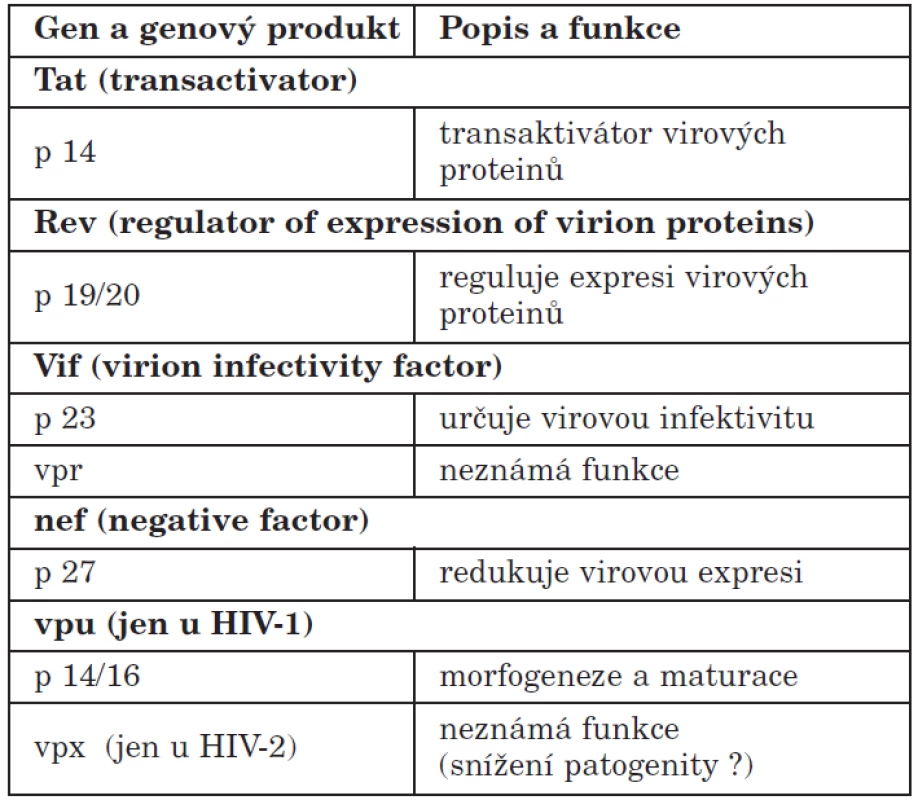
Virus HIV má velmi unikátní replikační cyklus. Zjednodušené schéma ukazuje obrázek 5. Pro infekci buňky virem HIV je nutná přítomnost receptoru CD4+ na jejím povrchu a součinnost dalších buněčných koreceptorů, jako CCR5, CXCR4. Povrchové virové struktury se spojí s povrchovými buněčnými receptory (zámek-klíč) a umožní průnik viru do buněčné cytoplazmy. Virus se tak zvaně svlékne, odhodí svůj plášť (uncoating), obnaží svůj genom a pomocí enzymu reverzní transkriptázy přepíše svou RNA na DNA. Ta se pomocí dalšího virového enzymu, integrázy, zabuduje do jaderného chromozomálního vybavení napadené buňky. Virový genetický signál zůstává v buňce po celý její život a spolu s ní se dělí a přenáší na potomstvo. Kromě toho se HIV replikuje také horizontálně, kdy buňka začíná opačným pochodem přepisovat virovou DNA na RNA, která se shromažďuje v cytoplazmě, obaluje proteiny působením enzymu proteázy a shromažďuje se jako inkompletní virus u buněčné stěny. Tou posléze proniká procesem zvaným pučení a získává z ní glykoproteiny pro dokončení stavby kompletního virionu schopného infikovat další citlivé buňky.
Obr. 5. Schéma replikačního cyklu HIV Fig. 5. Schematic representation of HIV replication cycle 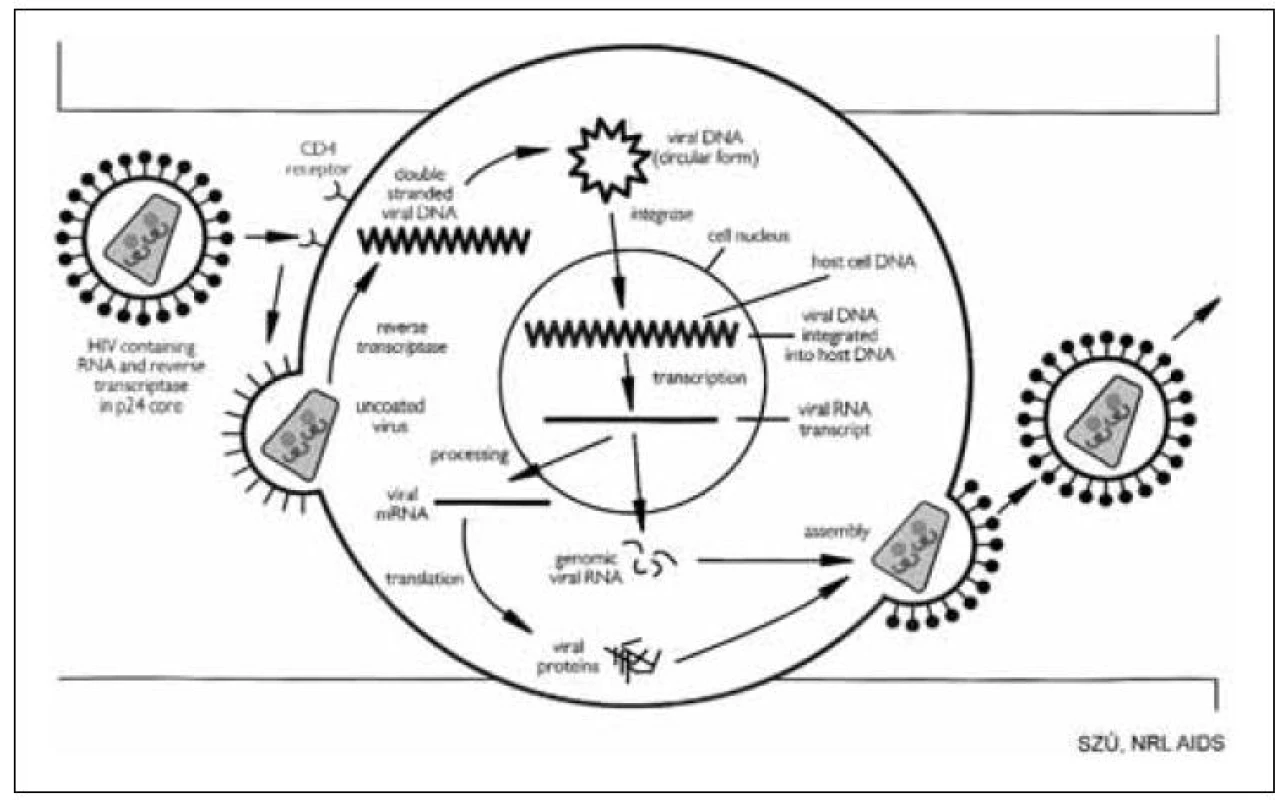
Reakci buňky na infekci HIV ukazuje další schéma – obrázek 6. Výše popsaným procesem se HIV virový signál zabuduje do jádra napadené buňky a v ní po určitou dobu přetrvává, aniž by ji nějak funkčně poškozoval (latentní stadium). Poté následuje fáze chronická, kdy buňka intermitentně začne v malém množství vylučovat nové virové partikule, její metabolismus i funkce začínají být poškozené, až posléze nastoupí fáze akutní, kdy buňka na úkor vlastního metabolismu a replikace syntetizuje velká kvanta nových virových partikulí a posléze zmírá.
Obr. 6. Reakce buňky na infekci HIV Fig. 6. Cell response to HIV infection 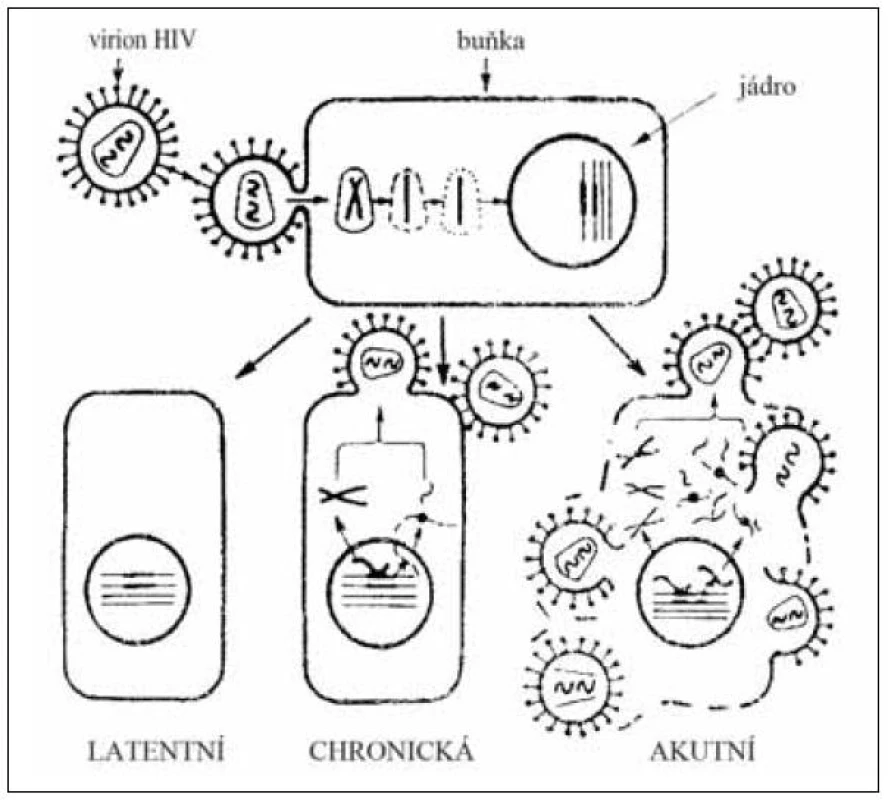
Takto tedy probíhá HIV virová infekce (velmi zjednodušeně popsaná) na buněčné úrovni. Jak reaguje celý infikovaný organismus schematicky znázorňuje obrázek 7. Po vstupu viru do cílových buněk začíná velmi rychlá replikace a vylučování viru – někteří autoři uvádějí, že k tomu dochází už za 3 hodiny po vstupu viru do organismu a že již v této fázi je infikovaný člověk vysoce infekční pro své okolí. Následuje tzv. akutní období, které se klinicky vyznačuje nikterak typickými příznaky, spíše upomínajícími na respirační onemocnění: zánět nosohltanu, bolesti hlavy, zvýšená teplota až horečka, zduření mízních uzlin (ponejvíce krčních), celková únavnost, malátnost. Snad jediným typickým příznakem, ne však vždy přítomným, je prchavý exantém, který připomíná „lékovou vyrážku“ a obvykle velmi rychle vymizí. Někdy jsou tyto příznaky akutní infekce HIV tak nenápadné, že nevyžadují ani lékařskou konzultaci a obvykle spontánně mizí. Z hlediska epidemiologického je tato fáze velmi nebezpečná, protože zdánlivě zdravý člověk o své infekci neví a může ji tak bez zábran dále šířit.
Obr. 7. Průběh infekce HIV Fig. 7. Course of HIV infection 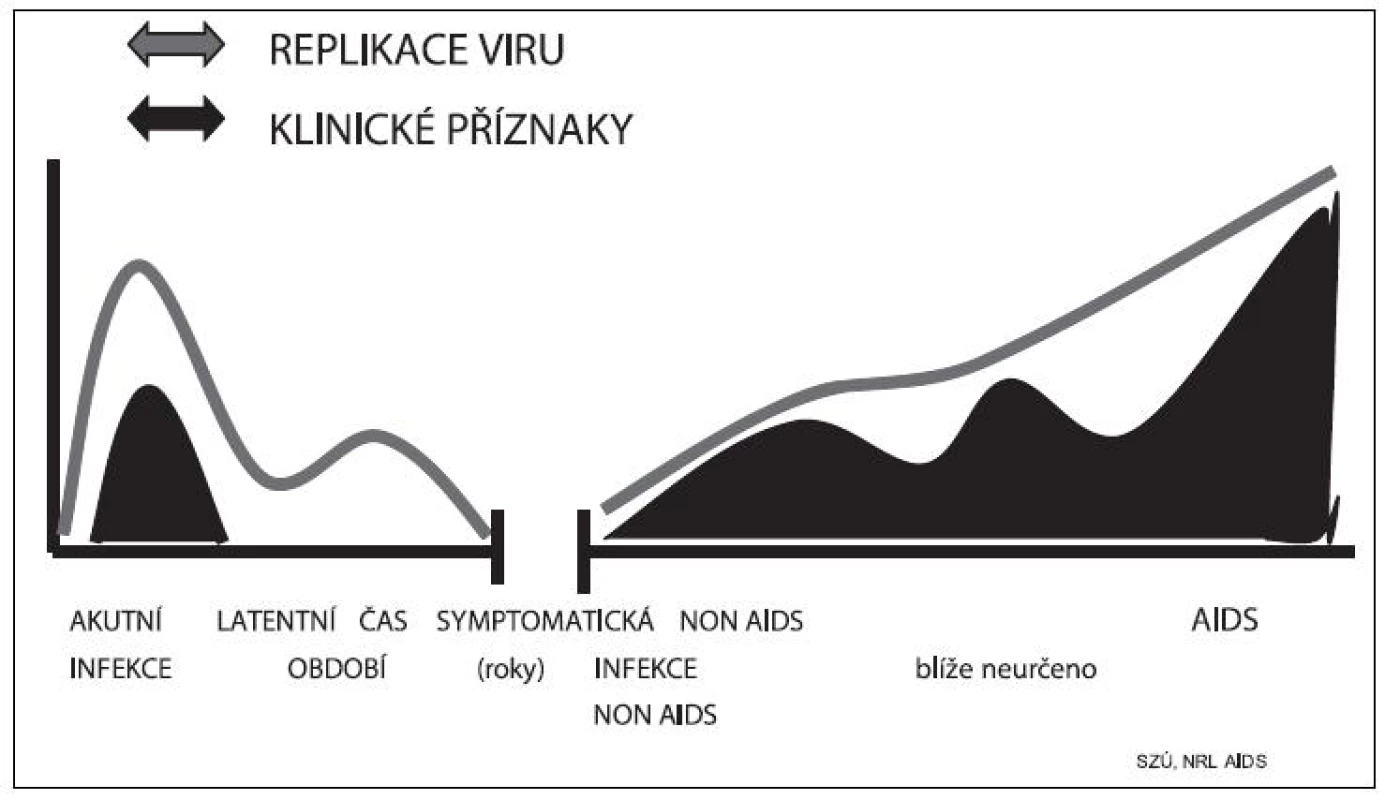
Po akutní fázi dochází k omezenému vyplavování HIV virových partikulí do krevního oběhu, ačkoliv replikace viru intenzivně pokračuje, ale zůstává omezena na mízní uzliny. Hodnoty tzv. virové nálože (počet HIV RNA kopií v plazmě) se dostávají v tomto období k neměřitelným hodnotám. Nastává dlouhá doba latence („němá infekce“), dochází jen k intermitentnímu vylučování viru v nízkých koncentracích do krve, a ani klinicky se infekce nikterak významně nemanifestuje. Toto období se v současné době, zejména se zdokonalováním specifické terapie, prodlužuje a počítá na roky.
Velmi – zejména diagnosticky – významným procesem je tvorba protilátek. Protilátky proti povrchovým glykoproteinům HIV se vytvářejí individuálně za různě dlouhou dobu, odhaduje se, že nejdříve za 10–21 dnů po vstupu HIV do organismu, nejpozději však do 2–3 měsíců po infekci. Vytvářejí se a spolehlivě identifikují u všech infikovaných osob. Přetrvávají po celý život infikovaného jedince, dají se prokazovat i v krvi odebrané post mortem. Tyto protilátky však, bohužel, nemají protektivní charakter. To je jedna ze zvláštností HIV infekce (někteří nazývali tyto zvláštnosti „mystérii“ HIV infekce).
STANOVENÍ DIAGNÓZY AIDS
Po různě dlouhé době latence dochází na nějaký podnět, či spíše soubor podnětů, k extrémně vysokým hodnotám vylučování HIV do krve, úbytku buněk imunitního systému (zejména CD4 buněk) a nastupuje rozvoj klinických příznaků infekce. Ty jsou především vyjádřeny jako následek zhroucení imunitního systému výskytem nejprve malých, posléze i velkých oportunních infekcí bakteriálního, virového, mykotického a parazitárního původu, často se vyskytuje i nádorové bujení související se ztrátou imunity. V této době se již stanoví diagnóza plně rozvinutého onemocnění AIDS, které bohužel, dříve či později končí úmrtím. Podle klinických příznaků se HIV infekce zařazuje do 4 stadií, z nichž posledním je AIDS. Pro účely surveillance se používá mezinárodně stanoveného schématu, specifikujícího 32 oportunních infekcí a nádorových onemocnění, která HIV infikovaného pacienta řadí do množiny AIDS nemocných. Kromě oportunních infekcí a nádorových onemocnění sem patří i výrazné poškození CNS a tzv. waisting syndrome, celková zchátralost s enormním úbytkem hmotnosti (koncentráčnický vzhled).
Kolik HIV infikovaných se dostane až do terminálního stadia AIDS končícího smrtí, není dosud přesně známo. Někteří říkají, že 100 % infikovaných, jiní se domnívají, že ne všichni tak končí. Co je ale jisté, že AIDS nelze vyléčit, ale lze jej úspěšně léčit, život infikovaného zkvalitnit a prodloužit. Dosud se totiž přes veškerá úsilí nepodařilo virus HIV z napadeného organismu vyloučit, jen potlačit jeho množení. Nicméně ani 30 let výskytu a zkoumání AIDS není dostatečně dlouhá doba pro stanovení obecně platných závěrů.
Stejně tak není dosud přesně známo, jaké klinické projevy se u kterého z HIV infikovaných pacientů rozvinou. V začátcích to byla velmi často pneumocystová pneumonie (PPC – Pneumocystis carinii pneumonia) a Kaposiho sarkom, nyní vzhledem k možnostem profylaktického používání různých léčiv se spektrum infekcí mění. V případě Pneumocystis carinii je nutno uvést přínos našeho světově významného parazitologa akad. prof. O. Jírovce, který jako první popsal výskyt pneumocystové pneumonie u novorozenců, vesměs s fatálním koncem. Na jeho počest byl organismus Pneumocystis carinii posléze přejmenován na Pneumocystis jiroveci (posmrtně). Je však ironií osudu, že tento organismus, který prof. Jírovec celý život pokládal za parazita, byl po důkladných studiích zařazen mezi houby.
ZÁKLADY TERAPIE HIV/AIDS
V počátcích bylo onemocnění AIDS označováno jako „onemocnění mnoha tváří“, které postihovalo všechny tělesné orgány a systémy. V poslední době se AIDS specifikuje jako chronické systémové onemocnění. Jeho léčba je komplexní, individuálně „šitá na míru“ každému z HIV infikovaných pacientů. Základem je antiretrovirá terapie, která se snaží potlačit replikaci viru se všemi jejími nežádoucími účinky. Tato terapie využívá poznatků ze studia množení viru v buňce a snaží se zasáhnout v citlivých místech jeho replikace. Je to zejména blokace viru při vstupu do cílové buňky, kdy vedoucí roli hraje virový enzym – reverzní transkriptáza. V začátcích léčby byl jediným dostupným antiretrovirovým preparátem inhibitor reverzní transkriptázy pod názvem zidovudin. Jednalo se o klasickou monoterapii. Postupem doby se objevovaly další preparáty, zasahující v různých fázích virového replikačního cyklu (inhibitory virové proteázy, integrázy či inhibitory ovlivňující proces fúze viru s buňkou), až se došlo k tzv. cART (kombinovaná antiretrová terapie) – kombinaci několika účinných antiretrovirových preparátů. Jejich základem bývá často výše zmiňovaný inhibitor reverzní transkriptázy. V otázce vývoje nových antiretrovirových preparátů je významným, světově uznávaným odborníkem prof. A. Holý, emer. ředitel Výzkumného ústavu organické chemie a biochemie ČAV, který se podílel na vývoji a syntéze několika úspěšných antiretrovirových preparátů.
Otázkou zůstává, kdy tuto antiretrovirovou terapii nasadit. Její užívání není totiž bez vedlejších účinků a pro pacienta přináší zátěž a nepohodlí. Zdá se, že převládajícím názorem je započetí léčby, jakmile HIV virová nálož (viral load) stoupne nad 200 HIV RNA kopií/ml plazmy. Komplikujícím faktorem je také snadný vzestup rezistence na podávaná antiretrovirotika. Adherence na léčebný postup je u HIV pozitivního pacienta nesmírně důležitým faktorem pro úspěšnost léčby.
Další nedílnou součástí terapie HIV/AIDS je podávání profylaktických preparátů k zamezení nejčastěji se vyskytujících doprovodných (oportunních) infekcí u HIV pozitivních osob. Klasickým případem této možnosti je např. profylaxe pneumocystové pneumonie, která prakticky vymizela v rozvinutých zemích jako příčina úmrtí u HIV pozitivních pacientů. Totéž se týká profylaxe toxoplazmové infekce a řady dalších (včetně TBC).
Samozřejmou součástí léčby jsou další běžné léčebné postupy používané u ostatních pacientů při řešení jejich aktuálních zdravotních potřeb.
GLOBÁLNÍ EPIDEMIE HIV/AIDS
Vzplanutí globální epidemie HIV/AIDS samozřejmě souvisí se způsobem přenosu viru HIV. Dosud platí jen 3 možné způsoby přenosu HIV: krevní cestou, pohlavním stykem a přenos z matky na dítě. Přenos krevní cestou se podařilo velmi brzy omezit testováním krve a krevních derivátů pro terapeutické podání na přítomnost HIV protilátek. Do této skupiny také patří přenos HIV mezi injekčními uživateli drog. Sexuální styk, zejména homosexuální praktiky, jsou v současné době nejčastějším způsobem přenosu HIV na celém světě. Přenos HIV z matky na dítě (vertikální přenos) se podařilo značně omezit, zejména v rozvinutých zemích, používáním specifické profylaxe u matky i novorozence a omezením kojení u HIV pozitivních matek.
K upřesnění je nutno dodat, že globální epidemie HIV/AIDS je způsobena virem HIV-1. Virus HIV-2 se vyskytuje jen v Africe, zejména na západním pobřeží (Pobřeží slonoviny). Má zřejmě méně agresivní patologii než HIV-1, vyvolává mírnější klinické projevy (slim disease) a velmi pomalu se šíří. Jeho výskyt nebyl zaznamenán na americkém kontinentu, v Evropě jen v Portugalsku, kde epidemie HIV/AIDS je vyvolána u poloviny diagnostikovaných případů virem HIV-2. Plyne to z významného mořeplaveckého styku Portugalska se západním africkým pobřežím. Z Portugalska se HIV-2 dostal do Španělska spolu s portugalskými dělníky, ale dále do Evropy se nerozšířil. Výskyt několika málo případů byl vždy spojen s pobytem v inkriminované oblasti a dále se nešířil.
Globální epidemie HIV/AIDS se skládá z jednotlivých sukcesivních regionálních epidemií. První nejvyšší a dosud přetrvávající vysoký výskyt byl zaznamenán v Africe, zejména její subsaharské části. K dalšímu rozšíření došlo v severní části amerického kontinentu (USA), kam se dostal HIV zřejmě jednak přímo z Afriky, jednak přes Haiti (viz Část I. publikace). Poté nastoupila západní část Evropy, později část centrální a nejmladší je epidemie HIV/AIDS v Evropě východní (Ukrajina, Bělorusko, Rusko a Pobaltské státy). Později než Evropa byla také postižena Jižní Amerika a asijský kontinent, kde nejdříve byla epidemie HIV/AIDS hlášena z jihovýchodní Asie.
Způsoby šíření HIV/AIDS se také regionálně liší. V opožděné epidemii HIV/AIDS v zemích východní Evropy se infekce nejvíce šířila a dosud šíří mezi injekčními uživateli drog. Klasickým příkladem tohoto způsobu přenosu HIV je Polsko, kde navíc zanechalo šíření HIV mezi narkomany těžké následky ve formě přenosu infekce z matky na dítě. Navíc bylo zjištěno, že virus HIV obsahovala vstřikovaná podomácku vyráběná halucinogenní látka tzv. „kompot“ (výluh ze zevního obalu makovic). Nicméně Polsko dokázalo s použitím širokého spektra intenzivních preventivních aktivit šíření epidemie efektivně zbrzdit.
Homosexuální přenos HIV je daleko snadnější než přenos heterosexuální. Plyne to z rozdílného způsobu tohoto styku. Styk homosexuální je především styk anální. Je známo, že střevní sliznice je bohatá na buňky k infekci HIV vnímavé, navíc tento styk bývá často krvavý. Přináší tedy skutečně vysoké riziko s dobrými podmínkami pro přenos viru HIV. Poševní sliznice a sekret ženského genitálu obsahuje relativně nízký počet HIV infikovaných buněk, a proto styk per vaginam je pro muže méně nebezpečný. Přenos HIV z muže na ženu je daleko vyšší – mužský ejakulát obsahuje vysoký počet virových partikulí a snadno infikuje slizniční buňky ženských genitálií. Je známo, že k infekci virem HIV je zapotřebí jeho velká koncentrace. Prokázalo se proto také, že prostitutky (komerční sexuální pracovnice) nejsou tím nejdůležitějším článkem v procesu šíření HIV/AIDS.
Obecně se zdá, že v současné době dosáhla epidemie HIV/AIDS svého vrcholu v zemích průmyslově vyspělých, nicméně v různých světových regionech a kontinentech jsou stále počty nově infikovaných osob a osob žijících s HIV/AIDS alarmující, jak ukazují čísla UNAIDS (United Nations AIDS Programme) z r. 2010. (grafy 1 a 2). Co se týče dětí (děti = věková skupina do 15 let), jedná se většinou o infekce přenesené z HIV infikované matky na dítě, i když aktivně získané infekce jsou také zaznamenávány (dětská prostituce).
Graf 1. Počet lidí žijícich s HIV, 1990–2010 (UNAIDS, WHO 2011) Graph 1. Numbers of people living with HIV, 1990–2010 (UNAIDS, WHO 2011) 
Graf 2. Počet nových HIV infekcí v letech 1990–2010 (UNAIDS, WHO 2011) Graph 2. Newly diagnosed HIV cases in 1990–2010 (UNAIDS, WHO 2011) 
PREVENCE HIV/AIDS
Specifická prevence ve formě efektivní HIV vakcíny není dosud, přes velké celosvětové úsilí renomovaných pracovníků na nejrenomovanějších pracovištích, k dispozici. Byly sice vyvinuty nejrůznější typy vakcín na nejrůznějších podkladech, některé z nich se dostaly až do fáze klinických zkoušek. Některé navodily i vysokou tvorbu specifických protilátek, nicméně protektivní charakter nevykazovaly. Má to řadu konkrétních příčin včetně vysoké mutagenosti viru HIV (není účelem tohoto článku je rozebírat), nicméně někteří špičkoví světoví imunologové, vakcinologové a virologové jsou tak skeptičtí, že možnost konstrukce účinné HIV vakcíny popírají, až vylučují.
Zbývá tedy prevence založená na výchově a osvětě, zejména populačních skupin ve vysokém riziku infekce. Široce založená, moderní osvětová činnost u mladistvých by měla jít ruku v ruce s výchovou morální a etickou. To je úkol přetěžký, který nespočívá jen na bedrech odborníků, ale celé lidské společnosti.
ZÁVĚR
Závěrem je možno říci, že odhadnout další průběh globální epidemie HIV/AIDS je nesnadný úkol. Přímo se nabízí hezký anglický výraz, „unpredictable“, který někteří v tomto případě užívají. Epidemii, její konec či další vzplanutí, skutečně předpovědět nelze. Nicméně pesimismus v boji proti ní rozhodně není na místě.
Pozn. Použité obrázky, tabulky, schémata a grafy jsou z archivu autorky textu. Za pomoc při jejich grafickém zpracování a uspořádání děkujeme Mgr. Martě Marešové.
Po domluvě autorky i šéfredaktorů, byl článek uveřejněn i v časopise Zprávy CEM (SZÚ, Praha).
Do redakce došlo dne: 10. 4. 2012
RNDR. Marie Brůčková
emeritní vedoucí NRL pro AIDS
marie.bruckova@centrum.cz
Štítky
Hygiena a epidemiologie Infekční lékařství Mikrobiologie
Článek vyšel v časopiseEpidemiologie, mikrobiologie, imunologie
Nejčtenější tento týden
2012 Číslo 3- Parazitičtí červi v terapii Crohnovy choroby a dalších zánětlivých autoimunitních onemocnění
- Vakcíny proti klíšťové encefalitidě
- Kdy je nejlepší očkovat
- Možné vedlejší účinky očkování
- Imunogenita vakcín
-
Všechny články tohoto čísla
- Vyšetřování rodinných a sexuálních kontaktů HBsAg pozitivních osob v Plzeňském kraji
- Chromozomální integrace šestého lidského herpesviru (HHV-6)
- Pravidla pro přepravu mikroorganismů
- Třicet let od popsání prvních případů AIDS: historie a současnost Část II.
- PhMgr. Jaroslav Švec – životní jubileum
- In memoriam MUDr. Jindřišky Galliové (28. 7. 1913 – 26. 3. 2012)
- Zemřela doc. MUDr. Milada Závadová, CSc.
- Epidemiologie, mikrobiologie, imunologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Chromozomální integrace šestého lidského herpesviru (HHV-6)
- Pravidla pro přepravu mikroorganismů
- Třicet let od popsání prvních případů AIDS: historie a současnost Část II.
- Vyšetřování rodinných a sexuálních kontaktů HBsAg pozitivních osob v Plzeňském kraji
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: MUDr. Petr Výborný, CSc., FEBO
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



