-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
PRERETINOPATIE U DIABETU 1. TYPU V KONTEXTU FUNKČNÍCH, STRUKTURÁL-NÍCH A MIKROCIRKULAČNÍCH ZMĚN MAKULÁRNÍ OBLASTI
PRE-RETINOPATHY OF TYPE 1 DIABETES IN THE CONTEXT OF FUNCTIONAL, STRUCTURAL AND MICROCIRCULATORY CHANGES IN THE MACULAR AREA
Aim: The authors assessed the development of intraocular changes in type 1 diabetes (T1DM) from the onset of the disease leading to diabetic retinopathy (DR). The quote: “There must be an intermediate stage between the physiological intraocular finding and the diabetic retinopathy itself “, (prof. Jan Vavřinec).
Methods: A two-year study (2018 and 2019) was conducted at the Department of Ophthalmology of the Teaching Hospital Kralovske Vinohrady in Prague (Czech Republic). There were 54 patients aged 17–42 years, the detection of T1DM ranged between the 1st and 14th year of life, with a duration of 12–35 years. Individual patients were always examined simultaneously by three methods: CS (contrast sensitivity), SD-OCT (spectral domain optical coherence tomography) and OCT-A (optical coherence tomography-angiography). We examined 106 eyes once and in a comprehensive manner.
Results: We have shown that there is an intermediate stage between the physiological finding on the retina and DR, so-called diabetic pre-retinopathy (DpR). Subsequent redistribution of the observed into two DpR subgroups was derived from the size of the FAZ, either with its smaller area or with a larger area determining the microvascularity of the central area of the retina. The results of both other methods were assigned to these values. For SD-OCT, the depth of the fovea (the difference between the central retinal thickness and the total average retinal thickness) was determined, which was affected by the increased the macular cubature. In all patients it was on average 10.3 μm3. The retina in the central area was significantly strengthened compared to the healthy population at the level of significance p ≤ 0,001. We divided the actual DpR into an image: DpR1 in 26.5 % of eyes – condition with an average shallower fovea only by 21.5 μm below the level of the surrounding retina and an average narrower FAZ: 0.165 mm2 and with a more significant decrease in CS; DpR2 in 40.5 % of eyes – condition with average deeper fovea by 42 μm, i.e., more significantly and average larger FAZ: 0.325 mm2 with lower decrease of CS. At the same time, other changes in microvascularity were noted, such as disorders in the sense of non-perfusion in the central part of the retina of various degrees. This finding differed significantly from changes in already established (non-proliferative) NPDR in 36 % of eyes, when a significant decrease in CS with normal visual acuity was found 4/4 ETDRS. Statistical differences in CS between DpR1 and DpR2 and NPDR were determined – always p ≤ 0.001. The average depth of the fovea was NPDR: 29.5 μm. NPDR had the largest average FAZ: 0.56 mm2. Also significant were the most significant changes in non-perfusion and especially the presence of microaneurysms.
Conclusions: These three non - invasive methods helped to monitor the dynamics of the development of ocular changes in T1DM of better quality than the determination of visual acuity and ophthalmoscopic examination. Increased retinal volume induced hypoxia of visual cells with subsequent dual autoregulatory mechanism conditioning two types of diabetic pre-retinopathy before the onset of DR.
Keywords:
contrast sensitivity – Diabetic retinopathy – OCT-A – SD-OCT – T1DM
Autoři: J. Krásný; L. Magera; P. Pluhovský; J. Čeledová; L. Holubová
Působiště autorů: Oční klinika Fakultní nemocnice Královské Vinohrady v Praze
Vyšlo v časopise: Čes. a slov. Oftal., 77, 2021, No. 4, p. 170-182
Kategorie: Původní práce
doi: https://doi.org/10.31348/2021/20Souhrn
Úvod: Autoři posuzovali vývoj nitroočních změn u diabetiků 1. typu (T1DM) od počátku choroby směřující až k diabetologické retinopatii (DR).
Motto: „Musí existovat mezistupeň mezi fyziologickým nitroočním nálezem a vlastní diabetickou retinopatií“, (prof. Jan Vavřinec).
Metodika: Na Oční klinice Fakultní nemocnice Královské Vinohrady v Praze proběhla dvouletá studie (2018–2019). Jednalo se o 54 nemocných ve věku 17–42 let, detekce T1DM se pohybovala mezi 1. a 14. rokem života, s délkou jeho trvání 12–35 let. Jednotliví pacienti byli vždy vyšetření současně třemi metodami: CS (citlivost na kontrast), SD-OCT (spektrální optická koherenční tomografie) a OCT-A (optická koherenční tomografie – angiografie). Jednorázově a komplexně jsme vyšetřili 106 očí.
Výsledky: Prokázali jsme, že existuje mezistupeň mezi fyziologickým nálezem na sítnici a DR, a to tzv. diabetická preretinopatie (DpR). Následné přerozdělení sledovaných do dvou podskupin DpR jsme odvodili od velikosti foveální avaskulární zóny (FAZ), buď s její menší plochou nebo s větší plochou určující mikrovaskularitu centrální části sítnice. K těmto hodnotám byly přiřazeny výsledky obou dalších metod. U SD-OCT byla určena hloubka foveoly (rozdíl mezi centrální tloušťkou sítnice a průměrnou tloušťkou sítnice), která byla ovlivněna zvýšenou kubaturou makulární oblasti. U všech nemocných byla v průměru 10,3 μm3. Sítnice v centrální oblasti byla signifikantně zesílena oproti zdravé populaci na hladině významnosti p ≤ 0,001. Vlastní DpR jsme rozdělili na obraz: DpR1 u 26,5 % očí – stav s průměrně mělčí foveou jen o 21,5 μm pod úrovní okolní sítnice a průměrně užší FAZ: 0,165 mm2 a s výraznějším poklesem CS; DpR2 u 40,5 % očí – stav s průměrně hlubší foveolou o 42 μm, tedy výrazněji a průměrně rozsáhlejší FAZ: 0,325 mm2 s nižším poklesem CS. Současně byly zaznamenány další změny microvaskularity jako jsou poruchy ve smyslu neperfuze v centrální části sítnice různého stupně. Tento nález se významně odlišoval od změn, u již vzniklé (neproliferativní DR) NPDR u 36 % očí, kdy byl zjištěn zásadní pokles CS při normální zrakové ostrosti 4/4 ETDRS. Byly stanoveny statistické rozdíly u CS mezi DpR1 a DpR2 a NPDR: vždy p ≤ 0,001. Průměrná hloubka foveoly byla u NPDR: 29,5 μm. NPDR měla nejrozsáhlejší průměrnou FAZ: 0,56 mm2. Také podstatné byly nejvýraznější změny neperfuze a hlavně přítomnost mikroaneurysmat.
Závěr: Tyto tři neinvazní metody napomáhaly sledovat dynamiku vývoje očních změn u T1DM kvalitněji než stanovení zrakové ostrosti a oftalmoskopické vyšetření. Zvýšená kubatura sítnice vyvolala hypoxii světločivých buněk s následným dvojím autoregulačním mechanismem podmiňujícím dva typy diabetické preretinopatie před vznikem DR.
Klíčová slova:
CS – diabetická retinopatie – OCT-A – SD-OCT – T1DM
ÚVOD
V rámci vývoje očních změn podmíněných T1DM (diabetes mellitus 1. typu) přechází fyziologický nález na sítnici v patologickou diabetickou retinopatii (DR). Objasňování patogeneze a patofyziologie DR je spojeno s Cunha-Vazovým objevem fluorofotometrie na konci 70. let minulého století [1,2]. Metoda umožnila popsat zhroucení hematookulární bariéry a vedla k zavedení termínu preretinopatie [3], která tvoří právě tento mezistupeň. Vlastní DR je definovaná svými příznaky, mezi které patří mikroaneurysmata (MA), hemoragie, flebopatie, intraretinální abnormality a vatovitá ložiska. DR se dělí na několik stupňů. Nejzávažnějším postižením z hlediska zrakové ostrosti představuje přítomnost diabetického makulárního edému (DME) [3,4]. Diabetická preretinopatie (DpR) je spojena především se změnami makulární oblasti pro metabolickou náročnost výživy této oblasti. Byla již popsána jako mikroangiopatické abnormality s nepravidelností kapilár a s jejich tortuositou a dilatací [5,6,7,8], zasahující hlouběji do avaskulární foveoly. K dalším příznakům DpR patří změna kresby makulární krajiny, tzv. skvrnitost makuly, což představovalo vymizení foveolárního reflexu a změnu pigmentace se světlejšími okrsky mapovitého charakteru, jak znázorňuje obrázek 1. K příznakům je možno přiřadit eventuální přítomností tečkovité formy tvrdého exsudátu (TE) [6,7], což jsou makrofágy plné lipoproteinů [3].
Obr. 1. Vlevo: obraz mapovité pigmentace a depigmentace v centrální oblasti sítnice a vpravo: detail „makulární skvrnitosti“ 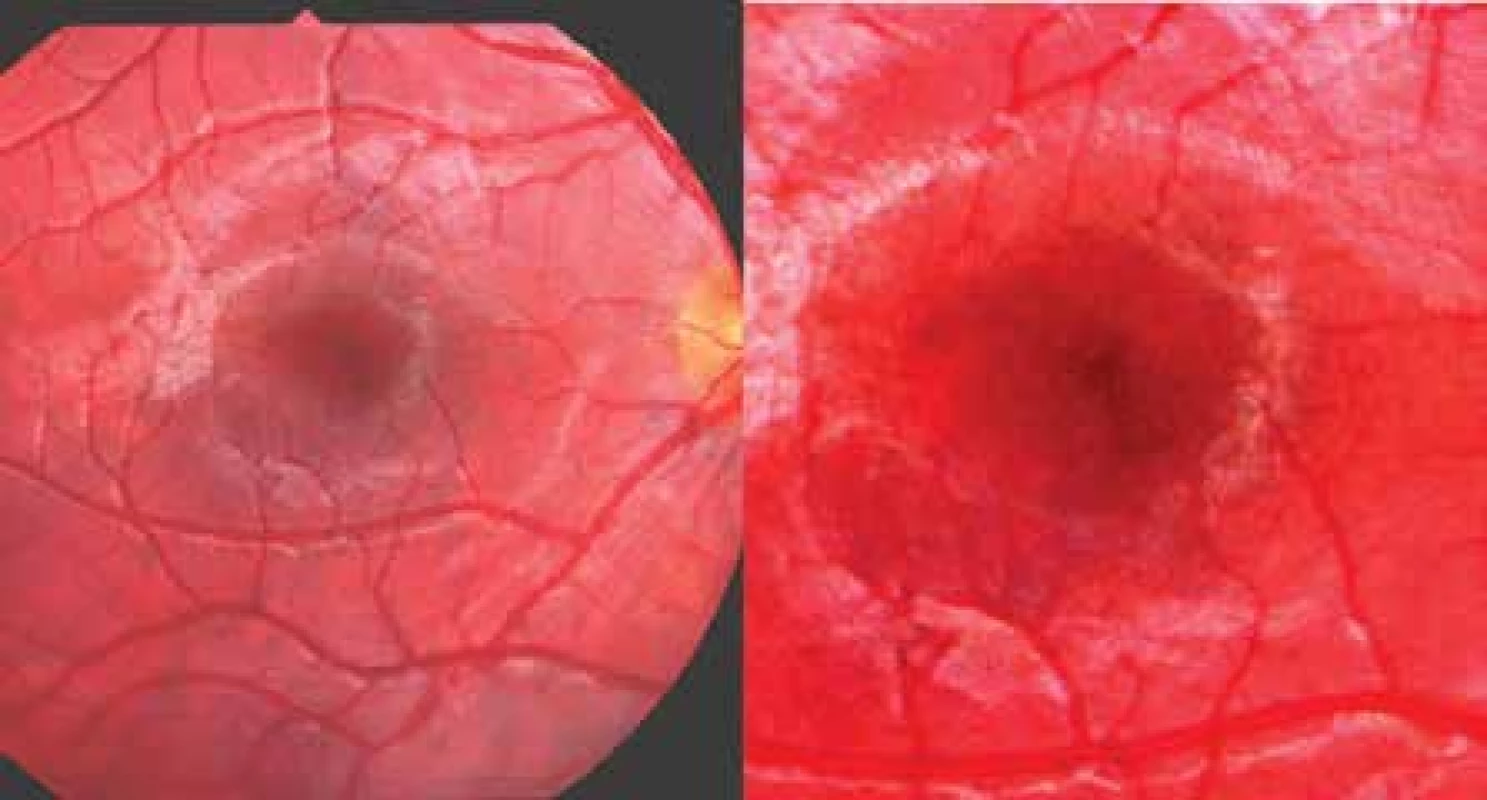
V uplynulých dvou desetiletích jsme se zabývali výzkumem DpR u T1DM z hlediska komplexních změn u citlivosti na kontrast (CS) [7,9]. Další pilotní studie srovnávaly změny fyziologické sítnice s DpR a NPDR (neproliferativní diabetická retinopatie) pomocí SD-OCT (spektrální optická koherenční tomografie) [10] a OCT-A (optická koherenční tomografie-angiografie) [11]. Náplní tohoto sdělení je posouzení DpR z hlediska komplexního vzájemného vztahu funkčních změn pomocí CS, strukturálních změn za využití SD-OCT a mikrocirkulačních změn při posouzení nálezů OCT-A.
SOUBOR A METODIKA
V letech 2018–2019 bylo na Oční klinice Fakultní nemocnice Královské Vinohrady v Praze vyšetřeno 54 pacientů s T1DM. Jednalo se o 28 mladých mužů a 26 mladých žen ve věku 17–42 let, průměr 24,6 let. Metabolické onemocnění začalo v rozmezí jednoho roku až čtrnácti let, průměr 5,5 let a doba jeho trvání byla 12–35 let, průměrně 18,4 let. Komplexní vyšetření zahrnovalo stanovení optimální zrakové ostrosti (ZO), která byla 4/4 ETDRS naturálně či s optimální korekcí (ojediněle s chybou 1–2 písmen), posouzení čirosti čočky na štěrbinové lampě, biomikroskopické vyšetření očního pozadí, ale také přímá oftalmoskopie ke sledování detailů v makulární krajině. Součástí hodnoceného vyšetření v daném věku muselo být současně provedené CS, SD-OCT a OCT-A.
CS je funkčním vyšetřením detekujícím lépe stav zrakového analyzátoru než vyšetření centrální ZO. Informuje o kvalitě zpracování daného optického stimulu, o rozdílných prostorových frekvencích, odesílaných ze světločivých buněk sítnice do zrakového centra v mozkové kůře různými kanály. Magnocelulární systém dominuje na zpracování nízkofrekvenčních prahových podnětů základní a chromatické CS, zatímco parvocelulární systém přenáší především data vysokofrekvenčních podnětů s vysokou prostorovou rozlišitelností [12]. CS jsme hodnotili pomocí přístroje CSV 1000 (Vector Vision, USA) se 4 dvojřadami (páry) kruhových podnětových terčů o prostorových frekvencích 3, 6, 12, 18 cyklů na úhlový stupeň (c./st.). Vedle vzoru je celkem vždy 8 sloupců terčů s klesající úrovní kontrastu. Vyšetření jsme prováděli v místnosti s konstantním osvětlením 450 lux a přístroj byl kalibrován na fotopickou hladinu 85 cd/m2. Jako prahový kontrast byl hodnocen posledně správně určený terč. Terče 18 c./st. představují oblast foveoly, 12 c./st. foveální, 6 c./st. parafoveální oblast a 3 c./st. perifoveární oblast [13]. Průměr foveoly je 350 μm, průměr centrální fovey je 1500 μm, průměr parafoveální oblasti je 2500 μm a perifoveální oblasti 5500 μm [14]. Za stanovený standard jsme určili pro 3 c./st.: 6,4 ±0,4 (A), že hraniční hodnotu představuje 6. terč. Pro 6 c./st.: 7,1 ±0,3 (B), pro 12 c. st.: 7,1 ±0,5 (C) a konečně pro 18 c./st.: 7,2 ±0,6 (D). Pro všechny tyto tři cykly představuje hraniční hodnotu 7. terč. Vzhledem k tomu, že se jedná o exponenciální funkci v rámci hodnocení jednotlivých cyklů, nikoliv o lineární křivku, má podobu neúplné exponenciální spirály. Měřené hodnoty pro vzájemné hodnocení se převádí do logaritmického vztahu, a to s posunem 0,15 log na jeden terč a jeden cyklus podle doporučení výrobce [13]. Vlastní standard pro věk 11–19 let se stal podkladem pro hodnocení CS v naší studii a využili jsme jej i u mladých diabetiků. Rozmezí pro dospělé uváděné výrobcem je pro veškeré věkové skupiny v dospělosti. Se svým rozptylem je pro mladší jedince nevhodné. Výstupem byly i normy pro věkovou skupinu 6 až 11 let a obě se staly náplní grantu IGA NR/7952-3 [15]. Oba standardy CS byly navíc zařazeny do podkladů v rámci doporučení výrobce [13].
SD-OCT je analogií B-skenu při ultrazvukovém vyšetření. Principem je nízko-koherenční interferometrie, která měří vzdálenosti různých struktur uvnitř tkáně s vysokou citlivostí k signálu světla odraženého od struktur oka. Představuje metodu trojrozměrného hodnocení struktur sítnice a cévnatky [15]. K vyšetření jsme využívali přístroj Cirrus OCT (Carl Zeiss, Německo). Do měřených parametrů SD-OCT jsme zařadili kubický obsah měřené kostky sítnice ve vymezeném kvadrantu makulární oblasti 36 mm2. Hodnotí eventuální ztluštění centrální části sítnice o větším rozsahu lépe než jen samostatná centrální tloušťka sítnice. Druhým statisticky hodnoceným parametrem byla skutečná hloubka vlastní foveoly jako rozdíl mezi centrální tloušťkou sítnice a průměrnou tloušťkou sítnice. Vztah lépe posoudil charakter tvaru foveoly ve vztahu s eventuálnímu ztluštění sítnice, které ovlivňuje oxygenaci sítnice dané oblasti než výše uvedené dvě tloušťky sítnice, z kterých nelze toto ovlivnění odečíst. Hodnotili jsme rovněž přítomnost TE a eventuální DME. Normou pro obsah kostky centrální části sítnice 6 x 6 mm2 jsme propočítali 10,0 ±0,3 μm3. Centrální tloušťku sítnice jsme změřili: 240 ±17 μm a průměrnou tloušťku sítnice: 281 ±10 μm. Výpočet výsledné hloubky foveoly stanovil odečet centrální od průměrné tloušťky sítnice a představoval -32 ±15 μm, neboť za fyziologického stavu je foveola pod úrovní ostatní sítnice svým vklesnutím [10]. Znaménko mínus vysvětluje tento stav na rozdíl od DME, který je nad úrovní centrální části sítnice včetně foveou, což značí plusovou hodnotu.
OCT-A hodnotí kvalitativní a kvantitativní hemodynamiku cév sítnice a cévnatky kvantitativním měřením rychlosti průtoku krve dosažené použitím Dopplerovy techniky pracující na principu proměnlivé reflektivity na membránách proudících krevních elementů [17]. Pro zobrazení mikrovaskulatury sítnice vyšetřením OCT-A jsme využívali přístroje Spectralis (Heidelberg Engineering, Německo/USA). K měření jsme použili vlastní specifické nastavení, kdy přístroj provedl v režimu vysokého rozlišení 7 snímků ve stejném řezu sítnice. Tímto způsobem jsme zobrazili plochu 15 x 15 stupňů, což odpovídá přibližně 4,4 x 4,4 mm výřezu sítnice a cévnatky. V daném nastavení jsme dosáhli kompromisu mezi potřebnou kvalitou zobrazení cév a hardwarovými možnostmi přístroje. Segmentace vrstev sítnice proběhla automaticky a ve všech případech správně (nebyla nutná manuální korekce). Z důvodu nejdokonalejšího a nejkontrastnějšího zobrazení foveolární avaskulární zóny (FAZ) jsme vybrali složený obraz ze všech vaskulárních komplexů sítnice, tedy superficiálního vaskulárního segmentu (SVC), dále intermediálního vaskulárního segmentu (IVC) a nakonec hlubokého vaskulárního segmentu (DVC). Terminologie je nejednotná, české označení vychází z rozsáhlé monografie o OCT-A [17] a zkratka vychází z anglického, významem, rozsáhlejšího označení SVC/DVC: „superficial/deep vascular complex“, stále je používaná i další, dřívější zkratka SCP/DCP: „superficial/deep capillar plexus“. Použitím vestavěné funkce „Draw Region“ bylo možné manuálně vyznačit oblast FAZ, a tímto způsobem jsme vypočítali její plochu. Za normu zdravé mladé populace pro FAZ jsme stanovili plochu o rozměru 0,253 ±0,092 mm². Všeobecně patologická hodnota FAZ u T1DM bez specifikace očního nálezu byla 0,300 +0,132 mm². Také jsme hodnotili tvar FAZ, kapilární aktivitu v okolí a přítomnost eventuálních MA.
DpR se projevovala celkem pravidelným tvarem FAZ, zatímco u NDPR byl tvar nepravidelný. Rozdílnost v kapilární aktivitě a její charakteru a plochy rozdělilo DpR na dva typy: DpR1 (užší FAZ) a DpR2 (širší FAZ). Při DpR1 provázela v SVC nepravidelnost parafoveolárních kapilár se známkami neperfuze, zatímco u DpR2 byly zóny neperfuze četnější, a navíc zde byl náznak přesahu kapilárních svazků do FAZ, což u DpR1 chybělo. Nález v DVC se lišil ve stupni prořídnutí kapilární sítě, neboť u DpR2 byl výraznější než u DpR1. U NPDR byla FAZ nepravidelná s mnohočetnými zónami neperfuze s MA v SVC a s dilatací kapilární sítě v DVC [11].
Obrázek 2 znázorňuje fyziologický nález na očním pozadí u zdravého 26letého pacienta s Hb1Ac 38 mmol/mol a rozsah standardu CS s grafem cyklů ve fyziologickém rozmezí, SD-OCT s hloubkou foveoly -37 μm a FAZ (OCT-A) o ploše 260 mm² v obrazu složených vaskulárních segmentů.
VÝSLEDKY
Tabulky 1 a 2 shrnují časové faktory T1DM ve vztahu k DpR a NPDR s absolutními hodnotami CS, SD-OCT a OCT-A u jednotlivých pacientů této 2leté studie. DpR je v tabulce rozdělena na horní část pro DpR 1. typu a dolní část pro DpR 2. typu, aby byly jasně patrné rozdíly v jednotlivých parametrech. Toto metabolické onemocnění s eventuálními očními příznaky jsme sledovali 12–17 let, v průměru 15 let. První příznaky vzniku DpR jsme diagnostikovali pomocí přímé oftalmoskopie v době trvání T1DM 14–23 let, v průměru 17,4 roku a na ně navazovaly nitrooční projevy NPDR vzniklé za dobu trvání choroby od 17 do 31 let, v průměru 23 let.
Tab. 1. Časové faktory T1DM a diabetická preretinopatie s absolutními hodnotami CS (cykly/stupeň), SD-OCT: makulární kubatura (μm3) a foveolární hloubka (μm), OCT-A (FAZ – mm2) 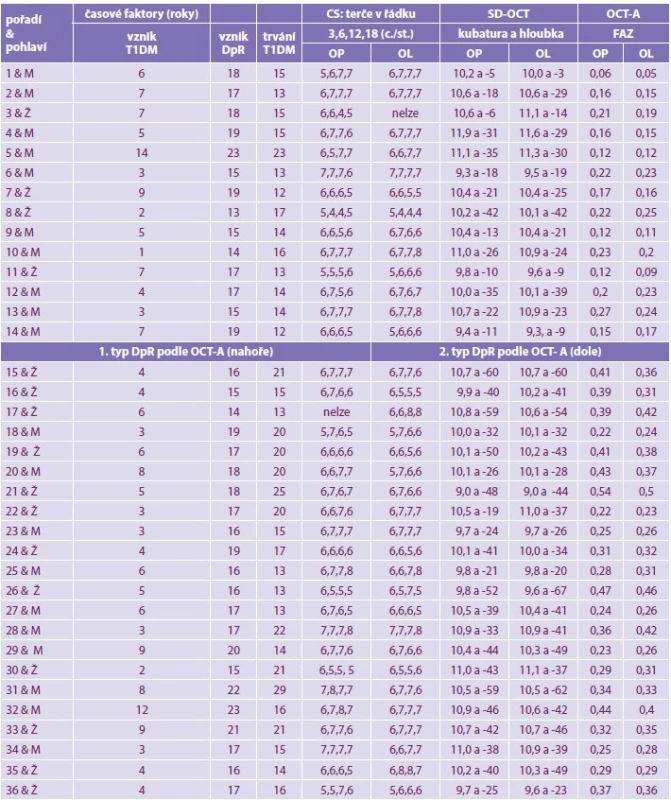
Tab. 2. Časové faktory T1DM a NPDR s absolutními hodnotami CS (cykly/stupeň), SD-OCT: makulární kubatura (μm3) a foveolární hloubka (μm), OCT-A (FAZ – mm2) 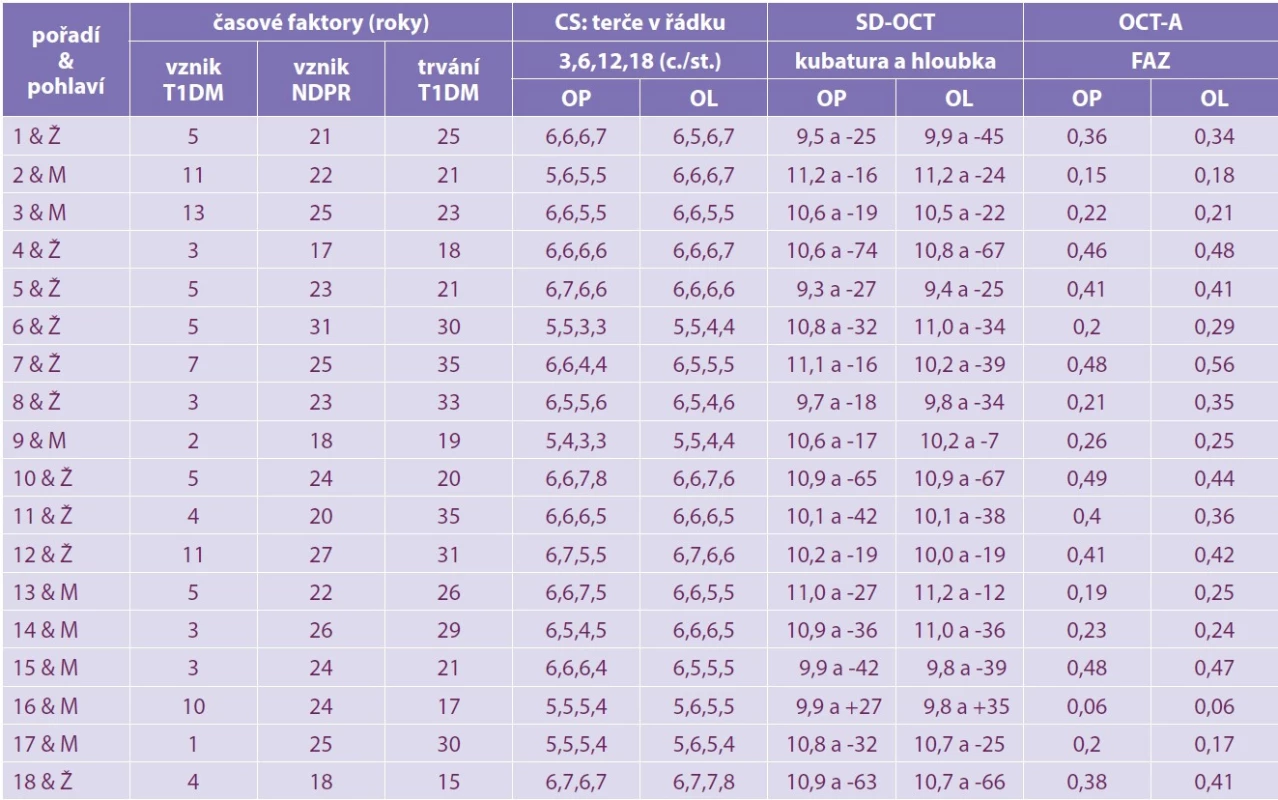
CS: Vyšetření u všech pacientů prokázalo změny v kvalitě hodnot (Tabulka 3). Ve srovnání jednotlivých cyklů na stupeň byla hodnota u DpR1, DpR2 i NPDR hraniční u 3 c./st. U DpR obou typů byla hodnota 6 c./st. také hraniční, ale zbývající cykly (12 i 18 c./st.) byly snížené. U NPDR byly cykly 6, 12 a 18 c./st. vždy snížené. Vzájemný statistický rozdíl mezi jednotlivými typy očního postižení byl významný: p ≤ 0,001. Nejmenší rozdíl p ≤ 0,001 byl ve vztahu DpR1 versus (vs) DpR2 a největší rozdíl p ≤ 0,0001 byl ve vztahu DpR1 vs NPDR.
Tab. 3. Logaritmické hodnoty CS (cyklů/stupeň v řádku) 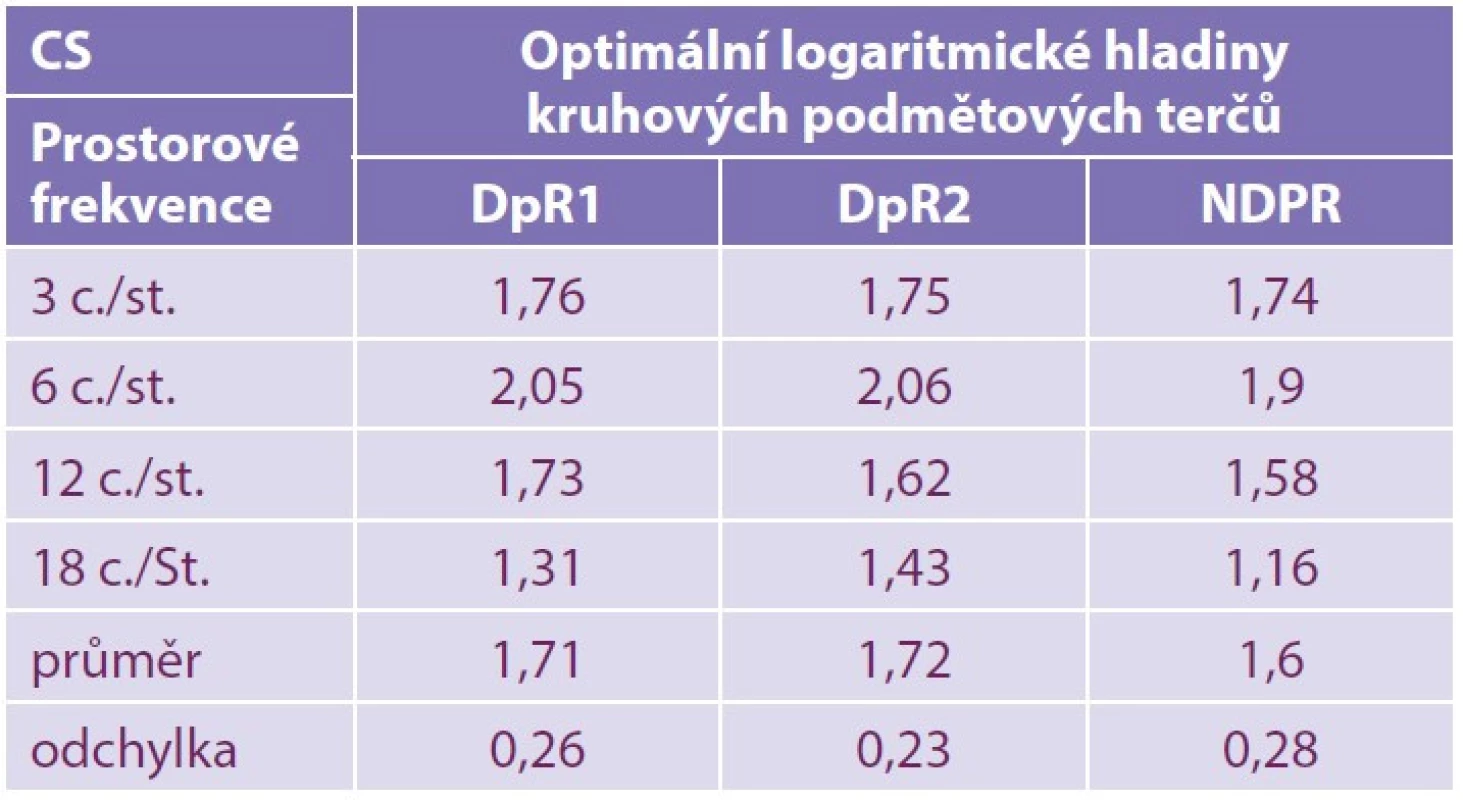
SD-OCT: Kubatura se pohybovala u DpR1 v rozmezí 9,3–11,9 μm3, v průměru 10,4 μm3 a u DpR2 to bylo 9,0–1,1 μm3, v průměru 10,3 μm3. U NPDR se příliš nelišila, a to od 9,3 do 11,2 μm3, v průměru 10,2 μm3 (Graf 1). Statistické porovnání nevykázalo zásadní rozdíl: DpR1 vs DpR2 – p = 0,198, DpR1 vs NPDR – p = 0,461 a DpR2 vs NPDR – p = 0,132. Vyplývá z toho, že ztluštění (prosáknutím) centrální části sítnice bylo po dobu trvání T1DM od 14 do 35 let obdobné v průměru 10,3 μm3. Byl to zásadní rozdíl ve srovnání s fyziologickou sítnicí u sledovaných bez metabolického onemocnění (10,0 ±0,3 μm3), na hladině významnosti p ≤ 0,001. Hloubka foveol vykazovala zásadní změny, a to u DpR1 se pohybovala mezi -42 μm až -3 μm, v průměru -21,5 μm, zatímco u DpR2 byl rozptyl větší, a to -67 μm až -19 μm, s průměrem -41 μm. Největší rozptyl vykazovala NPDR od -74 μm až +35 μm, v průměru -29,5 μm (Graf 2). Z uvedených hodnot také vycházel výrazný statistický rozdíl: DpR1 vs DpR2 – p = 0,007, DpR1vs NPDR – p ≤ 0,001 a DpR2 vs NPDR – p = 0,034. Tyto rozdíly byly podmíněny zastoupením mělkých foveol pod -17 μm na 36 % očí u DpR1 (u tohoto typu DpR nebyla zachycena žádná hlubší foveola) a jen potvrzených hlubších foveol nad -47 μm na 27 % očích u DpR2. NPDR vykazovala obě formy foveol, tedy mělkých a hlubších, ve stejném procentu, a to u 17 % očí.
Graf 1. Kubatura makul u diabetické preretinopatie 1,2 a NPDR 
Graf 2. Hloubka foveol u diabetické preretinopatie 1,2 a NPDR 
Obr. 2. Fyziologický nález tří neinvazních vyšetřovacích metod: CS, SD-OCT, OCT-A (povrchový/hluboký vaskulární segment – SVC/DVC) a fotografie fundu 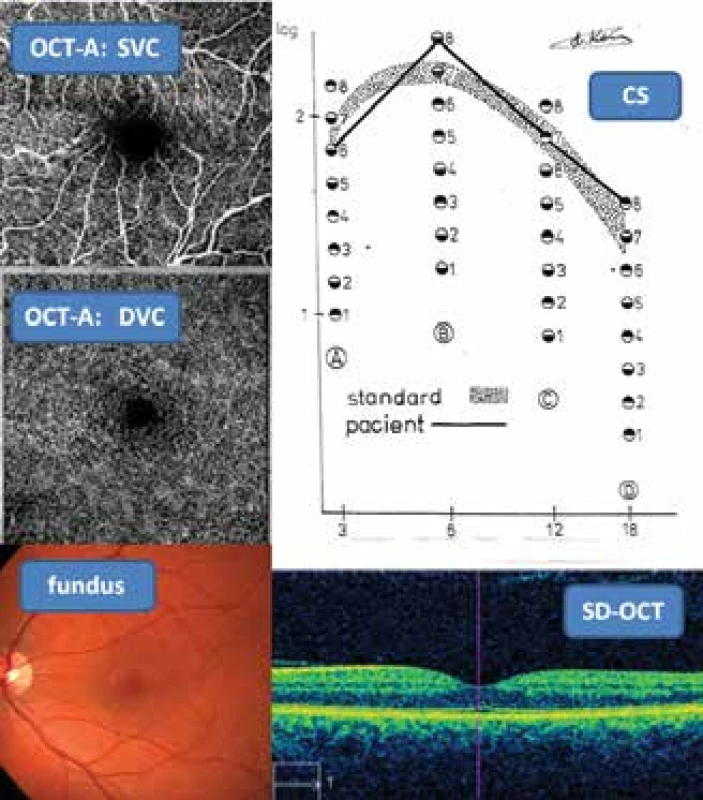
Graf 3. FAZ (foveolární avaskulární zóna) u diabetické preretinopatie 1,2 a NPDR 
OCT-A: FAZ se svými rozměry podobal DpR2 a NDPR. Lišil se přítomností MA, dilatací kapilár spolu s vyšším zastoupením avaskulárních zón a nepravidelností tvaru FAZ jen u NPDR. FAZ u DpR2 vykazoval rozmezí 0,06–0,54 mm², s průměrem 0,325 mm² a u NPDR byl rozsah širší od 0,06–0,565 mm², s průměrem 0,56 mm². U DpR1 byl rozsah užší, a to od 0,05 do 0,27 mm², s průměrem 0,165 mm² (Graf 3). Statistické hodnocení bylo proto zcela nevýznamné mezi DpR2 a NPDR – p = 0,212, zatímco bylo zásadní mezi DpR1 vs DpR2 či DpR1 vs NPDR – p ≤ 0,001.
Přímá oftalmoskopie versus OCT: Vinutost koncových kapilár v makulární krajině se na OCT-A projevila zúžením FAZ především u DpR1, ale ojediněle u DpR2 nebo u NPDR. TE byly přímo viditelné na sítnici. V souvislosti se „skvrnitostí“ sítnice se v obraze SD-OCT objevily hyperreflexní body s eventuálním akustickým stínem v zevní plexiformní vrstvě u DpR i NPDR. MA byly patrné oftalmoskopicky jako červené ostře ohraničené body na sítnici u NPDR, a to lépe v bezčerveném světle. V obraze OCT-A byly MA daleko lépe detekovatelné i nárůstem jejich počtu oproti oftalmoskopii.
SD-OCT versus OCT-A v kontextu s CS: Porovnání dvou objektivních vyšetřovacích metod prokázalo zásadní změlčení foveol ≤ 17 μm na SD-OCT u 10 očí s DpR1 (pacienti č. 1, 2, 6, 9, 11, 14 – Tabulka 2) a u 6 očí s NPDR (pacienti č. 2, 7, 9, 16 – Tabulka 1). Hodnota změlčení vycházela z hodnoty průměrné normy při odečtení směrodatné odchylky. Projev zásadního změlčení foveol jsme u DpR2 nedetekovali. Naopak výrazné prohloubení foveol ≥ 47 μm na SD-OCT bylo u 10 očí s DpR2 (pacienti č. 15, 17, 19, 21, 29, 31 – Tabulka 2) a u 6 očí s NPDR (pacienti č. 4, 10, 18 – Tabulka 1). Hodnota prohloubení foveol vycházela z průměrného standardu naopak s připočtením směrodatné odchylky. U pacientů s DpR1 jsme hlubší foveou neprokázali. Posouzení přiřazeného subjektivního vyšetření CS bylo proměnlivé. U mělčích foveol a menších ploch FAZ bylo vyšetření CS provázeno poklesem bez hraniční hodnoty u všech cyklů/stupeň, a to na jednotlivých očích v 75 % u DpR1 a 83 % u NDPR. Souhrnný patologický pokles hodnot CS na všech očích byl jen v 41 % u DpR2, dále u DpR1 v 60 % a nejvýraznější byl u NPDR v 68 %. U hlubších foveol s rozměrnější plochou FAZ byla CS bez patologických hodnot v 50 % u DpR2 a v 25 % u NPDR. Celkově normální či hraniční hodnoty CS byly u všech cyklů/stupeň na očích v 40 % u DpR1 a jen v 32 % u NDPR. Nejmenší postižení CS bez patologických hodnot představoval nález u DpR2 na 59 % jednotlivých očí. Rozhodující pro pokles CS u DpR, nebyl 1. či 2. typ DpR, ale hloubka foveol z hlediska oxygenace světločivých buněk a z toho vyplývající sekundární kapilární reaktivita. Zásadní rozdíl mezi oběma formami DpR a NPDR kromě poklesu CS byl nález na OCT-A. DpR2 i NPDR měly většinou rozsáhlejší plochu FAZ, ale u DpR2 to bylo celkovou konfigurací fovey podmíněnou hloubkou fovey a přesahem kapilár do FAZ pro zhoršenou oxygenaci sítnice. U NPDR byla konfigurace nepravidelná pro ztrátu kapilár, čemuž odpovídala výraznější neperfuze. Navíc u NPDR byla patrná přítomnost MA v SVC a nepravidelná dilatace kapilár v DVC.
HbA1c: Ve dvouletém sledování byl posouzen vývoj hladin HbA1c u dvou skupin pacientů, a to u 8 pacientů (DpR1 a NPDR) s mělčí foveolou a menší plochou FAZ. Jeho hodnota se pohybovala rozmezí 45–80 mmol/mol, v průměru 66 mmol/mol. Hodnotu Hb1Ac pod 60 mmol/mol v daném období měli jen dva pacienti. Druhou skupinu tvořilo 10 pacientů (DpR2 a NPDR) s hlubší foveolou a zvětšenou plochou FAZ, hodnota HbA1c byla v mezi 47–117 mmol/mol, v průměru 64 mmol/mol. Celkem čtyři nemocní z této podskupiny měli hodnotu Hb1Ac pod 60 mmol/mol. Nejednalo se o kumulativní hodnocení Hb1Ac v období nejméně 5 let. Navíc hodnocený soubor nebylo možno statisticky posoudit pro malý počet probandů. Metabolická kompenzace byla v průměru pro obě skupiny obdobná. Zařazený rozbor čtyř nemocných T1DM hodnotil individuálně dva typy DpR a dvakrát NPDR s rozdílnými hloubkami foveol a velikostí FAZ.
Obrázek 3 – DpR1: 21letý diabetik, kdy metabolické onemocnění vzniklo v 6 letech života a DpR1 se projevila před 3 roky (pacient č. 1 – Tabulka 1). Hladina Hb1Ac se v době trvání dvouleté studie pohybovala v rozmezí 52–62 mmol/mol. Dokumentovaný nález vpravo – CS byla patologická v 3 a 6 c./st. SD-OCT vykazovala centrální tloušťku 279 μm, průměrná tloušťka sítnice byla 284 μm, z čehož vyplynula velice mělká foveola -5 μm s přítomností hyperreflexních bodů. FAZ byla pravidelného tvaru o ploše 0,06 mm², v SPC s minimálními známkami neperfuze, což se projevilo i v DCP s prakticky vymizelou FAZ. Na fundu byla patrná „skvrnitost“ v oblasti foveoly a jejího okolí.
Obr. 3. DpR1: CS, SD-OCT, OCT-A a fundus u pacienta 1 (Tabulka 1) 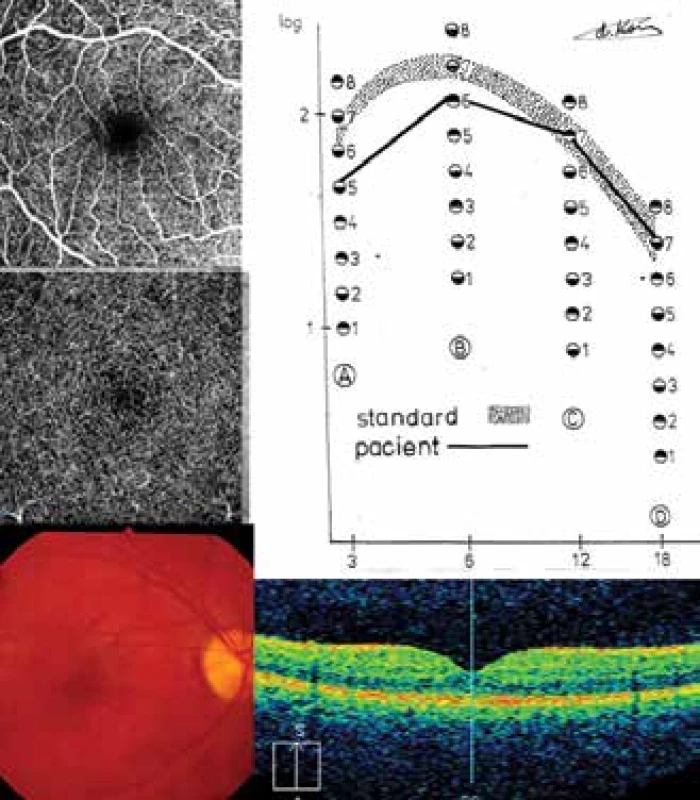
Obrázek 4 – DpR2: Mladá diabetička, se vznikem T1DM v 5 letech a trváním choroby již 25 let, DpR se projevila v 18 letech (pacientka č. 21 – Tabulka 1). H1Ac byl v minimálním rozmezí okolo 50 mmol/mol (rozmezí 47–52 mmol/mol) v posledních pěti letech. Dokumentovaný nález vpravo – CS byla ve třech cyklech hraniční, až na 12 c./st., která byla snížena. SD-OCT se projevila výrazně prohloubenou foveou -44 μm při centrální tloušťce sítnice 263 μm a průměrné tloušťce sítnice 307 μm. TE byly patrné oftalmoskopicky, doložené na fotografii očního pozadí. FAZ byla pravidelně okrouhlá o ploše 0,54 mm². SPC s minimální neperfuzí, ale s přesahujícími kapilárami do FAZ. DVC pravidelný s neperfuzí jen v těsném sousedství FAZ.
Obr. 4. DpR2: CS, SD-OCT, OCT-A a fundus u pacientky 20 (Tabulka 1) 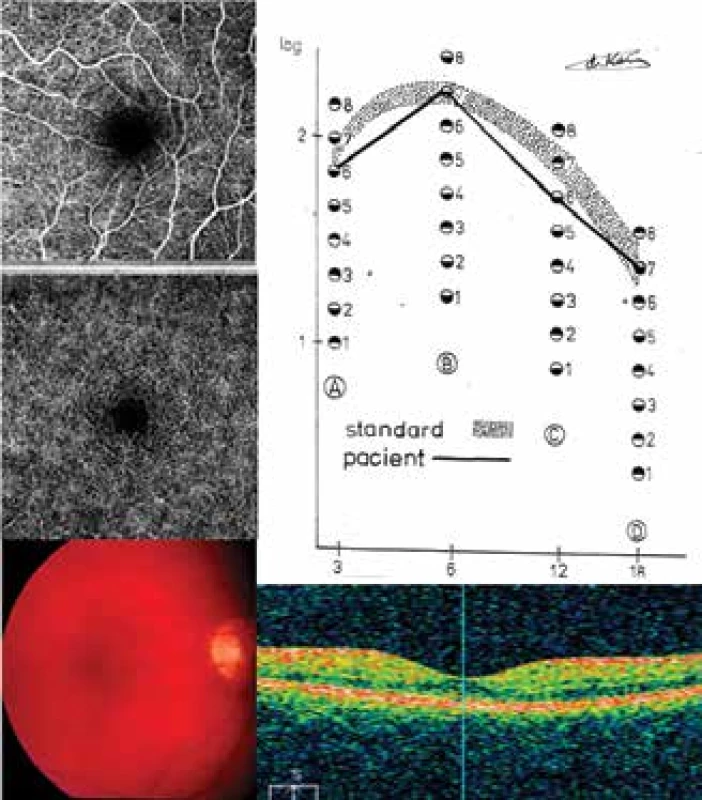
Obrázek 5 – NPDR: 21letá pacientka, kdy T1DM vznikl ve 3 letech života a NDPR se projevila před rokem (pacient č. 4 – Tabulka 2). Hladina Hb1Ac se v posledních dvou letech výrazně zhoršila v patologickém rozmezí mezi 98–117 mmol/mol. Do doby nabytí plnoletosti nepřekročila hodnota Hb1Ac 70 mmol/mol vzhledem k dohledu rodičů a nález připomínal DpR2. Dokumentovaný nález vpravo – CS byla ve třech cyklech snížená, jen v 3 c./st. hraniční. SD-OCT se projevila výrazně prohloubenou foveolou -74 μm (rozmezí mezi 220 μm centrální a 294 μm průměrné tloušťky sítnice) s navalitým okrajem foveoly, doloženo na fotografii očního pozadí spolu s její skvrnitostí. FAZ byla lehce nepravidelného tvaru s přesahujícími kapilárami o ploše 0,46 mm². SVC provázela nepravidelná neperfuze a ojedinělé MA. DVC byl nepravidelného tvaru s výraznou neperefuzí okolo FAZ a s ojedinělými dilatovanými kapilárami.
Obr. 5. NPDR: CS, SD-OCT, OCT-A a fundus u pacientky 4 (Tabulka 2) 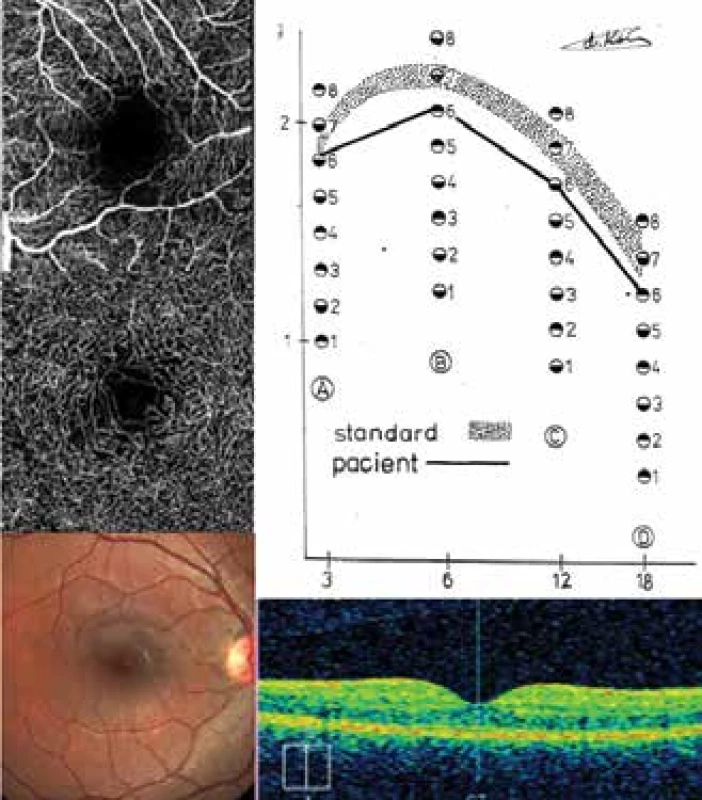
Obrázek 6 – NPDR: Mladý diabetik se vznikem T1DM v 10 letech života, s dobou trvání choroby 17 let, kdy NDPR byla diagnostikována v 24 letech (pacient č. 16 – Tabulka 2), HbA1c se v posledních dvou letech pohybovala mezi 60–77 mmol/mol. Dokumentovaný nález vlevo – CS byla v patologických hodnotách ve všech cyklech. SD-OCT vykazovala centrální tloušťku sítnice 310 μm, ale průměrná tloušťka sítnice byla 275 μm, z čehož vyplynula hloubka foveoly +35 μm (plusová hodnota byla diagnostikována jen u jediného pacienta ze souboru), navíc zde byla patrná kumulace tekutiny. FAZ byla pravidelného tvaru o ploše 0,06 mm² a přítomné ojedinělé MA (SVC) a dilatace kapilár (DVC) se známkami neperfuze v obou vaskulárních segmentech.
Obr. 6. NPDR: CS, SD-OCT, OCT-A a fundus u pacienta 16 (Tabulka 2) 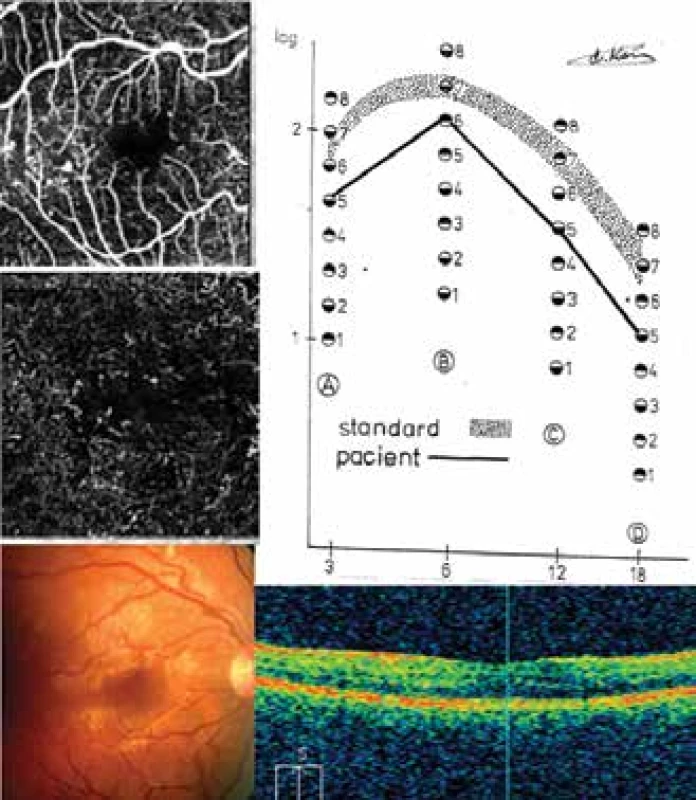
Uvedené příklady potvrdily, že rozhodující pro vývoj očních změn byl individuální přístup v dodržování životosprávy. Srovnání dvou pacientek ukázalo, že výrazné překročení normy HbA1c během dvou let vedlo k přechodu s DpR na NPDR, naopak dlouhou kompenzací Hb1Ac se udržoval obraz DpR po dobu čtvrtstoletí trvání T1DM. Také u dvou pacientů s obdobnými časovými faktory (trvání T1DM a obdobným vznikem DpR, ale i bohužel NPDR) byl vývoj očních změn v souvislosti s hladinou Hb1Ac, neboť nelze předpokládat, že by se vývoj jejich hladin příliš odlišoval v předchozím období.
DISKUZE
Prevalence T1DM v dětském věku předpokládá vzestup z 94 000 v roce 2005 na 160 000 v roce 2020 [18]. V české studii byly modelováním identifikovány dvě změny nárůstu T1DM: v roce 1995 se výskyt zrychlil, zatímco v roce 2001 růst výskytu výrazně zpomalil [19]. Poslední rozsáhlá studie nárůstu T1DM u dětí z 26 zemí Evropy, zpracovaná v roce 2019, se zabývá 25letou periodou 1989 až 2013. Bohužel České republice (ČR) patřilo svým průměrným nárůstem 4, 7 % (rozpětí mezi 4,3 až 5 %) páté místo v Evropské unii (EU), největší nárůst mělo Polsko s 6,6 % a nejmenší Španělsko jen s 0,5 %. Celkové rozpětí nárůstu T1DM v průměru v Evropě bylo mezi 2,8 až 3,9 % [20]. V roce 2013 bylo v ČR evidováno 861 000 diabetiků, což představovalo 8,3 % populace. Diabetes 2. typu (T2DM) postihovalo 790 000 osob (91,7 %) a T1DM byl u 61 000 osob (6,8 %). DR byla detekována u 103 000 nemocných [4]. Předpokládá se nárůst průměrně o 60 000 nových pacientů za rok, z toho s diabetem zemře ročně 22 000 pacientů. V současnosti lze předpokládat, že v ČR je přes milion nemocných s oběma typy tohoto závažného onemocnění. Vyplývá z toho celospolečenská nutnost zavádění screeningových programů prevence diabetu, a to i DR. T1DM jakožto autoimunitní onemocnění vzniká v dětství. Jeho problematika i oční postižení proto přechází do dospělosti. Za časnou známku DR předcházející vlastní obraz NPDR se považují neurodegenerativní procesy [21, 22] v rámci redukce plexiformních vláken a gangliových buněk [21], selektivní ztenčení vnitřních retinálních vláken [22] či defektní funkce amakrinních a bipolárních buněk [23] či naopak ztluštění plexiformní a nukleární vrstvy [22]. Toto umožnily detekovat moderní SD-OCT přístroje pracující na principu trojrozměrných obrazců stavby vlastní sítnice a jejich vrstev [24,25]. Peripapilární retinální nervová vlákna byla zredukována v závislosti na vyšší hladině HbA1 oproti 7 % u preklinické DR [26].
Sítnicová neurodegenarace je dříve přítomná oproti oftalmoskopické detekci mikrocirkulačních abnormalit. Neuroretinální poškození vyvolává funkční abnormality jako jsou snížení barvocitu, CS, adaptace na tmu [27] a dává podklad pro patologickou odpověď při elektrofyziologických vyšetřeních [28]. Při detekci počátečních změn se vychází z patofyziologie diabetických změn. Hyperglykémii doprovází oxidační stres, vzniklá pseudohypoxie, která může porušit buněčnou membránu endotelu cév. Další teorie mluví o poškození pericytů paradoxním glukózovým hladověním, což vede k jejich apoptóze [3]. Na tomto základě se předpokládá porušení výživy světločivých a dalších buněk sítnice. Tím je dán podklad pro patologickou odpověď při elektrofyziologických vyšetřeních a snížení citlivosti na kontrast. Interpretace a srovnání výsledků těchto metod nejsou jednoznačné. Snížení oscilačních potenciálů bylo provázeno poklesem kontrastní citlivosti v různých stadiích DR [29] a také u T1DM bez DR byl zaznamenán pokles amplitudy zrakových evokovaných potenciálů spolu se snížením CS [30] či jejich abnormality před vznikem retinopatie při normální ZO [31].
Existuje řada specializovaných očních vyšetřovacích metod, které zpřesňují diagnózu DR a DME, včetně posuzování výsledku jejich léčby. V ČR od roku 2016 zahrnovaly základní čtyři diagnostické postupy: vyšetření na štěrbinové lampě, stereoskopickou fotografii či digitální stereofotografii, fluorescenční angiografii (FAG) a OCT na principu nízkokoherenční interferometrie [4]. Mezi další diagnostické postupy patří: barvocit, CS, elektroretinogram (ERG), mikroperimetrie a především OCT-A. Jednotlivě nebo v kombinaci jsou schopné upozornit na riziko vzniku těchto očních komplikací ještě před jejich detekcí pomocí fotodokumentace. Právě kombinaci vyšetřovacích metod jsme využívali v této studii. Také důležitou součástí bylo i oftalmoskopické vyšetření, kdy jsme zaznamenali změnu v obrazu centrální krajiny, kterou jsme nazvali „skvrnitostí“. Tento příznak mapovitých změn jen v makule jsme přirovnali k obrazu a termínu „flecked retina“, který se týká krystalické retinopatie spojené s poruchou metabolismu tuků, která také současně postihuje i periferii sítnice [32].
V zahraničí studie o změnách CS u diabetických pacientů probíhaly již od 80. let minulého století [33,34] a stanovily, že CS je citlivější pro počátek diabetologických změn sítnice než ZO. CS prokázala patologickou progresi odpovídající zhoršujícím se diabetickým změnám na sítnici [35]. Změny CS byly odhaleny v souvislosti s laboratorními změnami u pacientů T1DM, a to pokles skóre CS u mikroalbuminurie [36], také u akutní hyperglykémie bylo CS skóre spolu s vizuální disturbancí, přičemž ZO byla v normě [37]. V průběhu hypoglykémie měla CS také tendenci se zhoršovat [38]. Systematické sledování CS u dětských a adolescentních pacientů nebylo časté [28,36,39,40], ale potvrdilo snížení CS u pacientů s T1DM až s abnormálními hodnotami u DR na rozdíl od kontrol. Informace o ovlivnění Hb1Ac jsou u CS rozdílné. Pokles Hb1Ac z patologických hodnot provázelo vyrovnávání CS [28,41]. Naopak žádné změny CS podmíněné metabolickou kontrolou T1DM pomocí Hb1AC nebyly prokázány [9,39,42]. Také v ČR se objevily práce na konci minulého století, které stanovily negativní ovlivnění CS faktorem věku nemocných nad 35 let a délkou trvání T1DM [42,43]. U pacientů s T1DM bez DR nebo s DR nebyla ZO postižena, zatímco barvocit a mesopická foveolární CS byly signifikantně narušeny oproti kontrolní skupině [44]. Paleta diagnóz, kde lze využít tuto neinvazní a časově nenáročnou metodu CS v oftalmologii, je široká. Neuritida optického nervu při roztroušené skleróze má vždy sníženou CS, a to i po odeznění ataky onemocnění a je citlivější na detekci změn než vizuální evokované potenciály [45]. U optické neuropatie pomůže zachytit pokles CS počáteční změny ještě před poklesem vidění [46]. CS může být ovlivněn akutní změnou refrakce či formováním katarakty u T1DM. Není žádná podpora pro teorii vzniku „diabetické myopie“, která by ji spojovala s metabolickou dysregulací. Jen u krátkozrakosti je delší doba trvání cukrovky, předchází jejímu vzniku [47]. Stupeň přechodné hyperopie je spojený rychlostí korekce hyperglykémie v závislosti na redukci hladiny glukózy v plasmě [47,48]. Akumulovaný účinek hyperglykémie je v přímé souvislosti se změnou transparence čoček u diabetiků [49]. Naštěstí významnou roli v ochraně čočky před vznikem katarakty má taurin, který slouží k osmoregulaci a zároveň je antioxidant. Na vznik katarakty má vliv vzestup sorbitolu i vody v čočkách před i po formaci katarakty [50]. Posuzovali jsme změny transparence čoček na CS již dříve, ale bez prokázání zásadního vlivu [51]. Naštěstí ani jednou jsme nezaznamenali do této doby vznik akutní katarakty v druhé dekádě života, který je vždy spojený s předchozím poklesem ZO, hyperglykémií a hyperopií [52,53].
Z dalších výše uvedených vyšetření vyplývá, že přestože barvocit a CS mají podobnou charakteristiku, CS je výrazněji citlivější a specifický [54]. DR může provázet žluto-modrá porucha barvocitu (tritanoanomálie) při normální ZO [55] především při progresi DME se stoupajícím věkem [56]. V naší předchozí studii jsme zásadní změny barvocitu u dětí a mladistvých oproti jeho rozložení v populaci nezaznamenali [7]. Signifikantní pokles b-vlny ERG v implicitním čase byl již u pacientů s počínající DR [57]. U pacientů s NPDR byl nárůst tloušťky makuly provázen kromě prodloužení implicitního času ERG ještě snížením aplitudy a zhoršením ZO [58]. Citlivost sítnice při mikroperimetrii byla snížena při zvýšené centrální tloušťce foveoly u NPDR, ale z pohledu současných jednotlivých moderních metod OCT nebyly zjištěny žádné podstatné rozdíly v rámci mikroperimetrické analýzy [59,60].
OCT se běžně využívá přes deset let k posouzení tloušťky makulární krajiny u cystoidního makulárního edému pro hodnocení frekvence změn [61]. Posouzení vlastní tloušťky sítnice prokázalo významný rozdíl mezi zdravou populací a pacienty s proliferativní i neproliferativní formou retinopatie pomocí přístroje Zeiss-Humphrey [62], kde byla retinální tloušťka mohutnější než u zdravých subjektů [61]. Toto jsme potvrdili, kdy u diabetiků po 10 letech trvání choroby nebyl zásadní rozdíl v již zvýšené tloušťce sítnice v dalším průběhu onemocnění. Vlastní normy makulární kubatury a centrální tloušťky sítnice publikačně zpracované v roce 2014 [10] lze brát za spolehlivé, neboť byly obdobné i s pozdějším pozorováním, které kubaturu uvádělo 9,98 ±0,43 μm3 a centrální tloušťka 280,67 ±12,79 μm u mužů a 276,63 ±11,61 μm u žen [63]. V naší studii jsme tuto rozdílnost neposuzovali. SD-OCT je schopna prokázat ztluštění sítnice v makulární oblasti při současném snížení CS ještě před klinickými projevy DME [10,44]. SD-OCT umožňuje ve svém řezu znázorňovat hyperreflexní body, skvrny ve vnitřní plexiformní vrstvě, tedy zasahující i do vrstvy gangliových buněk a vnitřní jádrové vrstvy. Při progresi se dostávají i do zevní plexiformní vrstvy v souvislosti s mikrogliální aktivací a jejich počet narůstá [64]. Tento nález vývoje jsme už potvrdili u DpR a často byl patrný i akustický stín. Za zevní plexiformní vrstvou (Henleho vlákna) následuje vnější jádrová vrstva, a potom jsou již jen světločivé buňky [14]. Po antiVEGF léčbě DME byla zaznamenána v případech jeho kompletního řešení jejich redukce, ale bez významné korelace ZO [65].
OCT-A pro svoji neinvazivnost v určitých indikacích může nahradit FAG, což umožňuje opakovatelnost vyšetření na rozdíl od FAG [17]. Velikost FAZ naměřená pomocí FAG i OCT-A je srovnatelná [66]. Průměr fyziologického kruhu FAZ je vysoce variabilní mezi 250–600 μm [14], což představuje plochu od 0,052 do 0,283 mm2. V kontrolní studii [10] jsme zjistili větší průměr kruhu FAZ, a to 700 μm. Opakovaná měření FAZ v přesnosti jsou srovnatelná, nezaleží na použitém přístroji [67] ani zda bylo měření provedeno automaticky či manuálně [68,69], jak jsme je prováděli sami. V ČR se využívají čtyři typy přístrojů [17], při posouzení cévní denzity není mezi nimi signifikantní rozdíl, ale v hodnocení počtu rozeznatelných rozdvojení cév je rozdíl mezi jednotlivými přístroji, ale bez statistického významu [70]. Rozhodující pro obraz OCT-A je posouzení kvantitativního průtoku krve sítnicí [71]. U zdravé populace a diabetiků bez DR je obdobný, naopak u již mírné formy NPDR je v arteriích průtok zpomalen a u vén je signifikantně snížen [72]. Zpomalení průtoku způsobuje jen 40% znázornitelnost MA u OCT-A na rozdíl od FAG [73], přesto je OCT-A kvalitnější v znázornitelnosti MA než SD-OCT [74], neboť se jedná o čistou vizualizaci a přesnější pozorování [75]. OCT-A ukazuje u pacientů s T1DM ještě bez DR snížení celkové density kapilár [76] a časné mikrovaskulární změny [77,78] především v parafoveolární oblasti [79,80], což jsme rovněž pozorovali. Také jsme zaznamenali prořídnutí kapilární sítě již u DpR1, a především u DpR2 ve shodě s analýzou v SVC [81] a v DVC [80], což potvrzuje kvantifikaci perfuze v každé vrstvě [82]. Další prořídnutí a ztráta kapilární sítě pokračuje progresí do NPDR [83], což jsme rovněž potvrdili. Zhoršení DR provází také další změny v DVC [84], příkladem je naše pozorování dilatace kapilár v tomto vaskulárním segmentu. Signifikantní rozdílnost v retinální mikrovakulatuře je patrná mezi zdravými subjekty a pacienty T1DM, může detekovat změny na sítnici dříve než biomikroskopický nález [85]. Odhalí kromě MA, také retinální neovaskularizaci, intraretinální mikrovaskulární abnormality a rozdílnou kresbu tepen či vén [86]. Nejnovější hodnocení gangliové buněčné vrstvy objevilo ohniskové ztráty, které mohou být v čase navýšeny, což by mohlo posloužit jako časný index poškození neuronů u pacientů s T1DM při zjevné absenci příznaků DR [87]. Tento fakt znovu potvrzuje primárnost neurodegenerativních změn v progresi očního postižení.
Kromě sítnicových změn se u diabetiků také popisují změny v cévnatce, v rámci této studie vzhledem k možnostem přístrojového vybavení jsme se touto problematikou nezabývali. Tloušťka cévnatky je celkově a ve vnější části tenčí u pacientů s NPDR oproti zdravé populaci [88], což platí i pro pacienty bez příznaků DR, navíc může být již funkčně odlišná [89]. Tento faktor je v přímé souvislosti s evolucí základní choroby [90] a ztenčení se projevuje také v oblasti fovey [91]. Do obrazu choroidálních změn patří zvýšení cévní tortuozity, neovaskularizace, ale i dilatace či naopak obstrukce s výpady projevující se neperfuzí [92]. Prevencí ztenčovaní cévnatky je udržování hladiny HbA1c pod 7 % [93].
Neopomenutelným faktorem pro vznik očních komplikací T1DM je doba jeho trvání. Wiskonsinské studie prokázaly, že existuje řada rizikových faktorů, které zásadně a významně podporují vznik DR, tak nárůst DME. Patří k nim vysoký krevní tlak, proteinurie, kouření, vysoký Body Mass index a prevalence k mužskému pohlaví [94,95,96]. Nárůst váhy v průběhu dětství je zásadním rizikovým faktorem pro vznik T1DM [97]. Variabilita HbA1c prezentuje další zásadní a nezávislý faktor spojený s rozvojem DR [96,98] a nefropatie [99]. Také proměnlivá hladina Hb1Ac je riziková, neboť vysoká základní hladina Hb1Ac a její následná výrazná redukce je rizikovým faktorem pro ztluštění makulární krajiny [100]. Naproti tomu změny denních hladin glukózy neprokázaly signifikantní závislost na vývoji mikrovaskulárních komplikací [27,101]. Kumulativním hodnocením HbA1c jsme se nezabývali, přesto jsme na uvedených příkladech doložili zásadní důležitost metabolické kompenzace i v prevenci rozvoje DR. Tyto vztahy [98,102] dlouhodobě stále dokládají mnohočetné studie DCCT (Diabetes Control and Complication Trial) a EDIC (Epidemiology Diabetes Intervention and Complication).
ZÁVĚR
Prokázali jsme, že existuje mezistupeň mezi fyziologickým nálezem na sítnici a NPDR, a to tzv. diabetická preretinopatie, což lze brát za preklinickou formu DR. Rozděluje se na obraz s hlubší foveolou, rozsáhlejší FAZ s nižším poklesem CS a stav s mělčí foveolou, užší FAZ s výraznějším poklesem CS. Současně byly zaznamenány další změny mikrovaskularity (OCT-A) jako jsou poruchy ve smyslu neperfuze v centrální části sítnice různého stupně. Tento nález se významně odlišuje od změn, u již vzniklé NPDR, kde byl zjištěn zásadní pokles CS, podstatné poruchy neperfuze a hlavně přítomnost mikroaneurysmat.
Autoři práce prohlašují, že vznik i téma odborného sdělení a jeho zveřejnění není ve střetu zájmů a není podpořeno žádnou farmaceutickou firmou. Dále autoři prohlašují, že práce nebyla zadána jinému časopisu ani jinde otištěna.
Předneseno on-line na 57. diabetologických dnech v Luhačovicích, duben 2021, s nabídkou spolupráce.
Věnováno památce prof. MUDr. Jana Vavřince, DrSc. (1947–2016), spoluzakladateli československé dětské diabetologie, od jehož úmrtí uplynulo pět let.
MUDr. Jan Krásný
Oční klinika FN Královské Vinohrady
Šrobárova 1150/50
10 034 Praha 10
E-mail: jan.krasny@fnkv.cz
Do redakce doručeno dne: 13. 1. 2021
Přijato k publikaci dne: 1. 6. 2021
Zdroje
- Cunha-Vaz JG. Pathophysiology of diabetic retinopathy. Br J Ophthalmol.1978;62(6):351-355.
- Cunha-Vaz JG, Goldberg MF, Vygantas C, Noth J. Early detection of retinal involvement in diabetes by vitreous fluorophotometry. Ophthalmology. 1979;86(2):264-275.
- Sosna T, Bouček T, Fišer I. Diabetická retinopatie [Diabetic retinopathy], 1. vyd. Praha (Česká republika); Jiří Cendelín; 2001. 255. Czech.
- Kalvodová B, Sosna T, Ernest J, at al. Doporučené postupy pro diagnostiku a léčbu diabetické retinopatie [Recommended procedures for the diagnosis and treatment of diabetic retinopathy]. Ces Slov Oftal. 2016;76(6):226-233. Czech.
- Filouš A, Rychnová J, Vavřinec J.: Rozšířená klasifikace diabetické retinopatie u dětí a mladistvých [Extended clessification of diabetic retinopathy in children and adolescents]. Cesk Pediatr. 1992;47(8):453-455. Czech.
- Klement UM, Freyler H.: Diabetic pre-retinopathy. Klin Mbl Augenheilk. 1980;176(2):313-316. German.
- Krásný J, Brunnerová R, Průhová Š, et. al. Test citlivosti na kontrast v časné detekci očních změn u dětí, dospívajících a mladých dospělých s diabetes mellitus I. typu [The contrast sensitivity test in early detection of ocular changes in the relation to the type 1 diabetes mellitus compensation in children, teenegers, and youg adults]. Cesk Slov Oftal. 2006;62(6):381-392. Czech.
- Verougstraete C, Tousweint D, De Schepper Z, Haehtjens M, Dorchy H. First microangiografic abnormalities in childhood diabetes – types of lesions. Graef´Arch Clin Exp Ophthal. 1991;229(1):24-32.
- Krásný J, Anděl M, Brunnerová R, et al. The contrast sensitivity test in early detection of ocular changes in the relation to the type 1 diabetes mellitus compensation in children, teenegers, and young adults. Recent Pat Inflamm Alergy Drug Discov. 2007;1(3):232-236.
- Krásný J, Vosáhlo J, Čeledová J, Hora I, Magera L, Veith M. Preretinopatie u mladistvých s diabetem 1. typu z pohledu vyšetření citlivosti na kontrast a koherenční tomografie [Contrast sensitivity and optic coherence tomography examinations in adolescent patients with diabetes mellitus type I preretinopathy (a pilot study)]. Cesk Slov Oftal. 2014; 70(4):123-130. Czech.
- Magera L, Krásný J, Pluhovský P, Holubová L. Foveal avaskular zone and macular microvasculature changes by OCT-Angiography in young pacients with type 1 diabetes (pilot study) Cesk Slov Oftal. 2020;76(4):111. doi:10.31348/2020/19
- Krásný J. Multidiciplinární využití citlivosti na kontrast [Multidisciplinary use of contrast sensitivity]. Cas Lek Ces. 2006;145(11):865-869. Czech.
- www. vectorvision.com /html/educationCSV1000norms.html
- Kolář P, et al. Věkem podmíněná okulární degenerace [Age-related macular degeneratin]. 1st ed. Praha: Grada Publishing; 2008. 148. Czech.
- Krásný J. Závěrečná zpráva výzkumného projektu MZ ČR IGA NR/7952-3 [Final report of the research project of the Ministry of health of the Czech Republic IGA NR/7952-3] Czech. MZ ČR, 2006.
- Wolf S, Wolf-Schnurrbusch U. Spectral-domain optical coherente tomography use in macular diseases: a review. Ophthalmologica. 2010;224(6):333-340.
- Němec P. Trendy soudobé oftalmologie (ed. Rozsíval P.), svazek 10, Praha (Czech Republic): Galén; 2017. OCT angiografie [OCT-angiographia] Czech; 33-55.
- Patterson ChC, Dahlquist GG, Gyürüs E, Green A, Soltész G; EURODIAB Study Group. Incidence trend for childhood type 1 diabetes in Europe during 1989-2003 and predicted new cases 2005-2020: multicentre prospective registration study. Lancet. 2009;373(9680):2027-2033.
- Cinek O, Kulich M, Sumik Z. The incidence of type 1 diabetes in young Czech children stopped rising. Pediatric Diabetes. 2012;13 : 559. doi: 10.1111lj.1399-5448.2012.00858x
- Patterson ChC, Harjutsalo V, Green A. Trends and cyclical variotion in the incidence of childhood type 1 diabetes in 26 Europen centres in the 25 years period 1989-2013: a multicentre progresive registration study, Diabetologica. 2019;62(6):408-417.
- DeBuc D, Gerding H, Cambera B, Somfai GM. The use optical koherence tomography foor the detection of early diabetic retinopathy. Klin Monbl Augenheilkd. 2018; 235(4):377-384.
- van Dijk HW, Kok PH, Garvin M, et al. Selective loss of inner retinal thickness in type 1 diabetic patients with minimal diabetic retinopathy. Invest Ophthal Vis Sci. 2009;50(7):3404-3409.
- Vujosevic S, Midena E. Retinal layer changes in human preclinic and early clinical diabetic retinopathy support early retinal and Müller cells alteration. J Diabetes Res. 2013; Jun 2013, doi: 101155/2013/90550058
- Asefzadeh B, Fich BM, Paramteau CE, Cavallareno AA. Macular thickness and systemic markers for diabetes in individual with no or mild diabetic retinopathy. Clin Experiment Ophthamol. 2008;36(5):455-463.
- DeBuc CD, Somfai GM, Ranganethon S, Tátrai E, Ferencz M, Puliafito CA. Reliability and reproducibility of macular segmentation using custom-built optical coherence tomography retrinal image analysis software. J Biomed Opt 2009;14(6 ). doi: 10.1117/1.3268773
- Toprak I, Frnkci SM, Yaylali GF, Marti C, Yaylali V. Early retinal neurodegeneration in preclinical diabetic retinopathy: a multifactorial investigetion. Eye (London). 2020;34(6):1100-1107.
- Vilarroel M, Ciudim A, Hermándes C, Simo R. Neurodegeneration: an early event of diabetic retinopathy. Word J Diabetes. 2010; May 2010, doi: 104339/Wi.v1.1257.
- Georgakopoulos CD, Elliopoulou MI. Exarchou AM, Tzimis V, Pharmamakakis NM, Spoiliotis BE. Decreased contrast sensitivity in children and adolescents with type 1 diabetes mellitus. J Pediatr Ophthalmol Strabismus. 2011;48(2):92-97.
- Kawasaki K, Yonemura K, Yokogawa Y, Saito N, Kawakita S. Correlation between EREG oscillatory potential psychophysical contrast sensitivity in diabetes. Doc Ophthalmol. 1986;64(2):209-215.
- Lopes de Faria JM, Katsumi O, Cagliero E, Nathan D, Hirosa T. Neurovcisual abnormalities preceding the retinopatrhyin púatients with long term type 1. diabetes mellitus. Graf Arch Clin Exp Ophthalmol. 2001;239(9):643-648.
- Martinelli V, Lacerenza M, Merenda M, Meschi F, Somazzi L. The objective assessment of visual contrast sensitivity by pattern reversal visual evoked potential in diabetes. J Diabet Complications 1988;2(1):44-46.
- Krill AE, Deutman HS. The varios categories of juvenile macular degeneration. Trans Am Ophtalmol Soc. 1972;70(3):220-245.
- Sokol S, Moskowitz A, Skarf B, Evans R, Molitch M, Senior B. Contrast sensitivity in diabetics with and without background retinopathy. Arch Ophthalmol. 1985;103(1):51-54.
- Della Sala S, Bertoni G, Somazzi L, Stubbe F, Wilkins AJ. Impaired contrast sensitivity in diabetic patients with and without retinopathy: a new technique for rapid assessment. Br J Ophthamol. 1985;69(2):136-142.
- Verrotti A, Lobefalo L, Petitti MT, et. Al. Relkationship between contraqst sensitivity and metabolit kontrola in diabetic with and without retinopathy. Ann Med. 1999;30(4):369-374.
- Bangstad HJ, Brochmann-Hansen O, Hultgren S, Dahl-Jorgensen K, Hanssen KF. Impaired contrast sensitivity in adolescents and young type 1 diabetic patients with microalbuminuria. Acta Ophthalmol. 1994;72(6):668-673.
- Mangouritaqs G, Katoulis E, Kepaptsoglou O, Zoupas C. Effect of induced hyperglycemia on contrast sensitivity function in insulin-dependent diabetioc patients. Ophthalmologe. 1995;92(2):142-147. German.
- Ewing FM, Deary IJ, McCrimmon RJ, Strachan MW, Frier BM. Effect of acute hypoglacemia on visual information processing in adults with type 1 diabetes mellitus. Physiol. Behav. 1998;64(5):653-660.
- Urban B, Bakunowicz-Lazarcyk A, Peczynska J, Urban M. The evaluation of contrast sensitivity in children and adolescents with insulin-dependent diabetes mellitus. Klin Oczna. 1999;101(2):111-114. Polish.
- North RV, Farrell U, Banford D, et asl. Visual fiction in young IDDM patiens over 8 years of age. A 4year longitudinal study. Diabetes Care. 1997;20(11):1724-1730.
- Bancroft D, North RV, Dolben J, Butler G, Owens DR. Longitudinal study of viosual functions in young insulin dependent diabetics. Ophtalmic Physiol Opt. 1994;14(4):339-346.
- Liska V, Dostalek M. Are contrast sensitivity functions impared in insulin dependent diabetics without diabetic retinopathy? Acta Medica (Hradec Kralove) 1999;42(4):133-138.
- Liska V. Funkce kontrastní citlivosti u diabetes 1. typu (IDDM) bez příznaků diabetické retinopatie [Function of contrast sensitivity in diabetics type 1 (IDDM) without sings diabetic retinopathy]. Cesk Oftal. 1999;55(4):237-245. Czech.
- Katz G, Levkovitch-Verbin H, Treister G, Belkin M, Ilany J, Polat U. Mesopic foveal contrast sensitivity is impaired in diabetic patient without retinopathy. Graef Arch Clin Exp Ophthalmol. 2010;248(12):1699-1703.
- Nordmann JP, Saraux H, Roullet E. Contrast sensitivity in Multiple sclerosis in 35 patients with and without optic neuritis. Ophtalmologica 1987;195(4):199-204.
- de Marco R, Ambrosio G, Ferrara G. Measuring contrast sensitivity in patients with Gravese ophthalmolopathy complicated by ocular hypertension and suspect glaucoma or dysthyroid optic neuropathy. Doc Ophthalmol. 2000;101(4):165-177.
- Fledelius HC, Fuchs J, Reck A. Refraction in diabetics during metabolic dysregulation, acute and chronic. With special reference to the diabetic myopia concept. Acta Ophthalmol. 1990;68(3):275-280.
- Oklamoto F, Sone H, Nonoyama T, Hommura S. Refractive chages in diabetic patients during intensive glycaemic control. Br J Ophthalmol. 2000;84(10):1097-1102.
- Kato S, Shiokawa A, Fukushima H, et al. Glycemic control and lens transparency in patients with type 1 diabetes mellitus. Am J Ophthalmol. 2001;131(3):301-304.
- Malone JI, Lowitt S, Cook WR. Nonosmotic diabetic cataracts. Pediatr Res. 1990;27(6):293-296.
- Krásný J, Vyplašilová E, Brunnerová R, et al. Změna transparence čočky u dětí, mladistvých a mladých dospělých s diabetes mellitus 1. typu [The human lens´transparence changes in children, adolescent, and young aduls]. Cesk Slov Oftal. 2006;62(5):304-314. Czech.
- Cornwell M, Lepre F. Acute irreversible cataracts in diabetes mellitus. Aust N Z J Ophthalmol. 1999;23(3):221-222.
- Orts VP, Devesa TP, Belmonte MJ. Juvenile diabetic cataract. A rare finding which lead us to diagnosis of this illness. Arch Soc Esp Ofalmnol. 2003;78(7):389-391. Spanish.
- Ewing FM, Deary IJ, Strachan MW, Frier BM. Seeing beyond retinopathy in diabetes: electrophysiological and psychophysical abnormalities and alterations in vision. Endocr Res. 1998;19(4):462-476.
- Ong GL, Ripley LG, Newsom RS, Casswell AG. Assessment of color vision as a screening test for sight threatening diabetic retinopathy before loss of vision. Br J Ophthalmol. 2003;87(6):747-752.
- Barton FB, Fong DS, Knatterund GL; ETDRS Research Group. Clůassification of Farnworth-Munsell 100 hue-test results in the early treatment diabetic retinopathy study. Am J Ophthalmol. 2004;138(1):119-124.
- Mortlock KE, Chiti Z, Drasdo N, Owens DR, North RV. Silent substitution A-cone elektroretinogram in subjects with diabetes mellitus. Ophthalmic Physiol Opt. 2005;25(5):322-329.
- Holm K, Larsson J, Lövestam-Adrian M. In diabetic retinopathy, foveolal thickness of 3900 mum seems to correlate with functionally significant loss of vision. Doc Ophthalmol. 2007;114(3):117-124.
- Sacconi R, Casaluci M, Borrelli E, et al. Multimodal paging assessment of vascular and neurodegenerative retinal alterations in type 1 diabetic patiens without fundoscopic sings of diabetic retinopapthy. J Clin Med. 2019 Sep 8;8(9):1409. doi: 10.3390/jcm8091409.
- Sacconi R, Lamanna F, Borrelli E, et al. Morphofunctional analysis of the retina in patients with type 1 diabetes without complicatins after 309 years of disease. Sci Rep. 2020 Jan 14;10(1):206. doi: 10.1038/s41598-019-57034-1.
- Koleva-Georgieva DN, Sivkova NP. Optical coherence tomography for the detection of early macular edema in diabetic patients with retinopathy. Folia Med (Plovdiv) 2010;52(1):40-48.
- Sanchez-Tocino H. Alvarez-Vidal A, Maldonado MS, Morena-montanes J, Gorcha-Layana A. Retinal thickness study with optical coherence tomography in patients with diabetes. Invest Ophthalmol Vis Sci. 2002;43(5):1588-1794.
- Sabouri MR, Kazemnezhad E, Hafezi V. Assessment of macular thickness in healthy eyes using Cirrus HD-OCT: a cross-sectional study. Med Hypothesis Discov Innov Ophthalmol. 2016;5(3):104-111.
- Vujosevic S, Bini S, Midena G, Berton M, Pilotto E, Midena E. Hyperreflectoive intraretinal spots in diabetics without and with nonproliferative diabetic retinopathy: an in vivo study using Spectral Domain OCT. J Diabetes Res 2013; 2013 Dec 9. doi: 10.1155/2013/491835
- Framme C, Schweizer P, Imesch M, Wolf S, Wolf-Schnurrbusch U. Behaviuor of SD-OCT detected hypperreflective foci in the retina of anti-VEGF treated patients with macular edema. Invest Ophthalmol Vis Sci. 2012;53(9):5814-5818.
- Enders C, Baeuerle F, Lang GE, et al. Comparison between findings in optical coherence tomography angiogramy in fluorescein angiogramy in patiens with diabetic retinopathy. Ophthalmologica 2019;28(1):1-6.
- Mihailovic N, Eter N, Alnawaiseh M. Foveolar avasculare zone OCT angiogramy. An overview of current knowledge. Ophthalmologe. 2019;116(7):610-616.
- Ashraf M, Nesper PL,Jampo LM, Yu F, Fawzi AA. Statistical model of optical coherence Tomography angiogramy parameters that correlate with severity of diabetic retinopathy. Invest Ophtalmol Vis Sci. 2018;59(10):4292-4298.
- Ishii H, Shoji T, Yoshikawa Y, Kanno J, Ibuki H, Shinoda K. Automated measurement of the foveal avascular zone in swept-source optical coherence tomography angiography images. Transl Vis Sci Technol. 2019;8(3):28. doi:10.1167/tvst.8.3.28.
- Munk MR, Giannakaki-Zimmermann H, Berger L, et al. OCT-angiography. A qualitative and quantitative comparison of 4 OCT-A devices. PLoS One. 2017 May 10; 12(5):e0177059.
- Ruminski D, Sikorski BL, Bukowska D, et al. OCT angiogramy by absolute intensity diference applied to norma l diseased human retinas. Biomedcal Optics Express. 2015;6(8):2738-2754.
- Bates NM, Tian J, Smiddy WE, et al. Relationship between the morfology of the foveal avascular zone, retinal structure, and macular circulation in patiens with diabetes mellitus. Sci Rep. 2018;8(1):5355. doi:10.1038/sr41598-018-23604-y
- Miwa Y, Murakami T, Suzuma K, et al. Relationship between functional and structural changes in diabetic vessels in optical coherence tomography angiography. Scintific Reports. 2016;6: e29064.
- Parravano M, De Geronimo D, Scarinci F, et al. Relationship between internal reflectivity of diabetic microaneurysms on SD.OCT and detection on OCT angiography. Am J Ophthalmol. 2017 May 5; doi: 10.1016/j.ajo.2017,04.021
- Ishibazawa A, Nagaoka T, Takahashi A, et al. Optical coherence tomography angiography in diabetic retinopathy: a prospective study. Am J Ophthalmol. 2015;160(1):35-44.
- Xu X, Chen C, Ding W, et al. Automated quantification of superficial retinal capillaries and large vessels for diabetic retinopathy on optical coherence tomography angiography. J Biophotonics. 2019 Nov; 12(11): e201900103.
- de Carlo TE, Chin RT, Bonini MA, et al. Detection of microvascular changes in eyes of patients with diabetes but not clinical diabetic retinopathy using optical coherence tomography angiography. Retina 2015;35(11):2364-2370.
- Gildea D. The diagnostic value of optical coherence tomography angiography in diabetic retinopathy: a systematic review. Int Ophthalmol. 2019;39(10):2413-2433.
- Inanc M, Tekin K, Kizitoprak H, Ozalkak S, Doguizi S, Aycan Z. Changes in retinal microcirculation precede the clinical onset of diabetic retinopathy in children with type 1 diabetes mellitus. Am J Opthalmol. 2019;207(1):37-44.
- Simonett JM, Scarinci F, Piccconi F, et al. Early microcircular retinal changes in optical coherence tomography angiography in patients with type 1 diabetes mellitus. Acta ophthalmol 2019;257(4):689-697.
- Sousa DC, Leal I, Moreire S, et al. Optical coherence tomography angiography study of the retinal vascular plexus in type 1 diabetes without retinopathy. Eye (London) 2019;34(2)307-311.
- Sambhav K, Abu-Almero KK, Chalam KV. Deep capillary macular perfusion indices obtained with OCT angiography correlate with degree of nonproliferative diabetic retinopathy. Eur J ophthamol. 2017 Mar 27; doi:5301/ejo.5000948
- Rosen RB, Andrade Romo JS, Krawitz BD, et al. Earliest evidence of preclinical diabetic retinopathy revealed using optical coherence tomography angiography perfused capillary density. Am J Ophthalmol. 2019 Jul;203 : 103. doi:10.1016/j ajo.2019.01.012
- Sun Z, Tang F, Wing R, et al. OCT angiography metrics predict progression of diabetic retinopathy and development of diabetic macular edema: a prospective study. Ophthalmology 2019; 126(12):1675-1684.
- Sousa DC, Leal I, Moreira S, et al. Optical coherence tomography angiography study of the retinal vascular plexus in type 1 diabetes without retinopathy. Eye (London) 2020 Feb;34(2):307-311.
- Botto de Barros Garcia JM, Leonardo D. Diabetic retinopathy and OCT angiography: clinical findings and future perspectives. Int J Retina Vitreous 2017 Mar 13;3. doi:1186/s400942-017-0062-2
- Bontzos G, Kabanarou SA, Gkizis I, Ragkousis A, Xirou T, Peto T. Retinal neurodegeneration, macular circulation and morfology of the foveal avascular zone in diabetic patiens: quantitative cross-sectional study usung OCT-A. Acta Ophthalmol. 2021 Jan 10; doi:10.1111/aos.14754
- Endo H, Kase S, Takahashi M, et al. Alteration of layer thickness in the choroid of diabetic patients. Clin Exp Ophthalmol. 2018 May 9; doi:10.1111/ceo.13299
- Tavares-Ferreira J, Vincente A, Proenca R. Choroidal thickness in diabetic patients without diabetic retinopathy. Retina. 2018;38(4):795-804.
- Orduna-Hospital E, Perdices L, Sanchez-Cano A, Acha J, Cueca N, Pinilla I. Choroidal changes of long-term type 1 diabetic patients without retinopathy. Diagnostics (Basel) 2020 Apr 19; 10(4). doi:10.3390/diagnostics10040235
- Yülek F, Ugürlu N, Önal ED, et al. Choroidal changes and duration of diabetes. Semin Ophthalmol. 2014;29(2):80-84.
- Sala-Puigdollers A, Figueras-Roco M, Hereu M, et al. Repeatability and reproductibility of retinal and choriodal thickness measurements in diabetic macular edema using swept-source optical coherence tomography. PLos One. 2018 Jul;13(7). e200819.
- Torabi H, Isfeedvajani MS, Ramezani M, Daryabari SH. Choroidal thickness and Haemoglobin A1c levels in patients with Type 2 diabetes mellitus. J Ophthamol Vis Res. 2019;14(3):285-290.
- Klein R, Klein BE, Moss SE, Cruickshanks KJ. The Wisconsin epidemiologic study of diabetic retinopathy: XVII. The 14-years incidence and progression of diabetic retinopathy and associated risk factors in type 1 diabetes. Ophtalmology 1988;105(10):1801-1815.
- Klein R, Klein BE, Moss SE, at al. Retinal vascular abnormalities in persons with type 1 diabetes. Ophthalmology. 2003;110(12):2118-2125.
- Klein R, Lee KE, Gangnon RE, Klein BE. The 25-year incidence of visual impairment in type 1 diabetes mellitus: the Wisconsin epidemiologic study of diabetic retinopathy. Ophthalmology. 2010;117(1):63-70.
- Evertsen J, Alemzadeh R, Wang X. Increasing incidence of pediatric type 1 diabetes mellitus in Southeastern Wisconsin: relationship with body weight at diagnosis. PLos One. 2009 Sep 3;4(9): e6873.
- Kilpatrick ES, Rigby AS, Atkin SL. HbA1C variability and the risk of microvascular complication in type 1 diabetes: data from Diabetes Control and Complication Trial. Diabetes Care. 2008;31(11):2198-2202.
- Waden J, Forsblom C; Finish Diabetic Nephropathy Study Group. Hb1AC variability predict incident cardiovascular events, microalubinuria, and overt diabetic nephropathy in patients with type 1diabetes. Diabetes. 2009; 58(11):2649-2655.
- Moon SW, Kim HY, Kim SW, Oh J, Huh K, Oh IK. The change of macular thickness measured by optical coherence tomography in relation to glycemic control in diabetic patients. Graef Arch Clin Exp Ophthalmol. 2011;249(6):639-648.
- Kilpatrick ES, Rigby AS, Atkin SL. Effect of glucose variability on the long-term risk of microvascular complication in type 1 diabetes. Diabetes Care. 2006;29(7):1486-1490.
- Diabetes Control and Complication Trial Research Group / Epidemiology of Diabetes Interventions and Complications Study Research Group. Long-term effect of diabetes and its treatment on cognitive function. N Eng J Med. 2007;356(18):1542-1452.
Štítky
Oftalmologie
Článek vyšel v časopiseČeská a slovenská oftalmologie
Nejčtenější tento týden
2021 Číslo 4- Selektivní laserová trabekuloplastika nesnižuje nitroční tlak více než argonová laserová trabekuloplastika
- Progresi glaukomu je třeba hodnotit strukturálními i funkčními parametry
- Ztráta centrálního vidění po filtrujících operacích glaukomu
- Od PGF-2 alfa-isopropyl esteru k latanoprostu: přehled vývoje Xalatanu
- Compliance u pacientů s glaukomem
-
Všechny články tohoto čísla
-
POKYNY PRO AUTORY A RECENZENTY
ČASOPIS ČESKÉ OFTALMOLOGICKÉ SPOLEČNOSTI A SLOVENSKÉ OFTALMOLOGICKÉ SPOLEČNOSTI - IMUNITNĚ PODMÍNĚNÉ NITROOČNÍ ZÁNĚTY. PŘEHLED
- PRERETINOPATIE U DIABETU 1. TYPU V KONTEXTU FUNKČNÍCH, STRUKTURÁL-NÍCH A MIKROCIRKULAČNÍCH ZMĚN MAKULÁRNÍ OBLASTI
- ZMENA ŠPECIFICKÝCH PARAMETROV ROHOVKY A ZRAKOVEJ OSTROSTI PO CROSSLINKING LIEČBE ROHOVKY PRE PROGREDUJÚCI KERATOKONUS
- ENCYKLOPÉDIA OFTALMOLÓGIE ANTON GERINEC
- VLIV ARTEFICIÁLNÍ MYDRIÁZY NA VÝPOČET DIOPTRICKÉ HODNOTY UMĚLÉ NITROOČNÍ ČOČKY U PACIENTŮ INDIKOVANÝCH K OPERACI KATARAKTY
- SYNDROM UVEÁLNÍ EFUZE. KAZUISTIKA
- RECIDIVUJÚCI BAZOCELULÁRNY KARCINÓM PERIOKULÁRNEJ OBLASTI. KAZUISTIKA
- MALÍGNY MELANÓM OKA A OČNÝCH ADNEXOV
- VYBRANÉ KAPITOLY Z HISTÓRIE OFTALMOLÓGIE NA SLOVENSKU
-
POKYNY PRO AUTORY A RECENZENTY
- Česká a slovenská oftalmologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- IMUNITNĚ PODMÍNĚNÉ NITROOČNÍ ZÁNĚTY. PŘEHLED
- SYNDROM UVEÁLNÍ EFUZE. KAZUISTIKA
- VLIV ARTEFICIÁLNÍ MYDRIÁZY NA VÝPOČET DIOPTRICKÉ HODNOTY UMĚLÉ NITROOČNÍ ČOČKY U PACIENTŮ INDIKOVANÝCH K OPERACI KATARAKTY
- ZMENA ŠPECIFICKÝCH PARAMETROV ROHOVKY A ZRAKOVEJ OSTROSTI PO CROSSLINKING LIEČBE ROHOVKY PRE PROGREDUJÚCI KERATOKONUS
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Revma Focus: Spondyloartritidy
nový kurz
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Autoři: prof. MUDr. Pavel Horák, CSc., doc. MUDr. Ludmila Brunerová, Ph.D., doc. MUDr. Václav Vyskočil, Ph.D., prim. MUDr. Richard Pikner, Ph.D., MUDr. Olga Růžičková, MUDr. Jan Rosa, prof. MUDr. Vladimír Palička, CSc., Dr.h.c.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání




