-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Klinické zkušenosti z dlouhodobé léčby axiální spondyloartritidy secukinumabem
Clinical experience in the long-term treatment of axial spondyloarthritis with secukinumab
Secukinumab is a monoclonal antibody that inhibits interleukin 17A, which has been introduced into the treatment of axial spondyloarthritis (axSpA) after successful phase III clinical trials. The open-label extension of MEASURE studies 1, 2 and 3 demonstrated the long-term efficacy and safety of the drug.
The aim of the analysis is to evaluate the long-term effectiveness in real clinical practice in the Czech Republic.
Methods: A retrospective, open-label, cohort study of patients with axSpA treated with secukinumab in the national ATTRA registry was performed, in which patients with axSpA (radiographic and non-radiographic axSpA), who met the indication criteria of the Czech Society for Rheumatology for the biological treatment of spondyloarthritis, were monitored and treated. The following indicators were evaluated: survival on treatment, BASDAI, ASDAS, HAQ, and SF-36.
Results: A total of 243 patients with radiographic axSpA were included in the study. The drug survival of secukinumab was 70.8% after 12 months and 63.5% after 24 months of treatment. Clinically significant improvement in ASDAS (≥ 1.1) was achieved in 71.7% of patients. The HAQ score decreased from a mean of 1.3 ± 0.6 to 0.8 ± 0.6 during the first 2 years of treatment. Furthermore, all quality of life parameters evaluated by SF-36 were improved. The ability to work was another parameter evaluating the quality of life. During the 2-year treatment, 37.7% of patients with disabilities or incapacity for work regained their ability to work. On the contrary, 15.7% of working patients or job-seekers lost their ability to work. The safety of the treatment was good, and no new signs of toxicity appeared. In the non-radiographic axSpA group, only 29 patients with similar results have been monitored and treated to date.
Conclusion: Treatment survival, efficacy, and safety of secukinumab in real clinical practice are very good, and secukinumab represents a new therapeutic alternative for active axial SpA.
Keywords:
axial spondyloarthritis – biological therapy – secukinumab
Autoři: K. Pavelka 1; Z. Křístková 2; L. Nekvindová 2
Působiště autorů: Revmatologický ústav Praha 1; Institut biostatistiky a analýz, s. r. o., Brno 2
Vyšlo v časopise: Čes. Revmatol., 28, 2020, No. 4, p. 206-215.
Kategorie: Originální práce
Souhrn
Secukinumab je monoklonální protilátka inhibující interleukin 17A, který byl po úspěšných klinických studiích fáze III zaveden do léčby axiálních spondyloartritid (axSpA). Prodloužené, otevřené extenze studií MEASURE 1, 2 a 3 prokázaly dlouhodobou účinnost a bezpečnost léku.
Cílem provedené analýzy je vyhodnocení dlouhodobé účinnosti v reálné klinické praxi v České republice.
Metodika: Byla provedena retrospektivní, otevřená, kohortová studie pacientů s axSpA léčených secukinumabem v národním registru ATTRA, v níž byli sledováni a léčeni nemocní s axSpA (radiografickou i neradiografickou axSpA) splňující indikační kritéria České revmatologické společnosti pro biologickou léčbu spondyloartritid. Hodnoceny byly následující ukazatele: přežívání na léčbě, BASDAI, ASDAS, HAQ, SF-36.
Výsledky: Do studie bylo zařazeno celkem 243 pacientů s radiografickou axSpA. Setrvání na léčbě bylo 70,8 % po 12 měsících léčby a 63,5 % po 24 měsících léčby. Klinicky významného zlepšení ASDAS (≥ 1,1) bylo dosaženo u 71,7 % pacientů. Skóre HAQ pokleslo z průměrné hodnoty 1,3 ± 0,6 na 0,8 ± 0,6 během prvních 2 let léčby. Dále došlo ke zlepšení všech parametrů kvality života hodnocených SF-36. Dalším parametrem kvality života, který byl hodnocen, byla práceschopnost. V průběhu dvouleté léčby došlo k obnovení práceschopnosti u 37,7 % pacientů invalidních či v pracovní neschopnosti a 15,7 % pracujících pacientů či práci hledajících naopak práceschopnost ztratili. Bezpečnost léčby byla dobrá a neobjevily se žádné nové signály toxicity. Ve skupině neradiografické axSpA bylo sledováno a léčeno dosud jen 29 pacientů s podobnými výsledky.
Závěr: Přežívání na léčbě, účinnost i bezpečnost secukinumabu v reálné klinické praxi jsou velmi dobré a secukinumab představuje novou léčebnou alternativu pro aktivní axiální SpA.
Klíčová slova:
axiální spondyloartritida – biologická léčba – secukinumab
ÚVOD
Ankylozující spondylitida (AS) (nebo také radiografická axiální spondyloartritida – axSpA) je chronické, zánětlivé onemocnění charakterizované progresivním ireverzibilním strukturálním poškozením sakroiliakálních kloubů a kloubů na páteři, vznikem syndesmofytů až ankylózou páteře, s čímž je spojeno snížení funkce, disabilita a zhoršená kvalita života (1). Bylo také prokázáno, že vyšší aktivita AS vede k výraznější strukturální progresi na páteři. Ještě závažnější je průběh, pokud jsou postiženy kořenové klouby horních i dolních končetin (kyčle a ramena), když hovoříme o tzv. rizomelické formě nebo při postižení periferních struktur (artritida, entezitida, daktylitida). Časté jsou i extraskeletální projevy, jako je uveitida, idiopatický střevní zánět a psoriáza (2). Pacienti s AS mají také zvýšené kardiovaskulární riziko a zkrácenou střední délku života.
Terapie AS má být komplexní a skládat se z léčby nefarmakologické a farmakologické. Z farmakologické léčby je evidence o účinnosti nesteroidních antirevmatik (NSA), lokálních glukokortikoidů, analgetik a sulfasalazinu u periferních forem (3).
Výrazným milníkem v léčbě AS bylo zavedení biologické léčby v roce 2003, a to konkrétně anti-TNF preparátů. Biologické chorobu modifikující antirevmatické léky (bDMARDs) působí u AS rychle a mohutně a ovlivňují všechny aspekty onemocnění (4). Při vysazení bDMARDs dochází poměrně rychle k exacerbaci nemoci, a proto je nutné tyto léky podávat dlouhodobě, někdy celoživotně. Existují i výsledky dlouhodobé léčby anti-TNF preparáty (5).
Anti-TNF léčba je účinná, ale stále zůstává 20–30 % pacientů bez adekvátní odpovědi. Proto se hledaly nové biologické léky s jiným mechanismem účinku. Na základě experimentálních výzkumů byl jako možný cíl léčby identifikován interleukin 17 (6).
Secukinumab je plně humánní, monoklonální protilátka, která přímo inhibuje interleukin 17A. Na základě úspěšných klinických studií fáze III, publikované pod názvem MEASURE 1, 2, 3 (7–9), byl registrován pro léčbu aktivní axiální spondyloartritidy (axSpA) a v současné době probíhá i registrace u tzv. neradiografické axSpA.
Studie MEASURE I měla otevřenou extenzi do trvání 5 let. Studie potvrdila velmi dobrý a přetrvávající efekt, když kritérium ASAS20/40 u pacientů, kteří ukončili léčbu, bylo splněno 78,5/65,2 % (7). Splněny byly také všechny sekundární ukazatele. Dlouhodobou pětiletou extenzi měla i studie MEASURE 2, kde ASAS 20 bylo splněno v 67 % a ASAS 40 v 50 %. Studie MEASURE 2 prokázala také výrazný efekt na zpomalení rentgenové progrese po 4 letech (8).
Studie MEASURE 3 testovala dávky 150 mg a 300 mg s.c. měsíčně. Nyní jsou k dispozici tříleté výsledky. Rozdíly v účinnosti obou dávek nebyly u celé skupiny signifikantní, ale výraznější byly při dávce 300 mg u pacientů se selháním anti-TNF léčby v minulosti (9).
Abychom získali vlastní data z reálné klinické praxe v České republice, provedli jsme retrospektivní studii pacientů léčených s radiografickou i neradiografickou spondylitidou v národním registru ATTRA.
METODIKA
Biologická léčba axiální spondyloartritidy (axSpA) je dle doporučení České revmatologické společnosti indikována u pacientů s radiografickou formou, kteří v minulosti selhali na konvenční léčbě a mají stále vysokou aktivitu (10). Konvenční léčba je charakterizována jako použití alespoň dvou NSA v maximální dávce po dobu 4 týdnů, sulfasalazin u periferních forem a obstřiky lokálním glukokortikoidem u forem s mono - nebo oligoartritidou. Aktivita nemoci by měla být vysoká a charakterizovaná sérovým CRP vyšším než 10 mg/l. Pacienti s neradiografickou formou by měli mít současně nález aktivní sakroiliitidy na MR a dvojnásobně zvýšené CRP. Všichni pacienti jsou léčeni v centrech biologické léčby a zařazeni do registru ATTRA.
U pacientů jsou sledovány demografické údaje, forma onemocnění a dále aktivita. Pro hodnocení aktivity se používá BASDAI (Bath Ankylosing Spondylitis Disease Activity Index) a ASDAS (Ankylosing Spondylitis Disease Activity Score), pro hodnocení kvality života pak HAQ (Health Assessment Questionnaire), EuroQol a SF-36. Dále se hodnotí počet aktivních kloubů (kloubní index) a počet aktivních entezitid (entezitický index). Vyšetření jsou prováděna 1. rok v tříměsíčních intervalech, dále pak v šestiměsíčních intervalech. Také je hodnoceno přežívání na léčbě a důvody k přerušení léčby
STATISTIKA
Kategoriální proměnné byly charakterizovány pomocí absolutních a relativních četností. Spojité proměnné byly popsány průměrem se směrodatnou odchylkou a mediánem s 5. a 95. percentilem. Porovnání rozdílů mezi hodnotami při zahájení léčby a po 2 letech léčby bylo provedeno Wilcoxonovým párovým testem (nebyla splněna podmínka normálního rozdělení). Hladina statistické významnosti byla nastavena na 5 %. K odhadu setrvání na léčbě byla použita Kaplanova-Meierova metoda přežití. Všechny statistické výstupy analýzy byly získány pomocí softwaru IBM SPSS Statistics 25.0.
VÝSLEDKY
Ankylozující spondylitida (radiografická axiální spondyloartritida)
Do studie bylo zařazeno celkem 243 pacientů, z toho 148 (60,9 %) mužů a 95 žen (39,1 %). Průměrné trvání symptomů při zahájení léčby bylo 11 ± 9 let a věk při diagnóze 35 ± 10 let (tab. 1). Onemocnění bylo na začátku léčby silně aktivní, když průměrné BASDAI bylo 6,1 ± 1,9, průměrné ASDAS 3,8 ± 1,0. Šlo již o pacienty s existujícím funkčním postižením, když průměrné HAQ bylo 1,3 ± 0,6. Anamnesticky mělo před léčbou secukinumabem 44 % glukokortikoidy, 60 % sulfasalazin a 28 % methotrexát. Co se týče předcházející biologické léčby, tak 35,8 % mělo biologickou léčbu poprvé, 26,7 % mělo selhání jednoho inhibitoru TNF a 37,5 % selhání dvou a více inhibitorů TNF.
Tab. 1. Charakteristika pacientů s axiální spondyloartritidou na začátku sledování (n = 243) 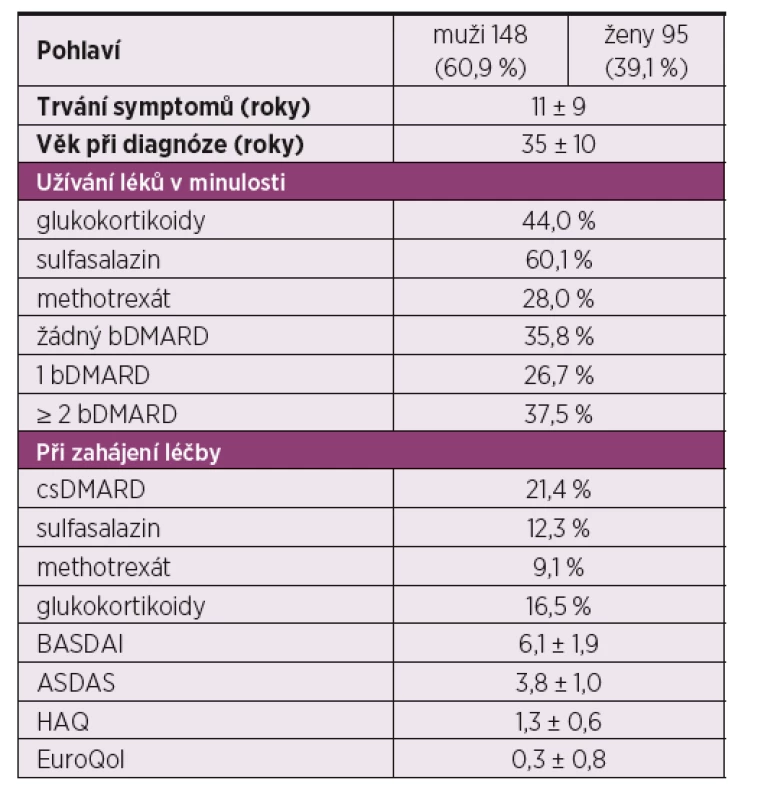
Při zahajování léčby secukinumabem mělo 21,4 % pacientů souběžnou medikaci syntetickými DMARD, konkrétně 12,3 % bylo léčeno sulfasalazinem a 9,1 % methotrexátem, glukokortikoidy pak mělo 16,5 % pacientů (tab. 1).
Index BASDAI klesl z počátečních průměrných 6,1 ±1,9 na 2,8 ± 2,0 po 24 měsících (p < 0,001) (obr. 1).
Obr. 1. Účinnost léčby secukinumabem (Cosentyx®): aktivita onemocnění dle BASDAI 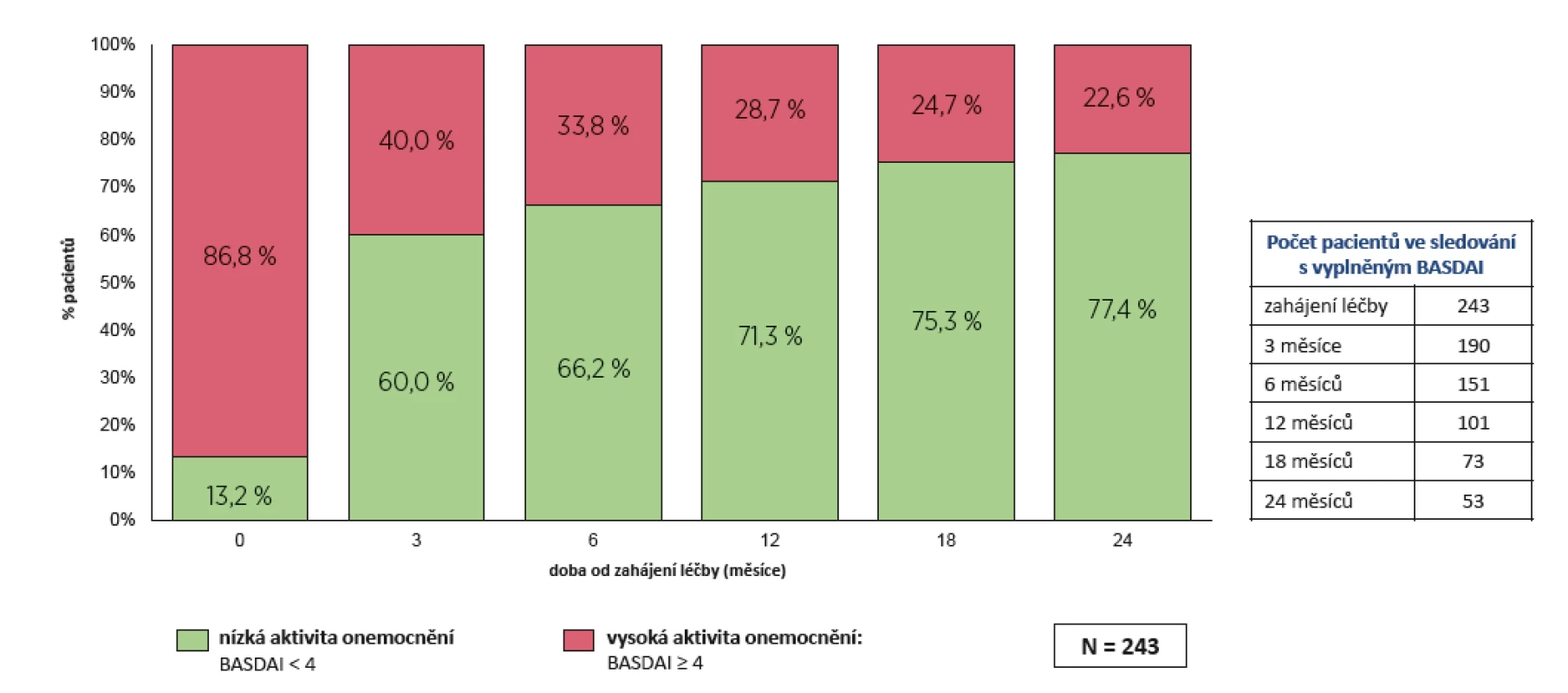
Skóre ASDAS kleslo z počátečních 3,8 ± 1,0 na 2,3 ± 0,9 po 24 měsících (p < 0,001) (obr. 2). Klinicky významného zlepšení ASDAS (> 1,1) bylo dosaženo u 71,7 % pacientů po 2 letech léčby (obr. 3). Pokud použijeme kritérium podstatného zlepšení ASDAS (změna > 2,0), pak bylo dosaženo v 39,6 % případů (obr. 4).
Obr. 2. Účinnost léčby secukinumabem (Cosentyx®): snížení ASDAS během 2 let léčby 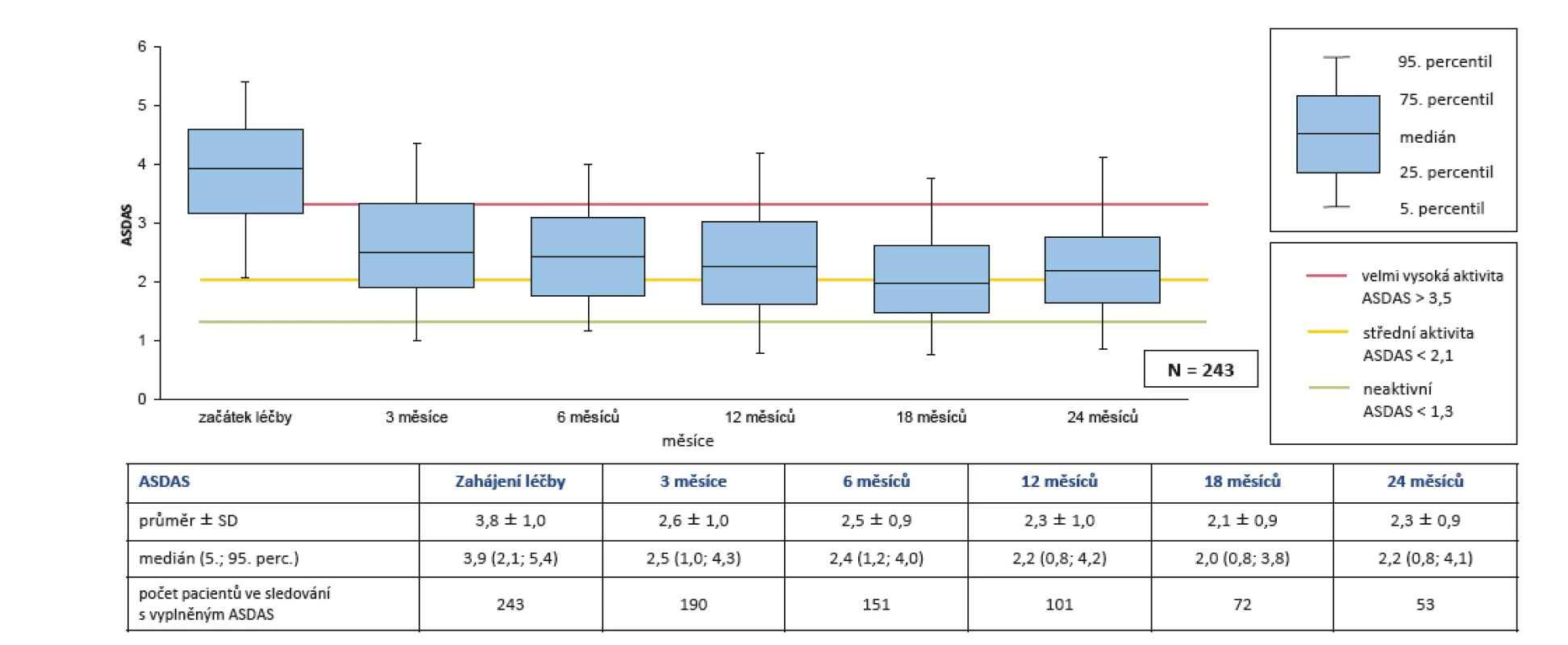
Obr. 3. Účinnost léčby secukinumabem: klinické významné zlepšení dle ASDAS ( 1,1) 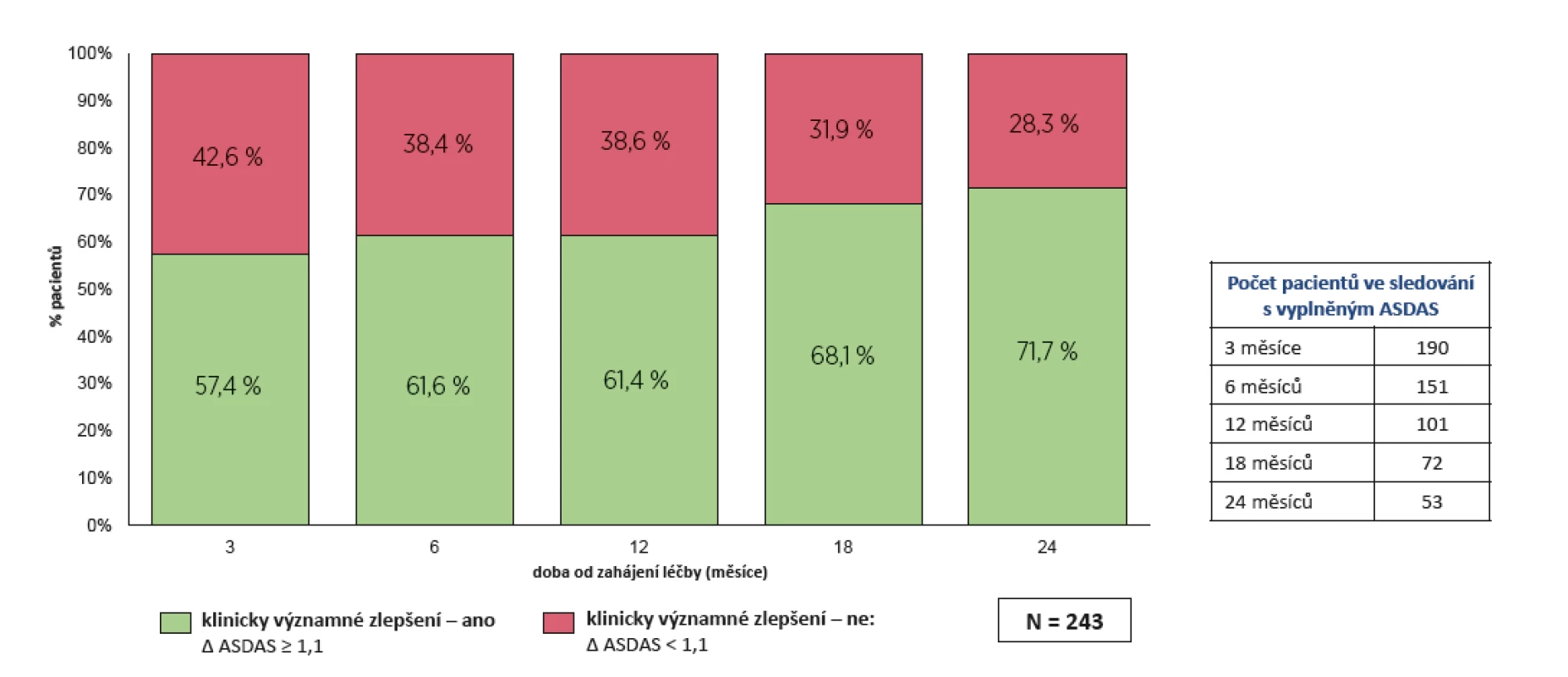
Obr. 4. Účinnost léčby secukinumabem: podstatné zlepšení dle ASDAS (∆ ≥ 2,0) 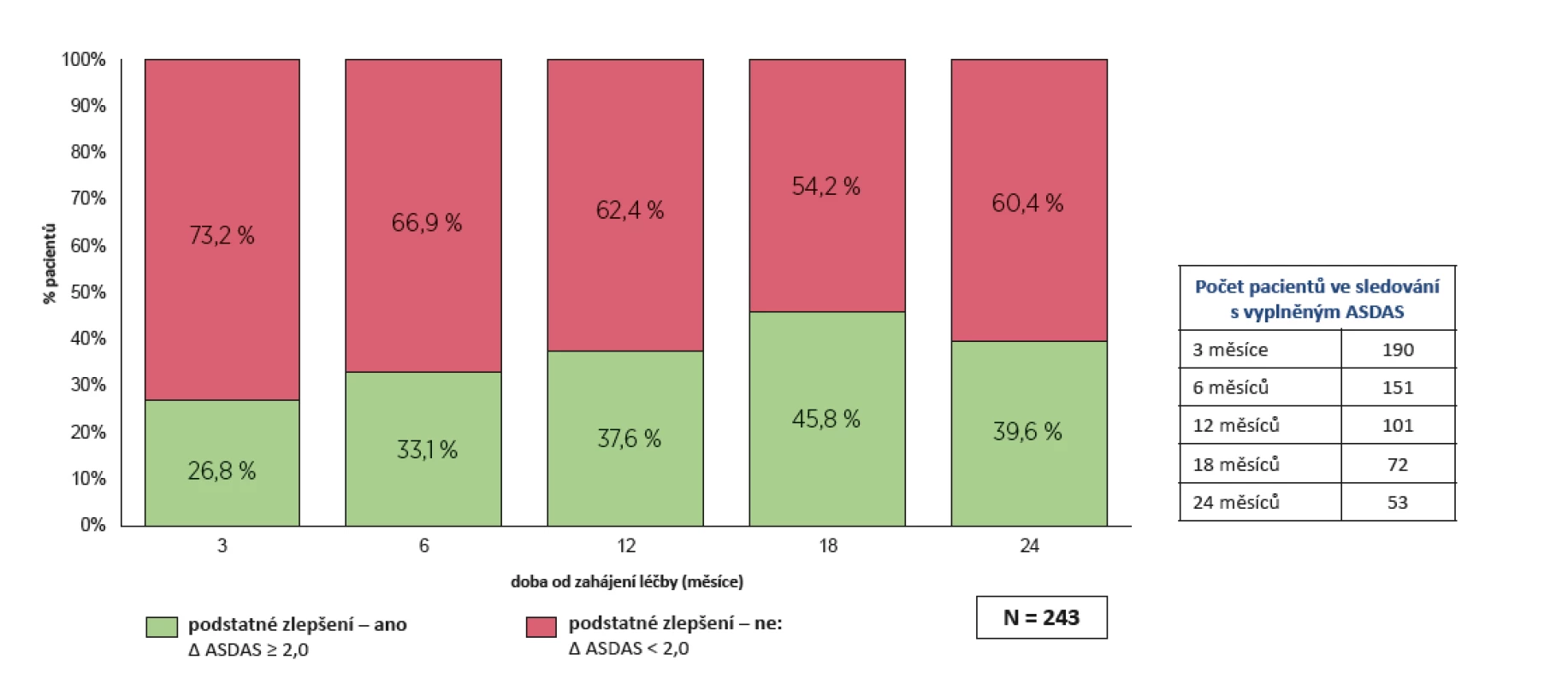
Stavu neaktivního onemocnění (ASDAS méně než 1,3) bylo dosaženo po 2 letech léčby v 13,2 % případů, stavu neaktivního onemocnění a stavu střední aktivity pak ve 45,3 % případů. Naopak počet pacientů s velmi vysokou aktivitou poklesl z 65,0 % na začátku léčby na 11,3 % po 24 měsících léčby (obr. 5).
Obr. 5. Účinnost léčby secukinumabem (Cosentyx®): aktivita onemocnění dle ASDAS 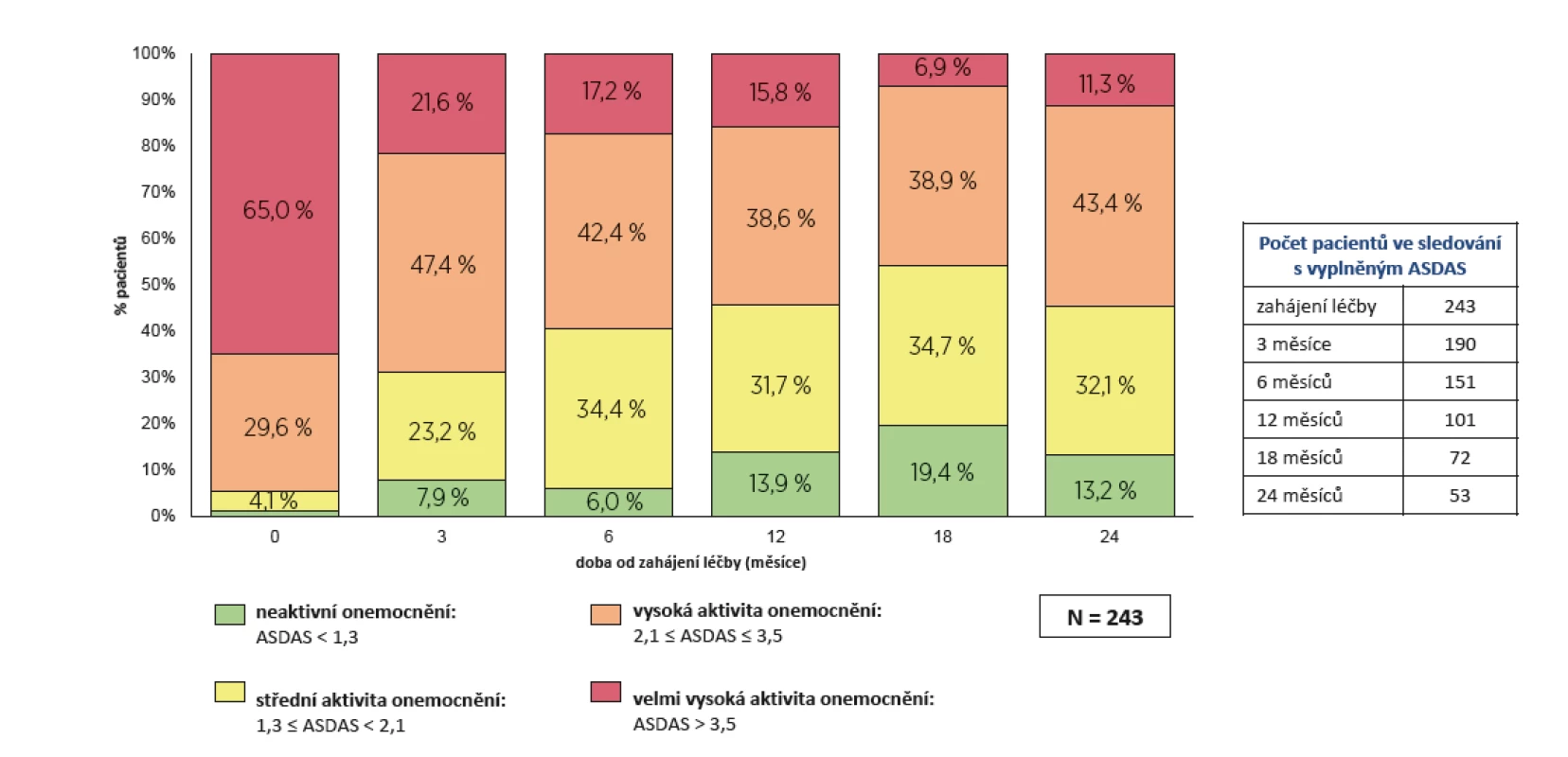
Skóre HAQ pokleslo z iniciálních 1,3 ± 0,6 na 0,8 ± 0,6 po 24 měsících léčby (p < 0,001) (obr. 6). Skóre EuroQol se zvýšilo z iniciálních 0,30 ± 0,32 na 0,67 ± 0,23 po 24 měsících (p < 0,001) (u tohoto skóre znamená zvýšení zlepšení – pozn. autora) (obr. 7).
Obr. 6. Účinnost léčby secukinumabem (Cosentyx®): snížení HAQ během 2 let léčby 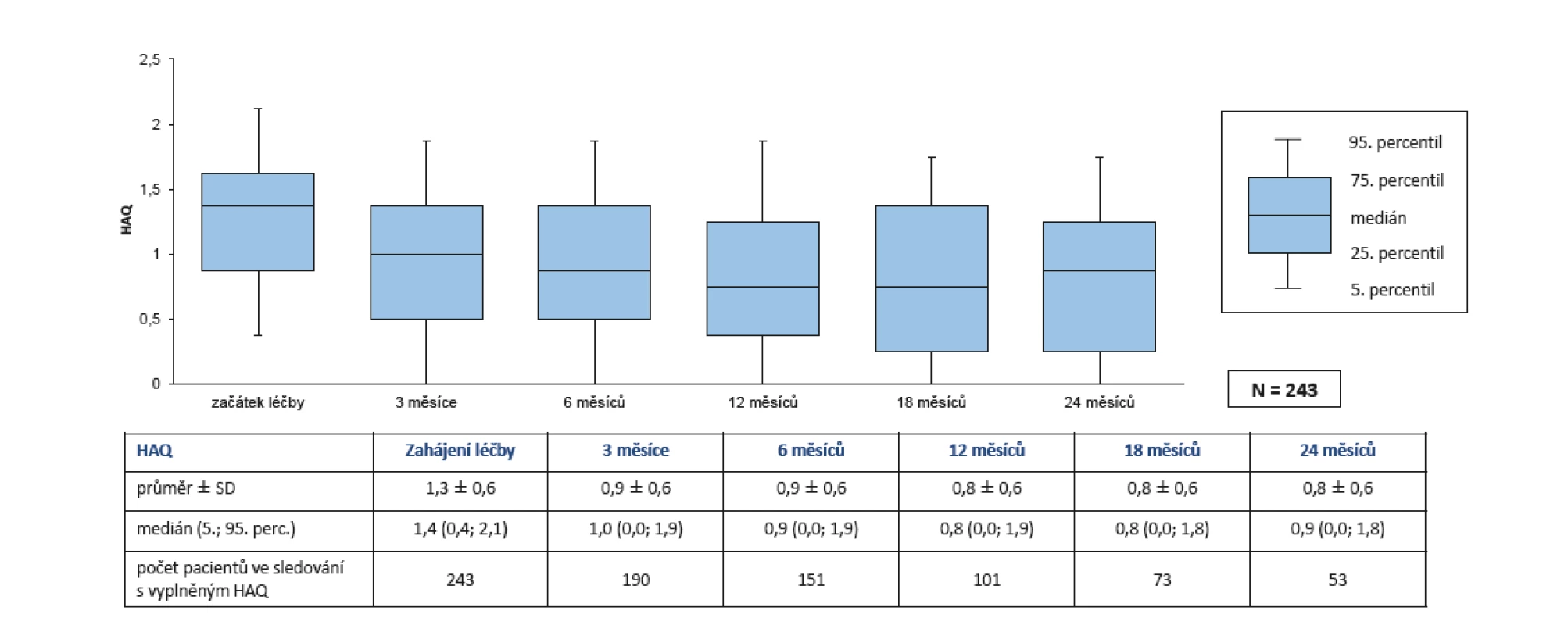
Obr. 7. Účinnost léčby secukinumabem (Cosentyx®): zvýšení kvality života (EuroQol) během 2 let léčby 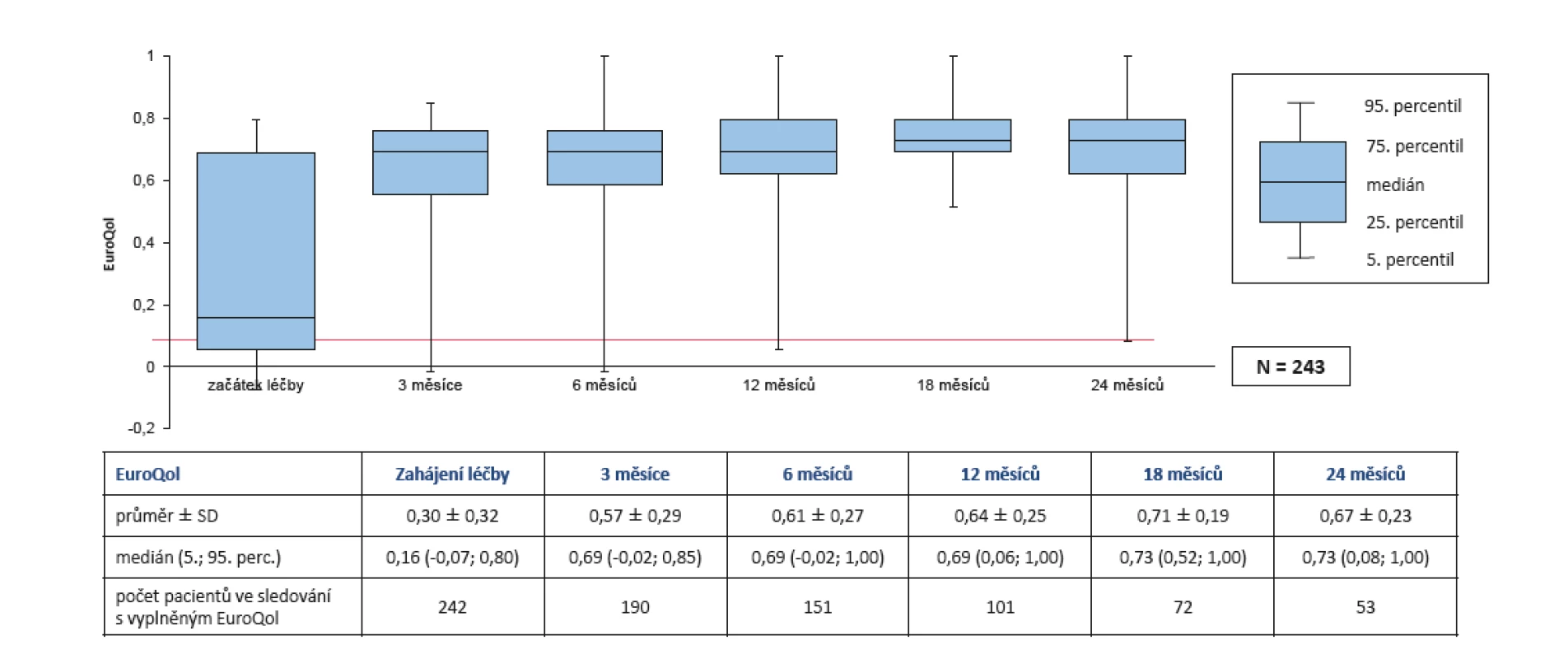
Dalším použitým dotazníkem, který hodnotí komplexně kvalitu života, je SF-36. Při léčbě Cosentyxem došlo k signifikantnímu zlepšení všech jeho osmi komponent (obr. č. 8).
Obr. 8. Účinnost léčby secukinumabem (Cosentyx®): zvýšení kvality života (SF-36) během 2 let léčby 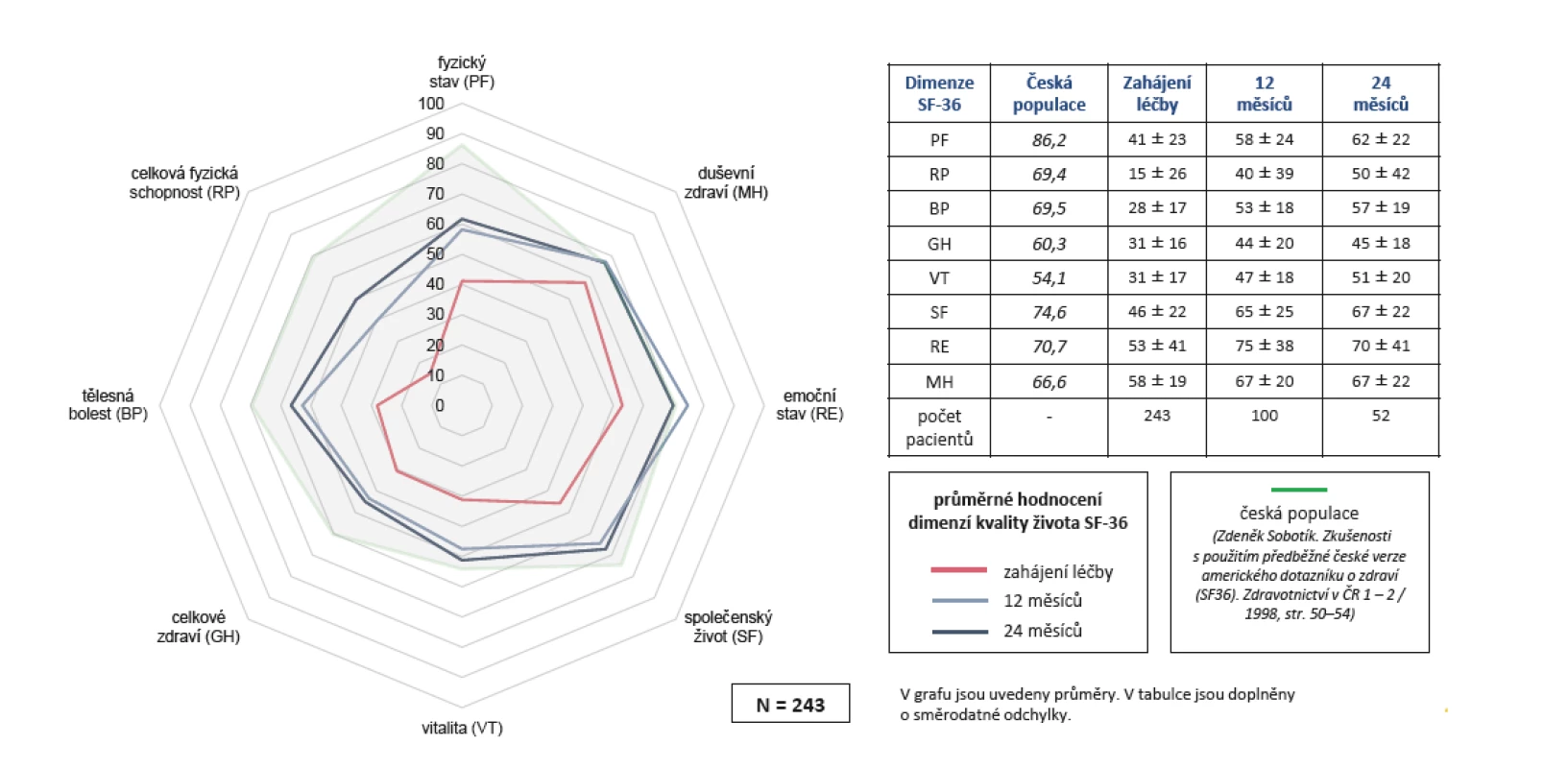
Setrvání na léčbě bylo 70,8 % (95% CI 64,7–77,0) po 12 měsících léčby a 63,5 % (95% CI 56,6–70,4) po 24 měsících léčby. Nejčastějším důvodem přerušení léčby byla primární neúčinnost (42,9 %), sekundární neúčinnost (23,4 %) a nežádoucí účinky (9,1 %), u 22,1 % byly důvody jiné či neznámé (obr. 9).
Obr. 9. Účinnost léčby secukinumabem (Cosentyx®): setrvání na léčbě 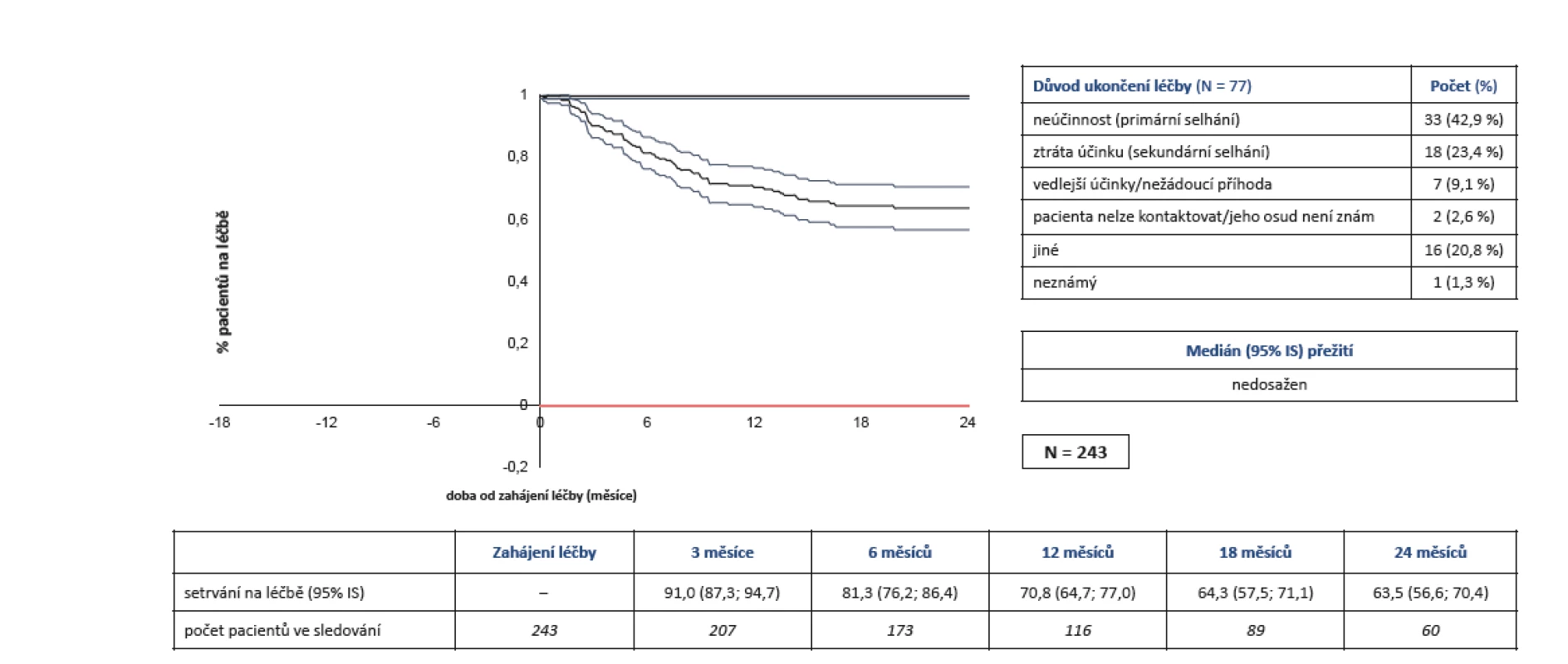
Dalším parametrem kvality života, který byl hodnocen, byla práceschopnost. V průběhu dvouleté léčby došlo k obnovení práceschopnosti u 37,7 % pacientů invalidních či v pracovní neschopnosti a 15,7 % pracujících či aktivně hledajících práci naopak pracovní schopnost ztratilo (obr. 10).
Obr. 10. Účinnost léčby secukinumabem (Cosentyx®): práceschopnost pacientů 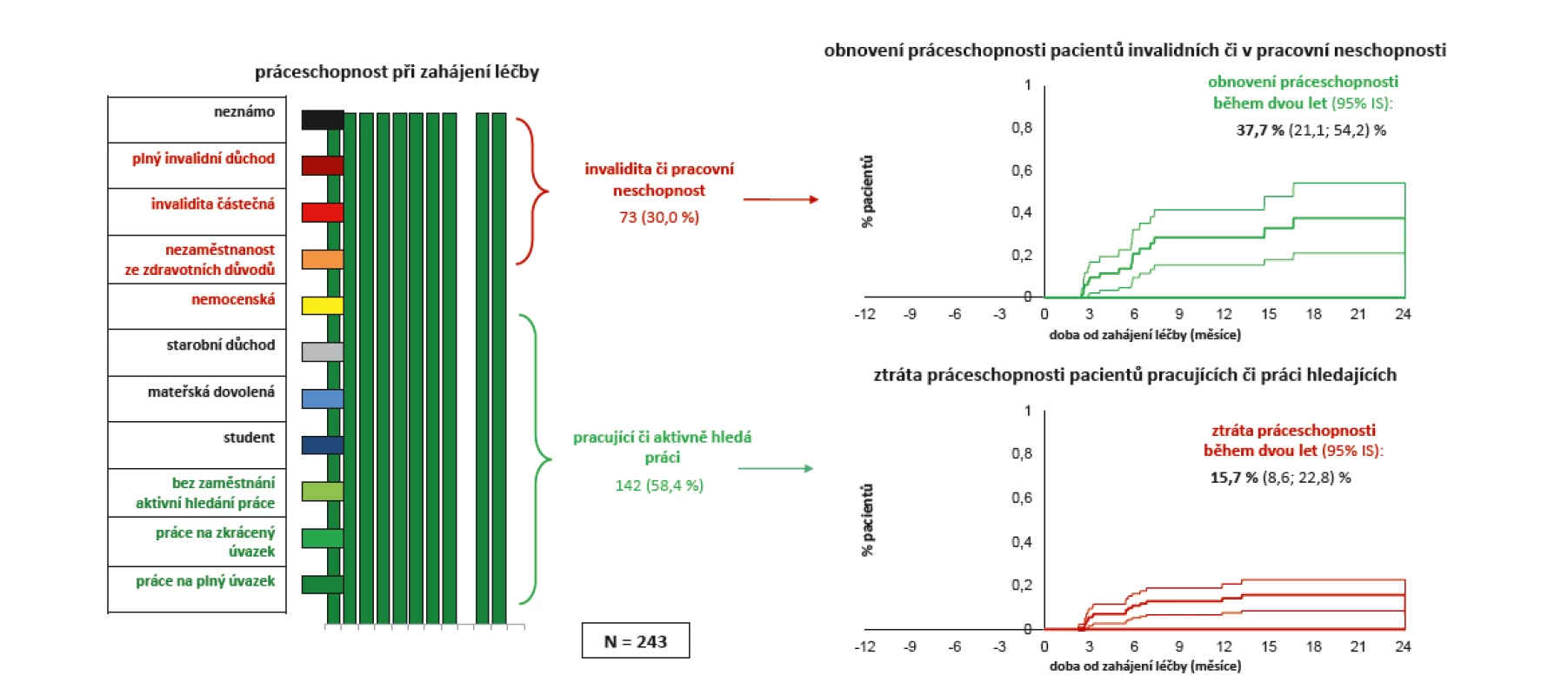
Neradiografická axiální spondyloartritida
Soubor pacientů s neradiografickou axSpA léčených Cosentyxem je podstatně menší než s formou radiografickou a činí pouze 29 pacientů, což souvisí s pozdějším zavedením Cosentyxu v této indikaci. Malý počet pacientů neumožnuje přímé statistické srovnání obou souborů, ale je možné konstatovat, že výsledky léčby radiografické a neradiografické formy jsou podobné. Iniciální BASDAI pokleslo z 5,9 ± 1,9 na 2,5 ± 1,3 po 12 měsících léčby. Iniciální ASDAS pokleslo z 3,7 ± 1,0 na 2,3 ± 0,8 po 12 měsících léčby. Klinicky významného zlepšení po 1 roce léčby bylo dosaženo v 72,7 % případů (obr. 11).
Obr. 11. Neradiografická SpA – účinnost léčby secukinumabem: klinické významné zlepšení dle ASDAS (Δ ≥ 1,1) 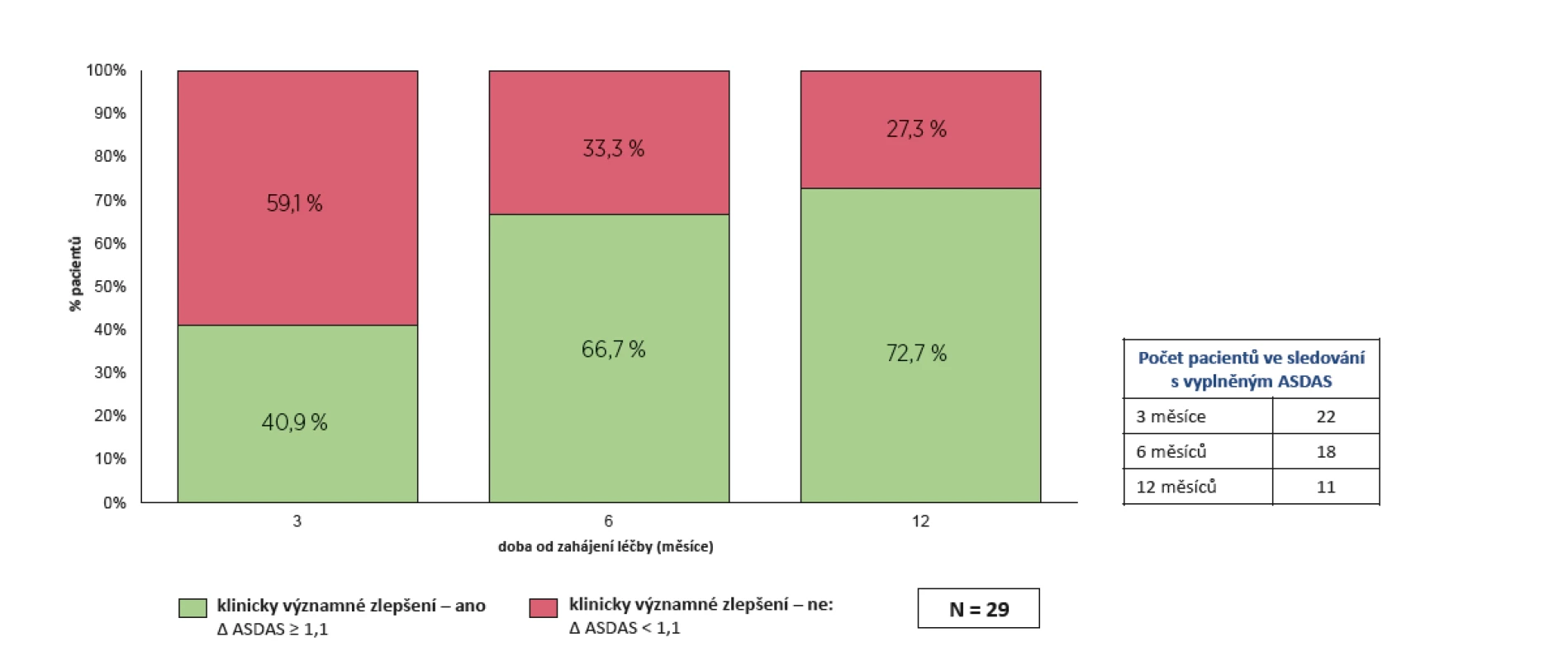
Bezpečnost léčby
Bezpečnost léčby Cosentyxem byla sledována ve skupině s radiografickou formou SpA. V souboru bylo 243 pacientů s mediánem sledování 10,6 měsíců a celkovou expozicí 302,2 paciento-roků. Výskyt nežádoucích účinků byl 129/1000 paciento-roků a nejčastější byly infekce (46/1000 paciento-roků). Frekvence závažných nežádoucích účinků byla 23,2/1000 paciento-roků. Vyskytly se dvě latentní infekce a jeden případ nádoru (obr. 12).
Obr. 12. Bezpečnost léčby secukinumabem (Cosentyx®): incidence nežádoucích příhod 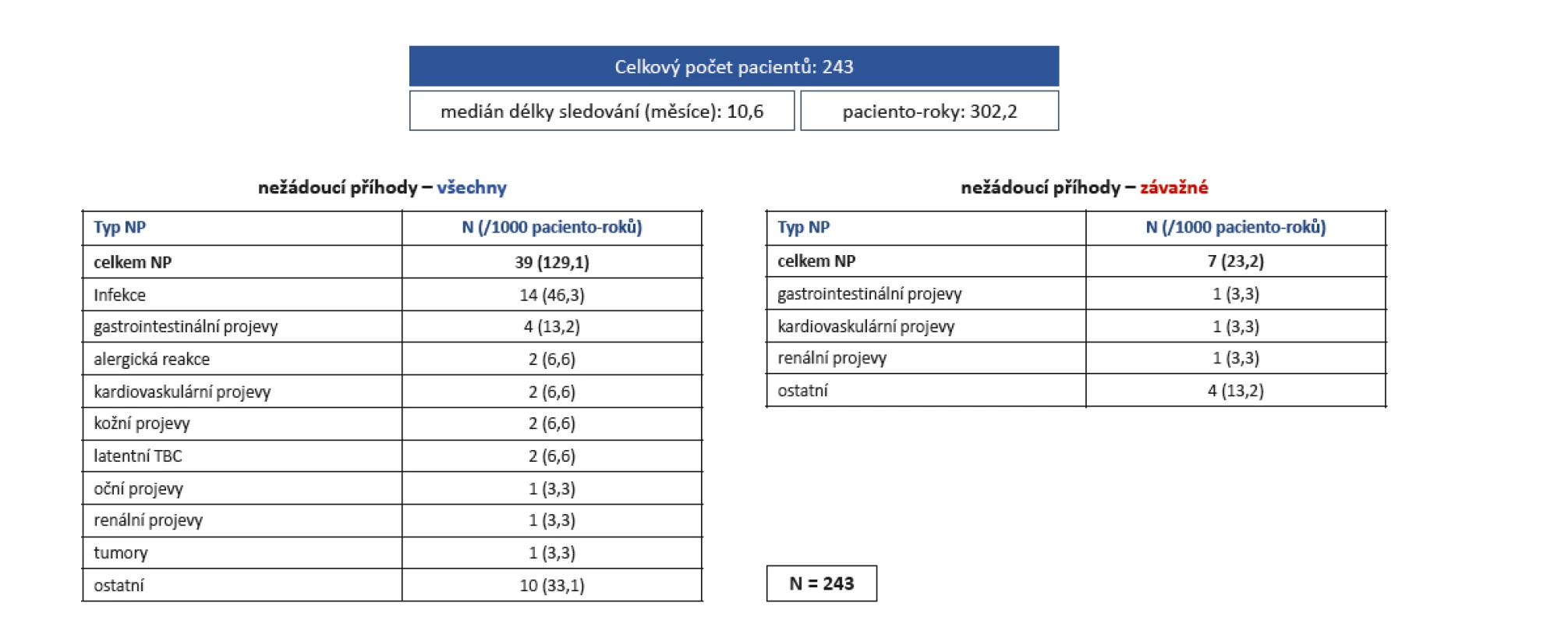
DISKUZE
Registry přinášejí na rozdíl od randomizovaných klinických studií data z reálné klinické praxe u neselektované populace. Další jejich výhodou je vyšší počet pacientů a delší doba sledování. Nevýhodou pak absence kontrolní skupiny a zpravidla horší dostupnost dat. Při hodnocení dlouhodobé léčby je jedním z nejdůležitějších parametrů (a někdy i primárním) adherence k léčbě, někdy také nazývaná přežívání na léčbě. Jde o složený ukazatel, který v sobě obsahuje jak faktor účinnosti, tak nežádoucích účinků léčby. Publikovaná data o anti-TNF lécích ve studiích u AS v délce trvání 3–5 let ukázala retenci 49–72 % (11, 12). Ve studiích MEASURE 1 a MEASURE 2 se secukinumabem dokončilo 5 let sledování 68–80 % pacientů (7, 8). V registru ATTRA byla dvouletá adherence k léčbě 63 % pacientů, což odpovídá údajům z registrů s anti-TNF i dlouhodobých extenzí studií s IL-17 inhibitory. Jeden z faktorů, který negativně ovlivnil tento ukazatel, byl fakt, že podíl pacientů dosud neléčených anti-TNF byl v registru ATTRA pouze 35,8 %. Retence na prvním bDMARD je u AS obecně lepší než u pacientů se selháním jednoho nebo více anti-TNF léků, jak prokázala i nedávno dokončená integrovaná analýza EuroSpA (13). Při analýze důvodů přerušení léčby byla relativně častým důvodem primární neúčinnost (42,9 %) a méně časté sekundární selhání (23,4 %) a nežádoucí účinky (9,1 %). Tato čísla mohou na jedné straně opravdu reflektovat aplikaci secukinumabu u již TNF selhaných nemocných, na druhé straně ale i další vlastnosti léku (menší imunogenitu, menší toxicitu).
Účinnost léčby Cosentyxem je nutné hodnotit jako dobrou. K signifikantnímu poklesu aktivity hodnocené pomocí ASDAS došlo již po 3 měsících a toto zlepšení s dalším mírným poklesem přetrvávalo až do konce sledování (tzn. po 24 měsících). Za klinicky významné snížení ASDAS se považuje pokles o 1,1 a tohoto ukazatele bylo dosaženo po 2 letech u 71,7 % pacientů, což se může jevit jako uspokojivé. Na druhé straně stavu neaktivního onemocnění dle kritéria ASDAS (< 1,3) bylo dosaženo pouze v 13,2 % a stavu mírné (dříve střední aktivity < 2,1) pak u necelé poloviny pacientů. Je nutné ale diskutovat, zda dosažení stanoveného cíle je v konceptu strategie léčba k cíli (treat to target – T2T) u axSpA vůbec vhodné a realistické. Koncept léčby k cíli byl na základě dobrých zkušeností z interní medicíny zaveden nejprve do léčby revmatoidní artritidy a později do léčby dalších zánětlivých revmatických onemocnění. Strategické studie pak prokázaly, že aplikování strategie T2T zmenšuje strukturální progresi onemocnění a tím zlepšuje kvalitu života nemocných. Strategie T2T u AS byla rovněž publikována relativně brzy, ale od začátku byla silně kritizována pro slabou evidenci a vágní definici cílů. Stav se poněkud zlepšil při publikaci novější verze T2T (15). Stále však trvá diskuse o tom, jaký ukazatel aktivity je pro axiální spondyloartritidy nejvhodnější a jak definovat stav remise či nízké aktivity. Dlouho se nejvíce používal index BASDAI, který je dodnes používán v České republice k měření prahové aktivity pro indikaci bDMARD u axSpA (16). Hlavní výtky proti indexu BASDAI jsou jednak, že hodnotí pouze subjektivní údaje pacienta a nemá žádný laboratorní údaj o aktivitě a dále že nehodnotí extraartikulární projevy SpA. Skóre ASDAS již obsahuje jeden reaktant akutní fáze (CRP nebo FW) (17). Nicméně opět nehodnotí extraartikulární projevy SpA a je to jeden z důvodů, proč ho ACR ve svých recentních doporučeních nedoporučuje používat (18). Domníváme se však, že základní principy T2T, tj. hodnotit aktivitu a adjustovat léčbu, jsou užitečné. A to, že až polovina našich pacientů s axSpA po 24 měsících léčby nedosáhla stavu nízké aktivity, vypovídá nepřímo i o tom, že aplikace T2T není v praxi dostatečně využívána.
Hodnocení léčby pacientem je stále více diskutovaným problémem hodnocení aktivity a účinnosti léčby u zánětlivých revmatických onemocnění včetně spondyloartritid. Ukazatele, které pacient hodnotí, se nazývají pacientem reportované ukazatele nebo zkratkou PRO (z anglického „patient reported outcomes“). Pacienta zajímají tyto ukazatele (např. bolest, ztuhlost, funkce, kvalita života) více než některé objektivní ukazatele, jako je CRP či biomarkery nebo strukturální progrese.
Při léčbě Cosentyxem v našem registru došlo k poklesu HAQ z průměrných 1,3 na začátku léčby na 0,8 po 2 letech léčby. Je nutné si v tomto kontextu uvědomit, že hodnota HAQ 1,5 je doporučovanou hranicí pro přiznání plného invalidního důchodu a hodnoty HAQ 1,0 pro částečný invalidní důchod. Podařilo se nám také prokázat, že během 2 let léčby došlo k obnovení práceschopnosti u 37,7 % pacientů a ke ztrátě práceschopnosti u 15,7 % pacientů. Terapie bDMARD je stále relativně nákladná, ale snížením nepřímých nákladů onemocnění a schopností pacientů pracovat je vysoce farmakoekonomicky efektivní.
Kromě zlepšení v dotazníku HAQ bylo průkazné i zlepšení v dotazníku EuroQol, který rovněž hodnotí kvalitu života. Jedním z nejvíce používaných dotazníků hodnotících komplexně kvalitu života, který se používá napříč různými medicínskými specializacemi, je dotazník SF-36. Hodnotí jak fyzické parametry, bolest, tak i duševní, emoční a sociální zdraví. Pomocí tohoto dotazníku jsme prokázali, že při léčbě Cosentyxem došlo prakticky k normalizaci kvality života pacientů se SpA.
Bezpečnost léčby Cosentyxem byla dobrá a neobjevily se žádné nové signály toxicity. Počet hlášených nežádoucích účinků léčby byl velmi nízký, což může odrážet jednak na registr relativně malý počet pacientů a krátkou dobu expozice, jednak ale také určité nedostatečné hlášení těchto nežádoucích účinků. Nejčastější byly infekce horního dýchacího traktu, což koresponduje i s analýzou dlouhodobě extenze studie MEASURE 2 (8). V naší studii se prakticky nevyskytovaly některé nežádoucí účinky, zejména infekce kandidou (udávaný výskyt 1,0 na 100/paciento-roků), exacerbace nebo vznik idiopatických střevních zánětů (frekvence 0,5 na 100/paciento-roků) a uveitidy (frekvence 0,5 na 100/paciento-roků), které se objevují jen zřídka, ale jsou u SpA pečlivě sledované. Zatím žádná studie neprokázala vyšší riziko nádorů a kardiovaskulárních komplikací při léčbě inhibitory IL-17
ZÁVĚR
Retrospektivní analýza dvouleté léčby pacientů s axiálními spondyloartritidami v registru ATTRA prokázala dobrou účinnost a bezpečnost léčby Cosentyxem v běžné praxi. Inhibitory IL-17 jsou bDMARD s jiným mechanismem účinku než inhibicí TNF-α a jejich zavedení do klinické praxe je nutné přivítat.
Podpořeno projektem Ministerstva zdravotnictví České republiky koncepčního rozvoje výzkumné organizace 00023728 (Revmatologický ústav).
Konflikt zájmů: žádný.
adresa pro korespondenci:
prof. MUDr. Karel Pavelka, DrSc.
Revmatologický ústav
Na Slupi 4, 128 00 Praha 2
e-mail: pavelka@revma.cz
Zdroje
1. Ramiro S, van der Heijde D, van Tubergen A, et al. Higher disease activity leads to more structural damage in the spine in ankylosing spondylitis: 12-year longitudinal data from the OASIS cohort. Ann Rheum Dis 2014; 73 : 1455–1461.
2. Dougados M, Baeten D. Spondyloarthritis. Lancet 2011; 377 : 2127–2137.
3. van der Heijde D, Ramiro S, Landewé R, et al. 2016 update of the ASAS-EULAR management recommendations for axial spondyloarthritis. Ann Rheum Dis 2017; 76 : 978–991.
4. Braun J, Kiltz U, Heldmann F, et al. Emerging drugs for the treatment of axial and peripheral spondyloarthritis. Expert Opin Emerg Drugs 2015; 20 : 1–14.
5. Baraliakos X, Listing J, Fritz C, et al. Persistent clinical efficacy and safety of infliximab in ankylosing spondylitis after 8 years – early clinical response predicts long-term outcome. Rheumatology 2011; 50 : 1690–1699.
6. Baeten D, Sieper J, Braun J, et al. Secukinumab, an interleukin 17A inhibitor, in ankylosing spondylitis. N Engl J Med 2015; 373 : 2534–2548.
7. Baraliakos X, Braun J, Deodhar A, et al. Long-term efficacy and safety of secukinumab 150 mg in ankylosing spondylitis: 5-year results from the phase III MEASURE 1 extension study. RMD Open 2019. doi:10.1136/rmdopen-2019-001005
8. Marzo-Ortega H, Sieper J, Kivitz A, et al. 5-year efficacy and safety of secukinumab in patients with ankylosing spondylitis: end-of-study results from the phase 3 MEASURE 2 trial. Rheumatology 2020; 2: e339–e346.
9. Pavelka K, Kivitz AJ, Dokoupilová E, et al. Secukinumab 150/300 mg provides sustained improvements in the signs and symptoms of active ankylosing spondylitis: 3-year results from the phase 3 MEASURE 3 study. ACR Open Rheumatol 2020; 2020; 2(2): 119–127.
10. Pavelka K. Doporučení České revmatologické společnosti pro léčbu ankylozující spondylitidy. Čes. Revmatol. 2012; 1 : 4–11.
11. Deodhar A, Braun J, Inman RD, et al. Golimumab administered subcutaneously every 4 weeks in ankylosing spondylitis: 5 year results of GO-RAISE study. Ann Rheum Dis 2015; 74 : 757–761.
12. van der Heijde D, Dougados M, Landewe R, et al. Sustained efficacy, safety and patient reported outcomes of certolizumab pegol in axial spondyloarthritis. 4 year outcomes of the GO-RAISE study. Ann Rheum Dis 2015; 74 : 757–761.
13. Michelsen B , Lindström U, Codreanu C, et al. Drug retention, inactive disease and response rates in 1860 patients with axial spondyloarthritis initiating secukinumab treatment – routine care data from 13 registries in the EuroSpA collaboration. RMD Open 2020; 6(3): e001280.
14. Smolen J, Breedveld FC, Burmestr GR, et al. Treating rheumatoid arthritis to target. 2014update of the recommendations of an international task force Ann Rheum Dis 2016; 75 : 3–15.
15. Smolen J, Schools M, Braun J, et al. Treating axial spondyloarthritis and peripheral spondyloarthritis to target. 2017 update of recommendations by international task force. Ann Rheum Dis 2018; 77 : 3–17.
16. Garret S, Jenkinson T, Kennedy LG, et al. A new approach to defining disease status in ankylosing spondylitis. The Bath Ankylosing Spondylitis Disease Activity Index. J Rheumatol 1994; 21 : 2286–2291.
17. Lukas C, Landewe R, Sieper J, et al. Development of an ASAS-endorsed disease activity score (ASDAS) in patients with ankylosing spondylitis. Ann Rheum Dis 2009; 68 : 18–24.
18. Liew JW, Dubreuil M. Treat to target in axial spondyloarthritis. Pros Cons and future directions. Rheum Dis Clin N Am 2020; 46 : 343–356.
Štítky
Dermatologie Dětská revmatologie Revmatologie
Článek vyšel v časopiseČeská revmatologie
Nejčtenější tento týden
2020 Číslo 4- Komplementární mechanismus účinku analog vitaminu D a topických kortikosteroidů v léčbě ložiskové psoriázy
- V patogenezi psoriázy jde o víc než jen o IL-17A
- Výhody subkutánně podávaného methotrexátu
- Revmaporadna – snadná cesta k psychologické podpoře pro pacienty se sklerodermií a myozitidou
- Léčba lupusové nefritidy v praxi
-
Všechny články tohoto čísla
-
Něco staré končí,
něco nové začíná…. - Stanovisko České revmatologické společnosti k léčbě revmatických onemocnění a očkování v kontextu infekce SARS-CoV-2
- Klinické zkušenosti z dlouhodobé léčby axiální spondyloartritidy secukinumabem
- Validace české verze dotazníků hodnotících funkční omezení pacientů se systémovou sklerodermií
-
Nízkodávková výpočetní tomografie s cínovou filtrací v diagnostice sakroiliitidy –
naše první zkušenosti - Kardiotoxicita cyklofosfamidu při léčbě mikroskopické polyangiitidy
- Úskalí diagnostiky ANCA asociovaných vaskulitid – kazuistika
-
Něco staré končí,
- Česká revmatologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Úskalí diagnostiky ANCA asociovaných vaskulitid – kazuistika
- Validace české verze dotazníků hodnotících funkční omezení pacientů se systémovou sklerodermií
- Stanovisko České revmatologické společnosti k léčbě revmatických onemocnění a očkování v kontextu infekce SARS-CoV-2
- Klinické zkušenosti z dlouhodobé léčby axiální spondyloartritidy secukinumabem
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



