-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Faktory ovlivňující účinnost anti-TNF terapie v klinické praxi: zkušenosti z národního registru ATTRA
Factors affecting the efficacy of anti-TNF therapy in clinical practice: experience from the ATTRA national registry
Aim:
This study characterized response to the first trial of antitumor necrosis factor (TNF) drugs among rheumatoid arthritis (RA) patients in the Czech registry of biological therapy (ATTRA).Materials & methods:
The study included all patients with disease activity scores (DAS28) >5.1, and a few with scores <5.1. Monoclonal antibodies were pooled and compared to etanercept for 1 year.Results:
1945 patients were enrolled (518 etanercept, 1427 antibodies). From week 10–54, mean DAS28 was significantly lower with etanercept; and remission and low disease activity (LDA) rates were significantly higher. Etanercept was a significant predictor of remission.Conclusions:
Remission and LDA were more frequent with etanercept than with monoclonal antibodies..Key words:
Rheumatoid arthritis, biological DMARDs, anti-TNF, etanercept, monoclonal antibodies
Autoři: K. Pavelka 1; K. Chroust 2; P. Němec 3
Působiště autorů: Revmatologický ústav a Revmatologická klinika 1. lékařské fakulty Univerzity Karlovy, Praha 1; DSC Services, s. r. o., Tišnov 2; II. interní klinika, Fakultní nemocnice u sv. Anny v Brně a Lékařská fakulta Masarykovy univerzity, Brno 3
Vyšlo v časopise: Čes. Revmatol., 22, 2014, No. 4, p. 115-123.
Kategorie: Původní práce
Souhrn
Cíl:
Tato práce podává přehled o odpovědi na první léčbu anti-TNF (anti-tumor necrosis factor) preparáty u pacientů s revmatoidní artritidou (RA) v českém registru biologické terapie (ATTRA).Metodika:
Do této studie byli začleněni všichni pacienti se skóre aktivity nemoci (DAS28) > 5,1 a několik pacientů se skóre < 5,1. Skupina pacientů na terapii monoklonálními protilátkami byla srovnána s pacienty na etanerceptu po dobu jednoho roku.Výsledky:
Do studie bylo začleněno celkem 1945 pacientů (518 na etanarceptu a 1427 na monoklonálních protilátkách). V průběhu 10. týdne až 54. týdne bylo u etanerceptu významně nižší průměrné skóre DAS28 a významně častější remise a nízká aktivita nemoci (LDA, low disease activity).Závěr:
Remise a LDA byly častější u etanerceptu než u monoklonálních protilátek.Klíčová slova:
Revmatoidní artritida, biologické DMARDs, anti-TNF, etanercept, monoklonální protilátkyÚvod
Anti-TNF (anti-tumor necrosis factor) terapie byla zavedena u pacientů s revmatoidní artritidou (RA) přibližně před 15 lety a způsobila revoluci v léčbě této závažné, chronické a invalidizující nemoci (1). Biologická léčba je účinnější než konvenční chorobu modifikující léky (DMARDs) jako například methotrexát (MTX). Četné studie prokázaly, že biologická léčba významně více zpomaluje rentgenovou progresi RA než MTX (2). Randomizovaná klinická hodnocení jsou podkladem tzv. evidence-based medicine (medicíny založené na důkazech) u RA, avšak další relevantní data lze také nalézt v národních registrech biologické léčby, které již existují v USA a většině evropských zemí (3). Tyto registry byly původně založeny, aby monitorovaly dlouhodobou bezpečnost biologických preparátů ve velkých kohortách pacientů, avšak nyní je kladen stejně velký důraz také na jejich účinnost. Data z registrů poskytují mnohem reálnější obraz o výsledku terapie než samotná klinická hodnocení: výsledky bývají méně pozitivní, protože do registrů jsou začleněni i starší pacienti s četnými komorbiditami a komedikací, kteří by nesplnili vstupní kritéria pro začlenění do klinického hodnocení.
V klinických studiích nebyly dostupné anti-TNF preparáty přímo srovnány, avšak registry nabízejí přehled o jejich relativní účinnosti. Například v dánském registru DANBIO byly nalezeny významné rozdíly mezi různými anti-TNF preparáty (4). Avšak výsledky z národních registrů by se měly interpretovat obezřetně kvůli otevřenému sledování a nedostatečné randomizaci. Pro účely analýzy musí být léčení pacienti zařazeni do skupin retrospektivně na základě vybraných kritérií, a proto nemusí být jednotlivé skupiny srovnatelné mezi sebou v době zahájení léčby. Český národní registr ATTRA (Anti-TNF Therapy of Rheumatoid Arthritis) byl založen v roce 2001 a jednotlivé biologické preparáty – infliximab, etanercept, adalimumab, rituximab, abatacept, certolizumab, golimumab a tocilizumab – byly do něj zařazeny, když se staly dostupnými. Pacienti jsou léčeni v centrech biologické léčby na základě doporučení České revmatologické společnosti (ČRS) (5).
Cílem této práce bylo srovnat jeden rok léčby pomocí solubilního receptoru (etanercept) s monoklonálními protilátkami u pacientů, kteří byli poprvé léčení anti-TNF preparátem. Tato studie byla také navržena tak, aby identifikovala prediktory léčebné odpovědi nebo remise.
Metody
Jde o observační retrospektivní studii českého národního registru ATTRA. Podle ČRS bylo indikací pro anti-TNF terapii v letech 2001–2007 selhání dvou DMARDs a skóre aktivity nemoci (DAS28) > 5,1. Kritérium selhání DMARDs bylo v roce 2007 zredukováno na selhání jednoho DMARD. Terapeutická odpověď je definována ČRS jako pokles DAS28 o > 1,2 ve 12. týdnu.
Pacienti v této studii nedostávali v minulosti žádnou anti-TNF léčbu a neměli žádné kontraindikace anti-TNF terapie (včetně latentní tuberkulózy, podle doporučení ČRS) (6). Jednotlivé anti-TNF preparáty byly zvoleny podle uvážení ošetřujícího revmatologa a pacienti byli sledováni po dobu 1 roku, s kontrolním vyšetřením u lékaře na začátku terapie, ve 2., 6. a 12. týdnu a poté každé 3 měsíce. Pacienti léčeni monoklonálními protilátkami byli seskupeni do jedné skupiny (dostatečné množství dat bylo dostupné pro infliximab, adalimumab a golimumab) a srovnáni s pacienty, kteří byli léčeni etanerceptem. Pro hodnocení účinnosti byly použity následující parametry: DAS28, počet oteklých kloubů, počet bolestivých kloubů a dosažení nízké aktivity nemoci (LDA, low disease activity) (DAS28 < 3,2), remise (DAS28 < 2,6) a dobré odpovědi na léčbu podle kritérií EULAR (European League Against Rheumatism) (7) a C-reaktivní protein (CRP).
Všichni pacienti, u kterých byla zahájena biologická léčba a byli začleněni do registru ATTRA, podepsali informovaný souhlas s léčbou. Projekt registru ATTRA byl schválen lokální etickou komisí. Jelikož byla tato studie retrospektivní, nebyl požadován žádný informovaný souhlas specifický pro tuto studii.
Statistické metody
Data byla analyzována pomocí Statistica sowftware (verze 9.1, StatSoft, Inc., 2010). Ke srovnání skupin pacientů léčených etanerceptem a monoklonálními protilátkami byl použitý t-test pro číselné parametry (věk, trvání nemoci, DAS28, CRP a počet oteklých a bolestivých kloubů) a Fischerův a M-L chí-kvadrát test byly použity pro kategorické parametry (věk, současná léčba MTX, dobrá odpověď na léčbu podle EULAR, LDA a remise). Všechny testy byly provedeny s hladinou významnosti p = 0,05. Data byla u všech pacientů vyhodnocena bez ohledu na délku léčby, přerušení léčby nebo převedení na jiný biologický preparát do jednoho roku.
Výsledky
Demografické a klinické charakteristiky na začátku léčby
Do studie bylo začleněno celkem 1945 pacientů z registru ATTRA: 518 z nich užívalo etanercept, 655 infliximab, 747 adalimumab a 25 golimumab (celkem 1 427 pacientů bylo léčeno monoklonálními protilátkami). I když byla vstupní hodnota skóre aktivity nemoci pro zahájení biologické léčby DAS28 > 5,1, mělo 19 z 518 pacientů ve skupině s etanerceptem a podobný podíl pacientů v dalších léčebných skupinách DAS28 < 5,1 v době zahájení léčby. Demografické charakteristiky jsou prezentovány v tabulce 1. Průměrné trvání nemoci bylo >10 let a průměrný počet selhaných DMARDs byl 3. MTX byl současně podáván 47 % pacientům při zahájení biologické léčby i v průběhu studie. Aktivita nemoci při zahájení léčby byla vysoká: průměrné DAS28 bylo 6,4, průměrné CRP přibližně 29 mg/l a průměrný počet oteklých kloubů byl 11 a bolestivých kloubů 14 (tabulka 1). Jediným významným rozdílem v demografických nebo klinických charakteristikách při zahájení léčby byl vyšší průměrný věk při začátku nemoci (p = 0,006) a delší průměrné trvání nemoci (p = 0,02) ve skupině pacientů s etanerceptem.
Tab. 1. Demografické a klinické charakteristiky pacientů v ATTRA registru při zahájení anti-TNF terapie (N = 1945). 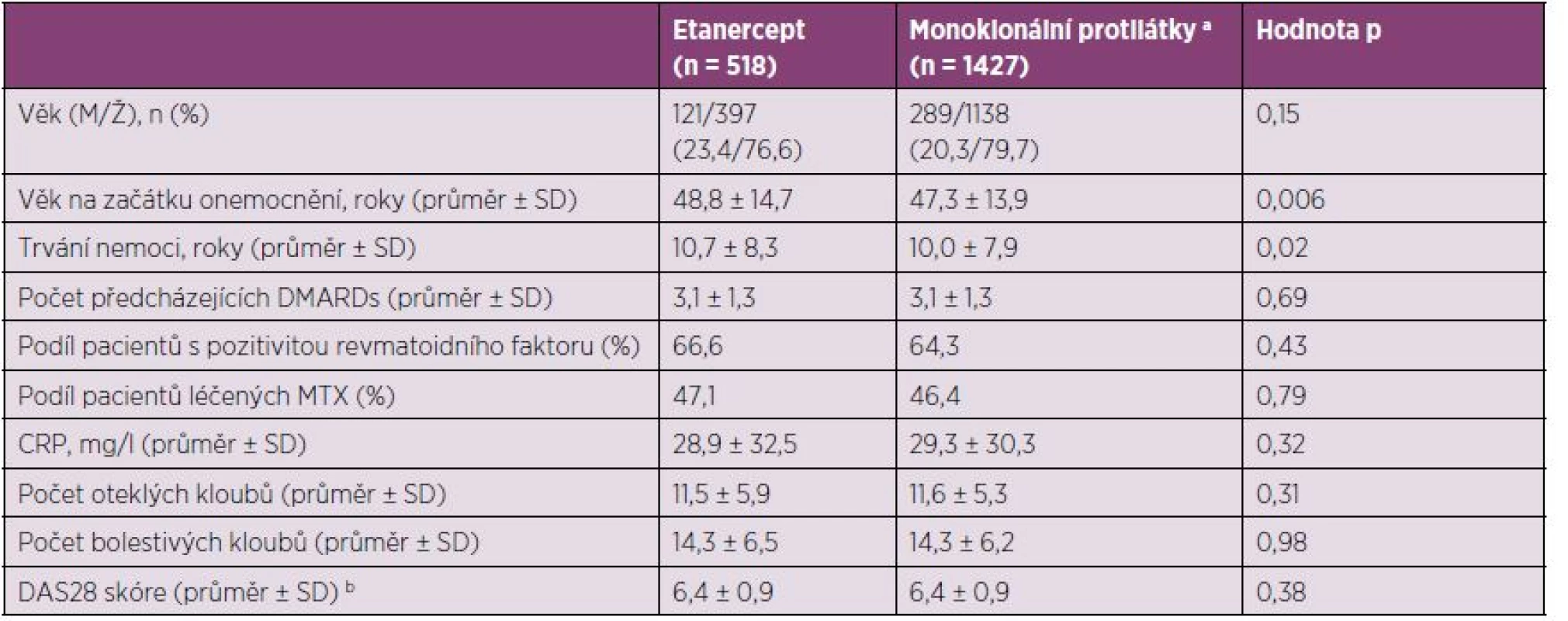
a Zahrnuje infliximab (n = 655), adalimumab (n = 747), a golimumab (n = 25). b Nezahrnuje 44 pacientů, kteří neměli dostupné skóre na začátku léčby. ATTRA – Anti-TNF Therapy of Rheumatoid Arthritis; CRP – C-reaktivní protein; DAS28 – skóre aktivity nemoci hodnotící 28 kloubů; DMARDs – chorobu modifikující léky; M – muž; MTX – methotrexát; SD – standardní odchylka; TNF – tumor necrosis factor; Ž – žena. V průběhu prvního roku léčby byla léčba přerušena anebo došlo k výměně biologického preparátu u 374 pacientů (19,2 %). Důvodem byla nedostatečná účinnost u 153 pacientů (40,9 %), nežádoucí účinky (NÚ) u 131 pacientů (35,0 %), ztráta účinnosti u 15 pacientů (4,0 %), stažení informovaného souhlasu s léčbou u 11 pacientů (2,9 %), dosažení remise u 7 pacientů (1,9 %), nespolupráce u 7 pacientů (1,9 %), úmrtí u 4 pacientů (1,1 %) a další důvody u 44 pacientů (11,8 %).
Účinnost
V obou skupinách významně pokleslo skóre DAS28 v průběhu studie (p < 0,001), ale pokles v 10. týdnu byl významně větší u etanerceptu než u monoklonálních protilátek (p < 0,001) a tento rozdíl mezi oběma skupinami zůstal statisticky významný po celou dobu studie (obr. 1). V 10. týdnu bylo u 34,8 % pacientů léčených etanerceptem dosaženo LDA a tento podíl pacientů nadále vzrůstal v průběhu studie na 51,6 % v 54. týdnu. Mezi pacienty léčenými monoklonálními protilátkami byl podíl dosažené LDA 28,1 % v 10. týdnu a 40,5 % v 54. týdnu. Podíl pacientů, u kterých bylo dosaženo LDA, byl významně vyšší u etanerceptu než u monoklonálních protilátek v každém sledovaném čase od 10. do 54. týdne (p ≤ 0,007) (obr. 2).
Obr. 1. Skóre DAS28 v průběhu sledování u pacientů léčených etanerceptem nebo monoklonálními protilátkami. Rozdíl mezi skupinami byl statisticky významný v průběhu celé studie (p < 0,001). <i>(osa y = skóre DAS, osa x = týden, šedá kostka = monoklonální protilátky)</i> 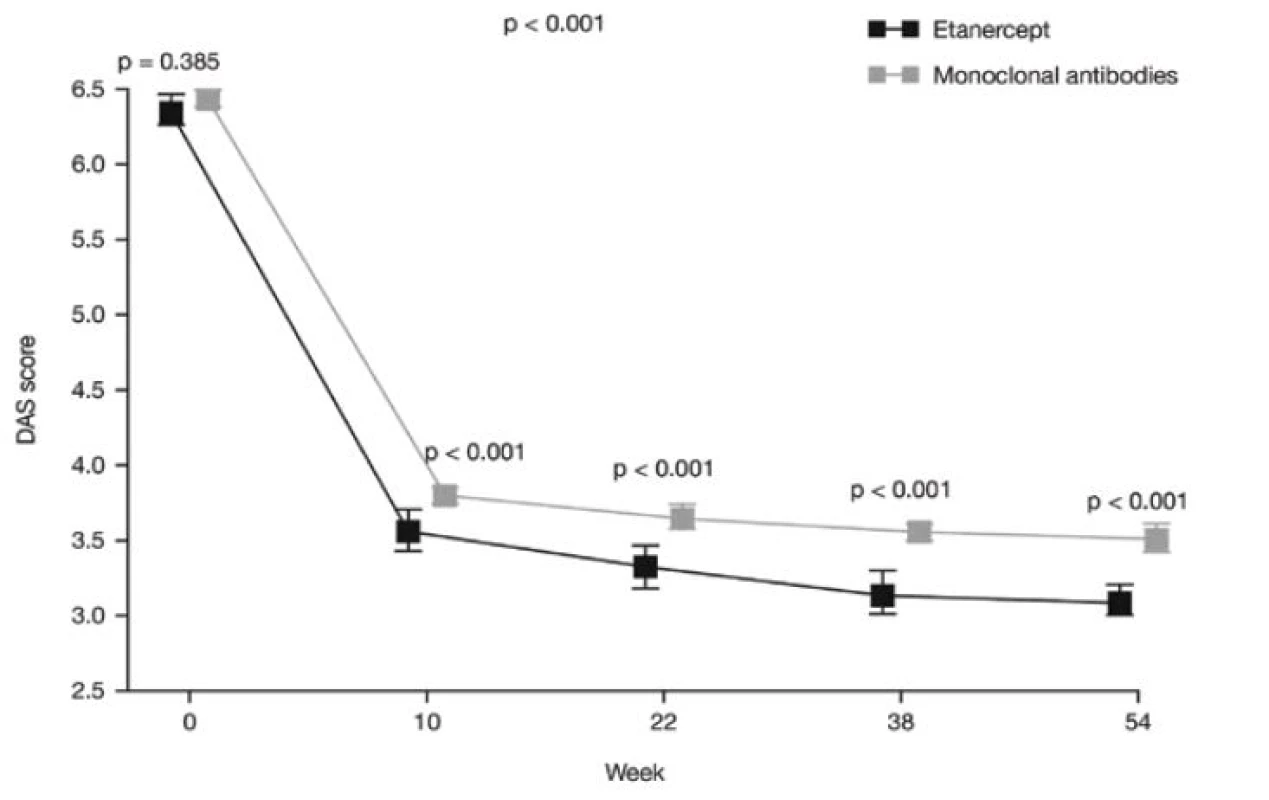
Obr. 2. Výskyt LDA (nízké aktivity nemoci) v průběhu sledování u pacientů léčených etanerceptem nebo monoklonálními protilátkami. <i>(osa y = podíl pacientů s LDA (%), osa x = týden, šedá kostka = monoklonální protilátky)</i> 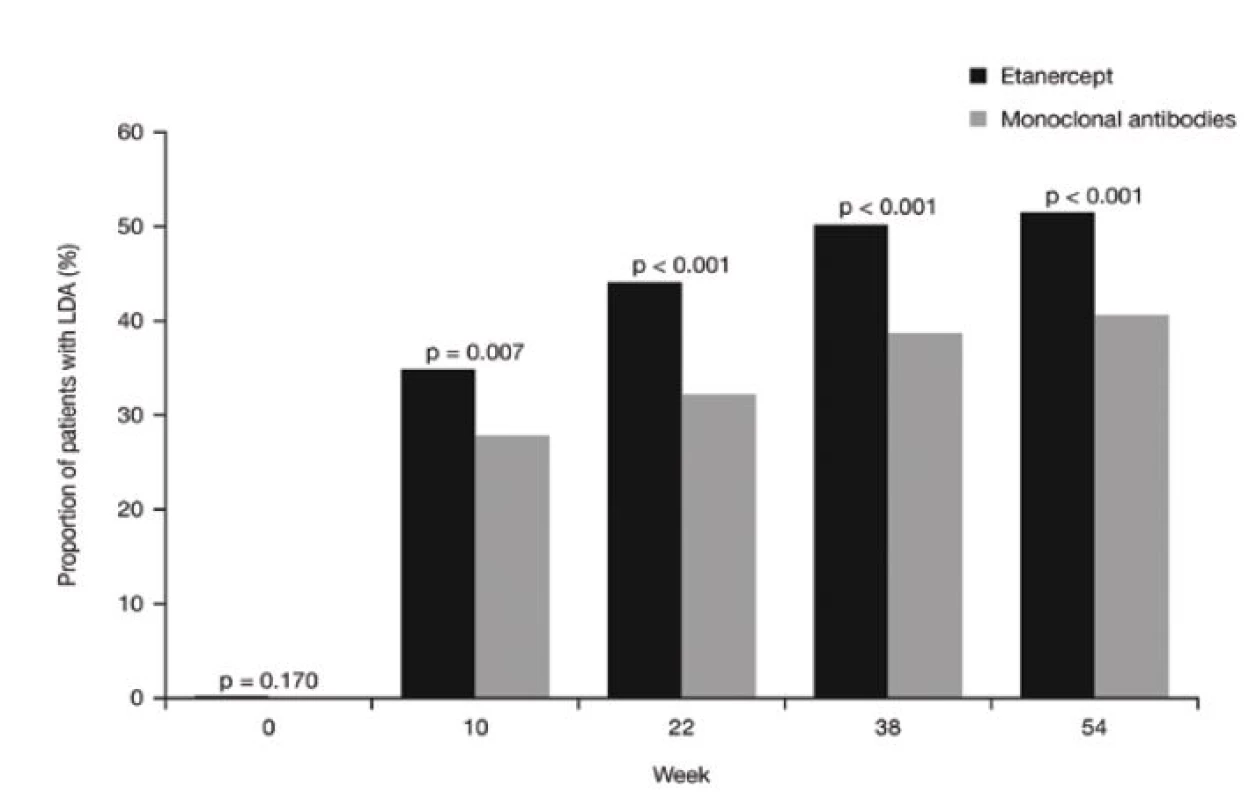
U 23,5 % pacientů léčených etanerceptem bylo dosaženo remise v 10. týdnu a tento podíl nadále vzrůstal v průběhu studie až na 35,5 % v 54. týdnu. U pacientů léčených monoklonálními protilátkami bylo dosaženo remise v 16,2 % v 10. týdnu a ve 24,1% v 54. týdnu. Dosažení remise bylo významně častější u etanerceptu než u monoklonálních protilátek v každém sledovaném čase (p < 0,001) (obr. 3).
Obr. 3. Výskyt remise (DAS28 < 2,6) v průběhu sledování u pacientů léčených etanerceptem nebo monoklonálními protilátkami. <i>(osa y = podíl pacientů s (DAS28 <2,6) (%), osa x = týden, šedá kostka = monoklonální protilátky)</i> 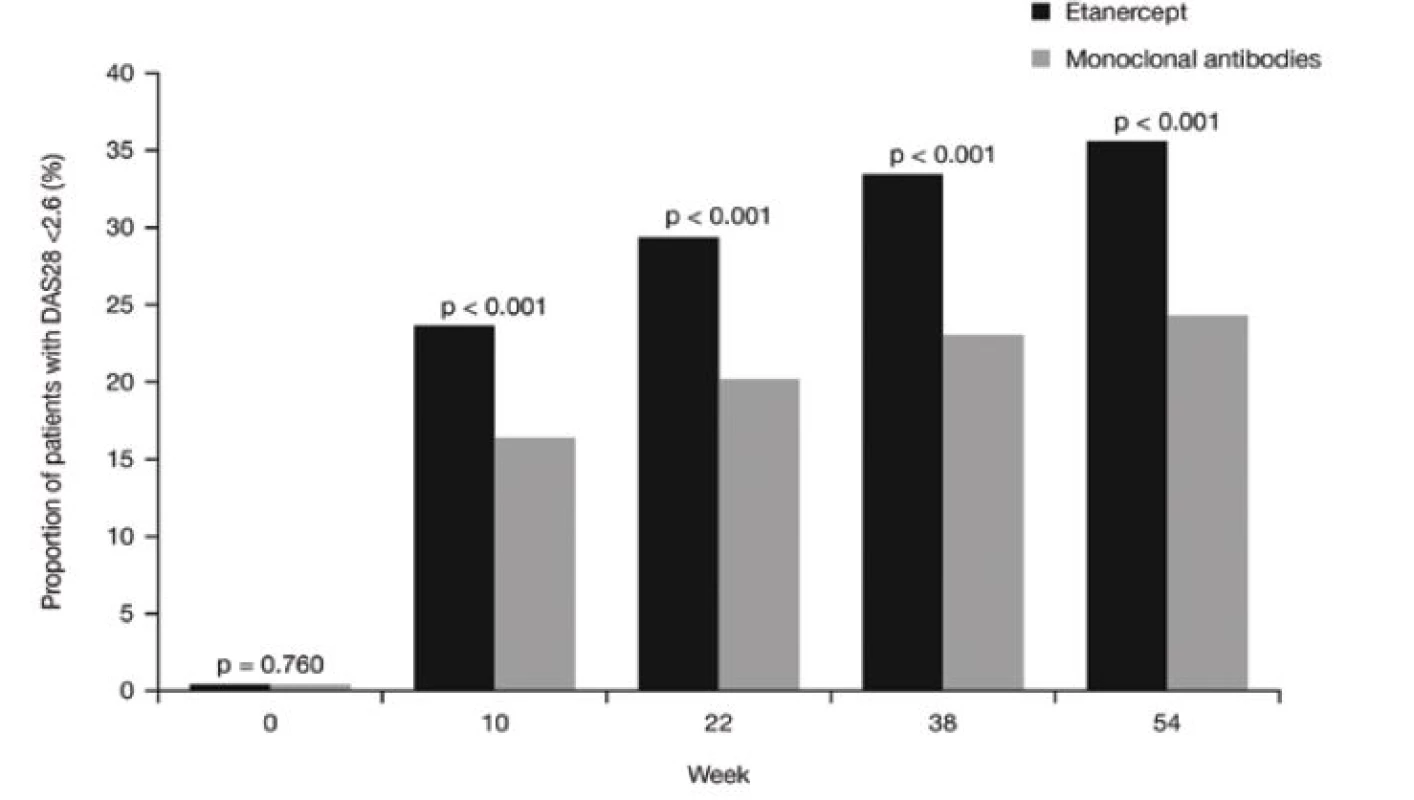
Dosažení dobré odpovědi na léčbu podle EULAR u etanerceptu bylo 34,1 % v 10. týdnu se vzestupem na 51,7 % v 54. týdnu, přičemž u monoklonálních protilátek to bylo 28 % v 10. týdnu a 40,2 % v 54. týdnu. Rozdíl mezi zmíněnými skupinami byl významný v 10. týdnu (p = 0,048) a ještě více se prohloubil v průběhu roku sledování (obr. 4).
Obr. 4. EULAR response (odpověď na léčbu) v průběhu sledování u pacientů léčených etanerceptem nebo monoklonálními protilátkami. Hodnota p je uvedena pro etanercept versus monoklonální protilátky v každém sledovaném čase. <i>(Nadpis grafů = Etanercept, Monoklonální protilátky, osa y = podíl pacientů (%), osa x = týden, černá kostka = dobrá, šedá kostka = střední, světle šedá kostka = žádná)</i> 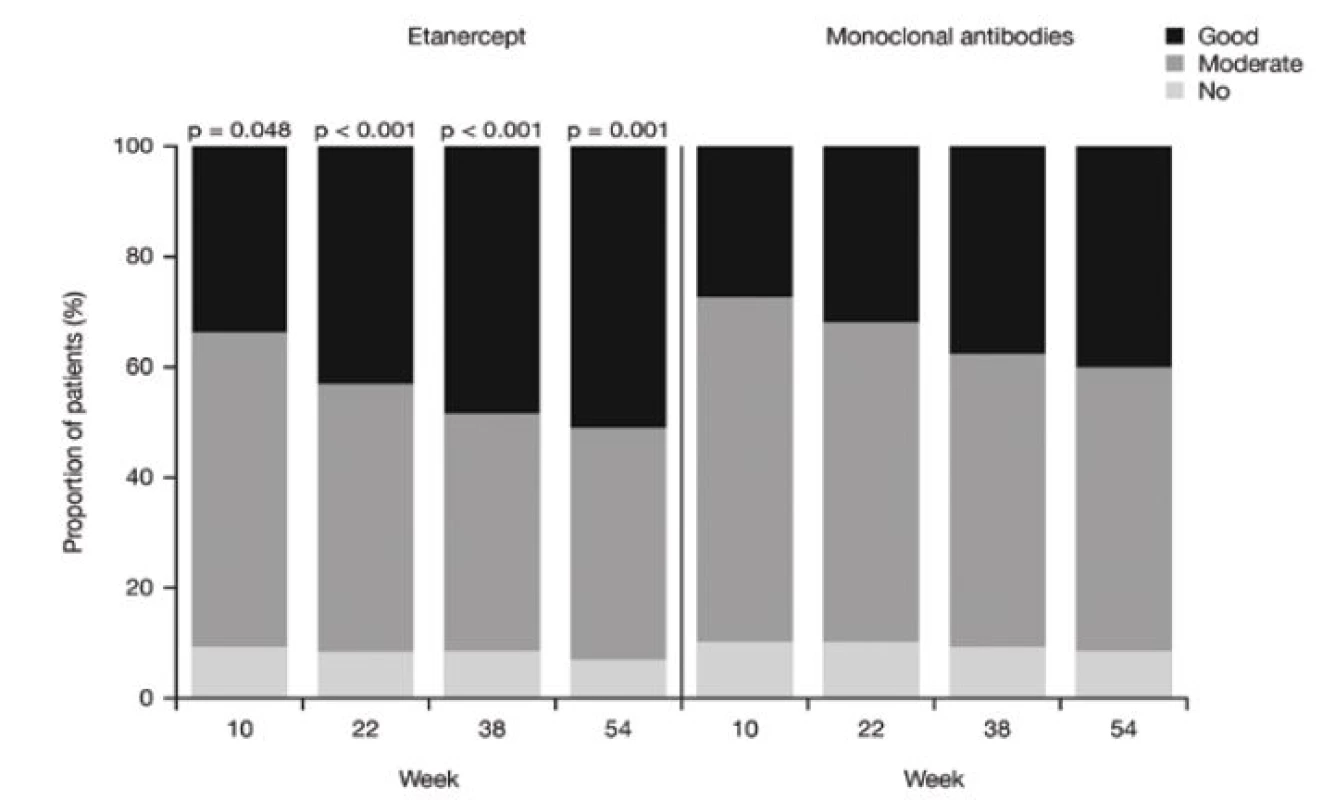
Průměrné koncentrace CRP významně poklesly z počátečních hodnot do 10. týdne u obou skupin (p < 0,001): z 28,9 mg/l na 10,7 mg/l u etanerceptu a z 29,3 mg/l na 11,9 mg/l u monoklonálních protilátek. Rozdíl mezi oběma skupinami v průběhu celé studie nebyl statisticky významný (p = 0,401). Hodnoty CRP pak mírně stouply od 10. do 54. týdne u skupiny s monoklonálními protilátkami, avšak u skupiny s etanerceptem zůstaly relativně stabilní (obr. 5). Rozdíly mezi skupinami byly významné ve 22. týdnu (p = 0,045), v 38. týdnu (p = 0,015) a v 54. týdnu (p = 0,012).
Obr. 5. Průměrné hodnoty CRP v průběhu sledování u pacientů léčených etanerceptem nebo monoklonálními protilátkami. Rozdíly mezi skupinami v průběhu sledování nebyly významné (p = 0,401). <i>(osa x = týden, šedá kostka = monoklonální protilátky)</i> 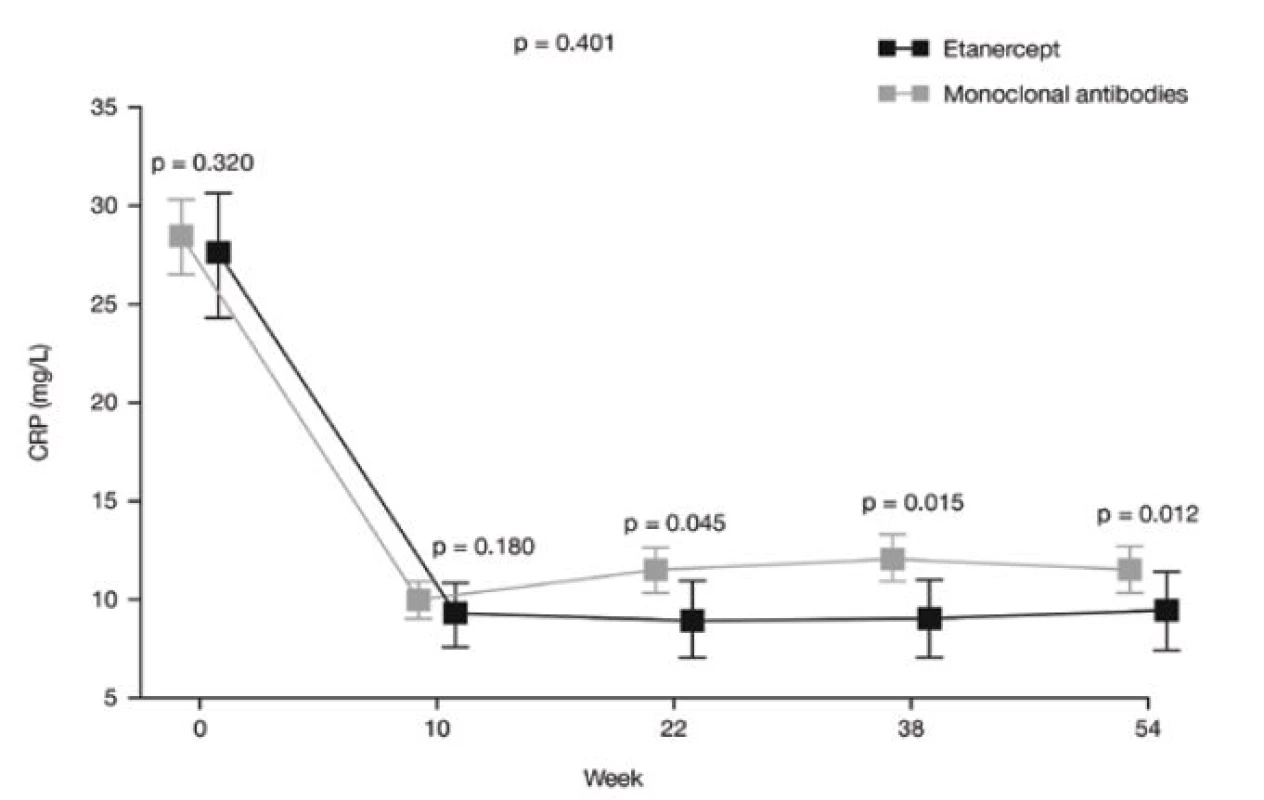
Prediktory odpovědi na léčbu
Významné prediktory odpovědi na léčbu byly stanoveny pomocí Coxova modelu proporčních rizik. Mezi základní parametry celé kohorty (N = 1065) patřil věk, trvání nemoci, počáteční skóre DAS28, pohlaví, pozitivita revmatoidního faktoru, počet selhaných DMARDs a současná terapie MTX. Mezi faktory, které významně předpověděly remisi, byla terapie etanerceptem, s HR (hazard ratio) 1,412 (95% confidence interval (CI): 1,167–1,708, p < 0,001); věk < 35 let (HR 2,086, 95% CI: 1,688–2,578, p < 0,001); trvání nemoci < 10 let (HR 1,438, 95% CI: 1,193–1,733, p < 0,001); počáteční DAS 28 < 4,5 (HR 2,65, 95% CI: 1,454–4,840, p = 0,001); a předcházející selhání > 3 DMARDs (HR 0,79, 95% CI: 0,647–0,963, p < 0,020). Mezi faktory, které neměly významnou prediktivní hodnotu, byl věk (p = 0,122), pozitivita revmatoidního faktoru (p = 0,102) a současná léčba MTX (p = 0,498).
Účinnost etanerceptu byla srovnána u pacientů s vysokou aktivitou nemoci (DAS28 > 5,1) a pacientů se střední aktivitou nemoci (DAS28 3,2–5,1) před zahájením terapie. Účinnost byla numericky, ale ne statisticky významně, vyšší u pacientů se střední aktivitou nemoci (tabulka 2). Remise (DAS 28 < 2,6) bylo dosaženo u 58,3 % pacientů se střední aktivitou nemoci a u 34,6 % pacientů s vysokou aktivitou nemoci. Příslušné podíly pacientů, u kterých bylo dosaženo LDA, byly 69,2 % a 50,9 %.
Tab. 2. Srovnání základních charakteristik a účinnosti etanerceptu po 1 roce léčby u pacientů s vysokou a střední aktivitou nemoci. 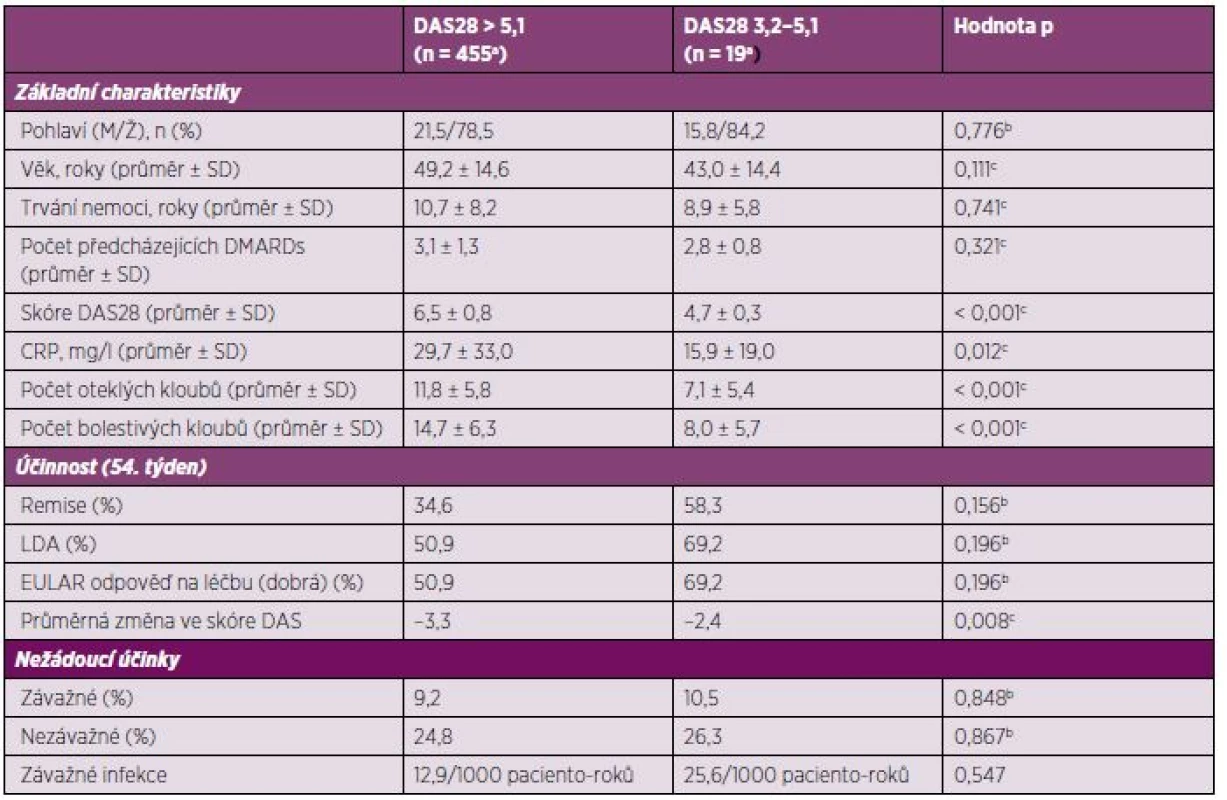
a Nezahrnuje 44 pacientů, u kterých nebylo počáteční skóre. b Fisherův test. c t-test. CRP – C-reaktivní protein; DAS28 – disease activity score 28, skóre aktivity nemoci hodnotící 28 kloubů; DMARDs – chorobu modifikující léky; EULAR – Evropská liga proti revmatismu; LDA – low disease activity, nízká aktivita nemoci; M – muž; SD – standardní odchylka; Ž – žena. Bezpečnost
V celkovém výskytu nežádoucích účinku nebo výskytu závažných nežádoucích účinků nebyly rozdíly mezi etanerceptem a monoklonálními protilátkami (tabulka 3). Nezávažné nežádoucí účinky se vyskytly u 26,4 % a 27,8 % pacientů, v uvedeném pořadí. Výskyt závažných infekcí u etanerceptu byl 12,9/1000 paciento-roků a 7,8/1000 paciento-roků u monoklonálních protilátek. Výskyt tuberkulózy byl 2,8/1000 a 1,2/1000 paciento-roků a výskyt nádorů byl 4,6/1000 a 1,8/1000 paciento-roků, v uvedeném pořadí.
Tab. 3. Nežádoucí účinky. 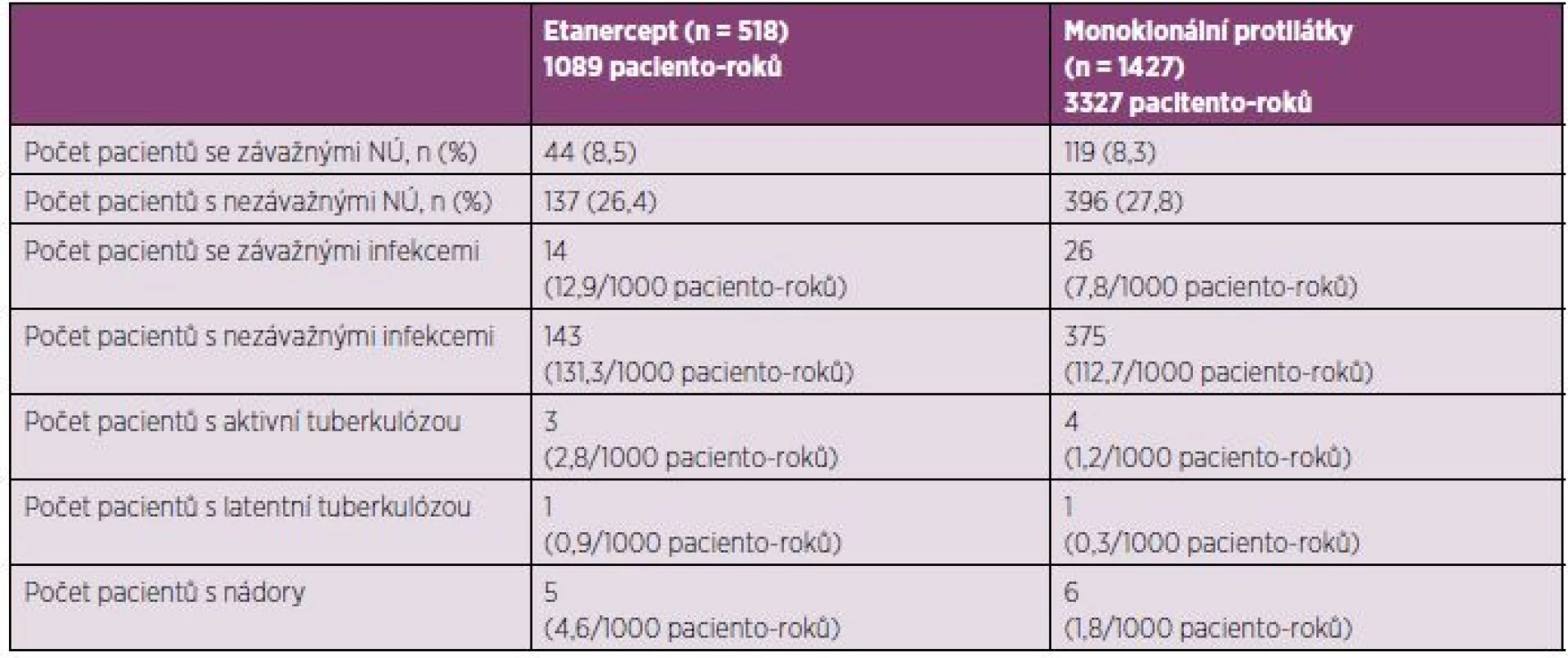
NÚ – nežádoucí účinky.Ve výskytu závažných nežádoucích účinků nebyl rozdíl mezi pacienty léčenými etanerceptem s vysokou nebo střední počáteční aktivitou nemoci (9,2 % vs 10,5 %); podobně nebyly nalezeny žádné rozdíly ve výskytu nezávažných nežádoucích účinků. Diskuse
Cílem léčby RA by měla být remise, zlepšení nebo zachování funkce a rentgenová non-progrese. U pacientů s perzistující RA by minimálním cílem terapie mělo být dosažení LDA (8). Nicméně výsledky této observační studie demonstrují, že jen přibližně u jedné třetiny pacientů bylo dosaženo remise po jednom roce léčby a u méně než poloviny bylo dosaženo LDA.
Toto může být spojené s definicí remise. V běžné klinické praxi v Evropě a České republice je remise definována jako DAS28 < 2,6 a LDA jako DAS28 < 3,2 (9). Nicméně jiné parametry, jako SDAI (Simplified Disease Activity Index), definují remisi jako skóre ≤ 3,2 (10). V současnosti má jen málo lékařů klinické zkušenosti s novou definicí remise podle ACR/EULAR (11). Naše výsledky demonstrují, že po jednom roce léčby etanerceptem bylo dosaženo remise u jedné třetiny pacientů. Tyto výsledky jsou v souladu se zkušenostmi s jinými anti-TNF preparáty z jiných registrů a odrážejí závažnost a perzistenci RA u těchto populací. Kdybychom stanovili cíl naší léčby jako DAS28 < 3,2 (LDA), přibližně u 50 % pacientů na etanerceptu by se dosáhlo primárního cíle léčby. Podíl pacientů, u kterých bylo dosaženo remise v jakémkoliv čase sledování, byl přibližně o 10 % vyšší ve skupině s etanerceptem než ve skupině s monoklonálními protilátkami.
Klinická praxe v registru ATTRA zjevně odráží fakt, že léčba byla podána dřív, než byl zaveden koncept cílené léčby („treatment-to-target“) (tj. bez jasného protokolu vyžadujícího úpravu léčby každé 3 měsíce, jestli nebylo dosaženo cíle – remise nebo LDA) (8). V současnosti navrhují doporučené postupy přísnou kontrolu, u které je aktivita nemoci měřena kompozitními indikátory na pravidelné bázi a terapie je jim adekvátně přizpůsobena. Tato strategie vede k lepším výsledkům a pomalejší rentgenové progresi, co bylo prokázáno studií TICORA (Tight Control for Rheumatoid Arthritis) (12). Meta-analýzy také prokázaly větší účinnost biologických preparátů ve studiích s přísnou kontrolou nezávisle na tom, jestli šlo o klinické studie, registry nebo observační studie (13).
Klíčovým cílem výzkumu RA je identifikovat faktory, které předpovídají odpověď na léčbu nebo remisi. Trvání nemoci patří mezi nejdůležitější faktory: ví se, že krátké trvání nemoci zvyšuje pravděpodobnost odpovědi na biologickou léčbu; z toho plyne, že by se tento typ léčby měl zahájit časněji v průběhu onemocnění. Ve většině registrů se zkracuje interval od začátku nemoci po první anti-TNF léčbu. Například první analýzy v České republice před 10 lety demonstrovaly průměrnou dobu nemoci 12 let před zahájením anti-TNF terapie, zatímco v současnosti se trvání nemoci přibližuje hodnotě 10 let. V registrech ze západní Evropy je trvání nemoci průměrně 4–5 let.
Dalším pozitivním prediktivním faktorem v naší studii bylo počáteční skóre DAS28 < 4,5. Ve skutečnosti odpovídali pacienti se střední aktivitou nemoci (DAS28 3,2–5,1) lépe na etanercept než pacienti s vyšším DAS28. Tyto výsledky mají podporu i v četných studiích, které prokázaly srovnatelnou nebo větší účinnost anti-TNF terapie u pacientů se střední aktivitou nemoci než u pacientů se závažnějším onemocněním (14). Tato skutečnost dále podporuje doporučení snížit hranici DAS28 stanovenou pro zahájení biologické terapie z dosavadních 5,1 na 3,2–3,9. Je známo, že u pacientů se střední aktivitou nemoci je vysoké riziko rentgenové progrese a zhoršování funkce bez adekvátní léčby (15). Dalším prediktorem odpovědi na léčbu v naší studii byl nižší věk v době zahájení léčby, co je v souladu s výsledky studie DANBIO (16).
Dosažení terapeutického cíle u 50 % pacientů po jednom roce léčby v běžné klinické praxi nemůže být považováno za úspěšný výsledek a je nutné podporovat princip cílené léčby („treatment-to-target“), aby se dosáhlo maximálního prospěchu biologické léčby.
V této naší studii byla hlavní pozornost kladena na účinnost, ale samozřejmě byla také sledována bezpečnost. Při hodnocení bezpečnosti léčby nebyly zjištěny rozdíly mezi monoklonálními protilátkami a etanerceptem u nezávažných i závažných nežádoucích účinků. Výskyt nádorů a tuberkulózy byl v této skupině velmi nízký a z našich výsledků nelze činit žádné závěry. Numericky vyšší výskyt u etanerceptu by bylo možné interpretovat jako určité „chaneling bias“ s tím, že rizikovější pacienti byli zaváděni na tuto léčbu.
Závěr
V českém národním registru biologické terapie RA nejsou dosud široce uplatňovány principy cílené léčby („treatment-to-target“) a po jednom roce terapie bylo dosaženo LDA jen u 50 % pacientů. Mezi faktory spojené s remisí patřil věk < 35 let na začátku sledování, trvání nemoci < 10 let, počáteční skóre DAS28 < 4,5 a použití etanerceptu vs monoklonálních protilátek. Etanercept byl podle několika parametrů účinnější než monoklonální protilátky, i přes vyšší věk při stanovení diagnózy a delší trvání nemoci ve skupině s etanerceptem. Ant-TNF terapie byla účinnější u pacientů se střední aktivitou nemoci (DAS28 3,2–5,1) než u pacientů s vysokou aktivitou nemoci (DAS28 > 5,1). Interpretace tohoto výsledku však musí být velmi opatrná, protože se jedná o retrospektivní, observační studii bez randomizace, takže skupiny nemusely být identické. Další limitací této studie je, že nebylo možné provést analýzu konkrétních monoklonálních protilátek, protože v původním zadání bylo analyzovat je dohromady proti solubilnímu receptoru.
Výhled do budoucnosti
Účinnost biologické léčby vyžaduje další zlepšení v reálné klinické praxi. Toho lze dosáhnout používáním nových biologických preparátů a/nebo optimalizací našich léčebných strategií se současnými biologickými léky. Mezi nejdůležitější strategie patří přísná kontrola, principy cílené léčby („treat-to-target“) a výběr pacientů, u kterých je nejvyšší pravděpodobnost odpovědi na biologickou terapii. Lepší odpovědi bylo rovněž dosaženo u pacientů se střední aktivitou nemoci. Zdá se, že běžně používaná hranice skóre DAS28 > 5,1 pro zahájení biologické léčby je příliš vysoká.
Poděkování
Statistické vyhodnocení a logistika této studie byla podpořena Organizací Ministerstva zdravotnictví České republiky pro koncepční rozvoj výzkumu, projekt č. 00023728 (Revmatologický ústav).
Registr ATTRA, úplně nezávislá akademická aktivita, je vlastnictvím České revmatologické společnosti a je současně sponzorována několika farmaceutickými společnostmi. Editorskou pomoc s přípravou manuskriptu poskytla Susanne Gilbert z ACUMED® (New York, NY, USA) s podporou společnosti Pfizer.
Finanční prohlášení a konflikt zájmů
Prof. MUDr. Karel Pavelka, DrSc., a RNDr. Ing. Karel Chroust, Ph.D., jsou konzultanti a/nebo přednášející pro společností Pfizer, Abbott, Bristol-Myers Squibb, Merck Sharp Dohme, a UCB.
Doc. MUDr. Petr Němec, Ph.D., prohlašuje, že nemá žádný konflikt zájmů.
Podpořeno projektem (Ministerstva zdravotnictví) koncepčního rozvoje výzkumné organizace 023728 (Revmatologický ústav)
Adresa pro korespondenci:
Prof. MUDr. Karel Pavelka, DrSc.
Revmatologický ústav, Na Slupi 4, 128 50 Praha 2
Tel: +420 234 075 244
Fax: +420 224 914 451
E-mail: pavelka@revma.cz
Zdroje
1. Maini R, St Clair EW, Breedveld F et al. Infliximab (chimeric anti-tumour necrosis factor alpha monoclonal antibody) versus placebo in rheumatoid arthritis patients receiving concomitant methotrexate: a randomised phase III trial. ATTRACT Study Group. Lancet 1999; 54 : 1932–4.
2. van der Heijde D, Klareskog L, Rodriguez-Valverde V et al. on behalf of the TEMPO Study Investigators. Comparison of etanercept and methotrexate, alone and combined, in the treatment of rheumatoid arthritis: two-year clinical and radiographic results from the TEMPO study, a double-blind, randomized trial. Arthritis Rheum 2006; 54 : 1063–74.
3. Du Pan SM, Dehler S, Ciurea A, Ziswiler HR, Gabay C, Finckh A. on behalf of the Swiss Clinical Quality Management Physicians. Comparison of drug retention rates and causes of drug discontinuation between anti-tumour necrosis factor agents in rheumatoid arthritis. Arthritis Rheum 2009; 61 : 560–8.
4. Hetland ML, Christensen IT, Tarp U et al. on behalf of all Departments of Rheumatology in Denmark. Direct comparison of treatment responses, remission rates, and drug adherence in patients with rheumatoid arthritis treated with adalimumab, etanercept, or infliximab: results from eight years of surveillance of clinical practice in the nationwide Danish DANBIO registry. Arthritis Rheum 2010; 62 : 22–32.
5. Pavelka K, Vencovský J. Doporučení České revmatologické společnosti pro léčbu revmatoidní artritidy. Česká Revmatol 2010; 18 : 182–191.
6. Vencovský J. a výbor České revmatologické společnosti. Bezpečnost biologické léčby – Doporučení České revmatologické společnosti. Česká Revmatol 2009; 3 : 146–160.
7. Felson DT, Smolen JS, Wells G et al. On behalf of the American College of Rheumatology and the European League Against Rheumatism. American College of Rheumatology/European League Against Rheumatism provisional definition of remission in rheumatoid arthritis for clinical trials. Arthritis Rheum 2011; 63 : 573–86.
8. Smolen JS, Aletaha D, Bijlsma JW et al. on behalf of the T2T Expert Committee. Treating rheumatoid arthritis to target: recommendations of an international task force. Ann Rheum Dis 2010; 69 : 631–7.
9. Prevoo ML, van’t Hof MA, Kuper HH, van Leeuwen MA, van de Putte LB, van Riel PL. Modified disease activity scores that include twenty-eight-joint counts. Development and validation in a prospective longitudinal study of patients with rheumatoid arthritis. Arthritis Rheum 1995; 38 : 44–8.
10. Smolen JS, Breedveld FC, Schiff MH et al. A simplified disease activity index for rheumatoid arthritis for use in clinical practice. Rheumatology (Oxford) 2003; 42 : 244–57.
11. Felson DT, Smolen JS, Wells G et al. American College of Rheumatology/European League against Rheumatism provisional definition of remission in rheumatoid arthritis for clinical trials. Ann Rheum Dis 2011; 70 : 404–13.
12. Grigor C, Capell H, Stirling A et al. Effect of a treatment strategy of tight control for rheumatoid arthritis (the TICORA study): a single-blind randomised controlled trial. Lancet 2004; 364 : 263–9.
13. Goekoop-Ruiterman YP, de Vries-Bouwstra JK, Kerstens PJ et al. DAS-driven therapy versus routine care in patients with recent-onset active rheumatoid arthritis. Ann Rheum Dis 2010; 69 : 65–9.
14. Deighton C, Hyrich K, Ding T et al. on behalf of the BSR Clinical Affairs Committee & Standards, Audit and Guidelines Working Group and the BHPR. BSR and BHPR rheumatoid arthritis guidelines on eligibility criteria for the first biological therapy. Rheumatology (Oxford) 2010; 49 : 1197–9.
15. Conaghan PG, Hensor EM, Keenen AM, Morgan AW, Emery P. on behalf of the YEAR Consortium. Persistently moderate DAS-28 is not benign: loss of function occurs in early RA despite step-up DMARD therapy. Rheumatology 2010; 49 : 1894–99.
16. Dahl LL, Geborek P, Englund M et al. TNF-inhibitors in established rheumatoid arthritis: The effect of age on treatment response and predictors of response. Presented at the 2009 ACR/ARHP Annual Scientific Meeting, Philadelphia, PA, USA, October 16–21, 2009. Arthritis Rheum 2009;60 Suppl 10 : 994; DOI: 10.1002/art.26071
Štítky
Dermatologie Dětská revmatologie Revmatologie
Článek vyšel v časopiseČeská revmatologie
Nejčtenější tento týden
2014 Číslo 4- Daivobet gel – lékový profil
- Komplementární mechanismus účinku analog vitaminu D a topických kortikosteroidů v léčbě ložiskové psoriázy
- Takrolimus v terapii atopické dermatitidy a analýza jeho nákladové efektivity ve srovnání s kortikosteroidní léčbou
- V patogenezi psoriázy jde o víc než jen o IL-17A
- Selektivní inhibitor IL-23 risankizumab: nejnovější posila v biologické léčbě psoriázy
Nejčtenější v tomto čísle- Belimumab v terapii systémového lupus erythematodes a v dalších indikacích
- 58. výroční sjezd českých a slovenských revmatologů
- Faktory ovlivňující účinnost anti-TNF terapie v klinické praxi: zkušenosti z národního registru ATTRA
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



