-
Články
Top novinky
Reklama- Vzdělávání
- Časopisy
Top články
- Témata
Top novinky
Reklama- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Top novinky
ReklamaProtilátky po prodělaném onemocnění COVID-19 poskytují dostatečnou a dlouhodobou ochranu před reinfekcí
Antibodies from previous infection bring sufficient and long-term protection against COVID-19
One of the basic manifestations of an adaptive anti-infective immunity is the production of specific antibodies. The presence of antibodies can be detected in serum and serves as one of the diagnostic tools used to confirm past infection. Very often it also serves as a confirmation that the body has acquired immunity to the disease. The appearance of COVID-19 has cast a shadow of doubt on these textbook examples of antibody behavior. Information that repeatedly questions antibody measurement and its significance has been circulating among professionals and the general public. The aim of our article is to summarize the current knowledge on the immunity acquired following SARS-CoV-2 infection and to present the results of antibody testing from four Czech laboratories which have been measuring these antibodies for over one year. Our data suggest that commonly available diagnostic methods reliably predict the results of a virus neutralization test, which is the gold standard of immunity detection. By acknowledging those with naturally acquired anti-infective immunity, in addition to vaccinated individuals, we will significantly increase the perceived level of collective immunity.
Keywords:
immunoglobulin G – vaccination – Antibodies – SARS-CoV-2 – COVID-19 – coronavirus – reinfection – neutralizing
Autoři: Zuzana Krátká 1,2; Václav Fejt 1,3; Radek Kučera 4,5; Tomáš Fürst 1,6; Hana Zelená 1,7
Působiště autorů: SMIS – Sdružení mikrobiologů, imunologů a statistiků 1; Imunologická laboratoř GENNET, s. r. o., Praha 2; Oddělení společných laboratoří, Nemocnice Havlíčkův Brod 3; Oddělení imunochemické diagnostiky, Fakultní nemocnice Plzeň 4; Ústav farmakologie a toxikologie LF UK v Plzni 5; Katedra matematické analýzy a aplikací matematiky PřF UP v Olomouci 6; Centrum klinických laboratoří, Zdravotní ústav v Ostravě 7
Vyšlo v časopise: Čas. Lék. čes. 2021; 160: 167-175
Kategorie: Původní práce
Souhrn
Jedním ze základních projevů adaptivní antiinfekční imunity je tvorba specifických protilátek. Jejich přítomnost můžeme detekovat v séru. Pozitivita slouží jako jedno z diagnostických kritérií potvrzujících prodělání virové nemoci, ale často i k potvrzení imunity vůči danému onemocnění. S příchodem onemocnění COVID-19 jako by tato učebnicová teze přestala platit. Mezi odbornou i laickou veřejností se šíří informace, které stanovení protilátek a význam jejich přítomnosti opakovaně zpochybňují. Proto nyní shrnujeme aktuální informace o imunitě po prodělané infekci virem SARS-CoV-2 a předkládáme výsledky vyšetřování protilátek ze čtyř českých laboratoří, které se jejich stanovení věnují déle než rok. Z našich dat vyplývá, že běžně dostupné diagnostické metody spolehlivě predikují výsledky virus neutralizačního testu, který je zlatým standardem stanovení imunity. Akceptací přirozeně získané antiinfekční imunity výrazně zvýšíme počet osob, které se podílejí společně s osobami očkovanými na kolektivní imunitě.
Klíčová slova:
imunoglobulin G – vakcinace – protilátky – SARS-CoV-2 – COVID-19 – koronavirus – reinfekce – neutralizační
ÚVOD
Po infekci SARS-CoV-2 nebo po očkování proti němu se vyvíjí specifická imunitní odpověď, která by měla potlačit primární infekci a nastavit dlouhodobou ochranu proti nákaze tímto koronavirem. Primárně se organismus brání vstupu infekce přirozenou imunitou (produkcí interferonů na sliznicích, aktivací komplementu apod.). Po aktivaci specifické imunity dochází u většiny osob k tvorbě protilátek a aktivaci T-buněčné imunity. Protilátky lze detekovat u většiny osob, jež onemocněly COVID-19, ale existují jedinci, kteří prokazatelně infekci SARS-CoV-2 prodělali (měli klinické příznaky a pozitivní výsledek PCR nebo antigenních testů z výtěru z nosohltanu), ale protilátky v séru nemají. Došlo však u nich k aktivaci T-buněčné imunity, kterou je možné prokázat různými typy testů. Jimi se po krátkodobé kultivaci krve nebo izolovaných lymfocytů s koronavirovými antigeny buď sleduje produkce cytokinů (IFN gama), nebo stanovuje počet aktivovaných T lymfocytů (cytometricky či metodou ELISPOT). Specifická humorální a buněčná imunitní reakce vytvořená v reakci na první infekci se postupně přetváří v dlouhodobou imunitu. Díky ní se jedinec umí lépe bránit opakovanému setkání s patogenem.
Dlouhodobou imunitní odpověď zajišťují paměťové B lymfocyty a paměťové T lymfocyty. Paměťové B buňky a plazmocyty se podílejí na produkci protilátek. Zatímco paměťové Th2 buňky podporují tvorbu protilátek, cytotoxické T lymfocyty (Tc) svým účinkem zabíjejí infikované buňky. V laboratoři umíme stanovit množství cirkulujících protilátek anebo zjistit přítomnost specifických T buněk (případně stanovit produkci jimi tvořených cytokinů), ale diskutuje se o správném nastavení hranice „protektivní imunity“. ECDC za spolehlivý důkaz protektivity považuje výskyt tzv. neutralizačních protilátek proti SARS-CoV-2 (1). Neutralizační protilátky představují nejlepší indikátor ochrany proti reinfekci u osob po prodělaném onemocnění a před infekcí u osob vakcinovaných (1). Neutralizační protilátky se stanovují virus neutralizačním testem (VNT), tedy funkčním in vitro testem, při kterém se zjišťuje, zda dané sérum pacienta, resp. protilátky vyskytující se v séru ochrání buněčnou kulturu před virovou infekcí. Pokud jsou neutralizační protilátky přítomny, buňky zůstanou živé, protože virus se nenamnoží. Nejsou-li přítomné, virus buňky napadne, namnoží se v nich a buňky odumřou (2).
Podrobné informace o tom, jak protilátky vznikají a jaká je jejich kinetika, poskytuje systematický přehled 150 studií popisujících protilátkovou odpověď vůči SARS-CoV-2 (3). V průběhu infekce se (na rozdíl od očkování) netvoří jen jeden typ protilátek (monoklonální protilátky), ale hned několik typů, které cílí na různé virové antigeny (polyklonální protilátky). Nejdůležitější jsou protilátky proti spike proteinu (proteinu S, resp. podjednotce S1), doméně vázající receptor (RBD – receptor-binding domain) a nukleokapsidovému proteinu (proteinu N). Spike protein je zodpovědný za vazbu na receptor pro angiotenzin konvertující enzym 2 (ACE2), což je cesta, jíž virus vstupuje do buňky (4). Protein N existuje intracelulárně a je důležitý v transkripci a replikaci virové DNA, a proto je vysoce exprimován v průběhu infekce. Nejspolehlivější ochranný efekt mají protilátky proti antigenu S1, případně proti jeho RBD. V průběhu virové infekce se tvoří různé izotypy protilátek (IgA, IgM, IgG) a všechny se mohou na výsledku VNT podílet. Výsledek VNT nejlépe pozitivně koreluje s přítomností protilátek IgG proti S1 nebo RBD antigenům (3).
Jako první protilátky vznikají při virové infekci IgM (3). Jejich koncentrace je nejvyšší v 2. až 5. týdnu od prvních příznaků onemocnění a potom dalších 3 až 5 týdnů klesá. K produkci IgG dochází přibližně od 10. dne a maximum IgG je detekováno mezi 3. a 7. týdnem po nástupu příznaků při první infekci. IgG jsou v séru přítomny dlouhodobě. Hladina IgA dosahuje maximálních hodnot mezi 16. až 22. dnem od nástupu příznaků (při první infekci) a také přetrvává dlouhodobě. Neutralizační protilátky jsou detekovatelné 7. až 15. den od začátku onemocnění a jejich koncentrace se postupně zvyšuje, přičemž maxima dosáhne 14. až 22. den onemocnění. Hladina neutralizačních protilátek později mírně klesá, ale na určitých hodnotách specifických pro daného pacienta se udržuje po dlouhou dobu. Protilátky nevykazují významnou zkříženou reaktivitu a jsou specifické. Protektivitu protilátek proti reinfekci prokázalo také několik studií provedených na souborech laboratorních zvířat.
Kromě protilátek se aktivuje také T-buněčná imunita. K maximální aktivaci T-buněčné imunity dochází přibližně 10 až 20 dnů po nástupu příznaků (1). Aktivují se jak Tc lymfocyty, tak Th lymfocyty. Systematický přehled 61 studií naznačil, že zvyšující se závažnost onemocnění je spojena s robustnější T-buněčnou odpovědí (5), přičemž u hospitalizovaných pacientů s vážnějším průběhem onemocnění se v akutní fázi vyskytuje méně Tc lymfocytů než u osob s mírnějším průběhem onemocnění. Paměťové Th i Tc buňky byly detekovány i po 8 měsících od infekce (6). Pro ověření specifické imunity po infekci koronavirem použili Dan et al. u pacientů po COVID-19 pětici základních testů, které zahrnovaly stanovení protilátek IgG a IgA proti proteinu S, detekci paměťových B lymfocytů, paměťových Tc a Th lymfocytů (6). Prakticky u všech pacientů se alespoň jedním vyšetřením specifická imunitní odpověď po 8 měsících potvrdila, ale mezi pacienty byly zjištěny rozdílné kombinace pozitivních nálezů.
Technicky a pro rutinní praxi nejjednodušším průkazem imunity stále zůstává stanovení protilátek, které se stalo běžně dostupným testem prováděným v mnoha imunologických a mikrobiologických laboratořích. Dokument Ministerstva zdravotnictví ČR nazvaný „Strategie testování onemocnění COVID-19 pro sezónu respiračních onemocnění 2020/2021“ popisuje, za jakých situací je vhodné protilátky stanovovat a kdy testy mohou být hrazeny ze zdravotního pojištění (7). Mezi tyto situace patří serologická a epidemiologická diagnostika u dárců rekonvalescentní plazmy (indikuje infektolog nebo hematolog), dále stanovení vnímavosti a ověření stavu imunity u pacienta (indikuje imunolog nebo infektolog, příp. epidemiolog KHS v ohnisku nákazy) a také diferenciální diagnostika kovidové nebo postkovidové pneumonie (indikují lékař akutní lůžkové péče a vybraných odborností – anesteziolog, internista, infektolog, pneumolog). Vyšetření je vykazováno výkonem 82097 a je hrazeno max. 6× měsíčně, nejvýše 3× za den; společně s výkonem je vykazována diagnóza U07.1 nebo U69.75 (8). Žádné další navrhované indikace zatím přijaty nebyly, i když ČSAKI a Společnost pro lékařskou mikrobiologii ČLS JEP připravily nový návrh indikací již v dubnu 2021. Vyšetření protilátek proti koronaviru z jiných důvodů si nadále hradí pacient sám. Pro stanovení protilátek není potřeba doporučení od lékaře. Mají o něj zájem zejména lidé po nemoci nebo po karanténě.
Virus neutralizační test se provádí jen v několika virologických laboratořích. Je určen zejména pro potvrzení hladiny neutralizačních protilátek u potenciálních dárců rekonvalescentní plasmy, případně pro potvrzení přítomnosti neutralizačních protilátek u imunokompromitovaných pacientů.
CÍL STUDIE
Účelem provedení studie bylo zjistit, jakou koncentraci IgG protilátek můžeme považovat za ochrannou, jak spolehlivým prediktorem přítomnosti ochranných protilátek je hladina IgG stanovená běžnými testy (ELISA, CLIA) a jak dlouho protilátky v této ochranné hladině přetrvávají.
METODIKA
Použili jsme výsledky rutinních vyšetření hladiny protilátek a/nebo VNT, získaných na základě informovaných souhlasů z informačních systémů čtyř laboratoří (virologické laboratoře Zdravotního ústavu v Ostravě, imunologické laboratoře FN Plzeň, imunologické laboratoře GENNET v Praze a laboratoře Nemocnice Havlíčkův Brod).
Stanovení virus neutralizačních protilátek
Přítomnost neutralizačních protilátek byla zjišťována laboratoří virologického oddělení Zdravotního ústavu v Ostravě, které má tuto metodu akreditovanou (9). Na 96jamkové sterilní mikrotitrační destičce se společně inkubuje suspenze živého viru SARS-CoV-2 s ředěným sérem pacienta (v ředění od 1 : 10 do 1 : 2560). Jsou-li v séru přítomné neutralizační protilátky proti SARS-CoV-2, navážou se na specifické epitopy proteinu S1 virové částice, čímž zabrání jeho vazbě na buněčné receptory a vstupu viru do buňky. Po inkubaci virů s protilátkami se přidá suspenze buněk opičích ledvin a vzorky se 3 dny kultivují. Po ukončení inkubace se do všech jamek přidá neutrální červeň, která obarví živé buňky, zatímco usmrcené buňky zůstanou neobarvené. To umožní makroskopické odečtení reakce – jsou-li buňky v jamce obarvené, tedy živé, pak byly v séru přítomné neutralizační protilátky, které ochránily buňky před virovou infekcí. Výsledek se uvádí jako neutralizační titr, který je převrácenou hodnotou nejvyššího ředění séra, jež ochrání před infekcí minimálně 50 % buněk v příslušné jamce. Titr 10 je považován za hraniční, titr 20 a vyšší za ochranný (10), titr ≥ 80 znamená vysokou koncentraci ochranných protilátek a možnost použít plazmu jako rekonvalescentní (9).
Tab. 1. Přehled pacientů a metod v jednotlivých centrech 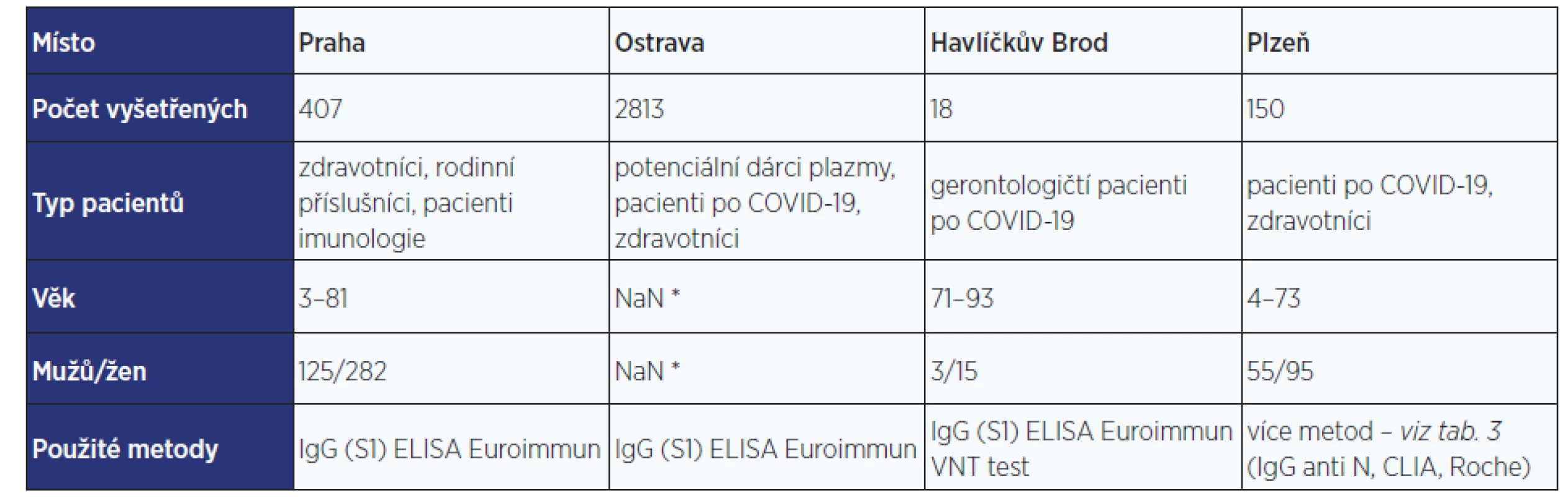
Pozn.: *Údaj není k dispozici, osobní data pacientů byla kódována číslem. Stanovení protilátek proti koronaviru
Protilátky proti koronaviru byly vyšetřeny metodou ELISA, Euroimmun Anti-SARS-CoV-2 (S1) IgG. Hodnoty udávají poměr optické denzity vzorku a kalibrátoru, který obsahuje hraniční množství protilátek. Nižší než 0,8 jsou považovány za negativní, vyšší než 1,1 za pozitivní. Podle výsledků nezávislých testů FDA je specificita vyšetření 100 % a senzitivita 90 % (11). Tato metoda byla použita v Praze, Ostravě a Havlíčkově Brodě. V Plzni byl vyšetřen celkový imunoglobulin proti proteinu N chemiluminiscenčně metodou Roche. V této metodě jsou za pozitivní považovány hodnoty > 1 (COI – cut-off index). Podle výsledků nezávislých testů FDA je specificita vyšetření 99,8 % a senzitivita 100 % (11).
VÝSLEDKY
Korelují protilátky IgG stanovené metodou ELISA s výsledkem VNT?
Data z ostravské laboratoře jsme využili k ověření korelace mezi koncentrací IgG a výsledkem VNT. Na obr. 1 je vyjádřeno zastoupení pacientů s negativním, či pozitivním výsledkem VNT ve skupinách rozdělených podle hodnot koncentrace protilátek vyšetřených metodou ELISA. Zjistili jsme, že z 1869 pacientů s pozitivním výsledkem IgG protilátek (≥ 1,1, dále označeni jako IgG pozitivní) mělo negativní VNT (tedy VNT = 0) pouze 8 osob. Tedy 99,6 % osob s pozitivitou IgG mělo neutralizační protilátky.
Obr. 1. Rozdělení výsledků VNT v jednotlivých skupinách pacientů s daným množstvím protilátek – ostravská laboratoř. 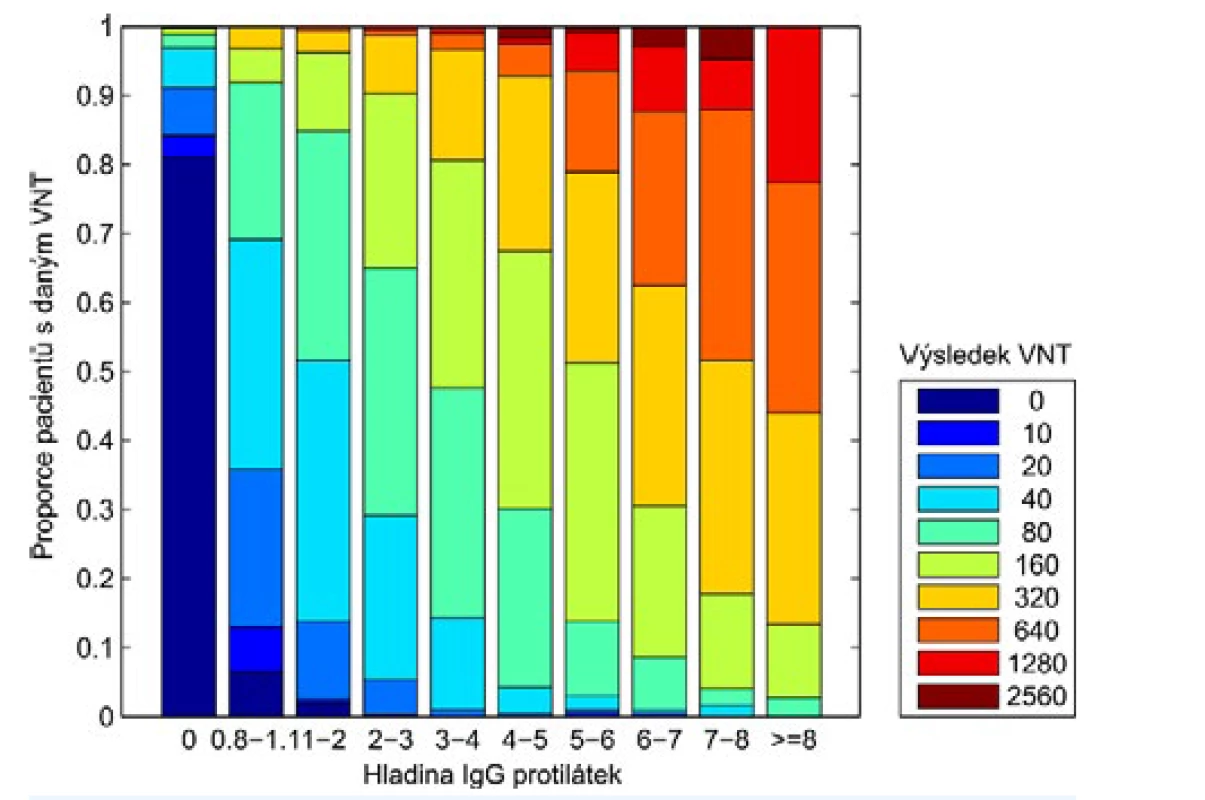
Každý sloupec představuje pacienty s daným množstvím protilátek. Výsledky VNT jsou barevně kódovány od negativní (tmavě modrá) po silně pozitivní (tmavě červená). Naopak z 1052 osob bez protilátek IgG mělo pozitivní VNT (VNT ≥ 20) 166, tedy 15,8 % sér, která neobsahovala IgG, mělo schopnost neutralizovat koronavirus. To znamená, že v těchto sérech nebyly protilátky proti proteinu S, ale jiné typy ochranných protilátek, které blokovaly virus a bránily rozvoji infekce.
Pro názornost uvádíme i konkrétní počty vyšetřených osob (tab. 2). Kategorizace koncentrace protilátek je uvedena podle hodnot OD ratio. Na základě těchto dat je možné zjistit další podmíněné pravděpodobnosti. Například můžeme spočítat, že pacient s hodnotou IgG > 4 má pravděpodobnost 97,6 %, že bude mít ve VNT titr ≥ 80, a bude vhodný jako dárce rekonvalescentní plasmy. Z dat ZÚ Ostrava tedy plyne, že koncentrace cirkulujících IgG je velmi dobrým prediktorem výsledku VNT. Osoby s pozitivním výsledkem měření IgG (≥ 1,1) mají téměř jistě ochranné protilátky.
Tab. 2. Korelace výsledku VNT a hladiny IgG – ostravská laboratoř. 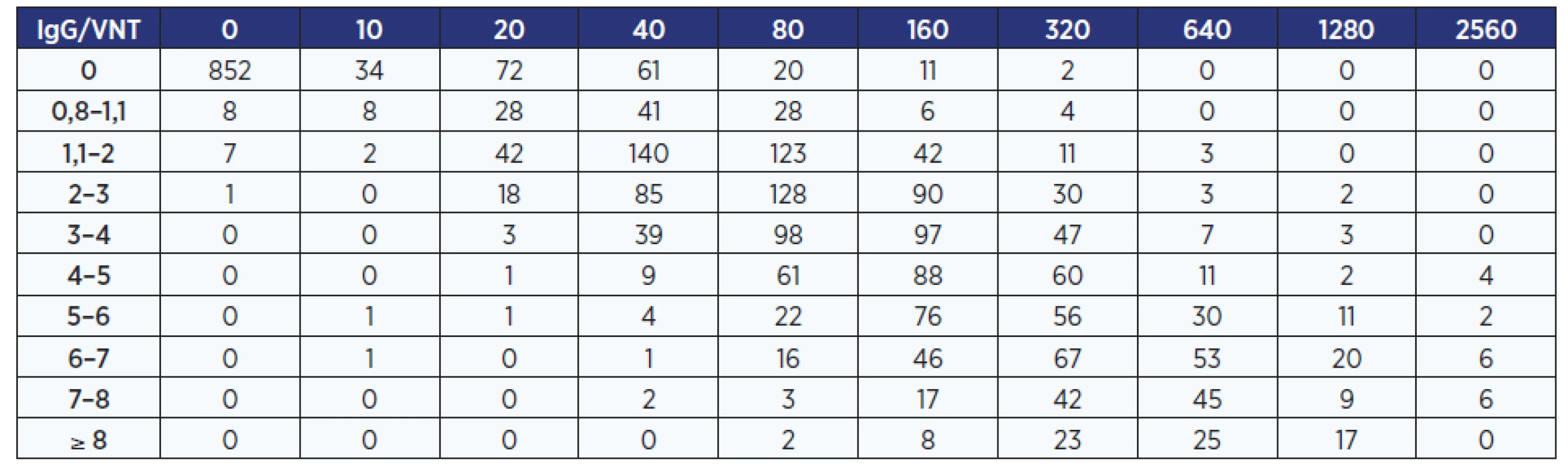
Pozn.: Na každém řádku je uveden počet pacientů s daným množstvím protilátek (zaznamenaným v 1. sloupci), v každém sloupci počet pacientů s daným výsledkem VNT (zaznamenaným v 1. řádku). Čísla v tabulce odpovídají počtu vyšetřených sér s tímto výsledkem. Malá část pacientů podstoupila více odběrů v časovém odstupu. Vyšetřeno bylo 3044 vzorků od 2813 pacientů. Korelují jednotlivé metody vyšetření protilátek navzájem?
Podobným způsobem jako výše můžeme ověřit spolehlivost jiných metod vyšetření protilátek pro predikci výsledku VNT. V práci plzeňské laboratoře (7) Šimánek a kol. porovnávali výsledky vyšetření protilátek metodami stanovujícími IgG oproti proteinu S (Euroimmun, Diasorin, Beckman), stanovením IgG oproti proteinu N (Abbott) nebo stanovením celkových protilátek proti N proteinu (Roche). U všech pacientů byl proveden VNT v ostravské laboratoři. V uvedené publikaci jsou spočítány hodnoty protilátek pro titry 80 a 160, tedy pro ověření vhodnosti potenciálních dárců rekonvalescentní plasmy. Ze stejných dat jsme nyní spočítali „protektivitu“, tedy zjistili jsme pravděpodobnost, že pacient bude mít pozitivní VNT (≥ 20), pokud bude mít pozitivní výsledek testu v dané metodě. Výsledky jsou uvedené v tab. 3. I z dat získaných na tomto menším souboru pacientů lze vyvodit poměrně jasný závěr: průkaz specifických protilátek jakoukoli metodou je velmi dobrým prediktorem výsledku VNT. Osoby s pozitivním výsledkem při použití jakékoli hodnocené metody mají téměř jistě ochranné protilátky.
Tab. 3. Určení pravděpodobnosti výskytu neutralizačních protilátek u pacientů s protilátkami stanovenými metodami CLIA a ELISA – plzeňská laboratoř. 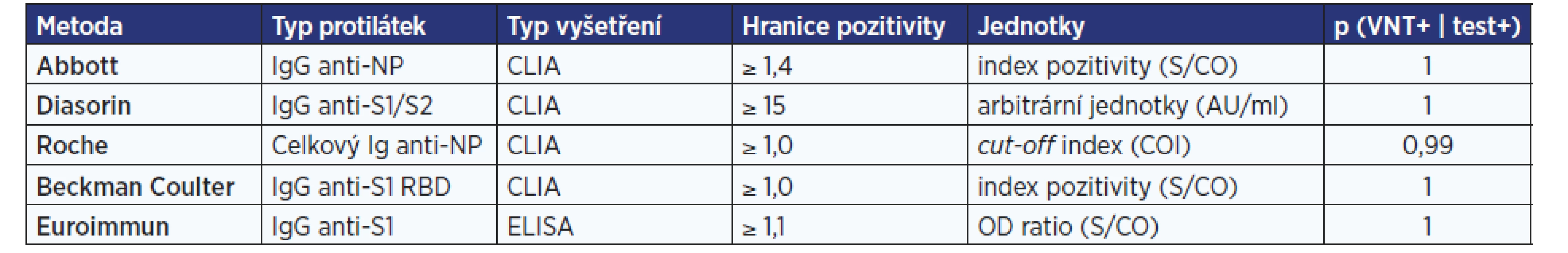
Pozn.: Poslední sloupec obsahuje odhad podmíněné pravděpodobnosti, že pacient s pozitivním výsledkem daného testu protilátek (test+) bude mít pozitivní výsledek VNT (VNT+). Jak dlouho přetrvávají protilátky po nákaze koronavirem?
Výše jsme ukázali, že uvedené metody stanovující cirkulující IgG jsou velmi spolehlivým prediktorem přítomnosti ochranných protilátek. Další významná otázka zní, jak dlouho se vyskytují v séru protilátky po nákaze koronavirem. Výsledky opakovaných vyšetření protilátek pocházejí z laboratoří v Praze a Plzni. Datum PCR testu jsme u pacientů zjišťovali dotazníky. Obr. 2 zachycuje koncentrace IgG naměřené v pražské laboratoři. Hladina protilátek u pacientů s pozitivním PCR testem se v čase snižuje, pokles však není statisticky významný. Bodový odhad směrnice regresní přímky je 2 x 10-4 za den, což by odpovídalo poklesu z hodnoty 10 na hodnotu 1 až za 10 let. Lze tedy konstatovat, že tento soubor pacientů ukazuje, že hladina IgG je velmi stabilní.
Obr. 2. Hladiny IgG proti koronaviru v závislosti na době uplynulé od data PCR testu – pražská laboratoř. 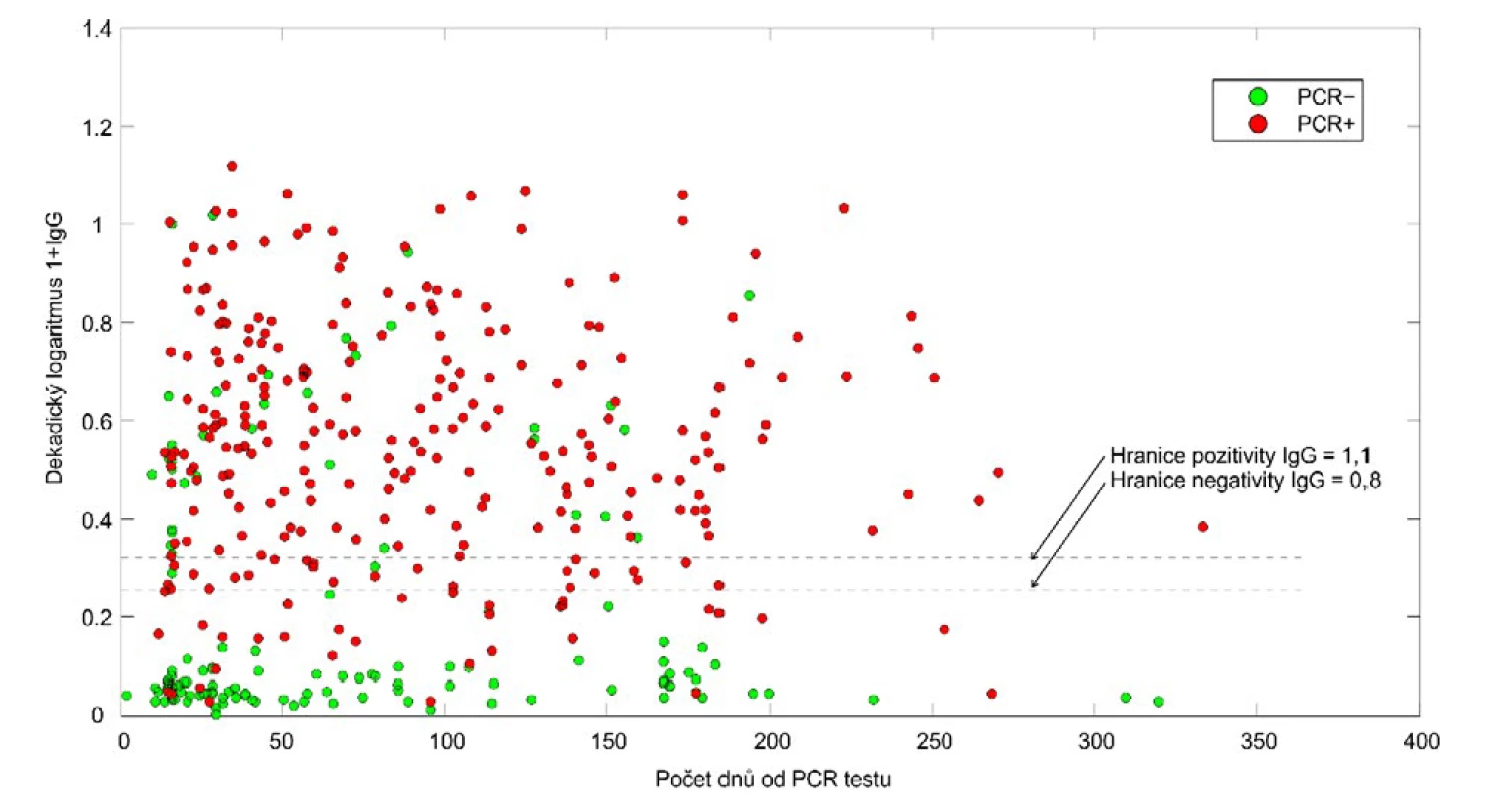
Zobrazena je hladina protilátek u osob, které nebyly očkované. Na ose y jsou vynesené hodnoty dekadického logaritmu OD ratio (poměr optické denzity vzorku a kalibrátoru) zvýšené o jedničku. Zobrazené jsou hranice negativity (OD ratio = 0,8) a pozitivity (OD ratio = 1,1). Dlouhodobý výskyt protilátek u pacientů z plzeňské laboratoře
Lépe je stabilita protilátek vidět v souborech dat z opakovaných vyšetření. Obr. 3 zachycuje hladiny protilátek u 100 osob vyšetřených v laboratoři v Plzni. Jednalo se o nehospitalizované pacienty se středně těžkým průběhem onemocnění COVID-19, s jasnými klinickými příznaky a pozitivním PCR testem. Protilátky byly stanoveny v intervalech s ohledem na jejich předpokládanou kinetiku zjištěnou z literatury. Většinou bylo vyšetření provedeno po 4, 6, případně 10 měsících od PCR testu. Ke zhodnocení byly u pacientů k dispozici dva, někdy i tři náběry. Je zřejmé, že po počátečním nárůstu se koncentrace protilátek u většiny osob ve sledovaném období snižovaly, ale tento pokles nebyl dramatický a i téměř po roce od infekce byly výsledky vyšetření stále pozitivní. Dekadický logaritmus hladiny protilátek (Roche, celkové protilátky) klesal rychlostí 2,8 x 10-3 za den, což znamená, že o hodnotu 1 (tj. například z hodnoty 100 na hodnotu 10, resp. z hodnoty 10 na hodnotu 1) klesne logaritmus přibližně za rok. Pouze u jednoho pacienta ze sledované skupiny se hodnoty snížily do pásma negativity.
Obr. 3. Dlouhodobý výskyt protilátek proti koronaviru – plzeňská laboratoř. 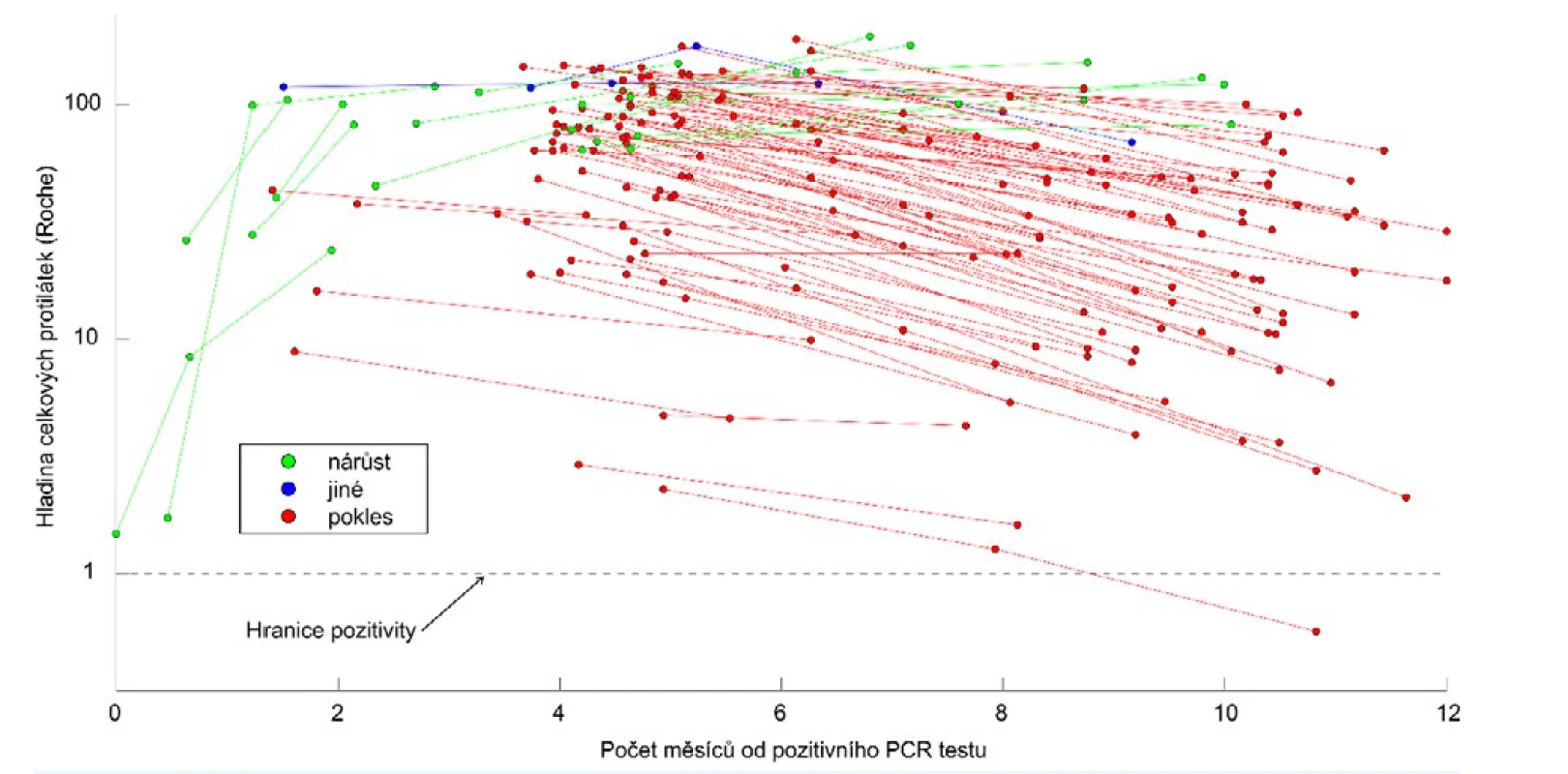
Vyšetření celkových protilátek proti koronaviru metodou Roche. Pro větší přehlednost jsou různé typy průběhů barevně odlišeny – nárůst je značen zeleně, pokles červeně a nemonotónní průběh modře. Na ose y jsou uvedeny hodnoty COI (cut-off index). Dlouhodobý výskyt protilátek u pacientů z havlíčkobrodské laboratoře
V laboratoři v Havlíčkově Brodě byl opakovaně v průběhu loňského roku vyšetřován soubor pacientů z Domova se zvláštní péčí v Břevnici. Výsledky této studie byly již publikovány v Časopise lékařů českých (12). Hladinu protilátek jsme sledovali po celé období u 18 seniorů, kteří měli pozitivní PCR test v březnu 2020. V domově byla poprvé zjištěna pozitivita dne 18. 3. 2020 a postupně až do 30. 3. 2020 přibývali další pacienti. Protilátky byly stanovené celkem pětkrát během 10 měsíců, a to několika různými metodami. Dvakrát byl proveden VNT test v Ostravě (v září a listopadu). Na obr. 4 uvádíme hodnoty vyšetření IgG metodou ELISA Euroimmun. Výsledky jednoho pacienta jsou v grafu propojené čárou, přičemž její barva odpovídá množství neutralizačních protilátek detekovaných v listopadovém séru (tedy asi 8 měsíců po infekci). U 15 seniorů se hladina protilátek pohybovala v pásmu pozitivity po celé sledované období. U tří seniorů k tvorbě protilátek nedošlo vůbec. Hladiny protilátek jsou konzistentní s VNT: všichni tři senioři, u nichž k tvorbě protilátek nedošlo, byli VNT negativní. Od jara 2020 do léta 2020 je patrný pokles hladiny protilátek u většiny osob. Ale v září 2020 došlo k opětovnému nárůstu, o jehož důvodu můžeme pouze spekulovat. Tou dobou již stoupala incidence infekce ve společnosti a také v domově se vyskytl jeden případ nemocného v ošetřujícím personálu. Poslední stanovení protilátek bylo provedeno před očkováním, které proběhlo v lednu 2021. Nikdo ze seniorů nebyl ve sledovaných 10 měsících opakovaně nemocný, i když byl zaznamenán výskyt infekce u personálu v září a v lednu.
Obr. 4. Opakované vyšetření hladiny protilátek u seniorů z Břevnice. 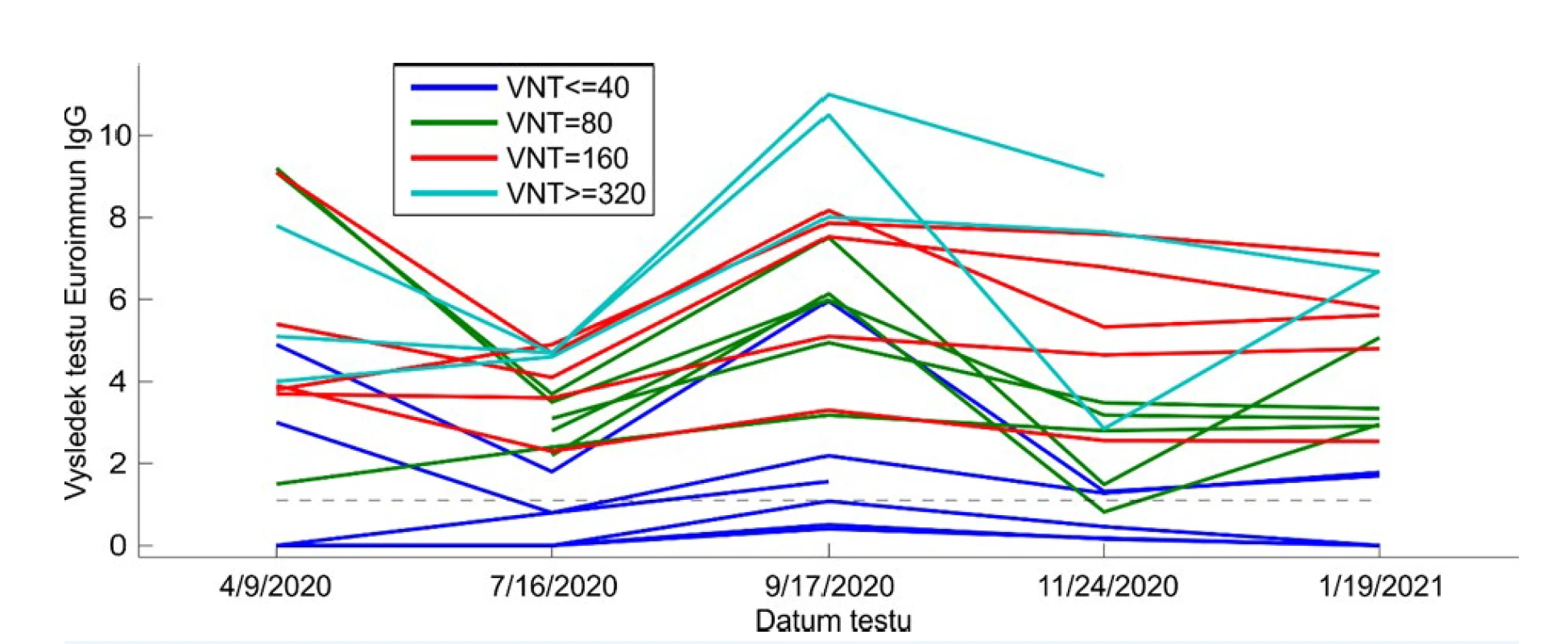
Stanovení IgG protilátek anti-S1 antigenu metodou ELISA Euroimmun. Každá čára odpovídá průběhu hladiny protilátek u jednoho pacienta. Čárkovaně hranice pozitivity. Na ose y jsou uvedeny hodnoty OD ratio. DISKUSE
Onemocnění COVID-19 je respirační choroba, která může mít různě závažný průběh, od bezpříznakového až po fatální. Nejzávažněji jsou postiženy nejstarší věkové skupiny, osoby se závažnými komorbiditami a/nebo obezitou. Celková smrtnost je uváděna 0,1–0,15 % (13), přestože původní odhady hovořily o výrazně vyšší mortalitě (0,5–2,8 %) (14). Mnoho nedorozumění v české literatuře bylo způsobeno zaměňováním celkové smrtnosti (infection fatality rate – IFR) a smrtnosti odhalených případů (case fatality rate – CFR), která je násobně vyšší a podstatně závisí na strategii testování.
Jak dlouho budou lidé, kteří infekci SARS-CoV-2 prodělali, imunní, je otázka, na kterou zatím neumíme jednoznačně odpovědět. Původně se vycházelo z výsledků zjištěných u lidí, kteří prodělali onemocnění po infekci sezónními koronaviry. Infekce příbuznými sezónními koronaviry (HCoV-NL63, HCoV-229E, HcoV-OC43, HCoV-HKU1) bývá velmi často asymptomatická nebo mívá lehčí klinický průběh. Hladinu protilátek a výskyt reinfekcí sledovali např. Edridge et al. (ale u skupiny pacientů s HIV, tedy imunokompromitovaných), kteří zjistili, že k reinfekcím dochází zpravidla až po roce, jen ve vzácných případech po 6 měsících (15). Také v případě SARS-CoV-2 se předpokládala přibližně stejně dlouhá imunita a odolnost vůči reinfekci (1).
Na specifické imunitě vůči koronavirům se podílejí jak paměťové T lymfocyty, tak paměťové B lymfocyty (5, 6). Např. Dan et al. potvrdili produkci neutralizačních protilátek IgG proti S a RBD antigenu u pacientů po 8 měsících od infekce (6). Jak vysvětlují zajištění dlouhodobé produkce protilátek? Paměťové B lymfocyty se objevují přibližně 14 dní po začátku onemocnění a jejich počet v průběhu prvních tří měsíců stoupá. Většinou jde o paměťové B lymfocyty produkující IgG protilátky proti RBD a proteinu S, ale dlouhodobě detekovatelné byly i paměťové B lymfocyty produkující protilátky IgA. Folikulární pomocné Th lymfocyty, které jsou klíčové pro aktivaci paměťových B lymfocytů, se také vyskytovaly v poměrně vysokém počtu po celé sledované období. Tc buňky byly naopak detekovány ve vyšším počtu v prvních měsících po infekci, ale později jejich počet klesal. Autoři zjistili, že pacienti s významně těžším průběhem onemocnění měli vysoké hladiny protilátek a větší počet Th a B lymfocytů než pacienti s mírnou formou onemocnění. U osob s těžším onemocněním však bylo zjištěno významně méně Tc lymfocytů. Autoři studie v závěru uvádějí, že produkce protilátek je zcela individuální a velmi se liší zastoupení Th, Tc a B lymfocytů.
V poslední zprávě ECDC, která hodnotila několik dlouhodobých studií, se uvádí, že předchozí infekce SARS-CoV-2 chrání 81–100 % pacientů po dobu pěti až sedmi měsíců od prodělané infekce (1), ale již nyní je zřejmé, že tento interval bude delší. Výskyt protilátek po 12 měsících publikovali např. Wang et al. (16). Princip dlouhodobé humorální imunity vysvětluje také práce Turnera et al. publikovaná v časopisu Nature (17). Zatímco v prvních měsících jsou protilátky produkovány krátce žijícími plazmoblasty, v pozdějším období zajišťují tvorbu dlouhodobě žijící plazmatické buňky, které jsou detekovatelné v kostní dřeni (BMPC – bone marrow plasma cells). Autoři zjistili u 15 z 19 pacientů specifické BMPC produkující IgG proti SARS-CoV-2 po 7 měsících a u 5 pacientů ještě test zopakovali po 11 měsících od infekce se stejným výsledkem. Spektrum protilátek se v čase měnilo, tvořily se protilátky s jinou strukturou vazebného místa v důsledku genetických mutací. Genetická informace pro vazebné místo protilátek se totiž modifikuje tzv. hypermutacemi. Takto vznikají různé varianty protilátek a selektují se takové buněčné klony, které tvoří nejkvalitnější neutralizační protilátky.
Naše výsledky jsou v souladu s publikovanými zjištěními. V našich souborech opakovaně testovaných osob jsme potvrdili výskyt protilátek jak u pacientů z loňské jarní vlny (tedy po 10 až 12 měsících), tak hlavně u velkého počtu nemocných v loňské podzimní vlně (tedy po 6 až 8 měsících po infekci). Pokud se pacient nesetkal v průběhu roku opakovaně s antigenem, hladiny protilátek u něj zpočátku zvolna klesaly, ale udržovaly se v pásmu pozitivity. V případě aktivace imunitního systému opakovaným kontaktem s antigenem docházelo k nárůstu, to je nejlépe vidět na datech ze září a ledna v břevnickém souboru (obr. 4).
Velká diskuse se vede o tom, jaká je protektivita protilátek. Problém je už v samotné definici tohoto termínu, protože nevíme přesně, co by měl znamenat. Poměrně exaktní možností ověření odolnosti vůči infekci je (v souladu se stanoviskem ECDC) ověření přítomnosti neutralizačních protilátek pomocí VNT (1). Pokud je VNT pozitivní, pak je dotyčný jedinec chráněn. Jelikož imunita se „nezapomíná“, ale spíše zlepšuje, pak by logicky mělo takové vyšetření provést jednou, případně zopakovat s časovým odstupem. Má-li někdo opakovaně pozitivní výsledek VNT, můžeme takového pacienta považovat v dlouhodobém měřítku přibližně jednoho roku za imunního. Jelikož VNT není dostupný všem pacientům, je možné používat ke stanovení protilátek standardní laboratorní testy (tab. 3). Důležitým zjištěním této studie je, že pozitivita testu na IgG (zjištěná jakoukoli metodou uvedenou v tab. 3) je prakticky dokonalým indikátorem pozitivity VNT. Vzhledem k podmíněným pravděpodobnostem z velkého ostravského souboru lze dokonce říct, že pozitivita IgG je spolehlivým indikátorem přítomnosti neutralizačních protilátek.
Zda po opakovaném styku s infekcí lidé s neutralizačními protilátkami již neonemocní nebo onemocní jen lehce, závisí na mnoha faktorech. Klíčové ale je, že tito jedinci již nejsou imunologicky naivní. Tedy SARS-CoV-2 pro ně nepředstavuje významné nebezpečí. Např. Lumley et al. sledovali od dubna do listopadu 2020 zdravotníky v oxfordské nemocnici, kterým byly na začátku studie stanoveny IgG proti koronaviru a sledovala se odolnost lidí s protilátkami ve srovnání s lidmi bez protilátek (1265 osob s protilátkami versus 12,5 tisíce osob bez protilátek) (18). V průběhu studie, která trvala 31 týdnů, byl opakovaně monitorován výskyt infekcí pomocí PCR. Mezi osobami s protilátkami byly během studie odhaleny pouze tři PCR pozitivní osoby, z nichž jedna měla mírný průběh reinfekce a dvě zcela asymptomatický. Mezi osobami bez protilátek bylo zjištěno 223 pozitivních osob. Závěr studie byl, že výskyt protilátek chrání před reinfekcí po dobu 6 měsíců. Jinými slovy člověk, který má protilátky, je odolný vůči nákaze, a proto ani nemusí být v karanténě, pokud se setkal s infikovanou osobou.
V další publikaci Abu-Raddat et al. (19) z Kataru sledovali výskyt infekce u 43 tisíc lidí s pozitivními protilátkami a u téměř 150 tisíc lidí bez protilátek po dobu 35 týdnů. Zatímco mezi osobami s protilátkami byla incidence koronavirové infekce < 1 na 10 000 osobodnů, u skupiny bez protilátek to bylo 14 na 10 000 osobodnů. Prodělání infekce omezilo výskyt reinfekce o 95 % a ani po 7 měsících nebyla zjištěna ztráta imunity. Převažovaly asymptomatický průběh nebo jen mírné klinické symptomy u osob s opakovanou infekcí. Podle doporučení CDC nemusí bezpříznakový člověk do karantény, pokud má protilátky, resp. pokud od vyšetření protilátek uplynuly maximálně 3 měsíce (20). V USA je tedy člověk s protilátkami uznán za imunního.
Podíváme-li se na data o opakovaných infekcích v Česku u lidí, kteří měli v minulosti COVID-19, tak od 1. 3. 2020 do 31. 5. 2021 mělo infekci 1,65 milionu lidí a opakovaně bylo symptomatických a PCR pozitivních 1982 lidí (21). U dalších 959 osob probíhalo ověření. Za reinfekci se považuje opakovaná symptomatická infekce po 60 dnech. Medián u nahlášených případů reinfekce činil 132 dnů (61–401). K tomu bylo nahlášeno 3070 případů možných reinfekcí COVID-19, u kterých alespoň jedna z epizod onemocnění proběhla asymptomaticky. Výskyt reinfekcí činí < 0,5 %, přesto MZ ČR doporučuje osoby po infekci očkovat. Toto doporučení však nikterak nezohledňuje možná rizika očkování osob s poinfekční imunitou. Osoby, které se ještě s infekcí nesetkaly, mají reakci na očkování zpravidla mírnější. Jedinci s imunitou po prodělané nemoci mohou reagovat vyšším výskytem nežádoucích účinků a zdravotních komplikací. Krammer et al. v klinické studii porovnávali protilátky a nežádoucí zdravotní účinky u vakcinovaných osob a zjistili nežádoucí účinky po očkování u 46 % osob, které infekci neprodělaly, ale u 89 % pacientů, kteří COVID-19 prodělali (22). Po první dávce vakcíny docházelo u lidí po infekci k výraznému navýšení hladiny protilátek, po druhé dávce vakcíny již k dalšímu nárůstu nedošlo. Autoři publikace proto doporučují pouze jednu „boostovací“ dávku očkování namísto dvou. Wang et al. zkoumali očkované pacienty, kteří měli ještě dostatečné množství protilátek, až po roce od infekce a očkování u nich vedlo k navýšení jejich koncentrace (16). Tedy i při delším odstupu (12 měsíců) od prodělané infekce je možné v případě potřeby stimulovat imunitní systém vakcínou; není nutné na vakcinaci spěchat.
Posledním sporným bodem je otázka, zda protilátky získané po infekci jedním typem koronaviru budou účinné i proti jiným, mutovaným variantám. Na ostravském pracovišti jsme potvrdili, že osoby po prodělání infekce původním, divokým kmenem viru i „britskou“ variantou alfa tvoří neutralizační protilátky také proti variantám beta (jihoafrická) a delta (indická), přičemž dosažený titr VNT byl v některých vzorcích nižší 2 - až 8krát, avšak v jiných vzorcích pokles nebyl zjištěn. Výraznější snížení titru VNT jsou pozorována u varianty beta, zatímco v případě varianty delta titr klesal méně a jen v některých vzorcích. I přes nižší hodnoty si všechny vzorky se všemi variantami viru zachovaly pozitivní výsledek VNT. Podobné výsledky uvádějí také Dupont et al.; podle jejich poznatků jsou neutralizační protilátky účinné u různých virových mutací (23). Pokud imunita po očkování funguje proti různým mutacím, není logicky žádný důvod, proč by neměla fungovat imunita po prodělané infekci.
Podle odborníků z klinické skupiny MZ ČR není stanovena žádná hranice, od níž protilátky poskytují ochranu před infekcí (24). Z našich dat ovšem plyne, že pozitivita IgG je lepším indikátorem přítomnosti neutralizačních protilátek, než je pozitivita PCR testu indikátorem přítomnosti živého viru na sliznici (25).
MZ ČR na základě stanoviska České vakcinologické společnosti ČLS JEP (ČVS) doporučuje vakcinaci celé dospělé populace včetně dětí od 12 let a těhotných žen (26, 27). Ministerstvo a některé odborné společnosti se neshodují z hlediska doby doporučeného odstupu vakcinace od prodělaného onemocnění. MZ ČR doporučuje očkovat bezprostředně po karanténě; v tom patrně vycházelo z názoru MeSES (28, 29). V médiích toto stanovisko podpořili někteří členové ČVS, ale na jejích stránkách je uvedena doba odstupu 3 měsíce (27). Takový přístup však popírá principy antivirové imunity, na kterých mnoho desetiletí stavíme řešení epidemií způsobených jinými respiračními viry. Pokud stimulace imunity vakcínou probíhá bezprostředně po prodělané infekci, tedy v době, kdy se specifická imunita teprve vyvíjí, přílišná aktivace imunitního systému může být pro organismus nebezpečná. Naopak ČSAKI navrhuje očkovat až se 6měsíčním odstupem, ideálně jednou dávkou, která stačí pro navození vyšší tvorby protilátek (30). Imunologové ve svém doporučení navrhují situace, kdy má smysl kontrolovat hladinu protilátek před očkováním, ale obecně podporují vakcinaci osob s protilátkami. Podobně situaci vnímá i Společnost pro lékařskou mikrobiologii ČLS JEP (31).
ZÁVĚR
Stanovení protilátek proti koronaviru je spolehlivou metodou prokazující prodělanou infekci SARS-CoV-2. Protilátky se vyskytují v krvi po velmi dlouhou dobu (minimálně 10 měsíců) a jsou schopné ochránit člověka při opakovaném kontaktu s touto infekcí natolik, že případná (a velmi vzácná) reinfekce ve většině případů bude mít mírný průběh nebo proběhne asymptomaticky. Využití běžně dostupných metod pro diagnostiku protilátek zcela spolehlivě predikuje výsledky virus neutralizačního testu, který je podle ECDC zlatým standardem stanovení imunity. Domníváme se, že na základě stále většího počtu důkazů je třeba akceptovat, že přirozeně navozená imunita po prodělané infekci zajišťuje dlouhodobou ochranu a lidé po infekci mají stejně významný podíl na zajištění kolektivní imunity jako lidé očkovaní.
Seznam zkratek
ACE2 angiotenzin konvertující enzym 2
BMPC plazmatické buňky kostní dřeně
CDC Centrum pro kontrolu a prevenci nemocí, USA
CFR smrtnost v populaci zjištěných případů (case fatality rate)
CLIA chemiluminescenční imunoanalýza
DNA deoxyribonukleová kyselina
ECDC Evropské centrum pro prevenci a kontrolu nemocí
ELISA enzyme-linked immunosorbent assay
FDA Úřad kontrolu léčiv a potravin
HcoV-229E lidský koronavirus 229E
HcoV-HKU1 lidský koronavirus HKU1
HcoV-NL63 lidský koronavirus NL63
HcoV-OC43 lidský koronavirus OC43
HIV virus lidské imunodeficience
IFR smrtnost infekce (infection fatality rate)
IgA imunoglobulin A
IgG imunoglobulin G
IgM imunoglobulin M
OD ratio poměr optické denzity vzorku a kalibrátoru u ELISA
PCR polymerázová řetězová reakce
protein N nukleokapsidový protein
protein S spike protein
RBD doména vázající receptor
S1 podjednotka 1 proteinu S
SARS-CoV-2 severe acute respiratory syndrome-related coronavirus
Tc cytotoxické T lymfocyty
Th pomocné T lymfocyty
Adresa pro korespondenci:
RNDr. Zuzana Krátká, Ph.D.
Imunologická laboratoř GENNET, s. r. o.
Sdružení mikrobiologů, imunologů a statistiků (SMIS)
e-mail: zuzana.kratka@smis-lab.cz
Zdroje
- European Centre for Disease Prevention and Control. Immune responses and immunity to SARS-CoV-2. ECDC, 2021 Sep 8. Dostupné na: www.ecdc.europa.eu/en/covid-19/latest-evidence/immune-responses
- Krátká Z, Fejt V, Kučera R, Zelená H. Protilátkové repetitorium – vyšetření protilátek proti koronaviru v běžné praxi. Časopis lékařů českých 2021; 160(2–3): 52–56.
- Post N, Eddy D, Huntley C et al. Antibody response to SARS-CoV-2 infection in humans: a systematic review. PLoS One 2020; 15(12): e0244126.
- Letko M, Marzi A, Munster V. Functional assessment of cell entry and receptor usage for SARS-CoV-2 and other lineage B betacoronaviruses. Nat Microbiol 2020; 5(4): 562–569.
- Shrotri M, van Schalkwyk MCI, Post N et al. T cell response to SARS-CoV-2 infection in humans: a systematic review. PLoS One 2021; 16(1): e0245532.
- Dan JM, Mateus J, Kato Y et al. Immunological memory to SARS-CoV-2 assessed for up to 8 months after infection. Science 2021; 371(6529): eabf4063.
- Všeobecná zdravotní pojišťovna ČR. Organizační opatření VZP ČR č. 2/2021 v souvislosti s onemocněním COVID-19 způsobeným virem SARS-CoV-2. VZP ČR, 25. 6. 2021. Dostupné na: https://media.vzpstatic.cz/media/Default/dokumenty/covid-19/organizacni-opatreni_02_2021-odberova-centra-laboratore.pdf
- Ministerstvo zdravotnictví ČR a Rada vlády pro zdravotní rizika. Strategie testování onemocnění COVID-19 pro sezónu respiračních onemocnění 2020/2021. MZ ČR, 15. 12. 2020. Dostupné na: https://ppo.mzcr.cz/upload/files/narodni-strategie-testovani-onemocneni-covid-19-a-ostatni-dokumenty-strategie-testova-ni-covid-19-v2-0-15-12-2020-6061f409a770e.pdf
- Šimánek V, Pecen L, Krátká Z et al. Five commercial immunoassays for SARS-CoV-2 antibody determination and their comparison and correlation with the virus neutralization test. Diagnostics 2021; 11(4): 593.
- Valcourt EJ, Manguiat K, Robinson A et al. Evaluation of a commercially-available surrogate virus neutralization test for severe acute respiratory syndrome coronavirus-2 (SARS-CoV-2). Diagn Microbiol Infect Dis 2021; 99(4): 115294.
- Food and Drug Administration. EUA Authorized serology test performance. FDA, 2021 Sep 28. Dostupné na: www.fda.gov/medical-devices/coronavirus-disease-2019-covid-19-emergency-use-authorizations-medical-devices/eua-authorized-serology-test-performance
- Fejt V, Krátká Z, Zelená H, Fürst T. Stáří není nemoc. Vývoj hladiny ochranných protilátek proti koronaviru SARS-CoV-2 u seniorů z Domova Břevnice. Časopis lékařů českých 2020; 159 (7–8): 303–311.
- Ioannidis JPA. Reconciling estimates of global spread and infection fatality rates of COVID-19: An overview of systematic evaluations. Eur J Clin Invest 2021; 51(5): e13554.
- Státní zdravotní ústav. Chřipka versus koronavirus – podobnosti a zásadní rozdíly, situace k 18. 3. 2020. SZÚ, 18. 3. 2020. Dostupné na: www.szu.cz
- Edridge AWD, Kaczorowska J, Hoste ACR et al. Seasonal coronavirus protective immunity is short-lasting. Nat Med 2020; 26 (11): 1691–1693.
- Wang Z, Muecksch F, Schaefer-Babajew D et al. Naturally enhanced neutralizing breadth against SARS-CoV-2 one year after infection. Nature 2021; 595 (7867): 426–431.
- Turner JS, Kim W, Kalaidina E et al. SARS-CoV-2 infection induces long-lived bone marrow plasma cells in humans. Nature 2021; 595 (7867): 421–425.
- Lumley SF, O'Donnell D, Stoesser NE et al.; Oxford University Hospitals Staff Testing Group. Antibody status and incidence of SARS-CoV-2 infection in health care workers. N Engl J Med 2021; 384 (6): 533–540.
- Abu-Raddad LJ, Chemaitelly H, Coyle P. SARS-CoV-2 antibody-positivity protects against reinfection for at least seven months with 95% efficacy. E Clinical Medicine 2021; 35 : 100861.
- Centers for Disease Control and Prevention. Interim guidelines for COVID-19 antibody testing. CDC, 2021 Sep 21. Dostupné na: www.cdc.gov/coronavirus/2019-ncov/lab/resources/antibody-tests-guidelines.html#anchor_1616006658343
- Státní zdravotní ústav. Absolutní počet případů reinfekcí covid-19 v ČR vzrostl, jejich frekvence výskytu ale nadále zůstává nízká. Dostupné na: http://www.szu.cz/tema/prevence/absolutni-pocet-pripadu-reinfekci-covid-19-v-cr-vzrostl
- Krammer F, Srivastava K, Alshammary H et al. Antibody responses in seropositive persons after a single dose of SARS-CoV-2 mRNA vaccine. N Engl J Med 2021; 384(14): 1372–1374.
- Dupont L, Snell LB, Graham C et al. Antibody longevity and cross-neutralizing activity following SARS-CoV-2 wave 1 and B.1.1.7 infections. medRxiv 2021.06.07.21258351.
- Ministerstvo zdravotnictví ČR. Klinická skupina COVID MZ. Zápis z jednání KS COVID II ze dne 13. 5. 2021. MZ ČR, 13. 5. 2021. Dostupné na: https://ppo.mzcr.cz/upload/files/zapisy-z-jednani-zapis-z-jednani-ks-covid-ii-ze-dne-13-5-2021-60a512dc3c938.pdf
- Watson J, Whiting PF, Brush JE. Interpreting a covid-19 test result. BMJ 2020; 369: m1808.
- Česká vakcinologická společnost ČLS JEP, Česká gynekologická a porodnická společnost ČLS JEP. Doporučení k očkování dětí ve věku 12–15 let a adolescentů proti nemoci COVID-19. ČVS, 16. 7. 2021. Dostupné na: www.vakcinace.eu/data/files/downloads/cvs_et_al_doporuceni_k_ockovani_ddti_proti_nemoci_covid_19_16072021.pdf
- Česká vakcinologická společnost ČLS JEP. Očkování proti onemocnění COVID-19 u těhotných a kojících. ČVS, 3. 6. 2021. Dostupné na: www.vakcinace.eu/data/files/downloads/ockovani_tehotnych_kojicich_cvs_cgps_3_cerven2021final.pdf?openfld=news-doporuceni
- Mezioborová skupina pro epidemické situace. Stanovisko k očkování proti nemoci COVID-19. MeSES, 8. 6. 2021. Dostupné na: www.meses.cz/stanovisko-k-ockovani-proti-nemoci-covid-19
- Ministerstvo zdravotnictví ČR. Lidé po prodělání onemocnění COVID-19 se mohou nově očkovat ihned po skončení izolace. MZ ČR, 24. 6. 2021. Dostupné na: https://koronavirus.mzcr.cz/lide-po-prodelani-onemocneni-covid-19-se-mohou-nove-ockovat-ihned-po-skonceni-izolace
- Česká společnost alergologie a klinické imunologie ČLS JEP. Stanovisko ČSAKI k vyšetřování protilátek u onemocnění COVID-19. ČSAKI, 9. 8. 2021. Dostupné na: www.csaki.cz/dokumenty/IGGCOVID.pdf
- Společnost pro lékařskou mikrobiologii ČLS JEP. Dvě aktuální prohlášení k necílenému plošnému testování a ke skupině MeSES. SLM, 14. 5. 2021. Dostupné na: www.splm.cz/_download/00000179-6e8f-d498-a97f-6ebfd2d60000
Štítky
Adiktologie Alergologie a imunologie Angiologie Audiologie a foniatrie Biochemie Dermatologie Dětská gastroenterologie Dětská chirurgie Dětská kardiologie Dětská neurologie Dětská otorinolaryngologie Dětská psychiatrie Dětská revmatologie Diabetologie Farmacie Chirurgie cévní Algeziologie Dentální hygienistka
Článek vyšel v časopiseČasopis lékařů českých
Nejčtenější tento týden
2021 Číslo 5- Přerušovaný půst může mít významná zdravotní rizika
- Efektivita kartáčku Sonicare For Kids u dětí předškolního věku
- Jak a kdy u celiakie začíná reakce na lepek? Možnou odpověď poodkryla čerstvá kanadská studie
- Takrolimus v terapii atopické dermatitidy a analýza jeho nákladové efektivity ve srovnání s kortikosteroidní léčbou
- Doc. Jitka Fricová: V USA nasazovali fentanyl poměrně nekriticky, v Česku je situace jiná
-
Všechny články tohoto čísla
- Protilátky po prodělaném onemocnění COVID-19 poskytují dostatečnou a dlouhodobou ochranu před reinfekcí
- Faktory ovlivňující proces rozhodování o péči v závěru života u hospitalizovaných pacientů
- Používání vybraných POCT metod všeobecnými praktickými lékaři v Česku
- Moderní trendy v ošetřování pacientů s komplikovanou derivační stomií
- Kontext a historické souvislosti vzniku a formování nejstaršího kontinuálně existujícího rezidenčního modelu léčby závislosti na alkoholu („apolinářský model“) ve střední Evropě v letech 1948–1960
- Uvádíte správně použitou literaturu?
- Zemřel prof. Oldřich Eliška, doyen českých anatomů
- Přednáškové večery Spolku českých lékařů v Praze (říjen - prosinec 2021)
- Časopis lékařů českých
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Protilátky po prodělaném onemocnění COVID-19 poskytují dostatečnou a dlouhodobou ochranu před reinfekcí
- Používání vybraných POCT metod všeobecnými praktickými lékaři v Česku
- Faktory ovlivňující proces rozhodování o péči v závěru života u hospitalizovaných pacientů
- Zemřel prof. Oldřich Eliška, doyen českých anatomů
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Revma Focus: Spondyloartritidy
nový kurz
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



