-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Patogeneticky komplikovaný případ osteoporózy u mladého muže
Pathogenetically Complicated Case of Osteoporosis in a Young Man
Osteoporosis, is a serious disease both in women and men, with a high risk of fractures. However, its pathogenesis differs markedly, with the secondary form being more common in men. The aim of this case study is to demonstrate the complex pathogenesis of a severe osteoporosis in a 23-year-old heavy smoker with histiocytosis X, diabetes insipidus (DI), subclinical hypogonadism and low serum levels of IGF-I. Later, after normalization of sex hormones and IGF-I levels, vasopressin substitution, cessation of smoking and after long-term antiresorption therapy, adequate increase in bone density at the hip was documented, but insufficient and very slow increase at the lumbar spine was observed. Severe osteoporosis at the spine is most probably the consequence of the interaction of smoking with multiple hormone insufficiency during development of peak bone mass. The effect of additional, unidentified factor(s) (gene or hormone) is also likely. On the other hand, a direct causal association between histiocytosis X and osteoporosis was not confirmed histomorphometrically in this patient.
Key words:
osteoporosis in men, histiocytosis X, free testosterone, IGF-I, diabetes insipidus, smoking.
Autoři: I. Žofková
Působiště autorů: Endokrinologický ústav, Praha
Vyšlo v časopise: Čas. Lék. čes. 2008; 147: 574-578
Kategorie: Kazuistika
Souhrn
Osteoporóza u mužů je stejně závažným onemocněním s vysokým rizikem fraktur jako u žen. Její patogeneze je však výrazně odlišná. Většinou jde o formu druhotnou komplikující jiná závažná onemocnění včetně endokrinopatií. Cílem tohoto sdělení je na případu 23letého silného kuřáka s histiocytózou X, s velmi nízkou hodnotou kostní denzity a hormonální nedostatečností ve smyslu diabetes insipidus (DI), subklinického hypogonadismu a nízkých hladin IGF-I v séru, ukázat na komplikovanou patogenezi osteoporózy u muže. Pozdější normalizace hladin sexuálních hormonů a IGF-I, substituce vazopresinem, abstinence kouření a antiresorpční léčba vedly téměř k normalizaci kostní denzity v kyčli, ale jen k velmi pomalému a nedostatečnému nárůstu v lumbální páteři. Závažná osteoporóza axiálního skeletu u tohoto pacienta je zřejmě důsledkem interakce kouření a mnohočetné hormonální nedostatečnosti v období vývoje vrcholu kostní hmoty. Nelze vyloučit ani vliv dalšího, zatím neidentifikovaného faktoru (genu nebo hormonu). Naopak přímou kauzální souvislost kostního postižení s histiocytózou X se histomorfometrickým vyšetřením prokázat nepodařilo.
Klíčová slova:
osteoporóza u mužů, histiocytosis X, volný testosteron, IGF-I, diabetes insipidus, kouření.Osteoporóza je stále vnímána především jako choroba žen. U mužů je poměrně málo prozkoumaným fenoménem lišícím se svou patogenezí i průběhem od osteoporózy postmenopauzální. Většinou jde o postižení druhotné vzniklé na podkladě medikace (glukokortikoidy a jiná imunosupresiva, antiepileptika, kličková diuretika), alkoholismu a kouření (1, 2). Jindy se vyvíjí jako komplikace závažného interního onemocnění. Ke ztrátě kostní hmoty dochází také u klinicky vyhraněných endokrinopatií, jakými jsou Cushingova choroba, tyreotoxikóza i u subklinických forem hormonální nedostatečnosti. Vztah fyziologického poklesu hladin IGF-I a testosteronu k úbytku kostní hmoty u stárnoucích mužů je dobře znám (3).
Příčinou ztráty kostní hmoty může být také deficit produkce vazopresinu u nemocných s diabetes insipidus (DI). Centrální forma onemocnění je patogeneticky heterogenní (4). Nejčastěji vzniká na podkladě autozomálně dominantního genetického defektu syntézy hormonu nebo mutace genu pro vazopresin-neurohypofysin II (5), jindy jako důsledek traumatu, zánětu, autoimunitního, nádorového nebo vaskulárního postižení (6–8). Až 50 % případů DI je však klasifikováno jako forma idiopatická.
Jednou z příčin centrálního DI může být histiocytosis-X. Toto onemocnění vzniká při fokální nebo systémové produkci histiocytů (Langerhansových nebo non-Langerhansových buněk), infiltrujících různé tkáně, zvláště plíce, kosti, kůži nebo centrální nervový systém (9, 10). Hypoteticky onemocnění vzniká na bázi hypersenzitivní reakce nebo imunodeficitu. Vyskytuje se i u dětí, o něco častěji u chlapců (k dívkám v poměru 1,36 : 1). Roční incidence u středoevropských dětí do 18 let je 2,24 případů/1 milion. Z počátku se projevuje necharakteristickou symptomatologií (poruchy spánku, adipsie, sklon k obezitě, granulomatózní kožní změny, bolesti v kostech nebo poruchy imunity). Později dochází k vývoji xanthelazmat a exoftalmu a až u 35 % pacientů k intersticiálnímu fibróznímu postižení plic. Granulomatózní infiltrace hypothalamu a neurohypofýzy se manifestuje progredující polydipsií a polyurií, které nakonec vyústí v diabetes insipidus s charakteristicky nízkými hodnotami specifické váhy a osmolality moče (méně než 200 mosmol/l) a obrazem ztluštění stopky hypofýzy při CT nebo MRI vyšetření. DI (úplný nebo parciální projevující se jen esenciální hypernatrémií) bývá někdy jediným projevem histiocytózy X a může poměrně dlouho předcházet rozvoji kostních změn. Zhruba u 50 % pacientů s histiocytózou X dochází k projevům deficitu některých adenohypofyzárních hormonů, především gonadotropinů a somatotropinu (11). Diagnózu potvrdí průkaz Langerhansových histiocytárních buněk, především v plicích a kostních lézích. Diferenciálně diagnosticky je třeba vyloučit histiocytózu z non-Langerhansových buněk a jiná granulomatózní onemocnění – Wegenerovu granulomatózu, sarkoidózu nebo lymfocytární infundibulo-hypofysitidu (s pozitivitou protilátek proti vazopresinu), nádorová onemocnění neurohypofýzy (u dětí především germinom a kraniofaryngeom) a souvislost s traumatem nebo operací.
Postižení skeletu při histiocytóze X se manifestuje lokalizovanými, někdy i vícečetnými lytickými ložisky (především v oblasti lebky) s charakteristickým sklerotickým lemem (12). Do jednoho roku od začátku manifestace DI se u více než 50 % nemocných vyvinou i léze extrakraniální (pánev, žebra, dlouhé kosti). Nejméně invazivní formou kostní histiocytózy je benigní eozinofilní granulom (13). Závažnější jsou multifokální Hand-Schüllerova-Christianova nemoc nebo Letterer-Siweho nemoc, probíhající, zvláště u malých dětí, pod obrazem diseminovaného postižení RES s fulminantním průběhem, jindy se spontánními remisemi. Postižení skeletu u histiocytózy-X však nemá charakter difuzní osteoporózy. Hypoteticky lze uvažovat o možném kauzálním vztahu kostních změn k nadprodukci osteoresorpčních cytokinů Langerhansovými buňkami, především TNF-alfa a agonisty receptoru pro interleukin-1 (14).
KAZUISTIKA
Popis případu
Muž ve věku 23 let, profesí zámečník, astenické konstituce (výška 176 cm, hmotnost 62 kg) bez klinických projevů hypogonadismu nebo jiné endokrinopatie si v průběhu roku 1996 stěžoval na chronický suchý kašel a progredující žízeň. Přiznal, že zhruba 2–3 roky kouří 15–20 cigaret denně. Konzumaci alkoholu popíral. Příjem mléčných výrobků byl údajně přiměřený. Prodělal 3 traumatické fraktury (loket v dětství, zápěstí a palec nohy v období puberty). Jinak byl vždy zdráv. Rtg plic ukázal retikulo-nodulární až nodulární stíny oboustranně v horním a středním plicním poli, které budily naléhavé podezření na histiocytózu X. Při bronchoskopii sice nebyla nalezena charakteristická Bürbeckova granula, ale byly zachyceny buňky produkující protilátku proti proteinu S100, také typické pro histiocytózu X. Při spirometrickém vyšetření byla zjištěna mírná restrikční porucha ventilace a DLCO byla snížena o 44 %. Pacientovi byly doporučeny pouze pravidelné bronchoskopické kontroly, jejichž výsledky v průběhu dalších let ukazovaly stacionární nález.
Pro podezření na diabetes insipidus bylo pacientovi ve stejném roce doporučeno endokrinologické vyšetření. Jak je patro z tabulky 1, diuréza v té době byla 9400 ml/den a specifická váha moči 1,002. Po aplikaci 4 kapek vazopresinu (Adiuretin) denně diuréza klesla na 2000 ml, později kolísala v rozmezí 1050–1500 ml a specifická váha moči se pohybovala mezi 1,013 a 1,018.
Vyšetření krajiny tureckého sedla pomocí CT provedené v roce 1996 zobrazilo malé přemostěné sedlo (výška 5 mm), ale širší infundibulum (4,5 mm). Suprasellární a parasellární oblasti byly bez patologického nálezu. Další kontroly v letech 2000–2007 byly prováděny pomocí MRI (v modu SE/T1W/, TSE /T2W): Sedlo bylo velikosti 4–5 mm a při zadním okraji žlázy bylo patrné drobné ložisko zvýšeného signálu v T1W. Zadní lalok byl proti normálu menší, ale ztluštění infunfindibula při dalších kontrolách již nebylo prokazatelné.
Rentgenovou kostní denzitometrií v roce 1996 byla zjištěna závažná osteoporóza v oblasti lumbální páteře (snížení denzity o 37 %) a těžší osteopenie v kyčli (snížení o 28 %) (tab. 1). Pacient neměl algickou vertebrogenní symptomatologii, a proto snímek páteře, který by vyloučil frakturu obratlových těl, nebyl indikován. Vzhledem k prokázané histiocytóze-X byla provedena biopsie z lopaty kosti pánevní. Histomorfometrické vyšetření však neprokázalo změny ve smyslu histiocytární infiltrace. V dřeňových prostorách byly patrné ostrůvky normální krvetvorby a tkáň byla přiměřeně mineralizovaná. Osteoid tvořil 1,5 % objemu trámců a kryl 15 % jejich povrchu (normální obraz). Nápadné však bylo necharakteristické ložiskovité prořídnutí skeletu (prof. C. Povýšil).
Z hormonálních vyšetření (tab. 1) byla opakovaně měřena nízká klidová hladina celkového i volného testosteronu v séru a nižší hladina FSH. Hodnota LH v séru byla pouze posunuta k dolní hranici normy. Nízkým hladinám testosteronu odpovídala zvýšená hladina SHBG. Naopak klidová hladina estrogenu kolísala v mezích mužské normy. Z tabulky 1 je dále patrné, že pacient měl opakovaně sníženou hladinu IGF-I v séru. Koncentrace PTH kolísala od lehce snížených hodnot k hodnotám normálním. Hladiny TSH, volného T4 a T3 a základní biochemická vyšetření byly v mezích normy. Také hladina osteokalcinu v séru byla normální, ale vysoká hodnota indexu deoxypyridinolin/kreatinin v moči ve dvou z měření dokumentovala aktivaci kostní resorpce. Nemocnému byla proto nasazena antiresorpční léčba bisfosfonátem, kalciem a vitaminem D. Vzhledem k průkazu DI byla současně zahájena substituční léčba vazopresinem. Opakovaná měření MIR okolí sedla a bronchoskopická vyšetření v dalších letech pozorování byla hodnocena jako stacionární, proto ani později nebylo přistoupeno k chemoterapii.
Tab. 1. Hormonální a biochemická vyšetření a hodnoty kostní denzitometrie (DXA) v páteři a v kyčli u nemocného s histiocytózou X 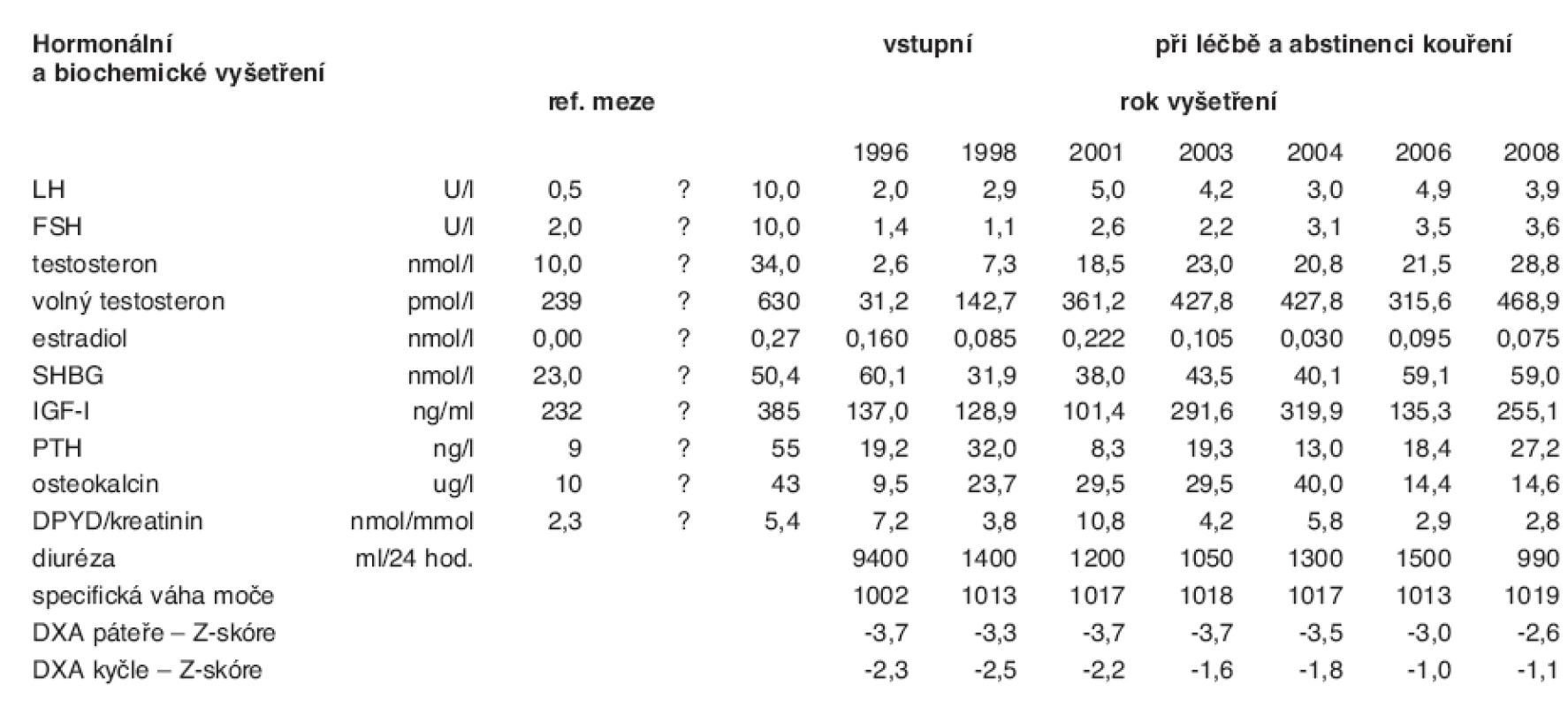
Normy volného testosteronu u mužů ve věku 16–25 let: 238,8–629,9 pmol/l, ve věku 25–40 let 238,9–586,6 pmol/l LH – luteotropní hormon, FSH – folikuly stimulující hormon, SHBG – sexuální hormony vázající globulin, IGF-I – insulin like growth factor, factor-I, PTH – parathormon, DPYD – deoxypyridinolin v moči Z časových průběhů v následujících letech je zřejmé, že hodnota testosteronu a IGF-I u našeho pacienta postupně stoupaly, takže v roce 2003 byly hladiny obou hormonů ve fyziologických mezích. Přestože nemocný respektoval doporučenou léčbu i zákaz kouření, vzestup kostní denzity byl zaznamenán pouze v osteopenické kyčli, zatímco nález závažné osteoporózy v páteři přetrvával celých 10 let sledování (tab. 1).
Za účelem vyloučení subklinické nedostatečnosti os adenohypofýza-gonády a somatotropin-IGF-I, které by vysvětlily jen velmi pomalý nárůst kostní hmoty v páteři, jsme v roce 2007 provedli testy sekreční rezervy gonadotropinů a testosteronu (po stimulaci LHRH) a sekrece somatotropinu (po stimulaci inzulínovou hypoglykémií nebo argininem). Tyto testy však, kromě mírně sníženého vzestupu FSH, ukázaly přiměřenou odpověď ostatních sledovaných hormonů.
Diskuze
U mladého muže s prokázanou histiocytózou X nebyl skelet postižen typickými ložiskovými osteolytickými lézemi, ale difuzním prořídnutím charakteru osteoporózy, jejímž základním, nikoliv však jediným, patogenetickým mechanismem byla polyglandulární hormonální nedostatečnost související pravděpodobně s postižením hypothalamických jader, neurohypofýzy a stopky hypofýzy granulomatózním procesem.
Jednou z nejčastějších příčin ztráty kostní hmoty u dospělých mužů je manifestní, ale i subklinický hypogonadismus. Prokázán byl prediktivní význam hladin volného testosteronu pro nárůst vrcholu kostní hmoty u mužů v době budování kostní hmoty (15, 16). Podobně jako u našeho pacienta odpovídal také ve studii Kuchuka et al. (17) nízkým hladinám celkového i volného testosteronu rychlejší kostní obrat a nízká hodnota kostní hmoty.
Přímý negativní vliv na skelet našeho pacienta mohla mít i vyšší hladina SHBG v séru. Tento vazebný protein, jenž je velmi citlivým ukazatelem funkce gonád, je i biologickým markrem rizika fraktur u mužů. Hladina SHBG v séru bývá významně vyšší u mužů s osteoporózou a negativně koreluje s kostní denzitou v kyčli i páteři, pozitivně pak s parametry kostní resorpce, a to těsněji než celkový nebo volný testosteron (18, 19). Na vývoj mužského skeletu má nepochybně příznivý vliv i estrogen (18, 19). U našeho pacienta však hladina estradiolu v séru byla opakovaně v mezích normy.
Závažným patogenetickým faktorem v období vývoje vrcholu kostní hmoty může být i nedostatečnost osy somatotropin-IGF-I. Kostní efekt IGF-I je vysvětlován přímým anabolickým působením na kost, ale i nepřímo prostřednictvím růstu svalové hmoty, která aktivuje kostní mechanostat. Nízké hladiny IGF-I měli dospělí muži s osteoporózou , ale i děti a adolescenti s nízkou kostní denzitou neodpovídající jejich věku (20). Nízké hodnoty tohoto peptidu v séru v průběhu adolescence mohly tedy u našeho pacienta také přispět ke zpomalenému nárůstu kostní hmoty.
Z dalších možných mechanismů podílejících se na trvající osteoporóze u popisovaného případu je nedostatečná produkce vazopresinu. Jak bylo zmíněno v úvodu, skelet bývá postižen u DI jakékoliv etiologie. Mechanismus kostního postižení není jasný. Údaje, které by dokumentovaly přímý kostní účinek deficitu vazopresinu, nebyly zatím publikovány. Mimoto ani trvalá plná substituce vazopresinem u našeho pacienta nevedla k odpovídajícímu nárůstu kostní hmoty v páteři. Je však možné, že se zde větší mírou uplatňoval útlum sekrece oxytocinu, který fyziologicky inaktivuje RANKL a aktivuje proformační osteoprotegerin (21).
Později, v období normalizace klidových hladin testosteronu a IGF-I, dynamické hormonální testy ukázaly zcela normální sekreční rezervu obou os, ale kostní denzita v páteři byla při antiresorpční léčbě a respektování zákazu kouření stále v mezích osteoporózy. Lze se tedy domnívat, že hypogonadismus spolu se sníženou funkcí osy somatotropin-IGF-I a DI nebyly jediným patogenetickým mechanismem při vzniku osteoporózy.
Je známo, že vedle body-mass indexu (BMI) a fyzické aktivity je silným prediktorem ztráty kostní hmoty a rizika fraktur u mužů kouření (22, 23). Mechanismus vlivu tabakismu na skelet není přesně znám. Uvažovalo se o útlumu produkce a metabolismu sexuálních steroidů. Avšak Kirbas et al. (24) nepotvrdili u kuřáků útlum hladin celkového testosteronu. Lorentzon et al. (25) na souboru více než 1000 mladých mužů dokonce zjistili, že kuřáci mají hladiny testosteronu vyšší než nekuřáci. Přesto jejich průřezová kostní denzita a šíře kortikalis (měřeno pomocí pQCT) byly významně nižší. Zdá se tedy, že ani u popisovaného případu nízká hladina testosteronu s kouřením nesouvisela. Mediátorem vlivu kouření na skelet mladého muže by mohla být hyperparatyreóza. Je však známo, že kuřáci mají hladinu PTH nižší než nekuřáci (26). Také náš pacient měl hladiny PTH v séru na dolní hranici normy, což vylučuje i vliv případné hypovitaminózy D, která může být u mladých mužů také příčinou osteoporózy a stresových fraktur (27).
Je prokázané, že nízká kostní hmota se při abstinenci kouření vrací k normě (28). Ale ani trvalá abstinence kouření u našeho pacienta nevedla k očekávanému zvýšení kostní denzity páteře. Bylo by možno uvažovat i o souvislosti s postižením plic. Je známo, že bronchitida jako chronický zánětlivý proces prostřednictvím cytokinů aktivuje kostní resorpci (29). V průběhu sledování pacienta však projevy bronchitidy zaznamenány nebyly.
U našeho pacienta byl zaznamenán nárůst kostní hmoty v páteři k hodnotám hraničícím s osteopenií teprve za 5 let po úpravě hladin testosteronu a IGF-I k normálním hodnotám. Přímou souvislost osteoporózy s histiocytózou se u tohoto případu prokázat nepodařilo. Lze tedy předpokládat, že klíčovým mechanismem závažné osteoporózy páteře je vliv interakce silného kuřáctví s nedostatečností několika hormonálních systémů v období, kdy dobíhá budování vrcholu kostní hmoty. Nelze vyloučit, že se na pomalém nárůstu kostní hmoty uplatňuje ještě vliv dalšího vnitřního faktoru, například genu nebo hormonu (30). Nízký vrchol kostní hmoty u mladého kuřáka s pozdějším rizikem fraktur však pravděpodobně zůstane jeho celoživotním handicapem.
Zkratky
BMI – body-mass index
DLCO – difuzní kapacita plic
FSH – folikuly stimulující hormon
LH – luteotropní hormon
SHBG – sexuální hormony vázající globulin
IGF-I – insulin like growth factor-I
PTH – parathormon
DI – diabetes insipidus
TSH – tyreotropin
T4 – tyroxin
T3 – trijodothyronin
TNF-alfa – tumor necrosis factor alpha
Práce byla podpořena grantem IGA NR/9055-4.
prof. MUDr. Ivanka Žofková, CSc.
Endokrinologický ústav
Národní 8, 116 94 Praha 1
e-mail: zofkova@endo.cz
Zdroje
1. Madeo, B., Zirilli, L., Caffagni, G. et al.: The osteoporotic male: overlooked and undermanaged? Clin. Interv. Aging, 2007, 2, s. 305–312.
2. Žofková, I.: Kvantitativní a kvalitativní parametry mužského skeletu ve vztahu k hormonální homeostáze. Osteologický bulletin, 2008, 13, s. 4–7.
3. Rucker, D., Ezzat, S., Diamandi, A. et al.: IGF-I and testosterone levels as predictors of bone mineral density in healthy, community-dwelling men. Clin. Endocrinol. (Oxf), 2004, 60, s. 491–499.
4. Marek J., Hána, V., Kršek, M.: Hypothalamické hypofunkční syndromy. In: Klener, P. et al.: Vnitřní lékařství, Praha, Galén, 2006, s. 903–904.
5. Ghirardello, S., Malattia, C, Scagnelli, P. et al.: Current perspective on the pathogenesis of central diabetes insipidus. J. Pediatr. Endocrinol. Metab., 2005, 18, s. 631–645.
6. Mikami-Terao, Y., Akiyama, M., Yanagisawa, T. et al.: Lymphocytic hypophysitis with central diabetes insipidus and subsequent hypopituitarism masking a suprasellar germinoma in a 13-year-old girl. Childs Nerv. Syst., 2006, 22, s. 1338–1343.
7. Hashimoto, K., Araba, K., Tamura, K. et al.: A case of lymphocytic infundibuloneurohypophysitis associated with systemic lupus erythematosus. Endocr. J., 2002, 49, s. 605–610.
8. Maghnie, M., Ghirardello, S., De Bellis, A. et al.: Idiopathic central diabetes insipidus in children and young adults is commonly associated with vasopressin-cell antibodies and markers of autoimmunity. Clin. Endocrinol. (Oxf), 2007, 65, s. 470–478.
9. Rush, W. L., Andriko, J. A., Galateau-Salle, F. et al.: Pulmonary patology of Erdheim-Chester disease. Mod. Pathol., 2000, 13, s. 747–754.
10. Shamburek, R. D., Brewer, H. B., Jr., Gochuico, B. R.: Erdheim-Chester disease: a rare multisystem histiocytic disorder associated with interstitial lung disease. Am. J. Med. Sci., 2001, 321, s. 66–75.
11. Maghnie, M., Cosi, G., Genovese, E. et al.: Central diabetes insipidus in children and young adults. N. Engl. J. Med., 2000, 343, s. 998–1007.
12. Stull, M.A., Kransdorf, M.J., Devaney, K.O.: Langershans cell histiocytosis of bone. Radiographics, 1992, 12, s. 801–823.
13. Per, H., Koc, K. R., Gümüs, H. et al.: Cervical eosinophilic granuloma and torticollis: a case report and review of the literature. J. Emerg. Med., 2008 (preprint).
14. Rosso, D. A., Ripoli, M. F., Roy, A. et al.: Serum levels of interleukin-1 agonist and tumor necrosis factor-alpha are elevated in children with Langerhans cell histiocytosis. J. Pediatr. Hematol. Oncol., 2003, 25, s. 480–483.
15. Meier, C., Nguyen, T. V., Handelsman, D. J. et al.: Endogenous sex hormones and incident fracture risk in older men: the Dubo Osteoporosis Epidemiology Study. Arch. Intern. Med., 2008, 168, s. 47–54.
16. Lorentzon, M., Swanson, C., Anderson, N. et al.: Free testosterone is a positive, whereas free estradiol is a negative, predictor of cortical bone size in young Swedish men: the GOOD study. J. Miner. Res., 2005, 20, s. 1334–1341.
17. Kuchuk, N. O., van Schoor N. M., Pluijm, S. M. et al.: The association of sex hormone levels with quantitative ultrasound, bone mineral density, bone turnover and osteoporotic fractures in older men and women. Clin. Endocrinol. (Oxf), 2007, 67, s. 295–303.
18. Lormeau, C., Soudan, B., d’Herbomez, M. et al.: Sex hormone-binding globulin, estradiol, and bone turnover markers in male osteoporosis. Bone, 2004, 34, s. 933–939.
19. Araujo, A. B., Travison, T. G., Leder, B. Z. et al.: Correlations between serum testosterone, estradiol, and sex hormone-binding globulin and bone mineral density in a diverse sample of men. J. Clin. Endocrinol. Metab., 2008, 93, s. 2135–2141.
20. Patel, M. B. R., Arden, N. K., Masterson, L. M. et al.: Investigating the role of the growth hormone-insulin-like growth factor (GH-IGF) axis as a determinant of male bone mineral density (BMD). Bone, 2005, 37, s. 833–841.
21. Elabd, S. K., Sabry, X., Hassan, W. B. et al.: Possible neuroendocrine role for oxytocin in bone remodeling. Endocr. Regul., 2007, 41, s. 131–141.
22. Bakhireva, L. N., Barrett-Connor, E., Kritz-Silverstein, D. et al.: Modifiable predictors of bone loss in older men: s prospective study. Am. J. Prev. Med., 2004, 26, s. 436–442.
23. Sharma, S., Fraser, M., Lovell, F, et al.: Characteristics of males over 50 years who present with a fracture: epidemiology and underlying risk factors. J. Bone Joint Surg. Br., 2008, 90, s. 72–77.
24. Kirbas, G., Abaky, A., Topcu, F. et al.: Obstructive slep apnoea, cigarette smoking and serum testosterone levels in a male sleep clinic cohort. J. Int. Med. Res., 2007, 35, s. 38–45.
25. Lorentzon, M., Mellström, D., Haug, E. et al.: Smoking is associated with lower bone mineral density and reduced cortical thickness in young men. J. Clin. Endocrinol. Metab., 2007, 92, s. 497–503.
26. Jorde, R., Saleh, F., Figenschau, Y. et al.: Serum parathyroid hormone (PTH) levels in smokers and non-smokers. The fifth Tromse study. Eur. J. Endocrinol., 2005, 152, s. 39–45.
27. Ruohola, J. P. Laaksi, I., Ylikomi, T. et al.: Association between serum 25(OH)D concentrations and bone stress fractures in Finnish young men. J. Bone Miner. Res., 2006, 21, s. 1483–1488.
28. Sneve, M., Emaus, N., Joakimsen R. M. et al.: The association between serum parathyroid hormone and bone mineral density, and the impact of smoking: the Tromso Study. Eur. J. Endocrinol., 2008, 158, s. 401–409.
29. Jorgensen, N. R., Schwarz, P.: Osteoporosis in chronic obstructive pulmonary disease patients. Curr. Opin. Pulm. Med., 2008, 14, s. 122–127.
30. Lorentzon, M, Landin, K, Mellström, D. et al.: Leptin is a negative independent predictor of areal BMD and cortical bone size in young adult Swedish men. J. Bone Miner. Res., 2006, 21, s. 1871–1878.
Štítky
Adiktologie Alergologie a imunologie Angiologie Audiologie a foniatrie Biochemie Dermatologie Dětská gastroenterologie Dětská chirurgie Dětská kardiologie Dětská neurologie Dětská otorinolaryngologie Dětská psychiatrie Dětská revmatologie Diabetologie Farmacie Chirurgie cévní Algeziologie Dentální hygienistka
Článek KNIHYČlánek Spolek lékařů v PlzniČlánek ABSTRAKTAČlánek Bochdalkův denČlánek LAUREÁTI NOBELOVY CENY
Článek vyšel v časopiseČasopis lékařů českých
Nejčtenější tento týden
- Jak a kdy u celiakie začíná reakce na lepek? Možnou odpověď poodkryla čerstvá kanadská studie
- Doc. Jitka Fricová: V USA nasazovali fentanyl poměrně nekriticky, v Česku je situace jiná
- U pacientů s traumatem je častěji dosaženo adekvátních hladin anti-Xa při dávkování enoxaparinu podle hmotnosti
- Sympozium věnované péči o pacienty s ALS jako odrazový můstek pro zlepšení kvality jejich života
- I mozek má svou krizi středního věku. Jak tyto změny souvisejí s rizikem demence ve stáří?
-
Všechny články tohoto čísla
- Galektiny v dlaždicových karcinomech hlavy a krku
- KNIHY
- Hiátová hernie a Barrettův ezophagus, četnost výskytu příznaků poruchy a komplikací
- Funkce eozinofilního granulocytu
- Sumoylizace v regulaci genové exprese
- Nejstarší pleiomorfní hormon – melatonin
- Dendritické buňky ve virové infekci
- Primárny B-bunkový non-Hodgkinov lymfóm Burkittovského typu: popis prípadu s typickými klinickými prejavy
- Spolek lékařů českých v Praze
- Patogeneticky komplikovaný případ osteoporózy u mladého muže
- Průvodní list k pitvě na soudním lékařství
- Z historie „jubilejního pavilonu“ v pražské všeobecné nemocnici
- Spolek lékařů v Plzni
- Racionalita a iracionalita v medicíně a v životě
- Udělení Cen předsednictva čLS JEP za nejlepší knižní publikace a odborné články v roce 2007
- ABSTRAKTA
- Bochdalkův den
- Zemřel doc. MUDr. Pavel Fiala, CSc.
- MVDr. Radslav Kinský 1928–2008
- LAUREÁTI NOBELOVY CENY
- Časopis lékařů českých
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Zemřel doc. MUDr. Pavel Fiala, CSc.
- Průvodní list k pitvě na soudním lékařství
- ABSTRAKTA
- Galektiny v dlaždicových karcinomech hlavy a krku
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: MUDr. Petr Výborný, CSc., FEBO
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



