-
Články
Top novinky
Reklama- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
Top novinky
Reklama- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Top novinky
ReklamaPerkutánní intervence chronického uzávěru koronární tepny – komu, kdy a proč
Percutaneous coronary intervention of chronic total occlusion – to whom, when and why
Chronic total occlusion is characterised by total discontinuation of a blood flow in coronary vessel present for at least three months. Typical finding involves filling of the distal arterial segments by collateral flow. Well developed collaterals usually provide sufficient supply to preserve myocardial viability, but frequently are not capable of preventing excercise ischemia in the occluded territory. Percutaneous intervention of a CTO is focused on ischemia reduction, improvement of excercise capacity and quality of life. A succesful recanalization of a CTO leads to an improvement of left ventricular systolic function. Patients presenting with acute coronary syndromes and a coincident CTO in non-infarct related artery show worse short and long-term outcomes as compared to patients without a CTO. Technolocigal and procedural evolvement over past decades with implementation of novel techniques used by experienced operators lead to a substantial succes rate imprevement with acceptable complications rate in contemporary CTO interventions.
Keywords:
percutaneous coronary intervention – chronic total occlusion – ischemia – viability
Autoři: Roman Štípal; Martin Poloczek; Marek Sůva; Petr Kala
Působiště autorů: Interní kardiologická klinika FN Brno a LF MU
Vyšlo v časopise: Vnitř Lék 2021; 67(E-4): 17-25
Kategorie: Přehledové články
Souhrn
Chronický uzávěr koronární tepny (CTO) je charakterizován jako úplné přerušení toku v koronární tepně trvající déle než 3 měsíce. Typickým nálezem v povodí CTO je plnění distálních segmentů tepny přes kolaterální řečiště. To mívá zpravidla dostatečnou kapacitu k zachování viability myokardu, ale většinou nedokáže zabránit zátěžové ischémii v okludované oblasti. Cílem perkutánní intervence CTO je snížení rozsahu ischemie myokardu, zlepšení funkční pracovní kapacity a kvality života, kdy úspěšná katetrizační rekanalizace CTO vede často i ke zlepšení systolické funkce levé komory. Pacienti s akutním koronárním syndromem a přítomným CTO v neinfarktovém povodí mají horší krátkodobou a dlouhodobá prognózu ve srovnání s pacienty bez CTO. Přístup k léčbě CTO se dramaticky změnil v posledních letech, kdy moderní postupy a techniky katetrizační rekanalizace CTO prodělaly dramatický vývoj. V současnosti má perkutánní koronární intervence CTO v rukou zkušených operatérů vysokou úspěšnost a přijatelnou míru rizika závažných komplikací.
Klíčová slova:
perkutánní koronární intervence – chronický kolateralizovaný uzávěr – ischemie – viabilita
Definice a epidemiologie
Chronický uzávěr koronární tepny (CTO – chronic total occlusion) je charakterizován jako úplné přerušení toku v koronární tepně trvající déle než 3 měsíce. Typickým nálezem je plnění distálních segmentů okludované tepny přes kolaterální řečiště. CTO jsou relativně častým nálezem a můžeme je pozorovat u přibližně 15–20 % katetrizovaných pacientů (1). U pacientů po bypassové operaci je pak CTO minimálně jedné koronární tepny přítomno ve více než v 90 % případů. Ve srovnání s pacienty s neokluzivním typem postižení koronárních tepen jsou pacienti s přítomným CTO obvykle starší, častěji se jedná o muže a mívají rizikovější profil – vyšší prevalenci diabetu (34 vs. 26 %), hypertenze (75 vs. 68 %), hyperlipidemie (82 vs. 78 %), ischemické choroby dolních končetin (8 vs. 4 %), častěji jsou kuřáci (33 vs. 24 %) a častěji mají anamnézu infarktu myokardu (40 % vs. 23 %) (2,3). Patofyziologickým mechanismem vzniku CTO je většinou postupná dlouhodobá stenotizace lumen koronární tepny, která umožňuje rozvoj kolaterálního řečiště. U části pacientů je CTO důsledkem nediagnostikovaného či neléčeného akutního trombotického uzávěru koronární tepny. V takových případech bývá doprovázeno segmentárními poruchami kinetiky myokardu a mohou být přítomné i patologické Q vlny na elektrokardiogramu (Obr. 1). Většina pacientů s CTO nicméně nemá anamnézu předchozího infarktu myokardu. Zejména u nemocných bez anamnézy infarktu má vyvinutí kolaterálního řečiště zásadní protektivní vliv na zachování viability myokardu (Obr. 2) a do jisté míry i omezení ischemie v okludované oblasti. Chronický uzávěr tepny se zachovanou kinetikou levé komory při absenci typických symptomů je tak poměrně častým nálezem (4).
Obr. 1. CTO ramus interventricularis anterior (RIA); vlevo nahoře angiografie, ostiální uzávěr RIA, nahoře uprostřed akineza přední stěny a hrotu levé komory při levostranné ventrikulografii (červené šipky); vpravo nahoře EKG s patologickými Q kmity v oblasti přední stěny srdeční (zelené šipky); dole snímky z magnetické rezonance s bíle vyznačeným převážně transmurálním postižením dané oblasti v LGE sekvenci (modré šipky) – CTO nevhodné k intervenci 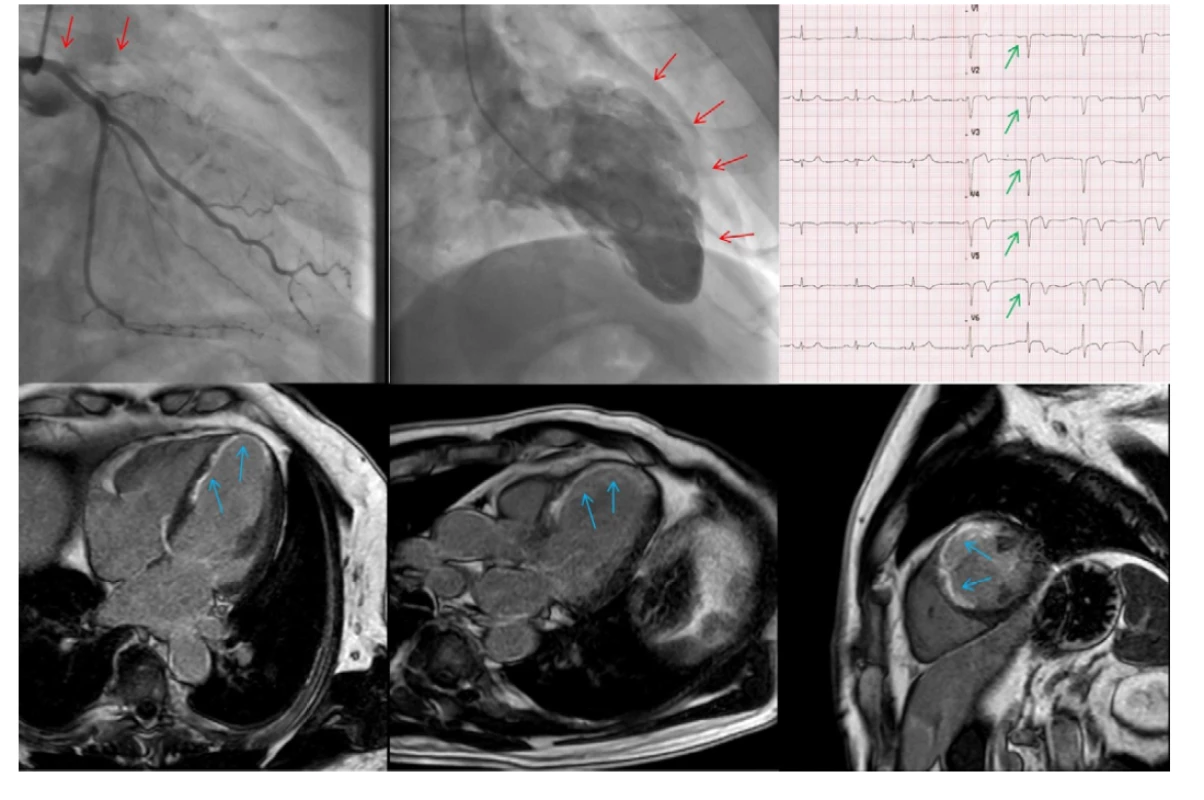
Klinický obraz
Přibližně jedna čtvrtina pacientů s CTO nemívá typické symptomy (5). Nicméně bolest na hrudníku je v obecné rovině relativně pozdním projevem v ischemické kaskádě a její absence nevylučuje přechodnou přítomnost i těžkého stupně myokardiální ischemie (6). Obdobně jako u neokluzivní formy ischemické choroby je nižší prevalence typických symptomů výraznější u populace pacientů s diabetem, která je v rámci kohorty nemocných s přítomným CTO široce zastoupena. U symptomatických pacientů pak bývají oproti typickým stenokardiím častěji vyjádřeny potíže jako námahová dušnost, nevýkonnost, únava či palpitace při arytmiích (3, 7). Přítomnost CTO má často také významný arytmogenní potenciál a za určitých okolností zvyšuje vulnerabilitu myokardu a četnost maligních arytmií (8). Pacienti s přítomným CTO a implantovaným kardiovertrem – defibrilátorem v primární či sekundární prevenci náhlé srdeční smrti mají vyšší četnost adekvátních výbojů pro maligní arytmie ve srovnání s pacienty s ischemickou chorobou srdeční bez přítomného CTO (9).
Význam a indikace perkutánní intervence CTO
Rozvinuté kolaterální řečiště mívá zpravidla dostatečnou kapacitu k zachování viability myokardu, ale vzhledem k obvyklému distálnímu perfúznímu tlaku kolem 30–40 mmHg většinou nemá dostatečnou kapacitu k zabránění zátěžové ischemie v okludované oblasti. Tyto poznatky nám umožnilo osvětlit několik intervenčních studií zaměřených na koronární fyziologii chronických uzávěrů. Ve studiích s využitím metody měření frakční průtokové rezervy (fractional flow reserve – FFR) distálně od tepenného uzávěru vykazovaly tato měření u více než tří čtvrtin pacientů hodnoty odpovídající klidové, tedy trvalé ischémii (Pd/Pa ≤ 0,80) (10). Ve studii obdobným způsobem využívající metodu měření iFR (instantaneous wave-free ratio) v distálním segmentu okludované tepny vykazovali pacienti s regionálními poruchami kinetiky levé komory hodnoty odpovídající těžšímu stupni ischemie oproti těm bez segmentárních poruch kinetiky. Nicméně i ve skupině pacientů bez regionálních poruch kinetiky byly běžně zaznamenány hodnoty výrazně pod cut-off hranicí (iFR ≤ 0,89) pro detekci ischemie (0,24 (0,18; 0,35) vs. 0,38 (0,28; 0,45), p = 0,013). V obou skupinách nemocných pak došlo k okamžitému efektu normalizace hodnot (tedy odstranění ischemických poměrů) bezprostředně po rekanalizačním zákroku (11).
Benefity revaskularizace chronických uzávěrů u pacientů se stabilní ischemickou chorobou srdeční
Jak bylo zmíněno, cílem perkutánní intervence CTO je snížení rozsahu ischemie myokardu, zlepšení funkční pracovní kapacity a kvality života. V tomto ohledu máme k dispozici data z několika randomizovaných studií. Studie EURO-CTO ukázala zlepšení funkčních zátěžových parametrů, zlepšení kvality života i ústup anginy pectoris v intervenční větvi (12). Studie IMPACTOR-CTO hodnotící pouze pacienty s uzávěrem pravé věnčité tepny prokázala kromě zlepšení symptomů i jednoznačný pokles rozsahu myokardiální ischemie v hodnocení pomocí adenosinové zátěžové magnetické rezonance (13). Podobně jako ve studii DECISION-CTO (14) se však nepodařilo prokázat přímý vliv CTO intervence na prognostické ukazatele. To však není překvapivé, neboť většina PCI u pacientů s onemocněním jedné tepny je, s výjimkou prognosticky závažného postižení proximální části ramus interventricularis anterior, zaměřeno na zlepšení symptomů a kvality života (Tab. 1) (15, 23). I přesto, že randomizovaná data, která by potvrzovala přímý vliv CTO intervence na dlouhodobou prognózu, dosud chybějí, máme k dispozici celou řadu dat z mezinárodních multicentrických registrů (16–20), ze kterých lze pozorovat zřetelný trend ke zlepšení prognózy po úspěšné PCI chronického uzávěru. Neméně důležité je však také narůstající množství důkazů, že dosažení kompletní revaskularizace zahrnující intervenci CTO vede ke zlepšení systolické funkce levé komory (21). Prediktorem významného zlepšení regionální i celkové systolické funkce levé komory je však přítomnost viabilního myokardu v okludované oblasti a bez jejího průkazu je přínos revaskularizace sporný (22).
Tab. 1. CTO PCI v recentních evropských a amerických guidelines 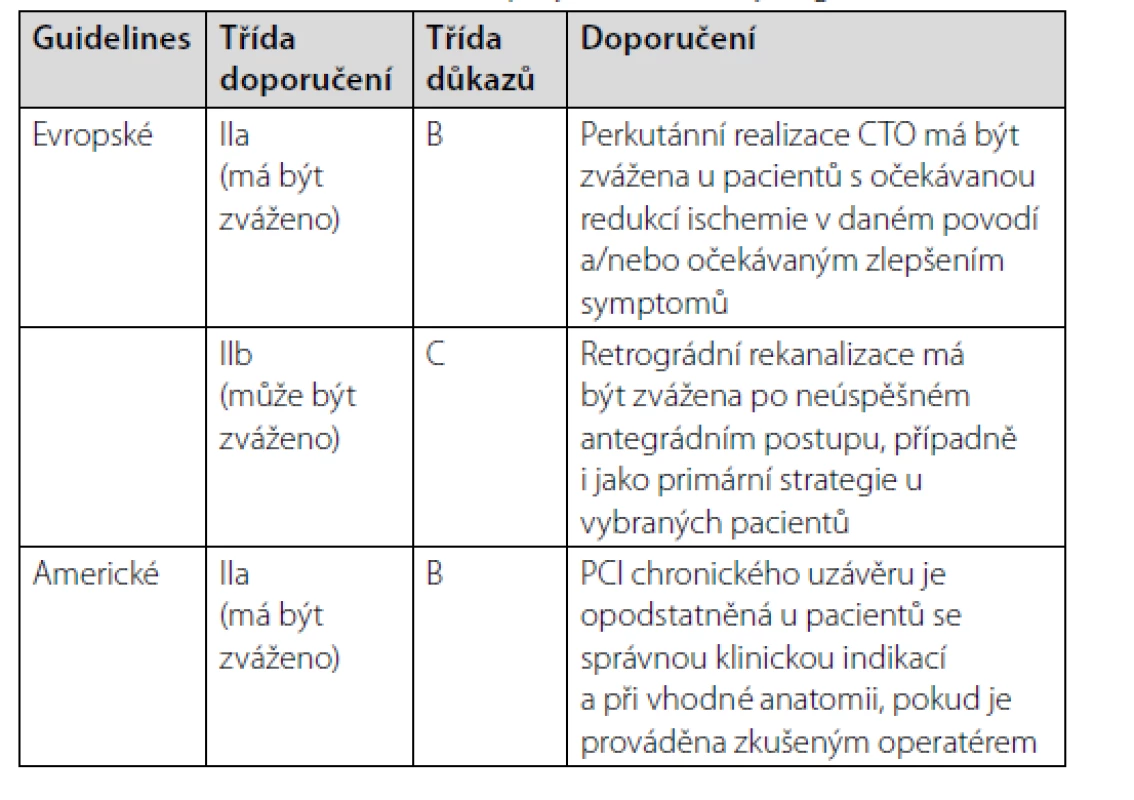
Význam CTO u pacientů s akutním koronárním syndromem
Pacienti s akutním koronárním syndromem a přítomným CTO v neinfarktovém povodí vykazují zhoršenou krátkodobou i dlouhodobou prognózu ve srovnání s pacienty bez CTO, a to obdobně v případě STEMI i non-STEMI (24, 25). CTO neinfarktové tepny je přítomno přibližně u 10 % pacientů se STEMI. Vliv na zhoršenou prognózu těchto nemocných je zejména vyjádřen v případě, kdy je chronicky okludované povodí kolaterálně zásobeno akutně uzavřenou „infarktovou“ tepnou. Tento fenomén „dvojího ohrožení“ je způsoben současnou ischémií ve dvou koronárních povodích, které jsou závislé na dostatečném průtoku infarktovou tepnou (26, 27). Na otázku vhodnosti rekanalizace CTO u pacientů s akutním srdečním infarktem se pokusila odpovědět randomizovaná nezaslepená studie EXPLORE, která hodnotila přeživší pacienty se STEMI a současným CTO v jiném povodí. Po primární intervenci infarktové tepny byli pacienti randomizováni ke konzervativnímu postupu nebo intervenční léčbě. Studie neprokázala významný rozdíl v primárním sledovaném ukazateli, kterým byla systolická funkce levé komory po čtyřech měsících. V hodnocení studie je nicméně potřeba uvážit některé limitace, kterými jsou například relativně nízká úspěšnost rekanalizačních zákroků (73 %), vyloučení pacientů v kardiogenním šoku, a chybějící testování subjektů na průkaz a rozsah myokardiální ischemie (28).
Symptomy, ischemie a viabilita – selekce vhodných kandidátů CTO intervence
Indikace k revaskularizaci se u pacientů s přítomným CTO řídí obdobnými pravidly, jako v případě stabilní ischemické choroby srdeční obecně – tedy dle přítomných symptomů, rozsahu myokardiální ischemie a viability (Graf 1) (30). Pacienti s CTO mívají častěji atypické potíže, zpravidla dominuje dušnost či zhoršená fyzická výkonnost namísto typických projevů anginy pectoris (5). Při nejasném klinickém obraze je vhodné symptomy objektivizovat zátěžovým testem. Normální systolická funkce levé komory nebo přítomnost lokální hypokinezy bez přítomnosti akinetického okrsku myokardu ze své definice vylučuje aviabilní povodí. V tom případě se další došetření soustředí především na průkaz a rozsah myokardiální ischemie. Dle současných guidelines je CTO revaskularizace indikována i při absenci typických symptomů, pokud rozsah myokardiální ischemie postihuje více než 10 % masy myokardu levé komory (15). Toto doporučení je založeno na mnoha poznatcích z observačních studií, ve kterých lze pozorovat trend ke zlepšené prognóze po úspěšné revaskularizaci u obecné populace pacientů s ischemickou chorobu srdeční a současně velkým rozsahem ischemie (Obr. 2) (29).
Graf 1. Vyšetřovací algoritmus u pacienta s CTO – indikace revaskularizace na základě symptomů, rozsahu ischemie a přítomnosti viability myokardu Pozn.: převzato z Galassi AR et al., Eur Heart J 2016; 37(35): 2692–2700 (30) 
Obr. 2. CTO ramus interventricularis anterior (RIA); vlevo nahoře a uprostřed chronický uzávěr RIA s epikardiálním kolaterálním plněním z ramus circumflexus (červené šipky); vpravo nahoře ventrikulogram se zachovanou kinetikou přední stěny levé komory a ejekční frakcí 53 %; dole snímky z magnetické rezonance potvrzující zachovanou kinetiku levé komory se subendokardiální ischémií v dané oblasti, vpravo dole pak absence sycení myokardu v LGE sekvenci – viabilní oblast přední stěny (modré šipky) – CTO indikované k intervenci 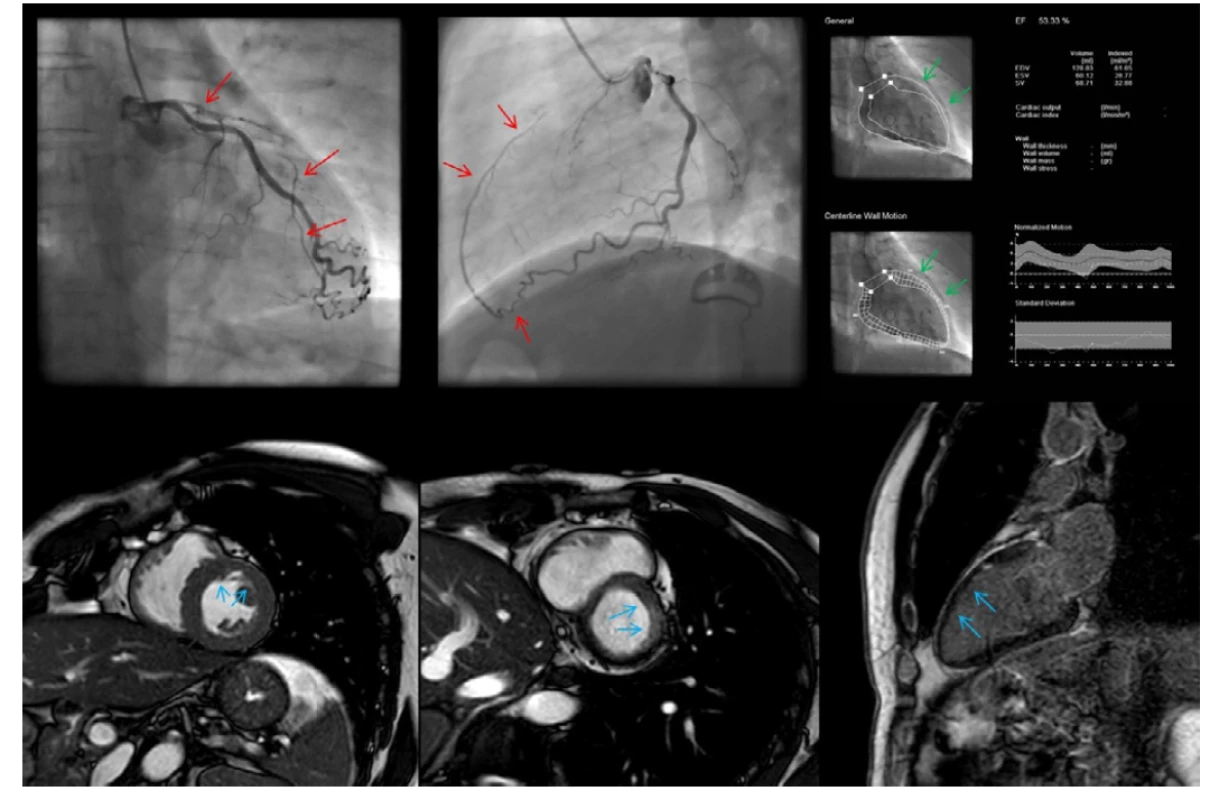
Naopak, v případě rozsáhlé lokální akinezy v okludované oblasti je došetření zaměřeno především na detekci viabilního myokardu. Bez přítomnosti významné masy viabilního myokardu nelze očekávat zlepšení systolické funkce levé komory a případná intervence v takovém případě není indikována (Obr. 1) (22). Predikce viability myokardu na základě angiograficky zobrazené přítomnosti kolaterálního řečiště a jeho kvality je často nepřesná a při indikaci případné intervence CTO je nutný průkaz viabilního povodí některou z neinvazivních zobrazovacích metod (30, 31).
V hodnocení zátěžové ischemie a viability myokardu lze využít dobutaminové echokardiografie či metod nukleární medicíny (SPECT – single photon emission computed tomography, PET – positron emission tomography) (32, 33), stále častěji se však v této oblasti využívá zátěžová magnetická rezonance srdce (CMR – cardiac magnetic resonance), která má excelentní prostorovou rozlišovací schopnost. Zároveň, na rozdíl od nukleárních metod, není CMR provázena přídatnou radiační zátěží a oproti dobutaminové echokardiografii má v hodnocení viability vyšší senzitivitu (34). Současně je magnetická rezonance považována za zlatý standard v hodnocení rozměrů a systolické funkce levé komory. V posledních letech se v hodnocení ischemie a viability uplatňuje zejména zobrazení s navozením farmakologické zátěže kontinuálním podáním adenosinu a následnou aplikací gadoliniové kontrastní látky (posouzení perfúze při prvním průchodu kontrastní látky a hodnocení viability pomocí analýzy pozdního sycení myokardu (LGE – late gadolinium enhancement). Tato metoda umožňuje mimo jiné i přesnou kvantifikaci myokardiální perfúzní rezervy. Recentní monocentrická prospektivní studie demonstrovala, že úspěšná rekanalizace CTO u pacientů s prokázanou významnou zátěžovou ischémií a zachovanou viabilitou při CMR vedla k normalizaci myokardiální perfúze, signifikantnímu zlepšení systolické funkce a poklesu enddiastolického rozměru levé komory po třech měsících (35). Tyto nálezy později prokázala i výše zmíněná randomizovaná studie IMPACTOR-CTO, která se zaměřila pouze na pacienty s chronickým uzávěrem pravé věnčité tepny a jinak nevýznamným koronárním nálezem. Pomocí zátěžové magnetické rezonance se zde rovněž podařilo prokázat normalizaci myokardiální perfúze korelující s ústupem symptomů při kontrolní vyšetření po 12 měsících (13). Alternativní vyšetřovací metodou je CMR s kontinuálním podáním dobutaminu, a to ve vysoké dávce k hodnocení ischemie a v nízké dávce k hodnocení viability (36). Významný vhled do problematiky optimální selekce a indikace intervence u pacientů s CTO s použitím adenosinové či dobutaminové magnetické rezonance by měla přinést právě probíhající studie CARISMA-CTO (37).
Přehled základních technik rekanalizace CTO, princip hybridního algoritmu
Obecné klinické indikace k revaskularizaci jsou v případě PCI doplněny o skórovací systémy hodnotící obtížnost a tedy i pravděpodobnost úspěchu případné intervence. Nejčastěji používaným skórovacím systémem je J-CTO, který vychází z japonského multicentrického registru (Japanese Multicenter CTO registry) (20). Skóre zahrnuje pět nezávislých atributů obtížnosti léze (nejasný charakter proximálního konce uzávěru – „cap“, délka uzávěru nad 20 mm, přítomnost kalcifikací, přítomný ohyb v okludovaném segmentu tepny a opakovaný pokus o rekanalizaci) a dle jejich přítomnosti je pak CTO léze hodnocena na škále od 0–5 bodů jako snadná (0 bodů) (Obr. 3), středně obtížná (1 bod), obtížná (2 body) a velmi obtížná (3 a více bodů) (Obr. 4).
Obr. 3. CTO ramus interventricularis anterior (RIA) – uzávěr má délku pod 20 mm, je zřejmá proximální „cap“ uzávěru (červená šipka) a nejsou přítomny zjevné kalcifikace (J-CTO 0); distální a střední segment RIA (zelená šipka) se plní přes septální kolaterály z pravé věnčité tepny (modré šipky) 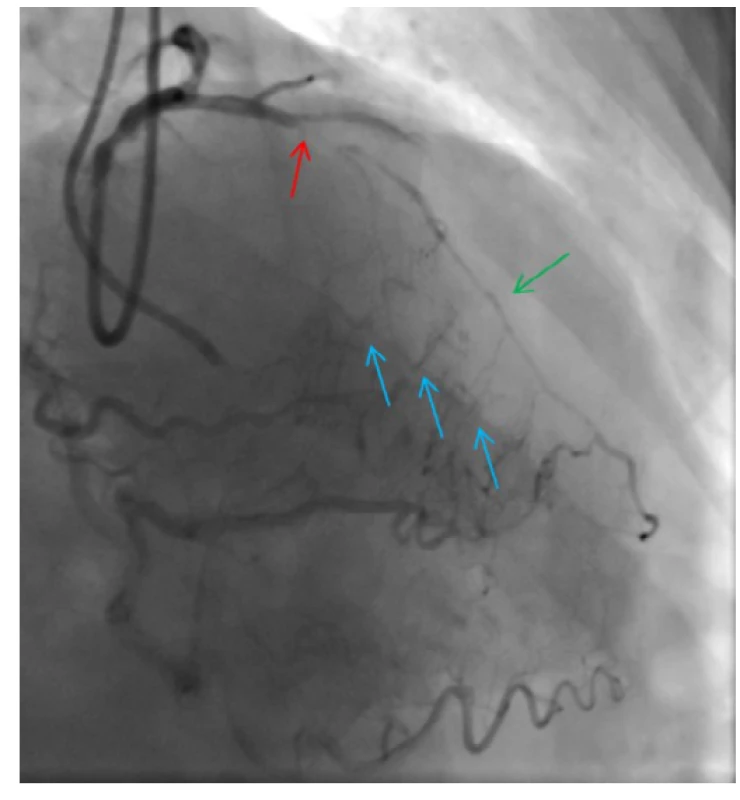
Obr. 4. CTO arteria coronaria dextra (ACD) – komplexní nález u pacienta s uzavřeným žilním bypassem na distální segment ACD; velmi dlouhý uzávěr s přítomnými kalcifikacemi a tortuozitami v průběhu uzávěru (J-CTO 3); patrná proximální „cap“ uzávěru a náznak reziduálního lumen s následným dalším uzávěrem ve střední části tepny (červené šipky), distální segmenty se plní z kolaterál z levé věnčité tepny (zelené šipky) 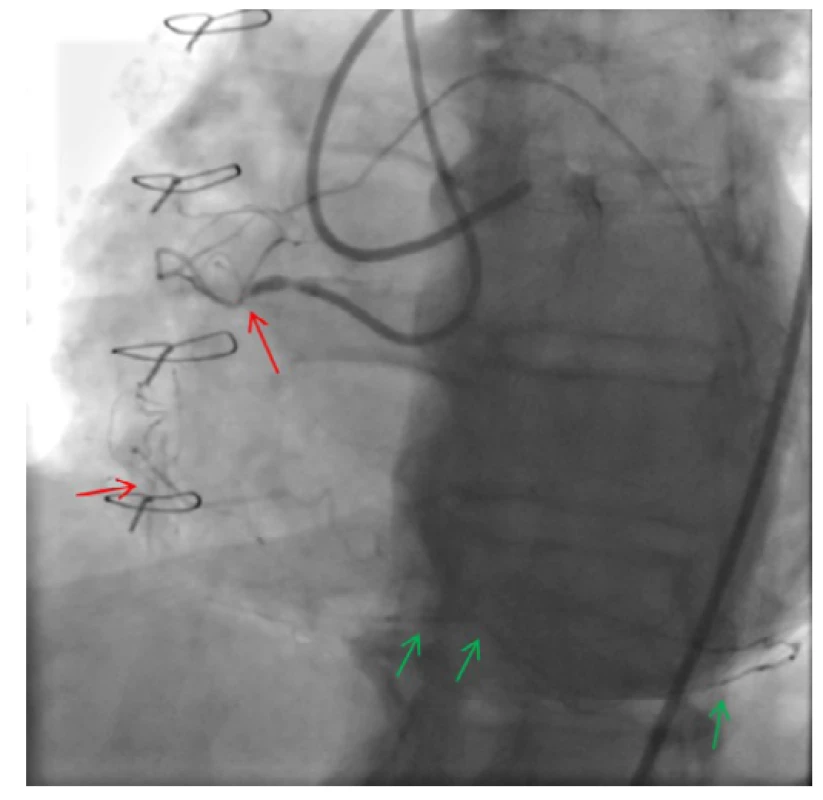
Techniky katetrizační rekanalizace prodělaly v posledních dvou dekádách dramatický vývoj a úspěšnost PCI chronických uzávěrů se v rukou zkušených operatérů dostala na úroveň 90 % při současném snížení frekvence závažných komplikací pod 3 % (31). Toto bylo umožněno mimo jiné i zásadním technologickým vývojem v oblasti speciálních rekanalizačních vodičů, mikrokatétrů, zaváděcích katétrů a jejich extenzí a v neposlední řadě intravaskulárních zobrazovacích metod (v případě CTO intervencí se jedná majoritně o intravaskulární ultrazvuk (IVUS)). Při intervenci je zpravidla využíván tzv. duální přístup se zavedením dvou vodících katétrů do ústí obou věnčitých tepen a to nejčastěji radiální a femorální cestou, případně bifemorálně či biradiálně. Intubace ústí obou věnčitých tepen umožňuje jednak současné zobrazení prográdního i retrográdního plnění tepny (tzv. „duální nástřik“), současně také nabízí možnost retrográdního postupu při samotné intervenci. V principu existují čtyři základní způsoby rekanalizace tepny. Lze postupovat tzv. antegrádně, tedy ve směru toku krve okludovanou tepnou, nebo naopak retrográdně přes kolaterální řečiště s následným průchodem uzávěrem z distální do proximální části artérie. Antegrádní přístup bývá využíván ve více než ¾ případů, retrográdní výkony jsou zpravidla rezervovány pro komplexnější anatomie (38, 39). Při retrográdním postupu jsou jednoznačně preferovány kolaterály septální. Průchod epikardiálními kolaterálami je také možný, nicméně jejich využití by mělo být vždy zvažováno jako rezervní strategie při selhání ostatních postupů a jen velmi zkušenými operatéry, neboť je spojena s vyšší četností komplikací, a to zejména s rizikem perikardiální tamponády (40).
V současnosti je využíván koncept tzv. „hybridního algoritmu“ (41), který byl poprvé představen v roce 2012 a který je založen na zevrubné analýze charakteru uzávěru na základě čtyř hlavních anatomických charakteristik (1. charakter proximální „cap“ uzávěru, 2. délka léze, 3. kvalita distálního segmentu tepny za uzávěrem a 4. přítomnost „intervenčních kolaterál“) s následným stanovením preferované primární, sekundární, případně terciární rekanalizační strategie. Vzhledem k takto přesně stanovenému plánu je možné jednotlivé postupy poměrně rychle střídat a tato strategie se ukazuje jako vysoce efektivní. Perkutánní intervence CTO lézí jsou oproti non-CTO PCI provázeny větší radiační zátěží a vyšší průměrnou spotřebou kontrastní látky a její indikace tak musí být vždy pečlivě a individuálně zvážena. Při správném provedení a dodržení doporučených postupů se nicméně jedná o bezpečnou a efektivní proceduru s nepochybným klinickým benefitem pro značnou skupinu nemocných. Četnost elektivních komplexních CTO intervencí se ve vysoce specializovaných centrech pohybuje mezi 5–10 % z celkového počtu provedených PCI. Pacienti po úspěšné intervenci s implantací lékových stentů (drug eluting stent – DES) užívají standardní duální protidestičkovou léčbu. Neexistují jednoznačná „CTO specifická“ doporučení ohledně délky jejího trvání, nicméně s ohledem na komplexitu léze, délku stentovaného úseku a zejména při využití technik spojených s disekcí a reentry tepny je obvykle doporučováno její ponechání v délce minimálně 12 měsíců, případně i déle. Doporučení se však stanovují případ od případu po pečlivém individuálním zvážení trombotického a krvácivého rizika u konkrétního pacienta.
Ukázka z praxe – retrográdní rekanalizace pravé věnčité tepny
Jako příklad úspěšného rekanalizačního zákroku uvádíme kazuistiku retrográdní rekanalizace arteria coronaria dextra (ACD) technikou reverse - -CART (controlled antegrade-retrograde tracking) u 34letého muže, kuřáka s hypertenzí, hyperlipidemií a rodinnou anamnézou kardiovaskulárního onemocnění. CTO pravé věnčité tepny byla vedlejším zjištěním při urgentní katetrizaci pro akutní srdeční infarkt bez ST-elevací v oblasti přední stěny srdeční a po ošetření kritické léze RIA pomocí PCI s implantací lékového stentu byl indikován elektivní katetrizační zákrok v povodí ACD v odstupu tří měsíců. Na obrázcích 5 a 6 je patrný „duální nástřik“ obou koronárních tepen zaváděcími katétry uloženými v ústích pravé a levé věnčité tepny. Zaváděcím katétrem v levé věnčité tepně bylo proniknuto koronárním rekanalizačním vodičem a tenkým mikrokatétrem cestou ramus interventricularis anterior do septální kolaterály a touto cestou dále do ramus interventricularis posterior pravé věnčité tepny (Obr. 7). Po průniku do místa uzávěru v pravé věnčité tepně byl druhý koronární rekanalizační vodič zaveden také antegrádně cestou vodicího katétru v pravé věnčité tepně. Po antegrádně zavedeném vodiči byl do místa uzávěru dále dopraven balonkový katétr, který po jeho insuflaci a následné desuflaci (Obr. 8) umožnil retrográdně zavedenému vodiči proniknout uzávěrem do lumen proximální části pravé věnčité tepny. Dále byl tímto retrográdně zavedeným vodičem nasondován zaváděcí katétr v pravé věnčité tepně, což po výměně vodiče za speciální dlouhý vodič o délce 330 centimetrů umožnilo takto retrográdně zavedený vodič přes zaváděcí katétr v ústí levé věnčité tepny vyvést katétrem v ústí pravé věnčité tepny (tzv. „externalizace vodiče“) (Obr. 9). Další postup již probíhá standardní prográdní cestou a po důsledné predilataci léze dalšími balonkovými katétry (Obr. 10) byly postupně implantovány tři lékové stenty s jejich následnou vysokotlakou postdilatací a dosažením optimálního výsledku PCI (Obr. 11 a 12).
Obr. 5. Vizualizace okludované pravé věnčité tepny (ACD) duálním nástřikem zaváděcími katétry v ústích obou věnčitých tepen (modré šipky); oblast chronického uzávěru ACD s přemosťujícími (tzv. „bridging“) kolaterálami (červená šipka); kolaterálně plněné periferní segmenty ACD, ramus interventricularis posterior (RIVP) a ramus posterolateralis dexter (RPLD) (zelené šipky) 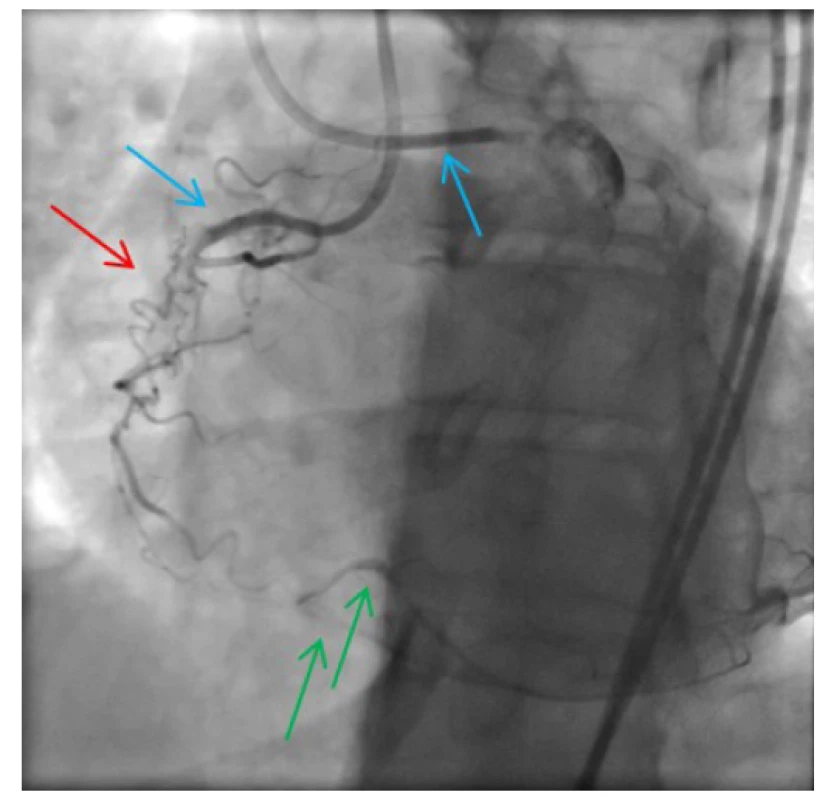
Obr. 6. Duální nástřik; oblast chronického uzávěru ACD s přemosťujícími (tzv. „bridging“) kolaterálami (červená šipka); kolaterálně plněné periferní segmenty ACD, ramus interventricularis posterior (RIVP) a ramus posterolateralis dexter (RPLD) (zelené šipky); septální kolaterály z RIA k RIVP (modré šipky) 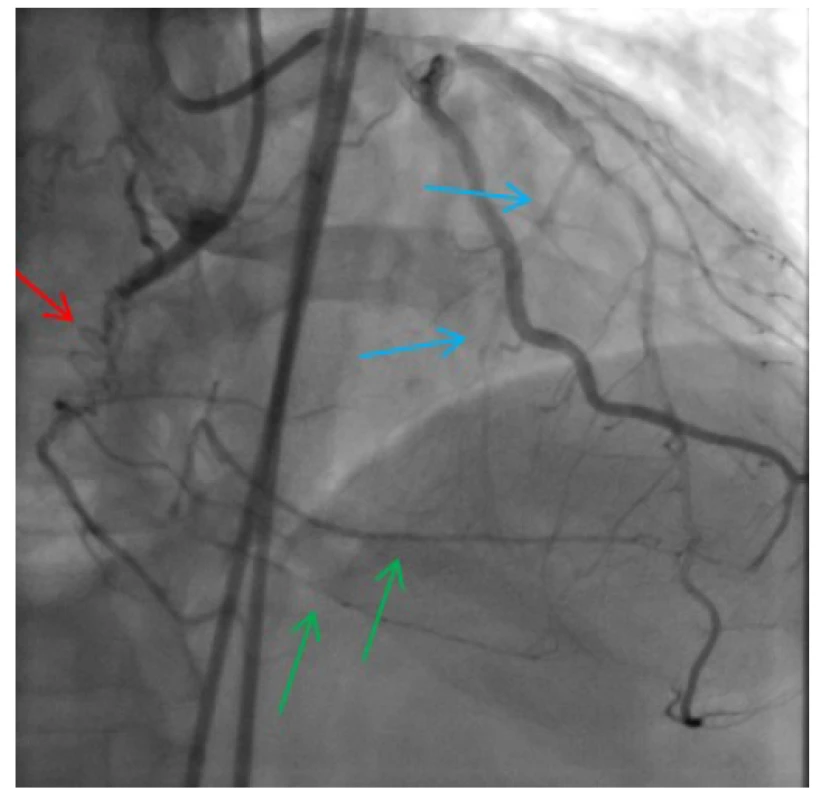
Obr. 7. Oblast chronického uzávěru ACD s přemosťujícími (tzv. „bridging“) kolaterálami (červená šipka); mikrokatétr retrográdně zavedený přes septální kolaterálu do distální části ACD (modrá šipka); nástřik kontrastní látky přes mikrokatétr umožňující vizualizaci distální části ACD (zelená šipka) 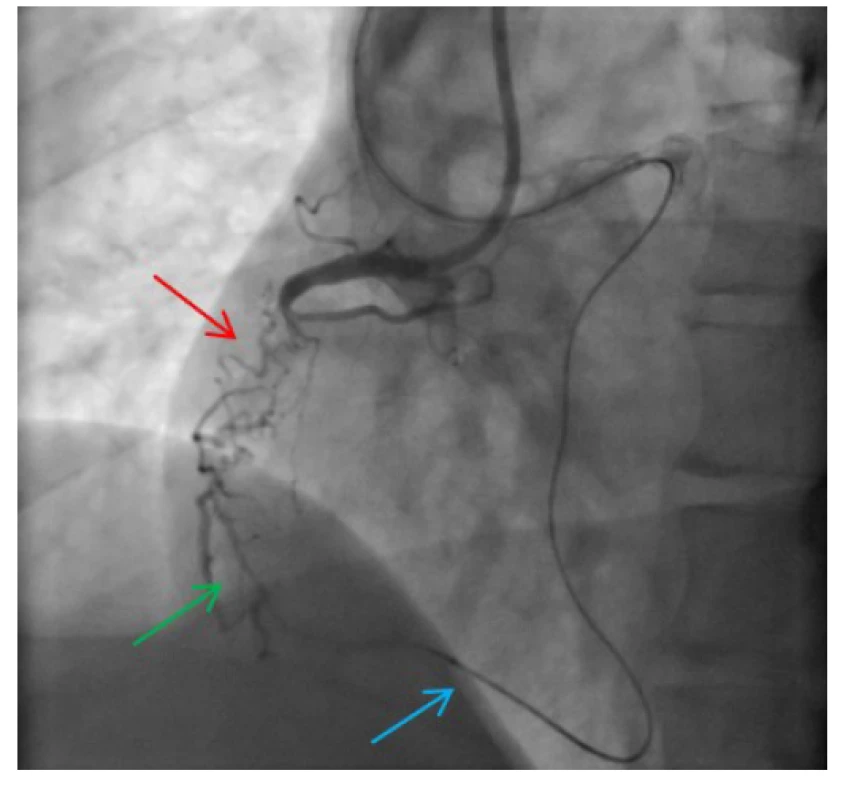
Obr. 8. Antegrádně zavedený vodič do oblasti uzávěru (zelená šipka); antegrádně zavedený balonkový katétr (modrá šipka); retrográdně zavedený rekanalizační vodič, který po desuflaci balonkového katétru proniká do lumen v proximální části ACD 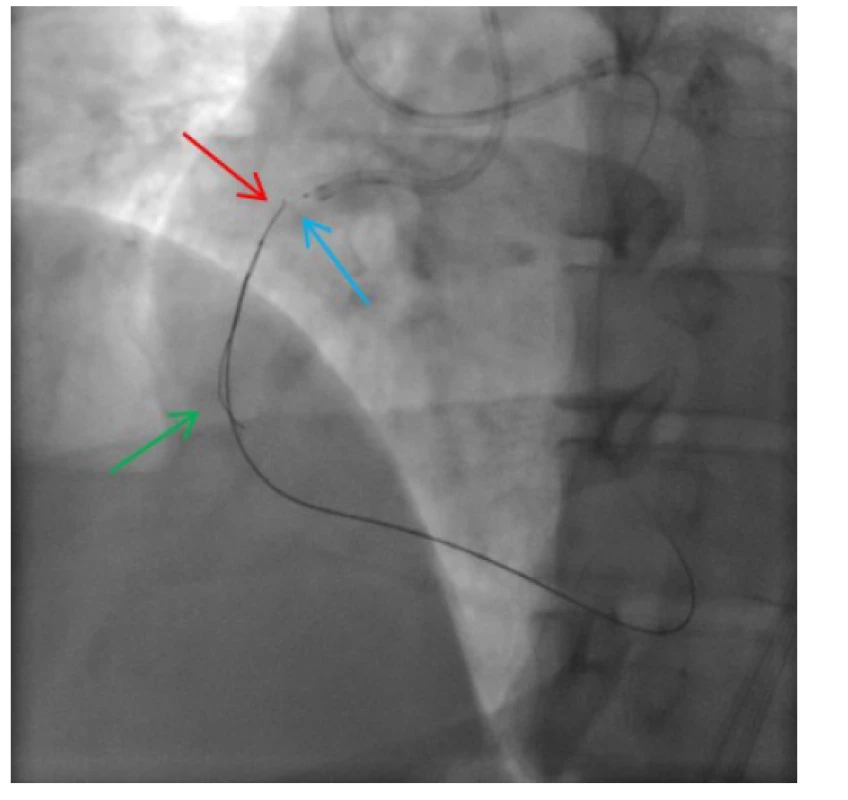
Obr. 9. Retrográdně zavedený prodloužený „externalizační“ vodič cestou septální kolaterály z levé do pravé věnčité tepny, kontrastní konec vodiče již vyveden do zaváděcího katétru v pravé věnčité tepně 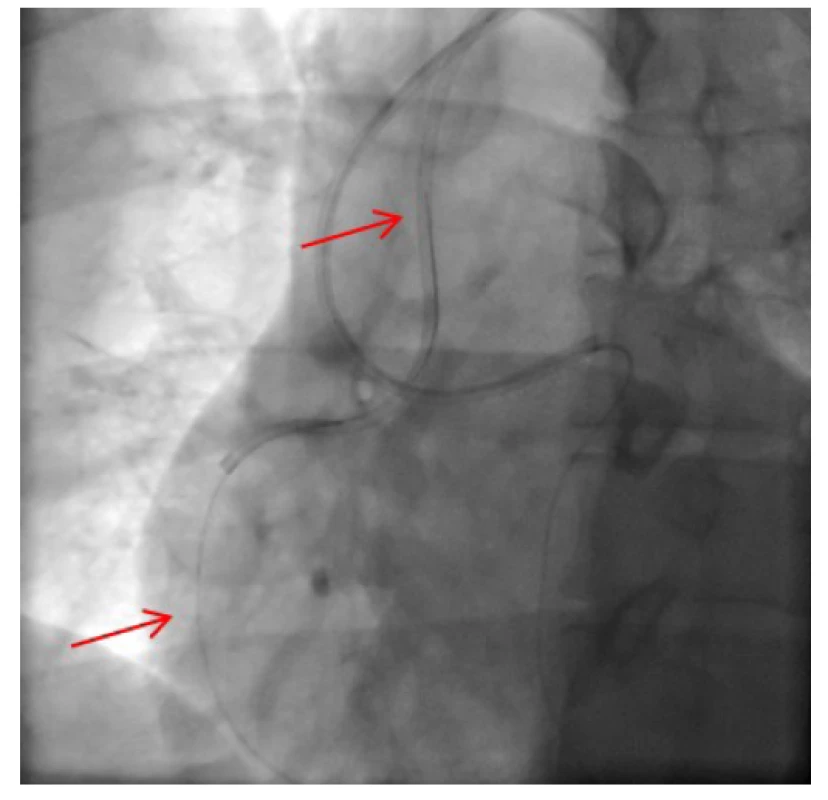
Obr. 10. Antegrádně zavedený a insuflovaný predilatační balónkový katétr v místě původního uzávěru 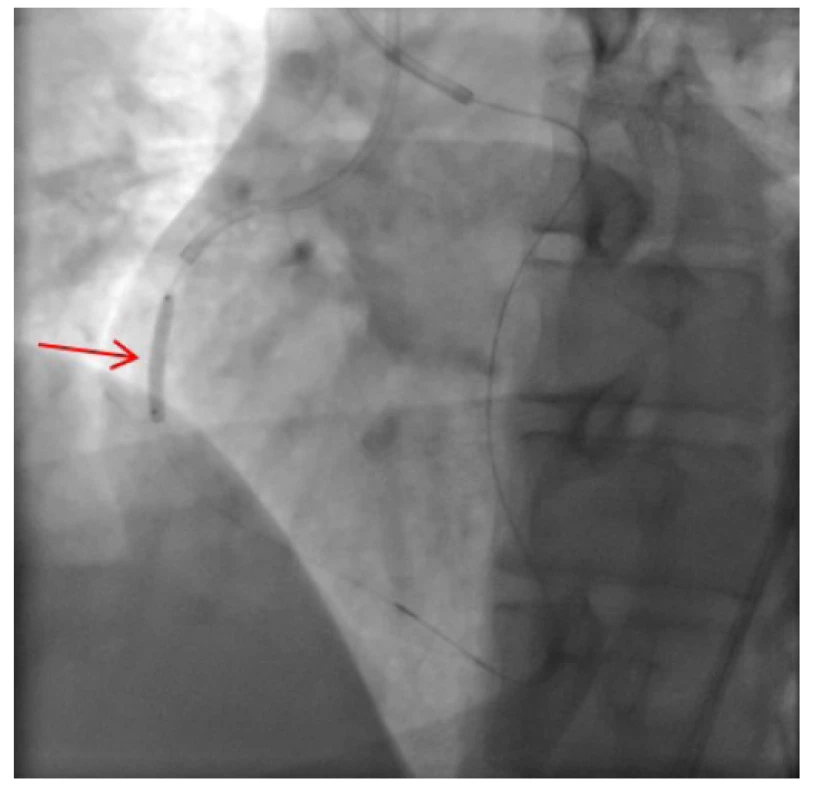
Obr. 11. Implantace lékového koronárního stentu do střední části pravé věnčité tepny, šipky ukazují pozici tří postupně implantovaných stentů 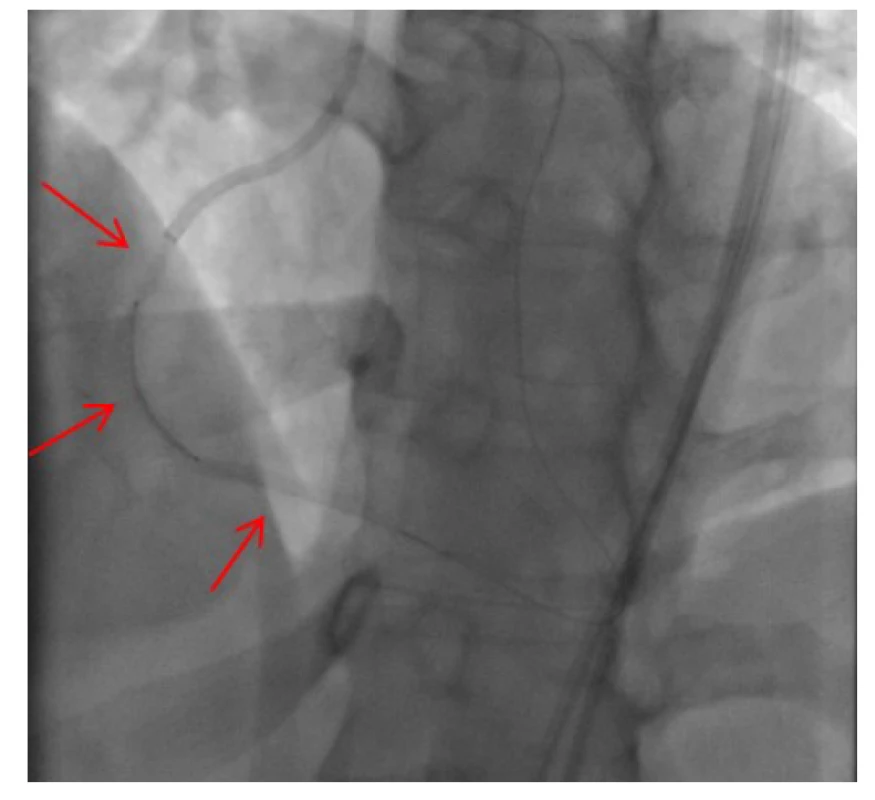
Obr. 12. Finální výsledek po implantaci a následné vysokotlaké postdilataci tří lékových stentů 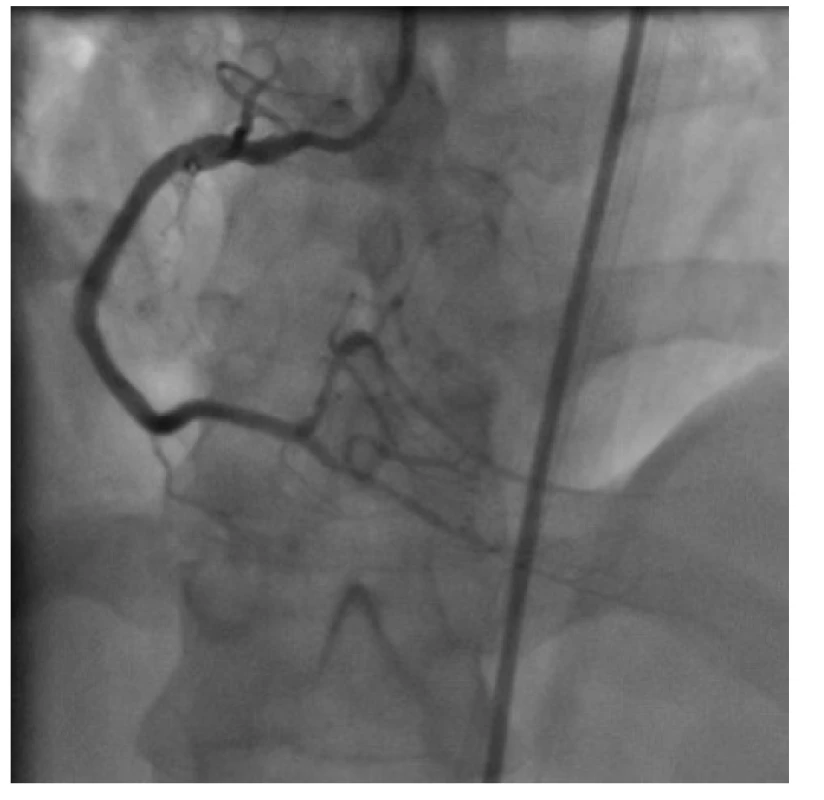
Závěr
Chronické uzávěry věnčitých tepen jsou v populaci pacientů s ischemickou chorobou srdeční častým nálezem a perkutánní koronární intervence ve specializovaných centrech je efektivní, bezpečnou a stále častěji indikovanou léčebnou metodou vedoucí k odstranění myokardiální ischemie, zlepšení kvality života a potenciálně ke zlepšení prognózy nemocných.
KORESPONDENČNÍ ADRESA AUTORA:
MUDr. Roman Štípal, Ph.D.
Pracoviště invazivní a intervenční kardiologie, Interní kardiologická klinika, Fakultní nemocnice Brno
Jihlavská 20, 625 00 Brno
Článek přijat redakcí: 9. 2. 2021
Článek přijat po recenzích k publikaci: 3. 6. 2021
Zdroje
1. Azzalini L, Jolicoeur EM, Pighi M et al. Epidemiology, Management Strategies, and Outcomes of Patients With Chronic Total Coronary Occlusion. Am J Cardiol 2016; 118 : 1128–35.
2. Fefer P, Knudtson ML, Cheema AN et al. Current perspectives on coronary chronic total occlusions: the Canadian Multicenter Chronic Total Occlusions Registry. J Am Coll Cardiol. 2012; 59(11): 991–997. doi:10.1016/j.jacc.2011.12.007.
3. Råmunddal T, Hoebers LP, Henriques JP et al. Chronic total occlusions in Sweden--a report from the Swedish Coronary Angiography and Angioplasty Registry (SCAAR) [published correction appears in PLoS One. 2014; 9(10): e112370. Hoebers, Loes [corrected to Hoebers, Loes P]]. PLoS One. 2014; 9(8): e103850. Published 2014 Aug 12. doi:10.1371/journal. pone.0103850.
4. Habib GB, Heibig J, Forman SA et al. Influence of coronary collateral vessels on myocardial infarct size in humans. Results of phase I thrombolysis in myocardial infarction (TIMI) trial. The TIMI Investigators. Circulation. 1991; 83(3): 739–746. doi:10.1161/01.cir.83.3.739.
5. Tomasello SD, Boukhris M, Giubilato S et al. Management strategies in patients affected by chronic total occlusions: results from the Italian Registry of Chronic Total Occlusions. Eur Heart J. 2015; 36(45): 3189–3198. doi:10.1093/eurheartj/ehv450.
6. Stuijfzand WJ, Driessen RS, Raijmakers PG et al. Prevalence of ischaemia in patients with a chronic total occlusion and preserved left ventricular ejection fraction. Eur Heart J Cardiovasc Imaging. 2017; 18(9): 1025–1033. doi:10.1093/ehjci/jew188.
7. Strauss BH, Shuvy M, Wijeysundera HC. Revascularization of chronic total occlusions: time to reconsider?. J Am Coll Cardiol. 2014; 64(12): 1281–1289. doi:10.1016/j.jacc.2014.06.1181.
8. Cetin M, Zencir C, Cakici M et al. Effect of a successful percutaneous coronary intervention for chronic total occlusion on parameters of ventricular repolarization. Coron Artery Dis. 2014; 25(8): 705–712. doi:10.1097/MCA.0000000000000138.
9. Nombela-Franco L, Iannaccone M, Anguera I et al. Impact of Chronic Total Coronary Occlusion on Recurrence of Ventricular Arrhythmias in Ischemic Secondary Prevention Implantable Cardioverter-Defibrillator Recipients (VACTO Secondary Study): Insights From Coronary Angiogram and Electrogram Analysis. JACC Cardiovasc Interv. 2017; 10(9): 879 – 888. doi:10.1016/j.jcin.2017.02.008.
10. Sachdeva R, Agrawal M, Flynn SE, et al. The myocardium supplied by a chronic total occlusion is a persistently ischemic zone. Catheter Cardiovasc Interv 2014; 83 : 9–16.
11. Kayaert P, Coeman M, Drieghe B et al. iFR uncovers profound but mostly reversible ischemia in CTOs and helps to optimize PCI results [published online ahead of print, 2020 Jun 17]. Catheter Cardiovasc Interv. 2020;10.1002/ccd.29072. doi:10.1002/ccd.29072.
12. Werner GS, Martin-Yuste V, Hildick-Smith D, et al. A randomized multicentre trial to compare revascularization with optimal medical therapy for the treatment of chronic total coronary occlusions. Eur Heart J. 2018; 39(26): 2484–2493. doi:10.1093/eurheartj/ehy220
13. Obedinskiy AA, Kretov EI, Boukhris M et al. The IMPACTOR-CTO Trial. JACC Cardiovasc Interv. 2018; 11(13): 1309–1311. doi:10.1016/j.jcin.2018.04.017.
14. Brilakis ES, Mashayekhi K, Burke MN. How DECISION-CTO Can Help Guide the Decision to Perform Chronic Total Occlusion Percutaneous Coronary Intervention. Circulation. 2019; 139(14): 1684–1687.
15. Neumann FJ, Sousa-Uva M, Ahlsson A et al. 2018 ESC/EACTS Guidelines on myocardial revascularization. EuroIntervention. 2019; 14(14): 1435–1534. doi:10.4244/EIJY19M01_01.
16. Alaswad K, Menon RV, Christopoulos G et al. Transradial approach for coronary chronic total occlusion interventions: Insights from a contemporary multicenter registry. Catheter Cardiovasc Interv. 2015; 85(7): 1123–1129. doi:10.1002/ccd.25827.
17. Muramatsu T, Tsuchikane E, Oikawa Y et al. Incidence and impact on midterm outcome of controlled subintimal tracking in patients with successful recanalisation of chronic total occlusions: J-PROCTOR registry. EuroIntervention. 2014; 10(6): 681–688.
18. Claessen BE, Dangas GD, Godino C et al. Impact of target vessel on long-term survival after percutaneous coronary intervention for chronic total occlusions. Catheter Cardiovasc Interv. 2013; 82(1): 76–82. doi:10.1002/ccd.24579.
19. Galassi AR, Sianos G, Werner GS, et al. Retrograde Recanalization of Chronic Total Occlusions in Europe: Procedural, In-Hospital, and Long-Term Outcomes From the Multicenter ERCTO Registry. J Am Coll Cardiol. 2015; 65(22): 2388–2400.
20. Morino Y, Kimura T, Hayashi Y et al. In-hospital outcomes of contemporary percutaneous coronary intervention in patients with chronic total occlusion insights from the J-CTO Registry (Multicenter CTO Registry in Japan). JACC Cardiovasc Interv. 2010;3(2):143–151. doi:10.1016/j.jcin.2009.10.029.
21. Megaly M, Saad M, Tajti P et al. Meta-analysis of the impact of successful chronic total occlusion percutaneous coronary intervention on left ventricular systolic function and reverse remodeling. J Interv Cardiol. 2018; 31(5): 562–571. doi:10.1111/joic.12538.
22. Stuijfzand WJ, Biesbroek PS, Raijmakers PG et al. Effects of successful percutaneous coronary intervention of chronic total occlusions on myocardial perfusion and left ventricular function. EuroIntervention. 2017; 13(3): 345–354. doi:10.4244/EIJ-D-16–01014.
23. Patel MR, Calhoon JH, Dehmer GJ et al. ACC/AATS/AHA/ASE/ASNC/SCAI/SCCT/STS 2017 Appropriate Use Criteria for Coronary Revascularization in Patients With Stable Ischemic Heart Disease: A Report of the American College of Cardiology Appropriate Use Criteria Task Force, American Association for Thoracic Surgery, American Heart Association, American Society of Echocardiography, American Society of Nuclear Cardiology, Society for Cardiovascular Angiography and Interventions, Society of Cardiovascular Computed Tomography, and Society of Thoracic Surgeons [published correction appears in J Am Coll Cardiol. 2018 Apr 13;:]. J Am Coll Cardiol. 2017; 69(17): 2212–2241. doi:10.1016/j.jacc.2017.02.001.
24. Claessen BE, Dangas GD, Weisz G, et al. Prognostic impact of a chronic total occlusion in a non-infarct-related artery in patients with ST-segment elevation myocardial infarction: 3-year results from the HORIZONS-AMI trial. Eur Heart J. 2012; 33(6): 768–775. doi:10.1093/eurheartj/ehr471.
25. Gierlotka M, Tajstra M, Gąsior M et al. Impact of chronic total occlusion artery on 12-month mortality in patients with non-ST-segment elevation myocardial infarction treated by percutaneous coronary intervention (from the PL-ACS Registry). Int J Cardiol. 2013; 168(1): 250–254. doi:10.1016/j.ijcard.2012.09.086.
26. Watanabe H, Morimoto T, Shiomi H et al. Chronic total occlusion in a non-infarct-related artery is closely associated with increased five-year mortality in patients with ST-segment elevation acute myocardial infarction undergoing primary percutaneous coronary intervention (from the CREDO-Kyoto AMI registry). EuroIntervention. 2017; 12(15): e1874 – e1882. doi:10.4244/EIJ-D-15–00421.
27. Fujii T, Sakai K, Nakano M et al. Impact of the origin of the collateral feeding donor artery on short-term mortality in ST-elevation myocardial infarction with comorbid chronic total occlusion. Int J Cardiol. 2016; 218 : 158–163. doi:10.1016/j.ijcard.2016.05.023.
28. Henriques JP, Hoebers LP, Råmunddal T et al. Percutaneous Intervention for Concurrent Chronic Total Occlusions in Patients With STEMI: The EXPLORE Trial. J Am Coll Cardiol. 2016; 68(15): 1622–1632. doi:10.1016/j.jacc.2016.07.744.
29. Hachamovitch R, Hayes SW, Friedman JD et al. Comparison of the short-term survival benefit associated with revascularization compared with medical therapy in patients with no prior coronary artery disease undergoing stress myocardial perfusion single photon emission computed tomography. Circulation. 2003; 107(23): 2900–2907. doi:10.1161/01. CIR.0000072790.23090.41.
30. Galassi AR, Brilakis ES, Boukhris M et al. Appropriateness of percutaneous revascularization of coronary chronic total occlusions: an overview. Eur Heart J. 2016;37(35):2692 – 2700. doi:10.1093/eurheartj/ehv391.
31. Galassi AR, Werner GS, Boukhris M et al. Percutaneous recanalisation of chronic total occlusions: 2019 consensus document from the EuroCTO Club. EuroIntervention. 2019; 15(2): 198–208. doi:10.4244/EIJ-D-18–00826.
32. Schumacher SP, Kockx M, Stuijfzand WJ et al. Ischaemic burden and changes in absolute myocardial perfusion after chronic total occlusion percutaneous coronary intervention. EuroIntervention. 2020; 16(6): e462–e471. Published 2020 Aug 7. doi:10.4244/EIJ-D-19–00631.
33. Galassi AR, Werner GS, Tomasello SD et al. Prognostic value of exercise myocardial scintigraphy in patients with coronary chronic total occlusions. J Interv Cardiol. 2010; 23(2): 139–148. doi:10.1111/j.1540–8183.2010.00527.
34. Löffler AI, Kramer CM. Myocardial Viability Testing to Guide Coronary Revascularization. Interv Cardiol Clin. 2018; 7(3): 355–365. doi:10.1016/j.iccl.2018.03.005.
35. Bucciarelli-Ducci C, Auger D, Di Mario C et al. CMR Guidance for Recanalization of Coronary Chronic Total Occlusion. JACC Cardiovasc Imaging. 2016; 9(5): 547–556. doi:10.1016/j. jcmg.2015.10.025
36. Gerbay A, Youssof E, Vola M et al. Prediction of recovery after revascularization in chronic Coronary Total Occlusion (CTO) patients. Adenosine or low-dose dobutamine stress with LGE CMR: which is the best combination? J Cardiovasc Magn Reson. 2015; 17(Suppl 1): P114. Published 2015 Feb 3. doi:10.1186/1532–429X-17-S1-P114.
37. Pica S, Di Giovine G, Bollati M et al. Cardiac magnetic resonance for ischaemia and viability detection. Guiding patient selection to revascularization in coronary chronic total occlusions: The CARISMA_CTO study design. Int J Cardiol. 2018; 272 : 356–362. doi:10.1016/j. ijcard.2018.08.061.
38. Okamura A, Yamane M, Muto M et al. Complications during retrograde approach for chronic coronary total occlusion: Sub-analysis of Japanese multicenter registry. Catheter Cardiovasc Interv. 2016; 88(1): 7–14. doi:10.1002/ccd.26317.
39. Galassi AR, Sianos G, Werner GS et al. Retrograde Recanalization of Chronic Total Occlusions in Europe: Procedural, In-Hospital, and Long-Term Outcomes From the Multicenter ERCTO Registry. J Am Coll Cardiol. 2015; 65(22): 2388–2400. doi:10.1016/j.jacc.2015.03.566
40. Mashayekhi K, Behnes M, Akin I, Kaiser T, Neuser H. Novel retrograde approach for percutaneous treatment of chronic total occlusions of the right coronary artery using ipsilateral collateral connections: a European centre experience. EuroIntervention. 2016;11(11):e1231-e1236. doi:10.4244/EIJV11I11A244.
41. Brilakis ES, Grantham JA, Rinfret S et al. A percutaneous treatment algorithm for crossing coronary chronic total occlusions. JACC Cardiovasc Interv. 2012; 5(4): 367–379. doi:10.1016/j.jcin.2012.02.006.
Štítky
Diabetologie Endokrinologie Interní lékařství
Článek vyšel v časopiseVnitřní lékařství
Nejčtenější tento týden
2021 Číslo E-4- Efekt itopridu na motilitu jícnu a funkci dolního jícnového svěrače
- Neuropatie u diabetu: Proč ji nepřehlédnout a kdy myslet i na deficit vitaminů B?
- Strava bohatá na arginin a prolin slibuje urychlení hojení ran u diabetických pacientů
- Úloha růstového faktoru TGF-β v procesu hojení ran
- Topicky aplikovaný propolis může urychlovat hojení diabetických bércových vředů
-
Všechny články tohoto čísla
- Aortálna stenóza a dysfunkcia pravej komory
- Perkutánní intervence chronického uzávěru koronární tepny – komu, kdy a proč
- Pancytopenie jako hlavní projev nákazy lidským virem imunodeficience ve stadiu AIDS
- Hodnocení validity metody palcového tlaku u diabetiků – průběžné výsledky
- Lymfangiomatóza – vzácné generalizované onemocnění lymfatického systému
- Vnitřní lékařství
- Archiv čísel
- Aktuální číslo
- Pouze online
- Informace o časopisu
Nejčtenější v tomto čísle- Perkutánní intervence chronického uzávěru koronární tepny – komu, kdy a proč
- Lymfangiomatóza – vzácné generalizované onemocnění lymfatického systému
- Aortálna stenóza a dysfunkcia pravej komory
- Pancytopenie jako hlavní projev nákazy lidským virem imunodeficience ve stadiu AIDS
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Revma Focus: Spondyloartritidy
nový kurz
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Autoři: prof. MUDr. Pavel Horák, CSc., doc. MUDr. Ludmila Brunerová, Ph.D., doc. MUDr. Václav Vyskočil, Ph.D., prim. MUDr. Richard Pikner, Ph.D., MUDr. Olga Růžičková, MUDr. Jan Rosa, prof. MUDr. Vladimír Palička, CSc., Dr.h.c.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



