-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Výživa u open abdomen
Nutrition in open abdomen
Open abdomen is known as a serious consequence of various intra-abdominal pathologies. Initially, patients often have a life-threatening condition, sepsis or septic shock. Severe stress related malnutrition, mineral and fluid imbalance develop as metabolic consequences. Intestinal fistulas also occur as a frequent complication in patients with open abdomen. In such patients, a comprehensive approach is needed, including rehabilitation, nutritional support using optimal formulas, and local care for the open abdomen. Our case report presents a patient with open abdomen and enterocutaneous fistulation. A complex nutritional approach in the course of the disease is described and its importance is discussed. Finally, a summary of nutritional care for open abdomen patients is provided based on current recommendations.
Keywords:
open abdomen – nutrition-energy need – protein need
Autoři: L. Urbánek; L. Veverková
; J. Žák; M. Reška
Působiště autorů: I. chirurgická klinika Lékařské fakulty Masarykovy univerzity a Fakultní nemocnice u svaté Anny v Brně
Vyšlo v časopise: Rozhl. Chir., 2021, roč. 100, č. 2, s. 83-87.
Kategorie: Kazuistika
Souhrn
Open abdomen je závažný důsledek rozličných nitrobřišních procesů provázených často sepsí až septickým šokem. Jako následek se pak rozvíjí těžká stresová malnutrice, poruchy hydratace a iontová dysbalance. Součástí open abdomen často bývá přítomnost střevní píštěle. U takto postižených pacientů je nutný komplexní přístup zahrnující rehabilitaci, nutriční péči v optimálním složení a lokální péči o otevřenou dutinu břišní. Na kazuistice pacientky s open abdomen a enterokutální fistulací popisujeme praktickou aplikaci výživy v průběhu celého onemocnění. Na závěr pak uvádíme souhrn doporučení nutriční péče u této skupiny nemocných.
Klíčová slova:
open abdomen – výživa/energetická potřeba – potřeba proteinu
Úvod
Open abdomen je stav, který vzniká jako následek komplikovaného nitrobřišního onemocnění jak úrazové, tak i neúrazové etiologie s rozvojem sekundární peritonitidy. Mezi hlavní příčiny patří perforace GIT, masivní krvácení do dutiny břišní a GIT s nutností operačního řešení, rozsáhlé střevní ischemie, nitrobřišní hypertenze a nekrotizující pankreatitida.
Klasifikaci open abdomen zavedl v roce 2009 Björck [1] a v roce 2016 ji upravil [2].
U pacientů s open abdomen pak může být jako komplikace přítomna střevní píštěl. Ta pak zhoršuje prognózu a prodlužuje hojení. Střevní píštěle můžeme dělit jak podle lokalizace na zažívacím traktu, tak i podle množství sekrece z píštěle. Pokud je sekrece do 500 ml/24 hodin, hodnotíme ji pak jako píštěl s nízkou Klasifikace open abdomen [2]sekrecí a nad 500 ml/24 hodin jako píštěl s vysokou sekrecí. Píštěle s vysokou sekrecí jsou asociovány s vyšším rizikem mortality [3,4].
Open abdomen bývá často provázen sepsí až septickým šokem. Tento stav dále komplikuje rozvoj stresové malnutrice s častou minerálovou dysbalancí a hypovolemií.
Další komplikací je infekce, při které rozsáhlá ranná plocha u open abdomen představuje významnou bránu vstupu infekčních agens do organizmu. Velká ranná plocha je pak také příčinou rozsáhlé ztráty tekutin a bílkovin. Vlivem malnutrice pak dochází k úbytku aktivní svalové hmoty, snížení funkce imunitního systému, postižení střevní bariéry, snížení koncentrace sérových proteinů, postižení transportní funkce krve a celkové zhoršení reparačních procesů.
Prevalence vzniku fistulací bývá závislá na základní příčině nitrobřišní patologie. Zatímco u pacientů po operaci pro trauma či po obecném chirurgickém zákroku bývá vyjádřena v jednotkách procent (1,5−3,6 %) [5,6], u pacientů podstupujících nitrobřišní výkon pro Crohnovu chorobu až v 35 % [7,8].
Pacient s open abdomen tak vyžaduje komplexní péči, která zahrnuje především v první fázi zvládnutí iniciální sepse s hemodynamickou stabilizací a optimalizací. Cílem managementu v počáteční fázi je především obnova adekvátní perfuze splanchnické oblasti s možností vysazení katecholaminů a dosažením následné mobilizace tekutin z intersticiálních prostor.
Dalším úkolem je volba vhodného krytí open abdomen. V současné době je již standardem aplikace NPWT (negative pressure wound therapy) [9]. U nemocného se snažíme dosáhnout normalizace vodního a iontového hospodářství, snížit odpady z eventuální píštěle a chránit tkáně v okolí fistulací. Indikována může být také blokáda střevní a žaludeční sekrece. Zvládnuty musejí být infekční komplikace. S ohledem na rozvoj malnutrice je jedním ze základních kamenů léčby kvalitní a odpovídající nutriční péče a rehabilitace k obnovení svalové síly.
Tab. 1. Klasifikace open abdomen [2]
Tab. 1: Classification of the open abdomen [2]![Klasifikace open abdomen [2]<br>
Tab. 1: Classification of the open abdomen [2]](https://pl-master.mdcdn.cz/media/cache/media_object_image_small/media/image_pdf/c98ddc33ab7f8d9552cda58e4326d6b2.png)
Ke zhojení píštěle může dojít i spontánně, v řadě případů je nutné s odstupem definitivní operační řešení. Pro spontánní zhojení jsou příznivé malé defekty do 1 cm. Mezi faktory, které mohou způsobit selhání spontánního zhojení, patří přítomný absces, zúžené nebo zanícené střevo, radiační terapie, cizí tělesa nebo překážka distálně od fistulace [3].
Pokud nedojde ke spontánnímu uzávěru fistulace, její chirurgické řešení by mělo být provedeno odloženě [10]. Míra recidivy pooperační píštěle je vyšší při dřívějším chirurgickém zákroku.
Kazuistika
55letá pacientka byla akutně přijata s anamnézou postupně se zhoršujících bolestí břicha trvajících několik dní a zvracením. Při klinickém vyšetření dominovala objemná silně bolestivá ventrální herniace průměru cca 35 cm, peristaltika nebyla. Pacientka udala, že tato herniace trvá dlouhá léta. Kožní kryt byl lividní, místy nekrotický. Pacientky měla hmotnost 105 kg při výšce 175 cm (BMI 34,2). V laboratorních výsledcích dominovala leukocytóza 18×109/l, CRP 110 mg/l, v iontogramu lehčí pokles Cl na 95 mmol/l. Provedené zobrazovací metody podporovaly diagnózu ileózního stavu. Po nezbytné přípravě byla pacientka neodkladně operována s nutností resekce podstatné části kožního krytu kýly. Byla provedena rozsáhlá deliberace akretních tenkých kliček jako příčiny ileu. Během operace při deliberaci a uvolňování tenkých kliček došlo k několika deserozacím. Rozsáhlý defekt břišní stěny byl kryt standardně naloženým NPWT s překrytím kliček abdominální fólií. S ohledem na rozsah defektu nebyl možný ani budoucí uzávěr břišní stěny, ani využití dynamické sutury. Po operaci pacientka vykazovala oběhovou nestabilitu s přechodnou nutností aplikace noradrenalinu. Během 24 hodin došlo k oběhové stabilizaci a vysazení katecholaminu. V pooperačním období u pacientky převážila dysfunkce GIT s výraznými odpady nasogastrickou sondou. Ve snaze o podporu peristaltiky kontinuálně byl podáván syntostigmin. Pacientka dostávala ATB v dávkách dle hmotnosti (amoxycilin/kys. klavulonová + metronidazol) a byl pravidelně měněn systém NPWT na operačním sále. S ohledem na nemožnost zahájení enterální výživy z důvodů dysfunkce GIT byla zahájena výživa cestou TPV s aplikací iontů a mikronutrientů v doporučených denních dávkách s přihlédnutím ke ztrátám za monitoringu laboratorních hladin. Výživa byla počítána iniciálně na energetickou potřebu 30 kcal/kg/den korigované tělesné hmotnosti s ohledem na nadváhu. Aminokyseliny podávány v dávce 1,5 g/kg/den. Používali jsme individuálně připravovaný vak plné parenterální výživy.
Desátý pooperační den se objevila tenkostřevní píštěl v oblasti ilea. Fistulace byla řešena zavedením katétru do píštěle a nadále jsme pokračovali v aplikaci NPWT. Iniciální sekrece z fistulace činila cca 1000 ml/den a průměr píštěle dosahoval 1 cm. S ohledem na tuto situaci jsme upravili výživu zvýšením jak energetické dávky na 35 kcal/kg/den, tak dávky aminokyselin na hodnotu 2 g/kg/den, stále v podobě individuálně připravovaného vaku. S ohledem na nemožnost aplikace výživy do GIT pro jeho pokračující dysfunkci jsme přidali glutamin i.v. v dávce 0,4 g/kg/den. Postupně se dařilo obnovit funkci GIT a peristaltiku. Obnovením funkce GIT se snižovala sekrece z píštěle pod 500 ml/den. Zrušili jsme katétr zavedený do píštěle, fistulace se ohraničila a začala regredovat. Lokálně jsme mohli na píštěl nalepit jímací sáček při aplikaci NPWT. Po snížení sekrece jsme zahájili aplikaci enterální výživy sondou. Nejprve jsme dodávali k parenterální výživě hypokalorický přípravek s obsahem 34 % bílkoviny (25 % glutamin), 15 % sacharidu a 1 % tuku. Následně byl přidán polymerní vysokoproteinový přípravek enterální výživy. Postupně se dařilo převést pacientku plně na enterální výživu a vysadit parenterální výživu. V té době se sekrece z píštěle pohybovala pod 200 ml/den. Cílovou dávku pro energii a bílkovinu jsme ponechali na stejné hodnotě ve snaze o maximální podporu hojení. Průměr fistulace se zmenšoval pod 1 cm. Při pravidelných převazech se tvořila nad kličkami granulační plocha tak, že bylo možné postupné odstranění NPWT a po definitivním vyčištění naložení plastiky Thierschovými štěpy. Píštěl byla kryta jímacím sáčkem. Funkce GIT se zcela obnovila a pacientka mohla být převedena na perorální příjem posílený sippingem. Pacientku sledovala nutriční terapeutka, která sestavovala individuální dietu a denně hodnotila reálný příjem potravy. V průběhu celé hospitalizace probíhala rehabilitační péče s přizpůsobením aktuálnímu stavu. Za necelé 2 měsíce byla pacientka s nalepeným jímacím sáčkem propuštěna do domácí péče. Při propuštění dosahovala sekrece z píštěle max. 100 ml/den. Pacientka byla plně mobilní, soběstačná i v péči o jímací systém píštěle. I po propuštění zůstala ve sledování nutriční ambulance (nutriční terapeutka i nutricionista). Sekrece se dále snižovala, průměr se zmenšoval. Za 2 měsíce při kontrole byla sekrece nulová a u píštěle došlo ke spontánnímu zhojení. Celková doba trvání píštěle do úplného spontánního zhojení byla 4 měsíce.
Obr. 1. Ventrální kýla
Fig. 1: Ventral hernia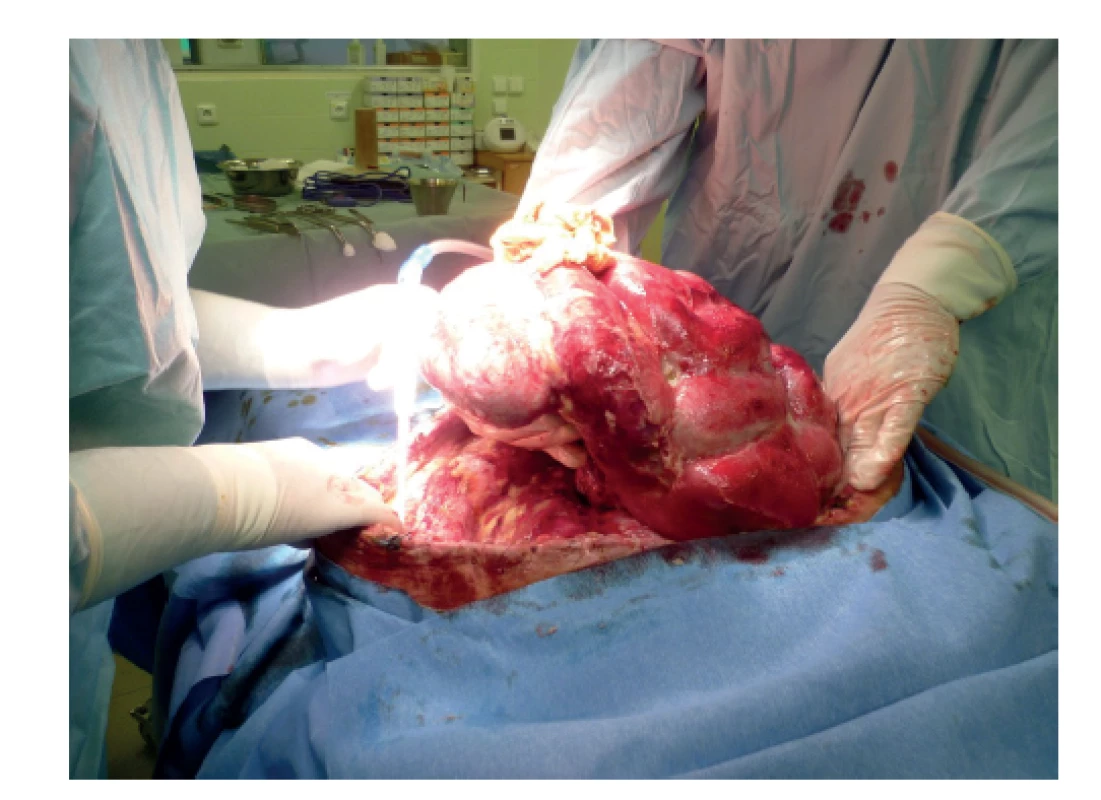
Obr. 2. Katétr v píštěli
Fig. 2: Catheter in the fistula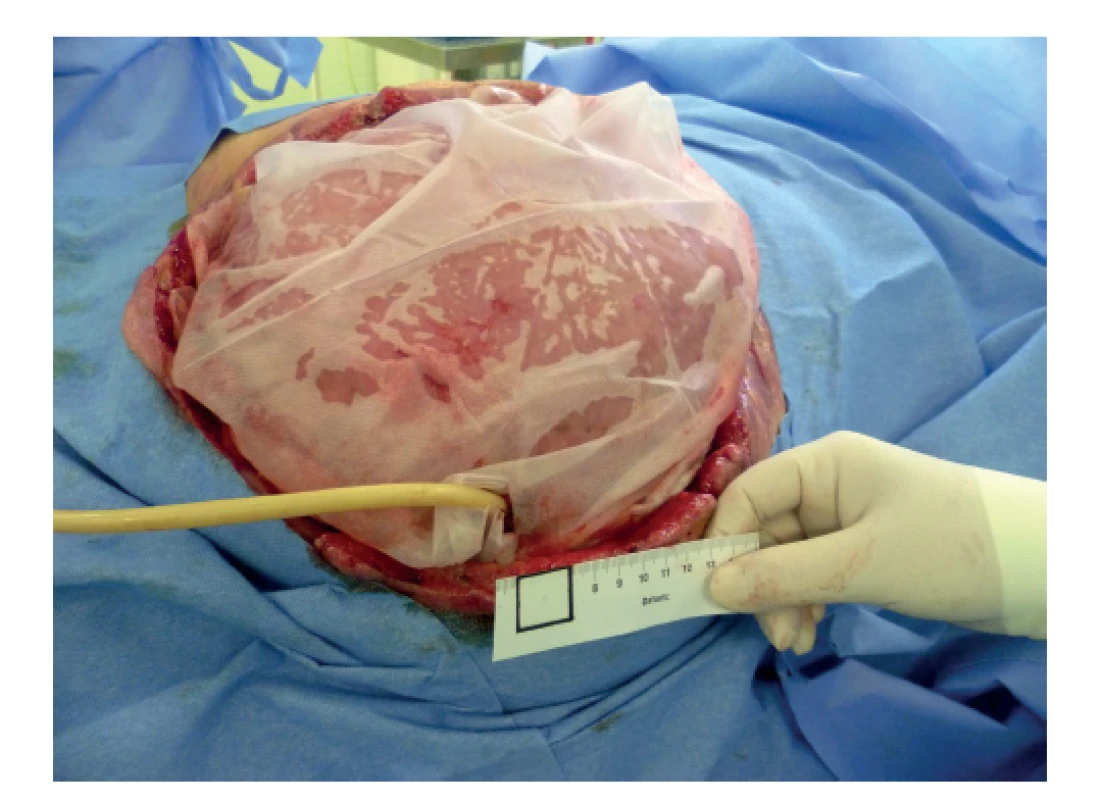
Obr. 3. Píštěl s jímacím sáčkem
Fig. 3: Fistula with a collection bag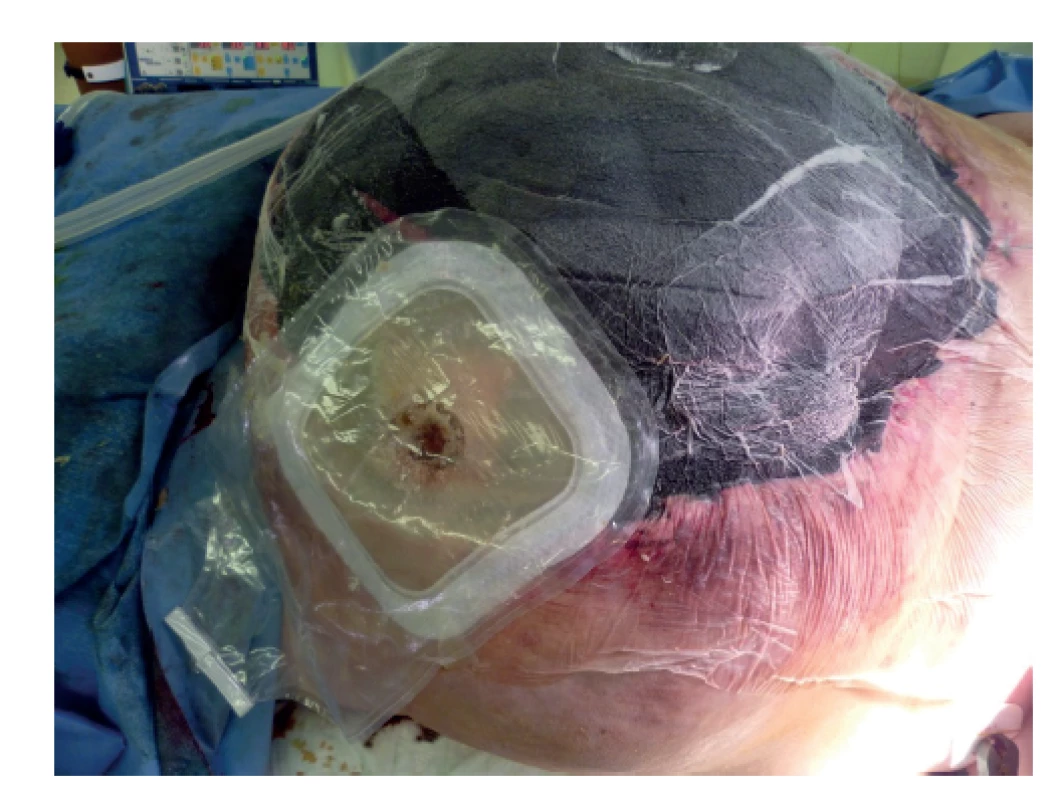
Diskuze
Aplikace dostatečné a kvalitní výživy je jedním ze základních předpokladů úspěšného zvládnutí open abdomen. To zvláště platí u pacientů, kteří mají střevní fistulaci. Nutriční péče bývá s ohledem na protrahované léčení dlouhá, často trvající několik měsíců s nutností individualizace i se zohledněním vývoje stavu v čase.
Tak jako u všech ostatních nemocných se u pacientů s open abdomen snažíme aplikovat výživu do GIT. Enterální výživa zachovává střevní bariéru, působí prokineticky a má pozitivní vliv na hormonální a imunitní funkce střeva. Schopnost aplikace enterální výživy nemocnému se jeví být asociována s nižším rizikem pro vznik enterokutální fistulace [11]. Iniciálně by měla být použita polymerní formule, v případě intolerance je pak třeba změnit na oligomerní [12]. U pacientů s již přítomnou enterokutální fistulací bývá pro aplikaci typu výživy často rozhodující množství sekrece píštělí. Pacienti s nízkou sekrecí bez distální obstrukce GIT často tolerují perorální příjem. V případě navýšení sekrece po perorální zátěži je pak alternativa podání enterální výživy distálně od fistulace, či přímo formou fistuloklýzy. V případě, že nelze dosáhnout nutričních cílů cestou enterální výživy, bývá nutná aplikace doplňkové parenterální výživy. Použití plné parenterální výživy bývá nezbytné při sekreci z píštěle vyšší než 500 ml/24 hodin, při střevní obstrukci či nemožnosti udržení tekutinové nebo elektrolytové rovnováhy [12].
Ve stanovení energetické potřeby pacienta má jistě svoji úlohu nepřímá kalorimetrie [13]. Tuto metodu však mnoho pracovišť nemá k dispozici, proto se většinou používá stanovení energetické potřeby výpočtem. Guidelines americké společnosti pro parenterální a enterální výživu doporučuje dávku 25–30 kcal/kg/den v závislosti na energetické potřebě založené na hodnocení stavu nemocného [12]. Evropská společnost klinické výživy pak dávku 25−35 kcal/kg/24 hodin v závislosti na anabolickém/katabolickém stavu a fázi onemocnění [14]. Některé práce [15] pak doporučují aplikaci energie založenou na výši sekrece píštělí. V případě nízkoodpadové píštěle je indikována výživa s energickou hodnotou 20−30 kcal/kg/den, v případě sekrece vyšší než 500 ml/den pak 25−35 kcal/kg/den. Stejně tak jako energetickou potřebu autoři rozdělují potřebu proteinu, a to u nízké sekrece 1−1,5 g/kg/den a vysokoodpadové fistulace 1,5−2,5 g/kg den.
Americká společnost pro parenterální a enterální výživu doporučuje dávku proteinu 1,5−2,0 g/kg/den také s nutností navýšení až na 2,5 g/kg/den u pacientů s vysokými odpady [12].
Samozřejmostí je doplnění elektrolytů, vitaminů a stopových prvků s korekcí dávky dle případných ztrát.
Mnoho autorů dnes diskutuje problematiku imunonutrice. Pro aplikaci vícesložkových preparátů, obsahujících směs komponent (omega-3, nukleotidy, arginin), nejsou důkazy o jejich pozitivním vlivu na hojení open abdomen a píštělí. Jako imunonutriční jednosložkové preparáty se dnes používají především omega-3 mastné kyseliny a glutamin.
Přidání omega-3 mastných kyselin může zlepšit imunitní funkce po těžkém inzultu, rozsáhlé nitrobřišní operaci či u pacienta v intenzivní péči [16,17,18], ale není známý pozitivní efekt na léčbu píštěle.
U intravenózního podávání glutaminu došlo k přehodnocení jeho aplikace u kriticky nemocných na základě výsledků REDOX studie [19] a nyní již není doporučován. Jeho aplikace je dle současných doporučení na zvážení u těch chirurgických nemocných, kteří nemohou být živeni enterálně a vyžadují pouze parenterální výživu [16]. Pozitivní efekt intravenózně aplikovaného glutaminu, stejně jako omega-3 mastných kyselin na sanaci střevních píštělí nebyl dosud prokázán [16,20].
Naproti tomu pro podávání glutaminu perorálně již dostupná data v literatuře existují. Výsledky studií ukazují jeho pozitivní vliv na hojení fistulace. Doporučené dávky se pohybují kolem 0,3 g/kg/den [21,22].
Závěr
Open abdomen představuje závažnou komplikaci rozličných nitrobřišních procesů provázených často sepsí až septickým šokem. Léčba takového stavu bývá často dlouhá a multidisciplinární. Jedním ze základních pilířů péče o takového nemocného je kvalitní zajištění pacienta výživou. Při volbě výživy je nutné zohlednit stav gastrointestinálního traktu, přítomnost střevní píštěle, její lokalizaci a odpady z ní, současně také celkový stav nemocného a jeho vývoj v čase. Vždy by měla být snaha o zajištění pacienta výživou aplikovanou do zažívacího traktu. Jen pokud to není možné, je nutno volit parenterální výživu. Dávka by měla být stanovena i s ohledem na možné ztráty jak rannou plochou, tak i případnou střevní píštělí. Zvláštní důraz je nezbytné dát na dostatečné zastoupení proteinu ve výživě. Z imunonutričních preparátů se zatím jeví jako prospěšný pouze glutamin aplikovaný do zažívacího traktu.
Konflikt zájmů
Autoři článku prohlašují, že nejsou v souvislosti se vznikem tohoto článku ve střetu zájmů a že tento článek nebyl publikován v žádném jiném časopise, s výjimkou kongresových abstrakt a doporučených postupů
MUDr. Libor Urbánek
I. chirurgická klinika
Fakultní nemocnice u svaté Anny v Brně
Pekařská 53
e-mail: libor.urbanek@fnusa.cz
Zdroje
- Björck M, Bruhin A, Cheatham M, et al. Classification—important step to improve management of patients with an open abdomen. World J Surg. 2009;33(6):1154−1157. doi: 10.1007/s00268-009-9996-3.
- Björck M, Kirkpatrick AW, Cheatham M, et al. Amended classification of the open abdomen. Scand J Surg. 2016;105(1):5−10. doi: 10.1177/1457496916631853.
- Evenson AR, Fischer JE. Current management of enterocutaneous fistula. J Gastrointest Surg. 2006;10(3):455−464. doi: 10.1016/j.gassur.2005.08.001.
- Lloyd DAJ, Gabe SM, Windsor ACJ. Nutrition and management of enterocutaneous fistula. Br J Surg. 2006;93(9):1045−1055. doi: 10.1002/bjs.5396.
- Teixeira PG, Inaba K, Dubose J, et al. Enterocutaneous fistula complicating trauma laparotomy: a major resource burden. Am Surg. 2009;75(1):30−32. doi: 10.1177/000313480907500106.
- Wercka J, Cagol PP, Melo ALM, et al. Epidemiology and outcome of patients with postoperative abdominal fistula. Rev Col Bras Cir. 2016; 43(2):117−123. doi: 10.1590/0100-69912016002008.
- Michelassi F, Stella M, Balestracci T, et al. Incidence, diagnosis, and treatment of enteric and colorectal fistulae in patients with Crohn‘s disease. Ann Surg. 1993;218(5):660−666. doi: 10.1097/00000658-199321850-00012.
- Annibali R, Pietri P. Fistulous complications of Crohn‘s disease. Int Surg. 1992;77(1):19−27.
- Šerclová Z, Ryska O, Dytrych P, et al. Uzávěr stěny břišní po laparostomii s použitím negativního tlaku pro těžkou peritonitidu pomocí dynamické fasciální sutury – výsledky prospektivní randomizované studie. Rozhl Chir. 2012;91(1):26−31.
- Lynch AC, Delaney CP, Senagore AJ, et al. Clinical outcome and factors predictive of recurrence after enterocutaneous fistula surgery. Ann Surg. 2004;240(5):825−831. doi: 10.1097/01.sla.0000143895.17811.e3.
- Collier B, Guillamondegui O, Cotton B, et al. Feeding the open abdomen. JPEN J Parenter Enteral Nutr. 2007;31(5):410−415. doi: 10.1177/0148607107031005410.
- Kumpf VJ, de Aguilar-Nascimento JE, Diaz-Pizarro Graf JI, et al. ASPEN‐FELANPE Clinical Guidelines. JPEN J Parenter Enteral Nutr. 2017;41(1):104−112. doi: 10.1177/0148607116680792.
- Dumas RP, Moore SA, Sims CA. Enterocutaneous fistula: Evidence-based management. Clin Surg. 2017;2 : 1435.
- Klek S, Forbes A, Gabe S, et al. Management of acute intestinal failure: A position paper from the European Society for Clinical Nutrition and Metabolism (ESPEN) Special Interest Group. Clin Nutrition 2016;35(6):1209−1218. doi: 10.1016/j.clnu.2016.04.009.
- Gribovskaja-Rupp I, Melton GB. Enterocutaneous fistula: proven strategies and updates. Clin Colon Rectal Surg. 2016;29(2):130−137. doi: 10.1055/s-0036-1580732.
- Satinský I, Havel E, Bezděk K, et al. Klinická výživa v chirurgii-doporučení ESPEN (European Society for Parenteral and Enteral Nutrition) s konsenzuálním hlasováním pracovní skupiny SKVIMP (Společnost klinické výživy a intenzivní metabolické péče). Anest Intenziv Med. 2019;30(2):104−110.
- Singer P, Berger MM, Van den Berghe G, et al. ESPEN guidelines on parenteral nutrition: intensive care. Clin Nutr. 2009;28(4):387-400. doi: 10.1016/j.clnu.2009.04.024.
- Kudsk KA. Immunonutrition in surgery and critical care. Annu Rev Nutr. 2006; 26 : 463−479. doi: 10.1146/annurev.nutr.26.061505.111230.
- Heyland D, Muscedere J, Wischmeyer PE, et al. A randomized trial of glutamine and antioxidants in critically ill patients. N Engl J Med. 2013;368(16):1489−1497. doi: 10.1056/NEJMoa1212722.
- Badrasawi Manal MH, Shahar S, Sagap I. Nutritional management of enterocutaneous fistula: A retrospective study at a Malaysian university medical center. J Multidiscip Healthc. 2014;7 : 365−370. doi: 10.2147/JMDH.S58752.
- Martinez JL, Bosco-Garate I, Souza-Gallardo LM, et al. Effect of preoperative administration of oral arginine and glutamine in patients with enterocutaneous fistula submitted to definitive surgery: a prospective randomized trial. J Gastrointest Surg. 2020;24(2):426−434. doi: 10.1007/s11605-018-04099-4.
- de Aguilar-Nascimento JE, Caporossi C, Dock-Nascimento DB, et al. Oral glutamine in addition to parenteral nutrition improves mortality and the healing of high-output intestinal fistulas. Nutr Hosp. 2007;22(6):672−676
Štítky
Chirurgie všeobecná Ortopedie Urgentní medicína
Článek vyšel v časopiseRozhledy v chirurgii
Nejčtenější tento týden
2021 Číslo 2- Riziko rozvoje závažné infekce po císařském řezu lze snížit provedením antiseptického výplachu vaginy
- Topicky aplikovaný propolis může urychlovat hojení diabetických bércových vředů
- Spolehlivý systém skórování jizev k hodnocení fotografií popálenin
- Spasmolytický účinek metamizolu
- Bezpečnostní profil metamizolu – systematický přehled
-
Všechny články tohoto čísla
- Výživa v chirurgii: jak dostat koně do Tróje?
-
Perioperační výživa ve světle doporučení
(a ve stínu praxe) - Nové ambulantní možnosti ovlivnění malnutrice chirurgem
- Intermitentní výživa v intenzivní péči – teorie a praxe
- Karcinom rekta – současná léčebná strategie a hodnocení stupně regrese tumoru po neoadjuvantní onkologické léčbě u pacientů operovaných na I. chirurgické klinice 1. LF UK a VFN v Praze v období 2012−2016
- Výživa u open abdomen
- Multidisciplinárny operačný prístup pri riešení nádoru obličiek s inváziou vena cava a embóliou a. pulmonalis
-
Perforace divertiklu tlustého střeva králičí kostí –
kazuistika
- Rozhledy v chirurgii
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle-
Perioperační výživa ve světle doporučení
(a ve stínu praxe) - Intermitentní výživa v intenzivní péči – teorie a praxe
- Karcinom rekta – současná léčebná strategie a hodnocení stupně regrese tumoru po neoadjuvantní onkologické léčbě u pacientů operovaných na I. chirurgické klinice 1. LF UK a VFN v Praze v období 2012−2016
- Výživa u open abdomen
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



