-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Zkušenosti revizního lékaře s posuzováním výše úhrad biologické léčby v centrech specializované péče
Experience of revision physician in evaluating the extent of compensation of biological therapy in specialized care centers
It is necessary and useful to follow the provision of costly biological therapy by a revision physician. The specialized care centers in collaboration with the attending physician represent professional controlling and revision opportunity to follow the quality of the provided care, the therapeutic effect as well as the aspect of financial compensation and purposeful allocation of financial remedies of public health insurance. The conclusions reached in collaboration with professional representatives of the center made it clear that there is a discrepancy in the level of real financial compensations of the health insurance company and the requirements of the medical institution to increase the established limit of the compensations of “center drugs” in the observed period of time. In connection with the application of biological therapy and provision of professional nursing and medical care it has become obvious that the participation in keeping the records of medical documentation in certain insured individuals was insufficient. In connection with the demonstrated regression and subsequent remission of the disease there is a medical-ethical as well as economic problem to be solved. It is associated with increasing financial cost influenced by purposeful duration of biological therapy as well as the number of therapeutic doses applied, frequency of their repetition in connection with securing a long-term effect of therapy and especially the quality of life of the insured individual. At the same time there is a connection of the decision of the attending physician when and under which conditions to end the therapy “lege artis” with proved clinical effect in favor of the patient and the economic aspect of purposefulness.
Key words:
control – revision physician – care provider – biological therapy – specialized care center – effect of therapy – therapeutic drug compensation – limit of compensation of center drugs – expensive therapy – medical-ethical and economic problem – purposeful therapy – quality of life
Autoři: MUDr. Hynek Dolanský, Ph.D.
Působiště autorů: Česká průmyslová zdravotní pojišťovna
Vyšlo v časopise: Reviz. posud. Lék., 15, 2012, č. 2, s. 58-61
Kategorie: Původní práce
Souhrn
Sledovat poskytování a úhradu nákladné biologické léčby revizním lékařem zdravotní pojišťovny je nezbytné a účelné. Ve spolupráci s ošetřujícími lékaři centra specializované péče představuje odborná kontrolní a revizní činnost také příležitost, jak vyjma finančních úhrad sledovat kvalitu poskytované péče, její léčebný efekt a posuzovat účelné nakládání s finančními prostředky veřejného zdravotního pojištění. Závěry zjištěné ve spolupráci s odbornými zástupci centra prokázaly nesoulad ve výši skutečných finančních úhrad zdravotní pojišťovny vůči požadavku zdravotnického zařízení navýšit stanovený limit úhrad „centrových léků“ ve sledovaném období. V souvislosti s aplikacemi biologické léčby a poskytováním odborné ošetřovatelské a lékařské péče byla u několika pojištěnců zjištěna insuficientní participace ve vedení záznamů zdravotnické dokumentace. V souvislosti s prokázanou regresí a následnou remisí onemocnění vyvstává zde nutnost řešit medicínsko-etický a zároveň ekonomický problém. Je spojen nejen s nárůstem finančních výdajů ovlivňovaných jak účelnou délkou trvání biologické léčby, tak množstvím aplikačních dávek, četností počtu jejich opakování v souvislosti se zajištěním dlouhodobého efektu terapie a především kvality života pojištěnce. Zároveň souvisí s rozhodnutím ošetřujícího lékaře kdy a za jakých podmínek účinnou léčbu s prokázaným klinickým efektem ve prospěch pojištěnce „lege artis“ a zároveň ekonomicky účelně ukončit.
Klíčová slova:
kontrola – revizní lékař – poskytovatel péče – biologická léčba – centrum specializované péče – efekt terapie – úhrada léčiv – limit úhrad centrových léků – nákladná terapie – medicínsko-etický a ekonomický problém – účelná terapie – kvalita životaÚvod
Crohnova choroba a ulcerózní kolitida postihují osoby všech věkových kategorií. Primárně se však jedná o nemoci dospívajících osob a mladých lidí. Typicky se projevují mezi patnáctým a čtyřicátým rokem života a vedou ke snížení jeho kvality.
Indikační kritéria pro biologickou léčbu léčivými přípravky Humira inj., s. c. v průměrné dávce 80 mg s. c. a Remicade 100 mg v infuzní terapii (podle pravidel zavedeného schématu centrem specializované péče) jsou středně těžká až těžká aktivní Crohnova choroba bez odpovědi na léčbu kortikosteroidy nebo imunosupresivy a terapie s fistulující formou choroby bez odpovědi na adekvátní terapii. V uvedených souvislostech léčivý přípravek Humira snižuje zánětlivý průběh onemocnění. Léčivá látka adalimumab je lidská monoklonální protilátka vytvářená buněčnými kulturami. Adalimumab se váže na specifickou bílkovinu (tumor nekrotizující faktor neboli TNF-alfa), která je přítomná ve zvýšené koncentraci u zánětlivých onemocnění.
Remicade – Infliximab blokuje aktivitu klíčového mediátoru biologické odpovědi TNF-alfa, kdy jeho nadprodukce vede k autoimunnímu poškození. Snižuje intestinální zánět vazbou a neutralizací TNF‑alfa na buněčnou membránu a v krvi. Tato aktivita vysvětluje, proč je Remicade zvlášť účinný inhibitor TNF‑alfa a má rychlý a silný klinický účinek včetně hojení endoskopických lézí. Je lékem dokazujícím snížení počtu otevřených fistul.
Specializované pracoviště zdravotnického zařízení – centrum specializované léčby – realizovalo biologickou léčbu indikovanou pojištěncům s Crohnovou chorobou a ulcerózní kolitidou. Požadavek k úhradě léčivých přípravků Humira a Remicade inj. byl zdravotní pojišťovnou na období r. 2010 stanoven smluvně, přílohou ke „Zvláštní smlouvě“ o poskytování a úhradě léčivých přípravků předepisovaných pro léčbu lékařem specializovaného pracoviště s maximální úhradou ve výši 2 600 000, - Kč. Za indikované léčivé přípravky zdravotnickému zařízení uhradila zdravotní pojišťovna v r. 2009 celkem téměř 3 380 000, - Kč.
Zdravotnickým zařízením – v rámci odvolání ke zdravotní pojišťovnou nízce stanovenému limitu – však byla nárokována částka nepoměrně vyšší, celkem 6 200 000, - Kč s požadavkem, aby do celkové výše byli zahrnuti i „rozléčení pojištěnci“, u nichž léčba z období r. 2009 pokračovala dále, po celé období r. 2010.
Cíl
Cílem odborné kontroly provedené revizním lékařem zdravotní pojišťovny s odstupem času a k možnostem řešení finančních úhrad bylo ověřit a posoudit, zda stanovený požadavek zdravotnického zařízení na zvýšení limitu pro úhradu „centrových léků“ byl oprávněný a odpovídal skutečné spotřebě a také , zda aplikace biologické léčby přinesla pojištěncům pozitivní efekt spojený se zlepšením kvality jejich života.
V souvislostech s kontrolou aplikované léčby specialisty zdravotnického zařízení byly k objektivizaci úhrad revizním lékařem stanoveny k posouzení následující okruhy zájmu:
- Kolik pojištěnců bylo k terapii do centra specializované péče indikováno?
- Byla dodržena indikační kritéria k zahájení biologické léčby léčivými přípravky Humira a Remicade inj.?
- Byl z prostudované zdravotnické dokumentace zřejmý efekt léčby?
- Byla zdravotnická dokumentace vedena v souladu s pravidly k vykazování biologické léčby a úhrad zdravotní pojišťovnou?
- Odpovídala spotřeba léčivých přípravků (počet kusů, ampulí v balení) finančním výdajům centra specializované péče a údajům o poskytnuté péči zaznamenané v informačním systému zdravotní pojišťovny?
- Byl požadavek k navýšení finančních prostředků na biologickou léčbu zdravotnickým zařízením oprávněný?
Výsledky a diskuse
Počet léčených pacientů v r. 2009 a plán terapie léčivými přípravky Humira a Remicade inj. pro r. 2010
V roce 2009 bylo ve zdravotnickém zařízení biologickou léčbou léčeno celkem 14 pojištěnců, pěti byla aplikována Humira inj., devíti Remicade inj. V roce 2009 léčivým přípravkem Humira inj. a Remicade inj. byla terapie celkem ukončena ve dvou případech, v roce 2010 podle indikačních kritérií byla zahájena u jednoho pojištěnce. Celkový počet léčených biologickou léčbou v r. 2010 představoval tedy celkem třináct pojištěnců, pět léčených léčivým přípravkem Humira inj. a osm léčivým přípravkem Remicade inj. (tab. 1 – 3)
Tab. 1. Počet léčených LP Humira a Remicade inj. v r. 2009 a plán pro r. 2010 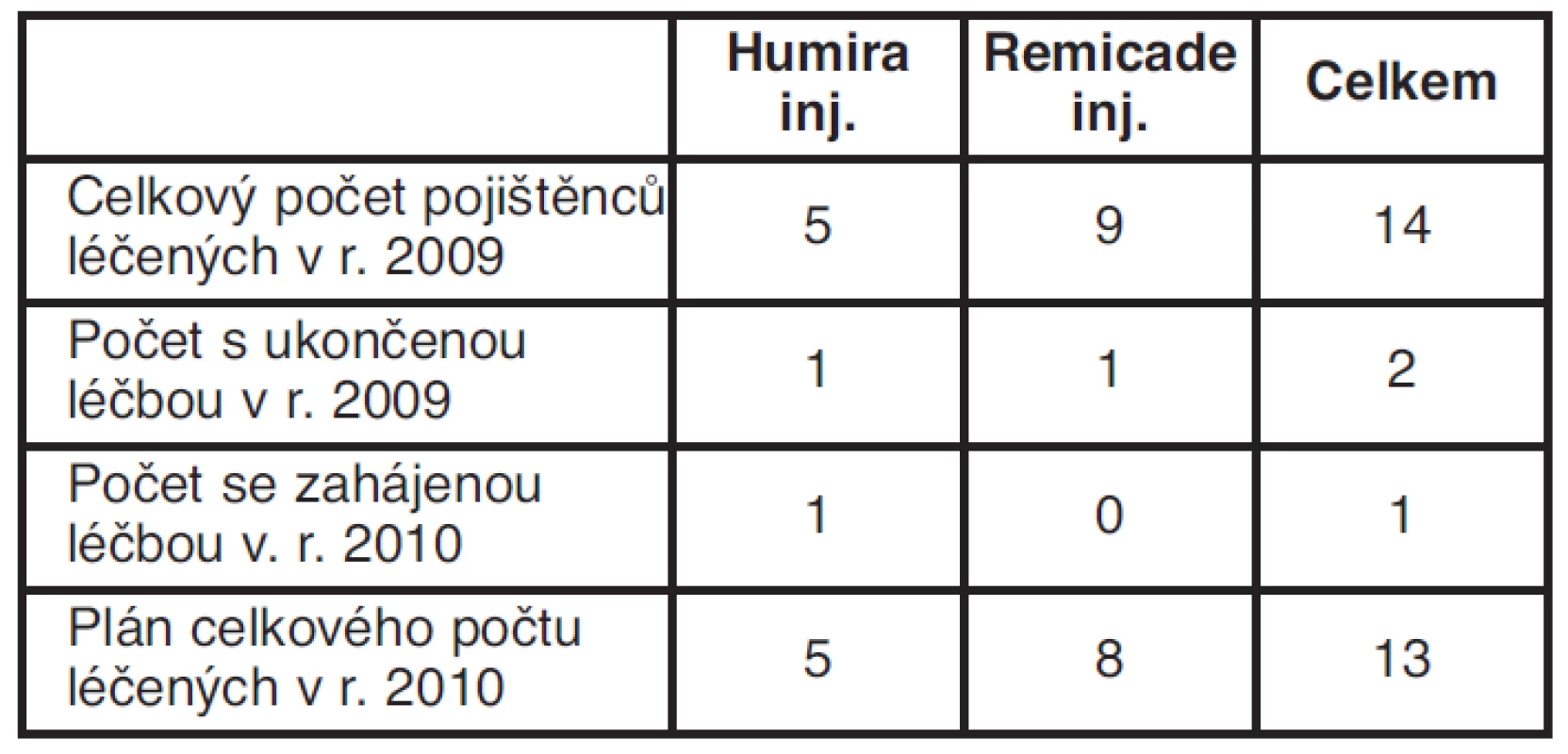
Tabulky 2 a 3 dokladují aplikovanou spotřebu léčivých přípravků podle množství v jednotlivých měsících roku 2009.
Tab. 2. Celková spotřeba počtu balení (kusů) + celkové výdaje Humira inj. á 40 mg u pěti pojištěnců léčených v r. 2009 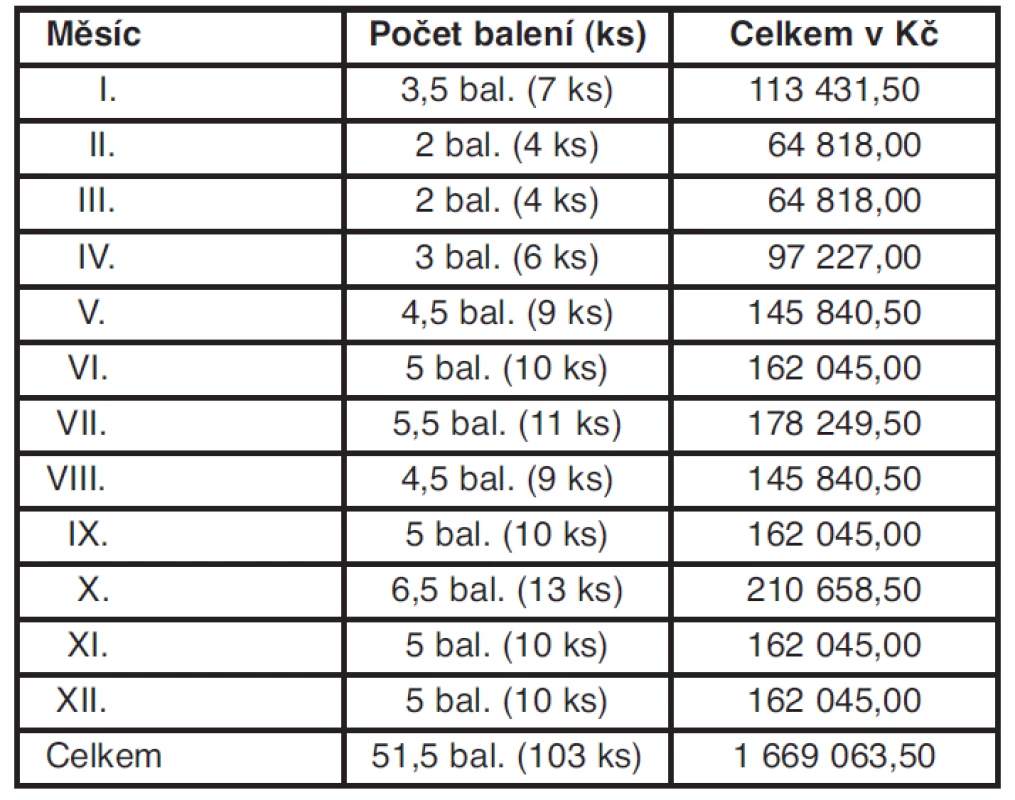
Tab. 3. Celková spotřeba počtu balení (kusů) + celkové výdaje LP Remicade inj. á 100 mg u devíti pojištěnců léčených v r. 2009 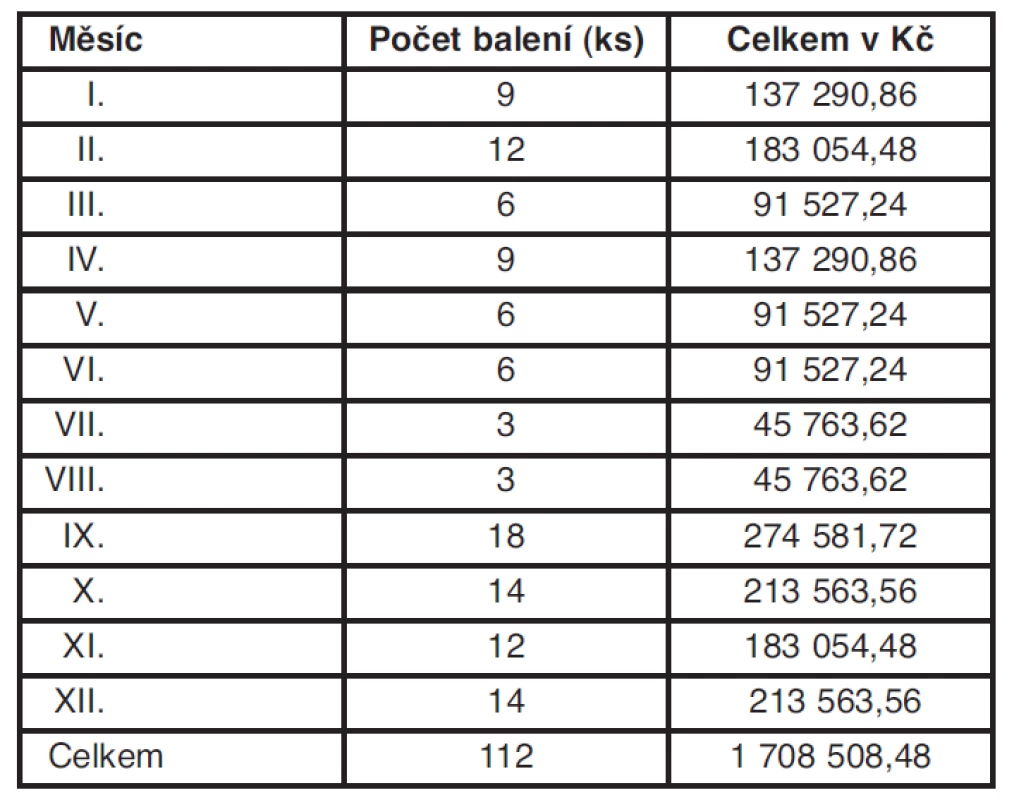
Tabulka 4 dokladuje celkové reálné – skutečné náklady na biologickou léčbu v r. 2009 a 2010, včetně způsobu výpočtu úhrady léčebného režimu v r. 2010.
Tab. 4. Celkové vyčíslení nákladů na biologickou léčbu léčivými přípravky Humira a Remicade inj. v období r. 2009 a 2010 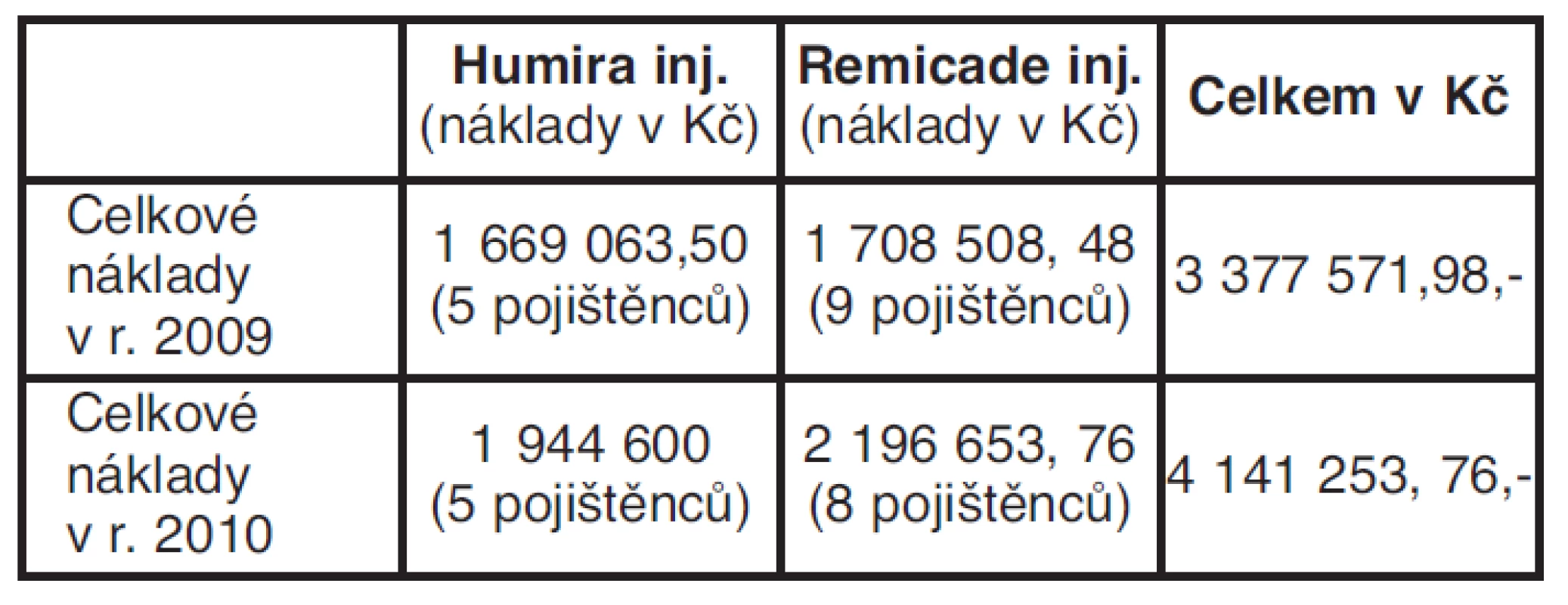
Humira 40 mg s. c., inj., v léčebném režimu každých 14 dní 1 balení (na měsíc = 2 ampule á 32 410 Kč x 12 = 388 920, - Kč x 5 pojištěnců – 1 944 600, - Kč).
Remicade inj., (1 ampule á 100 mg) průměrně v dávce 3 ampule = 300 mg v infuzi 250 ml F roztok, v režimu každé 2 měsíce 45 763, 62, - Kč x v průměru 6 aplikací = 274 582, - Kč x 8 pojištěnců = 2 196 653,76, - Kč.
V roce 2009 bylo do centra specializované péče k biologické léčbě indikováno celkem čtrnáct pojištěnců, pět léčených léčivým přípravkem Humira inj., a devět Remicade inj. Plán a reálná spotřeba v r. 2010 představovala stejný počet pro pět léčených přípravkem Humira inj., přičemž u dvou pojištěnců byla postupně terapie ukončena – u jednoho pro alergickou reakci a u druhého pro změnu místa trvalého bydliště (mimo stávající region specializovaného centra).
Osm pojištěnců bylo léčeno léčivým přípravkem Remicade inj. Pokud se jednalo o věkové zastoupení, jeden pojištěnec měl 21 let, jedna žena 61 a muž 65 let, ostatní léčení byli ve věku od 30 do 40 let.
Kontrolou záznamů ve zdravotnické dokumentaci bylo zjištěno, že pro zahájení biologické léčby byla dodržena indikační kritéria, kdy u všech pojištěnců předcházela dlouhodobá terapie bez odpovědi na léčbu kortikosteroidy nebo imunosupresivy. Průběh léčby byl v časovém odstupu dokladován opakovaně prováděným kontrolním endoskopickým vyšetřením se záznamy gastroenterologa o výsledcích ve zdravotnické dokumentaci pojištěnce.
Záznamy o regresi onemocnění a efektu terapie byly zcela zřejmé, představovaly zlepšení klinického stavu spočívající např. ve zhojení střevních ulcerací, uzavření píštělí, zlepšení fyzické kondice provázené zkvalitněním života apod.
Spotřeba počtu ampulí v balení léčivých přípravků u pojištěnců léčených v období r. 2009 odpovídala jak finančním výdajům centra specializované péče, tak údajům získaným z informačního systému zdravotní pojišťovny. Jiná však byla reálná spotřeba léčiv porovnávaná s požadavkem navýšení limitu úhrady v r. 2010. Reálná výše finanční částky spotřebované na biologickou léčbu v r. 2010 zjištěná provedenou kontrolou představovala celkem 4 141 253, 76, - Kč. Požadavek zdravotnického zařízení tedy nebyl oprávněný a v neprospěch zdravotní pojišťovny se jednalo o finanční částku vyšší o 2 196 653,76, - Kč.
Záznamy vedené odborným ošetřovatelským personálem a lékaři ve zdravotnické dokumentaci v některých případech pojištěnců postrádaly bližší informace spojené především s vlastní aplikací léčiv, se záznamy o jejich klinickém stavu před léčbou a po jejím ukončení, popř. bližší informace spojené s průběhem aplikace infuzí, o subjektivních potížích, o způsobu aplikace apod.
V souvislostech s aplikací finančně nákladné a dlouhodobě poskytované biologické léčby provázené jak prokazatelně příznivým efektem účinku, tak především zkvalitněním života pojištěnců, byla se zástupci vedení centra diskutovaná složitá problematika ukončení léčby. Ta je – při stanovených medicínských kritériích – v reálné praxi lékaře ve spolupráci s dalším odborným zdravotnickým personálem a odborníky provázená také aspekty etickými. Především ve smyslu jak efektivně ekonomicky a přitom lege artis rozhodnout: Za jakých podmínek a kdy léčbu ukončit, kdy a v jaké výši aplikační dávky léčivého přípravku snižovat, či časové intervaly mezi aplikacemi prodlužovat, do jaké míry lze akceptovat možné vedlejší účinky terapie apod.
Lze například již po třech nebo pěti aplikacích podle léčebného plánu při klinicky prokázané remisi onemocnění léčbu definitivně ukončit? Kdy lze pacienta-pojištěnce považovat za vyléčeného?
Diskuse vedené ve smyslu délky trvání léčby onemocnění v závislosti na prokazatelném klinickém efektu účinnosti s rozhodnutím, kdy ji přerušit či ukončit, potvrdily převahu obav lékařů z časných relapsů či progrese onemocnění provázené zhoršením klinického stavu a následné kvality života pacientů-pojištěnců. Z odborného pohledu se k zajištění dlouhodobého efektu účinku biologické léčby v současnosti pro plátce péče jako optimální jeví aplikovat léčbu dlouhodobě, kontinuálně a v pravidelných časových intervalech, až do úplného odeznění příznaků a klinických projevů nemoci. Zcela výjimečně byla v rámci léčebného procesu připuštěna možnost prodlužovat intervaly mezi aplikacemi či snížit dávky aplikovaných léčiv.
V uváděných souvislostech lze všeobecně ze závěrů diskuse uvést:
- Biologickou léčbu je nutné aplikovat včas, v návaznosti na příznivý vývoj nálezu a klinického stavu ji zbytečně neprodlužovat, tedy aplikovat ji účelně, s dlouhodobým efektem účinku.
- Výsledným efektem aplikace biologické léčby je pacientovi-pojištěnci zmírnit a odstranit zdravotní komplikace způsobené nemocí, s cílem zkvalitnit mu především každodenní život.
Závěr
Odborná kontrola potvrdila, že sledovat poskytování a úhradu nákladné biologické léčby revizním lékařem zdravotní pojišťovny je nezbytné. Ve spolupráci s ošetřujícími lékaři představuje příležitost, jak – vyjma výše finančních úhrad za poskytovanou nákladnou biologickou léčbu – lze sledovat především reálnou kvalitu poskytované péče a její skutečný léčebný efekt. V souvislosti s poskytováním odborné ošetřovatelské a lékařské péče spojené s aplikací biologické léčby byla řešena také akceptovatelná podoba obsahu a rozsahu záznamů ve zdravotnické dokumentaci. V souvislosti s regresí a následnou remisí onemocnění však stále trvá problém medicínsko-etický a zároveň ekonomický, spojený s rozhodnutím lékaře, kdy a za jakých podmínek léčbu „lege artis“ a „včas“ ukončit.
Zavedení nákladné biologické léčby v dosavadním režimu je nutno jak poskytovatelem, tak plátcem péče v porovnání s předcházejícími léčebnými postupy, často výrazně méně účinnými, jenž zásadní změnu v kvalitě života často příliš neposkytovaly, v současnosti považovat za relativně ekonomické.
Poděkování: Autor článku děkuje za spolupráci paní Evě Hrabcové, asistentce revizního lékaře ČPZP.
Adresa pro korespondenci:
MUDr. Hynek Dolanský, Ph.D.
V Zálomu 4
700 30 Ostrava-Zábřeh
e-mail: dr.hynek.dolansky@post.cz
Štítky
Posudkové lékařství Pracovní lékařství
Článek vyšel v časopiseRevizní a posudkové lékařství
Nejčtenější tento týden
2012 Číslo 2- Vedolizumab v léčbě středně těžké až těžké aktivní Crohnovy nemoci
- Vedolizumab je vhodný i pro déletrvající léčbu pacientů s IBD
- Nové možnosti v terapii zánětlivých střevních onemocnění
- Přístup k léčbě registrovaným léčivým přípravkem, který nemá stanovenou úhradu z veřejného zdravotního pojištění
- Syndrom dráždivého tračníku a nespecifické střevní záněty nejsou evolučně příbuzná onemocnění
-
Všechny články tohoto čísla
- Screening karcinomu prsu – kontrola a revize oprávněnosti jeho úhrady na smluvních pracovištích VZP ČR Moravskoslezského kraje
- Prevence a screening rakoviny děložního hrdla – kontrola a revize oprávněnosti jeho úhrady na smluvních pracovištích VZP ČR Moravskoslezského kraje
- Vzdělávací akce IPVZ – II. pololetí 2012
- Zkušenosti revizního lékaře s posuzováním výše úhrad biologické léčby v centrech specializované péče
- Vertebrogenní algický syndrom z pohledu pojistných a nepojistných systémů
- Karcinom prsu v posudkovém lékařství
- Senioři – kvalita života, zdravotní péče a sociální zabezpečení
- Revizní a posudkové lékařství
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Vertebrogenní algický syndrom z pohledu pojistných a nepojistných systémů
- Karcinom prsu v posudkovém lékařství
- Zkušenosti revizního lékaře s posuzováním výše úhrad biologické léčby v centrech specializované péče
- Senioři – kvalita života, zdravotní péče a sociální zabezpečení
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Revma Focus: Spondyloartritidy
nový kurz
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Autoři: prof. MUDr. Pavel Horák, CSc., doc. MUDr. Ludmila Brunerová, Ph.D., doc. MUDr. Václav Vyskočil, Ph.D., prim. MUDr. Richard Pikner, Ph.D., MUDr. Olga Růžičková, MUDr. Jan Rosa, prof. MUDr. Vladimír Palička, CSc., Dr.h.c.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



