-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Porovnání účinků ranibizumabu a pegaptanibu sodného na velikost ablace RPE při léčbě vlhké formy věkem podmíněné makulární degenerace
The Effect Comparison of Ranibizumab and Sodium Pegaptanib on the Retinal Pigment Epithelium Ablation Size in the Treatment of Age-Related Macular Degeneration
Aim:
To evaluate the effect difference of Ranibizumab and Sodium Pegaptanib in the ablation treatment of the retinal pigment epithelium (RPE) in age-related macular degenerationMaterial and methods:
Retrospective analysis of data of patients with age-related macular degeneration treated by means of anti-VEGF therapy at the Department of Ophthalmology, School of Medicine, Palacký University, Olomouc, Czech Republic, E.U. during the period May 2009 – October 2010. For the analysis were used data from patients with follow-up period longer than 6 months and present serous RPE ablation caused by occult choroidal neovascularization (CNV), verified by optic coherence tomography (OCT) and fluoresceine angiography (FAG).Study group:
Ranibizumab was used as treatment during the period in 37 eyes of 37 patients (average age 73.2 years; right eye (RE) in 20 cases, left eye (LE) in 17 cases. Sodium pegaptanib was applied in 17 eyes of 17 patients (average age 72.4 years; RE in 10 cases and LE in 7 cases), The follow-up period in the ranibizumab group was 8.51 (SD 3.32) months, and in the pegaptanib group 9.94 (SD 5.50) months.Results:
In the ranibizumab group decreased the average RPE ablation base from 2865 μm (SD 810 μm) to 2270 μm (SD 1265 μm) and the prominence of the ablation from 334 μm (SD 160) to 238 μm (SD 178 μm). In patients treated by pegaptanib, decreased the average basis from 3245 μm (SD 930 μm) to 2159 μm (SD 1185 μm), and the prominence of the ablation from 354 μm (SD 173 μm) to 208 μm (SD 107 μm). The statistical significance test did not prove significant differences (level of significance p = 0.05) in the change either of the base or the prominence of the RPE ablation in any group of patients (prominence p = 0.09, base p = 0.21; Mann-Whitney test). In three patients (8.1 %) treated by ranibizumab, the RPE rupture occurred. No RPE rupture was recorded in patients treated by sodium pegaptanib.Conclusion:
Although no statistically significant difference in the efficacy of both drugs in the treatment of the RPE ablation was found, in patients treated by sodium pegaptanib, there is evident tendency of higher efficacy in decrease of the RPE ablation prominence, and lower incidence of RPE rupture. The study is limited by small number of patients and short follow-up period.Key words:
age-related macular degeneration, retinal pigment epithelium ablation, retinal pigment epithelium rupture, ranibizumab, sodium pegaptanib
Autoři: M. Šín; M. Jakubcová; O. Chrapek; Z. Prachařová; J. Šimičák; J. Řehák
Působiště autorů: Oční klinika FN a UP, Olomouc, přednosta: doc. MUDr. Jiří Řehák CSc., FEBO
Vyšlo v časopise: Čes. a slov. Oftal., 68, 2012, No. 2, p. 57-60
Kategorie: Původní práce
Souhrn
Cíl:
Zhodnocení rozdílnosti účinku preparátů ranibizumab a pegaptanib sodný v léčbě ablace pigmentového listu sítnice (RPE) při věkem podmíněné makulární degeneraci (VPMD).Metoda:
Retrospektivní analýza pacientů léčených anti-VEGF terapií pro věkem podmíněnou makulární degeneraci na Oční klinice FN a LF UP Olomouc v období od května 2009 do října 2010. Do analýzy byli zařazeni pacienti se sledovací dobou delší než 6 měsíců a přítomnou serózní RPE na podkladě okultní choroidální neovaskularizace (CNV), potvrzenou optickou koherentní tomografii (OCT) a fluorescenční angiografií (FAg).Soubor:
Preparátem ranibizumab bylo ve sledovaném období léčeno37 očí 37 pacientů (průměrný věk 73,2 let; 20x pravé oko (OD)/17x levé oko (OS)). Pegaptanib sodný byl aplikován u 17 pacientů do 17 očí (průměrný věk 72,4 let; 10 x OD/7xOS). Sledovací doba ve skupině s ranibizumabem byla 8,51 (SD 3,32) měsíce a ve skupině s pegaptanibem 9,94 (SD 5,50) měsíce.Výsledky:
Ve skupině léčené ranibizumabem klesla průměrná šířka ablace RPE z 2865 μm (SD 810) na 2270 μm (SD 1265) a výška ablace z průměrných 334 μm (SD 160) na 238 μm (SD 178). U pacientů léčených pegaptanibem klesla průměrná šířka z 3245 μm (SD 930) na 2159 μm (SD 1185) a průměrná výška z 354 μm (SD 173) na 208 μm (SD 107). Test statistické významnosti neprokázal významné rozdíly (při a významnosti p = 0,05) ve změně výšky ani šířky ablace RPE v žádné skupině pacientů (výška p = 0,09, šířka p = 0,21; Mann-Whitney test) U tří pacientů ve skupině léčených ranibizumabem (8,1 %) došlo ve sledovaném období k ruptuře RPE. U pacientů léčených pegaptanibem sodným ruptura RPE zaznamenána nebyla.Závěr:
Přestože nebyl prokázán statisticky významný rozdíl v účinnosti obou preparátu v léčbě ablace RPE, u pacientů léčených pegaptanibem sondným se jeví jednoznačný trend vyšší účinnosti při oploštění výšky ablace RPE a nižší incidence ruptury RPE. Limitem studie je malý počet pacientů a krátká sledovací doba.Klíčová slova:
věkem podmíněná makulární degenerace, ablace retinálního pigmentového listu, ruptura retinálního pigmentového listu, ranibizumab, pegaptanib sodnýPředneseno ve zkrácené verzi na XII. Vejdovského dnu, Olomouc 2012
Úvod
Ablace pigmentového listu sítnice (RPE) je běžným projevem exsudativní věkem podmíněné makulární degenerace (VPMD) většinou v podobě vaskulární serózní ablace RPE (15). Vaskulární serózní ablace RPE představuje přibližně 10 % všech případů exsudativní VPMD (12). Vaskulární serózní ablace RPE vzniká na podkladě marginálně lokalizované okultní choroidální neovaskularizace (CNV), nebo centrální retinální angiomatózní proliferace. Byla popsána také jako projev polipoidní choroidální vaskulopatie (1). Neléčená vaskulární serózní ablace RPE vede v počátku k pomalému zhoršování centrální zrakové ostrosti (ZO) na podkladě postupné progrese atrofických změn. V konečném stadiu dochází k vytvoření disciformní jizvy. Celý proces může být dramaticky urychlen rupturou RPE nebo subretinálním krvácením (15).
Ruptura RPE představuje komplikaci, která vede k výraznému zhoršení centrální ZO. Poprvé byla popsána Hoskinem et al. v roce 1981 (6). Ablace RPE je nezbytným předpokladem pro vznik ruptury RPE. Dle práce Caswella et al., může spontánní ruptura komplikovat přibližně 10 % všech ablací RPE (2). V posledních letech se ruptura RPE vrací do popředí zájmu odborné veřejnosti vzhledem k diskutovanému možnému vlivu anti-VEGF terapie na zvýšení její incidence (8).
Přes výrazné změny, které přineslo zavedení preparátů blokujících vaskulární endotelový růstový faktor (VEGF), zůstává léčba ablace RPE stále velmi komplikovanou záležitostí. Laserová fotokoagulace a fotodynamická terapie, léčebné metody dostupné před érou anti-VEGF preparátů, často selhávaly pro vysoké procento relapsů CNV, respektive vysoké riziko výskytu ruptury RPE (12). Anti-VEGF preparáty se sice jeví jako metoda účinnější, stále však mají svá rizika a limity.
V součastné době jsou pro léčbu VPMD k dispozici 3 anti-VEGF preparáty: ranibizumab (Lucentis) a pegaptanib sodný (Macugen) jsou schváleny úřadem Spojených států pro potraviny a léčiva (FDA) k použití v indikaci exsudativní VPMD. Bevacizumab (Avastin) má schválení FDA jen pro onkologické indikace, avšak vzhledem k ceně je široce používán po celém světě i v oční indikaci (14). Pegaptanib sodný blokuje pouze VEGF-A isoformu 165, která byla identifikována jako nejdůležitější při růstu patologické CNV (10). Ranibizumab a bevacizumab blokují všechny isoformy VEGF-A. Rozdílné klinické vlastnosti ranibizumabu a pegaptanibu byly dobře doloženy v mnoha prospektivních studiích i v post-marketingovém klinickém sledování (5, 9, 16). Bevacizumab byl porovnáván ve studii CATT s ranibizumabem, kde účinnost i bezpečnostní profil byly bez statistického rozdílu u obou preparátů (3). Obecně jsou dnes neselektivní preparáty považovány za účinnější v léčbě CNV na podkladě exsudativní VPMD.
Metoda a soubor pacientů
Retrospektivní analýza optické koherentí tomografie (OCT) pacientů léčených ranibizumabem nebo pegatanibem sodným pro věkem podmíněnou makulární degeneraci na Oční klinice FN a LF UP Olomouc v období od května 2009 do října 2010. Do analýzy byli zařazeni pacienti s delší sledovací dobou než 6 měsíců a přítomnou serózní ablací RPE na podkladě okultní CNV, potvrzenou vyšetřením OCT (Cirrus, Zeiss Meditech, Dubline, CA, USA) a fluorescenční angiografií (FAg) před zahájením anti-VEGF terapie. Ve všech případech šlo o pacienty bez předchozí léčby exsudativní VPMD.
Preparátem ranibizumab bylo ve sledovaném období léčeno 37 pacientů (37 očí) s ablací RPE. Průměrný věk pacientů v této skupině byl 73,2 roku. Ve skupině bylo 25 žen a 12 mužů.Ve 20 případech bylo postiženo oko pravé a v 17 oko levé. Pegamtanib sodný byl aplikován u 17 pacientů (17 očí) s věkovým průměrem 72,4 let. Ve skupině bylo 11 žen a 6 mužů. Pravé oko bylo v této skupině postiženo v 10 případech a levé v 7 případech. Průměrná sledovací doba ve skupině s ranibizumabem byla 8,51 (SD 3,32) měsíce a ve skupině s pegaptanibem 9,94 (SD 5,50) měsíce.
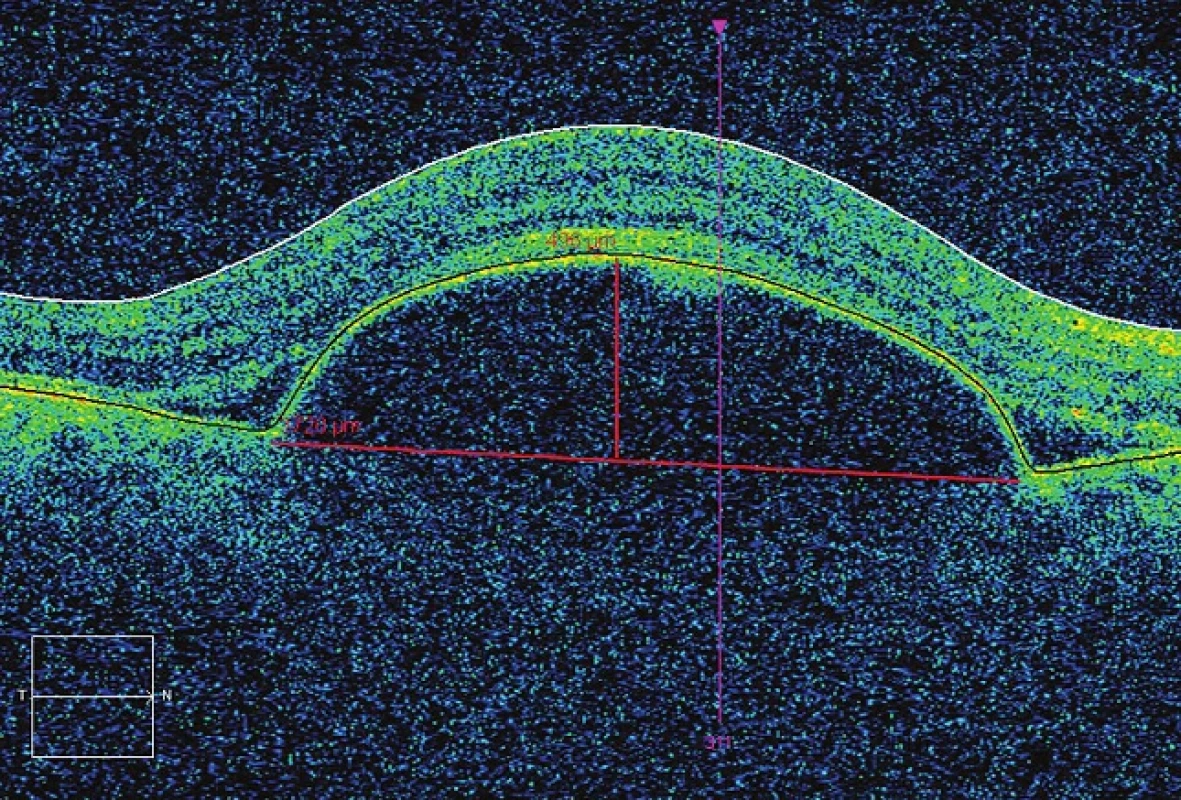
U všech pacientů bylo provedeno měření rozměru ablace RPE u skenu „fast macular 512x200“. Měření bylo provedeno manuálně softwarovým kaliperem v místě nejširšího a nejvyššího rozměru (programem Cirrus HD-OCT verze 5.2.0.210) obr. 1. Metoda byla popsána a provedena Chanem et al. (7). Každý pacient podstoupil měření před zahájením intravitreální léčby a dále na konci sledovací doby. Léčba anti-VEGF preparáty probíhala dle standardního protokolu Oční kliniky FN a LF UP Olomouc. Ranibizumab 0,5 mg intravitreálně s iniciální fází 3 aplikací po měsíci a dále dle potřeby. Pegaptanib sodný 1,25 mg v intervalu 6 týdnů po dobu 1 roku.
Výsledky
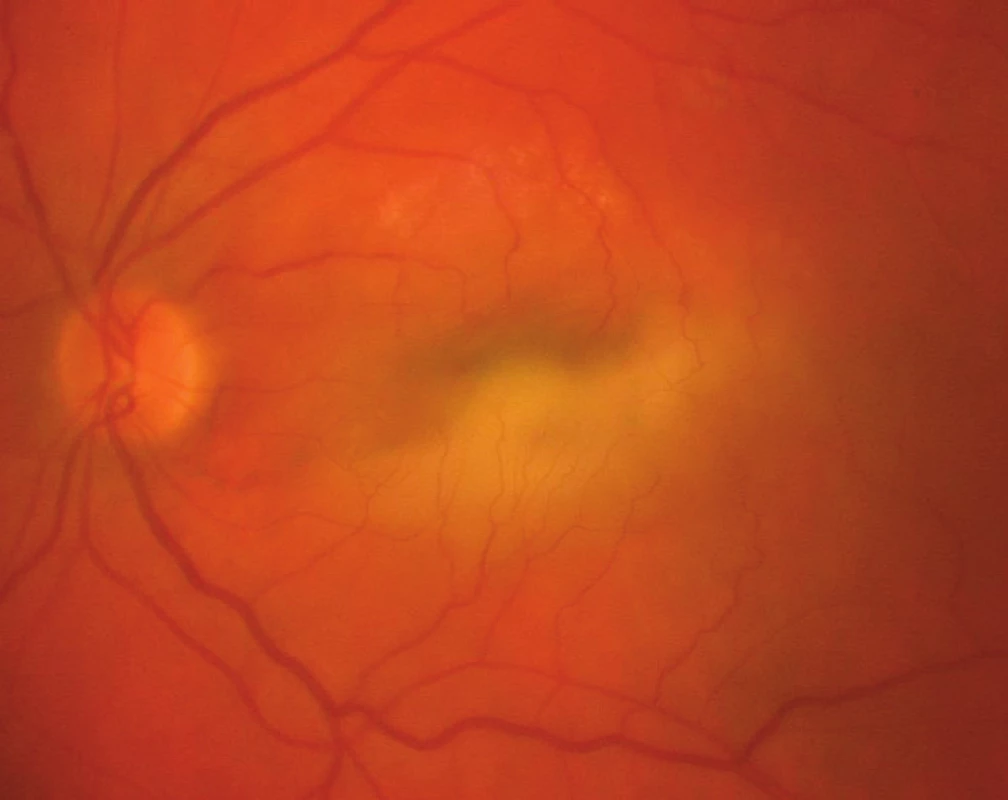
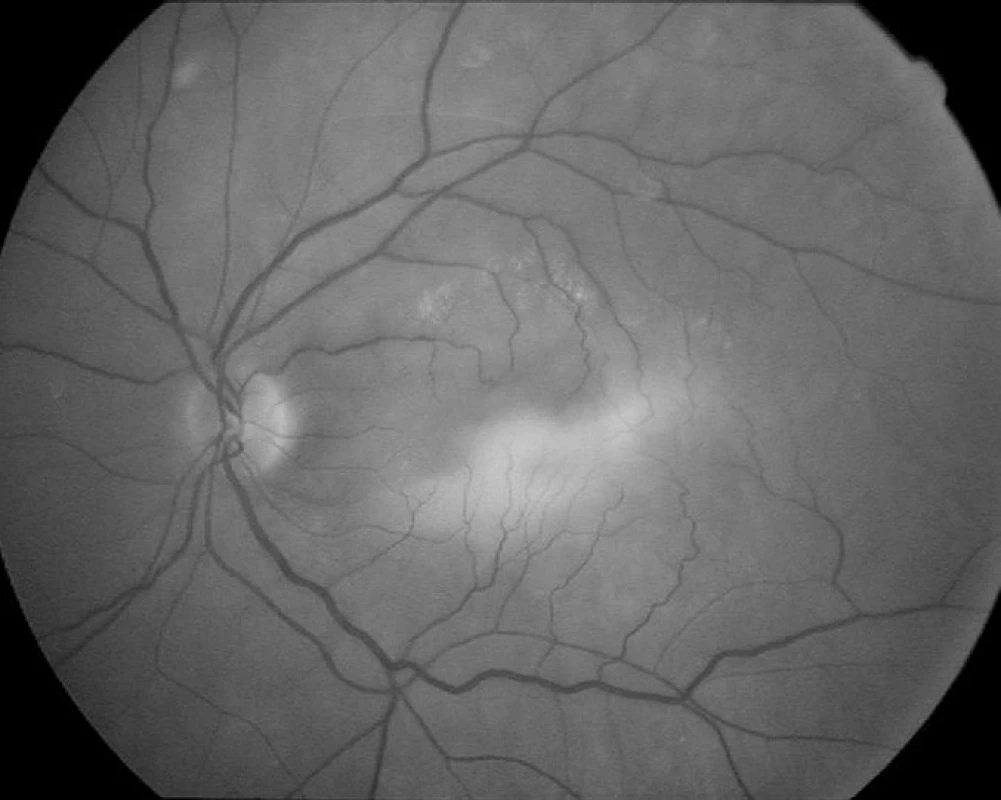
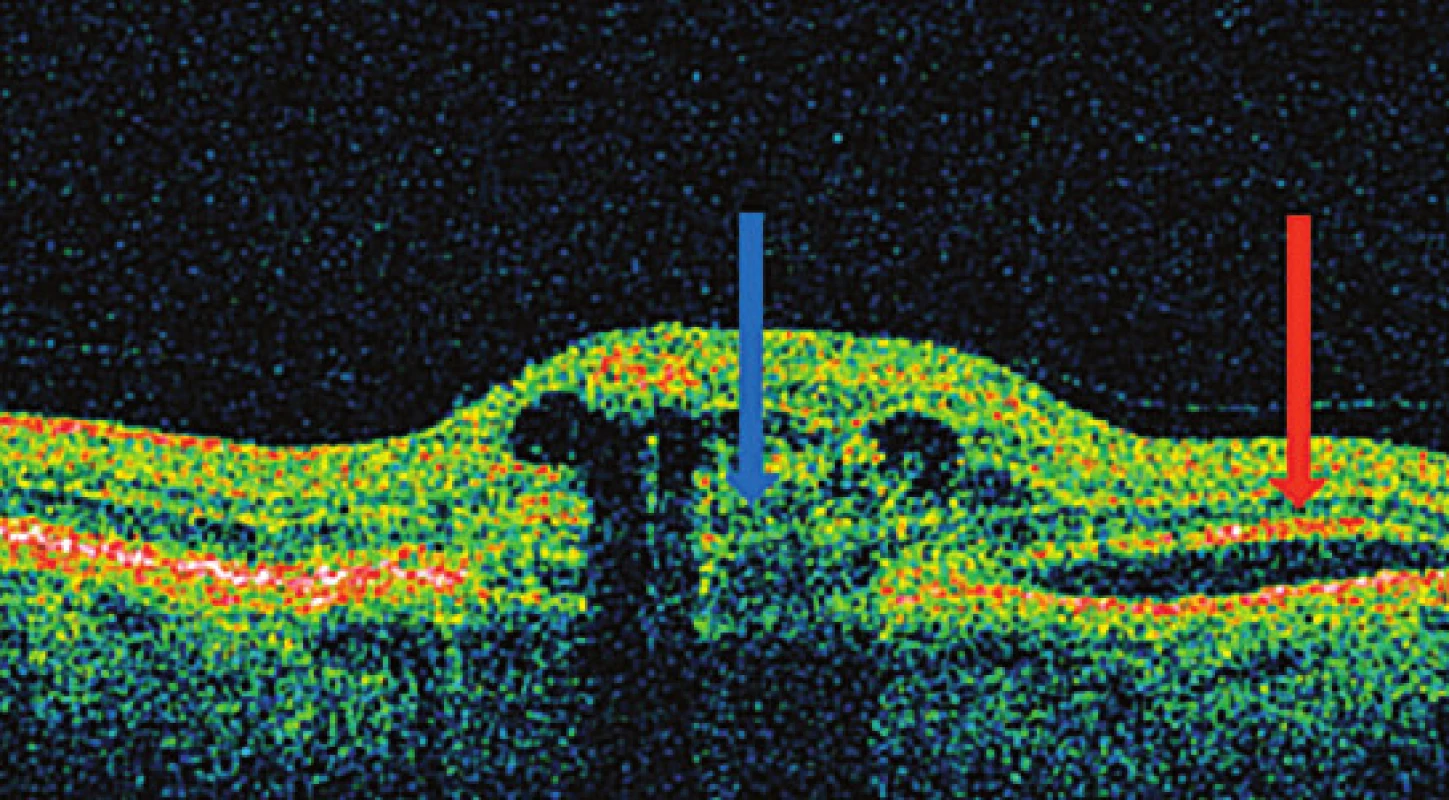
Ve skupině pacientů léčených ranibizumabem dostal pacient ve sledovaném období průměrně 5,64 aplikací. Stejný parametr byl u pacientů léčených pegaptanibem sodným 6,43 aplikace. Ve skupině léčené ranibizumabem došlo ve 3 případech k ruptuře RPE (obr. 2, 3, 4). Ruptura RPE se vyskytla u 2 žen a 1 muže. Časový odstup od zahájení anti VEGF terapie byl rozdílný. V prvním případě nastala ruptura v odstupu 4 dnů po 2. injekci ranibizumabu (36. den po zahájení terapie), u druhého pacienta v odstupu 10 dnů od 2. intravitreální aplikace (42. den po zahájení terapie), v posledním případě 7. den po 5. aplikaci (163. den po zahájení terapie). Výška ablace RPE byla před zahájením anti-VEGF terapie (512 μm, 621 μm, 457 μm) U všech tří pacientů došlo k výraznému zhoršení centrální ZO na úroveň počítání prstů s ohledem na centrální lokalizaci ruptur RPE. Ruptura RPE vedla k vyřazení těchto pacientů z finálního hodnocení rozměrů ablace pro nemožnost měření sledovaných rozměrů. Průměrné hodnoty rozměrů ablace ve skupině léčených ranibizumabem jsou tedy počítány u 34 pacientů. Ve skupině pacientů léčených pegaptanibem sodným ve sledovaném období k žádné ruptuře RPE nedošlo. Všech 17 pacientů je hodnoceno před i po léčbě.
Ve skupině léčené ranibizumabem klesla průměrná šířka ablace RPE z 2865 μm (SD 810) na 2270μm (SD 1265) a výška ablace z průměrných 334 μm (SD 160) na 238 μm (SD 178). U pacientů léčených pegaptanibem klesla průměrná šířka z 3245 μm (SD 930) na 2159 μm (SD 1185) a průměrná výška z 354 μm (SD 173) na 208 μm (SD 107). Ve skupině pacientů léčených preparátem ranibizumab bylo před léčbou 11 pacientů (29,73 %) s výškou ablace přesahující 400 μm a ve skupině léčených pegaptanibem sodným bylo takových pacientů 5 (29,41 %). Test statistické významnosti neprokázal významné rozdíly (při hladině významnosti p = 0,05) ve změně výšky ani šířky ablace RPE v žádné skupině pacientů (výška p = 0,09, šířka p = 0,21; Mann-Whitney test).
Diskuse
Naše výsledky ukazují vzhledem k doposud publikovaným datům překvapivě vyšší účinnost pegaptamibu sodného při snižování výšky ablace RPE. Přesto, že výsledky nedosáhly statisticky signifikantní hodnoty, je zde patrný jasný trend ve schopnosti oploštit i zmenšit ablaci RPE u preparátu pegaptanib sodný. Navíc u pacientů léčených ranibizumabem byl stav ve třech případech komplikován rupturou RPE, zatímco podobná komplikace se u pacientů léčených pegaptanibem sodným nevyskytla. Doposud prezentované práce ukazovaly výsledky opačné. Lommatzsch et al. prezentoval retrospektivní soubor 274 očí u pacientů s ablací RPE na podkladě neovaskulární VPMD léčených všemi 3 dnes dostupnými anti-VEGF preparáty. Výsledkem bylo statisticky signifikantní zlepšení ZO i oploštění ablace RPE u pacientů léčených neselektivními preparáty ranibizumab a bevacizumab v porovnání s pacienty léčenými pegaptanibem sodným (12).
Pravdou zůstává, že neselektivní preparáty jsou zřejmě účinnější u většího počtu pacientů a pokud pacient nedostatečně reaguje na pegaptanib sodný, je možno se pokusit o změnu léčby na neselektivní preparát. Tento fakt je v léčbě ablace dokumentován kazuistickými případy a nepříliš velkým souborem (11, 13, 17). Dle našeho názoru existuje doposud neobjasněný rozdíl v charakteru CNV, které mají zřejmě rozdílnou expresi jednotlivých isoforem VEGF. Otázkou dalšího výzkumu zůstává, zda jde o vrozenou genetickou predispozici, či výsledek selekčního tlaku na úrovni buněk RPE.
Dále v našem souboru byla rozdílná incidence trhlin RPE – jednoznačně převažuje ruptura u pacientů léčených ranibizumabem. Doposud nebyl publikován soubor, který by přímo porovnával rozdíl účinku těchto dvou preparátů na eventuální incidenci trhliny RPE. Některé práce dokonce vyvracejí vliv anti-VEGF preparátu na incidenci ruptury RPE (4) a vznik této komplikace připisují přirozenému průběhu choroby. V současnosti je však anti-VEGF terapie převážně uznávána jako rizikový faktor vzniku ruptury s incidencí kolem 17 % případů u pacientů s ablací RPE (7, 8). Za samostatný rizikový faktor je považována výška ablace více než 400 μm (7). Ve všech případech námi prezentovaných případech byl tento rizikový faktor přítomen, ale přítomnost tohoto rizikového faktoru je v obou sledovaných skupinách prakticky totožná. Ruptura RPE vzniká pravděpodobně na podkladě kontrakce CNV po anti-VEGF léčbě. Vyšší účinnost neselektivních preparátů by mohla být vysvětlením vyšší incidence ruptur RPE. Dalším hypotetickým vysvětlením rozdílu incidence ruptury RPE, vyplývajících z našich dat, by tedy mohla být vyšší schopnost pegaptanibu sodného eliminovat výšku ablace, jako rizikový faktor.
Problémem léčby ablace RPE zůstává schopnost průniku intravitreálně podaných anti-VEGF preparátů ze sklivcového prostoru skrz neporušený RPE. Schopnost průniku přes abladovaný RPE nebyl dle našich znalostí doposud prozkoumán ani u zvířecích modelů či lidských pacientů. V této oblasti by mohla být odpověď na eventuelní vyšší účinnost pegaptanibu sodného, který je RNA aptamerem s hypoteticky vyšší schopností penetrace pod ablaci RPE.
ZO nebyla záměrně předmětem našeho hodnocení. Důvodem je poměrně pomalá počáteční progrese zhoršení ZO u pacientů s ablací RPE, která je způsobena převážně atrofickými změnami makulární oblasti (15). Změny ZO na podkladě atrofických změn má dle našeho názoru cenu hodnotit v delším časovém období. Dále vzhledem k malému počtu pacientů by tři případy ruptury RPE s výrazným zhoršením ZO vedly k výraznému zkreslení konečného výsledku.
Závěr
Přestože nebyl prokázán statisticky významný rozdíl v účinnosti obou preparátu v léčbě ablace RPE, u pacientů léčených pegaptanibem sodným se jeví jednoznačný trend vyšší účinnosti při oploštění ablace RPE. Limitem studie je malý počet pacientů a krátká sledovací doba. V současnosti nemáme dostatek informací k jednoznačnému doporučení léčby ablace RPE. Je nutno provést další studie k jednoznačnému doporučení pegaptanibu sodného v léčbě vaskulární ablace RPE na podkladě okultní membrány.
Do redakce doručeno dne: 20. 2. 2012
Do tisku přijato dne: 7. 5. 2012
MUDr. Martin Šín, FEBO
Oční klinika UP a FN
I. P. Pavlova 6
775 20 Olomouc
e-mail: sin.martin@seznam.cz
Zdroje
1. Ahuja, R.M., Stannga, P.E., Vingerling, J.R., et al.: Polypoidal choroval vasculopathy in exsudative and hemorrhagic pigment epithelial detachment, Br J Ophtalmol, 84; 2000 : 479–484.
2. Casswell, A.G., Kohen, D., Bird, A.C.: Retinal pigment epithelial detachments in the elderly: classification and outcome, Br J Ophthalmol, 69; 1985 : 397–403.
3. CATT Research Group, Martin, D.F., Maguire, M.G., et al.: Ranibizumab and bevacizumab for neovascular age-related macular degeneration, N Engl J Med. 364; 2011 : 1897–908.
4. Cunningham, E.T.Jr., Feiner, L., Chung, C. et al.: Incidence of retinal pigment epithelial tears after intravitreal ranibizumab injection for neovascular age-related macular degeneration, Ophthalmology, 118; 2011 : 2447–2452.
5. Gragouhas, E.S., Adami, A.P., Cunningham, E.T., et al.: VEGF inhibation study in ocular neovaskularisation clinical trial group. Pegaptanib for neovascular age-relatd macular degeneration. N Engl J Med. 351; 2004 : 2805–2816.
6. Hoskin, A., Bird, A.C., Sehmi, K.: Tears of detached retinal pigment, Br J Ophthalmol., 65; 1981 : 417–422.
7. Chan, C.K., Abraham, P., Meyer, C.H., et al.: Optical coherence tomography-measured pigment epithelial detachment height as a predictor for retinal pigment epithelial tears associated with intravitreal bevacizumab injections, Retina, 30; 2010 : 203–211.
8. Chang, L.K., Sarraf, D.: Tears of the RPE: an old problem in a new era, Retina, 27; 2007 : 523–527.
9. Chrapek, O., Pitrová, Š., Dušek, L., et al.: Výsledky léčby vlhké formy věkem podmíněné makulární degenerace u pacientů evidovaných v celonárodním registru AMADEUS, Čes a lov Oftal, 66; 2010 : 110–118.
10. Ischida, S., Usui, T., Yamasiro, K., t al.: VEGF 164-mediated inflamtion is required for patological but not physiological, ischemia-induce retinal neovascularisation, J Exp Med, 198; 2003 : 483–489.
11. Khetpal, V., Heimmel, M.R., Rao, S.K., et al.: Resolution of retinal pigment epithelial detachment associated with exsudative age-related macular degeneration following intravitreal ranibizumab therapy, Acta Ophthalmol, 87; 2009 : 115–116.
12. Lommatzsch, A.P., Heimes, B., Gutfleisch, M., et al.: Serous pigment epithelial detachment in age-related macular degeneration: comparison of different treatments, Eye, 23; 2009 : 2163–2168.
13. Lommatzsch, A.P., Heimes B., Gutfleisch M., et al.: Treatment of vascularised serous pigment epithelium detachment in AMD - observations after changing the intravitreal agent due to lack of response, Klin Monatsbl Augenheilkd, 225; 2008 : 874–879.
14. Manish, N., Kamal, N., Nagpal, M.S.: A comparative debate on the various anti-vascular endothelial growth factor drugs: Pegaptanib sodium (Macugen), ranibizumab (Lucentis) and bevacizumab (Avastin), Ind J Oph, 55; 2007 : 437–439.
15. Pauleikhoff, D., Loffert, D., Spital, G., et al.: Pigment epithelial detachment in the eldery – clinical differentiation, natural course and pathogenetic implications, Graef. Arch Clin Exp Oph, 240, 2004 : 533–538
16. Studnička J.: Ranibizumab (Lucentis) v léčbě věkem podmíněné makulární degenerace, Čes a lov Oftal, 65; 2009 : 107–111.
17. Šín M., Šimičák J., Prachařová Z., et al.: Pegaptanib sodný a ranibizumab v léčbě ablace pigmentového listu sítnice u pacienta s věkem podmíněnou makulární degenerací – kazuistika, Čes a slov Oftal, 66; 2010 : 138–141.
Štítky
Oftalmologie
Článek vyšel v časopiseČeská a slovenská oftalmologie
Nejčtenější tento týden
2012 Číslo 2- Selektivní laserová trabekuloplastika nesnižuje nitroční tlak více než argonová laserová trabekuloplastika
- Progresi glaukomu je třeba hodnotit strukturálními i funkčními parametry
- Ztráta centrálního vidění po filtrujících operacích glaukomu
- Od PGF-2 alfa-isopropyl esteru k latanoprostu: přehled vývoje Xalatanu
- Compliance u pacientů s glaukomem
-
Všechny články tohoto čísla
- Hodnocení bakteriální kolonizace spojivkového vaku pacientů léčených intravitreálními injekcemi ranibizumabu
- Porovnání účinků ranibizumabu a pegaptanibu sodného na velikost ablace RPE při léčbě vlhké formy věkem podmíněné makulární degenerace
- Diabetický makulární edém – nové možnosti léčby
- Akutní retinální nekróza
- Opakovatelnost a spolehlivost vyšetření zrakové ostrosti na optotypových tabulích logMAR ETDRS a Snellen
- VOT králikov po instalácii zmesi L-Argininu.HCL so zvolenými antiglaukomatikmi pripravenej in vitro
- Posudková kritéria v oftalmologii
- Koincidence lokalizace defektů vrstvy junkce IS/OS fotoreceptorů na SD OCT s funkčními poruchami v případě Stargardtovy choroby
- Česká a slovenská oftalmologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Posudková kritéria v oftalmologii
- Opakovatelnost a spolehlivost vyšetření zrakové ostrosti na optotypových tabulích logMAR ETDRS a Snellen
- Akutní retinální nekróza
- Diabetický makulární edém – nové možnosti léčby
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání