-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Nesteroidovými antireumatikami indukovaná kolopatia imitujúca Crohnovu chorobu
Non-steroidal anti-inflammatory drugs induced colopathy, mimicking Crohn’s disease
The authors describe the case of a 47-year-old woman with rheumatoid arthritis who took, in the long term, nonsteroidal anti-inflammatory drugs (NSAID). Her state was complicated by sideropenic anaemia with high inflammatory humoral response during complete rheumatological therapy. She was examined by a gastroenterologist. Colonoscopy revealed severe colitis, which was preliminarily evaluated as a Crohn’s disease and a complete therapy including infliximab was administered. However, her condition did not improve and repeated colonoscopy was carried out. This investigation revealed a worse finding with severe continuous ulcerations of the large bowel. The diagnosis was re-evaluated for NSAID induced colopathy. The previous therapy was stopped and colectomy with ileosigmoideostomy was performed. After surgery the patient was feeling well, had no anaemia, and the humoral anti-inflammatory response decreased. The authors present a review of NSAID induced colopathy which can mimic Crohn’s disease.
Key words:
colopathy – non-steroidal anti-inflammatory drugs (NSAID) – Crohn’s disease – rheumatoid arthritis
Autoři: L. Gombošová 1; M. Zakuciová 1; E. Veseliny 1; I. Drahovská 2; M. Švajdler 3; J. Bober 4; M. Oetterová 1
Působiště autorů: I. Interná klinika, Univerzitná nemocnica L. Pasteura, Košice, 2Klinika rádiodiagnostiky a zobrazovacích metód, Univerzitná nemocnica L. Pasteura, Košice, 3Oddelenie patológie, Univerzitná nemocnica L. Pasteura, Košice, 4I. chirurgická klinika, Univerzitn 1
Vyšlo v časopise: Gastroent Hepatol 2010; 64(6): 15-20
Kategorie: Kazuistika
Souhrn
Autori popisujú prípad 47ročnej ženy s reumatoidnou artritídou, ktorá dlhodobo užívala nesteroidné antireumatiká. Počas kompletnej reumatologickej liečby sa stav komplikoval sideropenickou anémiou s vysokou zápalovou aktivitou. Bola vyšetrená gastroenterológom. Kolonoskopia odhalila závažnú kolitídu, ktorá bola predbežne hodnotená ako Crohnova choroba. Pacientke bola aplikovaná kompletná gastroenterologická liečba, vrátane infliximabu. Pre nezlepšovanie stavu bola realizovaná kontrolná kolonoskopia, ktorá ukázala zhoršenie nálezu so závažnými kontinuálnymi ulceráciami hrubého čreva. Diagnóza bola prehodnotená na kolopatiu indukovanú nesteroidovými antireumatikami. Pôvodná liečba bola ukončená a realizovaná kolektómia s ileosigmoanastomózou. Po operácii bola pacientka bez ťažkostí, krvný obraz sa upravil, klesla zápalová aktivita. Autori podávajú prehľad o kolopatii indukovanej nesteroidovými antireumatikami, ktorá môže imitovať Crohnovu chorobu.
Kľúčové slová:
kolopatia – nesteroidové antireumatiká – Crohnova choroba – reumatoidná artritídaÚvod
Nesteroidné antireumatiká (NSA) sú bežne a veľmi často užívané lieky pre ich protizápalové, antipyretické a analgetické účinky. 20 % dospelých aspoň raz ročne po dobu jedného mesiaca užíva nesteroidné antireumatiká z rôznych algických dôvodov [1]. Medzi najčastejšie predpisované a odporúčané NSA patrí ibuprofen (až 20 miliónov preskripcií ročne v USA) a diclofenac. 30 miliónov ľudí na svete dlhodobo užíva NSA z dôvodu chronickej bolesti a reumatologických indikácií [2]. Ich široké užívanie je spojené s častou gastrointestinálnou morbiditou. NSA asociované gastrointestinálne komplikácie môžu byť veľmi pestré od endoskopicky negatívnych dyspepsií, bolestí brucha, cez ulcerácie, krvácania, perforácie a obštrukcie pri fibrotických stenózach. Chronické užívanie NSA zvyšuje výskyt peptických ulcerácií 3–5násobne. Nežiadúce účinky NSA predstavujú viac ako 25 % všetkých nežiadúcich účinkov liekov. NSA kolopatia ako príčina hospitalizácií je najčastejšia u pacientov so spondylartritídou (30–70 %), s osteoartrózou (32 %) a reumatoidnou artritídou (13 %) [3–5].
Popis prípadu
47ročná žena bola od roku 1991 liečená pre séropozitívnu reumatoidnú artritídu, aktuálne v III. štádiu. Pre výraznú chronickú zápalovú aktivitu mala v liečbe kortikoidy, metotrexát, cyklosporín A. Denne užívala nesteroidné antireumatiká pre bolesti malých kĺbov, najčastejšie diclofenac sodný v dávke 2 × 75 mg. V klinickom obraze dominovali bolesti malých kĺbov, ranná stuhlosť, celková nevýkonnosť. Koncom roku 2008 pre nedostatočný efekt konvenčnej antireumatickej liečby bola u pacientky plánovaná biologická liečba etanerceptom (Enbrel).
Na prelome rokov 2008/2009 a počas celého roku 2009 bola prítomná sideropenická mikrocytová anémia ťažkého stupňa, ktorá si opakovane vyžiadala substitúciu erytrocytárnymi masami. Hodnoty hemoglobínu (Hb) počas roku 2009 boli 109.. 91.. 76.. 65 g/l. V krvnom obraze bola opakovane zachytená trombocytóza, ktorú sme hodnotili ako marker zápalovej aktivity. Hodnoty trombocytov (Tr) boli 531.. 929.. 705.. 750 × 109/l. O vysokej zápalovej aktivite svedčili aj hodnoty C reaktívneho proteínu (CRP) 115.. 70,5.. 60,6.. 115 mg/l. Hodnoty sérového železa boli aj napriek intenzívnej perorálnej substitúcii veľmi nízke: 1,5 umol/l. Pacientka nemala žiadne bolesti brucha ani hnačky, neboli prítomné enterorágie ani melény. Napriek dobrej chuti do jedla mierne chudla, jej hmotnosť bola 48 kg na výšku 160 cm. V rámci diferenciálnej diagnostiky chronických strát krvi bola pacientka vyšetrovaná gastroenterológom. Gastroskopické vyšetrenie bolo negatívne, bez zdroja krvných strát. Pre pozitivitu testu na okultné krvácanie sme realizovali kolonoskopické vyšetrenie, ktoré bolo prekvapivým nálezom, nakoľko pacientka nemala žiadne ťažkosti. V kolonoskopickom obraze dominovali početné tiahle veľké ulcerácie, edém a grafilita sliznice, kontaktné krvácanie, jazvovite zmenené úseky, reziduá kráterovitých ulcerácií (obr. 1, 2). Patologické endoskopické zmeny sa nachádzali v oblasti lienálnej flexúry, colon transverzum až cékum. Sliznica terminálneho ilea, colon descendens a rektosigmoideum bola intaktná. Histologické vyšetrenie sliznice ukázalo spodinu exulcerácie, fibrínovo hnisavý exsudát, chronický zápalový infiltrát s reaktívnymi zmenami epitelu a so známkami bazálnej plazmocytózy (obr. 3). Histologický nález bol nešpecifický, nepotvrdil jednoznačne črevný zápal typu Crohnovej choroby. Pre rozsiahly a závažný endoskopický nález sme aj napriek nešpecifickému histologickému nálezu suponovali Crohnovu chorobu hrubého čreva a doplnili sme CT enterografické vyšetrenie tráviacej trubice. CT enterografia odhalila cirkulárne zhrubnutie steny hrubého čreva do 2,0 cm s nerovnomerne zúženým lúmenom a s reaktívnymi zápalovými zmenami (obr. 4). Naviac bolo prítomné zvýšenie denzity tukového tkaniva s hypervaskularizáciou a dezmoplastickými zmenami mezentéria, s lymfoproliferatívnou aktivitou. Na základe CT nálezu a histologických zmien chronického zápalu s ulceráciami sme stav predbežne uzavreli ako kolitída typu M. Crohn. Upravili sme liečbu, pridali sme mesalazín v plnej dávke 4 g denne, metronidazol 2 × 500 mg tbl denne. Azatioprin sme do liečby nepridávali, pacientka už mala imunosupresívnu liečbu (metotrexát) z reumatologickej indikácie. Pre endoskopický nález rozsiahlych ulcerácií s vysokou zápalovou aktivitou, reaktívnou trombocytózou a so závažnými chronickými stratami krvi aj napriek hemosubstitučnej liečbe sme indikovali biologickú liečbu preparátom infliximab (Remicade) so zámerom oddialenia chirurgickej intervencie aj s ohľadom na plánovanú biologickú liečbu z reumatologickej indikácie. Liečbu etanerceptom sme kontraindikovali pre možnosť zhoršenia črevného nálezu.
Obr. 1. Edém, ulcerácie, kontaktné krvácanie sliznice colon transverzum. Fig. 1. Swelling of mucosa, ulcerations, contact bleeding in colon transversum. 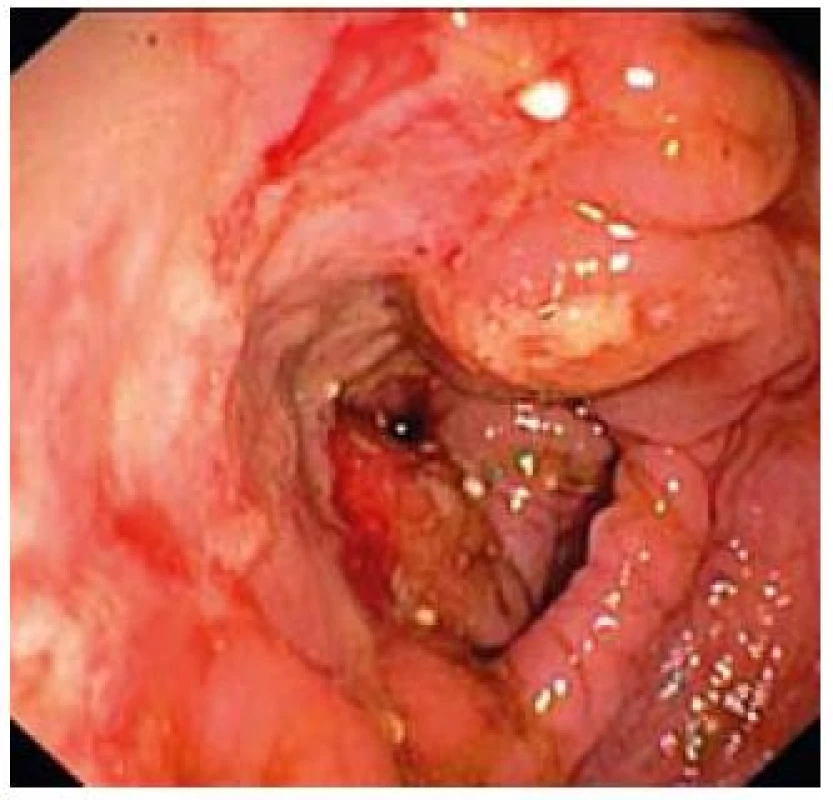
Obr. 2. Tiahnuce sa ulcerácie sliznice colon ascendens. Fig. 2. Far stretching ulcerations of mucosa in colon ascendens. 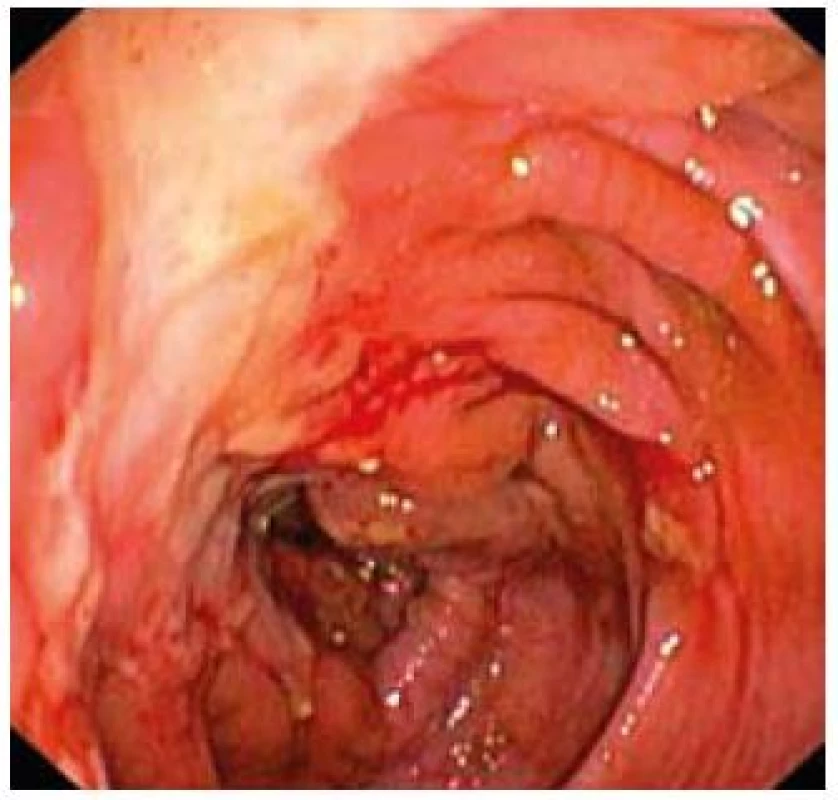
Obr. 3. Histologický obraz ulcerácie, colon ascendens, hematoxylín eozín. Fig. 3. Histologic specimen of ulceration in colon ascendens, haematoxylin eosin. 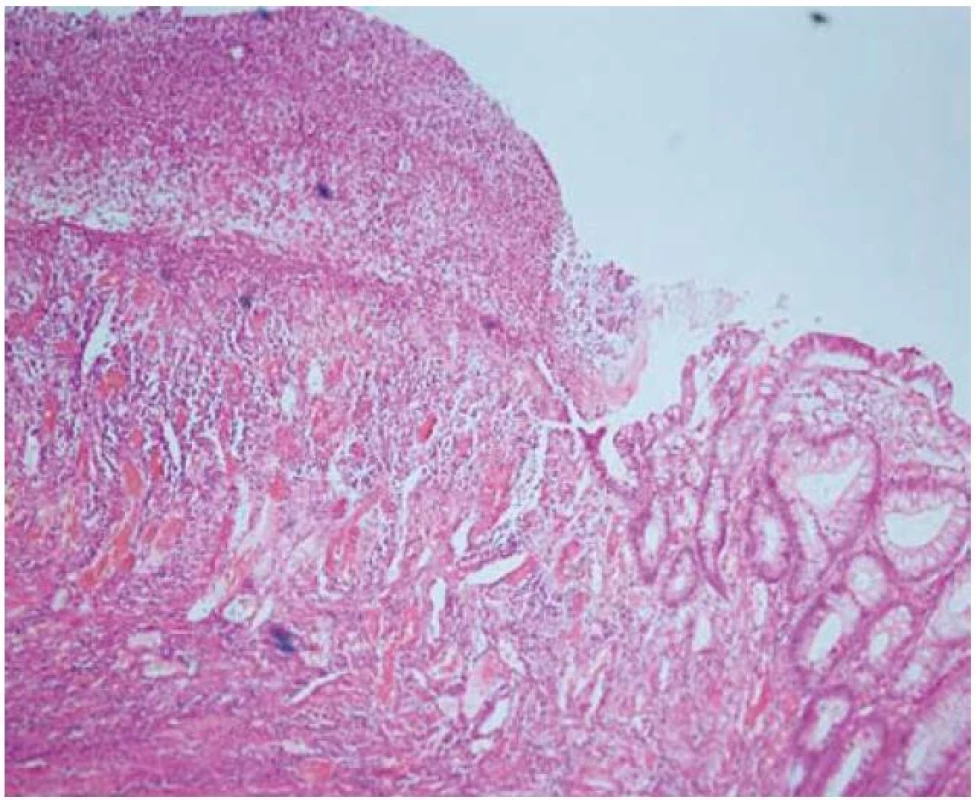
Obr. 4. CT enterografia, cirkulárne zhrubnutie steny hrubého čreva do 2,0 cm s nerovnomerne zúženým lúmenom s intenzívnym sýtením po podaní kontrastnej látky. Fig. 4. CT enterography, circular thickening of the large bowel wall to 2.0 cm with irregular stenosis of lumen with intensive enhancement after venous contrast administration. 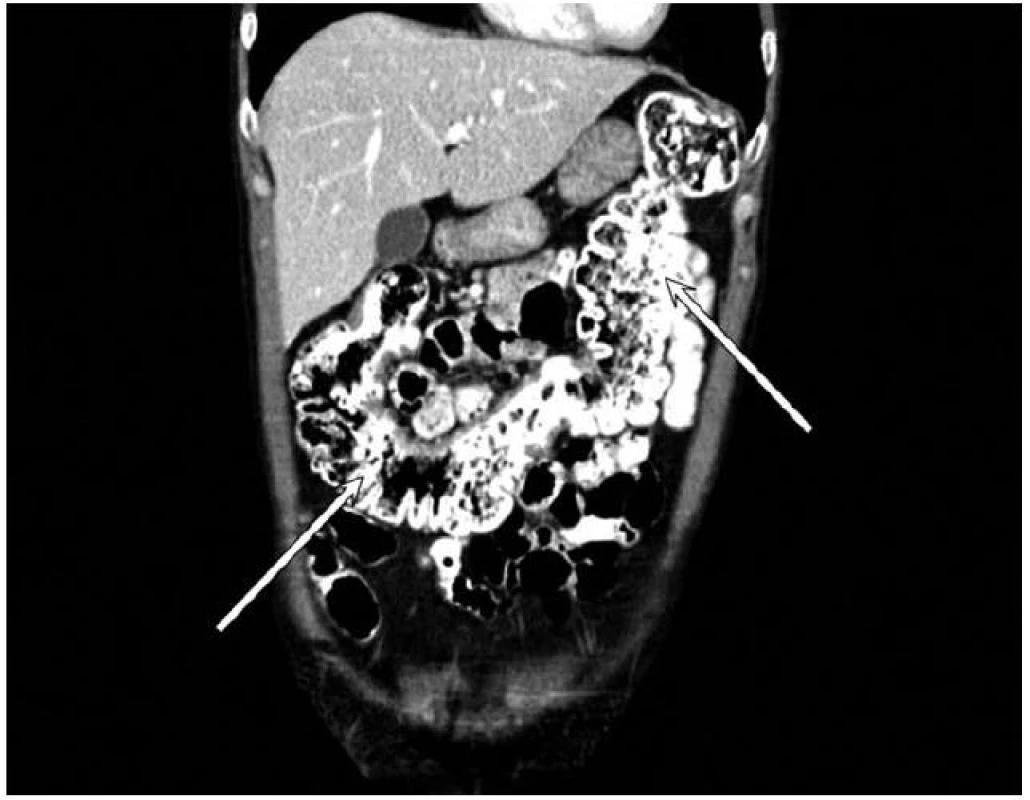
Pacientke sme v našom indikačnom a aplikačnom centre pre biologickú liečbu podali 6 dávok preparátu Remicade (dávkovanie 5 mg/kg, t.j. 300 mg na jedno podanie s úvodným indukčným režimom 0.–2.–6. týždeň a udržiavacím režimom každých 8 týždňov). Počas tejto liečby sme pozorovali len minimálne laboratórne zlepšenie, po 6. dávke sa po prechodnom ľahkom poklese zvýraznila zápalová aktivita, sideropénia a anémia (CRP: 115 mg/l, FeS: 1,5 umol/l, Hb: 65 g/l). Realizovali sme kontrolnú kolonoskopiu s odhalením mimoriadne ťažkého endoskopického nálezu ulceróznej pankolitídy s jednoliatymi cirkulárnymi ulceráciami hrubého čreva, rozsiahlymi kráterovitými defektmi mukózy až submukózy. Ulcerózne zmenená mukóza sa demarkovala vo veľkých plátoch (obr. 5–7). Colon rektosigmoideum bolo intaktné. Histologické vyšetrenie opäť potvrdzuje ulcerácie a chronický zápalový infiltrát. Na základe závažnosti endoskopického nálezu v súlade s klinickým a laboratórnym obrazom v teréne dlhodobého užívania nesteroidných antireumatík prehodnocujeme nález na NSA indukovanú kolitídu/kolopatiu ťažkého stupňa. Vzhľadom na hlboké ulcerácie so závažnými krvnými stratami, hroziacu perforáciu a inefektivitu kompletnej liečby navyše s nemožnosťou vynechania nesteroidných antireumatík sme indikovali chirurgické riešenie. Chirurg realizoval pankolektómiu s ileosigmoanastomózou, výkon a pooperačné obdobie boli bez komplikácií. Resekát bol histologicky bez známok Crohnovej choroby, ulcerácie a slizničné defekty boli v súlade so zmenami vyvolanými nesteroidnými antireumatikami. Už mesiac po operácii mala pacientka hodnoty krvného obrazu v medziach normy. Ľahko elevované CRP dávame do súvisu s chronickou aktivitou reumatologického ochorenia (Hb: 139 g/l, Tr: 157 × 109/l, CRP: 23,5 mg/l).
Obr. 5. Závažný nález kontinuálnej ulcerácie celej sliznice s hlbokými defektmi sliznice (colon ascendens). Fig. 5. Serious finding of continuous ulcerations of the entire mucosa with deep defects of mucosa (colon ascendens). 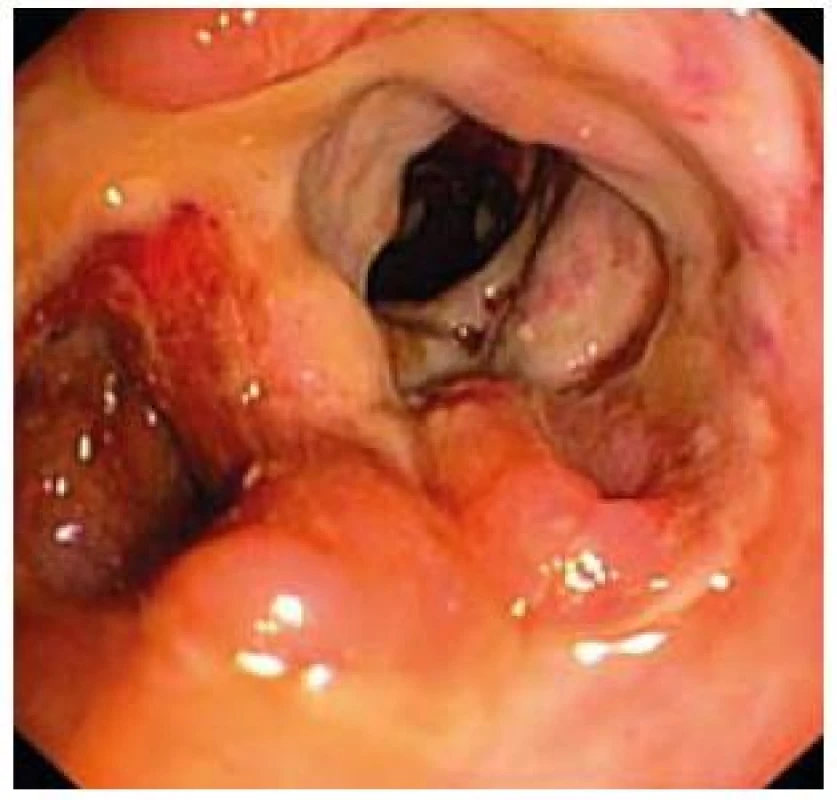
Obr. 6. Demarkácia ulcerózne zmenenej sliznice v colon ascendens. Fig. 6. Flaking of ulcerative mucosa in colon ascendens. 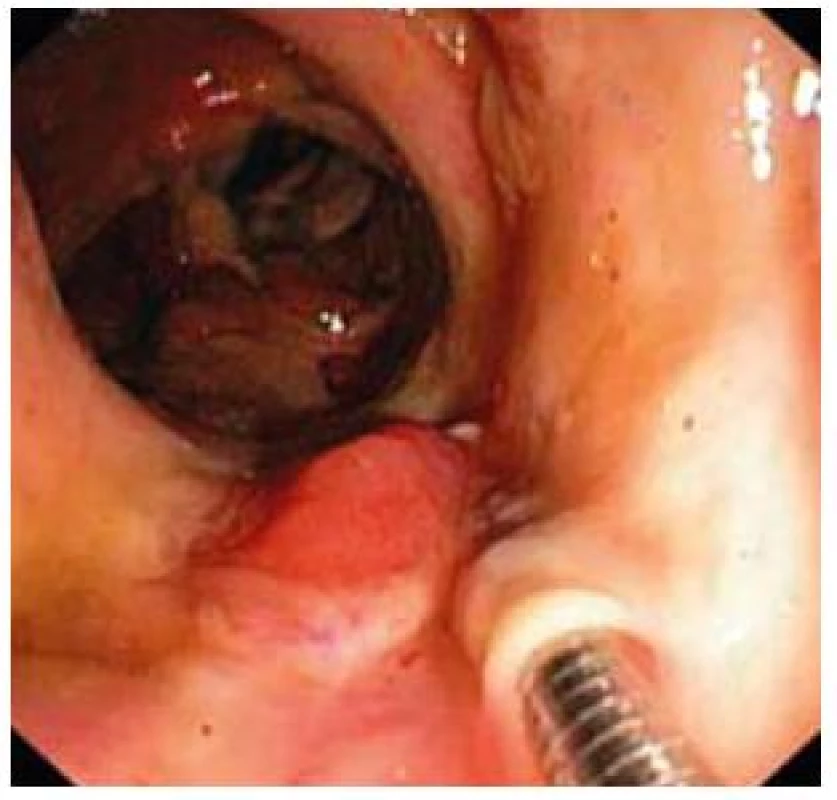
Obr. 7. Závažný nález kontinuálnej ulcerácie celej sliznice. Fig. 7. Serious finding of continuous ulcerations of the entire mucosa. 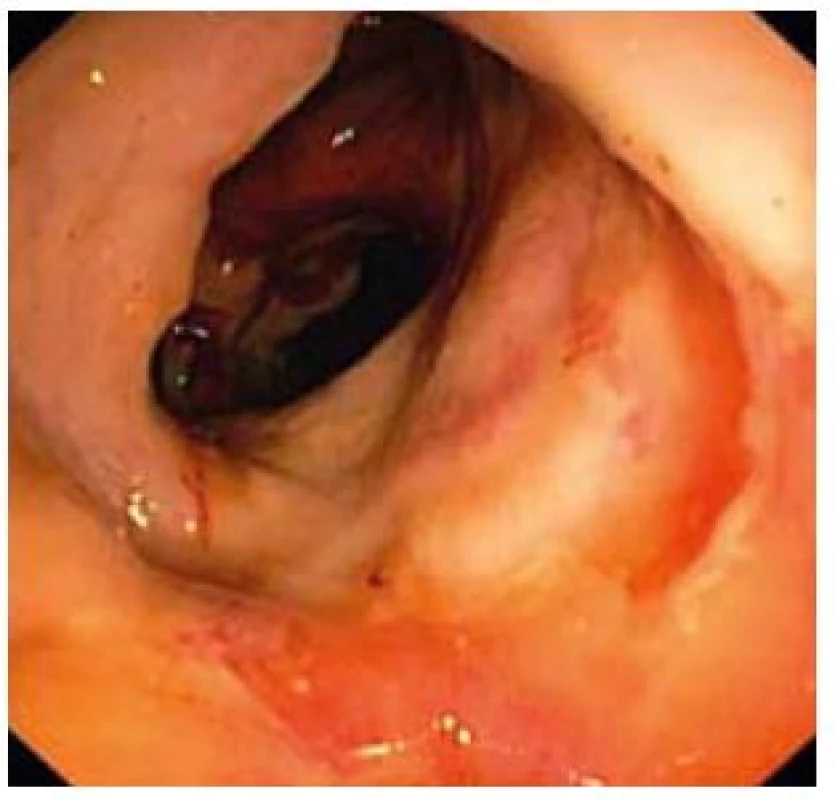
Reumatológmi bola indikovaná biologická liečba plne humánnym preparátom anti-TNFα – adalimumabom (Humira) v dávke 40 mg subkutánne každé dva týždne. Konkomitantnou terapiou je imunosupresívna liečba (metotrexát a kortikoidy), NSA (aceclofenac 100 mg denne a inhibítor COX-2 etoricoxib 90 mg denne). Pacientkin stav sa počas biologickej liečby adalimumabom (Humira) postupne zlepšuje, čo umožňuje aspoň čiastočne redukovať NSA. Pacientka má obavy z liečby NSA kvôli ďalšiemu poškodeniu iných častí tráviaceho traktu, nemôže ich však vynechať pre bolesti malých kĺbov rúk, bolesti lakťov a chodidiel. Preto NSA občas nahrádza paracetamolom. Z gastroenterologického hľadiska je pacientka bez ťažkostí, s pozitívnou hmotnostnou bilanciou, bez bolestí brucha, s 2–3 formovanými stolicami denne. Užíva ferropreparáty pre miernu sideropéniu a omeprazol za účelom gastroprotekcie pri nevyhnutnej liečbe NSA a kortikoidmi.
Diskusia
Kazuistika demonštruje závažné poškodenie hrubého čreva pri chronickej, niekoľkoročnej liečbe NSA pre séropozitívnu reumatoidnú artritídu. Ulcerácie sprvu imitovali Crohnovu chorobu, čo nie je výnimkou ani v literatúre, kde sú popisované viaceré kauzistické prípady mylnej diagnózy Crohnovej choroby [3,6]. Nález CT enterografických zmien, vyskytujúcich sa aj pri Crohnovej chorobe, vysvetľujeme prítomnosťou chronickej ulcerózne ischemickej kolitídy so sekundárnou lymfadenopatiou pri zvýšenej črevnej baktériovej translokácii a zvýšenej permeabilite. Po prehodnotení diagnózy a vyčerpaní komplexnej konzervatívnej liečby bolo u našej pacientky nutné radikálne riešenie v zmysle kolektómie s veľmi dobrým výsledkom, bez hnačiek a bez zhoršenia kvality života.
NSA môžu spôsobiť rôzne zmeny na sliznici hrubého čreva od minimálnych erozívnych lézií, cez ulcerácie, krvácanie, striktúry či membrány až po závažné zmeny vyžadujúce kolektómiu. Mechanizmus poškodenia sliznice NSA, faktory ovplyvňujúce ich toxicitu a možnosti prevencie sú podrobnejšie rozoberané v nasledujúcich odsekoch diskusie.
Výskyt NSA indukovanej kolopatie
Do spektra NSA indukovaných gastrointestinálnych (GI) poškodení patrí okrem poškodenia žalúdka a tenkého čreva aj poškodenie hrubého čreva, tzv. NSA indukovaná kolopatia, ktorá predstavuje až 43 % všetkých GI komplikácií pri chronickom užívaní NSA [7].
NSA indukovaná enteropatia a hlavne kolopatia sú podcenené a mnohokrát nepoznané diagnózy. Morfologický obraz NSA poškodenia v oblasti hrubého čreva závisí od dĺžky, množstva užívania a tiež od typu NSA. Nie všetky NSA majú rovnaký mukotoxický efekt na tráviaci trakt. Najnižšie riziko komplikácií je pri liečbe ibuprofénom, meloxikamom a tenoxikamom. Stredné riziko je pri liekoch: indometacín, sulindac, diklofenak a iné. Vysoké riziko je napr. u ketoprofénu, azapropazonu. Toxicita sa zvyšuje pri vyšších dávkach, ich vzájomným kombinovaním alebo kombinovaním s kyselinou acetylosalicylovou [2]. Krátkodobé užívanie NSA môže vyvolať edém, erózie a malé ulcerácie s klinickým prejavom bolesti brucha, hnačkou a neveľkou prímesou krvi. Po vynechaní NSA môže dôjsť k spontánnej reštitúcii sliznice bez následkov. Pri dlhodobom pravidelnom užívaní (hlavne pri reumatologických algických a zápalových stavoch) je dominantne poškodené pravé a priečne hrubé črevo, rektosigma je poškodená zriedkavo (v pomere asi 80 % : 20 %) [12]. Morfologicky sú prítomné rozsiahle ulcerácie, striktúry, membrány a cirkulárne početné tesné stenózy (tzv. fibrotizujúca NSA kolopatia). Klinicky sa nález prejaví hnačkou, bolesťami brucha, subileóznym až ileóznym stavom. Výnimkou nie sú ani perforácie hrubého čreva pri hlbokých penetrujúcich ulceráciách s klinickým obrazom náhlej brušnej príhody. Početné tesné fibrotizujúce stenózy sú indikáciou na kolektómiu [8].
Klinické prejavy NSA enteropatie a kolopatie môžu byť aj subklinické, oligosymptomatické. Prejavujú sa sideropenickým anemickým syndrómom bez bolestí brucha a bez hnačiek, hypoalbuminémiou pri početnejších vredoch tenkého čreva. Ulcerácie hrubého čreva môžu spôsobiť zvýšenú črevnú permeabilitu so zvýšenou baktériovou translokáciou, so subfebrilitami až febrilitami a vysokou zápalovou aktivitou. Môžu sa však prejavovať len neprospievaním a chudnutím aj napriek dobrej chuti do jedla [9]. Môžu imitovať Crohnovu chorobu v klinickom, endoskopickom, čiastočne histologickom, ba aj CT obraze, ako to demonštruje naša kazuistika.
Mechanizmus poškodenia
Poškodenie sliznice tráviaceho traktu NSA sa vysvetľuje ich lokálnym iritačným a systémovým vplyvom prostredníctvom blokády cyklooxygenázy (COX). Cyklooxygenáza a lipooxygenáza sú enzýmy metabolickej cesty kyseliny arachidónovej. Základným patogenetickým mechanizmom je zablokovanie COX a zníženie tvorby mukoprotektívnych prostaglandínov. Ďalšími následkami blokády COX je rozpojenie oxidatívnej fosforylácie v mitochondriách, uvoľnenie voľných radikálov a proteáz. Blokovaním COX vznikne relatívna prevaha metabolitov lipooxygenázovej metabolickej cesty (leukotriény). Prevaha vazokonstrikčných leukotriénov má za následok poruchu mikrocirkulácie, spazmy drobných ciev, adhéziu neutrofilov k endotelu. Následkom všetkých uvedených zmien je ischémia sliznice s tvorbou defektov v zmysle erózií až ulcerácií [9,12]. NSA tiež vedú k zhoršenému hojeniu ulcerácií v dôsledku excesívnej expresie cytokínov, predovšetkým TNF a IL-1β. Znížená je proliferácia epitelových buniek, angiogenéza a maturácia granulačného tkaniva. NSA blokujú angiogenézu priamym účinkom na endotelové bunky. Za účelom zníženia mukotoxicity boli vyvinuté preferenčné (nimesulid, etodolak, meloxikám) a vysokoselektívne inhibítory COX-2 (celexocib, etorikoxib, valdekoxib a iné) [5,11].
Faktory zhoršujúce vplyv NSA na sliznicu tráviaceho traktu
Z hľadiska spotreby patria NSA medzi najčastejšie predpisované lieky. V priebehu života má približne polovica obyvateľstva skúsenosti s bolesťami chrbta akejkoľvek etiológie. Pri všetkých týchto chorobách a príznakoch patria NSA k liekom prvej voľby pre ich veľmi dobrý efekt na somatické nociceptory. Nepriaznivý demografický vývoj populácie s nižším prirodzeným prírastkom spôsobuje starnutie populácie s vyšším výskytom reumatologických chorôb, čo má za následok aj vyššiu spotrebu NSA [10].
Výskyt gastrointestinálnej toxicity NSA je veľmi individuálny a ovplyvnený mnohými faktormi. Medzi faktory zhoršujúce vplyv NSA patrí vek nad 65 rokov. Až 40 % pacientov je vo veku nad 60 rokov. Pacienti s anamnézou vredovej choroby gastroduodena majú vyššie riziko dyspepsie 2,9×, riziko vzniku krvácania z vredu až 13,5×. Pacienti so zápalovými črevnými ochoreniami či divertikulovou chorobou majú tiež vyšší výskyt nežiadúcich účinkov NSA. Dlhšie trvajúca, event. chronická liečba NSA môže spôsobiť závažný relaps Crohnovej choroby či ulceróznej kolitídy, ktorá bola predtým v dlhodobobej remisii. NSAID aj COX-2 inhibítory zvyšujú intestinálnu permeabilitu, recirkulujú enterohepatálnym obehom a inhibujú syntézu prostaglandínov v hrubom čreve. V zdravom epiteli hrubého čreva COX-2 nie je detekovateľná. Inflamovaná mukóza pri zápalových črevných chorobách (IBD – inflammatory bowel disease) vo zvýšenej miere exprimuje inducibilnú COX-2 v snahe o slizničné hojenie. Zablokovanie COX-2 inhibítormi môže spôsobiť progresiu zápalového stavu, rozruší integritu sliznice. Krátkodobé užívanie NSA alebo COX-2 inhibítorov u pacientov s IBD je bezpečné a pre pacienta s benefitom. Kombinovaná liečba NSA a COX-2 inhibítormi, alebo spolu so steroidmi môže indukovať NSA enteropatiu či kolopatiu [5,12,14,15].
Vyššia gastrointestinálna morbidita pri liečbe NSA je u polymorbídnych pacientov, s chronickou renálnou insuficienciou, v chronickom dialyzačnom programe, u diabetikov, u pacientov so závažným aterosklerotickým postihnutím ciev. Nežiadúce prejavy NSA podporuje aj polypragmázia, alkoholizmus, antikoagulačná liečba a antitrombotická liečba, kde je vyššia tendencia ku krvácaniam zo slizničných lézií, pri warfarinizácii až šesťnásobne. Fajčenie a alkohol zvyšujú riziko perforácie [2]. Dĺžka užívania NSA tiež priamo úmerne ovplyvňuje gastrointestinálnu morbiditu. Chronická liečba vysokými dávkami, s nemožnosťou ukončenia liečby NSA sú faktormi zvyšujúcimi ich toxicitu. Z uvedených faktov je možné vyvodiť preventívne opatrenia, ktoré by znížili nežiadúci efekt na tráviaci trakt a hlavne hrubé črevo. Metódou voľby sú buď kombinované preparáty s misoprostolom, alebo COX-2 inhibítory. U pacientov s kardiovaskulárnymi chorobami a polymorbiditou môžu mať COX-2 inhibítory trombotický potenciál. Ten súvisí s mechanizmom inhibície, kedy zablokovanie COX-2 má za následok relatívnu prevahu tromboxánu A2 s proagregačnou aktivitou. U pacientov s polypragmáziou je nutné redukovať liečbu na nutné minimum. U pacientov s antikoagulačnou a antitrombotickou liečbou je treba minimalizovať liečbu NSA a voliť negastrotoxické analgetiká typu slabých či silnejších opioidov. Pri nevyhnutnej liečbe NSA je nutné stále pridať gastroprotektivom (H2 blokátory, alebo blokátory protónovej pumpy) a vynechať z liečby iné ulcerogénne lieky. V mnohých prípadoch nie je možná ideálna kombinácia liekov a gastrotoxicita NSA je evidentná [13].
Záver
NSA indukovaná kolopatia je ochorenie, na ktoré sa málo myslí. Jej výskyt sa zvyšuje a je stále častejšie publikovaná v literatúre. Zvyšujúci sa výskyt choroby súvisí s expanziou chronickej spotreby NSA, hlavne vo vyššom veku a u polymorbídnych pacientov. Neexistujú epidemiologické štúdie na sledovanie poškodenia hrubého čreva pri chronickej liečbe NSA, údaje sú publikované na základe skúseností. Krátkodobé prechodné užívanie môže vyvolať ľahké zmeny sliznice s rýchlou reštitúciou po vynechaní lieku. Chronické niekoľkoročné užívanie však môže vyvolať závažné poškodenie hrubého čreva s možnosťou perforácie či rozsiahlych hlbokých ulcerácií, striktúr a membrán s nutnosťou chirurgického riešenia. Nález môže imitovať črevný zápal typu Crohnovej choroby, ischemickú kolitídu, alebo malignitu. Na diagnózu NSA indukovanej kolopatie je nutné myslieť a cielene sa pacientov pýtať na užívanie NSA, nakoľko si ich mnohokrát sami kupujú a nepovažujú ich za lieky s relatívne závažnými nežiadúcimi účinkami.
Doručeno do redakce: 8. 8. 2010
Přijato po recenzi: 20. 9. 2010MUDr. Laura Gombošová, PhD.
I. interná klinika, Univerzitná nemocnica L. Pasteura
Tr. SNP č. 1
040 01 Košice
lauragombosova@yahoo.com
Zdroje
1. Lanas A, Esplugues JV, Zapardiel J et al. Education-based approach to addressing non-evidence-based practice in preventing NSAID-associated gastrointestinal complications. World J Gastroenterol 2009; 15(47): 5953–5959.
2. Bátovský M. Gastroprotekcia pri dlhodobom užívaní nesteroidných antireumatík, resp. nízkych dávok kyseliny acetylosalicylovej. Čes a Slov Gastroent a Hepatol 2010; 64(3): 18–23.
3. Stolte M, Hartmann FO. Misinterpretation of NSAID-induced colopathy as Crohn´s disease. Z Gastroenterol 2010; 48(4): 472–475.
4. Frech EJ, Go MF. Treatment and chemoprevention of NSAID-associated gastrointestinal complications. Ther Clin Risk Manag 2009; 5(1): 65–73.
5. Feagins LA, Cryer BL. Do non-steroidal anti-inflammatory drugs cause exacerbations of inflammatory bowel disease? Dig Dis Sci 2010; 55(2): 226–232.
6. Kirsch M. Nonsteroidal antiinflammatory drug colopathy: mimicry of Crohn´s disease and colon carcinoma. J Clin Gastroenterol 1997; 24(2): 121–123.
7. Leong RWL, Chan FKL. Drug-induced side effects affecting the gastrointestinal tract. Expert Opin Drug Saf 2006; 5(4): 1–8.
8. Masannat YA, Harron M, Harinath G. Nonsteroidal anti-inflammatory drugs-associated colopathy. ANZ J Surg 2010; 80(1–2): 96–99.
9. Malone G, Kaushik VY, Morris JA et al. Non-steroidal anti-inflammatory drug colopathy: case reports and review of literature. J R Coll Physicians Edinb 2004; 34 : 32–36.
10. Rybár I, Hyrdel R, Rovenský J. Peptické lézie navodené liečbou nesteroidovými antiflogistikami. In: Jurgoš Ľ, Kužela L, Hrušovský Š et al. Gastroenterológia. Bratislava: Veda 2006 : 289–297.
11. Rybár I. Nesteroidové antireumatiká s hľadiska reumatologickej praxe. In: Gastropatia vyvolaná nesteroidovými antireumatikami. Martin: Osveta 1997 : 8–27.
12. Stolte M, Karimi D, Vieth M et al. Strictures, diaphragms and erosions or ulcerations of ischemic type in the colon should always prompt consideration of non-steroidal anti-inflammatory drug-induced lesions. World J Gastroenterol 2005; 11(37): 5828–5833.
13. Scheiman MJ, Fendrick AM. Practical approaches to minimizing gastrointestinal and cardiovascular safety concerns with COX-2 inhibitors and NSAIDs. Arthritis Res Ther 2005; 7 (suppl 4): 23–29.
14. Guslandi M. Exacerbation of inflammatory bowel disease by nonsteroidal anti-inflammatory drugs and cyclooxygenase-2 inhibitors: Fact or fiction? World J Gastroenterol 2006; 12(10): 1509-1510.
15. Klein A, Eliakim R. Non steroidal anti-inflammatory drugs and Inflammatory bowel disease. Pharmac 2010; 3(4): 1084–1092.
Štítky
Dětská gastroenterologie Gastroenterologie a hepatologie Chirurgie všeobecná
Článek vyšel v časopiseGastroenterologie a hepatologie
Nejčtenější tento týden
2010 Číslo 6- Trombóza portální žíly jako komplikace infekce COVID-19 – kazuistika
- Itoprid v léčbě funkční dyspepsie
- Farmakokinetika a tolerance pantoprazolu v dětském věku
- Vliv podávání prokinetik na riziko syndromu bakteriálního přerůstání u pacientů užívajících inhibitory protonové pumpy
-
Všechny články tohoto čísla
- Extraezofageální reflux up-to-date
- Nesteroidovými antireumatikami indukovaná kolopatia imitujúca Crohnovu chorobu
-
Klíčové otázky a odpovědi v léčbě Crohnovy nemoci
Závěry mezinárodního projektu IBD-AHEAD
- Fertilita, gravidita, dojčenie a nešpecifické črevné zápaly vo svetle záverov konsenzu ECCO 2010
- Použití biodegradabilního stentu u benigní stenózy žlučových cest
- Zamyšlení nad UEGW 2010
- Rejstřík 64. ročníku 2010
- Postavení a výtěžnost koloskopie v rámci screeningového programu založeného na testu na okultní krvácení (TOK) ve stolici
- Gastroenterologie a hepatologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Extraezofageální reflux up-to-date
- Použití biodegradabilního stentu u benigní stenózy žlučových cest
- Nesteroidovými antireumatikami indukovaná kolopatia imitujúca Crohnovu chorobu
- Fertilita, gravidita, dojčenie a nešpecifické črevné zápaly vo svetle záverov konsenzu ECCO 2010
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Revma Focus: Spondyloartritidy
nový kurz
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Autoři: prof. MUDr. Pavel Horák, CSc., doc. MUDr. Ludmila Brunerová, Ph.D., doc. MUDr. Václav Vyskočil, Ph.D., prim. MUDr. Richard Pikner, Ph.D., MUDr. Olga Růžičková, MUDr. Jan Rosa, prof. MUDr. Vladimír Palička, CSc., Dr.h.c.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



