-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
NEUROTIZACE ROHOVKY U TĚŽKÉ FORMY NEUROTROFICKÉ KERATOPATIE. KAZUISTIKA
Autoři: Š. Rusňák 1; L. Hecová 1; D. Štěpánek 2; M. Sobotová 1
Působiště autorů: Oční klinika, Fakultní nemocnice Plzeň 1; Neurochirurgická klinika, Fakultní nemocnice Plzeň 2
Vyšlo v časopise: Čes. a slov. Oftal., 77, 2021, No. 3, p. 140-146
Kategorie: Původní práce
doi: https://doi.org/10.31348/2021/17Souhrn
Cíl: Neurotrofická keratopatie (NK) je degenerativní onemocnění rohovky způsobené poškozením trigeminální inervace vedoucí ke snížení citlivosti rohovky až k její úplné anestezii. Porucha rohovkové inervace vede k morfologickým a metabolickým poruchám epitelu a k rozvoji recidivujících nebo perzistujících defektů epitelu až vředů rohovky, které mohou progredovat ve stromální lýzu a perforaci rohovky. Jednou z možností řešení těžké neurotrofické keratopatie je reinervace anestetické rohovky s využitím n. supraorbitalis a autologního štěpu senzitivního nervu (nepřímá neurotizace).
V práci prezentujeme výsledky léčby pomocí této metody u pacienta s perzistujícím epiteliálním defektem a vředem rohovky po úrazu oka v terénu denervované rohovky.
Výsledky: 22letý muž s anamnézou neurochirurgického zákroku pro astrocytom mozečku a kmene vpravo ve 2 letech věku byl od dětství sledován pro pooperační parézu n. facialis vpravo s lagoftalmem, současně byla přítomna porucha funkce n. trigeminus vpravo. Ve 22 letech po kontuzi pravého bulbu došlo k rozvoji perzistujícího epiteliálního defektu a následně vředu rohovky. Vzhledem k vyčerpání jiných terapeutických možností byla u pacienta provedena reinervace rohovky vpravo cestou kontralaterálního n. supraorbitalis s využitím autologního štěpu z n. suralis z pravé dolní končetiny. 5 měsíců po výkonu došlo k částečné obnově citlivosti rohovky. Po následné transplantaci amniové membrány do chronického defektu epitelu se rozsáhlý epiteliální defekt uzavřel a došlo k projasnění zkaleného stromatu rohovky.
Závěr: Technika reinervace anestetické rohovky s využitím n. supraorbitalis a autologního štěpu senzitivního nervu představuje novou možnost řešení těžké formy neurotrofické keratopatie. U pacienta z naší kazuistiky operovaného touto metodou došlo po výkonu ke zhojení těžkého rohovkového nálezu.
Klíčová slova:
neurotrofická keratopatie – anestezie/hypestezie rohovky – neurotizace rohovky – trojklanný nerv – surální nerv
Úvod
Rohovka je inervována první větví trigeminálního nervu (n. ophthalmicus) a autonomními nervy. Neurotrofická keratopatie (NK) je vzácné degenerativní onemocnění rohovky s prevalencí kolem 5 na 10 000 osob [1]. NK je způsobena poraněním nebo poškozením trojklanného nervu (n. trigeminus) nebo jeho první větve (n. ophthalmicus). Nejčastější příčinou NK je herpetická keratitida (27 %), dále systémová onemocnění (např. diabetes mellitus, roztroušená skleróza a deficit vitaminu A), chemické a termické poranění povrchu oka, dlouhodobé používání kontaktních čoček, nadužívání lokálních anestetik, centrální poškození trojklanného nervu (neurinom akustiku, neurochirurgické zákroky atd.) nebo poškození ciliárních nervů při operacích na předním i zadním segmentu oka (antiglaukomové zákroky, refrakční chirurgie atd.) [2]. Tabulka 1.
Tab. 1. Příčiny neurotrofické keratopatie 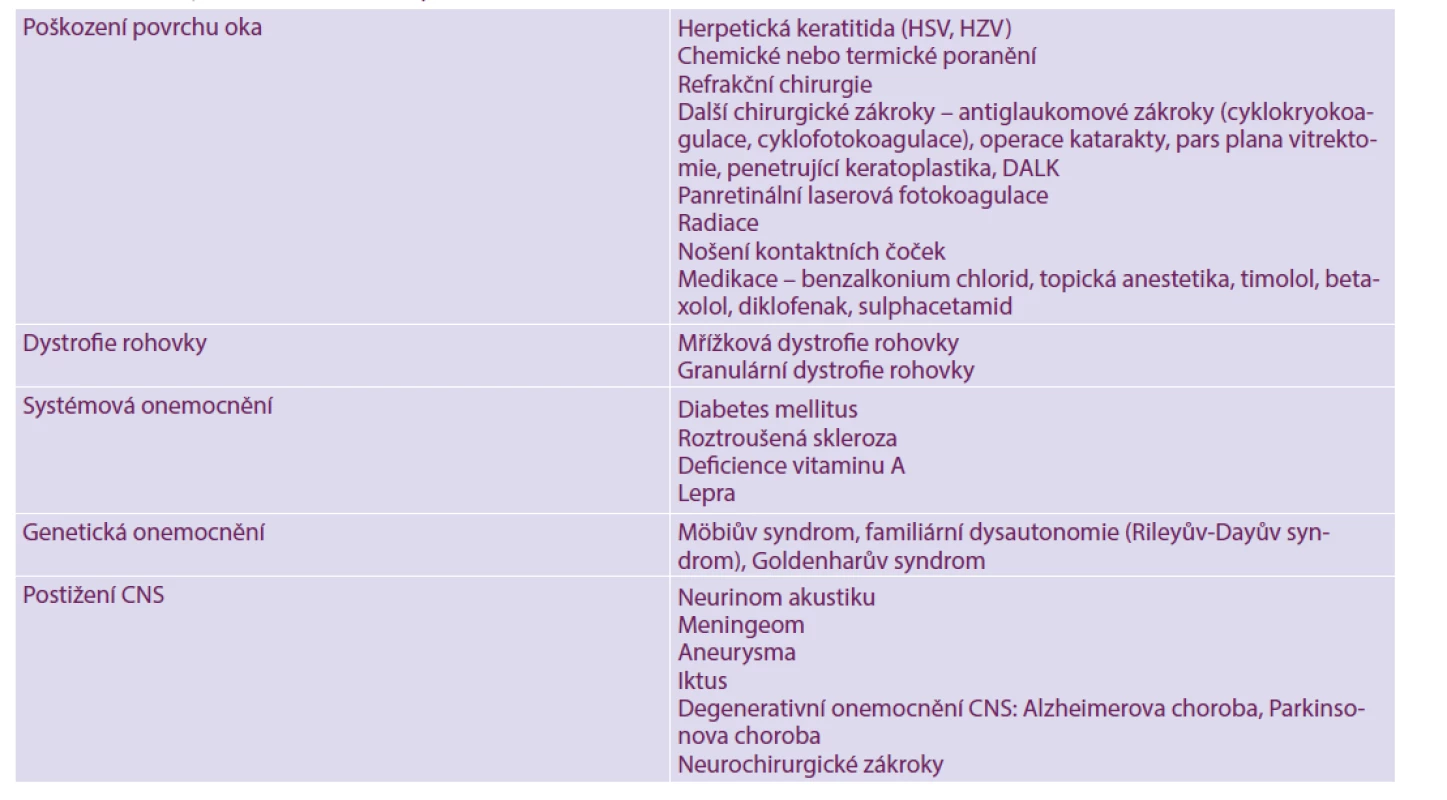
Nervové svazky vstupují do rohovky v oblasti limbu, v periferii rohovky jsou umístěny pod přední třetinou stromatu rohovky, poté pronikají Bowmanovou membránou a mezi ní a vrstvou bazálních epiteliálních buněk vytvářejí hustou síť nervových vláken, tzv. subbazální nervový plexus [3]. Senzitivní inervace rohovky reaguje na mechanické, chemické a tepelné podněty dvěma reflexními oblouky: motorickým stimulujícím mrkání a autonomním stimulujícím sekreci slz. Inervace hraje klíčovou roli v udržování zdravého povrchu oka – jednak spouštěním ochranných reflexů při poranění, jednak zajištěním trofických faktorů pro buňky rohovky. Snížení citlivosti rohovky indukuje změny v slzném filmu, ovlivňuje metabolismus a proliferaci epiteliálních buněk a vede k jejich zvýšené apoptóze. Dochází ke vzniku intracelulárního edému, ztrátě mikroklků a abnormalitám v oblasti bazální laminy [4].
Anestezie či hypestezie přítomná u NK tak může vést k recidivujícím nebo perzistujícím defektům epitelu rohovky, vředům, zakalení rohovky až k její perforaci. Léčba NK závisí na závažnosti onemocnění. Běžná lokální terapie spočívá především v substituci slzného filmu – umělé slzy bez konzervačních látek, lubrikační oční gely, oční kapky z autologního/allogenního séra, oční kapky ze séra z pupečníkové krve. Mezi další testované metody léčby patří lokální aplikace NGF (nerve growth factor, nervový růstový faktor) i dalších působků (ReGeneraTing Agents, tj. RGTA, thymosin beta-4, substance P, nicergolin nebo citikolin [4-7]. V posledním desetiletí je na vzestupu metoda tzv. neurotizace, tj. reinervace rohovky. Neurotizace, neboli nervový transfer, je technika využití jiného zdravého nervu nebo jeho části jakožto donoru zdravých nervových vláken k obnovení nevratně narušené senzorické nebo motorické dráhy. Obnova nervové dráhy může být přímá s lokálním nervovým přenosem nebo nepřímá za využití nervového štěpu [8]. Obrázek 1.
Obr. 1. Schéma nepřímé neurotizace rohovky postiženého pravého oka za využití nervového štěpu a kontralaterálního supraorbitálního nervu 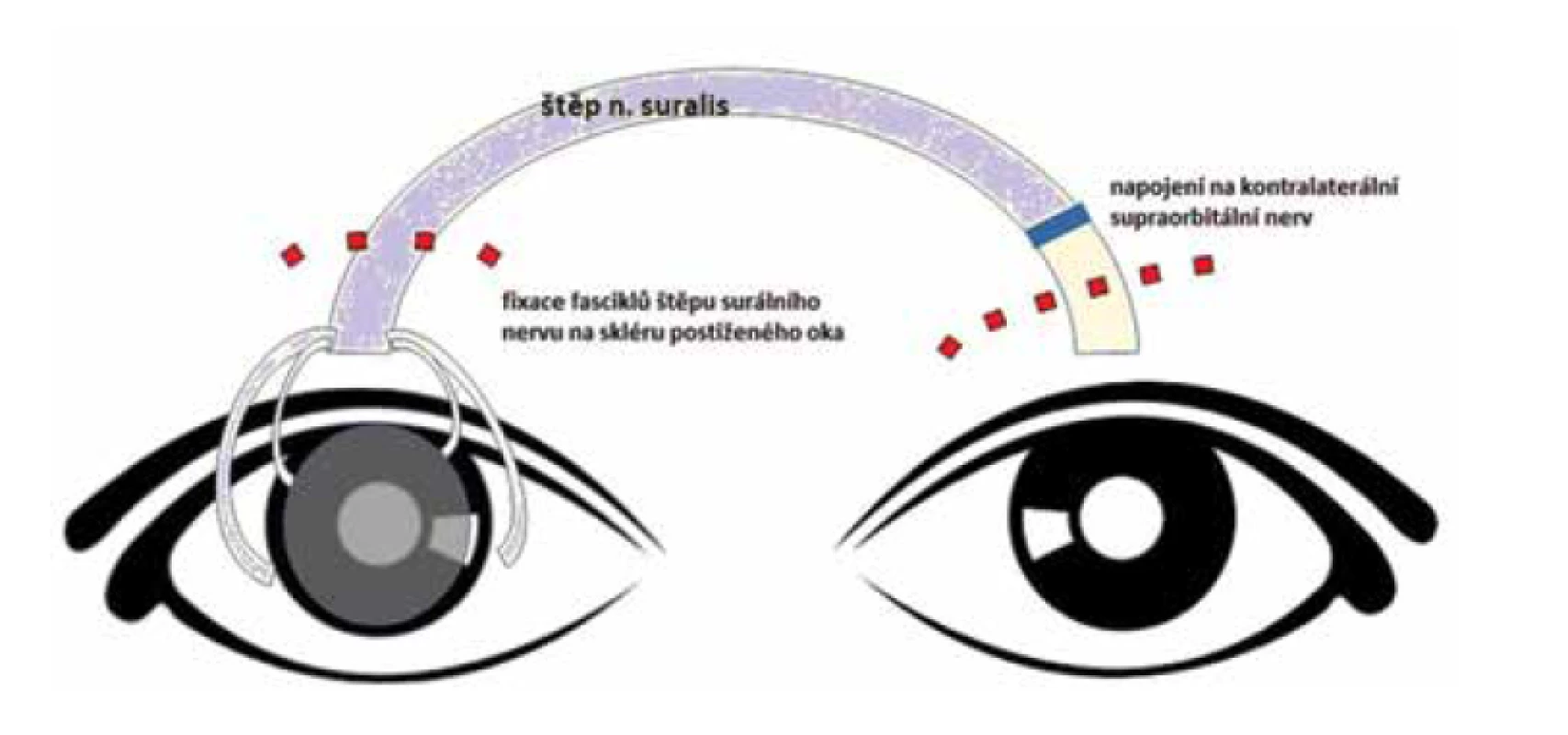
Cílem práce je prezentovat naši zkušenost s využitím nepřímé neurotizace rohovky u pacienta s těžkou formou NK a vředem rohovky vzniklým na podkladě perzistujícího epiteliálního defektu.
Kazuistika
22letý muž s anamnézou neurochirurgického zákroku pro astrocytom mozečku a kmene vpravo ve dvou letech věku byl od dětství sledován pro pooperační parézu n. facialis vpravo s lagoftalmem, současně byla přítomna porucha funkce trigeminálního nervu vpravo. Na spádové oční ambulanci byl pacient v adolescenci opakovaně léčen pro infiltráty rohovky (při lagoftalmu a hypestezii rohovky vpravo), podle dostupné dokumentace byly zhojeny nubekulou rohovky v temporálním kvadrantu. Ve 22 letech pacient utrpěl komoci mozkovou a kontuzi pravého bulbu úderem pěstí při napadení. Na našem pracovišti byl pacient poprvé vyšetřen 3 týdny po kontuzi pravého bulbu pro perzistující epiteliální defekt rohovky a pokles vidění pravého oka. Perzistující epiteliální defekt byl refrakterní na běžnou terapii (krycí měkká kontaktní čočka, lubrikační léčba, parciální tarsorafie, opakované transplantace amniové membrány), došlo k rozvoji vředu rohovky a zkalení stromatu rohovky. Centrální zraková ostrost poklesla na pohyb, certa. Nález odpovídal stupni 3 dle klasifikačního systému podle Mackieho.
Vzhledem k vyčerpání terapeutických možností u mladého pacienta s anestezií rohovky byla provedena reinervace rohovky cestou kontralaterálního n. supraorbitalis s využitím autologního štěpu z n. suralis z pravé dolní končetiny. Před zákrokem byl pacient podrobně informován o průběhu zákroku a možných komplikacích a podepsal informovaný souhlas s výkonem. Obrázek 2 a 3.
Obr. 2. Nepřímá neurotizace rohovky pravého oka za využití štěpu surálního nervu a kontralaterálního supraorbitálního nervu. Příprava štěpu surálního nervu z pravé dolní končetiny (A, B). Lokalizace kontralaterálního (tj. na straně levého zdravého oka) supraorbitálního nervu (C). Preparace podkožního tunelu mezi horním víčkem pravého a levého oka (D), protažení trubičky pro snazší a bezpečnější manipulaci s nervovým štěpem (E). Příprava tunelu z horního fornixu postiženého pravého oka do podkoží horního víčka (F).
Nález před aplikací nervového štěpu (G)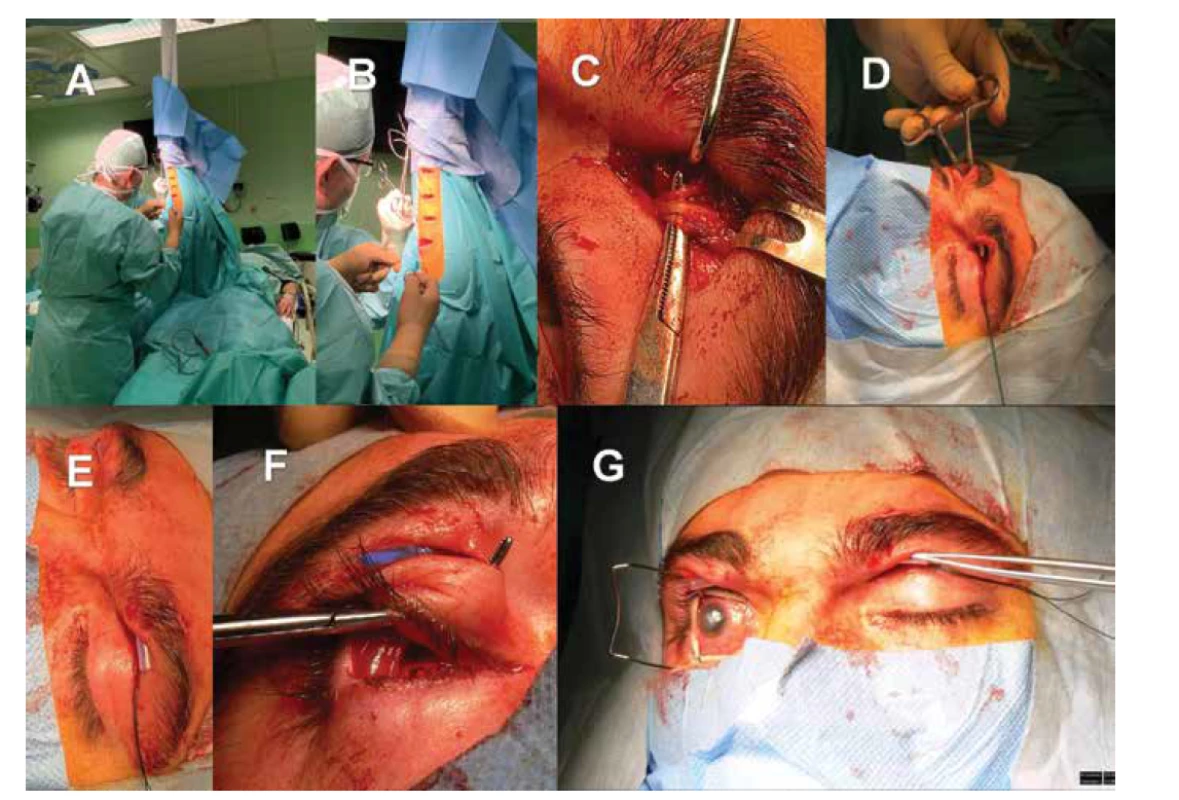
Obr. 3. Nepřímá neurotizace rohovky pravého oka za využití štěpu surálního nervu a kontralaterálního supraorbitálního nervu.
Nález po protažení štěpu surálního nervu – patrný konec štěpu na povrchu postiženého pravého oka, štěp prochází horním víčkem pravého oka, následně podkožním tunelem na levou stranu, kde je patrný jeho druhý konec (A). Preparace jednotlivých fasciklů na povrchu postiženého oka, stav před fixací fasciklů ke skléře (B). Nález po přišití nervových fasciklů štěpu a jejich krytí bulbární spojivkou (C). Podvázaný supraorbitální nerv na zdravé straně, v horním levém rohu je patrný konec nervového štěpu (D). Přerušení supraorbitálního nervu na zdravé straně (E). End-to-end anastomóza mezi supraorbitálním nervem a štěpem surálního nervu (F). zajištění anastomózy fibrinovým tkáňovým lepidlem před uzavřením rány (G)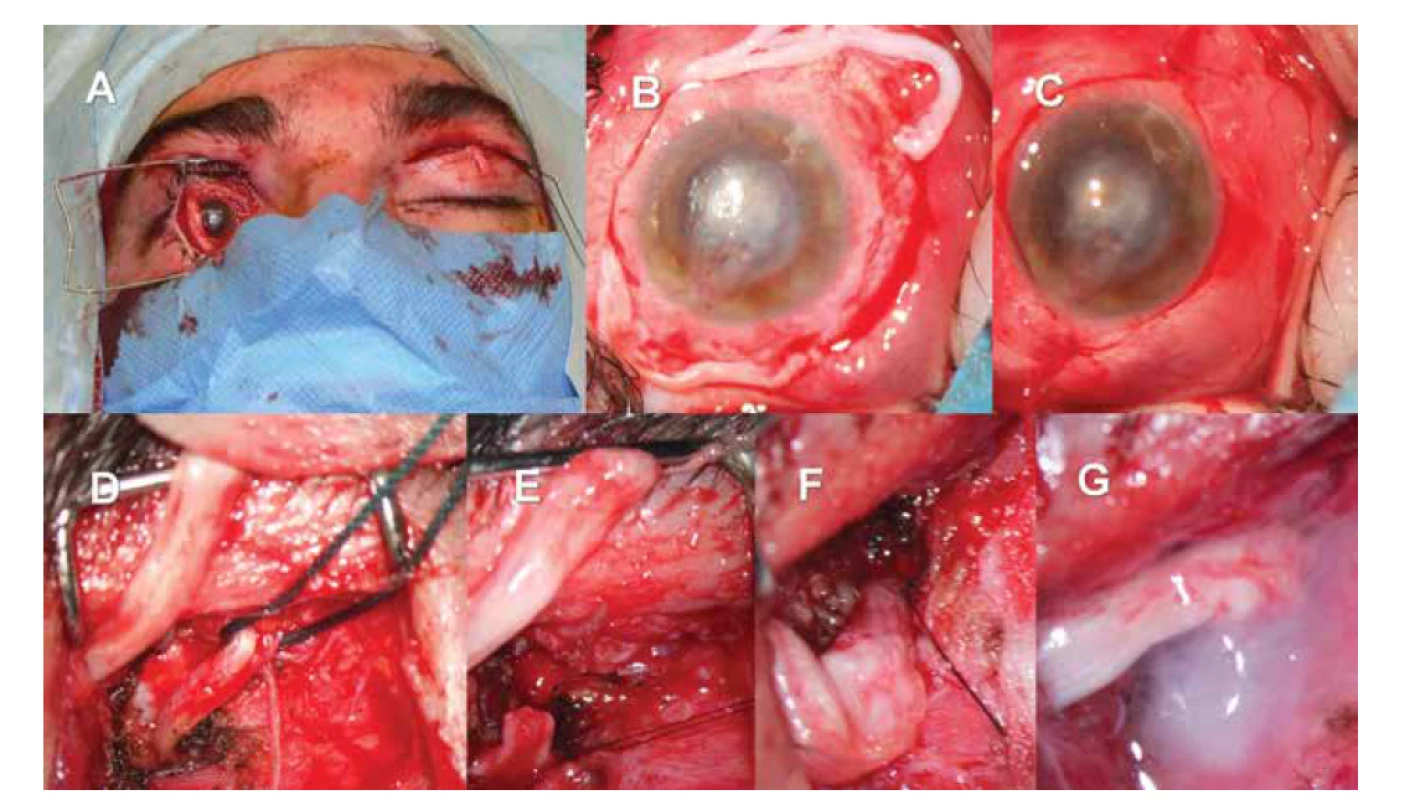
Chirurgický zákrok byl proveden ve spolupráci s neurochirurgem specializujícím se na chirurgii periferních nervů. Byl zvolen přístup využívající anastomózu na supraorbitální nerv. Jako zdroj nervového štěpu byl zvolen surální nerv. Bezpečné a šetrné protažení nervového štěpu přes glabelu bylo zajištěno dutým polyethylenovým zavaděčem. Zákrok i pooperační období proběhly bez komplikací. V bezprostředním pooperačním období byly prováděny převazy pravého oka s antibiotickou mastí (tobramycin), mydriatiky (homatropin gtt. 5%) a epitelizačním gelem, po odeznění chemózy bulbární spojivky byla rohovka kryta měkkou kontaktní čočkou, pacient frekventně (po 1 hod.) aplikoval umělé slzy v kombinaci s mydriatiky (homatropin gtt. 5% po 8 hod.), lokálním antibiotikem (tobramycin po 8 hod.) a lokálním kortikosteroidem (fluorometholon po 12 hod.).
Pět měsíců po výkonu se začala poprvé obnovovat citlivost rohovky pravého oka, která se během dalších pět měsíců postupně zlepšovala, v současné době je plně obnovená citlivost (testováno vatovou štětičkou) rohovky ve třech kvadrantech, jeden kvadrant (dolní nasální kvadrant) zůstal hypestetický. I přes zlepšující se citlivost rohovky pravého oka, přetrvával nehojící se vřed na rohovce, proto byla 6 měsíců po nepřímé neurotizaci rohovky znovu provedena transplantace amniové membrány do defektu (ve dvou vrstvách) s pooperačním krytím měkkou kontaktní čočkou. Po zákroku došlo k postupné epitelizaci rohovky, epitel rohovky byl přehojen a stehy byly extrahovány 8 týdnů po výkonu. Spolu s pokračující epitelizací rohovky se začalo projasňovat i zkalené rohovkové stroma, 11 měsíců po nepřímé neurotizaci rohovky přetrvává vaskularizovaná makula rohovky v temporálním kvadrantu, jinak je stroma rohovky zcela transparentní. Nejlepší korigovaná ostrost pravého oka 0,1 byla dosažena 7 měsíců po neurotizaci rohovky, postupně ale pro progresi komplikované intumescentní katarakty došlo k poklesu na 1/50, certa. Operaci katarakty plánujeme provést po dlouhodobé stabilizaci rohovkového nálezu. Obrázek 4.
Obr. 4. (A) Nález 2 týdny po výkonu – patrný perilimbální val pod bulbární spojivkou způsobený jednotlivými nervovými fascikly štěpu, dále rozsáhlá ulcerace rohovky. (B, C) Vývoj nálezu 6 měsíců (po transplantaci amniové membrány) a 8 měsíců po výkonu – postupné uzavírání ulcerace a projasňování stromatu rohovky. (D): Nález 9 měsíců po zákroku (obrázek zkresluje arteficiální mydriáza a intumescentní katarakta pravého oka) – rohovková ulcerace je uzavřena, nazální a centrální část rohovky je výrazně projasněna, přetrvává prošednutí v temporální části rohovky 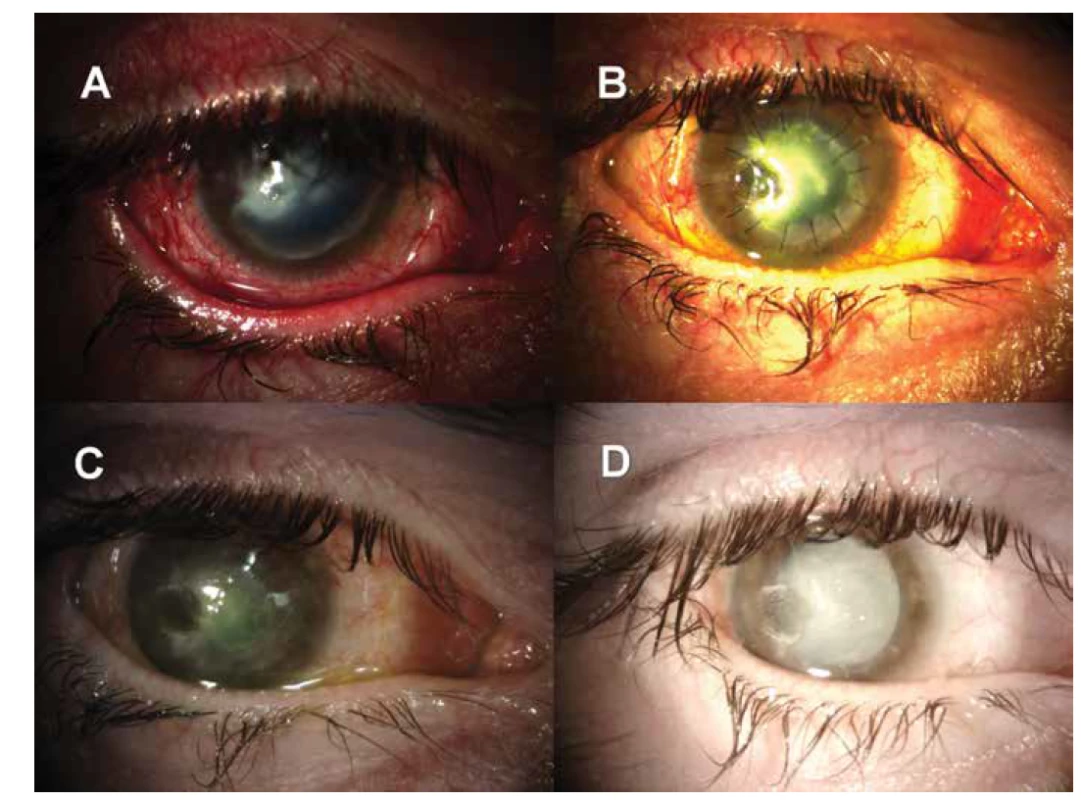
Jako trvalý následek nepřímé neurotizace rohovky u pacienta přetrvávají drobné anestetické okrsky ve kštici na levé straně (inervační oblast přerušeného n. supraorbitalis) a na malíkové straně pravé nohy (inervační oblast n. suralis použitého na nervový štěp).
Diskuze
Nervy rohovky a epiteliální buňky se vzájemně podporují prostřednictvím uvolňování trofických faktorů podporujících proliferaci, migraci a diferenciaci epiteliálních buněk, stejně jako růst a vývoj periferních nervů. Tyto faktory jsou zásadní pro udržení homeostázy povrchu oka a hojení ran. Rohovkové nervy exprimují mnoho neuromediátorů důležitých pro trofiku epitelu, jako je substance P, CGRP (calcitonin gene-related peptide), acetylcholin, noradrenalin, serotonin, neuropeptid Y a VIP (vasointestinální peptid). Naopak epiteliální buňky rohovky uvolňují různé neurotrofické růstové faktory, včetně NGF, CNTF (ciliary neurotrophic factor) nebo GDNF (glial-cell line derived neurotrophic factor) [4-6]. Tyto složité komplexní vzájemné vztahy mezi epiteliálními buňkami a nervy rohovky jsou rozhodující pro fyziologickou obnovu rohovky a hojení ran. Snížení citlivosti rohovky tyto trofické vztahy naruší a může vyvolat patologické změny typické pro NK.
Klasifikační systém podle Mackieho rozděluje dle závažnosti NK na 3 stupně. U 1. stupně dochází v důsledku snížené mitózy a obnovy epiteliálních buněk a zvýšené permeability epitelu ke snížení centrální tloušťky rohovky, poškození epitelu tlakem víček a k rozvoji tečkovité epitelopatie rohovky. U 2. stupně přetrvávají nehojící se epiteliální defekty rohovky, dochází k poškození Bowmanovy membrány a expozici stromatu rohovky. U 3. stupně je zasaženo stroma rohovky, rozvíjí se nerovnováha mezi aktivátory a inhibitory matrixových metaloproteináz (MMP) a nastupuje stromální lýza s rizikem perforace rohovky a ztráty vidění nebo oka [9]. Nález u našeho pacienta byl klasifikován jako stupeň 3.
Při léčbě našeho pacienta byly postupně vyčerpány možnosti standardní běžně dostupné konzervativní i chirurgické terapie. Studie publikované v poslední době popsaly velmi slibné výsledky lokální terapie pomocí NGF [4,10]. Cenegermin, prodávaný pod značkou OxervateTM (cenegermin-bkbj ophthalmic solution, Dompé), je rekombinantní forma lidského nervového růstového faktoru (rhNGF). V červenci 2017 byl v Evropské unii schválen jako přípravek pro oční kapky k léčbě středně těžké nebo těžké neurotrofické keratitidy u dospělých, v srpnu 2018 byl schválen v USA. Oční kapky obsahují 0,002 % (0,02 mg/ml) účinné látky. OxervateTM se aplikuje šestkrát denně ve dvouhodinových intervalech po dobu osmi týdnů. Nevýhodou je jednak uchovávání (kapky je nutno skladovat při teplotě -15 až -25 °C), jednak vysoká cena preparátu (dodací cena do ČR přesahuje 29500 Euro). Ve studiích se objevují i další lokální preparáty s dobrými výsledky: např. RGTA (Cacicol20®, laboratories Théa), thymosin beta-4, substance P, nicergolin nebo citikolin [4–7]. U pacienta z naší kasuistiky nebylo z finančních důvodů možno oční kapky z autologního séra, Cacicol20® ani další zmíněné působky pro léčbu použít. Proto jsme se po domluvě s pacientem rozhodli pro chirurgický zákrok.
Chirurgická léčba je vyhrazena pro 3. stadium neurotrofické keratopatie, tj. rohovkové ulcerace nereagující na konvenční lokální terapii a/nebo související komplikace. Mezi nejběžnější chirurgické postupy patří parciální tarsorafie, okluze oční štěrbiny pomocí aplikace botulotoxinu do zdvihače horního víčka (m. levator palpebrae superioris), spojivkový lalok či transplantace amniové membrány [11]. Malé perforace lze účinně ošetřit kyanoakrylátovým nebo fibrinovým lepidlem, větší defekty si mohou vyžádat lamelární nebo penetrující keratoplastiku [4,12]. U našeho pacienta jsme postupně vyčerpali dostupné chirurgické metody. Byla provedena parciální tarzorafie, aplikaci botulotoxinu A jsme nezvažovali pro jeho pouze přechodný efekt, opakovaně byly prováděny transplantace amniové membrány. Konjunktivální lalok nebyl použit, neboť po zákroku nelze čekat plné obnovení transparence rohovky. Byly proto hledány další terapeutické možnosti. Byla zvolena metoda neurotizace rohovky. Jde o zákrok, který je v zahraniční literatuře dobře dokumentován, jeho použití v naší republice však dosud nebylo publikováno. Výhodou zákroku je kauzální ovlivnění příčiny postižení rohovky, jedná se však o zákrok technicky náročný, vyžadující multidisciplinární přístup a podrobné pooperační sledování [13,14]. První zmínka o neurotizaci rohovky pochází z roku 1972, kdy Samii popsal připojení hlavního okcipitálního nervu k proximální části n. ophthalmicus pomocí štěpu surálního nervu [13]. V roce 2009 Dr. Terzis poprvé představil přímou neurotizaci rohovky v případech obrny lícního nervu s ipsilaterálním postižením trojklaného nervu a anestezií rohovky. Terzis využil přenos kontralaterálního supratrochleárního nebo supraorbitálního nervu přímo do neurotrofické rohovky [14].
Při neurotizaci rohovky je obvykle preferován supraorbitální nerv, lze ale využít i nerv supratrochleární, popř. vzácně infraorbitální [15]. Ipsilaterální přístup se indikuje pouze v případech, kdy je denervace limitována na oční bulbus (tj. postiženy jsou jen nn. ciliares longi). V ostatních případech je využíván kontralaterální přístup, kdy je potřeba vytvořit podkožní tunel do horního víčka postiženého oka [8].
U přímé neurotizace se po lokalizaci a preparaci supraorbitální (resp. supratrochleární) nerv stočí a provlékne do horního fornixu postiženého oka. Exponované nervové fascikly se poté protáhnou připravenými tunely v subtenonském prostoru do jednotlivých kvadrantů a fixují ke skléře při limbu (kolmo na limbus). Vzhledem k omezené délce použitého nervu je u přímé neurotizace obvykle využíván ipsilaterální přístup, teoreticky lze využít i přístup kontralaterální. Výhodou přímé neurotizace je rychlejší průběh reinervace a vytvoření jen jednoho nového senzorického defektu (v inervační oblasti použitého nervu), nevýhodou je pak nutnost provedení velkého bikoronárního řezu.
U nepřímé neurotizace je supraorbitální (popř. supratrochlární nerv) lokalizován a přerušen pod horní hranou očnice. Na přerušený nerv je přišit štěp sensitivního nervu (nejčastěji n. suralis, vzácně n. auricularis magnus), využívá se end-to-end nebo end-to-side anastomózy. Stejně jako v případě přímé neurotizace je nervový štěp provléknut do horního fornixu postiženého oka, obnažené nervové fascikly štěpu jsou protaženy tunely v subtenonském prostoru do jednotlivých kvadrantů a fixovány ke skléře do perilimbálního prostoru. U nepřímé neurotizace lze využít oba přístupy, tj. jak ipsilaterální, tak kontralaterální. Nevýhodou této varianty zákroku je delší trvání operace, delší doba reinervace rohovky a vytvoření dalšího senzorického defektu (v inervační oblasti nervu použitého na štěp). U našeho pacienta nebylo možné použít ipsilaterální přístup, neboť při podrobném předoperačním neurologickém vyšetření byla mimo anestezie rohovky zjištěna hypestezie v celé inervační oblasti trigeminálního nervu vpravo. Vzhledem k nutnosti kontralaterálního přístupu jsme se rozhodli použít autologní nervový štěp. Ze zkušeností z přípravných operací na kadaveru jsme se rozhodli pro anastomózu na supraorbitální nerv, který se jevil ve srovnání se supratrochleárním nervem silnější, a tudíž pro zákrok vhodnější. Jako zdroj nervového štěpu byl zvolen surální nerv s ohledem na dobrou přístupnost a malý pooperační denervační defekt. Nevýhodou zvoleného postupu je zejména délka trvání zákroku, která by mohla být v budoucnu redukována, např. pomocí paralelní preparace surálního nervu a přípravy kožních a podspojivkových tunelů. Jako nejnáročnější krok výkonu se jevila lokalizace a preparace surálního nervu. Fixace jednotlivých nervových fasciklů štěpu ke skléře postiženého oka je technicky náročná, fixace musí být pevná, zároveň ale nesmí dojít k traumatizaci velmi křehkých nervových fasciklů.
V roce 2018 Leyngold představil minimálně invazivní endoskopický přístup ze subgaleálního prostoru pomocí tupého endoskopického elevátoru k hornímu orbitálnímu okraji [15]. Endoskopický postup nebyl pro očekávanou technickou náročnost u našeho pacienta zvolen. Zajímavou a slibně vypadající modifikací výkonu je použití aloimplantátů acelulárního nervu (Avance Nerve Graft, AxoGen) k nepřímé neurotizaci [15,16]. V České republice jsou tyto aloimplantáty ale zatím špatně dostupné, jejich širší využití je navíc zatím limitováno omezenou délkou aloimplantátu (do 5 cm).
Reinervace po chirurgické neurotizaci rohovky pravděpodobně nastává kombinací přímého klíčení z proximálních nervových zakončení a uvolnění neurotrofních faktorů. Kompletní neurotizace rohovky je patrná 6 měsíců do 2 let po operaci, rychlost neurotizace ovlivňuje především věk pacienta a komorbidity [17,18]. U našeho pacienta se první známky reinervace rohovky objevily 5 měsíců po výkonu, což odpovídalo námi zvolenému postupu s využitím nervového štěpu. V případě naší kazuistiky byla citlivost rohovky před výkonem a v pooperačním průběhu sledována pomocí vatové štětičky, do budoucna by bylo výhodné ke sledování citlivosti použít esteziometr nebo postupující neurotizaci rohovky objektivizovat např. pomocí in vivo konfokální rohovkové mikroskopie [19].
Časnou komplikací výkonu může být hematom, popř. infekce rány. Mezi pozdní komplikace patří především neúčinná neurotizace a rozvoj neuromu v oblasti anastomózy (u nepřímé neurotizace). U našeho pacienta jsme žádné komplikace nezaznamenali. K dosažení výsledného dobrého efektu však bylo potřeba provést ještě znovu transplantaci amniové membrány do perzistujícího defektu.
Závěr
Přímá a nepřímá neurotizace rohovky za využítí n. supraorbitalis, n. supratrochlearis nebo n. infraorbitalis představuje možnost kauzálního řešení u pacientů s těžkými formami neurotrofické keratopatie. V naší kazuistice mladého muže s těžkou neurotrofickou keratopatií pravého oka byla použita technika nepřímé reinervace rohovky s využitím štěpu surálního nervu. Rohovkový nález u pacienta z naší kasuistiky se po zákroku výrazně zlepšil, první známky reinervace se objevily 5 měsíců po výkonu, došlo k uzavření chronické rohovkové ulcerace, 11 měsíců po výkonu je rohovka s výjimkou vaskularizované makuly v temporální periferii zcela transparentní. Samotný výkon je však technicky náročný, pooperační vývoj je komplexní a vyžaduje pečlivé sledování a v některých případech i nutnost dalších chirurgických zákroků.
Autoři práce prohlašují, že vznik i téma odborného sdělení a jeho zveřejnění není ve střetu zájmů a není podpořeno žádnou farmaceutickou firmou. Tato práce nebyla zadána ani otištěna v jiném časopise.
MUDr. Štěpán Rusňák, Ph.D.
alej Svobody 80
30460 Plzeň
E-mail: rusnak@fnplzen.cz
Do redakce doručeno dne: 24. 8. 2020
Přijato k publikaci dne: 2. 2. 2021
Zdroje
1. Sacchetti M, Lambiase A. Diagnosis and management of neurotrophic keratitis. Clin Ophthalmol. 2014 Mar;8 : 571-579.
2. Hsu HY, Modi D. Etiologies, Quantitative Hypoesthesia, and Clinical Outcomes of Neurotrophic Keratopathy. Eye Contact Lens. 2015 Sep;41(5):314-317.
3. Müller LJ, Marfurt CF, Kruse F, Tervo TM. Corneal nerves: structure, contents and function. Exp Eye Res. 2003 May;76(5):521-542.
4. Versura P, Giannaccare G, Pellegrini M, Sebastiani S, Campos EC. Neurotrophic keratitis: current challenges and future prospects. Eye Brain. 2018 Jun;10 : 37-45.
5. Dunn SP, Heidemann DG, Chow CY, et al. Treatment of chronic non-healing neurotrophic corneal epithelial defects with thymosin beta4. Ann N Y Acad Sci. 2010;1194 : 199-206.
6. Yamada N, Matsuda R, Morishige N, et al. Open clinical study of eye-drops containing tetrapeptides derived from substance P and insulin-like growth factor-1 for treatment of persistent corneal epithelial defects associated with neurotrophic keratopathy. Br J Ophthalmol. 2008;92(7):896-900.
7. Cinar E, Yuce B, Aslan F, Erbakan G. Neuroprotective Effect of Citicoline Eye Drops on Corneal Sensitivity After LASIK. J Refract Surg. 2019 Dec 1;35(12):764-770.
8. Weis E, Rubinov A, Al-Ghoul AR, Yau FM. Sural nerve graft for neurotrophic keratitis: early results. Can J Ophthalmol. 2018 Feb;53(1):24-29.
9. Dua HS, Said DG, Messmer EM, et al. Neurotrophic keratopathy. Prog Retin Eye Res. 2018 Sep;66 : 107-131.
10. Bonini S, Lambiase A, Rama P, et al. REPARO Study Group. Phase II Randomized, Double-Masked, Vehicle-Controlled Trial of Recombinant Human Nerve Growth Factor for Neurotrophic Keratitis. Ophthalmology. 2018 Sep;125(9):1332-1343.
11. Krčová I, Stanislavová M, Peško K, Furdová A, Koller J. Možnosti použitia amniovej membrány – naše skúsenosti [Amniotic membrane applications - our experience]. Cesk Slov Oftalmol. 2016;72(6):204-208. Slovak.
12. Fogle JA, Kenyon KR, Foster CS. Tissue adhesive arrests stromal melting in the human cornea. Am J Ophthalmol. 1980;89(6):795-802.
13. Samii M. Autologe Nerven-Transplantation im Trigeminusbereich. Med Mitt. 1972;46 : 189-94.
14. Terzis JK, Dryer MM, Bodner BI. Corneal neurotization: a novel solution to neurotrophic keratopathy. Plast Reconstr Surg. 2009;123(1):112-120.
15. Leyngold I, Weller C, Leyngold M, Tabor M. Endoscopic Corneal Neurotization: Technique and Initial Experience. Ophthalmic Plast Reconstr Surg. 2018 Jan/Feb;34(1):82-85.
16. Leyngold IM, Yen MT, Tian J, Leyngold MM, Vora GK, Weller C. Minimally Invasive Corneal Neurotization With Acellular Nerve Allograft: Surgical Technique and Clinical Outcomes. Ophthalmic Plast Reconstr Surg. 2019 Mar/Apr;35(2):133-140.
17. Malhotra R, Elalfy MS, Kannan R, Nduka C, Hamada S. Update on corneal neurotisation. Br J Ophthalmol. 2019 Jan;103(1):26-35.
18. Fung SSM, Catapano J, Elbaz U, Zuker RM, Borschel GH, Ali A. In Vivo Confocal Microscopy Reveals Corneal Reinnervation After Treatment of Neurotrophic Keratopathy With Corneal Neurotization. Cornea. 2018 Jan;37(1):109-112.
19. Mahelková G, Česká Burdová M, Odehnal M, Dotřelová D. In vivo corneal confocal microscopy: basic principles and applications. Cesk Slov Oftalmol. 2017;73(4):155-160. Available from: http://www.cs-ophthalmology.cz/en/journal/articles/40
Štítky
Oftalmologie
Článek SYNDROM SUCHÉHO OKA. PŘEHLED
Článek vyšel v časopiseČeská a slovenská oftalmologie
Nejčtenější tento týden
- Selektivní laserová trabekuloplastika nesnižuje nitroční tlak více než argonová laserová trabekuloplastika
- Progresi glaukomu je třeba hodnotit strukturálními i funkčními parametry
- Ztráta centrálního vidění po filtrujících operacích glaukomu
- Od PGF-2 alfa-isopropyl esteru k latanoprostu: přehled vývoje Xalatanu
- Compliance u pacientů s glaukomem
-
Všechny články tohoto čísla
- SYNDROM SUCHÉHO OKA. PŘEHLED
- RETROSPEKTIVNÍ ANALÝZA PŘÍTOMNOSTI CHOROIDÁLNÍ NEOVASKULARIZACE METODOU OPTICKÉ KOHERENČNÍ TOMOGRAFICKÉ ANGIOGRAFIE PŘI LÉČBĚ CHRONICKÉ CENTRÁLNÍ SERÓZNÍ CHORIORETINOPATIE POMOCÍ FOTODYNAMICKÉ TERAPIE
- OCT ANGIOGRAFIE A DOPPLEROVSKÁ SONOGRAFIE U HYPERTENZNÍCH GLAUKOMŮ
- CYKLOKRYOKOAGULÁCIA U SEKUNDÁRNYCH NEOVASKULÁRNYCH GLAUKÓMOV A NAŠE VÝSLEDKY
- NEUROTIZACE ROHOVKY U TĚŽKÉ FORMY NEUROTROFICKÉ KERATOPATIE. KAZUISTIKA
-
SKOTÓMY V ZORNOM POLI AKO PRVÝ PRÍZNAK INTRAKRANIÁLNEJ EXPANZIE.
KAZUISTIKA -
Čestná plaketa T. R. Niederlanda udelená
prof. MUDr. Andrejovi Černákovi, DrSc., FEBO,
pri príležitosti životného jubilea
- Česká a slovenská oftalmologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- SYNDROM SUCHÉHO OKA. PŘEHLED
-
SKOTÓMY V ZORNOM POLI AKO PRVÝ PRÍZNAK INTRAKRANIÁLNEJ EXPANZIE.
KAZUISTIKA - NEUROTIZACE ROHOVKY U TĚŽKÉ FORMY NEUROTROFICKÉ KERATOPATIE. KAZUISTIKA
- CYKLOKRYOKOAGULÁCIA U SEKUNDÁRNYCH NEOVASKULÁRNYCH GLAUKÓMOV A NAŠE VÝSLEDKY
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání




