-
Články
Top novinky
Reklama- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
Top novinky
Reklama- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Top novinky
ReklamaDoporučení České revmatologické společnosti pro léčbu osteoartrózy kolenních, kyčelních a ručních kloubů
Treatment of osteoarthritis
The author presents the recommendations of the Czech Society for Rheumatology for the treatment of osteoarthritis of the knee, hip and hand joints based on the available evidence on efficacy and consensus of the committee of the Czech Society for Rheumatology. In the introductory part of the report the problems that must be resolved before determining a treatment plan for each patient are analyzed: the correct diagnosis of osteoarthritis, osteoarthritis classification (primary, secondary, monoarticular, polyarticular or generalized), the type, intensity and frequency of pain, functional limitations, structural joint damage, rate of progression of degenerative changes, another diseases of the patient, the use of medication and their possible interactions. The basic goals in the treatment of osteoarthritis include: reduction of pain and stiffness of the joint, improvement or at least maintenance of joint mobility, improvement of physical function, alleviation of disability, improvement of health-dependent quality of life, retardation of the progression of joint destruction and education of the patient about the nature of his illness and its treatment. The treatment plan should be designed individually for each patient. Optimal care is provided by several experts, in addition to a rheumatologist, a patient with osteoarthritis should be also treated by a physical therapist, orthopedic surgeon, internist and obesitologist if needed. Each patient should be treated comprehensively. Complex treatment of osteoarthritis consists of non-pharmacological treatment, pharmacological therapy and surgery if needed. Evidence-based non-pharmacological methods of treatment include patient education, lifestyle modification (weight reduction, modification of biomechanical ratios), regular exercise, some means of physical therapy and the use of prosthetic and support devices. Pharmacological treatment with evidence-based effectiveness comprise paracetamol, systemically and locally administered NSAIDs, strong and weak opioids, intra-articular glucocorticoids and some symptomatic slow-acting drugs in osteoarthritis (SYSADOA – glucosamine sulfate, diacerein, an avocado and soy extract, chondroitin sulfate and hyaluronic acid). The surgical procedures with evidence-based effectiveness include replacement of hip and knee joints, both total and unicompartmental. There is no clear evidence on the effectiveness of arthroscopic procedures such as joint lavage and debridement. Osteotomy is recommended for osteoarthritis of the hip, especially in patients with dysplasia. Osteotomy in osteoarthritis of knee joints is not included in the new EULAR recommendations. In OA of the hand joints, there is a direct evidence of effectiveness for education and exercise, NSAIDs, COX-2 inhibitors, local NSAIDs and capsaicin, and chondroitin sulfate. Acetaminophen, glucosamine and local glucocorticoids were recommended upon extrapolation from other sites.
Key words:
osteoarthritis, pharmacological treatment, total joint replacemtent
Autoři: K. Pavelka
Působiště autorů: Revmatologický ústav Praha
Vyšlo v časopise: Čes. Revmatol., 20, 2012, No. 3, p. 138-157.
Kategorie: Doporučení
Na základě dostupné evidence o účinnosti a po konsenzu členů výboru České revmatologické společnosti předkládá autor Doporučení České revmatologické společnosti pro léčbu osteoartrózy kolenních, kyčelních a ručních kloubů. V úvodní části práce jsou analyzovány problémy, které je nutno vyřešit před stanovením léčebného plánu u každého pacienta: správná diagnóza osteoartrózy, klasifikace osteoartrózy (primární, sekundární, monoartikulární, polyartikulární, generalizovaná), typ bolesti u nemocného, intenzita a frekvence bolesti, funkční omezení, strukturální poškození kloubu, rychlost progrese degenerativních změn, další onemocnění pacienta, jaké léky užívá a jejich možné interakce. Základní cíle při léčbě osteoartrózy jsou: zmenšit kloubní bolest a ztuhlost, zlepšit nebo alespoň zachovat kloubní mobilitu, zlepšit fyzické funkce, zmírnit hendikep, zlepšit na zdraví závislou kvalitu života, zpomalit progresi kloubní destrukce a vzdělat pacienta o povaze jeho nemoci a její léčbě. Léčebný plán by měl být navržen individuálně pro každého pacienta.
Souhrn
Na základě dostupné evidence o účinnosti a po konsenzu členů výboru České revmatologické společnosti předkládá autor Doporučení České revmatologické společnosti pro léčbu osteoartrózy kolenních, kyčelních a ručních kloubů. V úvodní části práce jsou analyzovány problémy, které je nutno vyřešit před stanovením léčebného plánu u každého pacienta: správná diagnóza osteoartrózy, klasifikace osteoartrózy (primární, sekundární, monoartikulární, polyartikulární, generalizovaná), typ bolesti u nemocného, intenzita a frekvence bolesti, funkční omezení, strukturální poškození kloubu, rychlost progrese degenerativních změn, další onemocnění pacienta, jaké léky užívá a jejich možné interakce. Základní cíle při léčbě osteoartrózy jsou: zmenšit kloubní bolest a ztuhlost, zlepšit nebo alespoň zachovat kloubní mobilitu, zlepšit fyzické funkce, zmírnit hendikep, zlepšit na zdraví závislou kvalitu života, zpomalit progresi kloubní destrukce a vzdělat pacienta o povaze jeho nemoci a její léčbě. Léčebný plán by měl být navržen individuálně pro každého pacienta. Optimální je péče více odborníků, kromě revmatologa by měl o pacienta s osteoartrózou pečovat dále fyzioterapeut, ortoped, internista a event. obezitolog. Každý pacient by měl být léčen komplexně. Komplexní terapie osteoartrózy sestává z léčby nefarmakologické, farmakologické a ev. chirurgické. Mezi nefarmakologické způsoby léčby s evidencí o účinnosti patří edukace pacienta, režimová opatření (redukce hmotnosti, úprava biomechanických poměrů), pravidelné cvičení, některé prostředky fyzikální léčby a užívání protetických a opěrných pomůcek. Z prostředků farmakologické léčby mají evidenci o účinnosti paracetamol, systémově a lokálně podávaná nesteroidní antirevmatika (NSA), silné a slabé opioidy, intraartikulární aplikace glukokortikoidů a některé symptomaticky působící léky u osteoartrózy (SYSADOA – glukosamin sulfát, diacerein, výtažek z avokáda a sóji, chondroitin sulfát a kyselina hyaluronová). Z chirurgických postupů mají evidenci o účinnosti náhrady kyčelních a kolenních kloubů a to jak totální, tak unikompartamentální. Není jasná evidence o účinnosti artroskopických postupů jako je kloubní laváž a debridement. Osteotomie je doporučována u osteoartrózy kyčelních kloubů a to především u pacientů s dysplazií. V nových doporučeních EULAR není osteotomie zahrnuta u artrózy kolenních kloubů. Přímá evidence o účinnosti existuje u OA rukou pro vzdělávání a cvičení, NSA, COX-2 inhibitory, lokální NSA a kapsaicin a chondroitin sulfát. Extrapolací z jiných lokalizací byly doporučeny paracetamol, glukosamin a lokální glukokortikoidy.
Klíčová slova:
osteoartróza, rehabilitace, farmakologická léčby, totální náhrady kloubůLéčba osteoartrózy kyčelních a kolenních kloubů
Osteoartróza (OA) je nejčastějším kloubním onemocněním a je častou příčinou bolesti kloubů a zhoršení funkce. V populaci nad 65 let trpí obtížemi spojenými s artrózou kolenních a kyčelních kloubů až 40 % populace (1). Velmi častá je i artróza ručních kloubů a páteře. Vzhledem k demografickému vývoji také pacientů s OA přibývá.
Před zahájením léčby každého pacienta s OA je nutné analyzovat několik otázek.
- Má pacient skutečně osteoartrózu a je OA zodpovědná za bolesti a další příznaky, pro které pacient přichází? Diagnóza OA není snadná. Problémem může být nesoulad klinických obtíží s morfologickou závažností OA. V praxi lze použít diagnostická a klasifikační kritéria ACR (2) (tab. 1) nebo Doporučení Evropské ligy proti revmatismu (EULAR) pro diagnózu OA kolenních kloubů (3).
Tab. 1. Klasifikační kritéria gonartrózy. 
- Jaký je typ bolesti u nemocného? Za prvé je nutné určit, má-li pacient pouze bolesti při zatížení (např. při chůzi) nebo i v klidu. Někteří pacienti mají největší bolesti na začátku pohybu (tzv. startovací bolest). Je nutné určit, jak velká je zátěž, jež bolest vyvolává, bolest může např. vyvolávat ujití již několika metrů. U jiných to mohou být stovky metrů či několik kilometrů. Někteří pacienti mají bolesti pouze při určité specifické činnosti např. chůzi ze schodů u gonartrózy či obouvání se při koxartróze.
- Jaká je příčina bolesti u osteoartrózy? Příčin bolesti u OA může být celá řada. Kloubní chrupavka je sice primárním místem patologického děje, ale je avaskulární a aneurální a tudíž není primárním zdrojem bolesti. Tím je synoviální membrána, subchondrální kost, svalové úpony, šlachy, vazy a burzy (obr. 1). Příčinou bolesti může být také zánět při synovitidě, zvýšený nitrokostní tlak, napínání kloubního pouzdra, rostoucí osteofyty, kostní nekróza nebo se může více příčin kombinovat. Pokud např. zjistíme, že příčinou bolesti je zánět, jsou plně indikovány protizánětlivé postupy např. lokální aplikace glukokortikoidů nebo plná dávka NSA.
Obr. 1. 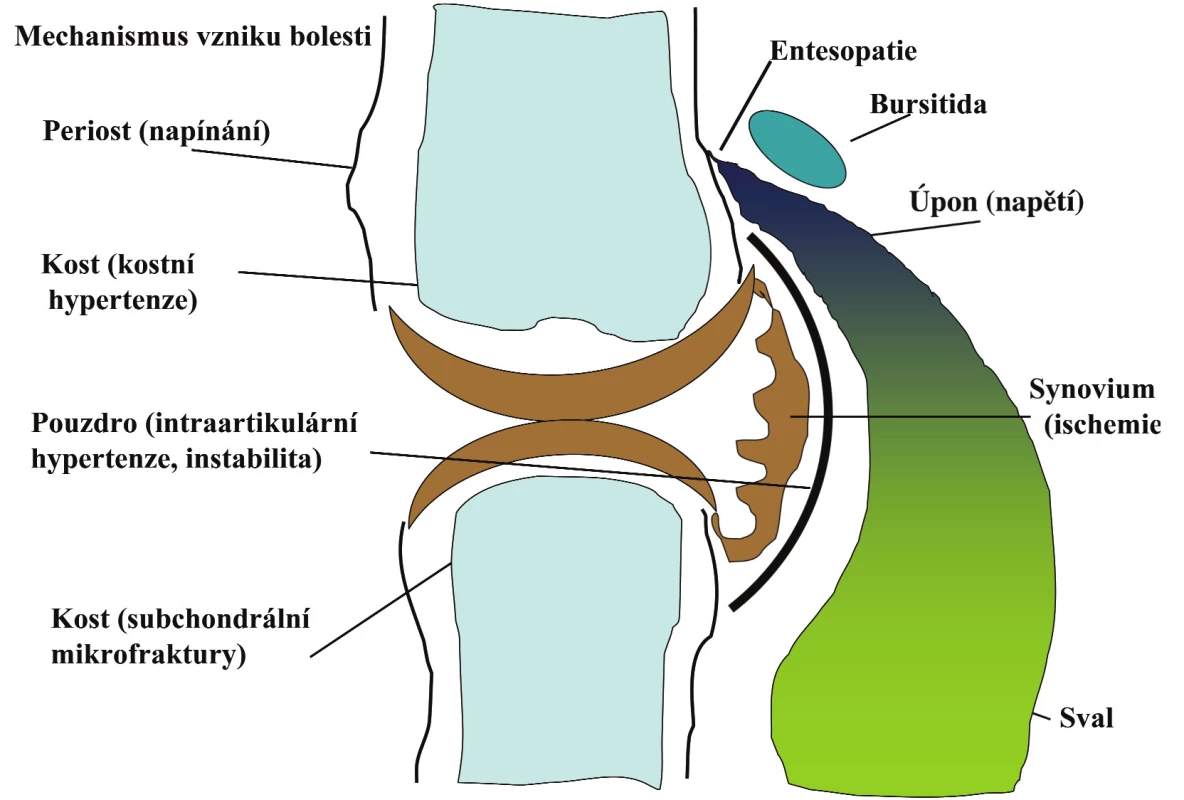
- Jaká je intenzita a frekvence bolesti? Bolest je subjektivní příznak a tudíž je objektivně neměřitelná, nicméně existuje celá řada metod moderní algeziologie, které se bolest snaží numericky hodnotit. Alespoň orientačně je nutné i v běžné praxi ohodnotit intenzitu bolesti (malá až nesnesitelná), její časový profil (bolest kontinuální, přechodná, intermitentní). Nepřímým ukazatelem bolesti, resp. pacientova vnímání bolesti, je i spotřeba analgetik a NSA (kolísá od kontinuálního denního podávání až po výjimečné používání 2x do měsíce).
- Jaké je omezení fyzických funkcí, event. hendikep u jedince? K hodnocení závažnosti OA je možné použít kompozitní, validizovaný index, jako je například WOMAC (4). Hendikep je omezení fyzických funkcí, aplikované na konkrétního jedince. Např. nemožnost sportovat nemusí u staršího jedince vyvolávat žádný hendikep, zatímco u jiného, mladšího může znamenat velké zhoršení kvality života.
- Jaké je strukturální poškození kloubu? Zlatým standardem je rentgenové hodnocení a známé dělení podle stadií (Kellgren-Lawrence). Zmíněné hodnocení je však příliš hrubé a v praxi bývá jeho význam přeceňován. Znalost o tom, do jaké míry je kloub poškozen je však důležitá. Hodnotí se především zúžení kloubní štěrbiny a vznik osteofytů. Důležité můžou být i další morfy, jako je osteonekróza, kostní pseudocysty, desaxace kloubu. Důležité je i určení, kde je kloub poškozen, např. mediální či laterální část tibiofemorálního kloubu nebo kloub patelofemorální. Magnetická rezonance (MR) může ukázat i doprovodné léze menisků, což může mít dopad při rozhodování o léčbě. Několik nových studií ukázalo i význam MR při hodnocení progrese OA. Přítomnost kostního edému je prediktivní ukazatelem rizika rychlé rentgenové progrese.
- Jak rychle OA progreduje? Většina pacientů s OA progreduje pomalu. Malá část ale progreduje rychle a patří do skupiny tzv. rychle progredující OA. Zatímco běžný úbytek chrupavky na rentgenovém snímku je u normální OA 0,1–0,2 mm za rok, u rychle progredujících artróz to může být i 1mm za rok. U těchto pacientů může být interval od prvních obtíží do terminálního stadia OA jen několik roků či dokonce měsíců. Rizikové faktory rychlé progrese OA zatím nejsou plně objasněny, možné rizikové faktory jsou uvedeny v tabulce 2. Větší riziko představuje např. unilaterální koxartróza u mladších mužů, nebo naopak postižení druhého kolene u gonartrózy, nebo generalizovaná OA zvláště u jedinců s genetickou predispozicí. Zvýšené riziko mají i nemocní s otokem kostní dřeně či synovitidou na MR. Význam biomarkerů pro predikci vývoje OA není zatím jasný.
Tab. 2. Rizikové faktory rychle progredující osteoartróz. 
- Jde o primární či sekundární OA? U sekundárních forem OA zvláště z biomechanických příčin (např. nestejná délka končetin, varózní postavení) je indikováno odstranění nebo alespoň zmírnění této příčiny.
- Má pacient další onemocnění, která mohou ovlivňovat způsob léčby? Závažnější onemocnění pacienta může ovlivňovat schopnost pacienta rehabilitovat nebo podstoupit ortopedický zákrok. Některá onemocnění omezují či znemožňují podávání nesteroidních antirevmatik (vředová choroba, ICHS, hypertenze).
- Jaké pacient užívá léky? Značná část pacientů je starších a užívá léky, které interferují s aplikací např. nesteroidních antirevmatik (warfarin aj.).
- Jaká jsou očekávání pacienta? Osteoartróza je onemocnění zatím nevyléčitelné a primárně progredující a tento fakt je nutné s pacientem prodiskutovat. Nicméně komplexní léčba OA může zlepšit kvalitu života nemocných s OA a stabilizovat další progresi.
Všechna výše uvedená pravidla se dají shrnout do bodu, který je také jedním ze základních doporučení EULAR pro léčbu OA (5): Léčba by měla být individualizována pro každého pacienta podle jeho subjektivních obtíží, objektivního nálezu, strukturální progrese, dalších onemocnění a současné medikace, ale i očekávání a přání pacienta.
Základními cíli při léčbě osteoartrózy jsou:
- zmenšit kloubní bolest a ztuhlost
- zlepšit nebo alespoň zachovat kloubní mobilitu
- zmenšit omezení fyzických funkcí a hendikep
- zlepšit kvalitu života, závislou na zdraví
- zmenšit progresi kloubní destrukce
- vzdělat pacienta o povaze jeho nemoci a její léčbě.
Každý pacient by měl léčen komplexně. Komplexní terapie sestává z léčby nefarmakologické, farmakologické a eventuálně chirurgické (tab. 3).
Tab. 3. Možnosti léčby osteoartrózy. 
Nejčastější a medicínsky nejzávažnější je osteoartróza kolenních a kyčelních kloubů. Následující doporučení jsou proto věnována těmto dvěma lokalizacím. V závěru jsou uvedeny určité specifikace pro OA drobných ručních kloubů.
Nefarmakologická léčba osteoartrózy
Mezi nefarmakologické způsoby léčby řadíme vzdělávání pacienta, režimová opatření, pravidelné cvičení, prostředky fyzikální léčby a užívání protetických a opěrných pomůcek.
Vzdělávání pacienta
Doporučení pro vzdělávání pacientů je důležité a většina „Doporučení“ odborných společností obsahuje vzdělávání jako nedílnou součást léčby především na začátku onemocnění, i když objektivní průkaz o užitečnosti vzdělávání ve smyslu randomizované studie podán nebyl. Kromě pohovoru s pacientem se používají i tištěné materiály, část pacientů má zájem o informace na elektronických médiích. V některých zemích jsou populární materiály pacientských organizací. Pacientovi by měla být vysvětlena podstata onemocnění a její pravděpodobný vývoj. Dále by mu měla být vysvětlena potřeba režimových opatření a nutnost cvičení a rehabilitace. Zdůrazněn by měl být fakt větší užitečnosti modalit s aktivní účastí pacienta než pasivních procedur (např. elektroléčby).
Režimová opatření
Mezi základní režimová opatření patří redukce hmotnosti u pacientů s nadváhou. Objektivní důkaz o účinnosti byl podán u pacientů s gonartrózou, nikoliv s koxartrózou. Nicméně i pacienti s koxartrózou a nadváhou by měli redukovat hmotnost. Objektivní důkaz o účinnosti redukce hmotnosti u gonartrózy byl podán ve dvou randomizovaných, kontrolovaných studiích vysoké kvality. Ve skupině s redukcí hmotnosti došlo k poklesu průměrné bolesti a ztuhlosti a zlepšení funkčních schopností pozitivní byla i metaanalýza publikovaných studií (6). Zařazeny byly celkem 4 studie a 454 pacientů. Velikost účinku na snížení bolesti byla signifikantní, ale malá (ES=0,20; 95% CI 0; 0,39) a rovněž tak na funkci 0,23 (95% CI 0,04; 0,42) při redukci hmotnosti v průměru o 6,1 kg. Regresní analýza ukázala signifikantní zlepšení bolesti a funkce při redukci hmotnosti o více než 5 % nebo více než 0,24 % týdně.
Odstranění nepříznivých mechanických faktorů patří mezi důležité způsoby léčby především u osteoartrózy kolenních a kyčelních kloubů. Patří mezi ně již výše zmíněná redukce hmotnosti, doporučení vhodných aktivit a zátěže, vhodná obuv a použití opěrných či podpůrných pomůcek. Klouby jsou determinovány k pohybu a pravidelný pohyb je podmínkou komplexního zdraví kloubu. U artrózy platí podobná pravidla jako např. u kardiovaskulárního aparátu - nalézt optimální zátěž. Žádná aktivita je škodlivá, přetěžování kloubu rovněž není vhodné. Důležitý je i výběr aktivit. U artrózy kolenních a kyčelních kloubů doporučujeme plavání, jízdu na kole či cvičení na rotopedu. Nedoporučuje se pěstování vrcholového sportu, sporty s doskoky, silové sporty, těžká atletika, zdvíhání těžkých břemen, dlouhé pochody po nerovném terénu, horská turistika, těžká fyzická práce, klečení a práce v podřepu.
Pacienti s osteoartrózou dolních končetin by měli být poučeni o nutnosti nošení vhodné obuvi. Boty by měly mít silnější, ale měkké podrážky bez zvýšených podpatků. U pacientů s OA mediálního kompartmentu (s anebo bez varózní deformity) se osvědčují vložky pod laterální část podrážky, u méně časté OA laterálního kompartmentu (s anebo bez valgózní deformity) pak vložky pod mediální část podrážky (6).
U pacientů s výraznějšími obtížemi se osvědčuje používání opěrných pomůcek, jako jsou hole a berle, u pacientů s výraznými bilaterálními potížemi chodítko. Nošení hole v kontralaterální ruce snižuje bolest. Pozitivní klinické zkušenosti jsou podporovány i několika kineziologickými studiemi (7), které prokazují snížení addukčního momentu v tibiofemorálním kloubu při nošení hole v kontralaterální ruce, který jinak přispívá k morfologické progresi OA. Pacienti by měli být o významu nošení holí poučeni, řada z nich sice hůl vlastní, ale stydí se ji nosit.
U pacientů s mírným stupněm varózní či valgózní nestability je doporučováno nošení ortézy, které snižuje bolest, zlepšuje funkci a snižuje riziko pádu. Pro běžnou OA, jež není komplikována instabilitou, však nejsou ortézy vhodné. Evidence o účinnosti nošení ortéz byla potvrzena i v Cochranské analýze (8).
Cvičení
Cvičení by mělo být předepsáno každému pacientu nezávisle na věku. Cvičení u OA lze rozdělit na dvě skupiny: a) aerobní cvičení, typu fitness, které zvyšuje celkovou aktivitu, zlepšuje celkový pocit zdraví, zlepšuje delta fázi spánku a příznivě ovlivňuje další onemocnění, často provázející artrózu, jako je obezita, hypertenze, diabetes a chronické srdeční selhání; b) lokální neuromuskulární cvičení, zaměřené na udržení nebo zvýšení rozsahu pohybů v kloubech a posílení důležitých svalových partií jako jsou quadricepsy u gonartrózy nebo gluteální svaly u koxartrózy.
Byla provedena řada randomizovaných, kontrolovaných studií, které prokazovaly účinnost cvičení u koxartrózy a gonartrózy (9). Nová metaanalýza potvrdila i účinnost cvičení u koxartrózy. Velikost účinku cvičení lze hodnotit jako střední na úlevu od bolesti (ES= 0,38) (10). Jiná analýza ukázala, že cvičení ve vodě bylo rovněž účinné (velikost účinku na bolest ES= 0,19, a na zlepšení funkce ES =0,26) (11). Ekonomická analýza ukázala rozdíly podle typu sledovaného cvičebního programu a jednotlivé země. Nepochybně je však cvičení z hlediska nákladovosti výhodné. Optimální může být kombinace domácího cvičení a pravidelného skupinového cvičení pod vedením zkušeného fyzioterapeuta. Analýzy neukázaly, že by cvičení ve vodě muselo být výhodnější (12).
Fyzikální léčba u osteoartrózy
Randomizovaných, kontrolovaných studií fyzikální léčby u OA je poměrně málo. Souvisí to s obtížností provádění dvojslepých studií, především pak s aplikací placeba a malou atraktivitou těchto studií. Nicméně určitá vědecká evidence je dostupná a většina publikovaných doporučení (7/10) prostředky fyzikální léčby uvádí (12).
Termoterapie. V léčbě symptomů OA se používají jak léčba teplem, tak léčba chladem (kryoterapie). Paradoxně mohou fungovat oba typy léčby. Obecným pravidlem, které ale nemusí být univerzálně účinné u jednotlivých pacientů, je, že kryoterapie se užívá u akutních bolestí spojených s exacerbací a zánětem, terapie teplem spíše u chronických stavů. Teplo může být aplikováno celou řadou metodik jako je diatermie, aplikace tepelných sáčků či zábalů nebo pomocí parafinu. Kryoterapie se provádí pomocí speciálních zmrazovacích sáčků, či aplikací chladného vzduchu ze speciálního přístroje. Jediná publikovaná metaanalýza analyzovala efekt masáží kryosáčky (13) a další efekt diatermie (14). Aplikace kryosáčků měla určitý vliv na snížení bolesti a zlepšení síly quadricepsů, ale rozdíly nebyly statisticky významné. Studie s aplikací diatermie byla negativní (14). Aplikaci termoterapie je nutné chápat jako levnou a bezpečnou součást analgetické terapie (či samoterapie) OA s ne zcela prokázaným efektem.
Elektromagnetická léčba. Pohled na elektrickou magnetoterapii (EM) je kontraverzní. Cochranská metaanalýza publikovaná v roce 2002 sice EM doporučila, nicméně následná metaanalýza provedená OARSI byla negativní a v Doporučeních OARSI pro léčbu OA kolenních a kyčelních kloubů EM doporučena nebyla (6). Po ukončení prací na této publikaci byla publikována nová metaanalýza, která zahrnula i některé nové studie. Kumulativní data ukázala, že vliv EM na funkci byl malý (ES = 0,33, 95 % CI 0,07; 0,59) a nebyl prokázán žádný vliv na snížení bolesti (ES = 0,16, 95 % CI 0,08; 0,39) (15). Lze tedy uzavřít, že účinnost EM u gonartrózy a koxartrózy je nutné považovat za neprůkaznou.
Akupunktura. Akupunktura je stará léčba, která má potenciální mnohočetný mechanismus účinku, mezi nějž patří také uvolnění endogenních opioidů. Je široce provozována mnohými zdravotnickými zařízeními, ale na druhé straně je i předmětem širokého výzkumu. Problémem u akupunktury je objektivní průkaz její účinnosti, protože prakticky není možná aplikace placeba. Tzv. stínové placebo (sham placebo – aplikace jehliček do neaktivních bodů) není zcela jen placebo. Není proto ani překvapivé, že výsledky akupunktury u OA jsou velmi heterogenní. V metaanalýze byla akupunktura účinnější než placebo (ES = 0,58, 95 % CI 0,38; 0,78) pro úlevu od bolesti. Nicméně při použití sham placeba efekt již klesal (ES = 0,35, 95 % CI 0,15; 0,55). Velikost účinku také klesala s časem a po 6 měsících byla již malá (ES = 0,13, 95 % CI 0,01; 0,24) (16). Podobný efekt byl i na funkci. Farmakoekonomika akupunktury také nebyla příznivá, když cena 1 QALY byla přes 30 000 EURO (6). Lze uzavřít, že akupunktura není příliš vhodná pro chronickou léčbu symptomů u OA a její použití by mělo být limitováno na určité krátké a výrazně bolestivé epizody.
Transkutánní nervová stimulace (TENS). TENS produkuje pulzní vlny pomocí elektrod umístěných na kůži. Mechanismem účinku je selektivní elektrická stimulace periferních senzorických vláken, které potom vyvolává inhibici nociceptivní nervové transmise. Pokud ji používají pacienti sami, měli by být písemně instruováni, jak nastavit stimulační intenzitu a jak umístit elektrody. TENS je doporučována v 8 z 10 publikovaných Doporučení (6). Nověji provedená metaanalýza prokázala účinnost celkem u 425 pacientů (17). Efekt přetrvával 2–4 týdny. Procedury byly velmi bezpečné. TENS lze doporučit k symptomatické léčbě bolesti u gonartrózy.
Farmakologická léčba osteoartrózy
Paracetamol
Paracetamol (acetaminofen) je analgetikum a antipyretikum s centrálním účinkem. Mechanismus jeho účinku není zcela jasný, přičemž často se uvádí jako možný mechanismus účinku inhibice cyklooxygenázy 3. Je důležité, že paracetamol vykazuje velmi slabou nebo téměř žádnou inhibici periferních prostaglandinů, což znamená absenci gastrointestinální, renální a kardiovaskulární toxicity, vyvolané deplecí prostaglandinů. Dále nemá lékové interakce, např. s warfarinem, což ho činí atraktivním pro velkou skupinu starších pacientů s OA, která musí tyto léky užívat.
Paracetamol je uváděn pozitivně ve všech publikovaných doporučeních (16) pro léčbu OA. Je doporučován jako lék první volby u mírné a střední bolesti a pokud má dostatečný efekt, tak i k dlouhodobé léčbě. Vychází se přitom z jeho velmi dobré bezpečnosti a snášenlivosti a nízké ceny. Nicméně v poslední době se objevují určité pochybnosti, co se týče účinnosti i bezpečnosti.
Účinnost paracetamolu byla u OA hodnocena v několika randomizovaných, kontrolovaných studiích a do doporučení OARSI byl paracetamol zahrnut po publikaci Cochranské analýzy (18) a dále metaanalýzy 10 randomizovaných studií v roce 2004, která analyzovala data 1712 pacientů. Tato analýza potvrdila statisticky významný efekt paracetamolu, ale velikost účinku byla malá (ES = 0,21, 95 % CI 0,02; 0,4). Později publikovaná Cochranská analýza zahrnula 15 studií a data od 5969 pacientů (19). Výsledek zůstal nadále signifikantní, ale velikost účinku se zmenšila (ES = 0,13, 95 % CI 0,04; 0,22) a pokud se analyzovaly pouze vysoce kvalitní studie, pak již efekt paracetamolu proti placebu nebyl statisticky signifikantní. Poslední analýzy také neukázaly žádný vliv paracetamolu na zlepšení funkce a ztuhlosti u OA. Srovnávací studie proti nesteroidním antirevmatikům (NSA) ukazují menší účinnost paracetamolu než NSA (viz dále).
Paracetamol byl vždy vnímán jako velmi bezpečný lék, který má ale relativně úzká pásma účinnosti a toxicity, takže jen několikanásobné zvýšení maximální dávky vede k závažným projevům hepatorenální toxicity. Paracetamol je také jedním z nejčastěji používaných léků při pokusech o sebevraždu. Jeho bezpečnost platí pro dávky do 4 g denně. Nová data však ukázala, že paracetamol ve vyšších dávkách může vyvolávat gastrointestinální nežádoucí účinky. Populační studie v kohortě 644 183 pacientů zjistila, že léčba paracetamolem v dávkách vyšších než 3 g denně zvyšuje riziko hospitalizace z důvodu perforace, ulcerace a krvácení do trávicího traktu (tzv. PUB) než dávky paracetamolu nižší než 3 g denně s relativním rizikem poškození HR 1,2 (1,03; 1,4) (20).
Paracetamol je doporučován v doporučení OARSI v dávkách do 4 g denně (6). V doporučeních EULAR je rovněž v dávkách do 4 g denně doporučován jako lék první volby v léčbě bolesti u OA (5). Nová evidence o toxicitě paracetamolu byla získána později po publikaci. FDA na tento fakt reagovala doporučením, aby maximální denní dávka paracetamolu byla nižší než 3 g denně a jednotlivá maximální dávka paracetamolu ve volně prodejných preparátech byla 650 mg (21). S uvedeným názorem se lze ztotožnit.
Nesteroidní antirevmatika
Nesteroidní antirevmatika (NSA) se u artrózy používají buď systémově, nebo lokálně ve formě mastí, gelů, sprejů a náplastí.
Systémově podávaná NSA
Perorálně podávaná nesteroidní antirevmatika jsou stále zdaleka nejvíce používaným lékem v léčbě bolesti u OA a do určité míry lze říci, že někdy až zbytečně. Zatímco u krátkodobé léčby NSA u OA se zdá být poměr přínosu a rizika příznivý, při dlouhodobě léčbě toto není jasné.
Byla provedena celá řada randomizovaných, placebem kontrolovaných studií s NSA u OA v lokalizaci kolenních, kyčelních a ručních kloubů. NSA jsou doporučována ve všech 15 publikovaných doporučeních. Evidence o účinnosti byla podána při metaanalýze 23 studií, jež zahrnovala data více než 10 000 pacientů s OA kolenního kloubu (22). Velikost účinku NSA na redukci bolesti byla 0,32 (95% CI 0,24; 0,39) což lze hodnotit jako efekt střední až malý. V nově publikované metaanalýze 27 randomizovaných, placebem kontrolovaných studií z roku 2007 byla velikost účinku ještě menší a to ES = 0,29 (95 % CI 0,22; 0,35) (23). Stále to však bylo dvakrát více než pro paracetamol (ES = 0,14). Při analýze dalších studií bylo zjištěno, že rozdíl mezi účinností NSA a placeba je v průměru 10 mm na VAS, což nemusí být více než tzv. minimální, klinicky důležitý rozdíl, který se u OA pohybuje mezi 10–16 mm.
Na začátku 90. let minulého století byly provedeny některé studie, které prokazovaly stejnou účinnost paracetamolu a NSA např. ibuprofenu. Novější studie však většinou potvrzují vyšší účinnost NSA. Byla provedena i studie typu vědeckého přehledu, která vyhodnocovala srovnávací studie NSA vs. paracetamol, která rovněž ukázala, že účinnost NSA je vyšší než účinnost paracetamolu (ES = 0,20, 95 % CI 0,10; 0,30). Počet pacientů s pozitivní odpovědí na analgetickou léčbu je u NSA vyšší a preference pacientů vyznívají rovněž pro NSA (24).
Existuje velké množství dokladů o tom, že NSA vyvolávají více GIT nežádoucích účinků než paracetamol, což potvrdila i publikovaná Cochranská metaanalýza (6). Závažnější je ale, že NSA vyvolávají více závažných gastrointestinálních nežádoucích účinků, jako jsou perforace, ulcerace a krvácení (tzv. PUB). Riziko PUB se zvyšuje s věkem, dávkou NSA, délkou léčby a aplikací dalších léků jako jsou antikoagulancia, malé dávky aspirinu a glukokortikoidy (tab. 4). Metaanalýza 16 randomizovaných studií NSA proti placebu uvádí podíl rizik (odds ratio; OR) pro PUB 5,36 (95 % CI 1,79; 16,1) a ve 23 kohortových studiích s kontrolou pak OR 3,0 (25). O tom, že aplikace NSA je spojena s vyšším výskytem závažných komplikací svědčí i výsledky obrovské populační studie u starších pacientů v Kanadě (26). Relativní riziko hospitalizace bylo po NSA signifikantně vyšší po NSA oproti paracetamolu (1,63 vs. 2,55). Relativní riziko hospitalizace pro PUB bylo téměř dvakrát tak vysoké po neselektivních NSA než po COX-2 selektivním léku celekoxibu (RR=2,18, 95 % CI 1,82; 2,61). Další publikovaná metaanalýza ukázala, že aplikace celekoxibu u vysoce rizikových osob byla sdružena s 9 % rizikem opakování krvácení, toto riziko mohlo být eliminováno současnou aplikací inhibitorů protonové pumpy (27). Tento nález byl podpořen další retrospektivní analýzou, která ukázala snížení rizika přijetí k hospitalizaci pro PUB po přidání inhibitorů protonové pumpy k neselektivním i selektivním NSA (28). Britská farmakoekonomická metaanalýza prokázala efektivnost současné preskripce inhibitorů PPI u všech typů NSA (29). Lze tedy doporučit, aby každý pacient byl vyhodnocen z hlediska rizika NSA indukované gastropatie a v případě výskytu rizikových faktorů by měl být použit efektivní gastroprotektivní princip tzn. buď koxib, nebo současně aplikovaný inhibitor PPI. U nemocných s nejvyšším stupněm rizika (např. u pacienta s nedávným gastrointestinálním krvácením), je nejúčinnější prevencí současná aplikace PPI inhibitoru s COX-2 selektivními léky. Riziko samozřejmě snižuje i aplikace nižších dávek po co nejkratší dobu.
Tab. 4. Rizikové faktory pro NSA gastropatii. 
Kardiovaskulární (KV) bezpečnost NSA je stále diskutovaným problémem. V roce 2004 byl stažen z distribuce COX-2 selektivní lék rofekoxib, protože byl v randomizované studii k chemoprevenci adenomu zaznamenán po aplikaci rofekoxibu vyšší výskyt infarktů myokardu a cévních mozkových příhod. Od té doby byla provedena celá řada randomizovaných studií a systémových přehledů o kardiovaskulární bezpečnosti COX-2 selektivních i neselektivních léků. Zatímco zvýšený výskyt KV nežádoucích účinků byl u rofekoxibu potvrzen, u celekoxibu byly výsledky nekonzistentní (6). Velká metaanalýza a systematický přehled publikovaný v roce 2006 nalezl výskyt KV příhod u koxibů 1 %, u neselektivních NSA pak 0,9 % (30). Ve skupině neselektivních NSA bylo nalezeno zvýšené riziko u ibuprofenu a diklofenaku, nikoliv však u naproxenu. Nicméně v současné době stále platí doporučení EMA, které říká, že koxiby jsou kontraindikovány u nemocných s anamnézou infarktu myokardu a cévní mozkové příhody a výrazné opatrnosti je třeba při podáváním koxibů nemocným s rizikovými faktory ICHS (31).
Dalším problémem dlouhodobé aplikace NSA může být výskyt muskuloskeletálních nežádoucích účinků. Diskutoval se efekt tzv. analgetického kloubu. Zmenšením bolesti je pacientovi umožněna větší fyzická aktivita, která může vést k rychlejší destrukci kloubů. Tento efekt nebyl nikdy jednoznačně prokázán, nicméně je vhodné doporučit pacientům, aby klouby nepřetěžovali např. při sportu pod clonou NSA. Dalším diskutovaným efektem byl vliv NSA na metabolismus chondrocytů a to ve smyslu snížení syntézy proteoglykanů. Toto je prokazatelné na tkáňových kulturách in vitro, ale při užití vyšších koncentrací NSA než v běžné humánní medicíně. Byla provedena jedna studie, která ukazovala rychlejší progresi OA po indometacinu než po tiaprofenu. Nicméně jiné studie rozdíly mezi NSA neukazovaly. Klinická relevance není tedy jasná.
Lokální NSA
Lokálně aplikovaná NSA jsou doporučována v 7 z 9 publikovaných „doporučení“ pro léčbu kolenních kloubů. V roce 2004 byla publikována metaanalýza 13 randomizovaných studií u OA kolenních kloubů a ručních kloubů, která ukázala statisticky významnou účinnost lokálně aplikovaných NSA oproti placebu (32). Dále byly publikovány 3 nové studie, které byly zahrnuty do nové metaanalýzy (33). Tato ukázala střední velikost účinku ES=0,44 (95 % CI 0,27; 0,62). Lokálně aplikovaná NSA byla méně účinná než systémově podávaná v prvním týdnu léčby, pak se již efekt vyrovnával. Mezi studiemi však jsou velké rozdíly. Dá se také říci, že starší studie ukazovaly stejnou účinnost lokálních i systémově podávaných NSA, novější studie ukazují vyšší účinnost systémově podávaných NSA (6). Nebyla také provedena studie, která by prokazovala dlouhodobou účinnost lokálně aplikovaných NSA. Lokálně aplikovaná NSA jsou však velmi bezpečná a výskyt nežádoucích účinků není vyšší než po placebu. Nebylo prokázáno, že by lokálně podávaná NSA způsobovala jakoukoliv iritaci trávicího traktu, což je logické vzhledem k minimálním plazmatickým hladinám, které jsou po jejich aplikaci dosahovány. Pronikání lokálních NSA přes kožní bariéru do měkkých tkání a přímo kloubu je omezené. Proto lze jejich aplikaci doporučit jen v kloubech uložených těsněji pod kůží, jako jsou kolenní a především ruční klouby, nikoliv však u koxartrózy nebo spondylózy.
NSA jsou účinná u osteoartrózy, ale zároveň přinášejí zejména pro starší populaci s OA nemalá rizika. NSA by měla být proto aplikována až jako druhý lék bolesti při nedostatečném účinku paracetamolu. V případě přítomného zánětu a silnější bolesti mohou být aplikována i jako lék první. Aplikace NSA by měla být omezena časově na doby vzplanutí tzn. řádově 2–3 týdny. Při delší aplikaci by měla být NSA podávána striktně na principu „on demand“ tzn. jen když potřebuji (rozumí se při bolesti, nikoliv ve fixních intervalech). Při každé aplikaci NSA by měla být zvažována rizika nežádoucích účinků a to především gastrointestinálních a kardiovaskulárních. V případě rizika gastrointestinálních nežádoucích účinků by měl být použit efektivní gastroprotektivní princip, tzn. buď koxiby, nebo kombinace s inhibitory protonové pumpy. Kombinaci koxibu a inhibitoru protonové pumpy lze doporučit u pacientů s vysokým gastrointestinálním rizikem. V řadě případů se lze vyhnout systémové aplikaci NSA podáváním lokálním, případně v kombinaci s fyzikální léčbou.
Lokální léčba kapsaicinem
Lokální léčba kapsaicinem je doporučována v 8 z 9 publikovaných doporučení (6). Lokálně aplikovaný kapsaicin v krému obsahuje lipofilní extrakt z chilli papriček. Tento aktivuje a senzitizuje periferní c-nociceptory. Paradoxně vyvolává pálení kůže v místě aplikace, ale ve studiích oproti placebu byl v léčbě bolesti u OA účinnější. Do metaanalýzy byla zahrnuta jedna dvojslepá studie v indikaci gonartrózy a dvě studie u OA ručních kloubů (34). Průměrné snížení bolesti dosahovalo 33 %. O účinnosti lokálně aplikovaného kapsaicinu obecně u bolestivých stavů svědčí i další metaanalýza. Léčba lokálně aplikovaným kapsaicinem je bezpečná, ale část pacientů ji pro pocity pálení kůže a erytém netoleruje.
Opioidy
Opioidy jsou doporučovány k léčbě bolesti u OA prakticky ve všech publikovaných doporučeních, ale randomizovaných, kontrolovaných studií u OA bylo publikováno relativně málo a vesměs byly krátkodobé. Metaanalýza 18 randomizovaných, placebem kontrolovaných studií u 3244 pacientů ukázala střední, až velký analgetický účinek (ES= 0,78, 95 % CI 0,59; 0,98), ale pouze malý efekt na zlepšení funkce (ES = 0,31, 95 % CI 0,24; 0,39) (35). Mezi studiemi však byly velké rozdíly. Příznivý účinek opioidů je však snižován výskytem nežádoucích účinků jako je nauzea (30 %), zácpa (23 %), závratě (20 %), somnolence (18 %), a zvracení (13 %) (6). Celkem 25 % pacientů na opioidech nedokončilo studie pro nežádoucí účinky oproti 7 % na placebu. Počet pacientů, kteří nedokončili studie, byl vyšší ve skupině silných opioidů (morfin sulfát, fentanyl, oxycodon, oxymorfon) než u opioidů slabých (tramadol, tramadol/paracetamol, propoxyfen) – 31 % vs. 19 %. Vznik závislosti a nutnost zvyšování dávek je dalším limitujícím faktorem dlouhodobé léčby. Nicméně aplikace opioidů např. v USA prudce stoupla po stažení rofekoxibu a zjištění dalších toxických účinků NSA.
Aplikaci slabých opioidů (tramadol, kodein, dihydrokodein) je možné doporučit po selhání paracetamolu a lokálních NSA jako další krok, alternativní k použití NSA. Vhodným typem pacientů jsou zejména starší nemocní s rizikovými faktory gastrointestinálními a kardiovaskulárními pro aplikaci NSA. Aplikaci silných opioidů (fentanyl, oxymorfon, tapentadol, morfin) lze doporučit pouze u velmi silných bolestí k časově omezené aplikaci, jakou je např. čekání na endoprotézu kloubu (35).
Intraartikulární aplikace glukokortikoidů
Intraartikulární aplikace (i.a.) glukokortikoidů se používá již více než 50 let a je uváděna pozitivně v 11 ze 13 publikovaných doporučení (6). Účinnost i.a. glukokortikoidů při léčbě gonartrózy byla potvrzena v Cochranské metaanalýze, ve které bylo analyzováno celkem 13 randomizovaných klinických studií (36). Efekt léčby je velmi rychlý a dobrý; po 2 a 3 týdnech je velikost účinku 0,72 (95% CI 0,42; 1,02). Po 4 týdnech však již analgetický efekt není průkazný. Rovněž nebyl prokázán vliv i. a. glukokortikoidů na zlepšení funkce. Některé studie prokazovaly lepší efekt i. a. glukokortikoidů u nemocných s přítomným zánětem (výpotkem), ale toto nebylo potvrzeno v dalších studiích. Nelze tedy považovat přítomnost výpotku za jednoznačně prediktivní faktor příznivé odpovědi na léčbu. Jestliže je efekt krátkodobý, jaká je evidence o účinnosti opakovaných i. a. injekcí glukokortikoidů? Ve dvouleté studii v Kanadě byla i. a. aplikace glukokortikoidů nebo placeba prováděna v 3měsíčních intervalech po dobu 2 let (37). Po jednom roce byla lepší úleva od bolesti ve skupině léčené opakovaně glukokortikoidy oproti placebu, po 2 letech léčby však již nebyl žádný efekt léčby glukokortikoidy oproti placebu průkazný. Celkově lze tedy říci, že efekt léčby i. a. glukokortikoidy lze považovat u gonartrózy za prokázaný, ale krátkodobý v délce trvání 1–4 týdny. Většina „doporučení“ limituje vhodný počet aplikací na maximálně 4 ročně.
Podstatně méně dokladů o účinnosti i. a. aplikace glukokortikoidů je u koxartrózy. V podstatě byly provedeny 2 randomizované studie, z nichž jedna byla zcela negativní a druhá prokázala krátkodobý symptomatický účinek (6). Určitá evidence svědčí o tom, že cíleně prováděné i. a. opichy pod fluoroskopickou či ultrazvukovou kontrolou u koxartrózy mají lepší výsledky než necíleně prováděné aplikace. Byly provedeny i pozitivní otevřené studie s i. a aplikací u bolestivé rhizartrózy.
Jaká jsou rizika i. a. aplikace? Asi nejzávažnějším je riziko vzniku septického kloubu. Rizika lze minimalizovat správnou technikou a přísnou asepsí. Data ze studií i vlastní zkušenosti ukazují na velmi malý výskyt septických komplikací i běžných nežádoucích účinků. Někdy lze pozorovat brzy po i. a. aplikaci zhoršení bolesti, tzv. postinjekční exacerbaci. Další nežádoucí reakcí může být vznik přechodné krystalové artritidy. Někdy lze pozorovat a to především u žen zarudnutí v obličeji trvající 24–72 hodin. Protože dochází k pronikání glukokortikoidu do systémové cirkulace, je někdy možné pozorovat i zhoršení diabetu.
Intraartikulární aplikaci glukokortikoidů lze doporučit při exacerbaci bolesti zvláště spojené se zánětem. Doporučovanou lokalizací je gonartróza a rhizartróza. Aplikace do jednoho kloubu by se měly opakovat maximálně 4x do roka.
Pomalu působící léky u OA (SYSADOA)
Název SYSADOA (symptomatic slow acting drugs in osteoarthritis) byl navržen zhruba před 15 lety a měl charakterizovat skupinu léků požívaných při léčbě OA. Koncept SYSADOA se udržel dodnes, ale není všeobecně akceptován, např. v některých anglosaských zemích.
V názvu SYSADOA je obsaženo, že efekt těchto léků je symptomatický. Řada léků z této skupiny však byla zkoušena i v dlouhodobých studiích a výsledky některých ukazovaly i možné ovlivnění struktury (zpomalení rentgenové progrese) (viz dále). Většina SYSADOA působí na úrovni metabolismu chrupavky a proto jsou logickými kandidáty na strukturu modifikující efekt. Dále je v názvu obsaženo, že nástup účinku je pomalý. Většinou nastupuje v intervalu 2–4 týdnů, což je zcela odlišné od rychle působících léků jako jsou analgetika a NSA, která většinou působí v intervalu hodin. SYSADOA nepůsobí inhibicí syntézy prostaglandinů jako NSA a nemají tudíž bezprostřední protizánětlivý a analgetický účinek. Na druhé straně nemají SYSADOA nežádoucí účinky spojené s inhibicí syntézy prostaglandinů. SYSADOA tvoří heterogenní skupinu léků, které jsou uvedeny v tabulce 5. Některé substance ze skupiny SYSADOA jako je glukosamin (GS) a chondroitin sulfát (CS) jsou distribuovány v řadě tzv. potravinových doplňků (nutritiv). Protože naprostá většina z nich nebyla zkoušena v randomizovaných studiích, mnoho není známo o kvalitě příslušeného preparátu a biologické dostupnosti. Následující doporučení jsou určena pro substance zkoušené a deklarované jako léky nebo jako léčebné prostředky, u kterých byla publikována kvalitní, dvojslepá, randomizovaná studie a tudíž průkaz odpovídá pravidlům medicíny založené na důkazech.
Tab. 5. SYSADOA (Symptomaticky pomalu působící léky). 
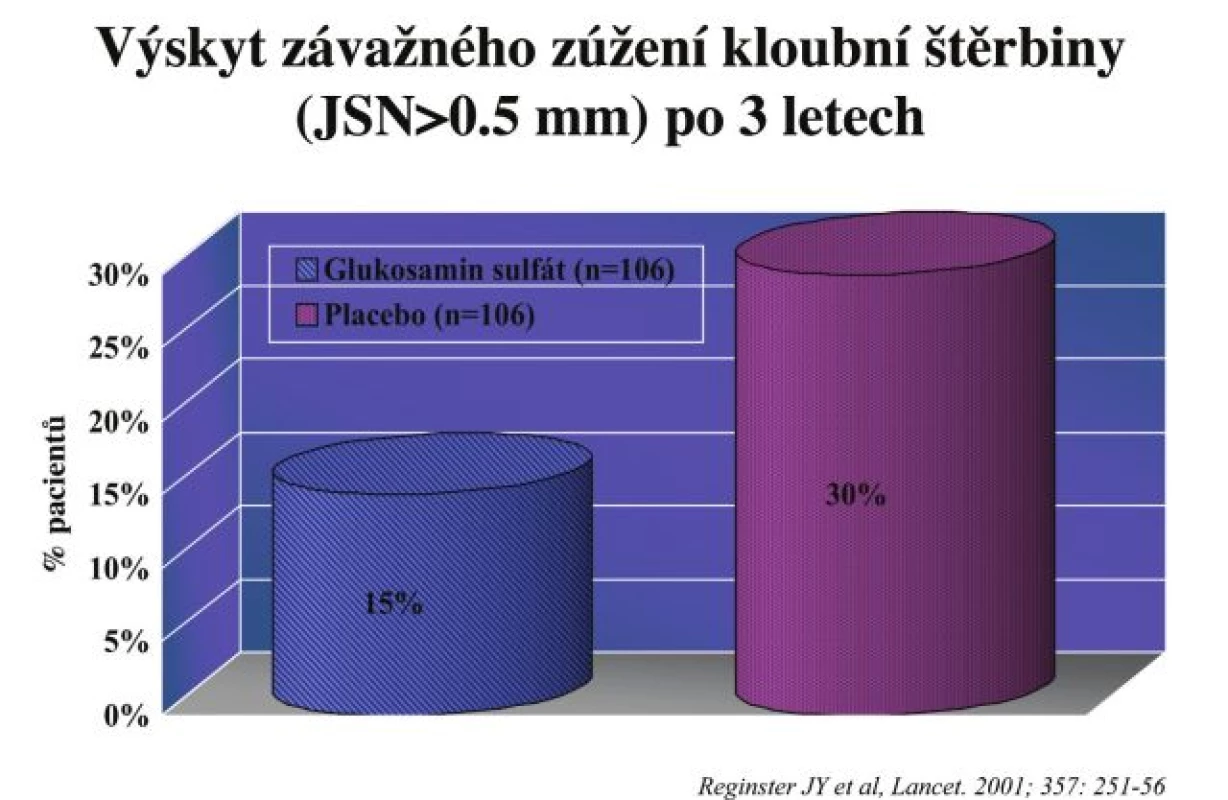
Glukosamin. Glukosamin (GS) je aminocukr, který je normální součástí proteoglykanů kloubní chrupavky. Po zevním požití je GS parciálně natráven a část GS se dostává do kloubu (37). Zde ovlivňuje činnost chondrocytů, když stimuluje některé anabolické pochody (např. syntézu proteoglykanů, kolagenu, a TIMP) a inhibuje některé katabolické funkce jako např. sekreci degradačních proteináz jako jsou metaloproteinázy a želatinázy. Glukosamin je uváděn v 6 z 10 „doporučení“, včetně EULAR a OARSI (5, 6). Evidence o jeho symptomatické účinnosti pochází především z metaanalýzy v rámci Cochranské knihovny (38). V této metaanalýze bylo hodnoceno 20 studií a celkem 2570 pacientů, přičemž zlepšení bolesti bylo o 28 % (ES = 0,61, 95 % CI 0,28; 0,95) a zlepšení funkce o 21 % při použití Lequesnova indexu. Ve většině studií bylo potvrzeno, že efekt je oproti NSA mírně opožděný, ale vyrovnává se po 24 týdnech a pak je již rovnocenný. Naopak analgetický efekt přetrvává 2–3 měsíce po skončení léčby (tzv. carry over efekt). Nicméně byla publikována i řada negativních studií. Nejednoznačné výsledky přinesla i velká, nezávislá, multicentrická studie v USA pod názvem GAIT (39). V této studii nebyl GS účinnější při ovlivnění bolesti než placebo. Nicméně při subanalýze skupiny pacientů se silnější bolestí byl GS účinný, ale ještě více byla účinná kombinace GS a chondroitin sulfátu. V této studii byl použit glukosamin hydrochlorid. Naopak glukosamin sulfát byl aplikován ve studii GUIDE, kde byl účinnější v ovlivnění bolesti než kontrolní skupina léčená paracetamolem (40). Nejnovější metaanalýza účinnost GS nepotvrdila, ale k této práci je řada metodologických výhrad (41). Byly provedeny i dvě dlouhodobé, tříleté, randomizované, placebem kontrolované studie s aplikací 1500 mg krystalického glukosamin sulfátu oproti placebu u gonartrózy (42, 43). V obou byla prokázána účinnost GS při ovlivnění bolesti a funkce. V obou studiích byla hodnocena i rentgenová progrese gonartrózy pomocí standardizovaných postupů. Obě studie ukázaly menší zúžení kloubní štěrbiny ve skupině léčené GS oproti placebu. Proporce pacientů s klinicky významnou progresí (zúžení více než 0,5 mm) bylo vyšší ve skupině léčené placebem oproti skupině léčené GS (obr. 2). Všechny analýzy ukázaly, že GS je lék velmi bezpečný a závažné nežádoucí účinky se prakticky nevyskytují. Podezření, že aplikace GS může zhoršovat nebo vyvolávat diabetes mellitus se nepotvrdilo.
Celkově lze říci, že přestože řada studií ukazuje konfliktní výsledky, mírně převažuje evidence o účinnosti GS u bolestivé gonartrózy. Je doporučeno používat GS v dávce 1500 mg denně. Otázkou je i způsob podávání. Původní algoritmus doporučoval dvě 3měsíční série do roka s pauzami. Nicméně strukturu modifikujícího efektu bylo dosaženo při podávání kontinuálním. Indikováni jsou pacienti s bolestivou gonartrózou, kde GS má být součástí komplexní léčby.
Diacerein. Diacerein je antrachinonový derivát, který inhibuje interleukin IL 1β, který je hlavním prokatabolickým cytokinem u OA (44). Kromě toho diacerein také stimuluje tvorbu některých chrupavkových růstových faktorů jako je TGFß a kolagenu. Mezi další farmakologické vlastnosti patří snížení leukocytární fagocytózy, migrace makrofágů a chemotaxe neutrofilů a snížení produkce volných kyslíkatých radikálů. Na zvířecích modelech OA diacerein signifikantně zmenšoval oproti placebu degradaci chrupavky (45).
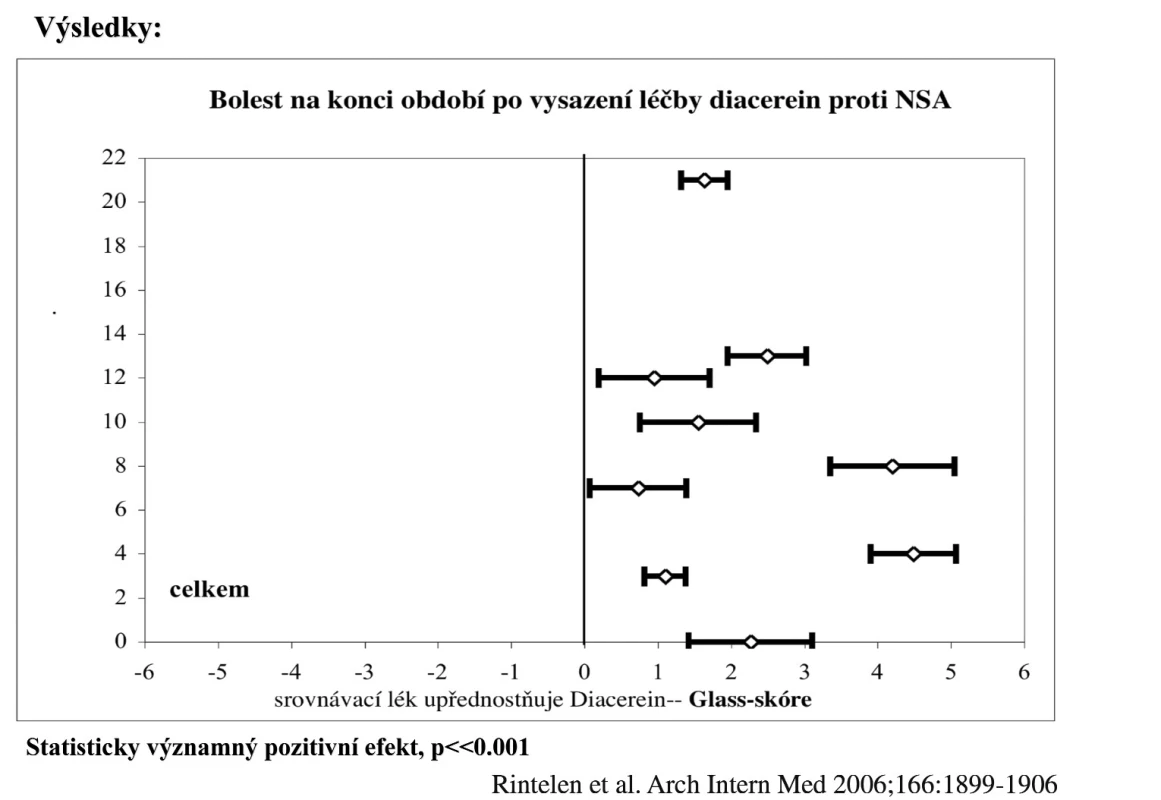
Symptomatická účinnost diacereinu byla testována v řadě dvojslepých, randomizovaných studií, ve kterých docházelo k signifikantnímu poklesu bolesti a zlepšení funkce (46). Při srovnávací studii s NSA byl nástup účinku diacereinu oproti NSA pomalejší, nicméně po 6–8 týdnech se již vyrovnával. Po vysazení léčby navíc tento analgetický efekt přetrvával po diacereinu ještě 2–3 měsíce, zatímco po vysazení NSA se pacienti brzy zhoršili. Ve studii s bolestivou gonartrózou byl podáván diacerein v dávce 100 mg denně nebo placebo po dobu tří měsíců, dále byli všichni pacienti léčeni placebem po dobu 3 měsíců. Primárním cílem bylo ovlivnění bolesti v 5 měsících, tedy 2 měsíce po vysazení léčby diacereinem. Byla prokázána výrazná, signifikantní superiorita oproti placebu a tak potvrzen tzv. carry over efekt, tzn. přetrvávání efektu i po vysazení léčby (47). Tento typ efektu je pro celou skupinu SYSADOA typický. Byla publikována metaanalýza 19 randomizovaných, dvojslepých studií s diacereinem, která prokázala účinnost diacereinu oproti placebu během podávání léčby (Glass skóre 1,5, 95 % CI 0,80; 2,20), přičemž diacerein a NSA byly stejně účinné. Analgetický účinek diacereinu byl lepší následující tři měsíce po vysazení léčby než po NSA (Glass skóre 2,06, 95 % CI 0,66; 3,46) (48) (obr. 3). Evidence o symptomatickém účinku diacereinu byla získána i v Cochranské analýze (49). Diacerein byl úspěšně zkoušen v lokalizacích osteoartrózy kolenních kloubů a kyčelních kloubů. V indikaci drobných kloubů ruky byly provedeny pouze menší otevřené studie. Kromě symptomatického účinku byl sledován i potenciální strukturu modifikující efekt. Byla provedena jedna tříletá studie u nemocných s koxartrózou, kteří dostávali po dobu tří let buď diacerein, nebo placebo. Strukturální progrese na kyčlích byla hodnocena měřením šířky kloubní štěrbiny pomocí lupových brýlí metodou popsanou Lequesnem. Ve skupině léčené diacereinem docházelo ke klinicky relevantní progresi v 47 % oproti 62 % v placebové skupině (p = 0,007) (50). K potvrzení potenciálního strukturu modifikujícího účinku by však bylo nutné provést další studie i se zavedením modernějších zobrazovacích technik.
Diacerein lze považovat za velmi bezpečný lék, protože závažné nežádoucí účinky se prakticky nevyskytují. Z běžných nežádoucích účinků jsou nejčastější řidší stolice či průjmy, které se v začátku léčby mohou vyskytovat až u 25 % pacientů. K přerušení léčby však vedou jen v malém počtu případů. Jejich výskyt lze snížit počátečním podáváním pouze 50 mg diacereinu. Počet nežádoucích účinků po diacereinu je numericky stejný jako po NSA, jsou však méně závažné. Diacerein neinhibuje syntézu prostaglandinů a tudíž nevyvolává nežádoucí účinky spojené s jejich deplecí v místech jejich fyziologického působení.
Výtažek z avokáda a sóji (ASU). Výtažek z avokáda a sóji obsahuje frakci těchto olejů, ze které po hydrolýze nevzniká mýdlo. Výsledky preklinických studií ukázaly, že ASU je schopné inhibovat IL-1 a stimulovat syntézu kolagenu v kloubních tkáňových kulturách (51). ASU také zpomaloval degenerativní změny na zvířecích modelech OA (52). Další práce také prokazují schopnost ASU stimulovat expresi TGF-β na kulturách chondrocytů. ASU také redukuje produkci stromelyzinu, IL-6, prostaglandinů (IL-8 a PGE2) (53).
Symptomatická účinnost ASU u OA kolenních a kyčelních kloubů byla zkoumána v šestiměsíční dvojslepé studii oproti placebu. Poklesu bolesti o 50 % bylo dosaženo u 39 % pacientů léčených ASU oproti 18 % po placebu (p = 0,001) (54). Do studie s bolestivou gonartrózou bylo zařazeno 260 pacientů, kteří užívali denně po dobu 3 měsíců buď 300, nebo 600 mg ASU nebo placebo. Primárním cílem bylo snížení analgetické medikace mezi dny 30–90, přičemž jako kritérium bylo použito redukce spotřeby analgetik nejméně o 50 %. Ve skupině léčené ASU bylo tohoto kritéria dosaženo v 71 % oproti 36 % po placebu (55). Symptomatická účinnost ASU byla také hodnocena v metaanalýze, do které byly zařazeny 4 studie a celkem 664 pacientů. Metaanalýza potvrdila účinnost ASU při redukci bolesti, přičemž velikost efektu byla střední (ES = 0,39, 95 % CI 0,01; 0,76). Efekt na zlepšení funkce byl podobný (56). Lepší efekt byl u nemocných s gonartrózou než s koxartrózou. Vliv ASU na zpomalení rentgenové progrese OA byl hodnocen ve starší studii Lequesna, ale především ve studii ERADIAS, která byla prezentována na symposiu EULAR. Šlo o prospektivní, dvojslepou, tříletou studii, do které byli zařazováni pacienti s bolestivou koxartrózou (57). Jedna skupina byla léčena 300 mg ASU denně, druhá pak placebem. Primárním kritériem bylo hodnocení zužování šířky kloubní štěrbiny. Za klinicky významné se většinou považuje větší zúžení než 0,5 mm. Ve skupině léčené ASU toto kritérium splnilo 40 % nemocných, zatímco ve studii léčené placebem 50 % (p = 0,03). ASU je lék velmi bezpečný a závažnější nežádoucí účinky se prakticky nevyskytují.
Chondroitin sulfát. Chondroitin sulfát (CS) je důležitou součástí extracelulární matrix hyalinní kloubní chrupavky. U osteoartrózy dochází k destrukci chrupavky. Klíčovým krokem v degradačním procesu je ztráta proteoglykanů. Jednou z důležitých změn jsou i změny délky CS řetězců, polohy sulfátových částí (CS/4-CS/6) a změna antigenicity CS řetězců. Biologický důvod této změny není znám, ale signalizuje velký význam pro CS v procesu reparace chrupavky.
Chondroitin sulfát pro léčebné použití je získáván z bovinní trachei nebo prasečích či žraločích chrupavek. Biologická dostupnost se udává kolem 12 %. V experimentálních studiích je prokazatelný vysoký tropismus pro chrupavku. Mechanismus účinku CS byl zevrubně testován a nejdůležitější poznatky lze shrnout (58): antiapoptotický vliv na chondrocyty, zvýšení syntézy proteoglykanů, snížení aktivity proteináz, přímý protizánětlivý efekt, příznivé ovlivnění metabolismu subchondrální kosti zásahem do systému OPG/RANKL. Na experimentálním modelu OA u králíků zpomaloval CS vývoj degenerativních změn.
Symptomatický účinek CS byl testován v řadě studií, někdy i s kontroverzními výsledky. Do roku 2009 bylo publikováno celkem 5 metaanalýz účinnosti CS. Tyto metaanalýzy se staly podkladem pro získání evidence o účinnosti CS na základě které, byl CS zařazen v doporučeních EULAR (3), ale i OARSI (6). Např. v analýze 8 randomizovaných, placebem kontrolovaných studií byl nalezen středně velký efekt na snížení bolesti (ES = 0,52, 95 % CI 0,37; 0,67) (59). Novější metaanalýza ukázala efekt signifikantní, ale již menší (3). Velké interpretační diskuse vyvolala známá studie GAIT provedená v USA (60). Jednalo se o velkou, multicentrickou, randomizovanou a na průmyslu nezávislou studii u nemocných s bolestivou gonartrózou. CS nebyl v této studii účinnější než placebo, ovšem v subanalýze pacientů s iniciálně vyšší bolestí CS účinek placeba převyšoval. Ještě více pak byla u této podskupiny účinná kombinace GS plus CS. Je to jediná kvalitní studie, která potvrzuje účinnost této kombinace. Byla také provedena dvojslepá, randomizovaná a placebem kontrolovaná studie s aplikací CS u bolestivé artrózy drobných ručních kloubů. CS vedl k signifikantnímu zmenšení bolesti a zlepšení funkce hodnocené pomocí indexu Dreiserové (61). Signifikantní rozdíl byl patrný od 4 týdne léčby a přetrvával i po ukončení léčby. CS byl zkoušen v dlouhodobé léčbě gonartrózy s primárním cílem prokázat možný strukturální efekt ve smyslu zpomalení zúžení kloubní štěrbiny. Bylo provedeno celkem 5 randomizovaných, placebem kontrolovaných studií a jedna metaanalýza (62). V této analýze byly hodnoceny výsledky po dvouleté léčbě 800 mg CS oproti placebu. CS měl signifikantní vliv na zpomalení zužování kloubní štěrbiny, ale tento efekt byl malý (0,23 mm 95 % CI 0,09; 0,37). Zpomalení rentgenové progrese bylo zjištěno i ve studii STOPP publikované po uzávěru metaanalýzy (62).
Preparáty CS jsou velmi dobře snášeny a nežádoucí účinky nejsou častější než po placebu. V distribuci se používá chondroitin sulfát pod názvem Condrosulf. Prakticky všechna výše uvedená data byla získána ve studiích s tímto preparátem. CS je také obsažen v celé řadě nutričních doplňků, kde je dostupnost evidence menší.
Kyselina hyaluronová. Kyselina hyaluronová (KH) je důležitou součástí normální synoviální tekutiny a velmi přispívá k homeostáze kloubního prostředí. U osteoartrózy je v kloubu snížena jak koncentrace, tak molekulární hmotnost KH, čímž dochází ke snížení viskoelasticity synoviální tekutiny. Původní představou při uvažování o aplikaci externí KH do kloubů bylo, že bude docházet k úpravě reologických poměrů v kloubu a princip byl nazván viskosuplementace. Hyaluronan je však odstraňován z kloubu poměrně rychle lymfatickou cirkulací a degradován jaterními endoteliálními buňkami. Byly proto hledány další mechanismy účinku. Bylo zjištěno, že externí KH působí na receptory CD44 na řadě buněk i na další extracelulární molekuly. Externí KH stimuluje chondrocyty a synoviální buňky k sekreci endogenní KH, která přetrvává i po odstranění původně aplikované externí KH. Dále byly zjištěny protizánětlivé a přímé analgetické účinky (63). KH může omezovat interakci endogenních látek vyvolávajících bolest (jako je např. substance P) s jejich receptory a modulovat nitrobuněčné děje, jež jsou aktivovány neuropeptidy produkujícími bolest. Dále bylo prokázáno, že KH má protizánětlivé účinky dané jejich působením na prostaglandiny, superoxidové radikály a cytokiny. In vitro zvyšuje KH syntézu proteoglykanů extracelulární matrix a snižuje aktivitu degradačních enzymů. Externě podávaná KH má tedy nejen lokální bariérové funkce, nýbrž i vlastní farmakologickou účinnost. Toto ale zatím bylo prokázáno pouze pro KH o nižší molekulové hmotnosti a proto je také KH o nižší molekulové hmotnosti (viz dále) v řadě zemí registrována jako lék, na rozdíl od KH vyšší hmotnosti, které jsou registrovány jako medicínské pomůcky.
Kyselina hyaluronová je testována u OA přes 20 let a byly provedeny stovky kvalitnějších či méně kvalitních studií. Bylo publikováno 17 systematických přehledů a metaanalýz a většina z nich byla u gonartrózy. Největší z nich je Cochranská analýza, která zahrnula 76 studií (64). Byly analyzovány různé produkty KH s rozdílnou molekulovou hmotností, ale většina se podávala v týdenních intervalech po dobu 3–5 týdnů. Výsledky léčby byly hodnoceny v intervalech 1–4 týdny, 5–13 týdnů, 14–26 týdnů a 45–52 týdnů. Maximálního účinku bylo dosahováno po 5–13 týdnech, kdy dosahovalo snížení bolesti 28–54 % a zlepšení funkce 9–32 %. Při vyhodnocení studií oproti glukokortikoidům byl nástup účinku KH pomalejší; glukokortikoidy byly do 2. týdne účinnější, ve 4. týdnu se efekt vyrovnával a od 5. do 13. týdne byla KH účinnější než i. a. glukokortikoidy (65). Mezi jednotlivými studiemi však byly velké rozdíly, které mohly být zčásti způsobeny velikostí, návrhem studie, počtem pacientů a obecně kvalitou studií. Jednou z otázek je také optimální velikost molekulové hmotnosti KH. Obecně se dají preparáty HK rozdělit na preparáty s malou molekulovou hmotností jako např. Hyalgan (500 –730 kDa), střední molekulovou hmotností (např. Synovial 800–1200 kDa) a velkou molekulovou hmotností např. Synvisc (7 000 kDa). Preparáty s velkou molekulovou hmotností bývají také nazývány hylany a velké molekuly je docíleno chemickou modifikací, konkrétně spojením řetězců KH tzv. zkříženými vazbami (cross-links). Preparáty s větší molekulovou hmotností mají delší rezidenční čas v kloubu. Některé analýzy ukazovaly možný větší efekt preparátů s větší molekulou (66). Nicméně metaanalýza 13 studií neprokázala, že by byly hylany účinnější než KH s nižší molekulovou hmotností (67). Preparáty KH jsou obecně považovány za léky, jež ovlivňují především symptomy, tzn. bolest a funkci. Potenciálně by mohly ovlivňovat i strukturální změny, ale jednoznačný průkaz podán nebyl. Některé studie na experimentálních modelech a jedna klinická studie ukázala při hodnocení pomocí artroskopie určitý ochranný vliv na integritu kloubní chrupavky. Byla provedena jediná dlouhodobá, randomizovaná, placebem kontrolovaná studie v délce 12 měsíců, ve které byl srovnáván vliv 3 sérií KH oproti vlivu placeba na šířku kloubní štěrbiny. Ve skupině se zachovalejší šířkou štěrbiny na začátku léčby bylo zjištěno menší zúžení kloubní štěrbiny po aplikaci KH než po placebu (68).
Zatímco bylo nashromážděno hodně dat o účinnosti KH v indikaci OA kolenních kloubů, bylo provedeno jen několik malých a otevřených studií u OA kyčelních kloubů s heterogenními výsledky. Aplikaci KH do kyčelních kloubů nelze proto doporučit.
Z analýzy studií vyplývá, že preparáty KH jsou relativně dobře snášeny. Místní reakce se vyskytují ve 2–4 %, což se blíží výskytu po i. a. injekcích fyziologického roztoku. Zahrnují bolesti kloubu, otok nebo výpotek. Většinou jsou krátkodobé a rychle odeznívají. Riziko septického kloubu je při správné technice minimální. Některé studie ukazovaly vyšší výskyt akutních zánětlivých reakcí po hylanech, což by mohlo souviset s chemickou modifikací jejich struktury.
Jaká je tedy současná pozice preparátů kyseliny hyaluronové v posledních oficiálních Doporučeních? KH je uvedena v Doporučeních EULAR, Osteoarthritis Research Society (OARSI) a Americké koleje revmatologů (ACR). Není doporučována NICE.
ČRS doporučuje aplikaci kyseliny hyaluronové u pacientů s bolestivou OA kolenních kloubů, u kterých selhala nebo byla kontraindikována léčba nesteroidními antirevmatiky, což je formulace identická pro FDA.
KH se aplikuje v sériích 3–5 injekcí po týdenních intervalech, což platí pro preparáty s nízkou molekulovou hmotností. Vysokomolekulární preparáty se většinou aplikují ve 3 injekcích. Nověji bylo prokázáno, že i jedna injekce vysokomolekulárního preparátu KH je účinná (69).
Chirurgická léčba osteoartrózy
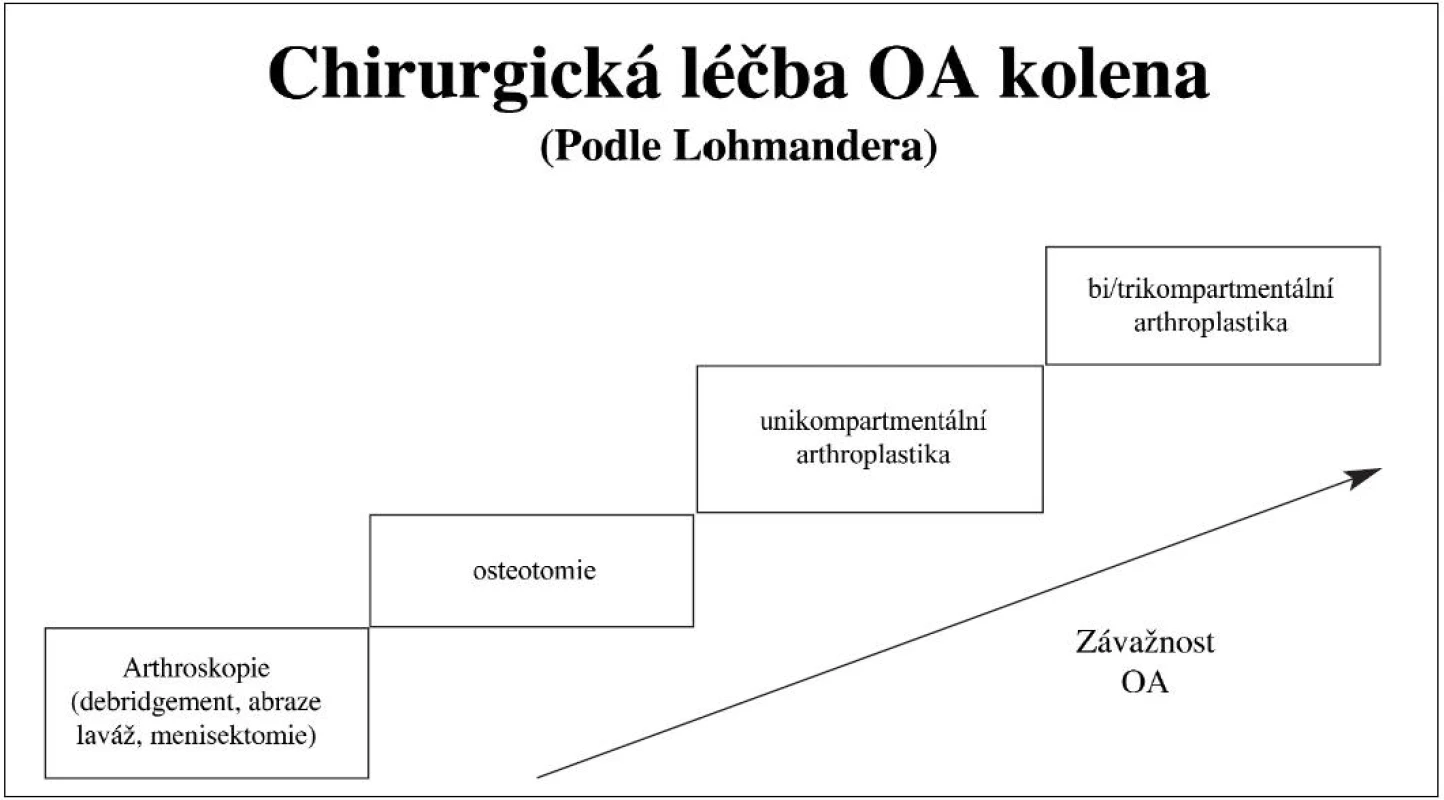
Chirurgická léčba OA zahrnuje několik metodik, které jsou uvedeny na obrázku 4.
Náhrada kloubů
U pacientů, u kterých selhává konzervativní léčba, se široce používá náhrada kolenního kloubu a kyčelního kloubu (TKA). Totální náhrady kolenních kloubů a totální náhrada kyčelních kloubů jsou uvedeny ve všech 14 publikovaných doporučeních. Evidence o účinnosti totální náhrada kolenních kloubů a totální náhrada kyčelních kloubů pochází z nekontrolovaných studií, velkých kohortových studií a registrů a z hodnocení expertů a pacientů. Po operaci dochází ke zmenšení bolesti, obnovuje se funkce a celkově se zlepšuje kvalita života. Např. metaanalýza 118 nekontrolovaných studií s totální náhrada kyčelních kloubů s celkem 77 375 pacienty s průměrným sledováním 10 let (2–20), že počet pacientů bez bolesti je v rozsahu 43–84 % (70). Kumulativní frekvence revizních operací byla 7 % pro kyčelní kloub a 10 % pro kolenní kloub (71). Úspěšnost operace může být ovlivněna vhodným výběrem pacientů, pečlivou předoperační přípravou, edukací pacienta a vhodnou předoperační rehabilitací. Velmi důležitá je i správně vedená anestesie, dobrá operační technika, výběr vhodného implantátu, včas a správně prováděná pooperační rehabilitace a podpora pacienta ze strany rodiny. Rehabilitace po operaci je rychlejší po totální náhradě kyčelních kloubů než po totální náhradě kolenních kloubů, ale většina pacientů docílí normálních aktivit během 12 týdnů. Až 95 % má dobrou funkci i ve druhé dekádě po operaci a většině je umožněna funkce bez bolesti do konce života. Nicméně přibližně jeden z pěti pacientů není s výsledkem operace spokojený a u malé skupiny není dosaženo téměř žádného zlepšení po operaci.
U pacientů, kteří mají u gonartrózy postižen jen jeden kloubní kompartment je možné implantovat unikompartmentální náhradu kolenního kloubu. Výsledky této operace byly v retrospektivní analýze rovnocenné TKA.
Jaký pacient je indikován k operaci? Jde o pacienta, který má silné bolesti, které jsou refrakterní na konzervativní léčbu. Zvláště klidové a noční bolesti jsou pro pacienta nepříjemné a snižují kvalitu jeho života natolik, že si operaci sám přeje. Při těchto stavech bývá přítomna i ranní ztuhlost a velké zhoršení funkce, které pacientovi brání v normálních životních aktivitách a velmi zhoršují nezávislost a obecně kvalitu života. Často musí užívat NSA a analgetika, která ho obtěžují a někdy i ohrožují nežádoucími účinky. Rozhodnutí o operaci by mělo optimálně vyplynout z rozhovoru mezi pacientem a jeho ošetřujícím revmatologem a ortopedem. Při indikaci k operaci je také vždy hodnocen morfologický stav, nejčastěji na rentgenovém snímku. Rentgenové známky OA by měly být patrné, nicméně jejich závažnost není rozhodující – důležitější je klinická závažnost symptomů pacienta.
Farmakoekonomické studie ukázaly, že TKA a TKA jsou vysoce výhodné a cena jednoho QUALY může být nižší, než při farmakologické léčbě (72).
Artroskopické výkony
Artroskopické výkony se u artrózy široce používají řadu desítek let. Patří mezi ně např. tzv. debridment, při kterém se rovněž provádí kloubní laváž, odstraňují se volná tělíska v kloubu, nestabilní a porušené části menisků či prominující osteofyty. Nicméně evidence o účinnosti artroskopických operací je u OA kontraverzní. Poslední metaanalýza artroskopického debridmentu u OA nižšího stupně byla negativní (73). Poslední doporučení EULAR artroskopickou laváž a debridment u gonartrózy nezahrnují (5). Nicméně artroskopická laváž by mohla být individuálně zvážena u pacientů s mechanickými blokádami kolenního kloubu nebo jasnou přítomností volných kloubních tělísek.
Osteotomie
Osteotomie pánve a femuru u dysplazií je používána s dobrými výsledky u mladých nemocných ještě před vznikem OA. Evidence o účinnosti u již vzniklé OA je menší a pochází z několika nekontrolovaných nebo retrospektivních studií (74). Nicméně osteotomie je ve většině doporučení pro léčbu koxartrózy uváděna včetně EULAR a OARSI (3, 5). Indikována by měla být především u mladých, aktivních jedinců, zvláště při přítomnosti dysplazie. Vysoká tibiální osteotomie femuru byla navržena pro léčbu gonartrózy v 60. letech minulého století. Biomechanickou podstatou je náprava varózní deformity kolenního kloubu, snížení zatížení mediálního kompartmentu kolenního kloubu a přenesení hmotnosti na zdravější laterální kompartment. Biomechanické studie však ukázaly, že tohoto efektu by bylo dosaženo při korekci o 25°, zatímco v klinických situacích je dosahovaná korekce ST 6–14. Byla provedena metaanalýza 19 nekontrolovaných studií s 2406 výkony (75). Dobré výsledky ve smyslu zlepšení bolesti byly dosahovány až v 75 % po 5 letech. Průměrný čas do TKA byl 6 let a zatím se nepodařilo prokázat, že by osteotomie čas do nutnosti provést TKA prodlužovala. EULAR proto korekční osteotomii u gonartrózy nedoporučuje.
Závěr
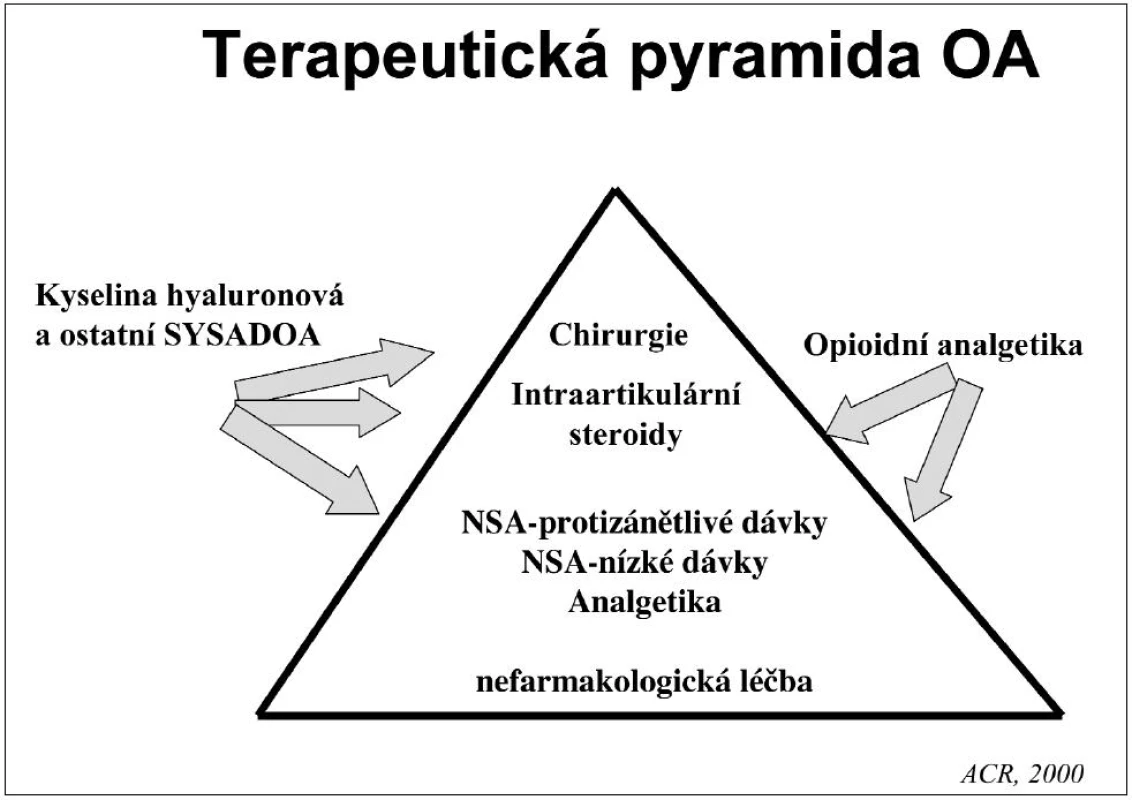
Osteoartróza kyčelních a kolenních kloubů probíhá často epizodicky, ale většinou pomalu progreduje. Terapeutická pyramida (obr. 5) přestavuje proto jen rámcový program, který by měl být individualizován u každého pacienta.
Léčba osteoartrózy rukou
Osteoartróza rukou je častou periferní lokalizací OA. Její výskyt stoupá s věkem. V populaci nad 66 let byla zjištěna prevalence symptomatické OA v 38 % u žen a ve 24 % u mužů (76). OA rukou byla dlouho považována za poměrně neškodné onemocnění, které jednak nevyvolává příliš symptomů (bolesti) a má malý vliv na zhoršení funkce a tím i kvalitu života. Vedlo to v praxi k hodnocení typu: kosmetický defekt, přechodná záležitost, s tím se stejně nedá nic dělat. Novější data však ukazují pravý opak, a to že OA rukou zhoršuje funkci rukou i kvalitu života nemocných s OA a v určitých ukazatelích se blíží revmatoidní artritidě (77).
Na začátku správné léčby OA rukou je řádná diagnostika. Jako u jiných lokalizací OA se kombinuje klinický nález s rentgenologickým. Při nedostupnosti rtg snímku lze diagnostikovat OA rukou dle kritérií ACR (78) (tab. 6). OA rukou je velmi heterogenní onemocnění. OA rukou postihuje nejčastěji distální interfalengeální klouby (DIP), přičemž postižení II. a III. DIP na dominantní ruce je vůbec nejčastější. Postižení distálních interfalengeálních kloubů nazýváme také tzv. Heberdenovými uzly. Dále jsou postiženy proximální interfalengeální klouby ve formě tzv. Bouchardových uzlů a postižení kořenového kloubu palce ruky (1. karpometakarpálního) ve formě rhizartrózy. Postižení MCP kloubů je méně časté a postižení radiokarpálních kloubů raritně vzácné a téměř vždy sekundární! Rhizartróza se může vyskytovat izolovaně nebo současně s OA interfalengeálních kloubů. Pokud jsou postiženy 3 klouby a více, hovoříme o tzv. generalizované osteoartróze. Zvláštní subset choroby tvoří tzv. erozivní osteoartróza (EOA). Pro ni je charakteristická přítomnost centrálně umístěné eroze na rentgenovém obraze. EOA má zpravidla více vyjádřenou zánětlivou složku. Vyvolává více bolestivých, zánětlivých epizod a má větší tendenci ke vzniku deformit. Vyskytuje se také sekundární OA při přítomnosti krystalů (pyrofosfátové artropatie) či při hemochromatóze.
Tab. 6. Klasifikační kritéria pro OA rukou (ACR). 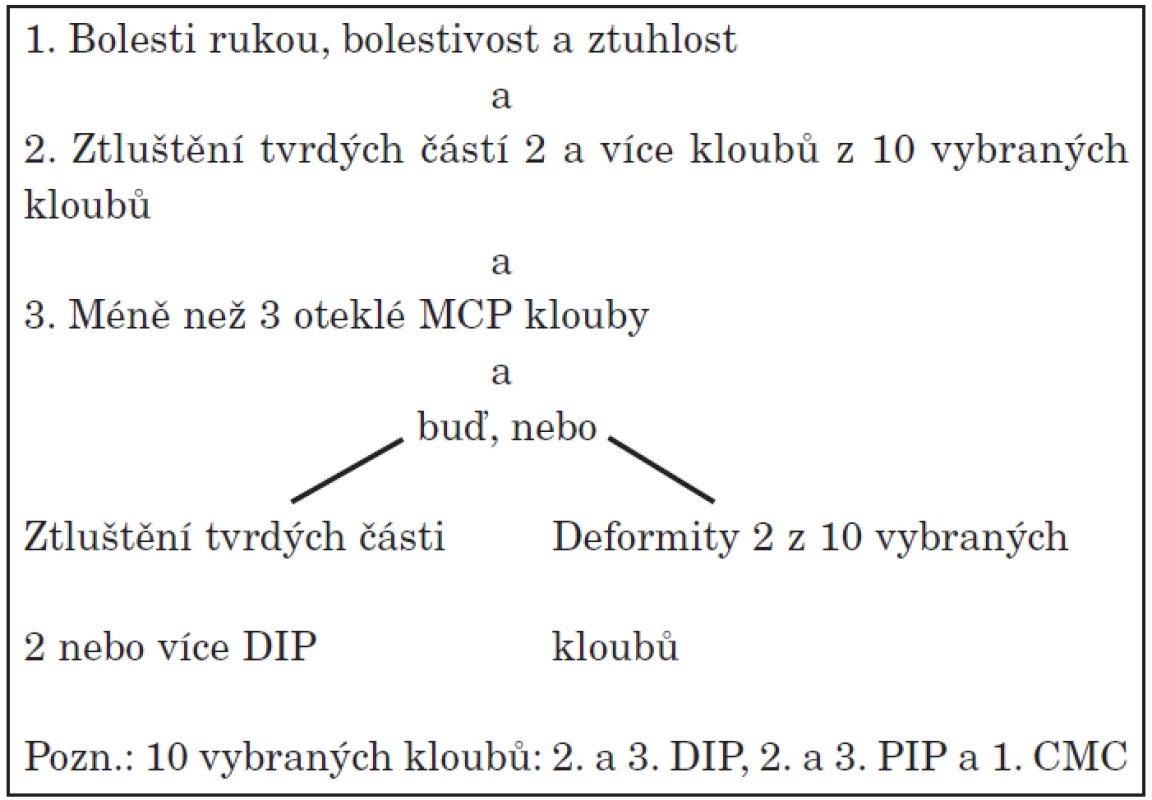
Publikací o léčbě osteoartrózy rukou je nesrovnatelně méně než u terapie OA kolenních a kyčelních kloubů. V systematickém přehledu navíc Towheed zjistil, že většina studií je nízké kvality a metaanalýza se mu v podstatě vůbec nepodařila udělat (79). Proto také EULAR při tvorbě svých nových doporučení pro léčbu OA rukou, musel často chybění evidence o účinnosti dané modality kompenzovat konsenzem nebo extrapolací zkušeností s danou léčebnou modalitou v jiné lokalizaci OA (80).
Cíle léčby jsou stejné jako u jiných lokalizací: Jde o zmenšení bolesti a udržení funkce a tím i zlepšení kvality života. Léčba by měla být individualizována pro každého pacienta podle jeho subjektivních obtíží, objektivního nálezu, strukturální progrese, dalších onemocnění a souběžné medikace. Každý pacient by měl být léčen komplexní léčbou, která se sestává z léčby nefarmakologické, farmakologické a eventuálně chirurgické.
Nefarmakologická léčba
Vzdělávání pacienta, jak má chránit klouby (aby odstranil negativní mechanické faktory) společně s cvičením se doporučuje všem pacientům s OA rukou. Byla provedena studie se 40 pacienty, kteří byli edukováni, jak chránit klouby a k tomu měli doporučeno cvičení na posilování svalů, zatímco kontrolní skupina obdržela pouze informaci. Skupina s kombinovaným režimem edukace a cvičení měla zlepšenou funkci rukou a počet pacientů nutných léčit (NNT) byl pouze 2 (81). Koncept ochrany kloubů se rutinně používá u revmatoidní artritidy, ale byl rozšířen i na další artropatie, jako je např. osteoartróza. Pro osoby s OA tento koncept znamená posilování svalové síly, směřující k absorpci šokových sil a snížení mechanického stresu kolem kloubů. V praxi dostane pacient ústní a písemné instrukce, o tom jak snížit tlaky na klouby, vibrace. Je poučen o používání asistenčních pomůcek, jako jsou zvětšené držáky na psaní, otevírání sklenic, držáky na knihy apod. Cvičení by měla obsahovat prvky vedoucí ke zvětšení rozsahu kloubů, tak posilování svalů.
Z fyzikálních procedur je u OA rukou často aplikován parafin a je i v doporučeních EULAR, nicméně Cochranská systémová analýza nepotvrdila u OA rukou účinnost ani teplých ani studených procedur (82).
Mezi další doporučované postupy lze zařadit užívání dlahy a ortéz na kořenový kloub palce k prevenci či korekci laterální angulace a flekční kontraktury. Ani toto doporučení není podpořeno randomizovanými, kontrolovanými studiemi. Dvě malé, srovnávací studie potvrdily, že kompletní dlaha pokrývající celou bázi palce a zápěstí je účinnější než poloviční dlaha pokrývající pouze bázi kořenového kloubu palce (83) (obr. 6).
Farmakologická léčba
Při farmakoterapii osteoartrózy rukou se používá v podstatě stejný sortiment léků jako u OA kolenních a kyčelních kloubů. Je však nutné poznamenat, že publikovaných, randomizovaných studií bylo v této lokalizaci podstatně méně než u OA kolenních a kyčelních kloubů. U některých preparátů dokonce nebyly provedeny studie žádné, takže při jejich doporučení bylo nutno zvážit a ev. extrapolovat výsledky z jiných lokalizací OA.
Lokální léčba
Při lokální léčbě se používají nesteroidní antirevmatika v různých formách (masti, gely, spreje, náplasti) nebo kapsaicin. Tato léčba má určitou logiku, protože jde o malé klouby těsně pod povrchem ruky, kde lokálně podávané NSA má šanci dosáhnout cílových struktur. Nicméně z kvalitních studií s lokálními NSA bylo provedeno poměrně málo. V metaanalýze publikované v roce 2005 byla prokázána účinnost lokálně aplikovaných NSA oproti placebu při úlevě od bolesti (84). Lokální léčba NSA není asociována s vyšším výskytem GIT komplikací, jako u systémové léčby NSA.
Další léčbu, kterou lze doporučit je aplikace lokálně aplikovaného kapsaicinu, protože v této indikaci byly provedeny dvě placebem kontrolované úspěšné studie (85, 86).
Paracetamol
Nebyla provedena žádná studie s paracetamolem u OA rukou, nicméně je doporučován na základě nepřímé evidence o účinnosti tohoto léku v jiných lokalizacích (80).
Nesteroidní antirevmatika
Bylo provedeno pouze několik málo studií s NSA u OA rukou, které ale všechny prokázaly účinnost. Velikost úlevy od bolesti byla středně velká (ES = 0,40). Na základě této evidence je možné NSA u OA rukou doporučit (87).
SYSADOA
Byly provedeny dvě kontrolované studie s chondroitin sulfátem. První dvě byly nezávislé studie v délce trvání 3 let. Byl prokázán určitý zpomalující efekt na vývoj strukturální progrese artrózy, ale nebyl zaznamenán žádný symptomatický efekt (88). Nová randomizovaná, kontrolovaná studie prokázala symptomatický efekt při ovlivnění funkce a bolesti u pacientů s bolestivou artrózou rukou (89). Nebyly provedeny žádné randomizované, kontrolované studie s glukosamin sulfátem a diacereinem u OA rukou a lze je doporučit pouze při extrapolaci výsledků s těmito preparáty v jiných lokalizacích. Byla provedena jedna malá kontrolovaná studie s aplikací kyseliny hyaluronové a kortikoidů do trapeziometakarpálního kloubu, jejíž výsledky byly pozitivní a mohly by indikovat použití tohoto preparátu v této lokalizaci (90). Je nutno provést další studie.
Glukokortikoidy
Klinických studií bylo provedeno velmi málo. Byla provedena řada nekontrolovaných studií s pozitivními výsledky, ale jediná malá placebem kontrolovaná studie, vyzněla negativně (91). Nicméně názor expertů po analýze klinických zkušeností a extrapolací z jiných lokalizací je, že aplikace glukokortikoidů při bolestivé rhizartróze je užitečná. Nicméně účinky jsou většinou krátkodobé.
Chirurgická léčba osteoartrózy rukou
Při selhávání konzervativní léčby je možno uvažovat o chirurgickém řešení OA rukou. Indikací k léčbě je přetrvávající refrakterní bolest a výrazná porucha funkce. Distální interfalangeální klouby se operují výjimečně a prakticky jedinou používanou metodikou je artrodéza. Na proximálních interfalangeálních kloubech se běžně provádí artroplastika. V klinické praxi je však častější artroplastika u revmatoidní artritidy než u OA. U části pacientů dochází k uvolnění umělého kloubu. Celá řada operací se provádí při artróze prvního CMC kloubu. V této indikaci se aplikují: trapeziektomie s/nebo bez syntetické nebo biologické interpozice, osteotomie a totální náhrada kloubu. Byly publikovány 2 systematické přehledy v Cochranské analýze (92). Analýza se zabývala i otázkou, zda-li je účinnější kombinace 2 procedur, což se nepotvrdilo. Možnosti chirurgické léčby OA rukou jsou shrnuty v tabulce 7.
Tab. 7. Možnosti chirurgické léčby rukou. 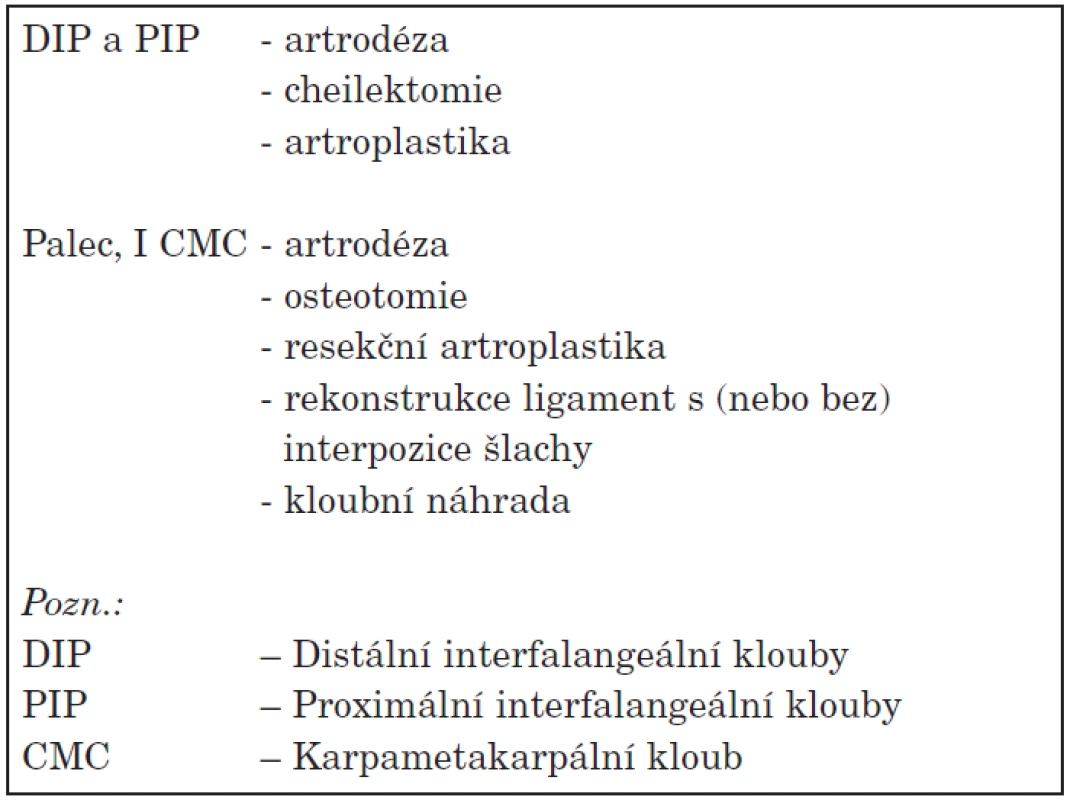
Závěr
Přímá evidence o účinnosti existuje u OA rukou pro: vzdělávání a cvičení, NSA, COX-2 inhibitory, lokální NSA a kapsaicin a chondroitin sulfát.
Extrapolací z jiných lokalizací byly doporučeny paracetamol, glukosamin a lokální glukokortikoidy.
Ostatní postupy jsou doporučovány pouze na základě konsenzu expertů (např. teplo pomocí parafinu, chirurgické postupy).
Prof. MUDr. Karel Pavelka, DrSc.
Revmatologický ústav Praha
Na Slupi 4
128 50 Praha 2
Zdroje
1. Dawson J, Linsell L, Zondervan K, et al. Epidemiology of hip and knee pain and its impact on overall health status in older adults. Rheumatology 2004;43 : 497-504.
2. Altmann RD, Asch E, Bloch D, et al. Development of criteria for the classification and reporting of osteoarthritis: classification of osteoarthritis of the knee. Arthritis Rheum 1986;29 : 1039-1049.
3. Zhang W, Doherty M, et al. EULAR evidence based recommendations for the diagnoses of the OA. Ann Rheum Dis 2010;69 : 483-489.
4. Bellamy N, Buchannan WW, Goldsmith CH. Validation study of WOMAC. General Rheum 1988;15 : 1833-40.
5. Zhang W, Doherty M, Arden N, et al. EULAR recommendations: an evidence based medicine approach to the management of hip osteoarthritis. Report of task force of ESCISIT. Ann Rheum Dis 2005;64 : 669-81.
6. Zhang W, Moskowitz RW, Nuki G, et al. OARSI recommendations for the management of hip and knee osteoarthritis, Part bII. OARSI evidence based, expert consensus guidelines. Osteoarthr Cartil 2008;16 : 137-162.
7. Van der Esch M, Heimans M, Dekker J. Factors contributing to the possession and use of walking aids among patients with rheumatoid arthritis and osteoarthritis. Arthritis Rheum 2003;49 : 838-842.
8. Brouwer RW, Jakma TS, Verhjagen AP, et al. Braces and orthoses for treating osteoarthritis of the knee. Cochrane Database Syst Rev Jan 2005;25/1/ CD004020
9. Roddy E, Zhang W, Doherty M, et al. Aerobic walking exercise for osteoarthritis of the knee? A systematic review. Ann Rheum Dis 2005;64 : 544-8.
10. Hernandez-Molina G, Reichenbach S, Bin Z, et al. Effect of therapeutic exercise for hip osteoarthritis pain: results of metaanalysis. Arthritis Care Res 2008;59 : 1221-1228.
11. Bartels EM, Lund H, Hagen KB, et al. Aquatic exercise for the treatment of knee and hip osteoarthritis. Cochrane Database Sy Rev 2007;CD 005523.
12. Zhang W, Nuki G, Moskowitz RW, et al. OARSI recommendations for the management of hip and knee osteoarthritis Part III. changes in evidence following systematic cumulative update of research published through January 2009. Osteoarthr Cartil 2010;18 : 476-499.
13. Brosseau L, Yonge KA, Robinson NV, et al. Thermotherapy of treatment of osteoarthritis. Cochrane Database Syst Rev 2003;4:CD004522.
14. Yurtkuran M, Kocagil T. TENS, electroacupuncture and ice massage: comparison of treatment of osteoarthritis of the knee. Am J Acupunct 1999;27 : 133-40.
15. Mc Carthy CJ, Callghan MJ, Oldham JH, et al. Pulsed electromagnetic energy treatment offers no clinical bendit in reducing the pain of knee osteoarthritis: a systematic review. BMC Musculoscelet Disord 2006;51.
16. Manheimer E, Linde K, Lao I, et al. Metaanalysis: acupuncture for osteoarthritis of the knee. Ann Intern Med 2007;146 : 868-77.
17. Bjordal JM, Johnson MI, Lopes-Martins RAB, et al. Short term efficacy of physical intervention of osteoarthritis knee pain. A systematic review and meta-analysis of randomised, placebo controlled trials. BMC Musculoscelet Disord 2007;8 : 51,doi: 101186/1471-2474/8/51l.
18. Towheed TE, Maxwell IL, Judd MG, et al. Acetaminophen for osteoarthritis. Cochrane Libr Oxford/2002;4:ID CD 004257.
19. Towheed TE, Maxwell IL, Judd MG, et al. Acetaminophen for osteoarthritis. Cochrane DATABASE Syst Rev 2006;1:CD 004257.
20. Rahme E, Barkun A, Nedjar H, et al. Hospitalizations for upper and lower GI events associated with traditional NSAIDs and acetaminophen among the elderly in Quebeck. Canada Am J Gastroenterol 2008;103 : 872-82.
21. FDA. Drug safety information http:www.fda.gov/ /Drugs/Drug Safety/information by drug class/ucm165107.htm:2009.
22. Bjordal JM, Ljungren AE, Klovning A, et al. Non-steroidal antiinflammatory drugs, including cyclooxygenase-2 inhibitors in osteoarthritis knee pain: meta-analysis of randomised placebo controlled trials. BMJ 2004;329 : 1317-20.
23. Bjordal JM, Klovning A, Ljungren AE, et al. Short term efficacy of pharmacotherapeutic innervations in osteoarthritis knee pain: a metaanalysis of randomised placebo controlled trials. Eur J Pain 2007;11 : 125-38.
24. Zhang W, Jones A, Doherty M, et al. Does paracetamol reduce the pain of osteoarthritis? A metaanalysis of randomised controlled trials. Ann Rheum Dis 2004;63 : 901-907.
25. Ofman JJ, MacLean CH, Straus WL, et al. A metaanalysis of severe upper gastrointestinal complications of nonsteroidal antiinflammatory drugs. J Rheumatol 2002; 29 : 804-812.
26. Rahme E, Barkun A, Nedie H, et al. Hospitalizations for upper and lower GI events associated with traditional NSAIDs and acetaminophen among the elderly in Quebec. Canada, Am J Gastroenteroll 2008;103 : 872-82.
27. Chan FK, Wong VW, Suen BY, et al. Combination of cyclo-oxygenase-2 inhibitor and a proton-pump inhibitor for preventive of recurrent ulcer bleeding in patients at very high risk: A double-blind, randomised trial. Lancet 2007;369 : 1621-6.
28. Rahme E, Barkun AN, Touboti Y, et al. Do proton pump inhibitors confer additional gastrointestinal protection in patients given celekoxib? Arthritis Rheum 2007;57 : 748-55.
29. Latimer N, Lord J, Grant RL, et al. Cost effectiveness of COX-2 selective inhibitors and traditional NSAIDs alone or in combination with a proton-pump inhibitor for people with osteoarthritis. BMJ 2009;339:b 2538.
30. Kearney PM, Baigent C, Godwin J, et al. Do selective cyclo-oxygenase inhibitors and traditional non steroidal anti-inflammatory drugs increase the risk of atherotrombosis? Meta-analysis of randomised trials. BMJ 2006;332 : 1302-1308.
31. EMEA/CHMP410051/2006.
32. Lin J, Zhang W, Jones A, et al. Efficacy of topical NSAIDs in the treatment of osteoarthritis: a metaanalysis of randomised controlled trials. Chin J Evid Based Med 2005;5 : 667-674.
33. Biswal S, Medhi B, Panhi P, et al. Long-term efficacy of nonsteroidal antiinflammatory drugs in knee OA: metaanalysis of randomized placebo controlled trials. J Rheumatol 2006;33 : 1841-1844.
34. Deal CL, Schnitzer TJ, Lipstein E, et al. Treatment of arthritis with topical kapsaicin: A double - blind trial. Clin Ther 1991;13 : 383-96.
35. Avouac J, Gossec L, Dougados M. Efficacy and safety of opioids for osteoarthritis: a metaanalysis of randomized, controlled trials. Osteoarthr Cartil 2007;15 : 957-965.
36. Pavelka K, Loet LX, Bjorneboe O, Herrero-Beuamont G, Richarz U. Benefits of transdermal fentanyl in patients with rheumatoid arthritis or with osteoarthritis of the knee or hip: an open-label study to assess pain control. Current Medical Research and Opinion 2004; Vol. 20, 12 : 1967-1977.
37. Persiani S, Rotinin R, Trisolino G, et al. Synovial and plasma concentrations in osteoarthritis patients following crystaline glucosamine sulphate at therapeutic dose. Osteoarthr Cartil 2007;15 : 764-772.
38. Towhead TE, Maxwell, Ana stassiades TP, et al. Glucosamine therapy for treating osteoarthritis .The Cochrane Libr /Oxford/ 2005;4:IDCD002946.
39. Clegg D, Reda DJ, Harris CL, et al. Glucosamine, chondroitin sulphate and the two in combination for painful knee osteoarthritis. N Engl J Med 2006;354 : 795-808.
40. Herrero-Beaumont G, Roman Ivora JA, del Carmen Trabado MC, et al. Glucosamine sulphate in the treatment of knee osteoarthritis symptoms: a randomized, double-blind, placebo-controlled study using acetaminophen as a side comparator. Arthritis Rheum 2007;56 : 555-567.
41. Wandel S, Juni P, Tendal B, et al. Effects of glucosamine, chondroitin, or placebo with osteoarthritis of hip or knee: network meta-analysis BMJ 2010;341:c4675 doi:10.10.1136/bmj.c.4675.
42. Reginster Y, Dereoisy R, Rovatti LC, et al. Long - term effects of glucosamine sulphate on osteoarthritis progression: a randomized, placebo controlled clinical trial. Lancet 2001;357 : 251-6.
43. Pavelka K, Gatterova J, Olejarova M, et al. Glucosamine sulphate use and delay of progression of knee osteoarthritis. Arch Intern Med 2002;162 : 2113-23.
44. Moldovan F, Pelletier JP, Jolicoeur FC, et al. Diacerein and rhein ruduce the ICE –induced IL-1β and IL 18 activation in human osteoarthritis cartilage cultures. Osteoarthr Cartil 2000;8 : 186-196.
45. Smith GN, Myers SL, Brandt KD, et al. Diacerein treatment reduces the severity of osteoarthritis in the canine cruciate-deficiency model of osteoarthritis. Arthritis Rheum 1999;42 : 545-54.
46. Pelletier JP, Yaron M, Harauuai B, et al. Diacerein study group .Efficacy and safety of diacerein in osteoarthritis of the knee: a double-blind, placebo controlled trial. Arthritis Rheum 2000;43 : 2339-48.
47. Pavelka K, Trč Tomáš, Karpaš K, et al. The efficacy and safety of diacerein in the treatment of painful osteoarthritis of the knee. Arthritis Rheum. 2007;56 : 4055-4064.
48. Rintelen B, Neumann K, Leeb B. A metaanalysis of controlled clinical studies with diacerein in the treatment of osteoarthritis. Arch Intern Med 2006;1661899-1906.
49. Fidelix TSA, Soares BGDO, Trevisani VFM, et al. Diacerein for osteoarthritis (Cochrane Review). The Cochrane database of Systemic Reviews 2006, Issue 1. Arit No:CD005117.
50. Dougados M, Nguyen M, Berdah L, et al. Evaluation of the structure modifying effects of diacerein in hip osteoarthritis. ECHODIAH: a three year placebo-controlled trial. Arthritis Rheum 2001;44 : 2539-47.
51. Mauviel A, Daireaux M, Hartmann D, et al. Effects des insaponifables diavocat et da soja sur la production de collagene par des cultures de synoviocytes, chondrocytes articulares et fibroblastes dermiques. Mal Osteoartic 1989;56 : 207-211.
52. Kawczak CE, Frisbie DD. Mc Ilwright CW, et al. Evaluation of avocado and soya been unsaponifables extracts for treatment of horses with experimentally induced osteoarthritis. Am J Vet Res 2007;68 : 598-604.
53. Boumediene K, Felisaz N, Bogdanowicz P, et al. Effects of free avocado soyabean insaponifables mixtures on metaloproteinases, cytokines and prostagalandins E 2 production by human articular chondrocytes. Clin Rheumatol 1998;17 : 31-39.
54. Maheu E, Valat JP, et al. Symtomatic efficacy of avocado/soya bean unsaponifables in the treatment of the osteoarthritis of knee and hip: a prospective, randomized, double blind, placebo controlled, multicenter clinical trial with a six-months follow up demonstrative a persistent effect. Arthritis Rheum 1998;41 : 81-91.
55. Appelboom T, Schuermans J, Verbruggen G, et al. Symptoms modifying effect of avocado/soyabean unsaponifables (ASU) in knee osteoarthritis. Scand J Rheumatol 2001;30 : 242-7.
56. Christensen P, Bartels EM, Astrup A, et al. Symptomatic efficacy of avocado-soybean unsaponifables (ASU) in OA patients: a metaanalysis of randomized, controlled trials. Osteoarthr Cartil 2007;29,doi: 10.1016/j.joca.2007.10.003.
57. Maheu E, Cadet C, Marty M, et al. Evaluation of the structure modifying effect of ASU in hip OA. Results of ERADIAS study. A 3 year prospective, randomized, double blind, placebo controlled trial. Osteoarthr Cartil 18:(Suppl.2):560.
58. Monfort J, Pelletier JP, Garcia-Giralt N, et al. Biochemical basis of the effect of chondroitin sulfate on osteoarthritis articular tissues. Ann Rheum Dis 2007 as 10.1136/ard.2006.068882.
59. Richy F, Bruyere O, Ethgen O, et al. Structural and symptomatic efficacy of glucosamine and chondroitin in knee osteoarthritis: a comprehensive meta-analysis. Arch Intern Med 2003;163 : 1514-1522.
60. Clegg DO, Reda DJ, Harris CL, et al. Glucosamine, chondroitin sulfate, and the two in combination for painful knee osteoarthritis. N Engl J Med 2006Ost;364 : 795-808.
61. Gabay C. Symptomatic effects of chondroitin 4 an chondroitin 6 sulfate on hand osteoarthritis: a randomized, double blind, placebo controlled clinical trial at a single center. Arthritis Rheum 2011;63 : 3383-3391.
62. Kahan A, Uebelhart D, Fathaire F, et al. Long term effects of chondroitin 4 and 6 sulphate on knee osteoarthritis. The study on osteoarthritis progression preventive, a two - year, randomized double blind, placebo controlled trial. Arthritis Rheum 2009;60 : 524-533.
63. Ghosh P. The role of hyaluronic acid (hyaluronan) in health and disease: interactions with cells, cartilage and components of synovial fluid. Clin Exp Rheumatol 1994;12 : 85-87.
64. Bellamy N, Campbell J, Robinson V, et al. Viscosupplementation for the treatment of osteoarthritis of the knee. Cochrane Database Syst Rev 2006;April19 th/2/:CD005321.
65. Bannuru RR, Natov NS, Obadan IE, et al. Therapeutic trajectory of hyaluronic acid versus corticosteroids in the treatment of knee osteoarthritis: a systematic review and metaanalysis. Arthritis Care Res 2009;61 : 1704-1711.
66. Lo GH, Lavalley M, Felson DT. Intraarticular hyaluronic acid in the treatment of knee osteoarthritis: A metaanalysis. JAMA 2003;290 : 3115-21.
67. Reichenbach S, Blank, Rutjes AW, et al. Hylan versus hyaluronic acid for osteoarthritis of the knee a systematic review and metaanalysis. Arthritis Rheum 2007;57 : 1410-1408.
68. Jubb RW, Piva M, Beinat L, et al. A one year, randomized trial of 500-730 kDa sodium hyaluronate on the radiological stage of osteoarthritis of the knee. Inter J Clin Practise 2003;57 : 1-8.
69. Pavelka K, Uebelhart D. Efficacy of highly purified intraarticular hyaluronic acid (Synovial) vs. hylan G-F20 (Synvisc) in the treatment of symptomatic knee osteoarthritis. A double blind, controlled, randomized, parallel-group non - inferiority study Osteoarthr Cartil doi:10. 1016/j.joca.2011.07.016.
70. Fitzpatrick R, Shortall E, Sculpher M, et al. Primary total hip replacement Summary: a systematic review of outcomes and modelling of cost–effectiveness associated with different prostheses. Health Technol Asssessss.1998;2 : 1-4.
71. Rand JA, Trousdale RT, Ilstrup DM, et al. Factors affecting the durability and primary total knee prostheses. J Bone Joint Surg Am 2003;85 : 259-65.
72. Rasanen P, Paavolainen P, Sintonen H, et al. Effectiveness of hip or knee replacement Summery in term soft quality-adjusted life years and cost. Acta Orthop 2007;78 : 108-15.
73. Siparsky P, Ryzewicz M, Peterson B, et al. Arthroscopic treatment of osteoarthritis of the knee: are there any evidence –based indications? Clin Orthop Relat Res 2007;455 : 107-112.
74. Koulovaris P, Stafylas K, Aznaoutoglou C, et al. Isolated varus intertrochanteric osteotomy for hip dysplasia in 52 patients: long term results. Int Orthop (SICOT) 2007;31 : 193-198.
75. Virolainen P, Aro HT High tibial osteotomy for the treatment of osteoarthritis of the knee: a review of the literature and a metaanalysis of follow up studies. Arch Orthop Trauma Surg 2004;124 : 258-61
76. Scott JC, Hochberg MC. Osteoarthritis: I. Epidemiology. Md State Med J 1984;33 : 712-716.
77. Jones G., Cooley HM., Bellamy N. A cross-sectional study of the association between Heberdenęs nodes, radiographic osteoarthritis of the hands, grip strength, disability and pain. Osteoarthritis Cart. 2001;9 : 606-611.
78. Altman RD, Alarcom G, Appelrouth D, et al. The American College of Rheumatology criteria for the classification and reporting of osteoarthritis of the hand. Arthritis Rheum. 1990;33 : 1601-1610.
79. Towheed TE. Systematic review of therapies for osteoarthritis of the hand. Osteoarthritis Cart. 2005;13 : 455-462.
80. Zhang W, Doherty M, Leeb B, et al. EULAR evidence based recommendations for the management of hand osteoarthritis – report of a task force of the EULAR standing committee for international clinical studies including therapeutics (ESCISIT). Ann Rheum Dis 2007; 66 : 377-388.
81. Stamm TA, Machold KP, Smolen JS, et al. Joint protection and home hand exercises improve hand function in patients with hand OA: a randomized, controlled trial. Arthritis Care Res 2002;47 : 44-49.
82. Brosseau L, Judd MG, Marchand S, et al. Thermo therapy for treatment of ostearthritis. The Cochrane Database of Systemic Reviewes: Reviews 2003; Issue 4, John Wiley and sons, Ltd. Chichester, UK DOI: 10 1002/ /14651858C 2003.
83. Weiss S, Lastayo P, Mills A, et al. Splinging the degenerative basal joint: custom - made or prefatricated neoprene? J Hand Ther 2004;17 : 401-406.
84. Lin J, Zhang W, Jones A, et al. Efficacy of topical non-steroidal anti-inflammatory drugs in the treatment of osteoarthritis: meta-analysis of randomised controlled trials. BMJ 2004;329 : 324.
85. Mccarthy GM, Mccarty DJ. Effect of topical capsaicin in the therapy of painful osteoarthritis of the hands. J Rheumatol 1992;19 : 604-7.
86. Schnitzer T, Morton C, Coker S. Topical capsaicin therapy for osteoarthritis pain: achieving a maintenance regimen. Semin Arthritis Rheum 1994;23 : 34-40.
87. Seiler V. Meclofenamate sodium in the treatment of degenerative joint disease of the hand (Heberden nodes). Arzneimittel-Forsch 1983;33 : 656-9.
88. Verbruggen G, Goemaere S, Veys EM, et al. Systems to assess the progression of finger joint osteoarthritis and the effects of disease modifying osteoarthritis drugs. Clin Rheumatol 2002;21 : 231-43.
89. Gabay C, Medinger-Sadowski C, Gascon D, et al. Symptomatic Effects of Chondroitin 4 and Chondroitin 6 Sulfate on Hand Osteoarthritis. Arthritis Rheum 2011; 63(11):3383-3391.
90. Fuchs S, Monikes R, Wohlmeiner A, et al. Intra-articular hyaluronic acid compared with corticoid injecions for the treatment of rhizarthrosis. Osteoarthritis Cartilage 2006;14 : 82-8.
91. Joshi R. Intraarticular corticosteroid injection for first carpometacarpal osteoarthritis. J Rheumatol 2005;32 : 1305-6.
92. Wajon A, Ada L, Edmunds I, et al. Surgery for thumb osteoarthritis. The Cochrane Database of Systemic Reviews: Review 2005, Issue 4, John Wiley and Sons, Ltd. Chichester, UK DOI:10 1002/14651858 CD 004631 pub 2 2005.
Štítky
Dermatologie Dětská revmatologie Revmatologie Chirurgie všeobecná Ortopedie Praktické lékařství pro dospělé
Článek vyšel v časopiseČeská revmatologie
Nejčtenější tento týden
2012 Číslo 3- Takrolimus v terapii atopické dermatitidy a analýza jeho nákladové efektivity ve srovnání s kortikosteroidní léčbou
- Naděje budí časná diagnostika Parkinsonovy choroby založená na pachu kůže
- Efektivita kartáčku Sonicare For Kids u dětí předškolního věku
- Efekt itopridu na motilitu jícnu a funkci dolního jícnového svěrače
- Podmínky užití mukolytik v dětském věku se v Evropě zpřísňují − která léčba je preferovaná?
Nejčtenější v tomto čísle- Multiorgánové selhání a syndrom aktivovaných makrofágů u Stillovy nemoci v dospělosti
- Doporučení České revmatologické společnosti pro léčbu osteoartrózy kolenních, kyčelních a ručních kloubů
- Zpráva z 56. výročního sjezdu českých a slovenských revmatologů, Olomouc
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Revma Focus: Spondyloartritidy
nový kurz
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Autoři: prof. MUDr. Pavel Horák, CSc., doc. MUDr. Ludmila Brunerová, Ph.D., doc. MUDr. Václav Vyskočil, Ph.D., prim. MUDr. Richard Pikner, Ph.D., MUDr. Olga Růžičková, MUDr. Jan Rosa, prof. MUDr. Vladimír Palička, CSc., Dr.h.c.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání