Následující kazuistika popisuje případ pacienta, který byl v prosinci 2020 akutně operován pro ileus na podkladě stenozujícího tumoru sigmatu. Peroperačně byly diagnostikovány 3 jaterní metastázy. Systémovou chemo-bioterapií bylo dosaženo významné regrese velikosti s následným radikálním výkonem – jaterní metastazektomií. V současné době je pacient vzhledem k recidivě jaterních metastáz a rozsevu do plic léčen další linií systémové léčby.
Anamnéza a klinický obraz
Pacient (nar. 1952) anamnesticky užíval perindopril, který byl pro sklon k hypotenzi při váhovém úbytku vysazen. Vzhledem k hyperlipidémii měl nasazen i atorvastatin. Byl nekuřák, alkohol užíval pouze příležitostně.
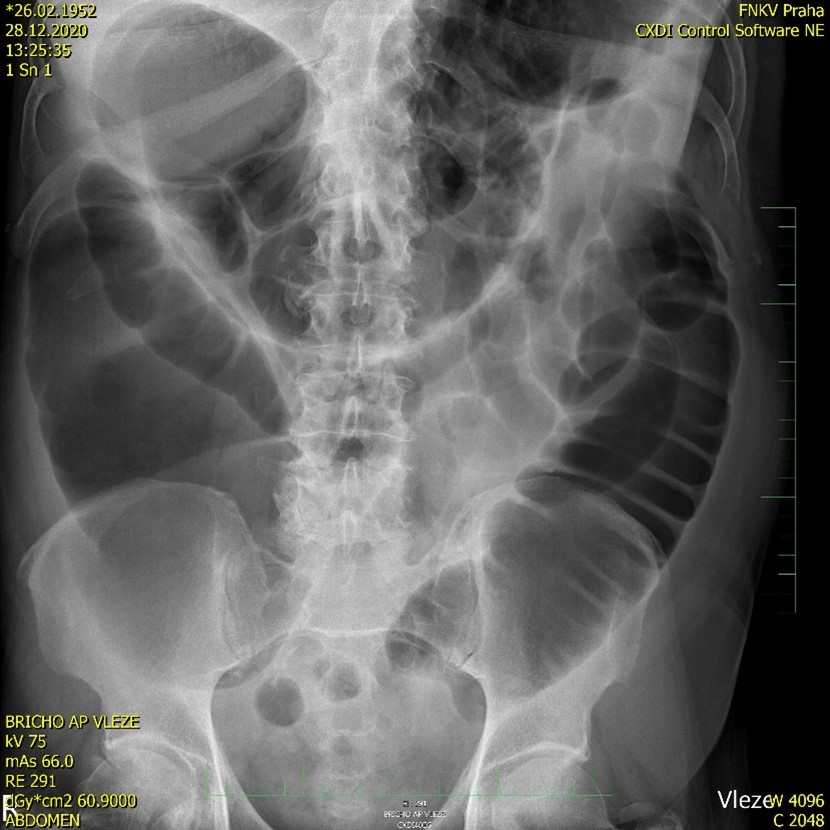
V prosinci 2020 byl s anamnézou 2 dni trvajících progredujících dyspeptických potíží a poruchy pasáže odeslán praktickým lékařem na chirurgii. V rámci vyšetření byl diagnostikován ileózní stav s dilatací celého tlustého střeva (distenze tračníku v celém průběhu, do šíře lumen 10 cm) s progresí až na kličky tenkého střeva (tenké kličky šíře 45 mm) na podkladě stenozujícího tumoru sigmatu (viz obr. 1).
Obr. 1 Ileus při stenozujícím tumoru sigmatu
Akutní chirurgický výkon a vstupní staging
Pacient byl akutně operován a vzhledem k pokročilosti peroperačního nálezu s distančními rupturami céka a colon ascendens byla provedena subtotální kolektomie s terminální ileostomií. Peroperačně byly popsány 3 jaterní metastázy. Histologické vyšetření resekátu prokázalo pokročilý nález. V sigmatu byl přítomen středně diferencovaný invazivní adenokarcinom intestinálního typu, fokálně s venózní vaskulární invazí a perineurální propagací. Nádor přerůstal celou stěnou střeva, šířil se až na serózní povrch. V perikolickém tuku bylo zastiženo celkem 22 lymfatických uzlin, ve 4 uzlinách s metastázou adenokarcinomu (4/22). Hodnoceno jako pT4a pN2a (4/22), V1, L0, Pn1, R0.
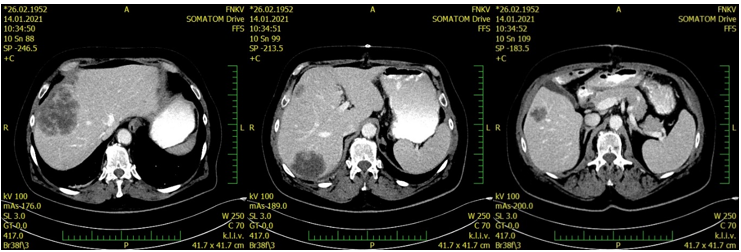
Pacient byl následně odeslán na onkologickou kliniku k další terapii. Bylo doplněno vyšetření prediktivních faktorů, které prokázalo wt-RAS, wt-BRAF, MSS status nádoru. Před zahájením terapie bylo doplněno stagingové CT vyšetření, které potvrdilo peroperační suspekci na generalizaci do jater. Dle CT byly popsány 3 jaterní metastázy: ložiska S8 85 mm, S7 56 mm, S5/S6 28 mm (viz obr. 2). Současně byla laboratorně přítomná výrazná elevace markerů: CEA 196,3 μg/l a CA 19-9 3557 kU/l. Vzhledem k velikosti jaterních metastáz a vysokým hodnotám nádorových markerů bylo rozhodnuto o zahájení systémové terapie s cílem konverze potenciálně resekabilního jaterního postižení.
Obr. 2 Vstupní staging (1/2021)
Iniciální systémová léčba a odpověď na ni
Pacient zahájil léčbu režimem mFOLFOX6 + panitumumab začátkem února 2021. V době zahájení léčby byl ve výkonnostním stavu PS 0 dle WHO, hmotnostně stabilní. Tolerance léčby byla i přes přítomnost ileostomie uspokojivá a nedošlo k navýšení odpadů do stomie. Kožní toxicita spojená s podáváním panitumumabu byla spíše mírnějšího charakteru a pacienta neomezovala, nezhoršovala kvalitu života ani nevyžadovala systémovou terapii. Poměrně časně se však při systémové léčbě objevila hematologická toxicita (trombocytopenie), která po 6. cyklu dosáhla grade 2 (62 × 109/l). Pacient i vzhledem k prvním projevům neuropatie dále pokračoval v monoterapii panitumumabem.
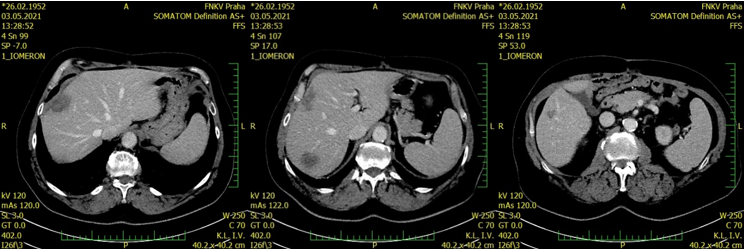
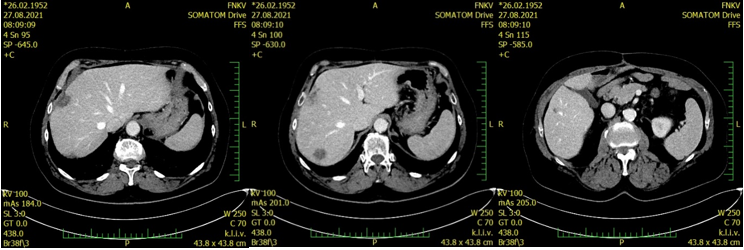
V rámci prvního restagingu byla popsána příznivá odpověď jaterních ložisek. Dle CT došlo k regresi všech 3 přítomných metastatických ložisek: ložiska S4/8 60 × 37 mm (vstupně 91 × 68 mm), S7 45 × 38 mm (vstupně 63 × 52 mm), S5 18 × 12 mm (vstupně 31 × 22 mm) (viz obr. 3). Současně došlo k normalizaci markerů: CEA 2,5 μg/l a CA 19-9 26,7 kU/l. Byla zvažována metastazektomie, nicméně pacient nebyl výkonu nakloněn, a navíc byla dle CT popsána drobná nespecifická plicní ložiska do 6 mm. Pacient dále pokračoval v monoterapii panitumumabem. V rámci dalších restagingových vyšetření byla opakovaně popsána regrese jaterních metastáz. Nález na plicích byl stacionární (nespecifický). Při restagingu v září 2021 byla popsána další regrese velikosti jaterních metastáz: v S8 34 mm, v S7 28 mm a v S5 8 mm. Plicní nález byl stále stejný, markery negativní (viz obr. 4).
Obr. 3 Re-staging (5/2021)
Obr. 4 Restaging (8/2021)
Metastazektomie
Vzhledem k pokračující odpovědi jaterních metastáz, stacionárním nespecifickým plicním ložiskům a negativním markerům byl pacient indikovaný k provedení metastazektomie. Do doby operace bylo celkem aplikováno 16 cyklů panitumumabu (z toho prvních 6 v kombinaci s mFOLFOX6). Operace proběhla v říjnu 2021, kdy byla provedena neanatomická resekce S2, S7 a S3/4/5. Histologické vyšetření potvrdilo metastázy středně diferencovaného adenokarcinomu tlustého střeva s pokročilými regresivními změnami charakteru nekrózy a hyalinizace. Krátce po dimisi však došlo k rozvoji septického stavu s nutností chirurgické revize, která prokázala absces v oblasti resekční plochy jater. V kombinaci s antibiotickou terapií postupně nastalo zlepšení stavu. Pro opětovnou elevaci zánětlivých markerů a recidivu abscesu bylo rozhodnuto o drenáži pod CT kontrolou, která byla provedena začátkem listopadu 2021. V průběhu listopadu až prosince byl pacient opakovaně vyšetřen na chirurgii, odpady drénu byly s poklesem a drén byl odstraněn.
Recidiva a nasazení další linie systémové léčby
Vzhledem k vleklým komplikacím po jaterní metastazektomii se pacient dostal zpátky ke kontrole na onkologickou kliniku až začátkem února 2022, kdy se zjistila opět elevace markerů: CEA 7,4 μg/l a CA 19-9 35,2 kU/l. Restagingové CT potvrdilo progresi onemocnění: rezidua po abscesech a nově nehomogenní hypoechogenní ložisko v S7/8 do 33 mm, v S6 do 15 mm; současně byla popsána i progrese v plicích: bilaterální vícečetná metastatická ložiska, největší v S1–2 vlevo cca 12 mm.
Vzhledem k progresi onemocnění v játrech a plicích byla zahájena další řada systémové léčby: FOLFIRI + aflibercept od února 2022. V dubnu 2022 byl aplikován 5. cyklus systémové léčby s překvapivě dobrou tolerancí jak gastrointestinální (nedošlo ke zhoršení odpadů ileostomií), tak hematologickou (bez přítomné trombocytopenie) a nebyla pozorována ani toxicita po afliberceptu ve smyslu akcelerace hypertenze či proteinurie. Restagingové vyšetření je v plánu po 3 měsících léčby. V případě alespoň stabilizace onemocnění je v plánu pokračování v systémové léčbě. Případný chirurgický zákrok ve smyslu jaterní či plicní metastazektomie je zejména vzhledem k vícečetným plicním metastázám velmi nepravděpodobný.
Závěr
Kazuistika potvrzuje významný benefit anti-EGFR preparátů v konverzní léčbě potenciálně resekabilního metastatického onemocnění, zejména v případě levostranné lokalizace primárního nádoru. Již po iniciální 3měsíční systémové terapii byla prokázána signifikantní regrese velikosti jaterního postižení umožňující provedení resekce. Nicméně vzhledem k nesouhlasu pacienta výkon proveden nebyl a pacient pokračoval v monoterapii anti-EGFR. I při ní došlo k další regresi velikostí jaterních metastáz a následně byla provedena metastazektomie. Bohužel již 4 měsíce od výkonu byla popsána recidiva v játrech a rozsev do plic. Je tedy potřeba identifikovat další potenciální ukazatele kromě aktuálně používaných (jako je odpověď na zobrazovacích metodách či negativizace markerů), které by pomohly predikovat benefit jaterní metastazektomie, s cílem selektovat pacienty a maximalizovat benefit tohoto přístupu.
MUDr. Marián Liberko
doc. MUDr. Renata Soumarová, Ph.D., MBA
Onkologická klinika 3. LF UK a FNKV Praha