Systémová léčba zhoubných nádorů aktuálně prochází zásadní změnou. Odklání se od paradigmatu, v němž se histopatologicky definovaná onemocnění léčí v první řadě cytostatiky, a směřuje k použití molekulárně cílených léků indikovaných pro vybrané skupiny pacientů se specifickými molekulárními změnami na úrovni DNA nádoru napříč různými typy nádorů. Cílená terapie slibuje být bezpečnější a účinnější.
MUDr. Jan Špaček1
prof. MUDr. Luboš Petruželka, CSc.2
1 Onkologická klinika 1. LF UK a VFN Praha, Onkologická klinika
2 Ústřední vojenská nemocnice - Vojenská fakultní nemocnice Praha
Systémová léčba zhoubných nádorů aktuálně prochází zásadní změnou. Odklání se od paradigmatu, v němž se histopatologicky definovaná onemocnění léčí v první řadě cytostatiky, a směřuje k použití molekulárně cílených léků indikovaných pro vybrané skupiny pacientů se specifickými molekulárními změnami na úrovni DNA nádoru napříč různými typy nádorů. Cílená terapie slibuje být bezpečnější a účinnější.
Pro cílenou individualizovanou terapií zhoubných nádorů jsou ovšem zapotřebí komplexní diagnostické přístupy, které pomohou každému pacientovi přiřadit specifickou terapii. Tyto prediktivní diagnostické postupy zvyšují nároky na optimalizaci a analytickou validaci testů, které analyzují miliony bází DNA nádoru změněných nesčetnými mechanismy. Kvůli molekulární heterogenitě nádorového onemocnění a interindividuální heterogenitě se zdá být pro pacienta velmi výhodné genetické profilování, které by mělo predikovat odpověď na molekulárně cílenou terapii.
Pacient narozený v roce 1947 trpěl od září roku 2017 na opakované žlučové koliky, které se objevovaly stále častěji. Stran osobních anamnestických údajů se jedná o kardiaka, který se anamnesticky léčil na vředovou gastroduodenální chorobu, jinak nikdy vážněji nestonal, dlouhodobě se neléčil a neužíval žádnou chronickou medikaci. Je nekuřák a alkohol pije příležitostně.
V říjnu roku 2017 se u něj objevil obstrukční ikterus a dle vyšetření pomocí ERCP byla potvrzena tumorózní stenóza v oblasti ductus choledochus. Následně proběhla opakovaná výměna biliárních stentů. Během listopadu 2017 byla v Institutu klinické a experimentální medicíny (IKEM) v Praze provedena resekce extrahepatálních žlučových cest s následnou bihepatikojejunoanastomózou. Nález však byl radikálně neoperabilní a skončil neradikální (R1) resekcí.
Dle pooperačního PET/CT nálezu byl zobrazen lokálně mírně zvýšený metabolismus glukózy v centru jater vedle proximálního konce zavedeného stentu, kde nešlo rozhodnout, zda se jedná o zánětlivou iritaci po ERCP, či neoplazii s nízkým metabolismem glukózy; jinde byl nález bez suspektních ložisek. Histologicky se jednalo o středně diferencovaný cholangiogenní adenokarcinom se známkami perineurální propagace a morfologicky byl hodnocen jako Klatskinův tumor pT2pN0M0, stadium 1B.
Následně byl pacient odeslán na Onkologickou kliniku 1. LF UK a VFN k zahájení paliativní chemoterapie. Na lůžkovém oddělení absolvoval 6 cyklů podání cisplatiny s gemcitabinem, tato terapie byla ukončena dne 19. 6. 2018. Kontrolní, restagingové PET/CT z 12. 7. 2018 bylo negativní. Vzhledem k R1 resekci byla indikovaná ještě adjuvantní radioterapie rizikové oblasti podjaterní krajiny v dávce 45 Gy (25× 1,8 Gy), kterou pacient absolvoval ve dnech 26. 7. – 30. 8. 2018.
Na kontrolním CT provedeném 6. 10. 2018 byla zobrazena lokální progrese postižení jaterního hilu s v. s. karcinomatózou peritonea. Nádorové markery zůstávaly stále negativní a klinický stav pacienta byl velmi dobrý. Proto se přistoupilo k strategii watch and wait. Vzhledem k dobrému výkonnostnímu stavu pacienta bylo provedeno další kontrolní CT s odstupem 2 měsíců v prosinci 2018 se stacionárním nálezem. Pacienta tedy dále sledujeme ambulantně a další restagingové CT je objednáno na květen 2019.
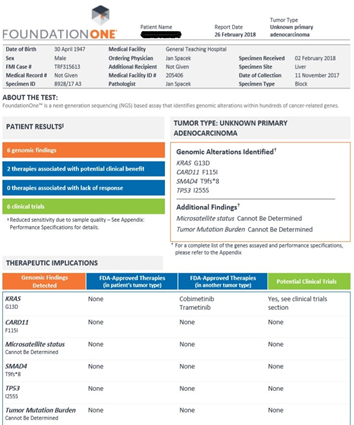
Před zahájením systémové terapie byl vzorek z resekátu extrahepatálních žlučových cest odeslán na vyšetření solidní biopsie FoundationOne s výsledkem 6 genomických alterací, z nichž 2 by bylo možné terapeuticky ovlivnit. Pokud by pacient při případné progresi lokálního nálezu nebyl z důvodu interních komorbidit či jiných komplikací schopný absolvovat chemoterapii (FOLFOX, kapecitabin), nabízela by se cílená terapie indikovaná na základě příslušného vyšetření.
Obr. 1 Výsledky a terapeutické možnosti u onkologického pacienta