-
Články
Top novinky
Reklama- Vzdělávání
- Časopisy
- Témata
Top novinky
Reklama- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Volná místa
Doporučené pozice
Reklama- Praxe
Top novinky
ReklamaProblematika vlivu antiresorptivní léčby osteoporózy na výskyt osteonekrózy čelisti
Datum publikace: 20. 9. 2015
Souhrn:
Osteoporóza je nejčastější metabolickou osteopatií s výrazným nárůstem incidence v posledních letech. V léčbě osteopatií jsou v dnešní době nejrozšířenější skupinou antiresorptivní/antiremodelační léky (bisfosfonáty, denosumab). I přes nesporný a významný přínos těchto preparátů pro pacienty s osteopatiemi má tato léková skupina i svá úskalí. K nežádoucím účinkům patří i riziko rozvoje osteonekrózy čelisti (ONJ). Tato stomatologická komplikace se relativně často vyskytuje při parenterální léčbě vysokými dávkami bisfosfonátů nebo denosumabu z indikace maligních onemocnění spojených s vysokou osteoresorpcí a hyperkalcémií. Toto sdělení poukazuje na riziko rozvoje této komplikace i po podání antiresorptivních léků při léčbě osteoporózy, byť je toto riziko výrazně nižší než u onkologických pacientů.
Etiologie vzniku ONJ jako komplikace antiresorptivní léčby zatím není uspokojivě vysvětlena. Epidemiologická data zatím postrádají větší soubory hodnocené metodikou Medicíny založené na důkazech (EBM). Nicméně komise odborníků (např. Americká asociace pro ústní a maxillofaciální chirurgii - AAOMS) zpracovávají podrobná doporučení pro diagnostiku, prevenci a léčbu této stomatologické komplikace.
Klíčová slova: osteoporóza, osteonekróza čelisti, antiresorptivní/antiremodelační medikace, bisfosfonáty, denosumab, AAOMS.
Úvod:
V současné době se mluví o osteoporóze jako o pandemii 21. století. Jedná se o významnou zdravotní komplikaci zejména stárnoucí populace. Zatěžuje zdraví pacientů svými následky a komplikacemi včetně zvýšené mortality a také společnost nárůstem přímých i nepřímých nákladů na péči o tyto pacienty. Spolu s prodlužujícím se věkem našich pacientů vidíme i nárůst komorbidit a rozličných rizikových faktorů, které zvyšují rizika komplikací léčby osteopatií.
Antiresorptivním preparátům používaným k léčbě metabolických osteopatií, převážně osteoporózy, již dlouho dobu dominují léčiva ze skupiny bisfosfonátů (BF), ke kterým se v posledních letech přidružila biologická léčba reprezentovaná denosumabem.
Poškození čelisti v důsledku užívání BF je relativně známou a podrobně popisovanou komplikací této léčby u maligních onemocnění - zejména u léčby malignitami indukované hyperkalcémie, kostních metastáz solidních tumorů (karcinom prsu, prostaty a plic) a osteolytických ložisek při mnohočetném myelomu. V těchto indikacích se používají pouze intravenózní (i. v.) formy BF a jejich dávkování je odlišné od schémat při léčbě osteoporózy (tab. 1). V poslední době však přibývá informací o výskytu ONJ i při podávání perorálních (p. o.) BF v indikaci léčby osteoporózy (1). Výskyt ONJ byl zaznamenán i při léčbě denosumabem, a to jak v indikaci maligního onemocnění (karcinom prostaty s hormonální ablací), tak i při léčbě postmenopauzální osteoporózy (PMO) (2).
Tab. 1 - Rozdíly v dávkování antiresorptivních preparátů při léčbě PMO a maligních onemocnění

Tým uznávaných expertů vyhodnotil dostupná literární data z let 2003 až 2014, která pojednávají o incidenci, patofyziologii, diagnostice a léčbě ONJ, a vytvořil doporučení pro vznik multidisciplinárního mezinárodního konsenzu (19).
Klinický obraz ONJ a definice:
Osteonekróza čelisti je nozologická jednotka známá již téměř 150 let (7). Klinicky se projevuje jako obnažení části čelistní kosti trvající minimálně osm týdnů bez předchozí anamnézy radioterapie v oblasti orofaciální a krku (při vyloučení radionekrózy) (obr. 1). Další přidružené příznaky jsou: bolestivost, otok, viklavost zubů v ložisku nekrózy, možná ztráta dentice, kolemčelistní zánět, svalová kontraktura, krvácení z gingivy, charakteristický foetor ex ore daný purulentním exsudátem, možný vznik píštěle a obnažení kosti extraorálně (9).
Obr. 1: BRONJ v oblasti dolní čelisti - oblast 43

obrázek z archivu autora
Spojení s léčbou BF poprvé popsal v roce 2003 Marx et al. (3) – výskyt ONJ u pacientů léčených i. v. BF pro myelom či metastatické postižení skeletu. V roce 2004 Ruggiero et al. popsal 63 kazuistik pacientů s ONJ, z nichž 7 bylo léčeno p. o. alendronátem (4).
Definice ONJ asociované s antiresorptivní léčbou (BF) dle ASBMR vychází z klinického obrazu – oblast obnažené kosti v maxilofaciální oblasti nehojící se 8 týdnů od identifikace stomatologem u pacienta, který užívá léčbu BF a nebyl vystaven radioterapii kraniofaciální oblasti (19). Americká asociace ústní a obličejové chirurgie (American Association of Oral and Maxillofacial Surgeons – AAOMS) revidovala tuto definici na ONJ související s léčbou a rozdělila ji do 3 bodů – 1) současná nebo předchozí léčba antiresorptivním preparátem nebo léčivem inhibujícím angioneogenezi, 2) obnažená kost nebo extraorální či intraorální píštěl v maxilofaciální oblasti perzistující déle jak 8 týdnů, 3) absence radioterapie v kraniofaciální oblasti a absence kostních čelistních metastáz (19).
The International Task Force on Osteonecrosis of the Jaw (Task Force) definuje ONJ podobně jako AAOMS. Tato iniciativa plánuje shromáždit více informací ohledně rizika vzniku ONJ u léčiv inhibujících angioneogenezi bez konkomitantní medikace BF. Dále se blíže zabývá výskytem ústních ulcerací a kostních sekvestrací. Tyto komplikace se vyskytují i u běžné populace, ale jejich incidence není dobře definována. Jejich výskyt by mohl být lépe dokumentován na základě registrů pro léčivy indukovanou ONJ (19,20).
Rizikové faktory:
Rizikové faktory rozvoje ONJ jsou podrobně popsány AAOMS. Jsou vztaženy převážně k léčbě BF - BRONJ (Bisphosphonate-Related Osteonecrosis of the Jaws) - update z roku 2009 (5). Následující update z roku 2014 již hovoří o osteonekróze čelisti související s léčbou (Medication-Related Osteonecrosis of the Jaw - MRONJ) (6).
Dle AAOMS lze rizikové faktory rozdělit do 3 skupin:
- Související s typem podávaného léčiva
- Lokální rizikové faktory
- Systémové rizikové faktory
Ad 1) Vliv podávaného léčiva úzce souvisí s teoriemi vzniku MRONJ. Důležitý je nejen typ léčiva, ale i indikace jeho podání - zda se jedná o osteoporózu, či o osteopatii spojenou s malignitami. S tím souvisí dávkování daného léčiva. Riziko rozvoje ONJ u pacientů užívajících kyselinu zoledronovou z maligní indikace je 50 - 100x vyšší než u pacientů s malignitou bez této léčby. Riziko ONJ u pacientů s malignitou při užívání denosumabu je obdobně zvýšené jako u kyseliny zoledronové. U pacientů užívajících antiresorptivní léčbu z indikace osteoporózy je toto riziko v porovnání s malignitami zhruba 100x nižší (6). Mezi riziková léčiva pro rozvoj MRONJ dnes řadíme antiresorptivní preparáty - intravenózní a perorální BF, RANK ligand inhibitory (denosumab) a inhibitory angioneogeneze. Posledně zmiňovaná léčiva interferují s angioneogenezou ovlivněním signálních molekul a narušením signální kaskády pro neoangiogenezu. Jejich terapeutické využití je např. v léčbě gastrointestinálních tumorů, světlobuněčného karcinomu ledviny a neuroendokrinních tumorů. Blíže se zaměříme na negativní vliv antiresorptivní léčby. Patofyziologie vzniku MRONJ dodnes není uspokojivě vysvětlena. Existuje sice množství hypotéz, ale validních dat, opírajících se o větší soubory pacientů, je zatím velice málo. Základním předpokladem negativního vlivu BF a denosumabu je ovlivnění kostní remodelace. Inhibice osteoklastické resorpce negativně ovlivňuje i funkčnost osteoblastů a osteocytů. Tento efekt probíhá u všech léčených pacientů v celém skeletu, ovšem ONJ se rozvíjí pouze u některých jedinců a převážně v oblasti maxilly a mandibuly. Dominantní se zdá být významná akumulace BF v čelistních kostech vzhledem k jejich intenzivnějšímu metabolismu – rychlejší remodelace vlivem žvýkání, z čehož vyplývá i větší kumulace BF. Při omezení remodelace pak následkem žvýkání může docházet ke kumulaci mikrofraktur (7,8). Zpomalení osteoklastické resorpce poškozené/nekrotické kosti zpomaluje proces hojení, a tím pádem se zvyšuje riziko bakteriální infekce. Dochází ke stimulaci prozánětlivých interleukinů a zřejmě i k negativnímu ovlivnění celé řady dalších buněk - epiteliálních slizničních buněk, buněk cévního endotelu (1). S tím souvisí poškozená epitelizace a poškození slizničního krytu, který se pak stává významnou cestou pro průnik mikroorganismů do kosti. Vznikají nehojící se slizniční defekty. Nemalý podíl může mít i případná toxicita chemoterapie a další léčiva, která mohou snižovat kvalitu slizničního krytu dutiny ústní (imunosupresiva, kortikosteroidy, cytostatika) (7,8). Výskyt ONJ byl pozorován u všech dostupných aminobisfosfonátů používaných při léčbě osteoporózy. Důležitý je nejenom výběr preparátu (síla vazby na kostní minerál, kumulativní potenciál BF, antiremodelační potenciál), ale také délka podávání - kumulativní dávka. Dle dostupných údajů riziko rozvoje ONJ a riziko výraznějšího poškození čelisti narůstá po 3. roce užívání BF (9, graf 1).
Graf 1: Prevalence ONJ v závislosti na trvání BF terapie (dle FDA - Background Document for Meeting of Advisory Committee for Reproductive Health Drugs and Drug Safety and Risk Management Advisory Committee, 2011)
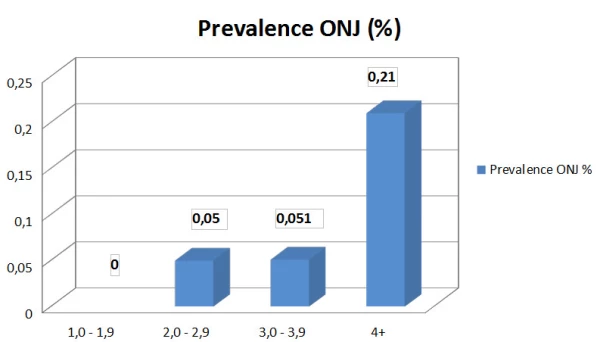
Trvání terapie p. o. BF (roky)
Není překvapením, že u většiny popisovaných případů ONJ u pacientů léčených BF nebo denosumabem byly velice nízké hodnoty markerů kostního obratu. Vztaženo k C-terminálnímu telopeptidu kolagenu typu I (CTX) byla ONJ manifestována zejména u pacientů s hodnotou nižší než 0,15 ng/ml. V práci Marxe et al (1) byla navržena stratifikace rizika dle hodnoty CTX - vysoké riziko pro hodnoty nižší než 0,1 ng/ml, střední riziko pro hodnoty 0,1-0,15 ng/ml a hodnoty nad 0,15 ng/ml s minimálním rizikem. V aktuálnější práci Baima - Millera (10) byl však význam stratifikace CTX zpochybněn, autoři jsou k prediktivnímu významu CTX skeptičtí. Existuje značná variabilita měření markerů kostního obratu (BTM). Nejsou standardizovány referenční meze pro CTX, existuje značná mezilaboratorní variabilita a nekonzistentnost, nejsou žádné větší soubory dat podpořené EBM. V současnosti lze pomocí BTM monitorovat účinnost léčby BF, ovšem v predikci rizika MRONJ hrají zatím jen podpůrnou a doplňující úlohu. Nejednoznačné se zdá i ovlivnění angioneogeneze při léčbě BF. Dostatečná a kvalitní vaskularizace čelistních kostí je velice důležitá pro hojení stomatologických defektů (trauma, extrakce, implantáty apod.). Velice potentní BF (kyselina zoledronová) negativně ovlivňuje angiogenezi a může zpomalovat procesy hojení stomatologických výkonů. Ovšem nejsou k dispozici žádná statisticky významná data, která by potvrdila vztah mezi ovlivněním angiogeneze a rozvojem ONJ (9).
Ad 2) Lokální rizikové faktory velice úzce souvisí se zákroky v dutině ústní a rizikem průniku mikrobiální flory ke kostnímu povrchu. Řadíme sem tudíž veškerou dentoalveolární operativu (zubní extrakce, dentální implantáty, operativa parodontopatií, orofaciální traumata apod.) - mnoho studií dokládá, že zubní extrakce se na rozvoji MRONJ podílí v 52 - 61 %. Odhaduje se, že u zubních implantátů a patologií parodontu je riziko obdobné. Bohužel, konzistentní data existují pouze u pacientů s malignitami (6). Rizikové jsou i zlomeniny čelistních kostí. Uvádí se, že každá zlomenina čelisti procházející zubním lůžkem je považována za otevřenou (9).
Anatomické rizikové faktory jsou zatím nedostatečně zmapovány. V oblasti mandibuly je výskyt ONJ častější (73 %) než v oblasti maxilly (22,5 %). V obou čelistech se vyskytuje zhruba ve 4,5 % (6). Dalším faktorem je i tloušťka sliznice alveolárního výběžku s minimem podslizničního vaziva. Tento slizniční kryt je dennodenně mechanicky namáhán při žvýkání, a to i u bezzubých pacientů. Jsou zaznamenány případy rozvoje ONJ u pacientů se špatně padnoucí zubní protézou a vznikem dekubitálního defektu v místě namáhaného slizničního krytu.
Je otázkou, zda spíše rozvoj ONJ (kolemčelistního zánětu, parodontopatie) není často indikací k zubní extrakci, než že by sama zubní extrakce ve zdravé kosti způsobila rozvoj ONJ (9).
Velice důležitá je otázka ústní hygieny. Nesanovaný chrup, zubní kámen, nevhodné čištění chrupu a nevhodné hygienické pomůcky poškozující parodont mohou být příčinou rozvoje MRONJ.
Ad 3) Ze systémových rizikových faktorů je třeba zmínit na prvním místě věk a pohlaví a také rasu. Starší populace je rizikovější. Ženy jsou postiženy více než muži, což souvisí zcela jistě s indikací podání BF (převaha osteopatií - PMO, karcinom prsu atd.). Riziková je i bílá rasa (caucasian). Výskyt v dětské populaci není popisován (11).
Z rizikové medikace je třeba jmenovat na prvním místě systémovou léčbu kortikosteroidy, dále léky inhibující angiogenezu, imunosupresiva, cytostatika.
Mezi rizikové komorbidity patří anémie (hemoglobin pod 100 g/dl), thalasémie, diabetes mellitus a obezita, chronická obstruktivní plicní nemoc, malignity, imunodeficity (včetně HIV), hypokalcémie a sekundární hyperparatyreóza a terminální stádium onemocnění ledvin vyžadují dialyzační péči. Tento výčet se podílí na zvýšení rizika MRONJ zejména u pacientů s malignitami, ovšem tyto komorbidity zvyšují riziko i u pacientů s osteoporózou. Další přidružené nemoci, jako je hypertenze, hyperlipoproteinémie/hypercholesterolémie a revmatoidní artritida se zřejmě mohou podílet na zvýšení rizika MRONJ u pacientů užívajících BF z nemaligních indikací (13).
Rizikové je kouření - jsou data o signifikantním nárůstu ONJ u pacientů s malignitami (15).
V současnosti se zkoumají i genetické faktory pro rozvoj ONJ. Genový polymorfismus ovlivňující aktivitu farnesyl-difosfát syntázy pozitivně koreluje se zvýšených rizikem rozvoje ONJ. Zdá se, že může existovat určitá zvýšená senzitivita na léčbu BF (6). Gen pro matrix metaloproteinazu 2 je dalším kandidátem zvyšujícím riziko BRONJ (12).
Kolektiv autorů (19) hodnotící práce zabývající se ONJ z let 2003-2014 vyzdvihuje následující faktory důležité pro patofyziologii ONJ – antiresorptivní efekt BF a denosumabu, efekt BF na gamma delta T-buňky a ovlivnění funkce monocytů a makrofágů, lokální bakteriální infekci, zánět a nekrózu. Další rizikové faktory, které popisuje pracovní skupina pro mezinárodní konsenzus, jsou – glukokortikoidní terapie, maxilární a mandibulární kostní chirurgie, špatná ústní hygiena, chronický zánět, diabetes mellitus, špatně sedící zubní protéza, další léčiva ovlivňující buněčné funkce včetně inhibitorů angioneogeneze (19).
Diagnostika a klasifikace (6) :
Při podezření na MRONJ se vychází z klinického obrazu, lékové anamnézy a zobrazovacích metod - rentgenový snímek (ortopantomogram - obr. 2) a CT vyšetření čelisti. Pokročilé zobrazovací metody zahrnují Cone beam CT (CBCT) hodnotící kortikální a trabekulární kost, kostní scintigrafii, magnetickou rezonanci (NMR) a pozitronovou emisní tomografii (PET).
Obr. 2: Ortopantomogram BRONJ dolní čelisti - oblast 43
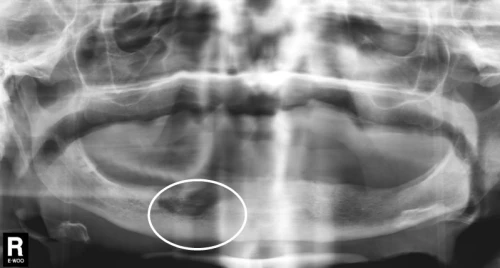
obrázek z archivu autora
Dle klasifikace AAOMS defekty dělíme do kvadrantů - pravý a levý, horní a dolní - a stanoví se stádium onemocnění. Rizikový pacient je každý, kdo užívá antiresorptivní/antiremodelační medikaci - BF, denosumab.
Stádium 0 - pacient bez klinické manifestace ONJ vykazující nespecifické symptomy, popř. který má klinické či radiologické nálezy.
Mezi symptomy patří - odontoalgie bez zjevné odontogenní příčiny
- tupá, pulzující bolest těla mandibuly vyzařující do temporomandibulárního skloubení
- bolesti v oblasti dutin, které mohou být spojeny se zánětem a ztluštěním stěny maxillární dutiny
- alterované neurosenzorické funkce
Klinické nálezy - ztráta dentice, která není spojena s chronickým parodontálním onemocněním
- periapikální/parodontální píštěl, která není asociována s nekrózou pulpy v důsledku kazu
Radiologické nálezy - alveolární kostní ztráta nebo resorpce, kterou nelze přičíst chronickému onemocnění parodontu
- změny trabekulární kosti a perzistence neremodelované kosti v okolí extrakčního lůžka
- oblasti osteosklerózy zahrnující alveolární kost a/nebo okolí bazilární kosti
- zesílení/zastření periodontálního ligamenta (zesílení lamina dura a snížení velikosti prostoru periodontálního ligamenta)
Stádium 1 - exponovaná a nekrotická kost nebo píštěl zasahující do kosti u asymptomatického pacienta bez známek infekce. Radiologický nález může být obdobný jako u stádia 0 v oblasti alveolární kosti.
Stádium 2 - exponovaná a nekrotická kost nebo píštěl zasahující do kosti se známkami infekce u symptomatického pacienta. Radiologický nález může být obdobný jako u stádia 0 v oblasti alveolární kosti.
Stádium 3 - exponovaná a nekrotická kost nebo píštěl zasahující do kosti se známkami infekce u symptomatického pacienta a jeden či více následujících příznaků - exponovaná nekrotická kost přesahující oblast alveolární kosti
- patologická zlomenina
- extraorální píštěl
- orálně-antrální/orálně-nasální komunikace
- osteolýza dolní čelisti, maxilární sinusitida
Doporučení pro identifikaci a monitoraci ONJ (19):
- pacienti s nízkou dávkou antiresorptivní medikace bez známek a příznaků ONJ – běžná stomatologická péče bez nutnosti zobrazovacích metod.
- pacienti na vysokých dávkách antiresorptivní medikace bez známek ONJ mající signifikantně zvýšené riziko rozvoje ONJ – důraz kladen na časnou identifikaci komplikací – kompletní vyšetření ústní dutiny, ideálně s ortopantomogramem stávající dentice. CT vyšetření (CBCT) v případě podezření na ONJ.
- pacienti vykazující známky ONJ (na nízkých či vysokých dávkách antiresorptivní medikace) – CT (CBCT) pro diagnostiku časných změn kortikální a trabekulární kosti čelistí. Diagnostika možných kostních sekvestrů a píštělí. Preference HR CBCT před klasickým CT vyšetřením – stejná výtěžnost při nižší dávce radiace. CBCT vyšetření může být doplněno panoramatickým RTG snímkem. Doplňující informace může poskytnout NMR.
- pacienti s rozvinutou ONJ léčeni konzervativně (stádia 1 a 2) – diagnostika kostních změn pomocí HR CBCT s doplněním panoramatického snímku stávající dentice.
- pacienti s rozvinutou ONJ léčeni stomatochirurgickou intervencí (stádia 2 a 3) – CBCT nebo CT doplněné NMR, scintigrafií skeletu, popřípadě PET pro monitoraci kostních změn a změn měkkých tkání.
Epidemiologie:
Zkušenosti s léčbou osteopatií bisfosfonáty jsou letité. Jen v České republice jsou k dispozici od roku 1996. První zmínky o výskytu BRONJ u maligních onemocnění a posléze i u léčby p. o. BF jsou již z roku 2003, resp. 2004 (3,4). Ovšem teprve od roku 2011 se užívá jednotná a správná terminologie dle Mezinárodní klasifikace nemocí (MKN) (9). Nejvíce propracovaná a široce používaná diagnostická kritéria a terapeutické postupy dle AAOMS se používají od roku 2007 s nejnovější aktualizací z roku 2014. Ovšem výsledky sledování incidence BRONJ z národních registrů a různých populačních studií v různých zemích se výrazně liší (Německo, USA, Kanada) - neexistují jednotná kritéria, jednotná stratifikace pacientů a nemocní v registrech jistě nereprezentují všechny pacienty s výskytem MRONJ.
Práce věnující se problematice MRONJ jsou uvedeny v tab. 2 a 3. Z přehledu je patrné, že oproti výskytu MRONJ u pacientů s malignitami je incidence u pacientů s osteoporózou relativně nízká. Dalším zdrojem informací je celá řada kazuistických sdělení.
Tab. 2 - Přehled výskytu MRONJ v jednotlivých klinických sledování ch u pacientů s malignitami, převzato z update AAOMS 2014

SR - systematic review
PCS - prospective cohort study
CS - cross-sectional (průřezová studie)
RCT - randomizovaná, dvojitě zaslepená, placebem kontrolovaná, multicentrická studie
Tab. 3 - Přehled výskytu MRONJ v jednotlivých klinických sledováních u pacientů s osteoporózou, převzato z update AAOMS 2014
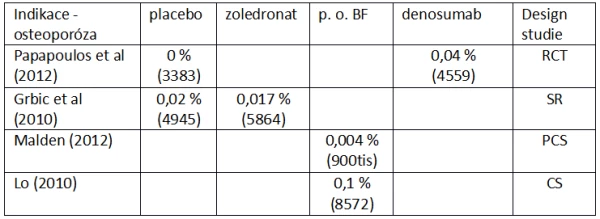
SR - systematic review
PCS - prospective cohort study
CS - cross-sectional (průřezová studie)
RCT - randomizovaná, dvojitě zaslepená, placebem kontrolovaná, multicentrická studie
Incidence ONJ u onkologických pacientů je uváděna od 1 % do 15 %. U pacientů s osteoporózou je incidence této komplikace odhadována na 0,001 % až 0,01 %, což je mírně zvýšené oproti výskytu v běžné populaci (odhad <0,001 %) (19).
Vzhledem k existujícímu riziku této komplikace se dnes v klinických studiích s antiresorptivními preparáty incidenci MRONJ věnuje náležitá pozornost.
Výskytu MRONJ při léčbě denosumabem se věnovala klinická studie FREEDOM, kde tříletá placebem kontrolovaná fáze byla prodloužena na celkové trvání deseti let. Přičemž všechny pacientky jsou v letech 4 - 10 léčeny denosumabem 60 mg s. c. 1x za 0,5 roku. Dle publikovaných dat bylo identifikováno 8 případů výskytu MRONJ - 3 byly ze skupiny denosumabu de novo, 5 případů z kontinuální skupiny (2). Nutno podotknout, že se jedná o vzácný nežádoucí účinek.
Obecně je nutné si uvědomit, že data z velkých farmakologických studií, designovaných dle zásad EBM, nejsou 100% aplikovatelná na běžnou populaci v klinické praxi, neboť výběr vhodných pacientů je zatížen množstvím vylučovacích kritérií, a tudíž se jedná o tzv. „skleníkové“ pacienty, kterých je v běžné klinické praxi menšina. Validnější data by mohly poskytovat národní registry. Toto téma bylo prezentováno v rámci kongresu Sekundární osteoporóza v Plzni 2014. Registr BRONJ v rámci FN Ostrava je zatím v počátcích své existence. Do budoucna by bylo zapotřebí velice úzké spolupráce nejenom lékařů, kteří se léčbou BRONJ zabývají, ale i osteologů, kteří tuto komplikaci své léčby zaznamenají.
Problémem pro stanovení rizika pro jednotlivé antiresorptivní preparáty mohou být i změny této medikace (např. změna typu BF, přechod z BF na denosumab apod.) během léčby konkrétního pacienta (14).
Vlastní zkušenosti:
V našem Osteologickém centru jsme doposud zaznamenali 8 případů osteonekrózy čelisti asociované s p. o. léčbou BF.
Pacientka C. M. (1944) - expozice BF přes 3 roky (ibandronát), glukokortikoidy v rámci roztroušené sklerózy, kardiačka, hypertonička. Suprimovaný kostní obrat (CTX 0,027 ng/ml, osteokalcin < 2 ng/ml), vitamin D 62 nmol/l.
Defekt v dutině ústní vznikl otlakem dásně zubní protézou.
Pacientka H. A. (1923) - BF přes 7 let (alendronát), vysoký věk, kardiačka, hypertonička, dyslipidémie, hypotyreóza. Snížený kostní obrat (CTX 0,165 ng/ml, osteokalcin 2,5 ng/ml).
Nekróza se rozvinula po otlaku snímatelnou zubní protézou.
Pacientka H. D. (1932) - 2,5 roku raloxifen, poté přes 6 let BF (risedronát, alendronát, ibandronát), vysoký věk, letitá léčba glukokortikoidy (astma bronch.), diabetes mellitus, hypertenze a ischemická choroba srdeční (ICHS).
Snížený kostní obrat (CTX 0,19 ng/ml, osteokalcin < 2 ng/ml), vitamin D 13,8 nmol/l.
Defekt v čelisti se rozvinul po extrakci zubu.
Pacientka K. M. (1930) - kalcitonin 0,5 roku, BF 7 let (risedronát, ibandronát), vysoký věk, letitá medikace glukokortikoidy v rámci revmatoidní artritidy, anémie, dyslipidémie. Kostní obrat snížený (CTX 0,193 ng/ml, osteokalcin < 2 ng/ml), vitamin D 30 nmol/l.
Defekt čelisti se rozvinul po odstranění 5 zubů.
Pacientka B. M. (1939) - raloxifen 6 let, BF 4 roky (ibandronát), ICHS, kortikodependentní revmatoidní artritida, chronická léčba warfarinem, suprimovaný kostní obrat (CTX 0,142 ng/ml, osteokalcin < 2 ng/ml), vitamin D 17,8 nmol/l.
Defekt čelisti se rozvinul po extrakci 2 zubů.
Pacientka K. M. (1938) - BF 6,5 roku (risedronát, alendronát, ibandronát), polymorbidita (diabetes, hypertenze, dyslipidémie, kardiomyopatie, warfarinizace, chronická renální insuficience), kostní obrat přiměřený (CTX 0,249 ng/ml, osteokalcin 3,95 ng/ml), vitamin D 143 nmol/l.
Defekt čelisti se rozvinul po extrakci 4 zubů, následovalo odloučení implantátu z dolní čelisti.
Pacientka H. M. (1948) - BF 7 let (alendronát, ibandronát), bez rizikových komorbidit, přiměřený kostní obrat (CTX 0,529 ng/ml, osteokalcin 4,66 ng/ml), vitamin D 43,6 nmol/l.
Rozvoj ONJ v rámci akutní exacerbace chronické periodontitis s extrakcí 2 zubů.
Pacientka L. M. (1935) - BF 4 roky (ibandronát), polymorbidita (preterminální stádium CHRI, hypertenze, dyslipidémie, anémie), kostní obrat přiměřený (CTX 0,391 ng/ml, osteokalcin 5,21 ng/ml - nevalidní vzhledem ke stupni CHRI).
Rozvoj ONJ s odstupem 2 měsíců po mnohočetné extrakci zubů otlakem nové snímatelné protézy.
U většiny našich pacientek jsme zaznamenali různou míru suprese kostního obratu (hodnoceno jak dle CTX, tak i podle osteokalcinu), suprese byla patrná zejména oproti vstupním hodnotám (v textu neuvedeno). Dále deficitní hladiny vitaminu D (negativní vliv na rozvoj ONJ není opřen o data z literatury, je to spíše charakteristika sledované populace), vyšší věk a dlouhodobou expozici BF. U všech pacientek jsme zaznamenali invazivní stomatologický zákrok nebo mechanickou iritaci sliznice dutiny ústní.
Preventivní opatření z pohledu osteologa:
Základním opatřením nutným ke snížení rizika rozvoje MRONJ je úzká spolupráce osteologa (či jiného specialisty) indikujícího antiresorptivní léčbu a stomatologa. Lékař indikující antiresorptivní medikaci musí znát její rizika a musí individuálně vyhodnotit u každého pacienta výskyt rizikových faktorů rozvoje ONJ. Je nezbytně nutné rozšířit odběr anamnézy i o stomatologickou problematiku - stav chrupu, kazivost, onemocnění parodontu, aktuální stomatochirurgické zákroky (implantáty, resekční zákroky), zubní extrakce, úrazy čelisti, stav protetiky, infekce dutiny ústní apod. V případě hrozících zubních výkonů či plánovaných stomatologických kontrol u problematického chrupu odložit nastavení antiresorptivní medikace do vyřešení stomatologických potíží. V případě zahájení léčby BF/denosumabem zhodnotit v písemné formě riziko případného rozvoje ONJ. Informovat pacienta o nutnosti uvedení této léčby při každé zubní prohlídce či před stomatologickým zákrokem s odkazem na spolupráci s indikujícím osteologickým pracovištěm kvůli zvážení managementu stomatologického zákroku a případné úpravy osteologické medikace.
Řada prací prokázala (Dimopoulos, Bonacina, Vandone - studie u onkologických pacientů), že preventivní ošetření chrupu a kontrola stavu ústní dutiny před nasazením i. v. antiresorptivní léčby významně snižuje riziko ONJ (6).
Nezbytně nutná je edukace pacienta stran důkladné ústní hygieny (nejlépe stomatologickým pracovníkem) a vyžadování preventivních stomatologických kontrol, zejména u rizikové populace.
Problém tzv. „drug holiday“ u pacientů s již nastavenou léčbou BF nebo denosumabem s plánovaným stomatologickým výkonem není zatím uspokojivě vyřešen. Chybí propracovanější data, která by toto doporučení podpořila. AAOMS dle update 2009 doporučuje 3 měsíce před a 3 měsíce po zákroku neužívat antiresorptivní léčbu. Neexistuje ale žádný důkaz, který by prokázal snížení rizika rozvoje ONJ po vysazení této léčby. V roce 2011 došlo k revizi doporučených postupů a bylo navrženo, že u pacientů s nižší kumulativní dávkou BF a krátkodobým užíváním denosumabu (do 2 let užívání) není nutno tuto léčbu vysazovat při invazivních stomatologických zákrocích. Lékové prázdniny jsou doporučovány u pacientů s vyšším rizikem rozvoje ONJ, delší expozicí antiresorptivní léčby (nad 4 roky) a rizikovými chorobami (revmatoidní artritida, předchozí či současná léčba glukokortikoidy, diabetes mellitus a kouření). Léčba by měla být vysazena do plného zhojení invazivního zákroku (16). V roce 2011 při hodnocení dlouhodobé bezpečnosti BF při léčbě osteoporózy FDA rozhodla, že „neexistují žádná spolehlivá data ohledně návodu pro zahájení a délku trvání lékových prázdnin“ (17).
Damm a Jones navrhli několik alternativ „drug holiday“ u pacientů na BF vyžadujících invazivní zubní zákrok. Nejsou zatím k dispozici žádné studie podporující jejich závěry. Autoři vycházejí z farmakokinetiky BF a fyziologie kosti - více jak 50 % sérové koncentrace BF je vyloučeno ledvinami, hlavním rezervoárem je kost - osteoklast, jehož životnost jsou 2 týdny. Odvozují, že po cca 2 měsících od poslední dávky p. o. BF jsou sérové hladiny velice nízké, a tudíž by dvouměsíční přerušení léčby před invazivním zákrokem mělo být dostatečné pro snížení rizika ONJ (18).
AAOMS se tudíž domnívá, že byť neexistují konzistentní data ohledně vysazování antiresorptivní medikace před stomatologickou invazivní péčí, je na místě obezřetnost, důraz je kladen na, byť teoretický, benefit pro pacienta, a jsou tudíž podporována doporučení vycházející z práce Damma a Jonese - u pacientů rizikových pro rozvoj ONJ užívajících léčbu více jak 4 roky je vhodné tuto léčbu 2 měsíce před výkonem přerušit a další opětovné nasazení BF provézt až po úplném zhojení ústního defektu (6).
Naproti tomu v doporučeních Americké stomatologické asociace je poukazováno na velice nízké riziko ONJ u pacientů užívajících antiresorptivní medikaci z důvodu léčby osteoporózy, a tudíž přerušení léčby před stomatoinvazivním zákrokem nedoporučují.
Velice zajímavá je epidemiologická dotazníková práce japonských autorů (21), která poukazuje na všeobecně špatnou kooperaci mezi stomatology a jinými lékařskými specializacemi. Autoři poukazují na fakt, že při přerušení antiresorptivní léčby (BF, denosumab) narůstá incidence fraktur a zvyšuje se výrazně riziko ukončení antiporotické léčby ze strany pacienta bez vlivu na snížení rizika rozvoje ONJ.
U léčby s prodlouženým dávkovacím schématem, kdy není možné pro akutní stomatologický výkon vyčkat na přerušení léčby (zoledronát, i. v. ibandronát, denosumab) musí být na riziko rozvoje ONJ brán zřetel a tomu musí odpovídat i stomatologická akutní a následná péče (rozsah výkonu, antibiotické krytí, častější kontroly defektu apod.). Zajištění antibiotickou clonou u rizikové populace by mělo být samozřejmostí.
Pokud jde o dentální implantáty, u onkologických pacientů na vysokých dávkách antiresorptivních léků tyto výkony nejsou doporučovány. U pacientů s osteoporózou by se mělo přihlédnout ke stupni kostní remodelace a v případě přílišné suprese zvolit „drug holiday“ a vyčkat s výkonem na vzestup kostních markerů osteoresorpce. Je třeba zmínit, že oproti BF, kdy depozice léku v kosti přetrvává dlouhodobě i po vysazení preparátu (v závislosti na síle vazby na kostní minerál), je u biologické léčby (denosumab, v experimentu např. odanacatib a protilátka proti sklerostinu - romosozumab) výhoda v rychlé reverzibilitě suprimovaného kostního obratu.
Shrnutí:
Naším cílem by měla být těsnější spolupráce osteologa a stomatologa a důkladná edukace všech pacientů užívajících antiresorptivní medikaci. Stomatologická anamnéza by se minimálně v této souvislosti měla stát nezbytnou součástí pacientovy zdravotnické dokumentace.
Každý pacient by měl být před nasazením BF/denosumabu poučen o možných rizicích spojených s touto léčbou. U rizikových pacientů (a před nasazením parenterálních forem medikace) by měla být doporučena minimálně stomatologická prohlídka, popř. sanace chrupu před nasazením léčby.
Důraz musí být kladen na dostatečnou ústní hygienu.
Pacient musí být poučen (ústně i písemně) o nutnosti informování stomatologa o užívání rizikové medikace (zejména před invazivním zákrokem).
U nemocných ve zvýšeném riziku rozvoje MRONJ se doporučuje šetrný výkon v antibiotické cloně.
V případě zjištění MRONJ stomatologem je nutné tuto skutečnost nahlásit příslušnému osteologovi a taktéž nahlásit příslušnému kontrolnímu úřadu (SÚKL) a nejlépe i registru ONJ.
Přerušení léčby před invazivním výkonem by se mělo posuzovat individuálně, vždy s ohledem na co největší benefit pro pacienta.
Závěr:
Osteonekróza čelisti indukovaná antiresorptivní/antiremodelační medikací osteoporózy je vážnou a bolestivou komplikací, která se může plně projevit u pacientů ve zvýšeném riziku (zejména rizikové komorbidity, riziková medikace, útlum kostní remodelace, dlouhodobá expozice BF/denosumabem, vysoký věk).
Oproti onkologickým pacientům užívajícím mnohem vyšší dávky léčby je u pacientů s osteoporózou výskyt ONJ poměrně vzácný a klinický obraz a průběh bývá méně dramatický. Z výše uvedeného vyplývá, že poměr risk/benefit antiresorptivní/antiremodelační léčby je pro osteoporotické pacienty příznivý. Nicméně je třeba naše klienty náležitě edukovat a snažit se o těsnější mezioborovou spolupráci, neboť tato komplikace může významně snižovat kvalitu života.
- Marx RE, Cillo JE Jr, Ulloa JJ. Oral bisphosphonate-induced osteonecrosis: risk factors, prediction of risk using serum treatment. CTX testing, prevention, and treat ment. J Oral Maxillofac Surg 2007; 65 (12): 2397–2410.
- Papapoulos S, Lippuner K, Roux C et al. Eight years of denosumab treatment in postmenopausal women with osteoporosis: results from the first five years of the FREEDOM extension. Poster presented at: American Society for Bone and Mineral Research 2013 Annual Meeting; October 4-7, 2013; Baltimore, MD, USA.
- Marx RE et al. Pamindronate (Aredia) and zoledronate (Zometa) induced avascular necrosis of jaw: a growing epidemic. J Oral Maxillofac Surg 2003; 1115–1117.
- Ruggiero SL et al. Osteonecrosis of the jaws associated with the use of bisphosphonates: a review of 63 cases. J Oral Maxillofac Surg 2004; 62 : 527–534.
- Ruggiero SL, Dodson TB, Assael LA, Marx RE et al. American Association of Oral and Maxillofacial Surgeons Position Paper on Bisphosphonate-Related Osteonecrosis of the Jaws—2009 Update, J Oral Maxillofac Surg 67 : 2-12, 2009, Suppl 1.
- Ruggiero SL, Dodson TB, Fantasia J, Goodday R et al. Medication-Related Osteonecrosis of the Jaw—2014 Update, Position Paper of AAOMS, 2014.
- Cvek J, Dvořáčková J, Gruna J, Hodan R. Osteonekróza čelistí u onkologicky nemocných. Remedia 2010; 10 : 338–342.
- Hodan R, Mendreková M, Cvek J, Gruna J. Prevence osteonekrózy čelisti před onkologickou léčbou. Onkologie 2009; 3(1): 62–65.
- Rosa J, Pavlíková G, Palička V. Osteonekróza čelisti u pacientů užívajících antiresorptivní léčbu osteoporozy. Osteo bulletin 2013, 18(3), 68-76.
- Baim S, Miller PD. Assessing the Clinical Utility of Serum CTX in Postmenopausal Osteoporosis and Its Use in Predicting Risk of Osteonecrosis of the Jaw, J Bone Miner Res 2009; 24 : 561–574.
- Brown JJ, Ramalingam L, Zacharin MR. Bisphosphonate-associated osteonecrosis of the jaw: does it occur in children? Clin Endocrinol (Oxf) 68 : 863, 2008.
- Lehrer S, Montazem Andre, Ramanathan Lakshmi et al. Bisphosphonate-induced osteonecrosis of the jaws, bone markers, and a hypothesized candidate gene. J Oral Maxillofac Surg 2009; 67(1): 159-161.
- Hess LM, Jeter JM, Benham-Hutchins M, Alberts DS. Factors associated with osteonecrosis of the jaw among bisphosphonate users. Am J Med 2008; 121 : 475-483.
- Rachner TD, Platzbecker U, Felsenberg D, Hofbauer LC. Osteonecrosis of the Jaw After Osteoporosis Therapy With Denosumab Following Long-term Bisphosphonate Therapy. Mayo Clin Proc 2013; 88(4): 418-419.
- Wessel JH, Dodson TB, Zavras AI. Zoledronate, smoking, and obesity are strong risk factors for osteonecrosis of the jaw: a case-control study. J Oral Maxillofac Surg 2008; 66 : 625-631.
- Khan AA, Morrison A, Hanley DA et al. International Consensus on Diagnosis and Management of Osteonecrosis of the Jaw. 2013 : 22.
- Background Document for Meeting of Advisory Committee for Reproductive Health Drugs and Drug Safety and Risk Management Advisory Committee. United States. Food and Drug Administration. September 9, 2011; http://www.fda.gov/downloads/AdvisoryCommittees/CommitteesMeetingMaterials/drugs/DrugSafetyandRiskManagementAdvisoryCommittee/ucm270958.pdf Accessed February 10, 2014.
- Damm DD, Jones DM. Bisphosphonate-related osteonecrosis of the jaws: a potential alternative to drug holidays. Gen Dent 61 : 33, 2013.3
- Aliya A Khan, Archie Morrison, David A Hanley, Dieter Felsenberg, Laurie K McCauley, Felice O’Ryan, Ian R Reid, Salvatore L Ruggiero, Akira Taguchi, Sotirios Tetradis, Nelson B Watts, Maria Luisa Brandi, Edmund Peters, Teresa Guise, Richard Eastell, Angela M Cheung, Suzanne N Morin, Basel Masri, Cyrus Cooper, Sarah L Morgan, Barbara Obermayer-Pietsch, Bente L Langdahl, Rana Al Dabagh, K. Shawn Davison, David L Kendler, George K Sándor, Robert G Josse, Mohit Bhandari, Mohamed El Rabbany, Dominique D Pierroz, Riad Sulimani, Deborah P Saunders, Jacques P Brown, and Juliet Compston; Diagnosis and Management of Osteonecrosis of the Jaw: A Systematic Review and International Consensus; Journal of Bone and Mineral Research, Vol. 30, No. 1, January 2015, pp 3–23.
- Peters E, Lovas GL, Wysocki GP. Lingual mandibular sequestration and ulceration. Oral Surg Oral Med Oral Pathol. 1993;75 : 739–43.
- Akira Taguchi et al., Impact of Osteonecrosis of the Jaw on Osteoporosis Treatment in Japan: Results of a Questionnaire-Based Survey by the Adequate Treatment of Osteoporosis (A-TOP) Research Group; Calcif Tissue Int., July 2015.
Kurz je již bez kreditace, vhodný k edukaci
Byl pro Vás kurz přínosný? Rádi byste se k němu vyjádřili? Napište nám − Vaše názory a postřehy nás zajímají. Zveřejňovat je nebudeme, ale rádi Vám na ně odpovíme.
Přihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



