-
Články
Top novinky
Reklama- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
Top novinky
Reklama- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariérní portál
Doporučené pozice
Reklama- Praxe
Top novinky
ReklamaOpioidy, chronická bolest, závislost
Datum publikace: 27. 3. 2017
Chronická bolest (CHB) představuje v současné době velký společenský a zdravotnický problém. Narušuje fyzické a psychické zdraví pacientů a snižuje jejich celkovou funkční kapacitu s dopadem i na běžné denní aktivity a rodinný život. Má i významné existenční a sociální důsledky a negativně ovlivňuje kvalitu života. Prevalence CHB neustále stoupá (19 % evropské populace) a v podstatě lze tento stav označit za pandemii. Stojí za tím zásadní změna v životním stylu, prodlužování lidského věku, následky léčby, která dříve nebyla myslitelná, a celá řada dalších faktorů. V mnoha případech je možno CHB považovat za nemoc „sui generis“. U polymorbidního pacienta představuje CHB často de facto jeho největší zdravotní problém. Závažným faktem je, že ve velké většině případů nemá CHB kauzální řešení. Na rozdíl od akutní bolesti (AB) reaguje CHB na léčebné postupy mnohem hůře. Základní lékařské obory, jako jsou ortopedie, chirurgie, neurochirurgie a neurologie, vyčerpaly své terapeutické možnosti, zaměřené logicky vesměs na kauzální řešení, a nemají pacientovi s perzistující bolestí již co nabídnout. Mnohdy dle jejich představ efektivní léčba zaměřená na CHB konkrétního pacienta úspěšně proběhla a objektivní diagnostické nálezy (rtg., CT, …) to potvrzují – jsou velmi dobré, takže pro bolest by přece neměl být důvod. Nemocný s CHB je velmi složitý pacient a jednoduché řešení neexistuje. Základní rolí algeziologa je stanovit pro daného pacienta individualizovaný léčebný postup, který by mu zajistil alespoň parciální, ale již přínosnou a stabilizovanou kontrolu CHB. Algeziolog je pod velkým tlakem, jelikož pacient s CHB má za sebou již řadu léčebných postupů a vyšetření v řadě zdravotnických zařízení. Neuspokojivý výsledek negativně ovlivňuje jeho psychické ladění a celkový postoj ke zdravotnickému systému.
Nejčastější diagnózy CHB
- Bolesti zad, FBSS
- Bolesti hlavy
- Kloubní bolesti
- Pooperační a posttraumatická bolest
- Neuropatické bolesti
- Viscerální bolesti
- KRBS I.
- Fibromyalgie a myofasciální syndrom
- Chronická nádorová bolest
Cíl léčby CHB
- Dosažení dostatečné analgezie a zlepšení kvality spánku
- Snížení funkčního oslabení
- Zlepšení kvality života
Principy léčby CHB
- Multidisciplinární přístup
- Stanovení diagnózy bolesti
- Kombinace farmakologických a nefarmakologických postupů
- Aktivní zapojení pacienta
Role opioidů v léčbě CHB
Opioidy jsou jednou z logických farmakologických možností k navození analgezie. Obecně se považují za nejúčinnější analgetickou třídu. Ovlivňují řadu orgánových systémů a funkcí – jejich účinek je komplexní. Indikací pro jejich podání je však intenzivní bolest! Analgetický účinek opioidů u intenzivní AB a u nádorové bolesti (NB) je nezpochybnitelný. Z farmakologického hlediska není u silných opioidů vyjádřen stropový efekt. Při progresi nádorového onemocnění je tak možno opakovanou titrací průběžně zajistit náležitou analgezii. Délka léčby NB bývá zpravidla časově limitovaná. U chronické nenádorové bolesti (CHNNB) je však situace poněkud odlišná. Ve většině případů nelze odstranit její příčinu. CHNNB nemá spontánní tendenci odeznívat jako AB. Příklady CHNNB, které bývají opioid senzitivní:
- CHB při osteoartróze,
- bolesti zad na podkladě degenerativní etiologie,
- bolesti při floridním ulcus cruris.
Pokud je zahájená léčba opioidy účinná, pro pacienta přínosná a jsou splněna kritéria efektivní léčby CHB, vzniká otázka, jak dlouho budeme léčebný postup s opioidy udržovat. Kdy terapii ukončíme nebo máme ji cíleně přerušit z obavy z rozvoje dlouhodobých opioidních NÚ a závislosti? Jelikož organická podstata CHB v takovýchto případech přetrvává, jen těžko můžeme předpokládat časově omezené použití opioidů. Musíme počítat spíše s dlouhodobou a možná i celoživotní léčbou. Pro řadu pacientů (např. senioři s CHB na podkladě degenerativní etiologie v oblasti myoskeletálního systému), respektujeme-li závažné kontraindikace třídy neopioidních analgetik, je opioidní léčba často jedinou využitelnou a relativně účinnou léčebnou modalitou. Když jsou opioidy tak analgeticky účinné u AB a NB, proč jsou u CHNNB výsledky léčby poměrně často problematické a rozporuplné? U CHNNB je ve srovnání s NB nebo AB léčebná odezva na opioidy (tzv. opioid responsiveness) odlišná. Na této odlišné terapeutické odpovědi se podílí celá řada faktorů, jež se u AB nestihnou rozvinout a uplatnit:
- diference ve vlastní podstatě nociceptivní aferentace s rozdíly v patofyziologii jednotlivých složek nociceptivního procesu (transdukce, transmise, percepce, modulace) – u AB je dominantní složka nociceptivní aferentace, u CHB se více uplatňují descendentní modulační vlivy,
- neuroplasticita CNS,
- rozvoj specifických neuroadaptivních mechanizmů CNS – farmakologická tolerance, fyzická závislost,
- lékové degradační a metabolické vlivy,
- genetická predispozice,
- psychosociální faktory,
- časový faktor léčby,
- komorbidity,
- lékové interakce při celkové farmakoterapii,
- psychiatrická onemocnění (anxiózně-depresivní stavy, …),
- účelové tendence,
- závislosti různé etiologie v anamnéze.
U CHNNB selhává postup založený na nekonečné další titraci opioidu při prvních známkách nedostatečné kontroly bolesti. Klinická praxe s dlouhodobou léčbou opioidy svědčí pro to, že zvyšování dávky opioidu u CHNNB je racionální jen maximálně do oblasti středních dávek (120–180 mg ekvivalentů morfinu p. o.). Další eskalace denní dávky nepřináší již zlepšení kvality analgezie, ale výrazně stoupá riziko dlouhodobých NÚ. Z klinického hlediska bychom tedy měli silné opioidy v indikaci u CHNNB považovat za látky se stropovým efektem! Již prakticky dvacetiletá klinická zkušenost ukazuje, že problematika léčby opioidy je značně složitější než jen pouhá preskripce a úprava dávkování. Rychlé řešení spočívající v prostém zvýšení denní dávky opioidu v naprosté většině případů situaci nevyřeší. Důležité je proto analyzovat příčiny nedostatečné kontroly bolesti, myslet na další diagnostiku, zařazení jiných terapeutických alternativ, ale především velmi pečlivě s pacientem jeho zdravotní stav probrat a zevrubně zkoumat aktuální symptomatologii. Příznačné a důležité jsou velké interindividuální rozdíly ve vnímavosti k opioidům. Jako každá léková skupina mají své výhody, ale bohužel i nevýhody. Výhody opioidů vyplývají na povrch především ve srovnání s nesteroidními antiflogistiky.
Výhody opioidů
- Nejsou parenchymově toxické.
- Nezpůsobují gastropatii.
- Nejsou hematotoxické.
- Neovlivňují koagulační proces.
- Častá je možnost redukce jiné analgetické léčby.
- Použitelnost u polymorbidity (s farmakoterapií interních onemocnění).
Nevýhody opioidů
Patří mezi ně typické nežádoucí účinky (NÚ), některé faktory příznačné pro třídu opioidních analgetik, dlouhodobé a specifické opioidní efekty.
Typické NÚ účinky opioidů (údaje z klinických studií)
- Nauzea – 28 %
- Obstipace – 26 %
- Sedace – 24 %
- Vertigo – 18 %
- Pruritus – 15 %
- Zvracení – 15 %
Další vedlejší účinky – bolest hlavy, suchost sliznice v dutině ústní, sexuální dysfunkce, flush, ztráta apetitu, únava, pocení, poruchy spánku, retence moči, neostré vidění, edémy, …
- Individuální tolerabilita (genetická predispozice)
- Nejistá opioidní senzitivita CHB (genetická predispozice – metabolizmus a degradace opioidů)
- Ovlivnění endokrinního systému (↓ testosteronu, estrogenů, T-hormonů, …)
- Imunosuprese (buněčná imunita)
- Hyperalgezie (alterace prahu bolesti, „celková“ alodynie)
- Specifické opioidní efekty
- Rozvoj tolerance
- Odvykací – abstinenční stav (rozvoj fyzické závislosti)
- Adiktivní potenciál, možný rozvoj psychické závislosti
Při dlouhodobé léčbě je však nutno vzít v úvahu především specifické opioidní efekty, jako jsou rozvoj tolerance, odvykací stav a psychická závislost. Musí se také počítat s adiktivním potenciálem opioidů.
Algeziologický pohled na problematiku závislosti
Termín závislost je víceznačný. Jinak ho chápe algeziolog, adiktolog či jiný lékař, který s opioidy rutinně vůbec nepracuje, jinak na tento pojem pohlíží laik. Mění se i pohled algeziologů na tento fenomén. Autoři zabývající se problematikou bolesti tradičně rozdělují závislost na fyzickou a psychickou. Klíčový význam má i fenomén tolerance.
Tolerance je farmakologický fenomén. K udržení původního analgetického účinku je nutno zvyšovat dávku opioidu. Klinické zkušenosti s opioidy v léčbě NB a CHNNB ukazují na to, že zatímco poměrně záhy se rozvíjí tolerance vůči některým nežádoucím účinkům (nauzea, zvracení, sedativní efekt, ovlivnění kognitivních funkcí), dávka opioidu pro zajištění analgezie zůstává po titrační periodě při profesionálně vedené léčbě nezřídka dlouhodobě poměrně stabilní. Vůči obstipačnímu účinku opioidů prakticky nikdy nevzniká tolerance. Trvale zůstává i mióza. Potřeba zvyšovat dávku při nedostatečném analgetickém účinku může souviset s progresí základního onemocnění, přidružením jiného onemocnění nebo se zvýšením aktivit pacienta. Přesto je nutno s rozvojem tolerance vůči analgetickému účinku opioidů počítat.
Fyzická závislost je fyziologická adaptace na trvalou přítomnost určité látky v lidském organizmu. Fyzickou závislost na opioidy charakterizuje rozvoj specifického abstinenčního syndromu (AS – syndrom z odnětí, withdrawal syndrom) následně po významné redukci denní dávky nebo po náhlém přerušení této léčby. AS má nezřídka iatrogenní příčinu. Příkladem může být pacient, který si s sebou nevezme opioidy, které pravidelně užívá, a další pokračování léčby není v průběhu hospitalizace zajištěno. AS může rovněž vzniknout, je-li v průběhu léčby µ-agonisty podán opioid s antagonistickou aktivitou na µ-receptoru (ze skupiny agonistů–antagonistů např. pentazocin, butorfanol, nalbufin) či antagonista opioidů (naloxon, naltrexon, nalmefen). AS vzniká v důsledku vysoké aktivity centrálního nervového sympatodrenálního systému po odeznění obecně tlumivého účinku opioidů na CNS.
Klinický obraz AS
- Somatické příznaky: pocení, lakrimace, zívání, mydriáza, piloerekce, nauzea, zvracení, abdominální kolika, hypertenze, tachykardie, arytmie, tremor, paroxyzmus křečí
- Psychické příznaky: anxieta, distres, nervozita, iritabilita, deprese, agresivita, hypervigilita, jiná bolest, poruchy spánku
Někdy jen pacient uvádí: „Cítím se nějak divně.“ Tyto příznaky lze zastihnout nejčastěji na konci dávkovacího intervalu (dle lékové formy a typu opioidu), ale také jako permanentní stav. Existuje i dlouhodobá forma AS, přetrvávající po vysazení opioidu řádově měsíce. Projevuje se jako:
- celkový diskomfort,
- anhedonie,
- hyperalgezie,
- poruchy koncentrace,
- poruchy spánku,
- depresivní ladění.
AS by se neměl zaměňovat s psychickou závislostí. Pacient s pravou psychickou závislostí může, ale nemusí být fyzicky závislý. U nemocných léčených pravidelně opioidy je nutno s fyzickou závislostí automaticky počítat.
Psychická závislost je komplexní biopsychosociální fenomén se zvláštním vzorcem chování, který charakterizuje nutkavý pocit a chorobná touha užívat danou látku i přes neblahé zdravotní, psychosociální a existenční důsledky. Typická je ztráta kontroly nad užíváním léku. Jedinec neužívá opioid pro potlačení bolesti, ale hledá specifický euforizující, psychogenní efekt opioidu. Touží po opakování stavu, jenž nastává po užití dané substance. Ke vzniku psychické závislosti však pravděpodobně nestačí pouhé podávání látky s potenciálem rizika rozvoje adiktivního chování. Ke vzniku psychické závislosti na opioidech jsou nutné tyto faktory:
- genetická predispozice (pro onemocnění z užívání návykových látek),
- sociální kontext,
- expozice látky s adiktivním potenciálem,
- stav bez bolesti.
Obrazně řečeno, přítomnost bolesti jakoby filtruje nebo eliminuje rizikový euforizující efekt, který v sobě mají opioidy zakódován, a farmakodynamický potenciál daného agens je využit především k navození analgezie. Lze konstatovat, že bolest svým způsobem antagonizuje adiktivní potenciál opioidu. Pro to svědčí i zkušenost s pacienty s bolestí léčenou opioidy. Značnou roli hraje rovněž aplikační cesta a léková forma. Jedinec s psychickou závislostí na opioidech vyhledává injekční podání s rychle vzniklou vysokou koncentrací dané látky v séru, jež je důležitá pro vznik narkomany vyhledávaného pocitu euforie a zdánlivé kontroly nad svou životní situací.
Pacient se někdy opakovaně a agresivně dožaduje úpravy a zesílení léčby pro insuficientní analgezii. Z těchto důvodů se snaží hledat pomoc jinde či si sám léčbu upravuje a zesiluje. Nemusí to vždy svědčit pro psychickou závislost, ale pro tzv. pseudozávislost. S pseudozávislostí se můžeme setkat relativně často např. v průběhu léčby pooperační bolesti (pokud je nedostatečně léčená), ale i u nádorové a CHNNB. Jde-li o tento typ „závislosti“, poruchy chování po náležité úpravě terapie a dosažení úlevy mizí. Zdravotnickým personálem však bývá taková situace hodnocena s despektem jako pravá závislost (pacient bývá označován za „feťáka“).
Jiným fenoménem je tzv. terapeutická závislost. Pacient, který dříve trpěl neztišitelnou bolestí, lpí na určité léčebné modalitě (např. „obstřiky“), o níž ví, že byla na bolest účinná, a ze strachu z recidivy algického stavu, na nějž zůstala silná paměťová stopa, si nedokáže představit opuštění této léčby. I s tímto stavem je možné se v průběhu léčby CHNNB opioidy setkat. Terapeutická závislost se může projevit jako sklon k hromadění opioidů do zásoby z obavy, že pokračování v této léčbě je v budoucnu nejisté. Takové jednání se může nepřesně označovat za projev a důkaz adiktivního chování. Tento jev je známý i v jiných oblastech medicíny (vytváření zásob inzulinu u diabetiků nebo nitrátů u nemocných s anginou pectoris).
Klasifikace závislosti u pacientů s CHB léčených opioidy
Z klinického hlediska se pojmy fyzická závislost a psychická závislost prolínají a i u pacientů s CHB léčenou opioidy se mohou vyskytovat v určitém poměru společně. Proto použití obecného termínu závislost i v souvislosti s léčbou CHB opioidy má své opodstatnění. Pacienty léčené lege artis pro refrakterní bolest však nelze automaticky řadit do stejné skupiny jako jedince, kteří ilegálně zneužívají návykové látky.
Podle poslední Mezinárodní klasifikace nemocí (MKN-10, tab. 1), uvedené v platnost v roce 1994, jsou však kritéria závislosti postavena tak, že prakticky každý pacient s CHB léčenou opioidy je splňuje. Pro psychiatrickou diagnózu závislost na opioidech stačí splnit tři kritéria ze šesti. Dvě kritéria – fyzická závislost a tolerance – jsou u pacientů s CHB léčenou opioidy splněna rovnou. S tolerancí a fyzickou závislostí se však musí počítat prakticky u všech pacientů léčených pravidelně opioidy!
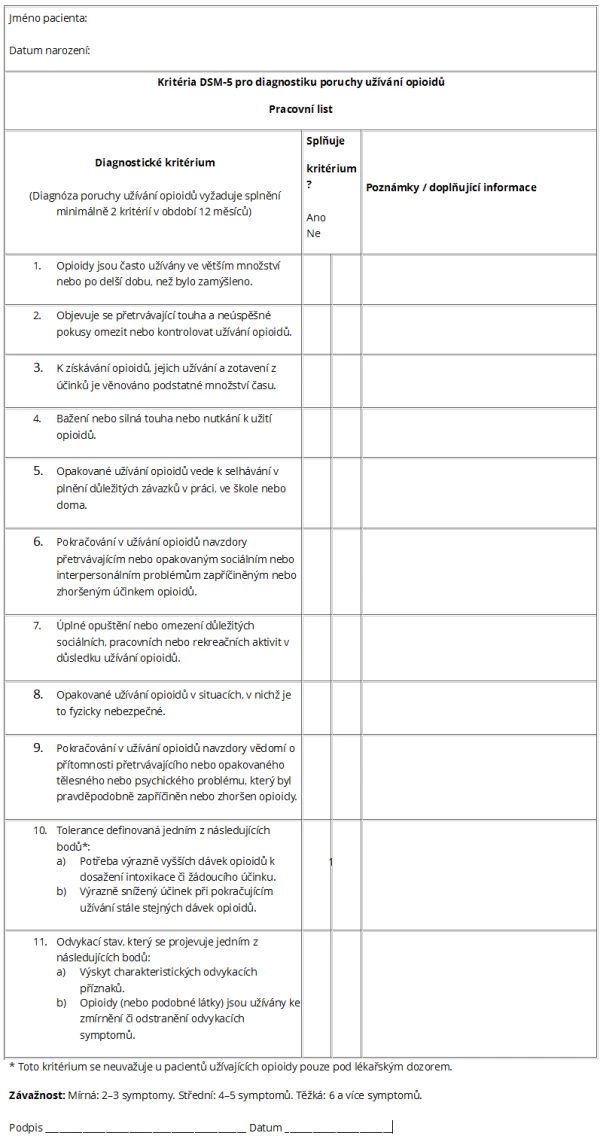
Změnu v klasifikaci přinesl DSM-V z r. 2013 (American Psychiatric Association, 2013; tab. 2). Zde se již nepoužívá termín léková závislost (substance dependence), ale je nahrazen pojmem substance use disorder, kterému odpovídá český pojem poruchy spojené s užíváním látek neboli v daném případě poruchy spojené s užíváním opioidů. Pro stanovení diagnózy zde musí být splněna alespoň dvě kritéria z jedenácti. Další změnou v DSM-V ve vztahu ke skupině pacientů léčených pro CHB opioidy pod lékařskou kontrolou však je to, že v těchto případech není průkaz tolerance a fyzické závislosti brán jako relevantní kritérium (Opioid used disorder check list, tab. 3) pro stanovení diagnózy onemocnění z užívání návykových látek.
Tab. 1

Tab. 2

Tab. 3 DSM-V checklist – porucha užívání opioidů
Závislost – nejasnosti v pojmech
V oblasti problematiky závislosti existuje ještě další pojem – adikce (addiction). Jaký je rozdíl v pojmech závislost, psychická závislost a adikce? Je nějaký? Již sám pojem závislost má v sobě cosi negativního v tom smyslu, že existuje určitý podstatný faktor, bez kterého pacient nemůže existovat. Je tím narušena nezávislost a autonomie jedince. Je-li u pacienta léčeného opioidy z indikace refrakterní CHB dosaženo kvalitní kontroly bolesti, je skutečně na této terapii závislý! Analogicky je diabetik závislý na inzulinu, hypertonik na antihypertenzní medikaci nebo astmatik na inhalační bronchodilatační léčbě s kortikoidy. Pojem adikce však v sobě obsahuje z psychosociálního hlediska cosi vysloveně negativního a má až kriminální podtext. Výrazným obsahem tohoto pojmu je zneužívání něčeho. Slovo adikce v podstatě odpovídá výše uváděnému termínu psychická závislost. K typickým projevům adiktivního chování patří např.:
- falšování receptů,
- injekční a jiné aplikace p. o. opioidů,
- nedodržování a modifikování léčby bez souhlasu lékaře, rychlá spotřeba předepsaných opioidů,
- prodej předepsaných opioidů,
- simultánní nekontrolovaný abúzus alkoholu a jiných drog,
- vyhledávání jiných lékařů k zajištění preskripce opioidů, časté návštěvy pohotovosti,
- opakované ztrácení receptů a léků s „klasickým“ typem omluvy,
- časté telefonáty za účelem včasnější kontroly,
- zdůrazňování alergie na neopioidní analgetika, kodein a případně lokální anestetika („jen jeden lék je účinný a vždy pomůže“ – např. petidin (dolsinová závislost),
- pacient tzv. „ve spěchu“,
- prezentace relativně dobré znalosti příslušné farmakologie a terminologie.
Styčné faktory mezi „závislostí u pacientů léčených lege artis opioidy pro CHB“ a „onemocněním z užívání návykových látek“
Přesně identifikovat pacienta s aberantním typem chování, jež by mohlo svědčit pro adikci (psychickou závislost), je často velmi obtížné. Přes všechny výše uvedené aspekty se s fenoménem závislosti chápaným komplexně v léčbě bolesti opioidy musí počítat. Vždy od sebe nelze mechanicky separovat fyzickou a psychickou závislost a toleranci. Platí, že pacient s CHB dlouhodobě léčený opioidy prakticky vždy vykazuje známky fyzické závislosti a tolerance. Může, ale nemusí mít příznaky psychické závislosti s rysy adiktivního chování. Tam, kde je léčba opioidy efektivní, bývá vidět zlepšení celkového funkčního stavu. Funkční stav jedince, který zneužívá opioidy, nemá organicky podloženou bolest, se z hlediska zdravotního i sociálního zhoršuje. Zneužívané opioidy jsou zde používány jako metoda ke zvládání životní situace. Opioidy se stávají ústředním bodem života závislého jedince. V takovém případě můžeme hovořit o adiktivním chování. V těchto případech může jedinec využívat i negativních účinků opioidů, jako jsou relaxační efekt, celkový útlum, eventuálně i potenciaci účinku dalších farmak a alkoholu. Správně vyhodnotit konkrétní stav je velmi složité zejména tehdy, když je pacient dlouhodobě léčen opioidy již ve vysoké dávce (nad 120 až 180 mg morfinových ekv. p. o.), ale terapie není efektivní. V podstatě zjistíme, že intenzita bolesti, stupeň úlevy, funkční stav a další terapeutická kritéria jsou na stejné (nebo horší) úrovni, jako tomu bylo v době zahájení léčby před řádově měsíci či lety při mnohem nižší dávce opioidu. Pacient často naléhá na zvýšení dávky opioidu. Má zkušenost, že se mu vždy po zvýšení dávky stav zlepšil. Otázkou někdy je, co se zlepšilo – zmírnila se bolest, nebo abstinenční příznaky? Další eskalace dávky opioidu v takové situaci (dávková past) může přinést maximálně jen krátkodobé zlepšení kontroly bolesti, ale každopádně zvýší stupeň fyzické závislosti a tolerance. Nikdy u těchto pacientů není zcela jasné, proč opioidy vyžadují! Jisté však je, že faktorem, který hraje roli, je závislost se silnou potřebou potlačit příznaky AS. Zkušenost s prožitkem AS je pro jedince velmi nepříjemná. Na tento negativní prožitek, podobně jako na intenzivní bolest zůstává silná paměťová stopa. Opioid jako látka s adiktivním potenciálem může při užití vyvolat vlnu euforie a pocitu blaženosti (ale ne vždy), což vede k touze po opakování dávky. Tento tzv. pozitivní posilující efekt (positive reinforcing effect), který je klíčový v iniciální fázi rozvoje psychické závislosti (adikce), po určité době oslabuje. Klinická zkušenost ukazuje, že u nemocných s bolestí se tento fenomén většinou nevyskytuje. Pozitivní posilující fenomén se uplatňuje především při nezákonném použití opioidů (illicit use), kdy nejsou užívány proti stavu s organicky podmíněnou bolestí. To, co však je motorem adiktivního typu chování spojeného s nutkavou potřebou neustále si opatřovat danou látku (nezákonné používání) nebo u pacientů s bolestí se lpěním na léčbě opioidy, je tzv. negativní podpůrný efekt (negative reinforcing effect), daný následkem rozvoje AS. Tomu se snaží za každou cenu zabránit jak ilegální uživatel opioidu, tak i pacient dlouhodobě léčený opioidy.
Styčnou plochou klinické symptomatologie závislosti mezi pacienty s CHB na opioidech a ilegálními uživateli je snaha předcházet rozvoji AS.
Chování vyznačující se permanentní snahou zajistit si opioid (opioid seeking behavior) je toho důsledkem. I u pacientů léčených opioidy lege artis můžeme nacházet podobné příznaky, ale nemusí to být ihned stav zařaditelný pod nozologickou jednotku „onemocnění z užívání návykových látek“.
Farmakoterapeutická alternativa léčby závislosti na opioidech u pacientů s CHB
Skupina pacientů s CHB na opioidech, kde léčba nepřináší uspokojivý výsledek a klíčovým problémem je silná závislost, existuje. V těchto případech již není další zvyšování dávky racionální, ale pacient má obavu se opioidů vzdát. Obava pramení z možnosti zhoršení bolesti a možná ještě více z rozvoje AS. Za takovéto situace není zcela jasné, zda algeziolog léčí bolest, nebo spíše AS. V podstatě může jít v některých případech o jakousi formu (substituční) léčby. Při vysokém dávkování se můžeme setkat mimo jiné i s rozvojem abnormálního čití s alterací prahu bolesti, kdy původní bolest již nehraje klíčovou roli (hyperalgezie).
V těchto případech může být řešením převedení na substituční léčbu sublingválním buprenorfinem s naloxonem (Suboxon), jež přináší některé výhody. Buprenorfin je v algeziologii dobře známý v transdermální aplikaci (Transtec). Osvědčilo se nízké dávkování zejména jako analgetická léčba volby pro seniory, kde se často vystačí s denní dávkou 0,2 mg. V algeziologii se většinou nepřekračuje dávka cca 3,2 mg/24 hod. (buprenorfin TDS 2× 70 μg/hod.). Buprenorfin je parciální agonista na receptoru µ, k němuž má však silnou afinitu a je antagonistou na receptoru κ. Naloxon, druhá složka Suboxonu, je antagonistou na receptoru µ. Tím se zabraňuje zneužití lékové formy narkomany, jelikož i. v. aplikace by vedla k silnému a obávanému AS. Při sublingvální aplikaci se naloxon neuplatní. Nižší aktivita buprenorfinu na receptoru µ stačí k zajištění analgezie, ale nevyvolá euforii, dechovou depresi ani bradykardii a rozvoj tolerance a fyzické závislosti je nižší než u ostatních silných opioidů. Antagonizaci na receptoru κ se přičítá nízký sedativní účinek a antidepresivní vlastnosti. Při substituci Suboxonem je zdokumentováno:
- potlačení touhy po opioidech,
- stabilní potlačení příznaků AS,
- zajištění stabilní kontroly bolesti,
- vysoká bdělost se zvýšením aktivit denního života,
- zlepšení compliance léčby.
Poměr buprenorfin/naloxon je v Suboxonu 4 : 1 a k dispozici jsou 2 síly: Suboxon 2/0,5 mg a 8/2 mg. Při dostatečném dávkování (16 mg/24 hod.) jsou receptory µ obsazeny až z 95 % a prakticky se nemohou vzhledem k vysoké afinitě buprenorfinu uplatnit žádné jiné opioidy. Typická je velká terapeutická šíře, dobrá kardiovaskulární stabilita a nemusí se brát zřetel na renální funkce.
Typy pacientů s CHB léčených opioidy s možnou indikaci k substituční léčbě:
- pacient s CHNNB a se symptomy AS (end of dose AS) a s nedostatečnou kontrolou bolesti,
- pacient s CHNNB, u něhož opioidy nepřinášejí analgetický efekt, ale který léčbu nechce opustit,
- pacient, u kterého je kontrola bolesti zajištěna jinak (neuromodulace), ale pro projevy AS se nepodařilo opioidy vysadit,
- pacient v nižším věku, u něhož může substituční léčba ve srovnání se stávající opioidní medikací vést ke zlepšení funkčního stavu a kvality života,
- pacient s ustupující CHNNB (spontánně či vlivem jiné terapie), který je motivován a chce přerušit léčbu opioidy, ale bez farmakologické podpory to nedokáže.
Algeziolog musí neustále balancovat poměr risk/benefit opioidní léčby. Dávka opioidu by vždy měla být ve vyváženém poměru proti bolesti a úvedlejším účinkům. Jde-li dávka opioidu již přes dosažení dostatečné úlevy nebo bolest není opioid senzitivní, vzniká problém v podobě deprese kognitivních funkcí, sedace, dysforie, dezorientace, zvyšování fyzické závislosti, tolerance a rozvoje abnormálního čití atd. Určitou analogií je výkon anesteziologa. Neadekvátně hluboká celková anestezie ve vztahu k relativně nízké nociceptivní aferentaci u operace menšího rozsahu má za následek protrahované buzení po ukončení výkonu a nemocný přespává.
V klinické dokumentaci by mělo být vyznačeno, že chronická bolest je léčena opioidy podobně jako u nemocných na kortikoidech nebo při léčbě diabetu mellitu inzulinem. Vhodným termínem pro tento stav v seznamu klinických diagnóz je opioid dependentní chronická bolest. Takový výraz je přesnější než pojem s určitým negativním nábojem – závislost na opioidech. Diagnóza opioid dependentní chronická bolest v sobě nese i naléhavé sdělení o nutnosti zajistit kontinuitu léčby opioidy v podmínkách hospitalizace.
Léčba CHB opioidy je celkově náročný a zodpovědný léčebný postup. Existuje skupina pacientů léčených vysokou dávkou opioidu s velmi neuspokojivým výsledkem léčby. U těchto nemocných nejsou splněna cílová kritéria léčby CHB, lze identifikovat známky silně rozvinuté fyzické závislosti a tolerance a možnosti další terapie jsou vyčerpány. V takových případech může být substituční léčba metodou volby a nadějným řešením i z hlediska kontroly vlastní bolesti.
Kurz je již bez kreditace, vhodný k edukaci
Byl pro Vás kurz přínosný? Rádi byste se k němu vyjádřili? Napište nám − Vaše názory a postřehy nás zajímají. Zveřejňovat je nebudeme, ale rádi Vám na ně odpovíme.
Přihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



