-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Inkretiny – přelomová léčba diabetu a obezity je jen začátek...
Autoři: Štěpán Svačina
Působiště autorů: 1. lékařská fakulta Univerzity Karlovy, Praha
Vyšlo v časopise: Svět praktické medicíny, 7, 2025, č. 1, s. 46-51
Kategorie: Medicína v ČR: přehledový článek
Souhrn
Inkretiny jsou hormony trávicího traktu, jejichž analoga dnes běžně využíváme v léčbě obezity a diabetu. GLP-1 analoga jsou od roku 2008 užívaná injekční antidiabetika, od roku 2006 využíváme blokádu dipeptidylpeptidázy 4 (gliptiny) k prodloužení efektu GLP-1 a léčbě diabetu. V posledních letech se liraglutid, semaglutid a tirzepatid staly také schválenými antiobezitiky. Provedené studie ukazují, že by inkretinové léky mohly být brzy využívány k léčbě téměř deseti dalších onemocnění. Výzkum a využití hormonů trávicího traktu čeká pravděpodobně velká budoucnost.
Pojem inkretinových hormonů není jasně ohraničený. Jde o hormony secernované trávicím traktem, zejména tenkým a tlustým střevem a v širším slova smyslu i žaludkem
a žlázami trávicího traktu, především pankreatem.Mezi nejvýznamnější zástupce inkretinů dnes patří glukagonu podobný peptid 1 (glucagon-like peptide 1, GLP-1) a inzulinotropní peptid závislý na glukóze/gastrický inhibiční polypeptid (glucose dependent insulinotropic polypeptid/gastric inhibitory polypeptid, GIP). Změna názvu tohoto hormonu ukazuje na vývoj našeho poznání od inhibice žaludeční sekrece až po významnější vliv na sekreci inzulinu. Podobně se měnil název jednoho z nejstarších inkretinů cholecystokininu/pankreozyminu. Někdy hovoříme také o sekretinové skupině hormonů a skupině hormonů vycházející z preproglukagonu (podrobně v 1).
Obr. 1. – Inkretinový efekt. Podání glukózy perorálně vyvolá větší sekreci inzulinu než podání stejné dávky inzulinu parenterálně. [Upraveno podle: Nauck M, et al. Diabetologia 1986;29:46–52.] ![– Inkretinový efekt. Podání glukózy perorálně vyvolá větší sekreci inzulinu než podání stejné dávky inzulinu parenterálně. [Upraveno podle: Nauck M, et al. Diabetologia 1986;29:46–52.]](https://pl-master.mdcdn.cz/media/cache/media_object_image_small/media/image/6649743499d4ab364f17e1568f92d6c8.png)
Historie objevu a využití inkretinových hormonů
Historie objevu těchto hormonů je dávná, byly popsány již počátkem 20. století Baylissem a Starlingem (podrobně v 1). Podávání extraktů střevní sliznice diabetikům ale nebylo úspěšné. V 60. letech byl popsán tzv. inkretinový efekt (Obr. 12) – podání glukózy orálně vyvolá větší sekreci inzulinu než podání stejné dávky inzulinu parenterálně.3, 4, 5, 6, 7 Tento rozdíl popsal ale již francouzský fyziolog Claude Bernard, žijící v Purkyňově době v 19. století. Domníval se však, že je vysvětlitelný vychytáním orálně podané glukózy játry.3 Až po desítkách let byly popsány GLP-1 a GIP. V roce 1980 byl ze slin ještěrky korovce jedovatého (Gila monster) izolován exendin stimulující produkci inzulinu. Endokrinolog John Eng požádal o patent a v roce 1990 prodal licenci firmě Amylin Pharmaceuticals. Na základě výsledků těchto výzkumů byl vyvinut první preparát působící na bázi GLP-1 exenatid, tzv. GLP agonista neboli inkretinové mimetikum (podrobně v 1). Tato molekula je na rozdíl od původního GLP-1 produkovaného střevními buňkami odolná proti rychlému rozložení. Exenatid byl jako Byetta povolen v USA pro léčbu diabetiků 2. typu v dubnu 2005 a v Evropě získal souhlas začátkem roku 2007. U nás je podáván od roku 2008. Nevýhodou subkutánně podávaného analoga GLP-1 exenatidu s poločasem 2,4 hodiny je jeho krátký hypoglykemizující efekt (6–8 hodin), který znamená nutnost podávání léku dvakrát denně. Později byla vyvinuta inkretinová analoga podávaná 1× denně (liraglutid, lixisenatid) a dokonce 1× týdně (dulaglutid, semaglutid a Bydureon – depotizovaný exenatid). Souhrn zkušeností s podáváním těchto látek v diabetologii uvádí obrázek 2.8 Jde o účinná antidiabetika, v diabetologii zcela běžná.8 Hmotnost ovlivňují více u diabetiček a podle některých studií je i efekt na kompenzaci diabetu větší u žen. Dnes jsou některá podávána i ve fixní kombinaci s inzulinem. Liraglutid a semaglutid jsou schváleny i jako antiobezitika (podrobně v 9). Od září 2024 je v ČR dostupný tirzepatid – peptid, který účinkuje současně jak na receptory GLP-1, tak na receptory GIP.10 Je u nás velmi úspěšným antiobezitikem a antidiabetikem, které si zatím hradí pacient (letos bude pravděpodobně schválena úhrada pojišťovnou pro některé diabetiky 2. typu).
Inkretinů se dotýká i historie výzkumu dipeptidylpeptidázy 4 (DPP-4). Ta rovněž sahá daleko do minulosti. Tento enzym byl popsán již v 60. letech minulého století a první inhibitory byly vyvinuty koncem 80. let (podrobně v 1). V roce 1994 se začaly zkoumat tzv. cyanopyrrolidiny. Úpravami těchto molekul se podařilo vyvinout antidiabeticky působící látky koncem 90. let a byly zahájeny pokusy na zvířatech a později klinické studie (podrobně v 1). Sitagliptin pak byl v roce 2006 první schválený inhibitor DPP-4. Vývoj léků byl komplikován problematikou selektivity, kdy starší látky inhibovaly rovněž dipeptidylpeptidázy 8 a 9 s mnoha potenciálními nežádoucími účinky. Dnes jde o běžně podávaná antidiabetika, slabší než injekční inkretinová mimetika. Nesnižují však hmotnost a nepřinášejí podobné pozitivní orgánové vlivy jako inkretinová analoga.
Obr. 2. Pohlavně specifické účinky GLP-1 RA. [Upraveno podle: Rentzeperi E, et al. J Pers Med 2022;12(3):454.] ![Pohlavně specifické účinky GLP-1 RA. [Upraveno podle: Rentzeperi E, et al. J Pers Med 2022;12(3):454.]](https://pl-master.mdcdn.cz/media/cache/media_object_image_small/media/image/62463ffefae5096b0e4030a33007f333.png)
Obr. 3. Úloha klíčových hormonů v glukózové a energetické homeostáze. 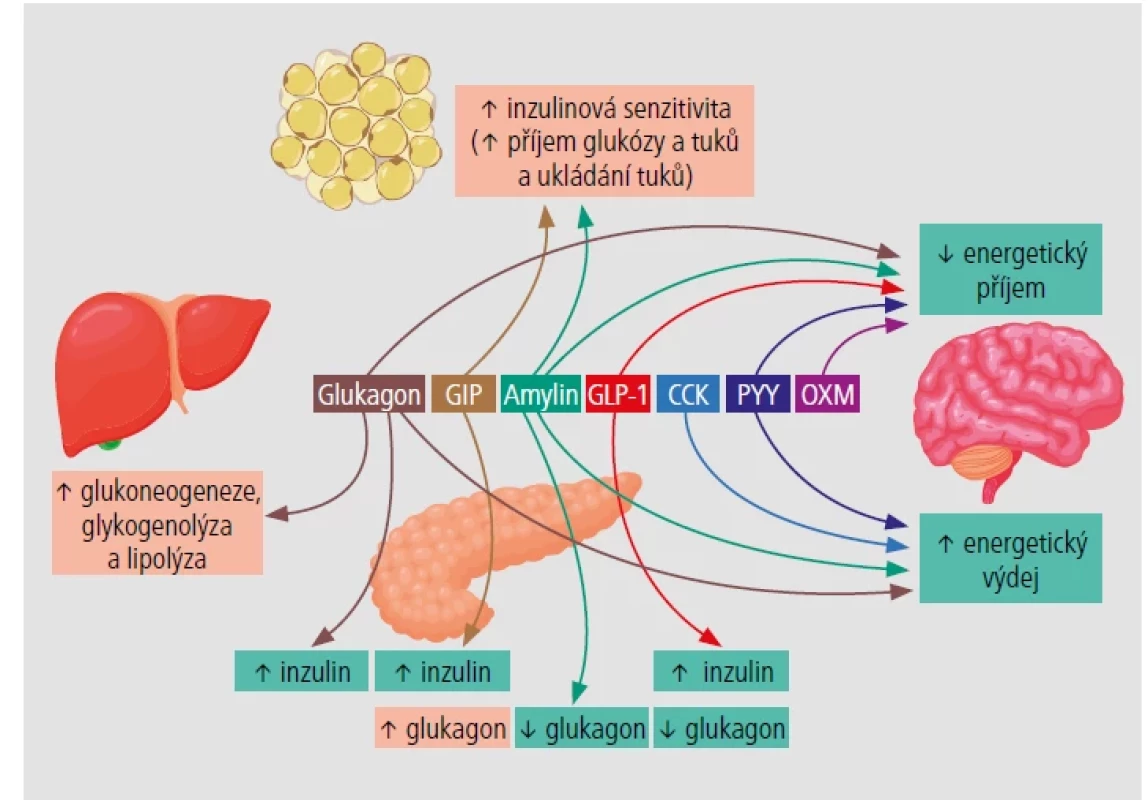
Glukagon, glukagonu podobný peptid 1 (GLP-1), inzulinotropní peptid závislý na glukóze (GIP) a oxyntomodulin (OXM) jsou deriváty preproglukagonu s různými účinky na slinivku, játra, tukovou tkáň a mozek k regulaci glukózové a energetické homeostázy. Cholecystokinin (CCK) a peptid tyrosin-tyrosin (PYY) jsou pankreatické peptidy působící převážně prostřednictvím centrálních mechanismů na pravidelný příjem a výdej energie. [Upraveno podle: Dissanayake HA, Somasundaram NP. Curr Diab Rep 2024;24:1–12.] Inkretiny – široká skupina peptidů
Skupina hormonů trávicího traktu je velmi široká. Obvykle se dělí na gastrinovou (např. gastrin a cholecystokinin) a sekretinovou skupinu (např. GLP-1, glukagon, GIP). Původem jsou z tenkého střeva (od duodena až po ileum), ale i z tlustého střeva, pankreatu, žaludku a štítné žlázy. Zmíněný GLP-1 (sekretinová skupina) je tvořen zejména v ileu.1 Zvyšuje sekreci inzulinu a supresi glukagonu, zpomaluje evakuaci žaludku a působí anorekticky. Vyskytuje se i v centrálním nervovém systému. GIP, secernovaný především v duodenu a jejunu, ovlivňuje žaludeční sekreci, a zejména sekreci inzulinu a glukagonu. Některé inkretiny nepůsobí systémově, ale jen lokálně parakrinně. Řada jich zatím ve farmakoterapii nenašla využití, například gastrin, cholecystokinin, vazoaktivní intestinální peptid (VIP), apelin, motilin, pankreatický polypeptid (PP), peptid YY, neuropeptid Y neurotenzin (vznikající v nervových zakončeních GIT), polypeptid uvolňující gastrin (GRP), ghrelin, glicentin, GLP-2, glicentinu podobný pankreatický peptid (GRPP). V kombinační léčbě je využíván kalcitonin – hormon štítné žlázy a inkretin v širším smyslu slova. Většinu hormonů lze odvodit z molekuly preproglukagonu (Obr. 311).
Farmakologickému využití se v diabetologii a obezitologii blíží amylin, glukagon, kalcitonin a oxyntomodulin. Oxyntomodulin je secernován v colon a působí na receptory GIP, receptor GLP-1 a nejspíš i ovlivňuje cirkadiánní efekty ve funkcích jater. Je to také výrazné anorektikum. Amylin vzniká společně s inzulinem v beta-buňkách pankreatu, ovšem je secernován ve 100× nižším množství než inzulin. Zpomaluje motilitu žaludku a má anorektický efekt. Byl injekčně používán ve Spojených státech k tlumení postprandiálních hyperglykemií. Nyní zažívá nový rozvoj v kombinační léčbě (viz dále). Efekty některých inkretinů jsou na obrázku 3.
Tab. 1. Inkretinoví polyagonisté u DM2 podle Dissanayake. [Upraveno podle: Dissanayake HA, Somasundaram NP. Curr Diab Rep 2024;24:1–12.] Lék Analog Trvání studie [týdny] Pokles % HbA1c ![Inkretinoví polyagonisté u DM2 podle Dissanayake. [Upraveno podle: Dissanayake HA, Somasundaram NP. Curr Diab Rep 2024;24:1–12.] Lék Analog Trvání studie [týdny] Pokles % HbA1c](https://pl-master.mdcdn.cz/media/cache/media_object_image_small/media/image/d3f29144126b77460e44378d0f2e32f0.png)
Perspektivy farmakoterapie obezity a diabetu
V současné době zažíváme nástup tirzepatidu do běžné praxe. Známé jsou výsledky studie SURMOUNT-1, kdy pacienti v závislosti na dávce tirzepatidu redukovali hmotnost po 72 týdnech užívání až o 22,5 %.12 Dlouhodobým podáváním tirzepatidu se zabýval Jastreboffův autorský tým, který své výsledky publikoval v roce 2024 se závěrem, že tříletá léčba tirzepatidem u osob s obezitou a prediabetem vedla k podstatnému a trvalému snížení hmotnosti a výrazně nižšímu riziku progrese do diabetu 2. typu než u placeba.13 Perspektivy farmakoterapie inkretinovými analogy obezity a diabetu jsou však větší, půjde o užití peptidů působících na dva až tři receptory a v jednom případě o fixní kombinaci inkretinových analog. V práci kolektivu autorů z roku 2024, který vedl Haiqiang Yao,14 je porovnán efekt na glykemii a hmotnost za použití výpočtů korelujících efekt vždy vůči placebu (Obr. 4a, b, c). CagriSema je fixní kombinace cagrilintidu (syntetický analog amylinu) a semaglutidu. Retatrutid je trojitý agonista působící na receptory GLP-1, GIP a glukagonu. Orforglipron je nízkomolekulární perorální analog GLP-1. Mazdutid je injekční analog GLP-1 a glukagonu. Liraglutid, dulaglutid, semaglutid, efpeglenatid a pegylovaný exenatid, lixisenatid a PEG-loxenatid jsou GLP-1 analoga. Retatrutid působí na receptory GLP-1, GIP a glukagonu.
Velmi účinné jsou i další léky. Survodutid je duální agonista glukagonu/receptoru GLP-1 a má i menší efekt na oxyntomodulinový receptor. Cotadutid je agonista glukagonu/receptoru GLP-1. Mazdutid je agonista receptoru GLP-1 a glukagonu a více se váže i na receptor oxyntomodulinu.
Pořadí efektu na úbytek hmotnosti (Obr 4a), pokles glykovaného hemoglobinu HbA1c (Obr. 4b) a glykemii nalačno (Obr. 4c) se mírně liší. Víceméně ale u diabetiků obvykle koreluje pokles hmotnosti s poklesem HbA1c. Porovnání efektu více polyagonistů u diabetiků 2. typu je uvedeno v tabulce 1.11, 15
Obr. 4a – Inkretinová analoga – efekt na úbytek hmotnosti vůči placebu. [Upraveno podle: Yao H, et al. BMJ 2024;384:e076410.] ![Obr. 4a – Inkretinová analoga – efekt na úbytek hmotnosti vůči placebu. [Upraveno podle: Yao H, et al. BMJ 2024;384:e076410.]](https://pl-master.mdcdn.cz/media/image/e060c2367ba0e337b1496ea393dc399a.png?version=1748899992)
Obr. 4b – Inkretinová analoga – efekt na snížení glykovaného hemoglobinu HbA1c vůči placebu. [Upraveno podle: Yao H, et al. BMJ 2024;384:e076410.] ![Obr. 4b – Inkretinová analoga – efekt na snížení glykovaného hemoglobinu HbA1c vůči placebu. [Upraveno podle: Yao H, et al. BMJ 2024;384:e076410.]](https://pl-master.mdcdn.cz/media/image/2c141057f8402d4a5a4f3bac551c2725.png?version=1748900019)
Obr. 4c – Inkretinová analoga – efekt na glykemii nalačno vůči placebu.[Upraveno podle: Yao H, et al. BMJ 2024;384:e076410.] ![Obr. 4c – Inkretinová analoga – efekt na glykemii nalačno vůči placebu.[Upraveno podle: Yao H, et al. BMJ 2024;384:e076410.]](https://pl-master.mdcdn.cz/media/image/8a99ce1296047d23d6a0954dba8cf9c9.png?version=1748900033)
Další efekty inkretinové léčby
V literatuře lze zachytit mnoho dalších efektů inkretinové léčby (podrobně v 16). Je otázkou, jak dlouho bude trvat schválení a proniknutí indikací těchto molekul do SPC jednotlivých léků. Situace je ovlivněna tím, že léčba obezity a diabetu 2. typu se týká obrovské populace, což odčerpává kapacity na rozšíření indikací. Lze zachytit například efekty kardioprotektivní a nefroprotektivní, snížení systolického i diastolického tlaku, hepatální efekty (ovlivnění steatózy, přechodu do fibrózy a cirhózy – včetně bioptických studií), snížení rizika embolizací, prevenci a možná i léčbu Alheimerovy choroby, prevenci a léčbu v adiktologii či léčbu neplodnosti, léčbu endometriální hyperplazie a léčbu osteoporózy.
Závěr
Inkretinová léčba zcela zásadně změnila moderní léčbu diabetu 2. typu a obezity. Rozvoj této léčby lze očekávat až v deseti dalších oborech medicíny a možná dojde i k preventivnímu využití v řadě oborů.
V prevenci diabetu 2. typu je pokles výskytu diabetu až o 93 %, výrazné jsou efekty na prevenci kardiovaskulárních a renálních komplikací. Osud již dnes užívaných léků bude pravděpodobně podobný jako u gliflozinů. Brzy je budou předepisovat kromě diabetologů i nefrologové a kardiologové. Jaký bude další vývoj medicíny v oblasti inkretinů, nelze do detailu předvídat. Před dvaceti lety jsme se domnívali, že trávicí trakt mají živočichové jen na trávení a vstřebávání živin. Jakým způsobem ovlivní objevené hormony trávicího traktu mnoho dalších orgánů a orgánových systémů, nikdo netušil. Rozvoj inkretinové léčby lze snad už dnes srovnat s úspěchy cílené biologické léčby v onkologii, gastroenterologii, oftalmologii či revmatologii. Nejbližších dvacet let přinese zcela jistě ještě větší změny farmakoterapie, než zaznamenala historie minulých dvaceti let.
Zdroje
1.
Svačina Š. Antidiabetika, historie, současnost a budoucnost. Praha: Axonite, 2016.2.
Nauck M, et al. Reduced incretin effect in type 2 (non-insulin-dependent) diabetes. Diabetologia 1986;29(1):46–52.3.
Rehfeld JF. The origin and understanding of the incretin concept. Front Endocrinol (Lausanne) 2018;9 : 387.4.
Marks V. The early history of GIP 1969–2000: From enterogastrone to major metabolic hormone. Peptides 2019 : 122 : 170155.5.
Gregory RA. The Bayliss-Starling lecture 1973. The gastrointestinal hormones: a review of recent advances. J Physiol 1974;241(1):1–32.6.
Helrick H, et al. Plasma insulin response to oral and intravenous glucose administration. J Clin Endocrinol Metab 1964;24 : 1076–82.7.
Nauck MA, Meier JJ. Incretin hormones: Their role in health and disease. Diabetes Obes Metab 2018;20(Suppl 1):5–21.8.
Rentzeperi E, et al. Sex differences in response to treatment with glucagon-like peptide 1 receptor agonists: Opportunities for a tailored approach to diabetes and obesity care. J Pers Med 2022;12(3):454.9.
Svačina, Š. Antiobezitika – vývoj, současnost a perspektivy. Praha: Grada Publishing, 2022.10.
Svačina, Š. Tirzepatid jako posel budoucnosti – nové antidiabetikum se širokými perspektivami. Aktuální medicína 2023;7(1):43–48.11.
Dissanayake HA, Somasundaram NP. Polyagonists in type 2 diabetes management. Curr Diab Rep 2024;24 : 1–12.12.
Rosenstock J, et al. Efficacy and safety of a novel dual GIP and GLP-1 receptor agonist tirzepatide in patients with type 2 diabetes (SURPASS-1):
a double-blind, randomised, phase 3 trial. Lancet 2021;398 : 143–155.13.
Jastreboff AM, et al. Tirzepatide for obesity treatment and diabetes prevention. NEJM-OA November 13, 2024.14.
Yao, H, et al. Comparative effectiveness of GLP-1 receptor agonists on glycaemic control, body weight, and lipid profile for type 2 diabetes systematic review and network meta-analysis. BMJ 2024;384:e076410.15.
https://www.amgen.com/newsroom/press-releases/2024/11/amgen-announces-robust-weight-loss-with-maritide-in-people-living-with-obesity-or-overweight-at-52-weeks-in-a-phase-2-study.16.
Svačina Š. Inkretinová léčba – historie, současnost a budoucnost. Mlečice: Axonite 2025. [Před tiskem.]Štítky
Praktické lékařství pro děti a dorost Praktické lékařství pro dospělé
Článek Úvodní slovoČlánek Remise diabetu
Článek vyšel v časopiseSvět praktické medicíny
Nejčtenější tento týden
- Na inkontinenční pomůcky nově dosáhne více pacientů
- MUDr. Jiří Kornoušek: Program našich konferencí stavíme tak, aby reflektoval skutečně aktuální a praktická témata
- Naděje budí časná diagnostika Parkinsonovy choroby založená na pachu kůže
- Úloha praktického lékaře v péči o inkontinentní pacienty
- Zápach při inkontinenci je častou obavou pacientů
-
Všechny články tohoto čísla
- Úvodní slovo
- Dysurie: hodnocení a diferenciální diagnostika u dospělých
- Dysurie: hodnocení a diferenciální diagnostika u dospělých
- Polymorbidní pacient v ordinaci všeobecného praktického lékaře
- Remise diabetu
- Semaglutid, zejména perorální, a jeho vliv na kardiovaskulární riziko
- Wegovy® (semaglutid 2,4 mg s. c.) v terapii nadváhy a obezity
- Inkretiny – přelomová léčba diabetu a obezity je jen začátek...
- Rozhovor s MUDr. Janem Šoupalem, Ph.D. Umělá inteligence může řešit nedostupnost a standardizaci péče o pacienty
- Jaké inzuliny máme v současnosti k dispozici? (změny v portfoliu)
- Diabetické onemocnění ledvin – jak jej nepřehlédnout a správně léčit v roce 2025 podle moderních poznatků?
- Steatotické postižení jater a pankreatu u diabetiků
- Diagnostika a management hypertenze
- Zácpa – choroba více odborností
- Cílená léčba intersticiálních plicních procesů
- Probiotika a diabetes mellitus
- Znalostní test: 2 kredity ČLK
- Nové registrace Evropskou lékovou agenturou
- Svět praktické medicíny
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Wegovy® (semaglutid 2,4 mg s. c.) v terapii nadváhy a obezity
- Inkretiny – přelomová léčba diabetu a obezity je jen začátek...
- Dysurie: hodnocení a diferenciální diagnostika u dospělých
- Zácpa – choroba více odborností
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: MUDr. Petr Výborný, CSc., FEBO
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



