Pacientka trpí psoriázou od 27 let věku. Jedná se o chronickou ložiskovou psoriázu, současně mnoho let trvá těžké postižení nehtů a žena rovněž trpí výraznými šupivými projevy ve kštici. Byla odeslána ambulantním dermatologem ke zvážení indikace biologické léčby. V péči naší ambulance je od dubna 2024.
Rodinná anamnéza stran psoriázy je negativní. Pacientka neudává žádné alergie. Léky dlouhodobě neužívá. S ničím vyjma psoriázy se neléčí. Onkologické onemocnění nikdy neprodělala, na gastroenterologii se nikdy neléčila. 3 roky nekouří, alkohol pije příležitostně – 2 jednotky za týden. Pracovala jako dělnice v kovovýrobě.
Mnoho let se léčila lokálními externy s kortikoidy, keratolytiky, kalcipotriolem. Stran deformit nehtových plotének byla léčena u svého ambulantního dermatologa opakovaně lokálními i celkovými antimykotiky, avšak bez efektu.
Methotrexát užívala v dávce 10 mg týdně od února 2024 do července 2024, poté byl vysazen pro neúčinnost. Při této léčbě nebylo dosaženo zlepšení PASI o > 50 %.
Acitretin užívala v dávce 50 mg/den od 17. 9. do 7. 10. 2024, poté byla dávka snížena na 25 mg/den pro netoleranci (sucho v ústech, časté opary na rtech, olupování kůže na ploskách s bolestivostí). Léčivo užívala celkem 2 měsíce, do 22. 11. 2024, avšak nedošlo ani k částečnému zlepšení stavu. Acitretin navíc musel být vysazen pro netoleranci.
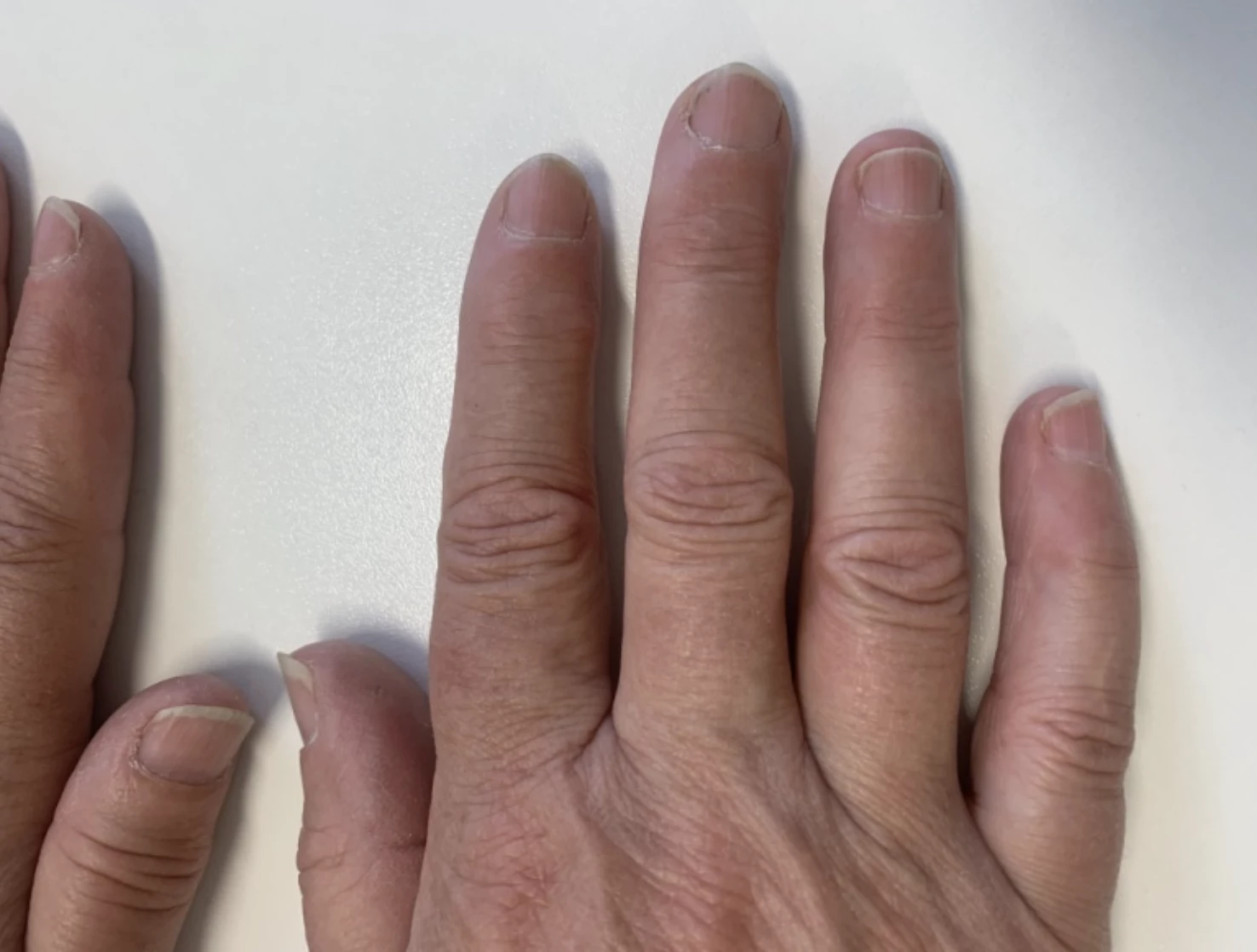
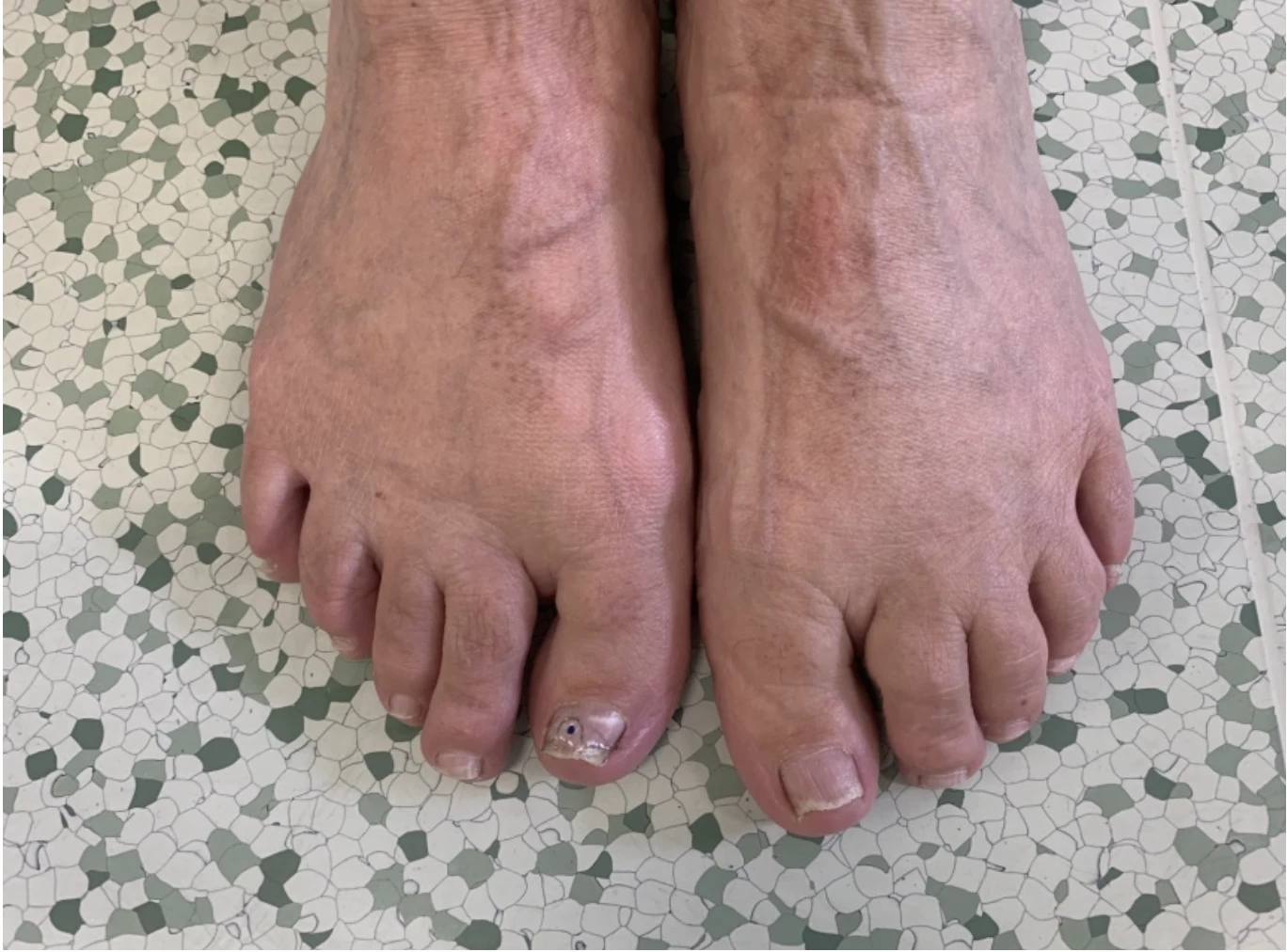
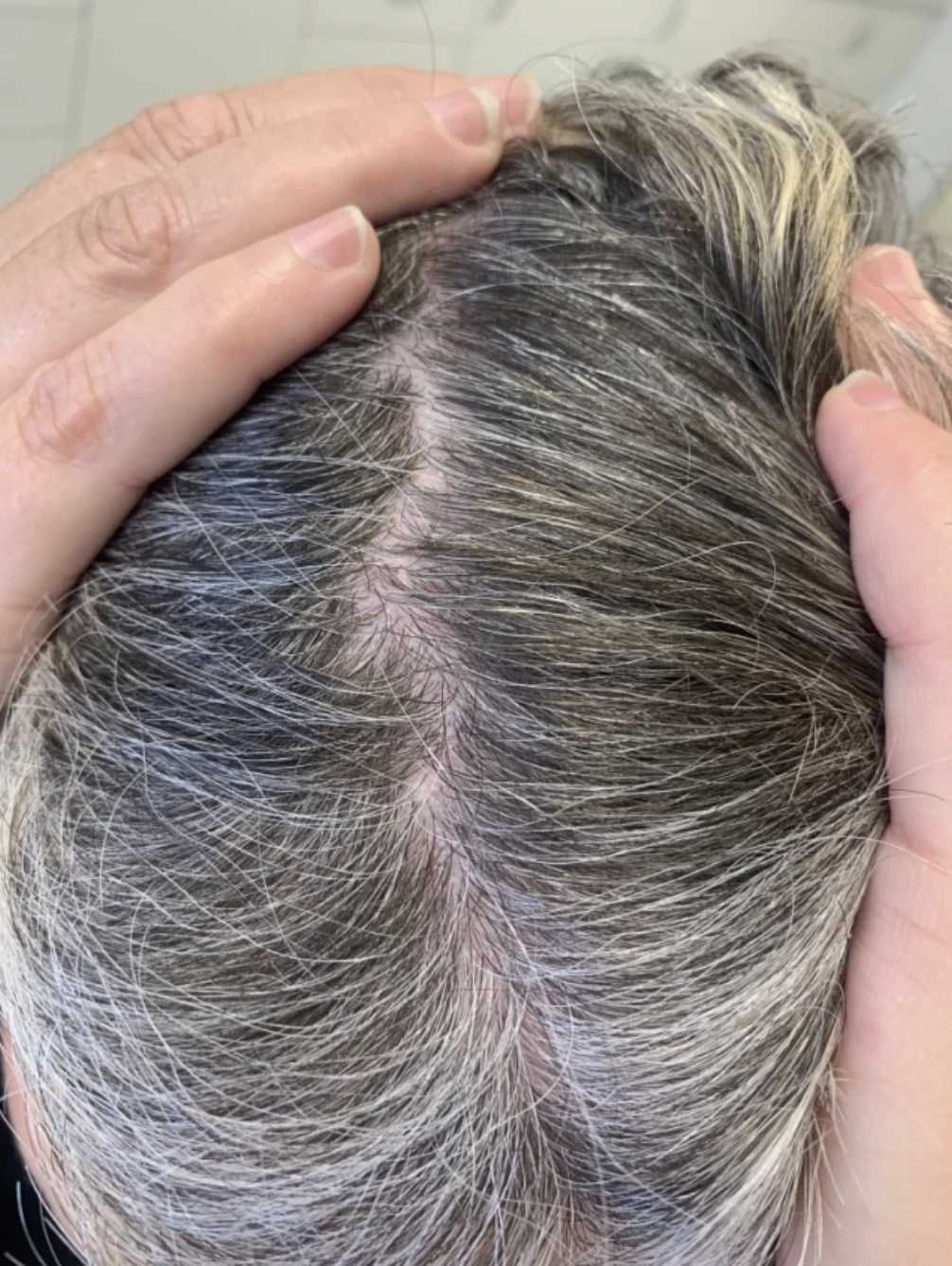
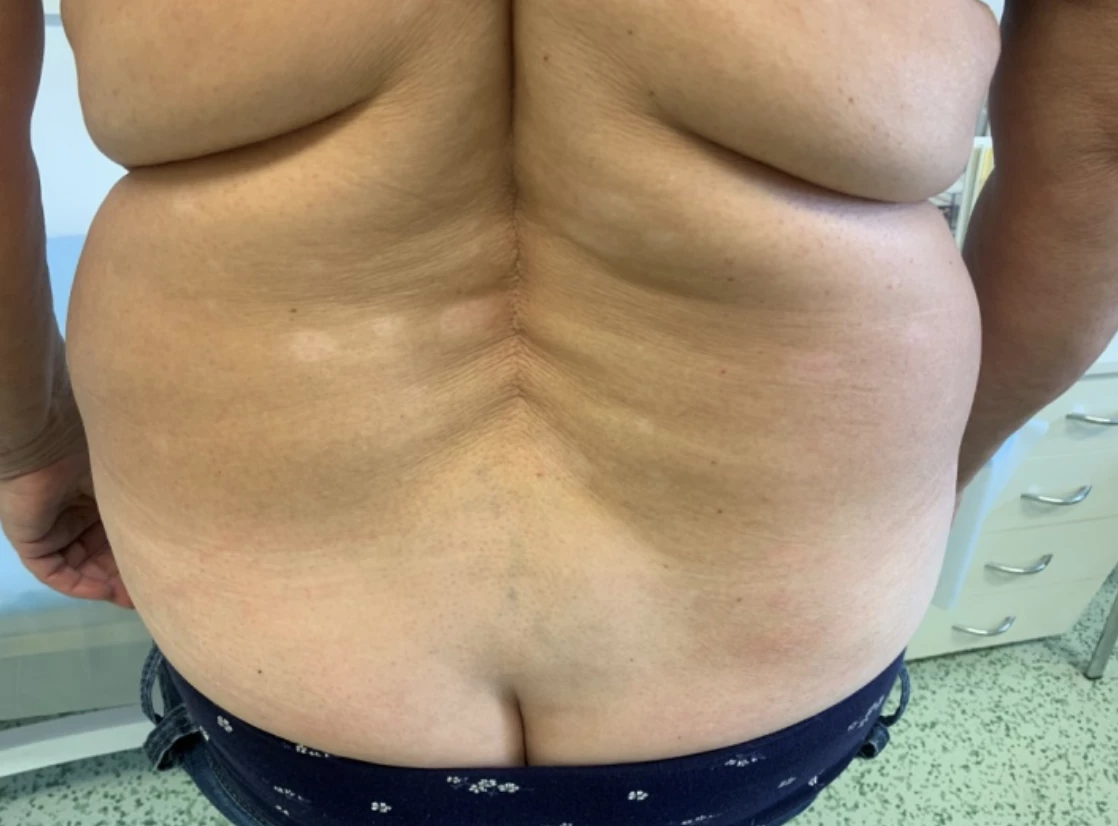
Jedná se o středně těžkou psoriázu s postižením kštice a všech nehtů na rukou a nohou. Nehty na horních (HKK) i dolních končetinách (DKK) silně dystrofické s onycholýzou. Skóre NAPSI dosahuje 122. Na trupu a hýždích jsou psoriatické zašupené červené plaky, ve kštici nánosy stříbrných šupinek. Skóre PSSI činí 40, BSA 15 %, PASI 11,6, DLQI 18.
Obr. 1 Stav před nasazením bimekizumabu: a) postižení nehtů HKK, b) postižení nehtů HKK, c) postižení kštice, d) psoriatické plaky na trupu a hýždích
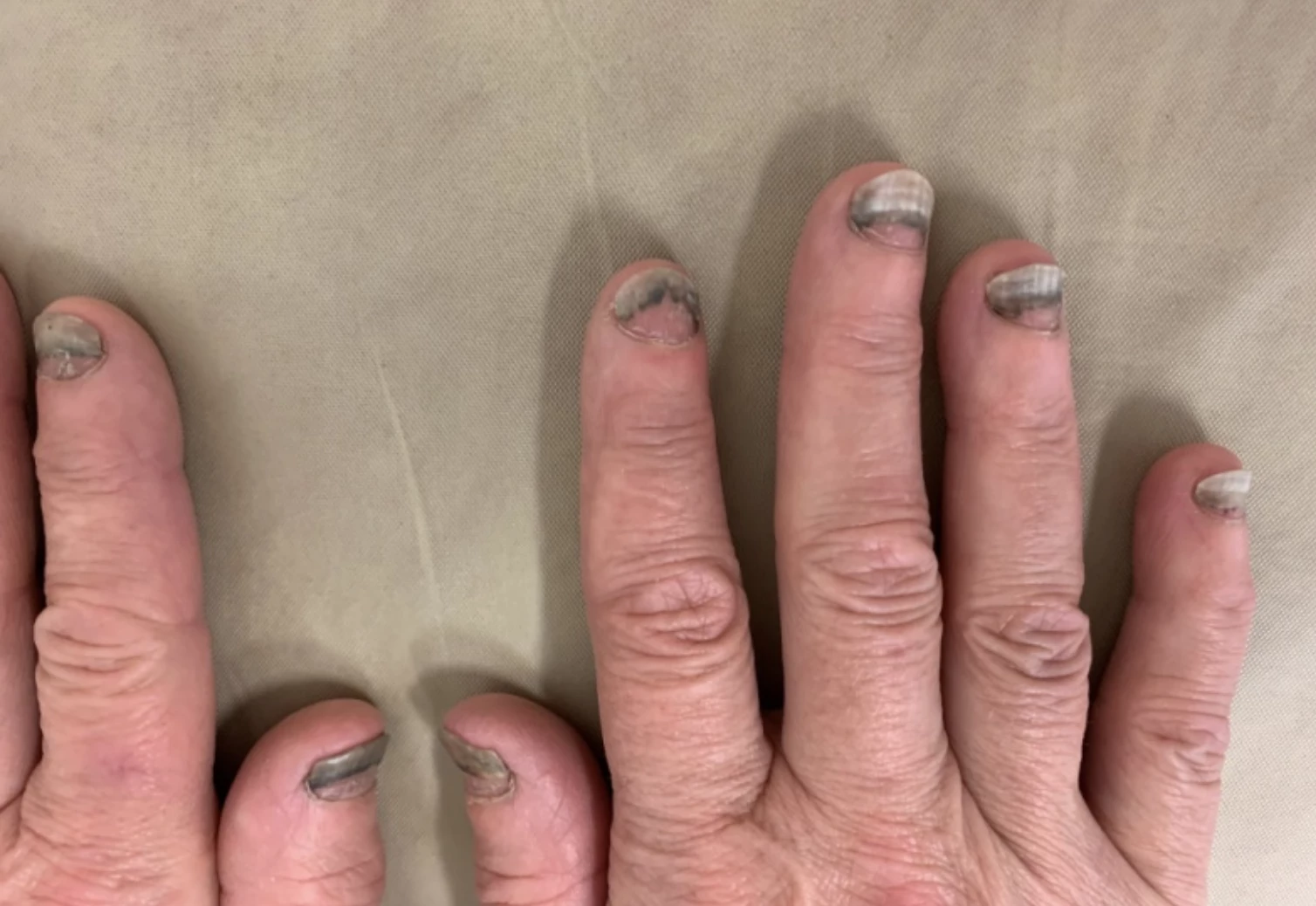
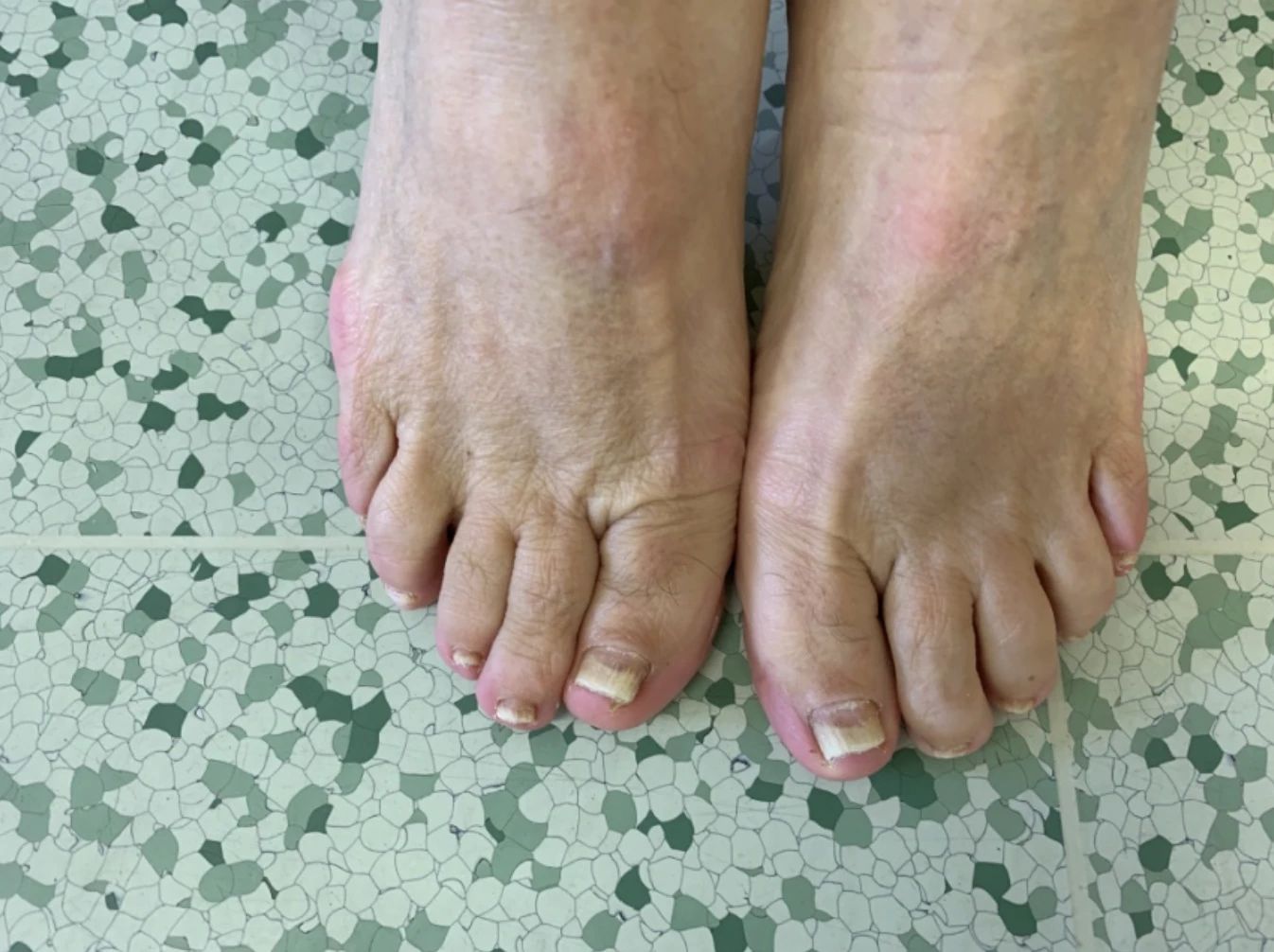
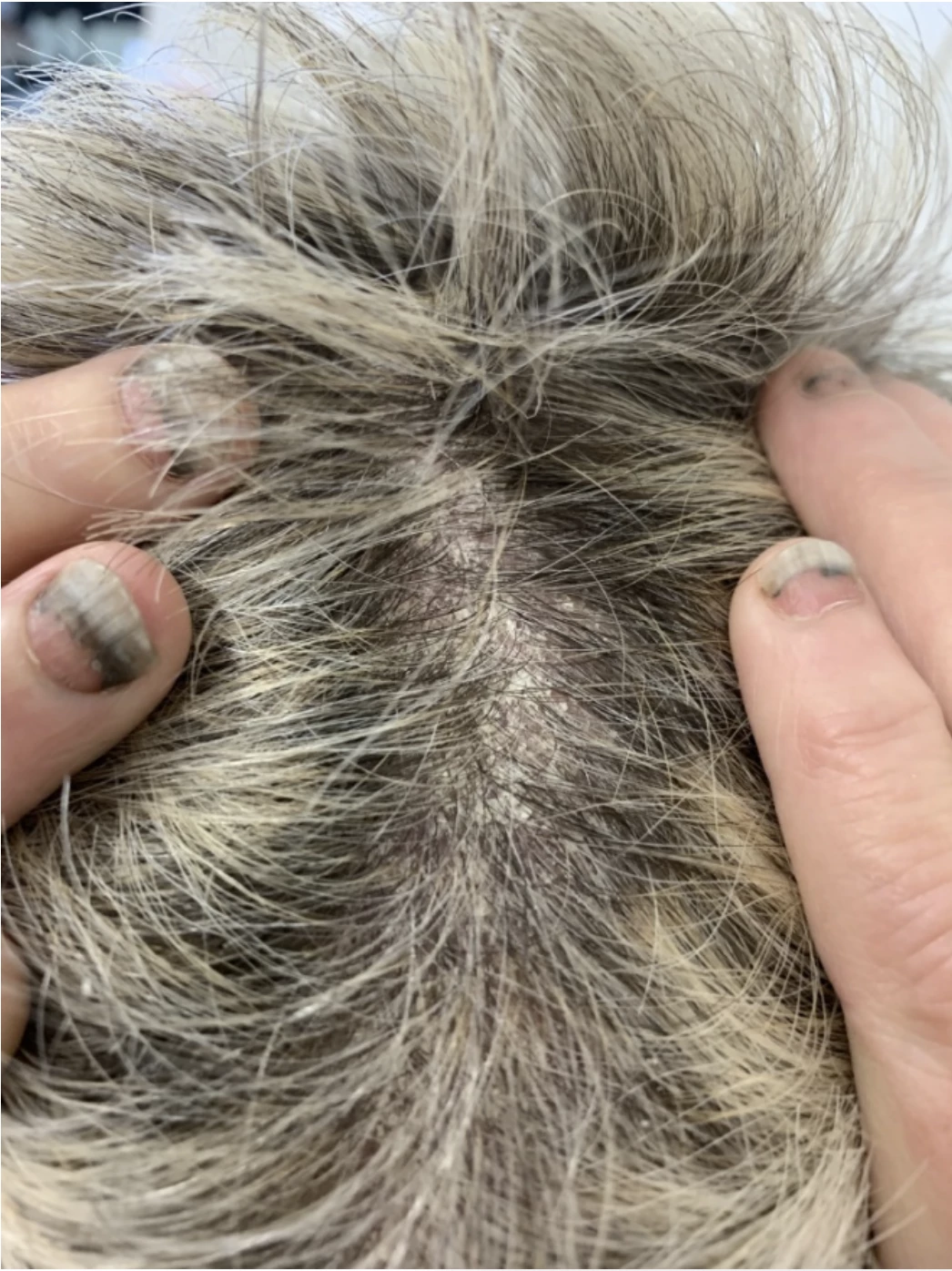
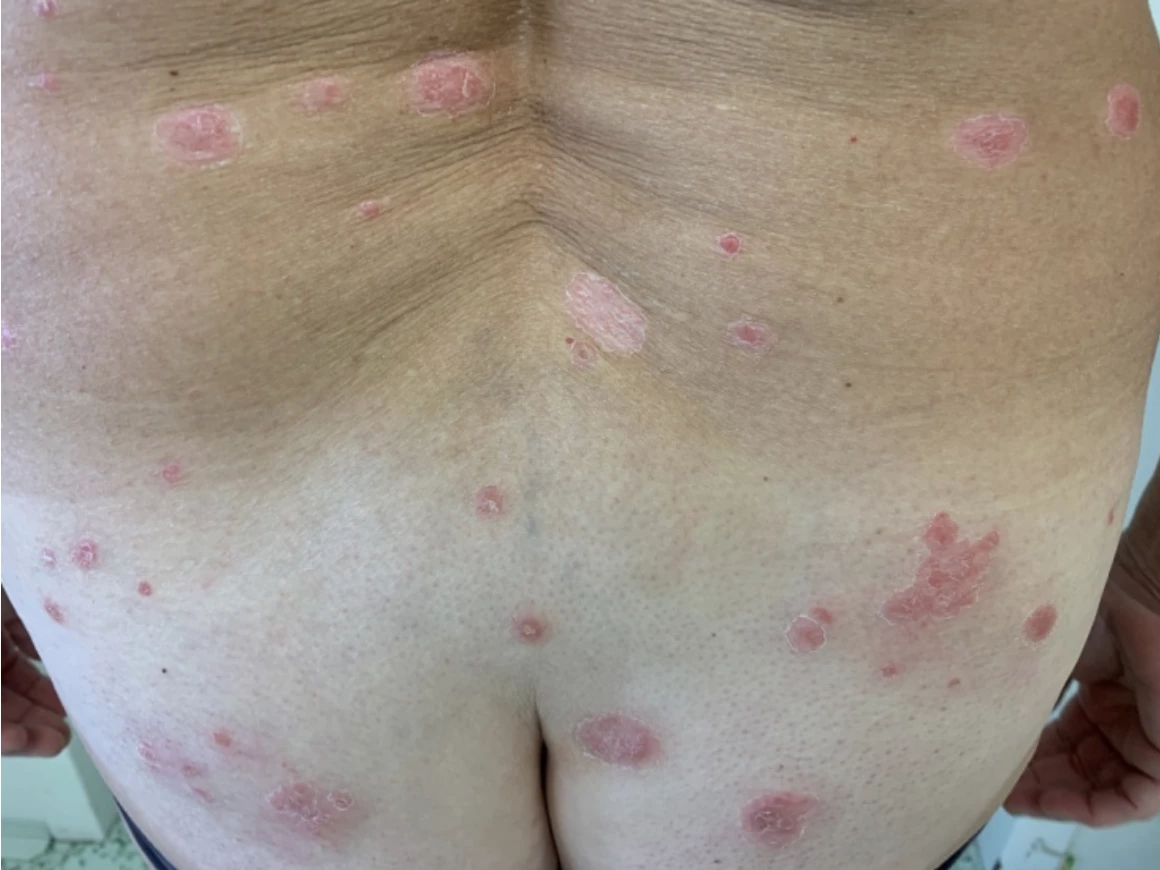
Pacientka splnila kritéria pro podání biologické léčby stran rozsahu onemocnění psoriázou (viz výše) i co se týká dosud proběhlé terapie, kdy nebylo dosaženo uspokojivého léčebného efektu na methotrexátu ani acitretinu, který byl navíc netolerován. Nedošlo ke zlepšení skóre PASI o > 50 s těmito 2 modalitami celkové léčby. Pacientka měla výrazně zhoršenou kvalitu života. Především postižení nehtů ji velmi omezovalo v každodenním životě a při kontaktu s lidmi.
Vstupní laboratorní vyšetření byla bez patologických odchylek, plicní vyšetření v pořádku a odběr kvantiferonu negativní. Od počátku ledna 2025 byla zahájena léčba bimekizumabem v dávce 160 mg 2 inj. s.c. v týdnu 0 a každé 4 týdny do 16. týdne, dále každých 8 týdnů.
Při kontrolním vyšetření po 16 týdnech léčby byly psoriatické plaky na kůži trupu i končetin zcela zhojeny, nehty odrůstají zdravé – na rukou již zdravé celé, na nohou jen distálně ztluštění do 2 mm. Psoriáza kštice zhojena. Pacientka je velmi spokojená. Potíže s kvasinkovou dermatitidou nemá žádné, nevyskytly se ani jiné nežádoucí vedlejší účinky. Klouby nebolí. Bylo dosaženo hodnot BSA 0, PASI 0, DLQI 0, NAPSI 0, PSSI 0.
Obr. 2 Stav postižených oblastí po 16 týdnech terapie bimekizumabem
Bimekizumab je humanizovaná monoklonální IgG1 protilátka vyvinutá pro selektivní inhibici IL‑17A a IL‑17F. Molekula má inovativní uspořádání s duální specificitou pro IL‑17A a IL‑17F a s vysokou afinitou k těmto interleukinům. Cílí na 3 dimery: IL‑17A/A, IL‑17A/F, IL‑17F/F. Inhibitory IL‑17A efektivně neutralizují dimery IL‑17A/A a IL‑17A/F. Experimentem in vitro byl bimekizumab porovnáván se secukinumabem a ixekizumabem a bylo doloženo, že bimekizumab inhibuje navíc k IL‑17A/A a IL‑17A/F také IL‑17F/F. Poměr IL‑17A a IL‑17F je velmi důležitý u onemocnění zprostředkovaných IL‑17. Samotná inhibice IL‑17A je účinná při poměru IL‑17A a IL‑17F 1 : 1. Avšak pokud je mnohem vyšší koncentrace IL‑17F, je třeba jej více blokovat. V případě psoriázy je tento poměr 1 : 30, z tohoto důvodu je tedy působení bimekizumabu na onemocnění mnohem efektivnější než samotná inhibice IL‑17A.3
U pacientů léčených bimekizumabem bylo v 16. týdnu pozorováno zlepšení psoriázy postihující pokožku hlavy, nehty, dlaně a chodidla. U pacientů s výchozí hodnotou skóre mNAPSI > 10 na začátku léčby se míra zhojení nehtů zvyšovala do 1. roku a udržela se do 3. roku; míra zhojení odrážela delší dobu potřebnou pro růst a regeneraci nehtů. Ve studii BE VIVID dosáhlo v 52. týdnu 60,3 % pacientů léčených bimekizumabem 320 mg každé 4 týdny kompletní clearance nehtů (mNAPSI 100). Ve studii BE READY dosáhlo v 56. týdnu 67,7 % a 69,8 % respondérů ze stavu PASI 90 v 16. týdnu kompletní clearance nehtů s bimekizumabem 320 mg aplikovaným každých 8 týdnů, respektive každé 4 týdny. Pacienti s výchozí hodnotou skóre scalp IGA ≥ 3 na začátku léčby dosáhli vysoké míry zhojení po 16 týdnech a ta přetrvávala po dobu 3 let.2
Dlouhodobá bezpečnostní data (až 3 roky trvající sledování) potvrzují nízký výskyt závažných infekcí, malignit, velkých kardiovaskulárních příhod (MACE) či idiopatických střevních zánětů (IBD) na terapii bimekizumabem Mykotické infekce se při terapii bimekizumabem vyskytují ve zvýšené míře (hlavně orální kandidóza), ale v průběhu času se jejich výskyt snižuje.
Tyto výsledky potvrzují první data z reálné praxe, kde běžné infekty horních cest dýchacích (HCD) a orální kandidóza jsou jediné časté nežádoucí účinky, nejsou však zpravidla hodnoceny jako závažné.2, 3
Doporučená dávka bimekizumabu pro dospělé pacienty s ložiskovou psoriázou činí 320 mg (podaných jako 2 s.c. injekce po 160 mg nebo 1 s.c. injekce po 320 mg) v 0., 4., 8., 12. a 16. týdnu a poté každých 8 týdnů. Terapeutickými indikacemi bimekizumabu jsou ložisková psoriáza, psoriatická artritida, axiální spondylartritida a hidradenitis suppurativa.
Bimekizumab v našem případu prokázal velmi dobrou účinnost na psoriázu kštice, nehtů i na ložiskovou psoriázu. V rámci terapie se nevyskytly žádné nežádoucí vedlejší účinky.
Pozorovali jsme rychlý nástup léčebného účinku na ložiskovou psoriázu, psoriázu kštice i na psoriatické změny nehtů. Pacientka je s léčbou velmi spokojena a má významně zlepšenou kvalitu života.
MUDr. Hana Janatová
Kožní oddělení, Nemocnice České Budějovice
Reference:
1. Šternberský J., Tichý M. Bimekizumab – nové biologikum v terapii psoriázy. Dermatologie pro praxi 2022; 16 (4): 231–234, doi: 10.36290/der.2022.047.
2. SPC Bimzelx. Dostupné na: www.ema.europa.eu/en/documents/product-information/bimzelx-epar-product-information_cs.pdf
3. Reich K., Papp K. A., Blauvelt A. et al. Bimekizumab versus ustekinumab for the treatment of moderate to severe plaque psoriasis (BE VIVID): efficacy and safety from a 52‑week, multicentre, double‑blind, active comparator and placebo controlled phase 3 trial. Lancet 2021; 397: 487–498, doi: 10.1016/S0140-6736(21)00125-2.
Fotodokumentace: archiv kožního oddělení Nemocnice České Budějovice