-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Diferenciální diagnostika vrozených vad hrtanu u dětí
Differential diagnosis of congenital laryngeal anomalies in children
Congenital laryngeal anomalies present a heterogeneous group of conditions, most commonly manifesting as inspiratory or biphasic stridor and swallowing difficulties in neonates and infants. Their true prevalence is likely underestimated, particularly in milder forms. The aim of this article is to provide an overview of the most common congenital laryngeal anomalies and current diagnostic and therapeutic approaches in paediatric otolaryngology. The review summarizes literature-based knowledge on key congenital laryngeal pathologies, including laryngomalacia, bilateral vocal fold paresis, subglottic stenosis, subglottic haemangioma, laryngeal webs, and clefts. Both conservative and surgical strategies are presented, including pharmacological treatment (e. g., propranolol for subglottic haemangioma), as well as endoscopic and open surgical interventions. The article also highlights frequent associations with other congenital malformations and syndromes, underscoring the need for multidisciplinary management. Early diagnosis and timely intervention are essential to prevent complications such as respiratory failure or aspiration. A comprehensive and individualized approach is crucial for the effective management of congenital laryngeal anomalies in the paediatric population.
Keywords:
laryngomalacia – congenital subglottic stenosis – vocal fold paresis – subglottic haemangioma – paediatric otolaryngology
Autoři: Anna Švejdová 1,2
; Jana Šatanková 1,2
; E. Šejvlová 1; V. Chrobok 1,2
Působiště autorů: Klinika otorinolaryngologie a chirurgie hlavy a krku, Fakultní nemocnice Hradec Králové 1; Univerzita Karlova, Lékařská fakulta v Hradci Králové 2
Vyšlo v časopise: Otorinolaryngol Foniatr, 74, 2025, No. 4, pp. 316-323.
Kategorie: Přehledová práce
doi: https://doi.org/10.48095/ccorl2025316Souhrn
Vrozené vady hrtanu představují heterogenní skupinu onemocnění, která se nejčastěji manifestují inspiračním nebo inspiračně-exspiračním stridorem a poruchami polykání u novorozenců a kojenců. Jejich výskyt je pravděpodobně podhodnocen, zejména u lehčích forem. Cílem článku je poskytnout přehled nejčastějších vrozených malformací hrtanu a současných diagnostických a terapeutických možností v dětské otorinolaryngologii. Přehledová práce shrnuje literární poznatky týkající se hlavních kongenitálních vad hrtanu, mezi které patří laryngomalacie, oboustranná paréza hlasivek, subglotická stenóza, subglotický hemangiom, srůsty a rozštěpy hrtanu. Uvedeny jsou jak konzervativní, tak invazivní terapeutické strategie, včetně farmakoterapie (např. propranolol u subglotického hemangiomu), endoskopických i otevřených chirurgických výkonů. Článek rovněž upozorňuje na časté asociace s jinými malformacemi a syndromy, které vyžadují mezioborovou spolupráci. Včasná diagnostika a správně zvolený léčebný postup jsou zásadní pro prevenci komplikací, jako je respirační selhání nebo aspirace. Komplexní a individualizovaný přístup je klíčem k úspěšnému zvládnutí vrozených vad hrtanu v dětské populaci.
Klíčová slova:
laryngomalacie – kongenitální subglotická stenóza – paréza hlasivek – subglotický hemangiom – dětská otorinolaryngologie
Úvod
Vrozené vývojové vady hrtanu a průdušnice tvoří nejčastější příčinu vrozených stridorů u novorozenců a kojenců, jejich incidence je udávána okolo 0,2–1 na 10 000 živě narozených dětí [1]. Mezi nejčastější vrozené vady patří laryngomalacie, oboustranná paréza hlasivek, subglotická stenóza hrtanu, vrozené srůsty, tzv. webs, hemangiom hrtanu, rozštěpy hrtanu a průdušnice, stenózy průdušnice a tracheomalacie [1–3]. Přestože některé z nich mají tendenci ke spontánnímu zlepšení (např. laryngomalacie), jiné se mohou projevit akutní dušností a vyžadují aktivní intervenci, včetně chirurgické léčby. Mezi nejčastější symptomy patří stridor, který bývá typicky inspirační či inspiračně-expirační dle místa stenózy. Často bývají vrozené vady hrtanu spojeny s chraplavým pláčem, zatahováním pomocného svalstva, ale i cyanózou, poruchami polykání a neprospíváním [4]. V případě aspirací může docházet k opakovaným bronchopneumoniím. Diagnostika je založena na komplexním pediatrickém a ORL vyšetření s důrazem na flexibilní laryngoskopii [3, 4], velkou výhodou je možnost provedení videonahrávky, opětovného prohlédnutí a zpomalení videa. V případě nejasných nálezů nebo nutnosti zmapování rozsahu vady doplňujeme vyšetření v celkové anestezii (rigidní laryngoskopie a tracheobronchoskopie) a zobrazovací vyšetření, jako je CT či MR. Ke zhodnocení polykacích obtíží využíváme flexibilní endoskopické vyšetření polykání (FEES) a videofluoroskopii. Terapie je multidisciplinární a zahrnuje jak konzervativní, tak chirurgické postupy.
Obr. 1. Laryngomalacie, fl exibilní laryngoskopie, dle Olney typ I (nadbytek tkání arytenoidních hrbolů, které jsou nasávány nad nitro hrtanu) a II (zkrácené aryepiglotické řasy, omegovitá epiglotis). Fig. 1. Laryngomalacia, fl exible laryngoscopy, type I (prolapsing supra arytenoid fl oppy tissue) and II (shortened aryepiglottic folds, omega- -shaped epiglottis) according to Olney. 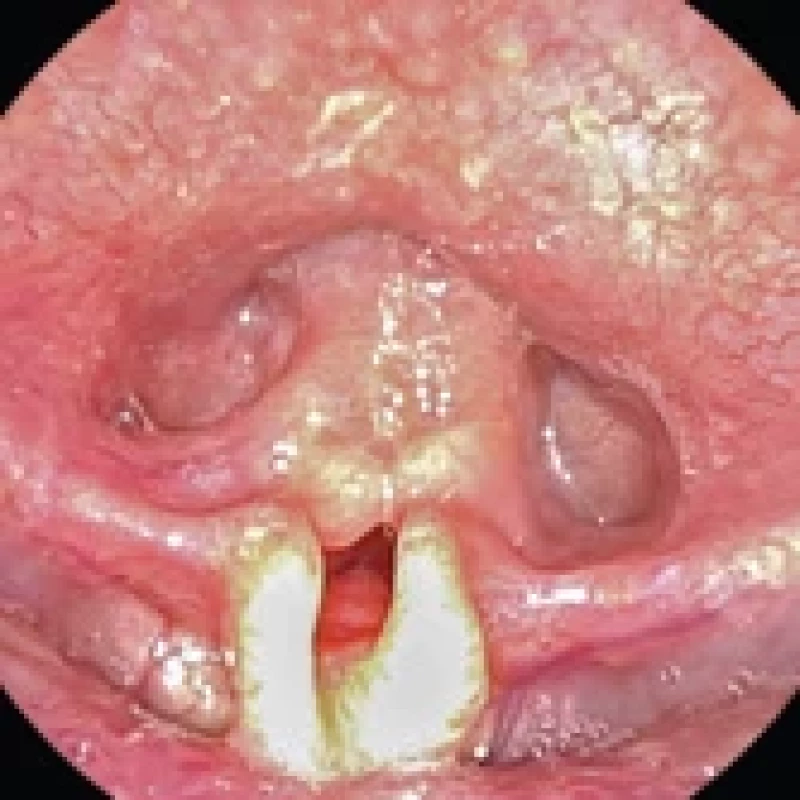
Přehled nejčastějších vrozených vývojových vad hrtanu
Laryngomalacie
Laryngomalacie je nejčastější vrozenou vadou hrtanu a příčinou inspiračního stridoru asi v 60–75 % [1, 5]. Popsali ji již Jackson a Jackson v roce 1942. Vzniká důsledkem nevyzrálosti či nadbytku supraglotických tkání a vede k jejich kolapsu a nasávání směrem do nitra hrtanu při inspiriu (obr. 1). Etiologie onemocnění není dosud objasněna, jednou ze zvažovaných teorií je neurogenní příčina vedoucí k abnormální integraci laryngeálních nervů [6]. Gastroezofageální reflux (GERD) se zatím neprokázal jako kauzální příčina, ale až 60 % dětí s laryngomalacií má projevy GERD. Laryngomalacie se také častěji projeví u dětí s přidruženým neuromuskulárním onemocněním a hypotonickým syndromem, dětí s nízkou porodní hmotností a při prematuritě [7]. Incidence se pohybuje okolo 1 : 2 000–3 000, bez závislosti na pohlaví [7].
Klasifikace dle Olney [8] rozděluje laryngomalacii na tři typy dle postižené sublokality:
- typ I s nadbytkem tkáně v oblasti arytenoidů, které kolabují do nitra hrtanu;
- typ II se vyznačuje krátkými aryepiglotickými řasami a omegovitě stočenou epiglotis;
- typ III má měkké tkáně epiglotis, která přepadává posteriorně a zakrývá nitro hrtanu.
V klinickém nálezu dominuje inspirační stridor, který se může projevit již krátce po narození, zhoršuje se při krmení, pláči a poloze na zádech. Při těžším stupni laryngomalacie může být doprovázen také cyanózou, zástavami dechu, dysfagií a neprospíváním. Diagnózu stanovujeme na základě anamnézy, klinických obtíží a vyšetření flexibilním laryngoskopem. Při vyšetření je třeba se zaměřit také na zhodnocení přítomnosti a stupně refluxních změn (EER – extraezofageální reflux), které jsou většinou přítomny u dětí s mírnými a středně těžkými obtížemi [6]. Důležité je zhodnocení polykacích obtíží, obtíží při krmení a nepřibývání na hmotnosti.
Aspekty diagnostiky a terapie dětí s laryngomalacií lze dle konsenzu mezinárodní pediatrické ORL skupiny [9] rozdělit na:
1. zhodnocení stupně závažnosti (apnoické pauzy, cyanóza, neprospívání apod.);
2. zhodnocení přítomnosti refluxních změn;
3. zhodnocení polykání (FEES, videofluoroskopie);
4. další přidružená onemocnění či syndromy (tab. 1).
Obtíže často vymizí po prvním roce života bez nutnosti chirurgické terapie, většina pacientů je tedy léčena konzervativně. V případě závažné symptomatiky, asi u 10 % dětí (neprospívání, aspirace, nepřibývání na hmotnosti, dušnost), je indikována chirurgická terapie. První volbou je supraglotoplastika, kterou lze provádět pomocí laseru nebo studenými technikami [10], v případě trvajících obtíží a dušnosti je někdy nutné zajistit dýchací cesty tracheostomií, častěji u dětí s přidruženými neurologickými komorbiditami [6]. Doporučený postup péče o děti s laryngomalacií dle stupně postižení uvádí tabulka (schéma 1).
U dětí s laryngomalacií a projevy GERD/EER je třeba zahájit antirefluxní terapii. Lze zvolit dva různé přístupy – eskalační, nebo deeskalační terapii [9]. V případě deeskalační terapie lze současně začít s inhibitory protonové pumpy (PPIs) a inhibitory histaminových H2-receptorů (H2RA), po zmírnění obtíží následně pokračovat v monoterapii (schéma 2). U eskalační terapie naopak začít v monoterapii a při nelepšení obtíží přidat lék z druhé skupiny. Terapie by měla trvat po dobu min. 3 měsíců, po zlepšení obtíží není vhodné vysadit léky naráz, ale postupně snižovat dávku. Užití PPIs však není schváleno u dětí mladších než 1 rok a postup v jejich předepisování není celosvětově jednotný. V případě, že nedochází ke zlepšení obtíží při plné antirefluxní terapii, je nutné doplnit gastroenterologické vyšetření, jícnovou pH-metrii a event. zvážit přidání prokinetik.
Tab. 1. Aspekty diagnostiky a terapie laryngomalacie (převzato od Carter et al. [9]). Tab. 1. Diagnostic and therapeutic aspects of laryngomalacia (according to Carter et al. [9]). ![Aspekty diagnostiky a terapie laryngomalacie (převzato od Carter et al. [9]). Tab. 1. Diagnostic and therapeutic aspects of laryngomalacia (according to Carter et al. [9]).](https://pl-master.mdcdn.cz/media/cache/media_object_image_small/media/image/255cda4b860034400963dcc071beb652.png)
Oboustranná vrozená paréza hlasivek
Oboustranná vrozená paréza hlasivek je druhou nejčastější vrozenou vadou hrtanu asi v 10–20 % případů [11], incidence i prevalence nicméně mohou být podhodnocené. V některých případech bývá jako oboustranná kongenitální paréza hlasivek nesprávně vyhodnocena zadní glotická stenóza. Etiologie není zcela jasná, výskyt bývá častější u dětí s prematuritou, u syndromových dětí nebo je součástí dalších vrozených vad dýchacího traktu (laryngomalacie, stenóza průdušnice, tracheomalacie atd.) [12–14]. Diferenciálně diagnosticky je třeba dále zvažovat traumatickou příčinu, tumory, infekce, neurologická onemocnění, iatrogenní či idiopatický původ. Až u dvou třetin dětí dojde ke spontánní úpravě hybnosti hlasivek do 1–2 let života [15]. Diagnostika se opět opírá o flexibilní endoskopické vyšetření, v rámci pátrání po příčině lze doplnit elektromyografii hrtanu (LEMG), kterou však u dětí provádí jen velmi málo pracovišť, dále vyšetření přímou laryngoskopií v celkové anestezii, zobrazovací vyšetření a neurologické vyšetření.
Mezi symptomy patří inspirační stridor, dechová tíseň, zatahování pomocného dechového svalstva, spánková apnoe a neprospívání asi u 62 % dětí [14]. Při vyšetření přímou laryngoskopií v celkové anestezii je možné se pokusit o zhodnocení mobility krikoarytenoidních skloubení [11] k rozlišení od zadní glotické stenózy [16], mobilita zadní části hlasivek by se však spíše měla hodnotit v rámci vyšetření flexibilní laryngoskopií neboli „awake laryngoskopií“. V rámci vyšetření v celkové anestezii je nutné zhodnotit subglotickou oblast a průdušnici. Opět je důležité také zhodnotit, zda není přítomna porucha polykání. Terapie závisí na stupni obtíží, lze ji rozdělit na akutní (akutní dušnost) a dlouhodobou (hlas, polykací obtíže), chirurgickou a nechirurgickou, dočasnou a permanentní. Snahou je vyhnout se trvalé tracheostomii, pokud to je možné, a preferovat méně invazivní možnosti, umožnit dekanylaci [14], zachovat hlas a nezhoršit polykací obtíže [17]. Mezi nejčastější dočasné chirurgické intervence patří tracheostomie a laterofixace hlasivky, mezi trvalé pak jednostranná a oboustranná chordotomie, arytenoidektomie nebo trvalá tracheostomie [11]. U dospělých pacientů lze ještě zvažovat laryngeální neurostimulaci, u dětí se však tato operace zatím neprovádí [18]. Přehled terapeutických možností a chirurgických intervencí uvádí tab. 2. Každé dítě je třeba řešit individuálně dle přidružených onemocnění a dle symptomatiky.
Schéma 1. Management terapie dětí s laryngomalacií (převzato od Carter et al. [9]). Scheme 1. Therapeutic management of childern with laryngomalacia (according to Carter et al. [9]). ![Schéma 1. Management terapie dětí s laryngomalacií (převzato od Carter et al. [9]). Scheme 1. Therapeutic management of childern with laryngomalacia (according to Carter et al. [9]).](https://pl-master.mdcdn.cz/media/image/70dc4eb60e5be56b46328a8014dbc15d.png?version=1766157459)
Schéma 2. Doporučená antirefl uxní terapie u dětí s laryngomalacií dle Cartera et al. [9]. Scheme 2. Recommendations for refl ux therapy in children with laryngomalacia (according to Carter et al. [9]). ![Schéma 2. Doporučená antirefl uxní terapie u dětí s laryngomalacií dle Cartera et al. [9]. Scheme 2. Recommendations for refl ux therapy in children with laryngomalacia (according to Carter et al. [9]).](https://pl-master.mdcdn.cz/media/image/95fe85a0dfc23c160159ab780a20b2cb.png?version=1766157471)
Tab. 2. Management oboustranné vrozené parézy hlasivek. Tab. 2. Managment of bilateral vocal fold paresis. 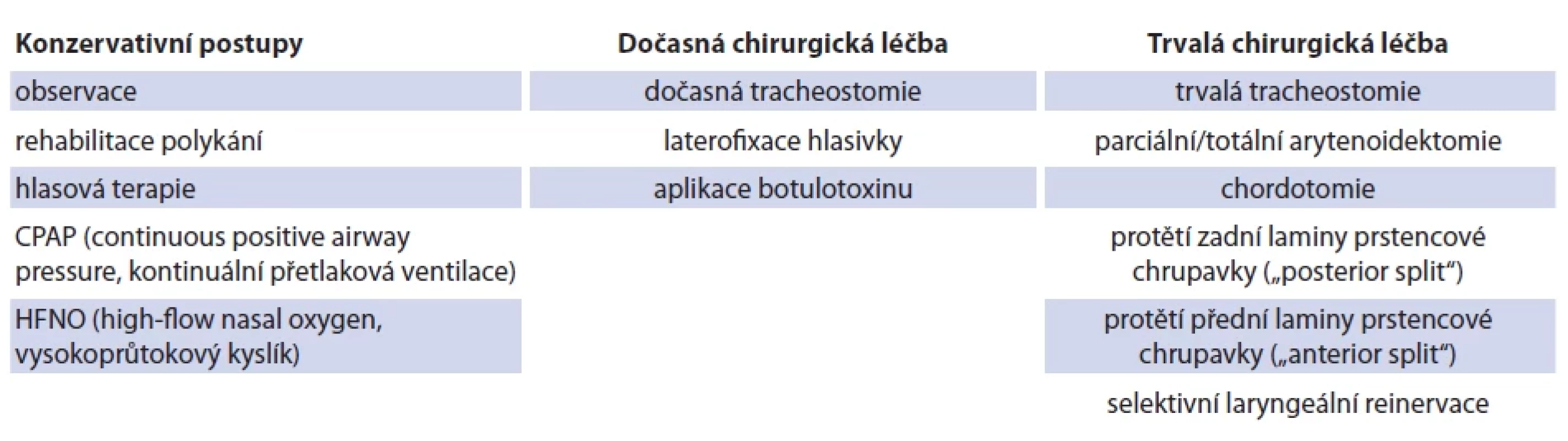
Obr. 2. Kongenitální subglotická stenóza, fl exibilní laryngoskopie, blanitá. Fig. 2. Congenital subglottic stenosis membranous, fl exible laryngoscopy. 
Kongenitální subglotická stenóza
Kongenitální subglotická stenóza je třetí nejčastější vrozenou vadou hrtanu. Je charakterizována průměrem lumen v oblasti prstencové chrupavky < 4 mm u donošeného novorozence a < 3 mm u předčasně narozených dětí [17]. Je nejčastější vrozenou vadou vyžadující tracheostomii [3]. Bývá často asociována s jinými vrozenými vadami v oblasti hlavy a krku, např. s Downovým syndromem. Je způsobena nesprávnou či nekompletní rekanalizací laryngotracheální trubice ve 3. gestačním měsíci, charakterem může být membranózní (blanitá, způsobená hypertrofií submukózní oblasti), anebo chrupavčitá (abnormální tvar prstencové chrupavky), dle tvaru zúžení ji dále rozdělujeme na cirkulární, nebo oválnou/laterolaterální, může přecházet směrem kraniálně ke glottis, nebo kaudálně do průdušnice (obr. 2). Lehký stupeň zúžení se může projevit až v rámci infektů dýchacích cest nebo při zátěži, středně těžká a závažná stenóza se projevuje chronickým inspiračně-expiračním stridorem, chrapotem, dušností a namáhavým dýcháním. Flexibilní laryngoskopie může často ukázat normální nález v hrtanu v oblasti glottis a supraglottis. Při podezření na subglotickou stenózu je nutná rigidní laryngotracheobronchoskopie a event. dále zobrazovací vyšetření. V rámci diferenciální diagnostiky se subgloticky také může nacházet hemangiom, anamnéza stridoru zde však nezačíná ihned po narození, ale okolo 6.–9. týdne věku dítěte [17] (viz dále v textu).
U vrozené kongenitální subglotické stenózy často dojde k vymizení obtíží s růstem dítěte na rozdíl od získané subglotické stenózy, která perzistuje [19]. U těchto dětí je však třeba dbát zvýšené pozornosti v rámci respiračních infektů, při intubaci se maximálně snažíme snížit traumatizaci a event. profylakticky podáváme kortikoterapii. Závažné obstrukce vyžadují v akutní fázi endotracheální intubaci, event. tracheostomii. Možnosti chirurgické léčby závisí na charakteru stenózy, lze provádět endoskopické dilatace a rozrušení či rozsáhlejší výkony, jako je např. laryngotracheoplastika s vložením chrupavčitého štěpu do prstencové chrupavky [20] nebo krikotracheální resekce [17].
Tab. 3. Klasifi kace hrtanových srůstů dle Cohena. Tab. 3. Classifi cation of laryngeal webs according to Cohen. 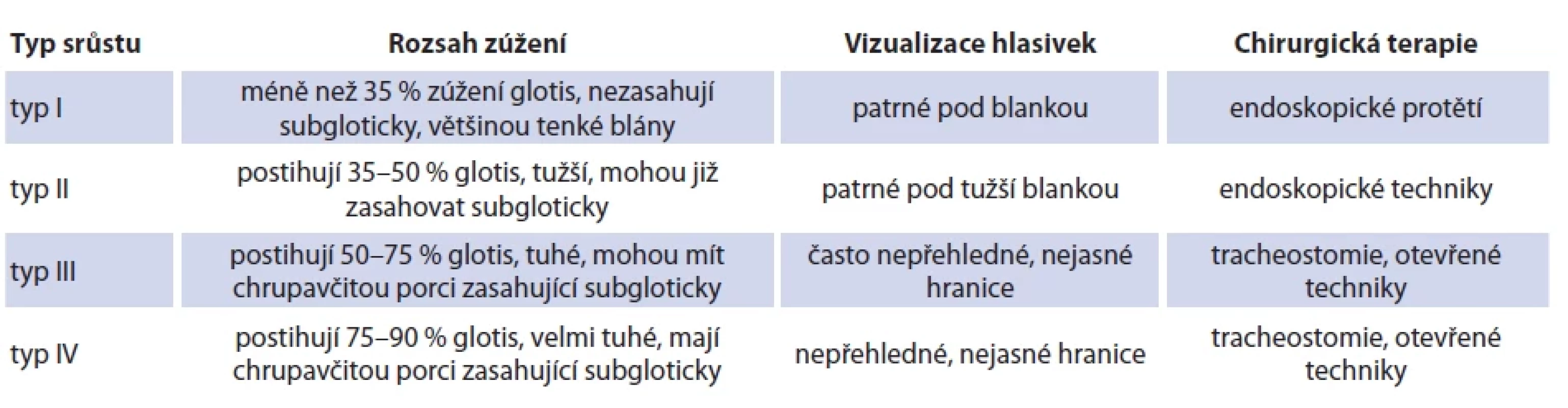
Vrozené srůsty hrtanu („laryngeal webs“), atrezie hrtanu a syndrom vrozené obstrukce horních cest dýchacích („CHAOS – congenital high airway obstruction syndrome“)
Obdobně jako vrozená subglotická stenóza jsou vrozené srůsty hrtanu („webs“) a atrezie způsobeny chybnou rekanalizací laryngotracheální trubice v průběhu embryonálního vývoje [21]. Srůsty se většinou nacházejí v oblasti glottis, asi 95 % v přední komisuře [17], někdy se propagují dále subgloticky jako tzv. plachta. Symptomy závisí na velikosti srůstu (tenké průsvitné blanky až silné vazivové přepážky), může se jednat o mírné formy dysfonie včetně tzv. kočičího mňoukání až o závažnou, život ohrožující obstrukci (syndrom vrozené obstrukce horních cest dýchacích / CHAOS – congenital high airway obstruction syndrome). Stridor bývá po narození přítomen vzácně, nejčastěji v případě interarytenoidního srůstu (zadní glotická stenóza). Syndrom vrozené obstrukce horních cest dýchacích lze diagnostikovat již prenatálně pomocí ultrasonografie. Typickým nálezem jsou zvětšené echogenní plíce, dilatované dolní dýchací cesty, oploštěná nebo evertovaná bránice a fetální ascites. V těchto případech často dojde k úmrtí plodu. Pokud dojde k porodu plodu, pak je třeba ihned zajistit dýchací cesty intubací nebo tracheostomií při zachovaném placentálním oběhu [1]. Tradičně se hrtanové srůsty klasifikují dle Cohena na čtyři subtypy (tab. 3) [21].
V literatuře se popisuje asociace srůstů hrtanu s kongenitální subglotickou stenózou a tracheoezofageální píštělí [21], asociace přední glotické stenózy se Sphrintzen-Goldbergovým [3] a DiGeorgovým syndromem (mikrodelece chromozomu 22q11.2) [17]. U těchto dětí je proto vhodné zvážit genetické vyšetření. V diagnostice se uplatňuje jak flexibilní, tak rigidní bronchoskopie. Léčba závisí na velikosti blány, tenké blanky v oblasti přední komisury mohou prasknout během intubace nebo je lze řešit protětím při přímé laryngoskopii. Silnější vazivové přepážky pak tracheostomií a event. odloženou operací a etapovým přístupem (otevřené techniky s vložením keelu do přední komisury, rekonstrukce z otevřené laryngofisury).
Subglotický hemangiom hrtanu
Hemangiomy patří mezi nejčastější vrozené benigní cévní tumory u dětí [22], vyskytují se především na kůži, mohou však postihovat i jiné části těla. Subglotická oblast je nejčastějším místem výskytu v dýchacích cestách. Dívky jsou postiženy dvakrát častěji než chlapci. Průběh je stejný jako u kožních hemangiomů. Během 1.–3. měsíce života dochází k rychlé proliferaci buněk, po několika měsících pak ke spontánní involuci. Děti jsou nejvíce symptomatické mezi 3. a 6. měsícem života, kdy se začne objevovat inspiračně-expirační stridor, štěkavý kašel, chraptivý pláč a dítě přestane prospívat, většina dětí má i dechové obtíže. Léze je patrná na zobrazovacím vyšetření (MR T2 vážení nebo CT vyšetření) a při flexibilní laryngoskopii (obr. 3). Asi polovina dětí má současně kožní hemangiomy v oblasti hlavy a krku [1], riziko výskytu subglotického hemangiomu se zvyšuje, pokud se kožní hemangiom nachází v oblasti, kde bývají vousy (brada, čelist a preaurikulárně) [23]. Vzhledem k riziku krvácení se nedoporučuje provádět biopsii léze. Většina dětí vyžaduje léčbu, dnes je na prvním místě podávání propranololu (neselektivní betablokátor). Ostatní farmakoterapie, jako je systémová a intralezionální kortikoterapie, vinkristin, bleomycin a interferon alfa-2a, jsou používány jako záchranná terapie, chirurgické techniky a tracheostomie jsou vyhrazeny pro život ohrožující případy a při nedostatečném efektu farmak [24]. V současnosti nejsou stanovena guidelines pro terapii propranololem, dle Schwartz et al. [22], kteří provedli systematickou review, je obvyklá dávka 2 mg propranololu/kg/den (1–3 mg/kg/den), průměrný věk při zahájení terapie 2,9 měsíců, průměrná délka podávání 7,6 měsíců. U menší části dětí může dojít k rebound fenoménu a opětovnému nárůstu hemangiomu po vysazení propranololu, jeho vysazení je proto třeba provádět postupně [22].
Obr. 3. Subglotický hemangiom, fl exibilní laryngoskopie. Fig. 3. Hemangioma of subglottis, fl exible laryngoscopy. 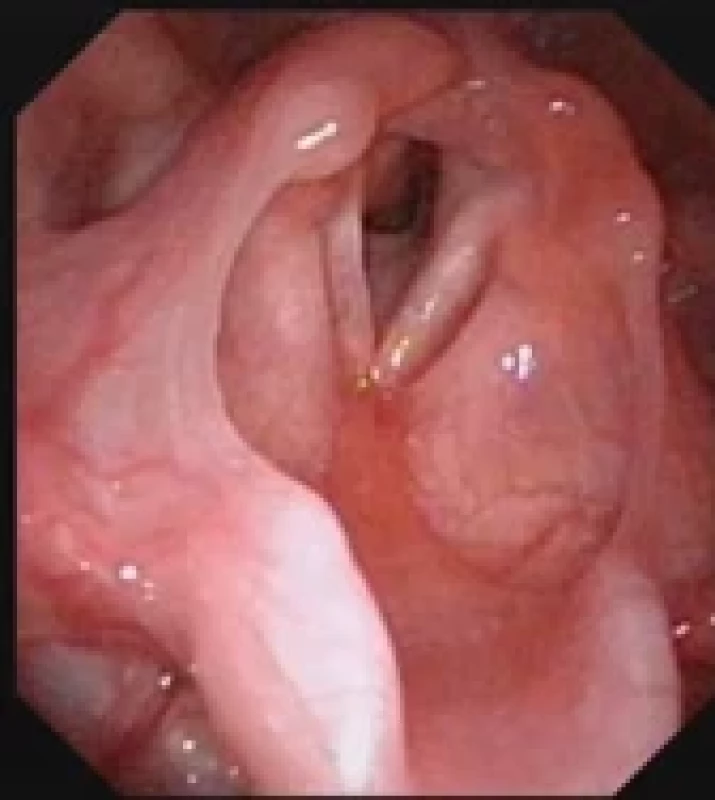
Zadní rozštěp hrtanu
Zadní rozštěp hrtanu vzniká neúplným uzavřením laryngotracheální výchlipky během embryonálního vývoje. Bývá asociován s dalšími vadami, jako je tracheomalacie (až v 80 % případů), tracheoezofageální píštěl (asi 20 %), malformace anogenitální oblasti [17]. Nejčastějším asociovaným syndromem je Opitz-Frias [1] charakterizovaný hypertelorizmem, anogenitálními malformacemi a zadním rozštěpem hrtanu. Dle rozsahu se nejčastěji rozštěpy klasifikují dle Benjamina a Inglise [25] na typ I–IV (tab. 4).
Mezi hlavní symptomy patří chronické aspirace a recidivující bronchopneumonie, obtížné krmení, zakuckávání a promodrávání při sání, vytékání mléka přes nos nebo ústy. Stridor bývá přítomen u těžších typů, u nichž se přidává také dechová tíseň, kterou ještě zhoršuje často přidružená tracheomalacie.
Diagnostika bývá obtížná, provádí se kombinace awake vyšetření flexibilní laryngoskopií a videofluoroskopie, základem však je rigidní laryngotracheobronchoskopie s ezofagoskopií v celkové anestezii. Výjimkou nejsou opakovaná vyšetření, protože rozštěp nemusí být přes vrstvu sliznice primárně patrný. Léčba je cílena na zamezení aspirací a zajištění ventilace. Zavádí se podpůrná opatření jako zahušťování stravy, polohování při krmení, event. zavedení výživové sondy. U vyšších stupňů rozštěpu lze provést dočasnou tracheostomii a gastrostomii, následně korekci rozštěpu endoskopicky (typ I) nebo otevřenou technikou přes laryngotracheofisuru (typ II–IV) z předního přístupu přes průdušnici, některá pracoviště provádějí endoskopický uzávěr i rozštěpu typu II a III [26]. V případě předního přístupu je nejnižší riziko poranění zvratných nervů. Typ III a IV mají vysoké riziko komplikací a selhání sutury, prognóza je závažná a bývá komplikována dalšími anomáliemi trávicího traktu, srdečními vadami apod.
Tab. 4. Klasifi kace zadních rozštěpů hrtanu dle Benjamina a Inglise [25]. Tab. 4. Classifi cation of posterior laryngeal splits according to Benjamin and Inglis [25]. ![Klasifi kace zadních rozštěpů hrtanu dle Benjamina a Inglise [25]. Tab. 4. Classifi cation of posterior laryngeal splits according to Benjamin and Inglis [25].](https://pl-master.mdcdn.cz/media/cache/media_object_image_small/media/image/f785c710d1c2b9cc036368ed22ffea9f.png)
Postkrikoidní vaskulární polštář
Postkrikoidní vaskulární polštář je, na rozdíl od předchozích klinických jednotek, anatomickou variantou, při níž je více prominentní žilní plexus postkrikoidně, který se plní při zapojení břišního lisu a vytváří dojem žilního polštáře [27, 28]. Předpokládá se, že funkcí tohoto vaskulárního polštáře je podpoření funkce horního a dolního jícnového svěrače a snížení refluxních epizod při pláči a zvracení [29]. Může se manifestovat stridorem nebo polykacími obtížemi, aspiracemi a refluxními epizodami, dle literatury je však třeba spíše pátrat po jiných vadách hrtanu (např. laryngomalacii), které by tyto obtíže vysvětlily, samotný vaskulární polštář obtíže většinou nezpůsobuje [28]. Ke stanovení diagnózy je nejvhodnější flexibilní awake laryngoskopie s Valsalvovým manévrem, díky němuž dojde k naplnění a ozřejmění plexu (obr. 4). Klinicky je třeba tuto anatomickou variantu odlišovat od ostatních postkrikoidních vaskulárních lézí – postkrikoidních hemangiomů a venózních malformací, za které byly v minulosti mylně vydávány a které na rozdíl od vaskulárního polštáře nejsou závislé na zvýšení tlaku. Většina dětí s postkrikoidním vaskulárním polštářem je spíše asymptomatická nebo mírně symptomatická a jsou pouze sledovány. V případě polykacích obtíží je doporučena rehabilitace polykání a antirefluxní terapie. S věkem vymizí i obtíže. Chirurgická léčba, kortikoterapie ani terapie propranololem nejsou doporučeny. U symptomatických pacientů lze zvážit lokální ošetření laserem [27].
Obr. 4. Postkrikoidní vaskulární polštář: 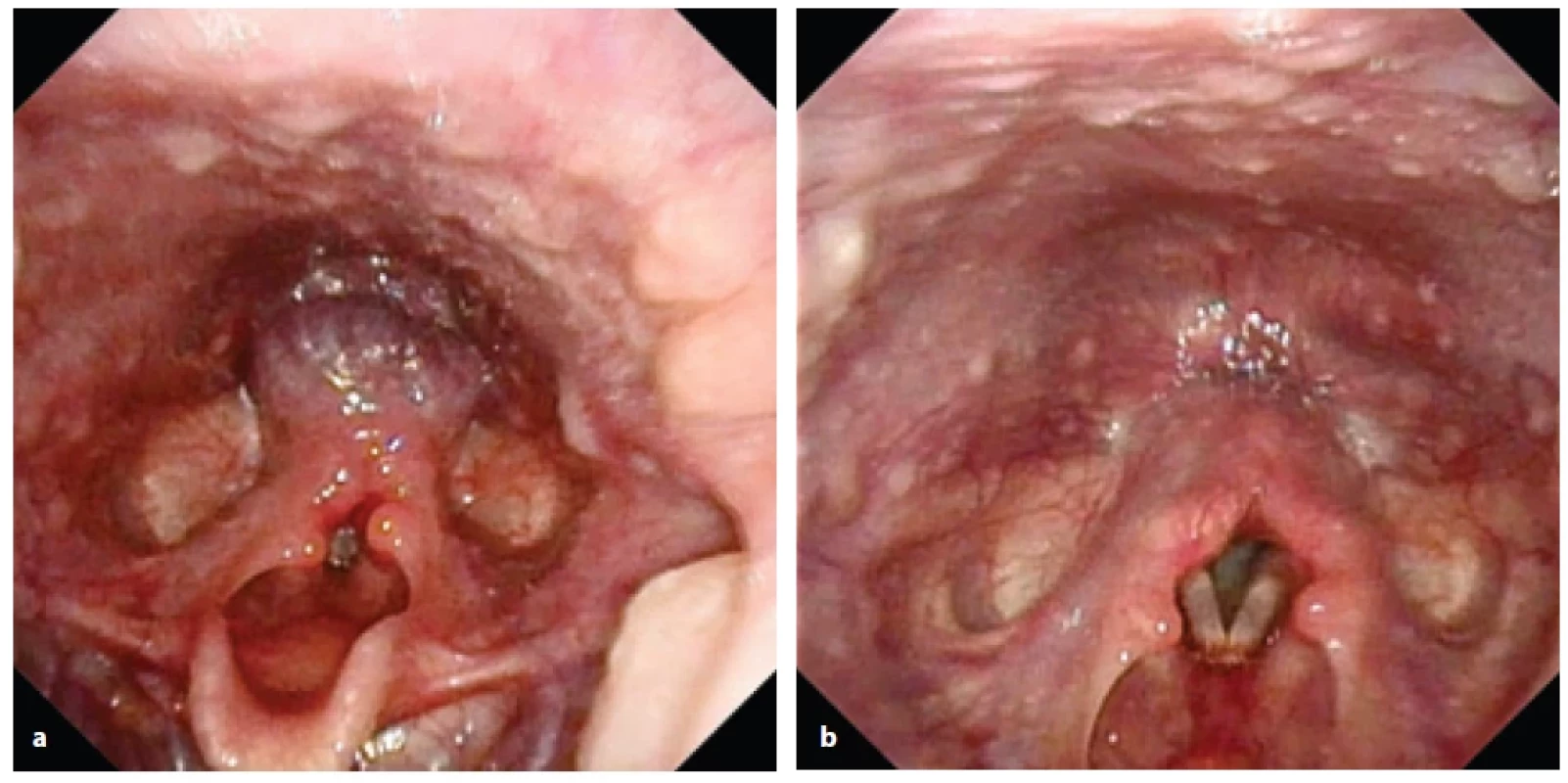
a) při zapojení břišního lisu je patrný naplněný venózní polštář postkrikoidně;
b) při zklidnění dítěte polštář mizí.
Fig. 4. Postcricoid vascular cushion:
a) during Valsalva maneuvre, venous cushion becomes visible;
b) veins collapse during relaxation.Závěr
Vrozené vady hrtanu představují heterogenní skupinu onemocnění, jejichž diagnostika je často protrahovaná a komplikovaná. Včasné rozpoznání a zahájení terapie je zásadní pro prevenci komplikací, jako je respirační selhání a recidivující aspirační bronchopneumonie. Incidence vrozených vad hrtanu bude pravděpodobně vyšší, než udává literatura, protože některé menší vady jsou asymptomatické nebo příznaky málo vyjádřené, dostupnost vyšetření je v různých částech světa také různá.
I závažné vady se mohou projevit až s odstupem několika týdnů až měsíců po narození. Děti bývají velmi tolerantní v případě postupně progredujícího zúžení dýchacích cest a symptomy se mohou objevit při obstrukci až 80–90 % průsvitu v subglotické oblasti.
Stridor u novorozence a dětí vyžaduje vyšetření otorinolaryngologem s důrazem na flexibilní (video) laryngoskopii, vyšetření polykání, dále event. laryngotracheobronchoskopii v celkové anestezii a zobrazovací metody. Mezi nejčastější příčiny kongenitálního stridoru patří laryngomalacie a vrozená paréza hlasivek. Většinu těchto případů lze zvládnout konzervativně a obtíže spontánně vymizí s vyšším věkem dítěte. Mezi méně časté vady patří kongenitální subglotická stenóza, vrozené srůsty až atrezie, rozštěpy hrtanu, postkrikoidní vaskulární léze (hemangiom, venózní malformace, prominentní vaskulární polštář). Pokud je indikována chirurgická terapie, stále více se uplatňují endoskopické techniky s cílem zachování hlasu a umožnění dekanylace. Závažnější vady hrtanu bývají asociovány s postižením jiných orgánů v rámci syndromových vad a mají horší prognózu. Management dětí s vrozenými vadami hrtanu vždy vyžaduje mezioborový a individuální přístup.
V rámci diferenciální diagnostiky je dále třeba pomýšlet také na získané příčiny stridoru, jako je juvenilní papilomatóza, získaná paréza hlasivky nebo aspirace cizího tělesa.
Zdroje
1. Varela P, Schweiger C. Congenital airway anomalies. Semin Pediatr Surg 2021; 30 (3): 151055. Doi: 10.1016/j.sempedsurg.2021.151055.
2. Holinger PH, Johnston KC, Parchet VN et al. Congenital malformations of the trachea, bronchi and lung. Ann Otol Rhinol Laryngol 1952; 61 (4): 1159–1180. Doi: 10.1177/00034894 5206100420.
3. Daniel SJ. The upper airway: congenital malformations. Paediatr Respir Rev 2006; 7 (Suppl 1): S260–S263. Doi: 10.1016/j.prrv.2006.04.227.
4. Thorne MC, Garetz SL. Laryngomalacia: Review and Summary of Current Clinical Practice in 2015. Paediatr Respir Rev 2016; 17 (Suppl 1): 3–8. Doi: 10.1016/j.prrv.2015.02.002.
5. Bodláková M, Jurovčík M, Katra R, Skřivan J. Stridor kongenitálního původu. Otorinolaryngol Foniatr 2019; 68 (1): 30–35.
6. Thompson DM. Abnormal sensorimotor integrative function of the larynx in congenital laryngomalacia: a new theory of etiology. Laryngoscope 2007; 117 (6 Pt 2 Suppl 114): 1–33. Doi: 10.1097/MLG.0b013e31804a5750.
7. Boogaard R, Huijsmans SH, Pijnenburg MWH et al. Tracheomalacia and bronchomalacia in children: incidence and patient characteristics. Chest 2005; 128 (5): 3391–3397. Doi: 10.1378/chest.128.5.3391.
8. Olney DR, Greinwald JH, Smith RJ et al. Laryngomalacia and its treatment. Laryngoscope 1999; 109 (11): 1770–1775. Doi: 10.1097/00005 537-199911000-00012.
9. Carter J, Rahbar R, Brigger M et al. International Pediatric ORL Group (IPOG) laryngomalacia consensus recommendations. Int J Pediatr Otorhinolaryngol 2016; 86 : 256–261. Doi: 10.1016/j.ijporl.2016.04.007.
10. Reinhard A, Gorostidi F, Leishman C et al. Laser supraglottoplasty for laryngomalacia; a 14 year experience of a tertiary referral center. Eur Arch Otorhinolaryngol 2017; 274 (1): 367–374. Doi: 10.1007/s00405-016-4252-6.
11. Lechien JR. Management of Pediatric Bilateral Vocal Fold Paralysis: A State-of-the - -Art Review of Etiologies, Diagnosis, and Treatments. Children (Basel) 2024; 11 (4): 398. Doi: 10.3390/children11040398.
12. Nemry N, Lechien JR et al. Surgical treatments of pediatric bilateral vocal fold paralysis: a systematic review. J Otolaryngol Head Neck Surg 2024; 53 : 19160216241291807. Doi: 10.1177/19160216241291807.
13. Thorpe RK, Kanotra SP, Hartley BE et al. Surgical management of bilateral vocal fold paralysis in children: a systematic review and meta-analysis. Otolaryngol Head Neck Surg 2021; 164 (2): 255–263. Doi: 10.1177/0194599820944892.
14. Trozzi M, Meucci D, Salvati A et al. Surgical options for pediatric bilateral vocal cord palsy: state of the art. Front Pediatr 2020; 8 : 538562. Doi: 10.3389/fped.2020.538562.
15. Jomah M, Jeffery C, Campbell S et al. Spontaneous recovery of bilateral congenital idiopathic laryngeal paralysis: systematic non-meta-analytical review. Int J Pediatr Otorhinolaryngol 2015; 79 (2): 202–209. Doi: 10.1016/j.ijporl.2014.12.007.
16. Schneiderová J, Zeleník K, Komínek P. Zadní glotická stenóza. Otorinolaryngol Foniatr 2018; 67 (2): 67–70.
17. Rutter MJ. Congenital laryngeal anomalies. Braz J Otorhinolaryngol 2014; 80 (6): 533–539. Doi: 10.1016/j.bjorl.2014.08.001.
18. Mueller AH, Hagen R, Pototschnig C et al. Laryngeal pacing for bilateral vocal fold paralysis: voice and respiratory aspects. Laryngoscope 2017; 127 (8): 1838–1844. Doi: 10.1002/lary.26428.
19. Jefferson ND, Cohen AP, Rutter MJ et al. Subglottic stenosis. Semin Pediatr Surg 2016; 25 (3): 138–143. Doi: 10.1053/j.sempedsurg.2016. 02.006.
20. Rovó L, Erdélyi E, Tóbiás Z et al. Slide laryngotracheoplasty for congenital subglottic stenosis in newborns and infants. Laryngoscope 2020; 130 (4): E199–E205. Doi: 10.1002/lary.28192.
21. Avelino MAG, Pazinatto DB, Rodrigues SO et al. Congenital laryngeal webs: from diagnosis to surgical outcomes. Braz J Otorhinolaryngol 2022; 88 (4): 497–504. Doi: 10.1016/j.bjorl.2020.06.018.
22. Schwartz T, Faria J, Pawar S et al. Efficacy and rebound rates in propranolol-treated subglottic hemangioma: a literature review. Laryngoscope 2017; 127 (11): 2665–2672. Doi: 10.1002/lary.26818.
23. Orlow SJ, Isakoff MS, Blei F. Increased risk of symptomatic hemangiomas of the airway in association with cutaneous hemangiomas in a “beard” distribution. J Pediatr 1997; 131 (4): 643–646. Doi: 10.1016/S0022-3476 (97) 70079-9.
24. Chen W, Zhu P, Xu M et al. Diagnosis of infantile subglottic hemangioma and the effect of oral propranolol. Am J Otolaryngol 2022; 43 (6): 103610. Doi: 10.1016/j.amjoto.2022. 103610.
25. Benjamin B, Inglis A. Minor congenital laryngeal clefts: diagnosis and classification. Ann Otol Rhinol Laryngol 1989; 98 (6): 417–420. Doi: 10.1177/000348948909800602.
26. Gergin O, Rahbar R, Adil E et al. Endoscopic repair of laryngeal cleft. Oper Tech Otolaryngol Head Neck Surg 2016; 27 (2): 100–103. Doi: 10.1016/j.otot.2016.04.004.
27. Lee A, Patel NA – Systematic review of pediatric postcricoid cushion and postcricoid lesions. Int J Pediatr Otorhinolaryngol 2022; 162 : 111293. Doi: 10.1016/j.ijporl.2022.111293.
28. Haugen TW, Wood WE, Helwig C et al. Postcricoid vascular abnormalities: hemangiomas, venous malformations, or anatomic variant. Int J Pediatr Otorhinolaryngol 2012; 76 (6): 805–808. Doi: 10.1016/j.ijporl.2012.02.059.
29. Hoff SR, Koltai PJ. The “postcricoid cushion”: observations on the vascular anatomy of the posterior cricoid region. Arch Otolaryngol Head Neck Surg 2012; 138 (6): 562–571. Doi: 10.1001/archoto.2012.932.
Prohlášení o střetu zájmů
Autor práce prohlašuje, že v souvislosti s tématem, vznikem a publikací tohoto článku není ve střetu zájmů a vznik ani publikace článku nebyly podpořeny žádnou farmaceutickou firmou. Toto prohlášení se týká i všech spoluautorů
Grantová podpora
Tento výstup vznikl v rámci programu Cooperatio, vědní oblasti SURG.
Přijato k recenzi: 19. 4. 2025
Přijato k tisku: 4. 7. 2025
MUDr. Anna Švejdová
Klinika otorinolaryngologie a chirurgie hlavy a krku
LF UK a FN Hradec Králové
Sokolská 581
500 05 Hradec Králové
anna.svejdova@fnhk.cz
Štítky
Audiologie a foniatrie Dětská otorinolaryngologie Otorinolaryngologie
Článek EditorialČlánek Poděkování recenzentům
Článek vyšel v časopiseOtorinolaryngologie a foniatrie
Nejčtenější tento týden
2025 Číslo 4- Fexofenadin – nesedativní a imunomodulační antihistaminikum v léčbě alergických projevů
- Výhody kombinace olopatadinu a momethasonu v terapii alergické rinitidy
- Moderní přístupy zvyšující efektivitu antibiotické léčby v nemocniční praxi
- Primární a sekundární imunodeficience, přehled a klasifikace
- Diagnostika primárních imunodeficiencí
-
Všechny články tohoto čísla
- Editorial
- Hodnocení poruchy hlasu v klinické praxi
- Screening sluchu novorozenců v České republice – změny v monitoringu a kontrole
- Screening sluchu pětiletých dětí
- Prasečí hrtan jako vhodný model pro nácvik chirurgie hrtanu
- Vývoj incidence, mortality a prevalence zhoubných nádorů hlavy a krku, karcinomu hrtanu a štítné žlázy v letech 1977– 2023 v České republice
- Širokopásmová tympanometrie v klinické praxi: přehled literatury
- Chronická sekretorická otitida – mikrobiomem indukované onemocnění
- Diferenciální diagnostika vrozených vad hrtanu u dětí
- Kalorický test: metodika, principy a obecné pojmy
- Akutní zygomatitida – vzácná otogenní zánětlivá komplikace
- Středně diferencovaný chondrosarkom hrtanu: čtyři kazuistiky a přehled literatury
- Historický okamžik pro screening sluchu novorozenců a předškolních/ pětiletých dětí v České republice
- Prof. MUDr. Ivan Hybášek, DrSc., 22. 4. 1929 – 3. 10. 2025
- Poděkování recenzentům
- Otorinolaryngologie a foniatrie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Hodnocení poruchy hlasu v klinické praxi
- Kalorický test: metodika, principy a obecné pojmy
- Vývoj incidence, mortality a prevalence zhoubných nádorů hlavy a krku, karcinomu hrtanu a štítné žlázy v letech 1977– 2023 v České republice
- Screening sluchu novorozenců v České republice – změny v monitoringu a kontrole
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Revma Focus: Spondyloartritidy
nový kurz
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Autoři: prof. MUDr. Pavel Horák, CSc., doc. MUDr. Ludmila Brunerová, Ph.D., doc. MUDr. Václav Vyskočil, Ph.D., prim. MUDr. Richard Pikner, Ph.D., MUDr. Olga Růžičková, MUDr. Jan Rosa, prof. MUDr. Vladimír Palička, CSc., Dr.h.c.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



