-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Vznik autoimunitní hepatitidy v průběhu léčby psoriázy infiximabem – popis případu
Autoimmune Hepatitis during by Infliximab Treatment of Psoriasis: Case Report
Autoimmune hepatitis is a rare complication of treatment with biologicals. Author describes a case of autoimmune hepatitis in 46-year-old women with psoriasis and psoriatic arthritis treated with infliximab. He emphasizes the importance of liver function test monitoring before each drug administration and the difficulties in diagnosis of this serious disease.
Key words:
psoriasis – psoriatic arthritis – infliximab monotherapy – autoimmune hepatitis
Autoři: Z. Antal
Působiště autorů: Kožní oddělení, Ústřední vojenská nemocnice Praha, primář MUDr. Jaroslav Hoffmann
Vyšlo v časopise: Čes-slov Derm, 86, 2011, No. 1, p. 23-26
Kategorie: Kazuistiky
Souhrn
Autoimunitní hepatitida je vzácná komplikace léčby biologiky. Autor popisuje případ autoimunitní hepatitidy, která se objevila u 46leté ženy s psoriázou a psoriatickou artritidou léčenou infliximabem. Poukazuje na význam kontrol jaterních testů před každým podáním léku a na obtíže související se stanovením diagnózy této vážné choroby.
Klíčová slova:
psoriáza – psoriatická artropatie monoterapie infliximabem – autoimunitní hepatitidaÚVOD
Léčba biologiky přináší novou dimenzi do léčby psoriázy. Je to léčba velmi účinná, elegantní a zdá se být i bezpečná. Jelikož jde o léčbu poměrně novou, zdaleka ještě nejsou známy všechny možné nežádoucí efekty, které s sebou může přinášet. Následující případ poukazuje na výskyt raritní komplikace – autoimunitní hepatitidy – vyvolané v souvislosti s léčbou infliximabem u pacientky s psoriázou a psoritickou artritidou.
Do roku 2010 bylo popsáno 11 případů AIH indukovaných infliximabem [2] a jeden případ AIH navozené adalimumabem [1]. Jednalo se o pacienty s revmatoidní artritidou, Crohnovou nemocí, Bechtěrevovou chorobou, ulcerózní kolitidou a s psoriázou a psoriatickou artropatií [2].
POPIS PŘÍPADU
Pacientka (46 let) byla od roku 1984 ve sledování dermatologické ambulance ÚVN pro psoriázu s následným rozvojem psoriatické artropatie od roku 1997. Rodinná anamnéza byla nevýznamná. Osobní anamnéza zahrnovala polynodózní eufunkční strumu na substituční léčbě levothyroxinem 100 μg, smíšenou dyslipidémii na dietě, refluxní chorobu jícnu. Pacientka podstoupila následující operace – 1998 adnexektomie vpravo pro benigní adnextumor a apendektomie, 2000 hysterektomie pro endometriózu s preventivní adnexektomií vlevo, 2006 laparoskopická cholecystektomie pro cholecystolitiázu.
V roce 1998 byla zjištěna elevace jaterních testů s ALT 4,7 μkat/l (norma do 0,73 μkat/l) po krátkodobém užívání danazolu (inhibitor hypofyzárních gonadotropinů), indikovaného pro endometriózu, se spontánní normalizací ALT po vysazení léku a dočasném užívání hepatoprotektiv.
V roce 1997 byla diagnostikována psoriatická artropatie s rychlou progresí choroby, až imobilizací, pro kterou byl nasazen methotrexát (i. m.). Byl prokázán dobrý efekt na kloubní obtíže, avšak žádný na psoriázu. Léčba byla ukončena přibližně po roce. Revmatologové pacientku následně převedli na užívání metylprednisolonu, který se stabilizoval v dávce 4 mg/den, v kombinaci s nesteroidními antirevmatiky. V této léčbě pacientka pokračovala až do roku 2008.
V dermatologické ambulanci byla pacientka léčena lokálními externy v kombinaci s fototerapií, s nejlepším efektem úzkopásmové UVB 311 nm. Onemocnění s krátkou remisní fází, po většinu roku s hodnotami PASI a BSA přes 10. Celková léčba acitretinem byla kontraindikována pro dyslipidémii.
Léčba infliximabem byla zahájena 17. 4. 2008 v monoterapii, v dávce 5,5 mg/kg, a to po předchozím provedení všech standardních vyšetření doporučených před zahájením této léčby. V průběhu dvou měsíců byly podány tři infuze (v klasickém schématu 0., 2., 6. týden). Došlo k vymizení psoriatických eflorescencí a nastala úleva kloubních obtíží. Léčba byla objektivně bez komplikací, pouze subjektivní pocity malátnosti a nauzey, vždy druhý až třetí den po aplikaci infuze. Laboratorní nález byl v normě.
Čtvrtá infuze měla být pacientce aplikována 12. 8. 2008. V laboratoři však byla zjištěna elevace jaterních enzymů s hodnotami ALT 6,21 μkat/l (norma do0,73 μkat/l), AST 3,45 μkat/l (norma do 0,68 μkat/l), GMT 0,72 μkat/l (norma do 0,70 μkat/l), ALP 1,34 μkat/l (norma do 4,82 μkat/l), hodnota celkového bilirubinu 19,7 μmol/l (norma do 21 μmol/l). Léčba byla zastavena. Vyšetřili jsme panel hepatitid a herpesvirů s negativním výsledkem.
Pacientka byla předána do hepatologické poradny. Při následných kontrolních vyšetřeních jaterní enzymy dále stoupaly, stav si vyžádal 24. 9. 2008 příjem pacientky na Interní kliniku ÚVN. Subjektivní obtíže pacientky představovaly celkovou slabost, únavu, tlakové bolesti ve středním epigastriu a pravém hypochondriu, pocit vzedmutí břicha, nauzeu, zimnici. Objektivně byla mírně tmavší moč a ikterus sklér. Znovu byl nabrán panel hepatitid a herpesvirů a doplněna sérologie autoimunit (AMA, ASMA, SLA, LKM, ANA, ANCA), gamaglobulin – vše s negativním nálezem. Pro další progresi jaterních testů (ALT 21 μkat/l, AST 20 μkat/l, GMT 4,6 μkat/l, ALP 4 μkat/l, celkový bilirubin 188 μmol/l) byla indikována jaterní biopsie. Vzhledem k charakteristickému histologickému obrazu se patolog i přes negativní sérologii přiklonil k závěru autoimunitní hepatitida (obr. 1, 2, 3). Pacientce byl nasazen prednison v denní dávce 60 mg, po kterém byl pozorován poměrně rychlý pokles jaterních enzymů i bilirubinu. Pacientka byla propuštěna do domácí péče s dispenzarizací v hepatologické poradně.
Obr. 1. Fibrotizace a rozšíření portálních polí (barvení retikulin) 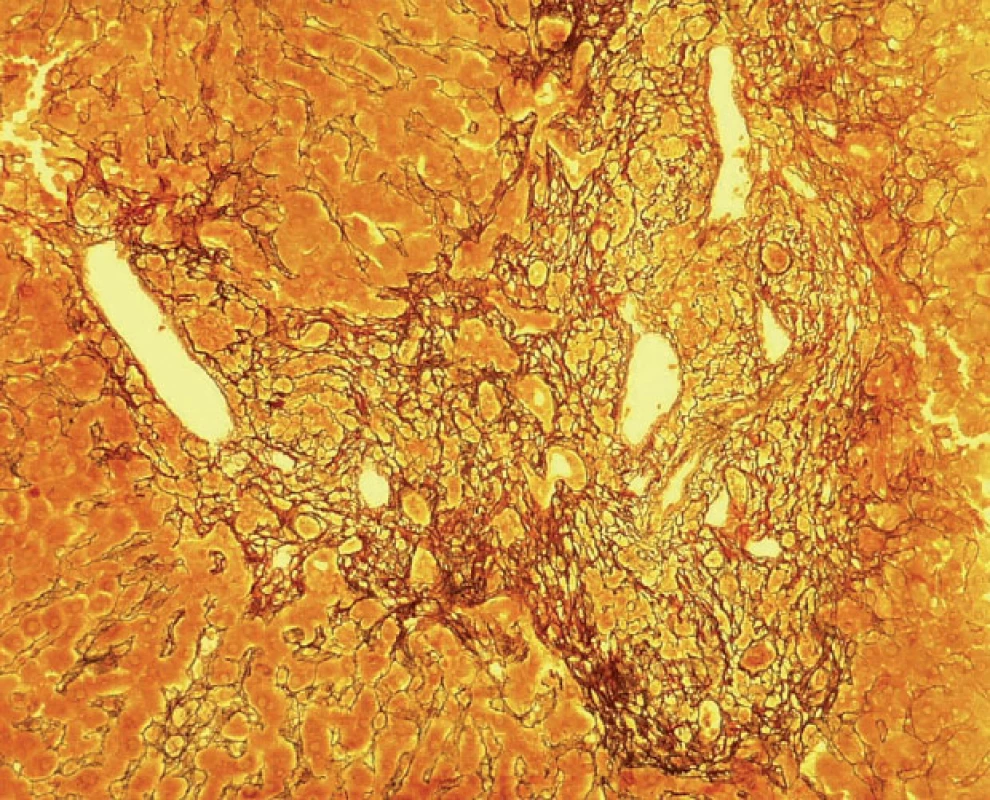
Obr. 2. Intenzivní smíšená celulizace portálních polí s průnikem buněk zánětlivé celulizace hluboko do parenchymu Četné apoptotické hepatocyty (barvení HE). 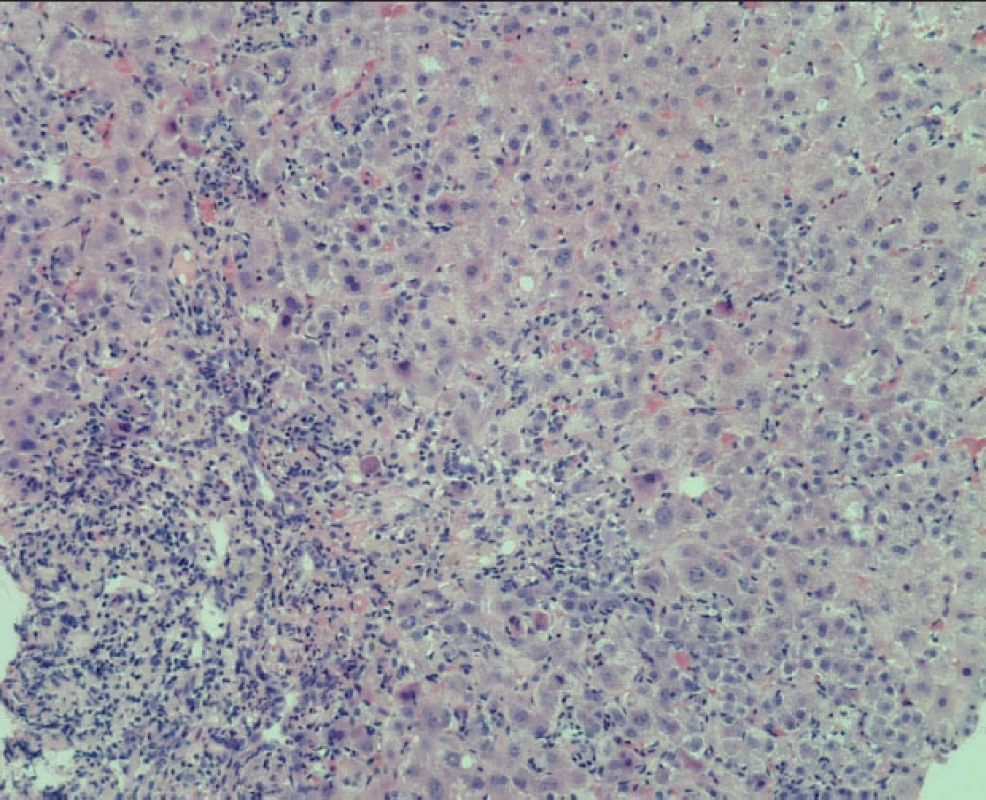
Obr. 3. Fokální nekróza hepatocytů v centrálnější části lobulu s kulatobuněčnou reakcí včetně plazmocytů a s makrofágy Apoptotické jaterní buňky (barvení HE). 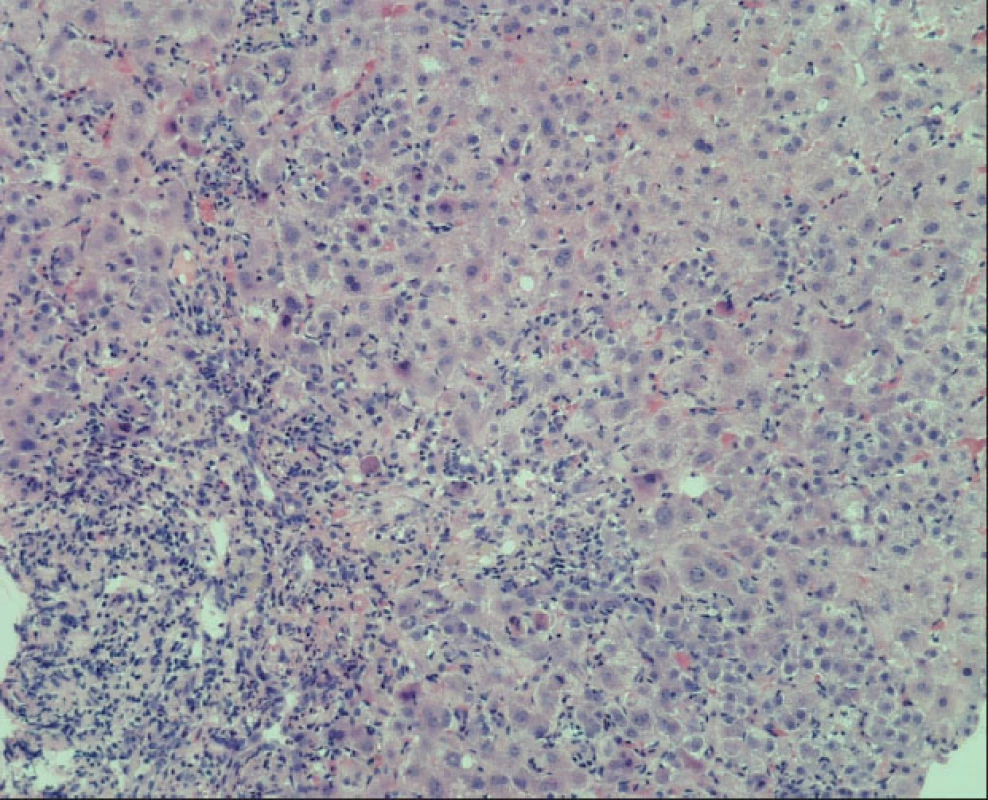
Zde při první kontrole (13. 10. 2008) byly hodnoty jaterních testů následující: ALT 2,28 μkat/l, AST 1,02 μkat/l, GMT 1,42 μkat/l, ALP 2,37 μkat/l, bilirubin 44,9 μmol/l. Dávka prednisonu byla zredukována na 40 mg denně a dále byla postupně snižována. Nově byl nasazen azathioprin 50 mg 2krát 1 tbl. denně. 27. 11. 2008 se již hodnoty jaterních testů normalizovaly a pacientka byla ponechána na udržovací dávce 5 mg prednisonu denně. 11. 2. 2009 se snížil také azathioprin na dávku 50 mg 1krát denně a 2. 6. 2009 se zopakovalo vyšetření autoprotilátek (AMA, LKM1, ASMA, AMA, ANA) – opět s normálními hodnotami.
Přes negativitu specifických autoprotilátek byl nález uzavřen jako autoimunitní hepatitida. (Odběr na specifické protilátky, protilátky proti infliximabu nebyl proveden.)
Stav pacientky na současné dávce imunosupresiv je uspokojivý. Podle očekávání se psoriáza u pacientky po ukončení léčby infliximabem postupně zhoršila a nález se vrátil do původního rozsahu před léčbou. Progrese onemocnění nebyla tak výrazná, jak by se dalo očekávat po ukončení léčby infliximabem, což bylo jistě dáno imunosupresivním efektem prednisonu. V současné době je pacientka na zevní léčbě a dvakrát ročně absolvuje kúru fototerapie.
DISKUSE
Autoimunitní hepatitida (AIH) je zánětlivé onemocnění jater neznámé etiologie. Obvykle je charakterizováno přítomností autoprotilátek (ANA – proti buněčným jádrům, AMA – proti mitochondriím, LKM-1 – proti jaterním a ledvinovým mikrozomům 1. typu, ASMA – proti hladkému svalu) a hypergamaglobulinémií. Příznačné je zvýšení hodnot aminotransferáz a bilirubinu od horní hranice normy po vysoké hodnoty. Aktivita alkalické fosfatázy je normální, nebo může dosahovat tří - až pětinásobku normy. Predilekčně jsou postiženy ženy věkových skupin 14–25 let a ženy po menopauze [3, 8, 10].
Patogenetickým mechanismem u AIH je porucha imunoregulace vyjádřená defektem supresorových T lymfocytů. Výsledkem je produkce autoprotilátek proti povrchovým antigenům hepatocytu. Není jasné, zda porucha imunoregulace je primární nebo sekundární (získané změny antigenů tkání). Molekulární infiltrát portálních polí je tvořen B lymfocyty a pomahačskými T lymfocyty, s relativně menším zastoupením cytotoxických supresorových buněk. To podporuje teorii, že hlavním mechanismem je cytotoxicita závislá na protilátkách [5].
Histologický obraz je typický nálezem infiltrace portálních prostor mononukleáry, které přecházejí hluboko do okolního parenchymu a vytvářejí periportální infiltrát, známý jako „interface hepatitis“ (dříve peace-meal nekrózy) – viz obrázek 2. V lobulu bývají difuzně ve všech zónách známky fokální nekrózy a hepacytolýzy, někdy s perivenulární akcentací (viz obr. 3). Částé jsou infiltráty z plazmatických buněk a přemosťující nekrózy s tvorbou portoportálních či portocentrálních sept (viz obr. 1) a multilobulární kolaps (viz obr. 3). Ačkoliv popsaný histologický obraz je charakteristický, není patognomický. Podobné nálezy lze nalézt i u chronických hepatitid jiné etiologie [7, 9]. Konečnou diagnózu je nutné stanovit současně s laboratorními výsledky, klinickým obrazem a jeho vývojem [9].
Léčbou autoimunitní hepatitidy je podávání imunosupresiv, ať již samotného prednisonu nebo kombinace prednison-azathioprin. Úvodní dávka prednisonu činí 30–60 mg 1krát denně, azathioprin je přidáván po dosažení alespoň částečné remise, a to obvykle v dávce 50 mg 1krát denně. Nelze podat jednoznačné doporučení ohledně snížení dávky nebo ukončení léčby. Postup musí být vždy individuální a po snížení dávky prednisonu je nutné počítat s možností reaktivace choroby, vyžadující opět zintenzivnění imunosuprese. Pokud by byl nemocný léčený prednisonem a azathiopronem v úplné remisi déle než rok, je možné remisi nadále udržovat samotným azathioprinem ve vyšší dávce. Někteří autoři uvádějí, že léčbu nelze ukončit nikdy [8].
V našem případě jsme diferenciálně diagnosticky rozhodovali o tom, zda se jedná o virovou hepatitidu, kterou se pacientka nakazila během léčby infliximabem, nebo toxické poškození jater infliximabem, nebo zda se jedná o autoimunitní hepatitidu navozenou touto léčbou.
K vyloučení virové hepatitidy přispěla opakovaně negativní sérologie. Teorii podpořil i fakt, že po nasazení imunosupresiv se stav pacientky rychle zlepšil, což je velmi typickou známkou pro autoimunitní hepatitidu a nesvědčí pro hepatitidu virového původu [9]. U toxické jaterní léze bychom očekávali spíše kratší interval rozvoje jaterní léze od podání preparátu. U toxické lékové hepatitidy je popisován rychlý spontánní pokles jaterních enzymů po vysazení noxy. Pokles ALT o 50 % a více do 8 dnů, bez dalšího následného vzestupu (do 1 měsíce) značí velmi pravděpodobnou kauzální souvislost s lékovým poškozením. Pokles ALT o 50 % a více do 30 dnů – pravděpodobná kauzální souvislost s lékovým poškozením. Pokud změny ALT nesplňují první dvě kritéria, je kauzální souvislost s lékovým poškozením nepravděpodobná [4, 6]. Biologický poločas rozpadu infliximabu je 8–10 dnů, detekovatelnost této látky v séru je do 8. týdne od podání (údaje z SPC). U naší pacientky dochází k rozvoji onemocnění 10. týden od poslední aplikace. Toxická etiologie se tedy jeví jako nepravděpodobná.
Nález jsme uzavřeli jako autoimunitní hepatitidu (negativita autoprotilátek by mohla být vysvětlena vlivem dlouhodobého užívání metylprednisolonu).
Situace je však zřejmě složitější. Otázkou totiž zůstává, jaká byla příčina zvýšení transamináz po krátce nasazeném danazolu v roce 1998, spontánně se normalizující po ukončení podávání léku a nasazení hepatoprotektiv. A zda by došlo k indukci stejného jaterního postižení (např. po delší době užívání) jinými biologickými preparáty podávanými subkutánně.
Přestože jsme v naší diferenciální úvaze poukázali na malou pravděpodobnost toxického poškození, nelze to zcela vyloučit. Jiným možným vysvětlením celého našeho případu by totiž mohlo být, že se nejednalo o akutní indukovanou AIH v pravém slova smyslu, ale o latentně probíhající chronickou hepatitidu, dlouhodobě tlumenou užíváním metylprednisolonu, která mohla být toxickým vlivem infliximabu akutně aktivována (jako v roce 1998 po užívání danazolu).
ZÁVĚR
Autoimunitní hepatitida vyvolaná v souvislosti s léčbou infliximabem je vzácná komplikace. Do roku 2010 bylo popsáno již jedenáct případů indukovaných infliximabem [2]. V březnu 2009 se v odborných publikacích objevila kazuistika první AIH vyvolané jiným anti-TNF preparátem než infliximabem, a to adalimumabem [1]. Zatím nebyl publikován žádný případ AIH vzniklé v souvislosti s užíváním etanerceptu. Vzhledem k tomu, že zdaleka ne všechny případy musí být nutně hlášeny, může být tento počet podhodnocen. Se zvyšováním dostupnosti moderní biologické léčby stoupá i počet pacientů užívajících infliximab. Měli bychom proto zvážit kontrolu jaterních testů před každým podáním infuze tohoto léku, a tak pomoci k včasnému rozpoznání možného vážného jaterního postižení. A dále se snažit o větší informovanost o této možné komplikaci, a to nejen v dermatologii, ale také v jiných oborech využívajících biologickou léčbu.
Poděkování: Rád bych vyjádřil poděkování plk. MUDr. Petru Hrabalovi, primáři patologie ÚVN Střešovice, za poskytnutí obrazové dokumentace a konzultaci při jejím popisu.
Do redakce došlo den 15. 9. 2010.
Kontaktní adresa:
kpt. MUDr. Zdeněk Antal
Ústřední vojenská nemocnice Praha
U Vojenské nemocnice 1200
169 02 Praha 6
e-mail: zdenek.antal@uvn.cz
Zdroje
1. ADAR, T., MIZRAHI, M., PAPPO, O., SCHEIMAN - -ELAZARY, A., SHIBOLET, O. Adalimumab-induced Autoimmune Hepatitis. J. Clin. Gastroenterol., 2010, 44, 1, p. e20–e22.
2. BJÖRNSSON, E., TALWALKAR, J., TREEPRASERTSUK, S., KAMATH, P., TAKAHASHI, N., SANDERSON, S., NEUHAUSER, M., LINDOR, K. Drug-Induced Autoimmune Hepatitis: Clinical Characeristics and Prognosis. American Association for the Study of Liver Diseases. Hematology, 2010, 51, 6, p. 2040–2049.
3. BRODANOVÁ, M. Onemocnění jater. In KLENER, P. et al. Vnitřní lékařství. Praha: Galén, Karolinum, 1999. s. 544–558.
4. BRODANOVÁ, M. Toxické poškození jater. II. díl. Interní medicína pro praxi, 2003, 1, s. 19–23.
5. HŮLEK, P. Autoimunitní onemocnění jater. In BUREŠ, J., HORÁČEK, J. Základy vnitřního lékařství. Praha: Galén, Karolinum, 2003. s. 355.
6. HOLOMÁŇ, J., GLASA, J. et al. Liver and drugs 98. Toxic Liver Disease: Bratislava, 1999, p. 5–33.
7. HORÁK, J. Autoimunitní hepatitida. Alergie, 2006, 2, p. 118–121
8. HORÁK, J., STŘÍTESKÝ J. Chronické hepatitidy. 1. vyd. Praha: Grada Publishing, 1999. p. 192.
9. KANEL, G. C., KORULA, J. Atlas of Liver Patology. 2. ed. Philadelphia: Elsevier, 2005.
10. KOPÁČOVÁ, M. Autoimunitní onemocnění jater. In BUREŠ, J., HORÁČEK, J. Základy vnitřního lékařství. Praha: Galén, Karolinum 2003. p. 354–356.
Štítky
Dermatologie Dětská dermatologie
Článek vyšel v časopiseČesko-slovenská dermatologie
Nejčtenější tento týden
2011 Číslo 1- Komplementární mechanismus účinku analog vitaminu D a topických kortikosteroidů v léčbě ložiskové psoriázy
- V patogenezi psoriázy jde o víc než jen o IL-17A
- Léčba chronické blefaritidy vyžaduje dlouhodobou péči
-
Všechny články tohoto čísla
- DOŠKOLOVÁNÍ LÉKAŘŮ – KONTROLNÍ TEST
- Kožní změny po transplantaci ledvin – první výsledky klinického sledování
- Úspěšná léčba těžké formy hidradenitis suppurativa pomocí adalimumabu
- Vznik autoimunitní hepatitidy v průběhu léčby psoriázy infiximabem – popis případu
- Klinický prípad: Tuhý belavý uzol v skrotálnej koži
- Evropa a my
- Diagnosticky cenné cévy
- Klinicko-patologické aspekty tzv. pendulujúceho mäkkého fibrómu
- Aktuální informace a zpráva z venerologické sekce ČDS a Národní referenční laboratoře pro syfilis
- Zápis ze schůze výboru ČDS konané dne 9. září 2010
- Hidradenitis suppurativa
- Zápis ze schůze výboru ČDS konané dne 21. října 2010
- Zápis ze schůze výboru ČDS konané dne 2. prosince 2010
- Zápis ze schůze výboru ČDS konané dne 13. ledna 2011
- Zápisnica zo zasadnutia výboru Slovenskej dermatovenerologickej spoločnosti dňa 10. 12. 2010
- K významnému životnímu jubileu prof. MUDr. Věry Semrádové, CSc.
- Sedmdesátiny profesora MUDr. Vladimíra Resla, CSc.
- Odborné akce v roce 2011
- Česko-slovenská dermatologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Úspěšná léčba těžké formy hidradenitis suppurativa pomocí adalimumabu
- Hidradenitis suppurativa
- Klinicko-patologické aspekty tzv. pendulujúceho mäkkého fibrómu
- Vznik autoimunitní hepatitidy v průběhu léčby psoriázy infiximabem – popis případu
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



