-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Rostliny v terapii idiopatických střevních zánětů
Plants in the therapy of inflammatory bowel disease
Medicinal plants have been used to treat various diseases for thousands of years. Although their popularity has changed in the course of history, the interest in plants and in their active compounds is currently increasing. Today’s research focuses on determining the active substances responsible for the effect and their mechanism of action. Plants have also their place in complementary therapy of chronic inflammatory diseases. Inflammatory bowel disease (IBD), such as Crohn’s disease and ulcerative colitis, are chronic diseases of the gastrointestinal tract. Their incidence has been increasing in recent years and it is difficult to predict the progression of the disease. Due to the unclear aetiology of inflammatory bowel disease, current therapy is not completely successful. Complementary and alternative medicine is widely used by patients because of frequent side effects and lack of effectiveness of the standard therapy. Plant products may provide an alternative or supplementary treatment option to patients. This review brings a survey of plants and their content compounds used in complementary therapy of inflammatory bowel disease with special relevance to clinical studies.
Key words:
experimental animal models – phytotherapy – inflammatory bowel disease – clinical trials
The authors declare they have no potential conflicts of interest concerning drugs, products, or services used in the study.
The Editorial Board declares that the manuscript met the ICMJE „uniform requirements“ for biomedical papers.Submitted:
5. 2. 2014Accepted:
31. 3. 2014
Autoři: Z. Vochyánová; K. Sikorová; K. Šmejkal; J. Hošek
Působiště autorů: Ústav přírodních léčiv, Farmaceutická fakulta, Veterinární a farmaceutická univerzita Brno
Vyšlo v časopise: Gastroent Hepatol 2014; 68(3): 248-254
Kategorie: IBD: přehledová práce
Souhrn
Léčivé rostliny slouží již několik tisíc let jako prostředky v léčbě různých onemocnění. Přestože se jejich obliba v průběhu historie měnila, zájem o rostliny a jejich obsahové látky dnes opět vzrůstá. Výzkum se nyní zaměřuje na určení obsahových látek zodpovědných za účinek a na objasnění jejich mechanizmu působení. Rostliny mají své místo i v doplňkové terapii chronických zánětlivých onemocnění. Chronické střevní záněty, jako jsou Crohnova choroba a ulcerózní kolitida, jsou chronická onemocnění gastrointestinálního traktu. Jejich incidence v posledních letech neustále narůstá a onemocnění má těžko předvídatelný průběh. Vzhledem k nejasné etiologii střevních zánětů není dosavadní terapie zcela úspěšná. Z důvodů častých nežádoucích účinků a nedostatečného efektu standardní léčby je použití komplementární a alternativní medicíny u pacientů velmi rozšířené. Rostlinné produkty tak mohou nemocným poskytnout alternativní nebo doplňkovou možnost léčby. Toto review přináší přehled rostlin a případně jejich obsahových látek používaných v doplňkové terapii chronických střevních zánětů s ohledem na jejich hodnocení v klinických studiích.
Klíčová slova:
experimentální modely – fytoterapie – idiopatické střevní záněty – klinické studieCrohnova choroba (Crohn’s disease – CD) a ulcerózní kolitida (ulcerative colitis – UC) jsou chronické zánětlivé nemoci souhrnně označované jako idiopatické střevní záněty (inflammatory bowel disease – IBD). Postihují různé části gastrointestinálního traktu, především tenké a tlusté střevo. Liší se od sebe hloubkou postižení trávicí trubice a lokalizací zánětu. Příčina vzniku IBD není doposud zcela objasněna. Předpokládá se spolupůsobení několika faktorů: abnormální slizniční imunitní reakce, genetické predispozice a mikrobiální či environmentální vlivy [1]. V současnosti se v terapii IBD uplatňuje zejména farmakoterapie a chirurgické postupy. Hlavními skupinami používaných látek jsou aminosalicyláty, glukokortikoidy, imunosupresiva, antibiotika, chemoterapeutika a biologická léčiva. Současná léčebná strategie však není vždy zcela efektivní, a řada pacientů se tak uchyluje ke komplementární a alternativní medicíně (complementary and alternative medicine – CAM).
CAM je označením pro nekonvenční medicínu a zahrnuje širokou škálu diagnostických a léčebných postupů. Na rozdíl od klasické medicíny je přístup k péči o pacienta holistický, což je obzvláště důležité u chronických onemocnění. V řadě případů přináší alternativní metody možnost snížit dávku a počet užívaných léčiv nebo se vyhnout operaci [2]. Z různých typů CAM je u pacientů s IBD preferována homeopatie, akupunktura a v neposlední řadě také fytoterapie [3].
Byla již provedena celá řada studií hodnotících účinnost a mechanizmus působení rostlinných extraktů nebo čistých látek in vivo na laboratorních zvířatech či v klinických studiích u pacientů s IBD. Různé internetové stránky a diskuze určené pacientům doporučují každodenní užívání aloe gelu, zeleného čaje, kurkumy nebo pelyňku [4,5]. Některá doporučení jsou podložena relevantními klinickými studiemi, jiná pouze experimenty na laboratorních zvířatech. Dlouhodobé zkušenosti s alternativní léčbou, včetně fytoterapie, mají především asijské země. Tradiční léčba IBD v Iránu zahrnuje např. podávání pryskyřice z keře Pistacia lenticus a stromu Boswellia serrata, semen jitrocele a řeřichy nebo plodů fenyklu [6].
Toto review si klade za cíl shrnout dosud známé výsledky in vivo studií a závěry klinických hodnocení. Publikační podklady byly vyhledány v databázích PubMed a Web of Knowledge pod klíčovými slovy: „experimental colitis“, „clinical trials“, „Crohn’s disease“, „ulcerative colitis“, „protective“, „plant extracts“.
In vivo experimenty
Studie na laboratorních zvířatech využívají několika možných způsobů navození střevního zánětu. Každý způsob má svou charakteristickou patogenezi a žádný zcela lidskou IBD nekopíruje, přesto přináší možnost otestovat aktivitu a zjistit mechanizmus účinku nových biologicky aktivních látek. Nejčastěji jsou používány modely kolitidy indukované chemickými látkami, např. podáním kyseliny 2,4,6-trinitrobenzensulfonové (TNBS), kyseliny octové, dextran sulfátu sodného (DSS) nebo indomethacinu. Tyto chemické látky vyvolávají u laboratorních zvířat imunitní reakci, ovlivňují hladinu ochranných prostaglandinů nebo způsobují přímé poškození střevní tkáně. Další modely vedou ke spontánnímu vývoji kolitidy využitím genových manipulací (interleukin (IL)-7 transgenní myši, myši s knock-outovaným genem pro IL-10). Historicky nejstarší způsob navození střevního zánětu je založen na adoptivním buněčném transferu T lymfocytů do imunodeficientních zvířat, nejnovější modely využívají vlivu γ-záření [7].
Testované přírodní látky účinkují na experimentálních modelech kolitidy různými mechanizmy – působí antioxidačně, ovlivňují expresi zánětlivých cytokinů nebo zasahují do metabolizmu kyseliny arachidonové a signální dráhy vedoucí k aktivaci nukleárního faktoru (NF)-κB [8].
Jedním z etiologických faktorů Crohnovy choroby a ulcerózní kolitidy je abnormální slizniční imunitní reakce. V zánětlivě změněné sliznici gastrointestinálního traktu pacientů s IBD bylo nalezeno zvýšené množství TH lymfocytů, makrofágů, neutrofilů a mastocytů. S tím souvisí i vyšší exprese prozánětlivých cytokinů jako např. IL-1ß, IL-6, IL-12, tumor nekrotizujícího faktoru – TNFα, interferonu (IFN)-γ [8]. Vliv na expresi těchto proteinů byl prokázán u celé řady rostlinných extraktů a izolovaných látek. Například kurkumin z rostliny Curcuma longa vykazoval tyto účinky v řadě in vivo studií [9–11] a na jejich základě byl zahrnut do klinických hodnocení, stejně jako látky získané z Cannabis sativa [12,13] či Tripterygium wilfordii [14,15].
Významnou roli by v etiologii střevních zánětů mohl hrát také oxidativní stres. Nedávné studie poukázaly na sníženou antioxidační kapacitu a zvýšené množství volných kyslíkových radikálů u pacientů s IBD [8]. U rostlin je v in vivo studiích testována schopnost redukovat peroxidaci lipidů a zvyšovat celkovou antioxidační kapacitu. Proto je sledována aktivita myeloperoxidázy, hladiny malondialdehydu, superoxiddismutáz, katalázy či glutathionu. Antioxidační efekt byl na experimentálních modelech kolitidy prokázán např. u rostlin Polygonum multiflorum [16], Vitis vinifera [17], Camellia sinensis [18,19] nebo Zingiber officinale [20].
V zánětlivém procesu hraje důležitou roli metabolizmus kyseliny arachidonové související s produkcí cyklooxygenáz (COX). COX-2 je inducibilní formou enzymu katalyzujícího syntézu prostaglandinů na základě působení prozánětlivých cytokinů. Snížit hladinu COX-2 u experimentálních modelů kolitidy dokázal resveratrol z Vitis vinifera [17,21,22], kurkumin z Curcuma longa [23–25], berberin z Berberis vulgaris [26] nebo glykoprotein z plodů rostliny Gardenia jasminoides [27]. Tyto přírodní látky také snižovaly hladinu oxidu dusnatého a inducibilní syntázy oxidu dusnatého (iNOS), která je rovněž zapojena do zánětlivých reakcí [9,17,22,25–27]. Nadprodukce dalšího metabolitu kyseliny arachidonové, leukotrienu (LT) B4, byla pozorována u pacientů s různými chronickými zánětlivými chorobami, včetně IBD. Prozatím byl efekt redukce LT B4 popsán u Aloe vera [28] a Plantago ovata [29].
U pacientů s chronickými střevními záněty byla dále zjištěna nadměrná aktivace NF-κB, transkripčního faktoru regulujícího expresi řady genů spojených se zánětlivou reakcí a apoptózou. Rostliny jako např. Berberis vulgaris [26], Curcuma longa [30], Camellia sinensis [31–33] a Ginkgo biloba [34] inhibují aktivaci nukleárního faktoru na různých úrovních signální dráhy.
Klinické studie
Klinické studie sledující účinnost fytoterapie jsou prováděny u pacientů s Crohnovou chorobou i ulcerózní kolitidou. Hodnotí se především změna aktivity onemocnění, endoskopický nález, doba setrvání v remisi nebo její dosažení a potřeba užití dalších léků. Vyšší výpovědní hodnotu mají studie randomizované, dvojitě zaslepené a s větším počtem pacientů. Ze studií s malým počtem pacientů, nekontrolovaných a nezaslepených nelze vyvodit spolehlivé závěry, mohou však sloužit jako podklady pro další hodnocení.
Jednou z přírodních látek, která by mohla mít do budoucna své využití v doplňkové terapii IBD, je kurkumin (v potravinářství označovaný jako E100), žluté přírodní barvivo extrahované z oddenku rostliny Curcuma longa. V řadě in vivo studií na různých modelech kolitidy se potvrdily jeho protizánětlivé i antioxidační účinky. Podávání kurkuminu zlepšilo makroskopické i histologické skóre, snížilo expresi prozánětlivých a zvýšilo expresi protizánětlivých cytokinů. Kurkumin potlačuje aktivaci NF-κB, snižuje expresi COX-2 a iNOS a neutrofilní infiltraci [9–11,23–25,30]. Výsledkem pilotní studie u pacientů s CD bylo snížení indexu aktivity onemocnění [35]. Pacientům s UC umožnilo přidání kurkuminu ke stávající terapii snížit dávky nebo úplně vysadit léčbu mesalazinem. Tato přírodní látka se rovněž osvědčila jako doplněk ke standardní terapii v udržovací léčbě UC. Randomizovaná, dvojitě zaslepená multicentrická studie vykázala nižší frekvenci relapsu onemocnění při kombinaci standardní terapie s kurkuminem ve srovnání s monoterapií aminosalicyláty [35,36].
Účinek srovnatelný s mesalazinem prokázal také extrakt z rostliny Andrographis paniculata u pacientů s různě aktivní UC. Rostlina je široce používaná k léčbě zánětlivých a infekčních onemocnění v asijských zemích. Za účinek extraktu jsou pravděpodobně zodpovědné diterpenické laktony andragrafolidy [37,38].
Další diskutovanou rostlinou je Boswellia serrata a její pryskyřice, která je testována ve formě různých extraktů. Efekt srovnatelný se standardní terapií vykázal pouze chloroform/metanolický extrakt s označením H15 u pacientů s aktivní CD [39] a čistá pryskyřice u pacientů s aktivní UC [40,41]. Větší frekvence remise u pacientů užívajících pryskyřici naznačuje, že by mohla být účinným lékem v terapii UC s minimálními vedlejšími účinky. Za působení je pravděpodobně zodpovědný derivát triterpenické kyseliny boswellové, acetyl-11-keto-ß-boswellová kyselina (AKBA), které je přiřazována řada biologických účinků [42]. To potvrzuje také in vivo experiment na modelu indomethacinové kolitidy. Extrakt H15 a AKBA prokázaly protizánětlivé i antioxidační působení a významně snížily poškození střevní tkáně [43]. Ostatní typy extraktů nevykazovaly účinek [44].
Vědci se v klinických studiích rovněž zaměřili na Aloe vera, rostlinu, která byla u pacientů s IBD roky používána i přes nedostatek důkazů o jejích účincích na střevní záněty. Nedávné in vivo studie na modelu DSS indukované kolitidy u potkanů prokázaly, že gel z aloe i jeho složky, aloin a aloesin, významně snižují hladinu prozánětlivých markerů jako TNFα, IL-1ß či aktivitu myeloperoxidázy [28]. Klinické studie hodnotily účinnost gelu u pacientů s aktivní ulcerózní kolitidou. Perorální léčba gelem z aloe dokázala snížit index aktivity onemocnění a zlepšit histologické skóre více než placebo [45].
Svými výsledky v klinickém testování zaujaly i obiloviny z čeledi Poaceae, ječmen (Hordeum vulgare) a pšenice (Triticum aestivum). Užívání pšeničné šťávy je pro léčbu různých gastrointestinálních obtíží a pro celkovou detoxikaci organizmu doporučováno po více než 30 let [46]. Randomizovaná dvojitě zaslepená kontrolovaná studie prokázala u pacientů s aktivní UC významné snížení indexu aktivity onemocnění a snížení závažnosti rektálního krvácení [46]. Naklíčený ječmen se pak v různých studiích projevil jako vhodná doplňková léčba u aktivní UC [47] i u pacientů v remisi [48]. Ječmen snížil klinickou aktivitu choroby, snížil hladinu zánětlivých interleukinů a prodloužil dobu remise [49]. Za účinek naklíčeného ječmene jsou pravděpodobně zodpovědné kyselina máselná a propionová, které vznikají jeho fermentací ve střevě. Podobně je tomu u semen Plantago ovata. Randomizovaná klinická studie prokázala, že jejich přidání ke standardní terapii usnadňuje u UC dosažení remise [50]. In vivo studie na transgenních potkanech potvrdila, že právě mastné kyseliny s krátkým řetězcem inhibují produkci TNFα [29].
Léčebné účinky Cannabis sativa jsou již řadu let zkoumány v různých oborech medicíny. K popisu účinku konopí u pacientů s CD byla provedena retrospektivní observační studie, která zjistila, že konopí snižuje index aktivity onemocnění a potřebu užívání dalších léků a operací. Přestože kouření bylo nejčastějším způsobem aplikace, protizánětlivý účinek mohl být stejně dobře dosažen i perorálním podáním [51]. In vivo studie potvrzují účinky na různých modelech kolitidy. Testovaný kanabidiol a kanabigerol, nepsychotropní kanabinoidy, snižují expresi iNOS, modulují hladiny cytokinů a vykazují antioxidační účinky [12,13,52].
Součástí řady doplňků stravy je olej ze semen pupalky, Oenothera biennis. Studie srovnávala účinky pupalkového oleje, olivového oleje a rybího tuku jako doplňku obvyklé terapie. Pupalkový olej jako jediný zlepšil konzistenci stolice, ale nepřinesl žádný jiný terapeutický efekt, stejně jako ostatní [53].
Klinické hodnocení rostliny Angelica sinensis proběhlo v návaznosti na zjištění, že u pacientů s UC jsou výrazně aktivovány trombocyty, což by mohlo souviset s vaskulárním poškozením endotelu. Andělika zpracovaná do lékové formy pro injekční podání inhibovala aktivaci trombocytů, snížila vaskulární poškození endotelu a zlepšila mikrocirkulaci. S účinkem je spojován ferulát sodný, hlavní složka injekcí [54].
Borůvky, plody Vaccinium myrtillus, jsou bohatým zdrojem fenolických látek, především anthokyaninů, u nichž byly prokázány antioxidační a protizánětlivé účinky. Pilotní studie ověřovala efekt vysokých dávek anthokyaninů u pacientů s ulcerózní kolitidou. Po šesti týdnech léčby došlo ke snížení aktivity onemocnění až ke kompletní remisi, která však nebyla udržitelná po vysazení testovaného preparátu [55].
Možnost vysazení terapie kortikoidy u pacientů s CD zjišťovala studie s bylinnou směsí obsahující prášek z pelyňku Arthemisia absinthium. I přes postupné snižování dávek kortikoidů se příznaky CD zmírňovaly a po několika týdnech došlo u pacientů užívajících bylinnou směs ke kompletní remisi onemocnění. Mimo jiné vyhodnocení Hamiltonovy stupnice deprese ukázalo, že pelyněk má vliv na náladu a kvalitu života pacientů [56].
V pilotní studii s pryskyřicí keře Pistacia lenticus u pacientů s aktivní CD bylo zjištěno snížení plazmatických hladin IL-6 a C-reaktivního proteinu (CRP). Významně se snížil i index aktivity choroby. Hlavní složkou pryskyřice, tzv. mastichy, je kyselina oleanolová, triterpen s protizánětlivými a protinádorovými účinky [57,58].
Extrakt z rostliny Tripterygium wilfordii byl také testován u pacientů s aktivní CD. Terapie extraktem vedla k poklesu plazmatických hladin CRP, TNFα a IL-1ß [59]. Účinek je přiřazován diterpenoidní látce triptolidu, jejíž aktivita byla potvrzena i na experimentálních modelech kolitidy. Podávání triptolidu vedlo u myší ke snížení exprese prozánětlivých cytokinů a k inhibici signální dráhy NF-κB [14,15].
Výsledky klinických studií na pacientech s UC a CD shrnují tab. 1 a 2.
Tab. 1. Přehled klinických studií u pacientů s ulcerózní kolitidou. Tab. 1. Summary of clinical trials of patients with ulcerative colitis. 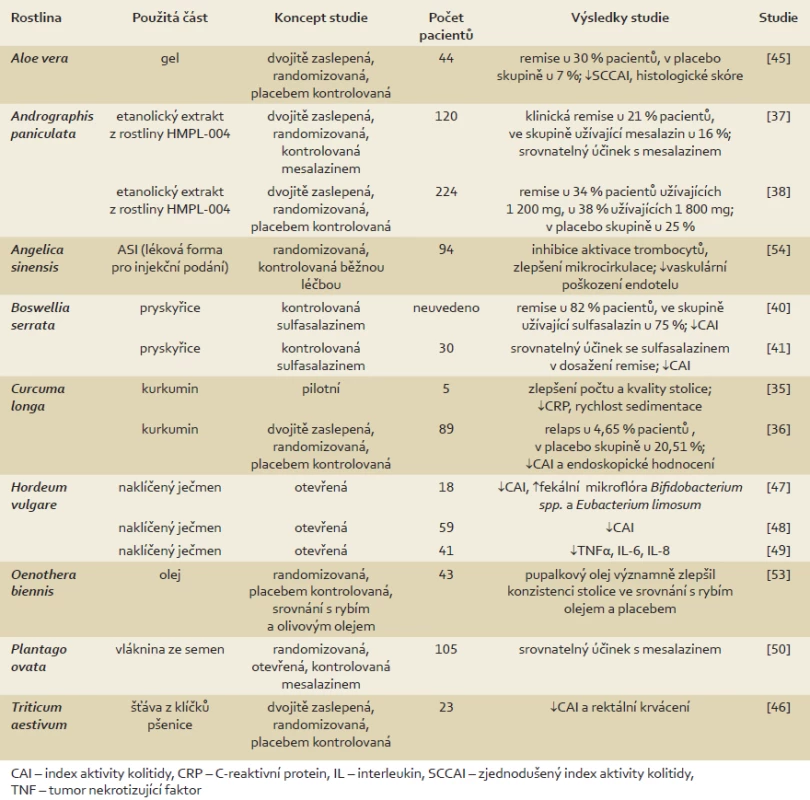
Tab. 2. Přehled klinických studií u pacientů s Crohnovou chorobou. Tab. 2. Summary of clinical trials of patients with Crohn’s disease. 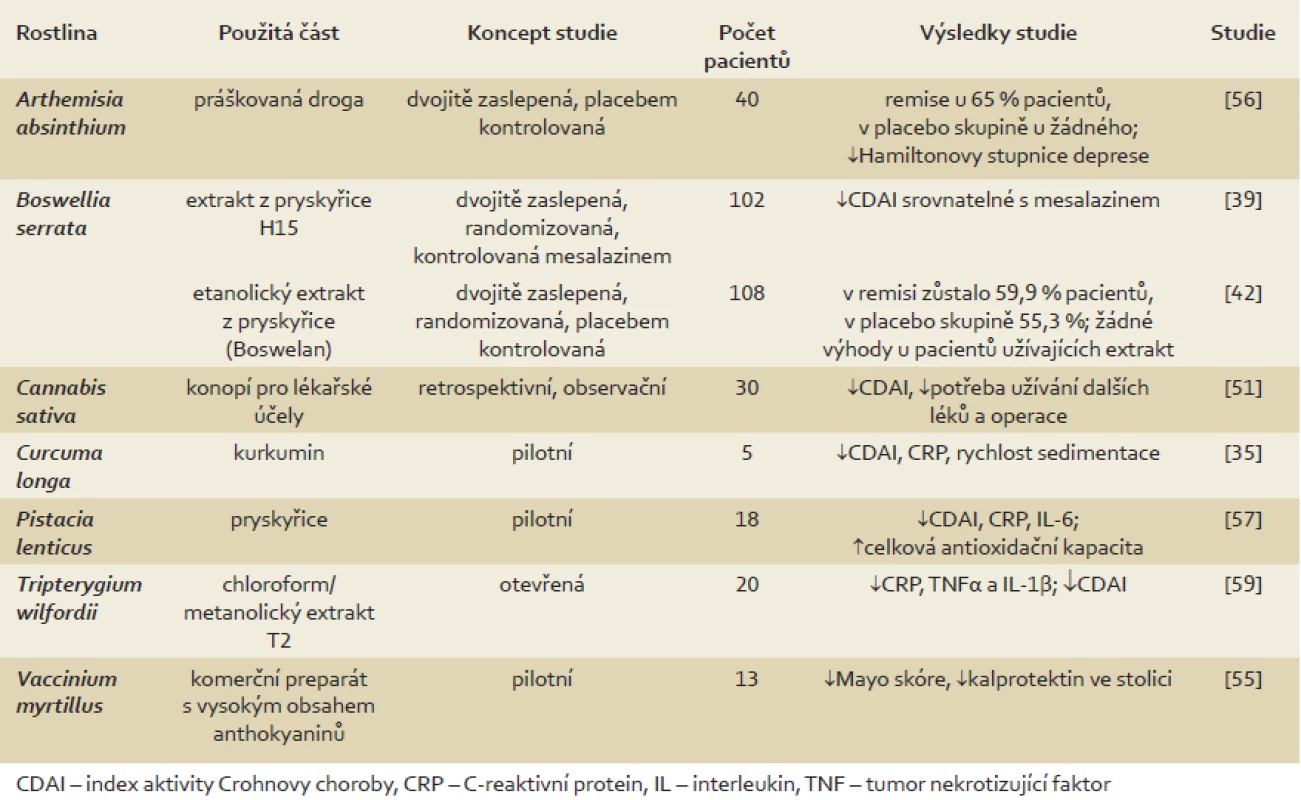
Závěr
Rostlinná říše je zdrojem obrovského množství účinných látek, které by mohly přispět k zefektivnění terapie idiopatických střevních zánětů. Řada látek a extraktů je schopna snižovat index aktivity onemocnění, prodlužovat dobu klinické remise a snižovat poškození střevní tkáně a potřebu užívání dalších léků nebo nutnost operace. Rostliny, které pozitivně ovlivňují průběh onemocnění, jsou různorodou skupinou, ať už svým systematickým zařazením nebo obsahovými látkami. In vivo experimenty osvětlují mechanizmus účinku a klinická hodnocení sledují jejich působení na lidský organizmus. Výsledky studií poukazují na možnost využití některých přírodních látek v terapii chronických střevních zánětů samostatně či v kombinaci se standardní léčbou. Pro získání přesvědčivých důkazů o benefitu fytoterapie je však nutné provedení dalších, rozsáhlejších a zejména multicentrických, studií.
Tato práce byla podpořena grantovým projektem IGA VFU Brno 85/2013/FaF (Z. V.) a projektem Operační program Vzdělávání pro konkurenceschopnost CZ.1.07/2.3.00/30.0014 (J. H.).
Autoři deklarují, že v souvislosti s předmětem studie nemají žádné komerční zájmy.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
Doručeno: 5. 2. 2014
Přijato: 31. 3. 2014
Zora Vochyánová
Ústav přírodních léčiv
Farmaceutická fakulta
Veterinární a farmaceutická univerzita Brno
Palackého 1–3, 612 42 Brno
z.vochyanova@gmail.com
Zdroje
1. Sartor RB. Mechanisms of disease: pathogenesis of Crohn’s disease and ulcerative colitis. Nat Clin Pract Gastroenterol Hepatol 2006; 3(7): 390–407.
2. Bensoussan M, Jovenin N, Garcia B et al. Complementary and alternative medicine use by patients with inflammatory bowel disease: results from a postal survey. Gastroenterol Clin Biol 2006; 30(1): 14–23.
3. Langmead L, Rampton DS. Review article: complementary and alternative therapies for inflammatory bowel disease. Aliment Pharmacol Ther 2006; 23(3): 341–349. doi: 10.1111/j.1365-2036.2006.02761.x.
4. Life and IBD. Complementary and Alternative medicines (CAMs). [online]. Available from: http://www.lifeandibd.org/ulcerative-colitis-teenager/taking-control-of-your-ibd/complementary-and-alternative-medicines.html.
5. Mayo Clinic. Ulcerative Colitis – Alternative medicine. [online]. Available from: http://www.mayoclinic.com/health/ulcerative-colitis/DS00598/DSECTION=alternative--medicine.
6. Rahimi R, Shams-Ardekani MR, Abdollahi M. A review of the efficacy of traditional Iranian medicine for inflammatory bowel disease. World J Gastroenterol 2010; 16(36): 4504–4514.
7. Jurjus AR, Khoury NN, Reimund JM. Animal models of inflammatory bowel disease. J Pharmacol Toxicol Methods 2004; 50(2): 81–92.
8. Rahimi R, Mozaffari S, Abdollahi M. On the use of herbal medicines in management of inflammatory bowel diseases: a systematic review of animal and human studies. Dig Dis Sci 2009; 54(3): 471–480. doi: 10.1007/s10620-008-0368-x.
9. Ukil A, Maity S, Karmakar S et al. Curcumin, the major component of food flavour turmeric, reduces mucosal injury in trinitrobenzene sulphonic acid-induced colitis. Br J Pharmacol 2003; 139(2): 209–218.
10. Jian YT, Wang JD, Mai GF et al. Modulation of intestinal mucosal inflammatory factors by curcumin in rats wih colitis. Di Yi Jun Yi Da Xue Xue Bao 2004; 24(12): 1353–1358.
11. Zhang M, Deng CS, Zheng JJ et al. Curcumin regulated shift from Th1 to Th2 in trinitrobenzene sulphonic acid-induced chronic colitis. Acta Pharmacol Sin 2006; 27(8): 1071–1077.
12. Borrelli F, Aviello G, Romano B et al. Cannabidiol, a safe and non-psychotropic ingredient of the marijuana plant Cannabis sativa, is protective in a murine model of colitis. J Mol Med 2009; 87(11): 1111–1121. doi: 10.1007/s00109-009-0512-x.
13. Borrelli F, Fasolino I, Romano B et al. Beneficial effect of the non-psychotropic plant cannabinoid cannabigerol on experimental inflammatory bowel disease. Biochem Pharmacol 2013; 85(9): 1306–1316. doi: 10.1016/j.bcp.2013.01.017.
14. Wei X, Gong J, Zhu J et al. Therapeutic effects of triptolide on interleukin-10 gene-deficient mice with colitis. Int Immunopharmacol 2008; 8(13–14): 1808–1812. doi: 10.1016/j.intimp.2008.08.019.
15. Wei X, Gong J, Zhu J et al. The suppressive effect of triptolide on chronic colitis and TNF-alpha/TNFR2 signal pathway in interleukin-10 deficient mice. Clin Immunol 2008; 129(2): 211–218. doi: 10.1016/j.clim.2008.07.018.
16. Wang X, Zhao L, Han T et al. Protective effects of 2,3,5,4'-tetrahydroxystilbene-2-O-beta-d-glucoside, an active component of Polygonum multiflorum Thunb, on experimental colitis in mice. Eur J Pharmacol 2008; 578(2–3): 339–348.
17. Wang YH, Yang XL, Wang L et al. Effects of proanthocyanidins from grape seed on treatment of recurrent ulcerative colitis in rats. Can J Physiol Pharmacol 2010; 88(9): 888–898. doi: 10.1139/y10-071.
18. Maity S, Ukil A, Karmakar S et al. Thearubigin, the major polyphenol of black tea, ameliorates mucosal injury in trinitrobenzene sulfonic acid-induced colitis. Eur J Pharmacol 2003; 470(1–2): 103–112.
19. Brückner M, Westphal S, Domschke W et al. Green tea polyphenol epigallocatechin-3-gallate shows therapeutic antioxidative effects in a murine model of colitis. J Crohns Colitis 2012; 6(2): 226–235. doi: 10.1016/j.crohns.2011.08.012.
20. El-Abhar HS, Hammad LN, Gawad HS et al. Modulating effect of ginger extract on rats with ulcerative colitis. J Ethnopharmacol 2008; 118(3): 367–372. doi: 10.1016/j.jep.2008.04.026.
21. Martín AR, Villegas I, La Casa C et al. Resveratrol, a polyphenol found in grapes, suppresses oxidative damage and stimulates apoptosis during early colonic inflammation in rats. Biochem Pharmacol 2004; 67(7): 1399–1410.
22. Sánchez-Fidalgo S, Cárdeno A, Villegas I et al. Dietary supplementation of resveratrol attenuates chronic colonic inflammation in mice. Eur J Pharmacol 2010; 633(1–3): 78–84. doi: 10.1016/j.ejphar.2010.01.025.
23. Jiang H, Deng CS, Zhang M et al. Curcumin-attenuated trinitrobenzene sulphonic acid induces chronic colitis by inhibiting expression of cyclooxygenase-2. World J Gastroenterol 2006; 12(24): 3848–3853.
24. Zhang M, Deng C, Zheng J et al. Curcumin inhibits trinitrobenzene sulphonic acid-induced colitis in rats by activation of peroxisome proliferator-activated receptor gamma. Int Immunopharmacol 2006; 6(8): 1233–1242.
25. Camacho-Barquero L, Villegas I, Sánchez-Calvo JM et al. Curcumin, a Curcuma longa constituent, acts on MAPK p38 pathway modulating COX-2 and iNOS expression in chronic experimental colitis. Int Immunopharmacol 2007; 7(3): 333–342.
26. Lee IA, Hyun YJ, Kim DH. Berberine ameliorates TNBS-induced colitis by inhibiting lipid peroxidation, enterobacterial growth and NF-κB activation. Eur J Pharmacol 2010; 648(1–3): 162–170. doi: 10.1016/j.ejphar.2010.08.046.
27. Oh PS, Lim KT. Plant originated glycoprotein has anti-oxidative and anti-inflammatory effects on dextran sulfate sodium-induced colitis in mouse. J Biomed Sci 2006; 13(4): 549–560.
28. Park MY, Kwon HJ, Sung MK. Dietary aloin, aloesin, or aloe-gel exerts anti-inflammatory activity in a rat colitis model. Life Sci 2011; 88(11–12): 486–492. doi: 10.1016/j.lfs.2011.01.010.
29. Rodríquez-Cabezas ME, Gálvez J, Camuesco D et al. Intestinal anti-inflammatory activity of dietary fiber (Plantago ovata seeds) in HLA-B27 transgenic rats. Clin Nutr 2003; 22(5): 463–471.
30. Jian YT, Mai GF, Wang JD et al. Preventive and therapeutic effects of NF-kappaB inhibitor curcumin in rats colitis induced by trinitrobenzene sulfonic acid. World J Gastroenterol 2005; 11(12): 1747–1752.
31. Ran ZH, Chen C, Xiao SD. Epigallocatechin-3-gallate ameliorates rats colitis induced by acetic acid. Biomed Pharmacother 2008; 62(3): 189–196. doi: 10.1016//j.biopha.2008.02.002.
32. Abboud PA, Hake PW, Burroughs TJ et al. Therapeutic effect of epigallocatechin-3-gallate in a mouse model of colitis. Eur J Pharmacol 2008; 579(1–3): 411–417.
33. Ukil A, Maity S, Das PK. Protection from experimental colitis by theaflavin-3,3´-digallate correlates with inhibition of IKK and NF-kappaB activation. Br J Pharmacol 2009; 149(1): 121–131.
34. Zhou YH, Yu JP, Liu YF et al. Effects of Ginkgo biloba extract on inflammatory mediators (SOD, MDA, TNF-alpha, NF-kappaBp65, IL-6) in TNBS-induced colitis in rats. Mediators Inflamm 2006; 2006(5): 92642.
35. Holt PR, Katz S, Kirshoff R. Curcumin therapy in inflammatory bowel disease: a pilot study. Dig Dis Sci 2005; 50(11): 2191–2193.
36. Hanai H, Iida T, Takeuchi K et al. Curcumin maintenance therapy for ulcerative colitis: randomized, multicenter, double-blind, placebo-controlled trial. Clin Gastroenterol Hepatol 2006; 4(12): 1502–1506.
37. Tang T, Targan SR, Li ZS et al. Randomised clinical trial: herbal extract HMPL--004 in active ulcerative colitis – a double-blind comparison with sustained release mesalazine. Aliment Pharmacol Ther 2011; 33(2): 194–202. doi: 10.1111//j.1365-2036.2010.04515.x.
38. Sandborn WJ, Targan SR, Byers VS et al. Andrographis paniculata extract (HMPL--004) for active ulcerative colitis. Am J Gastroenterol 2013; 108(1): 90–98. doi: 10.1038//ajg.2012.340.
39. Gerhardt H, Seifert F, Buvari P et al. Therapy of active Crohn disease with Boswellia serrata extract H 15. J Gastroenterol 2001; 39(1): 11–17.
40. Gupta I, Parihar A, Malhotra P et al. Effects of Boswellia serrata gum resin in patients with ulcerative colitis. Eur J Med Res 1997; 2(1): 37–43.
41. Gupta I, Parihar A, Malhotra P et al. Effects of gum resin of Boswellia serarata in patients with chronic colitis. Planta Med 2001; 67(5): 391–395.
42. Anthoni C, Laukoetter MG, Rijcken E et al. Mechanisms underlying the anti-inflammatory action of boswellic acid derivatives in experimental colitis. Am J Physiol Gastrointest Liver Physiol 2006; 290(6): G1131–G1137.
43. Krieglstein CF, Anthoni C, Rijcken EJ et al. Acetyl-11-keto-beta-boswellic acid, a constituent of a herbal medicine from Boswellia serrata resin, attenuates experimental ileitis. Int J Colorectal Dis 2001; 16(2): 88–95.
44. Holtmeier W, Zeuzem S, Preiss J et al. Randomized, placebo-controlled, double-blind trial of Boswellia serrata in maintaining remission of Crohn´s disease: good safety profile but lack of efficacy. Inflamm Bowel Dis 2011; 17(2): 573–582. doi: 10.1002/ibd.21345.
45. Langmead L, Feakins RM, Goldthorpe S et al. Randomized, double-blind, placebo-controlled trial of oral aloe vera gel for active ulcerative colitis. Aliment Pharmacol Ther 2004; 19(7): 739–747.
46. Ben-Arye E, Goldin E, Wengrower D et al. Wheat grass juice in the treatment of active distal ulcerative colitis: a randomized double-blind placebo-controlled trial. Scand J Gastroenterol 2002; 37(4): 444–449.
47. Kanauchi O, Suga T, Tochihara M et al. Treatment of ulcerative colitis by feeding with germinated barley foodstuff: first report of a multicenter open control trial. J Gastroenterol 2002; 37 (Suppl 14): 67–72.
48. Hanai H, Kanauchi O, Mitsuyama K et al. Germinated barley foodstuff prolongs remission in patients with ulcerative colitis. Int J Mol Med 2004; 13(5): 643–647.
49. Faghfoori Z, Navai L, Shakerhosseini R et al. Effects of an oral supplementation of germinated barley foodstuff on serum tumour necrosis factor-alpha, interleukin-6 and -8 in patients with ulcerative colitis. Ann Clin Biochem 2011; 48(3): 233–237. doi: 10.1258//acb.2010.010093.
50. Fernández-Banares F, Hinojosa J, Sánchez-Lombrana JL et al. Randomized clinical trial of Plantago ovata seeds (dietary fiber) as compared with mesalamine in maintaining remission in ulcerative colitis. Spanish Group for the Study of Crohn’s Disease and Ulcerative Colitis (GETECCU). Am J Gastroenterol 1999; 94(2): 427–433.
51. Naftali T, Lev LB, Yablecovitch D et al. Treatment of Crohn´s disease with cannabis: an observational study. Isr Med Assoc J 2011; 13(8): 455–458.
52. Schicho R, Storr M. Topical and systemic cannabidiol improves trinitrobenzene sulfonic acid colitis in mice. Pharmacology 2012; 89(3–4): 149–155. doi: 10.1159/000336871.
53. Greenfield SM, Green AT, Teare JP et al. A randomized controlled study of evening primrose oil and fish oil in ulcerative colitis. Aliment Pharmacol Ther 1993; 7(2): 159–166.
54. Dong WG, Liu SP, Zhu HH et al. Abnormal function of platelets and role of angelica sinensis in patients with ulcerative colitis. World J Gastroenterol 2004; 10(4): 606–609.
55. Biedermann L, Mwinyi J, Scharl M et al. Bilberry ingestion improves disease activity in mild to moderate ulcerative colitis – an open pilot study. J Crohns Colitis 2013; 7(4): 271–279. doi: 10.1016/j.crohns.2012.07.010.
56. Omer B, Krebs S, Omer H et al. Steroid-sparing effect of wormwood (Artemisia absinthium) in Crohn’s disease: a double-blind placebo-controlled study. Phytomedicine 2007; 14(2–3): 87–95.
57. Kaliora AC, Stathopoulou MG, Triantafillidis JK et al. Chios mastic treatment of patients with active Crohn's disease. World J Gastroenterol 2007; 13(5): 748–753.
58. Liu J. Oleanolic acid and ursolic acid: research perspectives. J Ethnopharmacol 2005; 100(1–2): 92–94.
59. Ren J, Tao Q, Wang X et al. Efficacy of T2 in active Crohn’s disease: a prospective study report. Dig Dis Sci 2007; 52(8): 1790–1797.
Štítky
Dětská gastroenterologie Gastroenterologie a hepatologie Chirurgie všeobecná
Článek Neobvyklá komplikace ERCPČlánek Profesor Zdeněk MařatkaČlánek Ideo centisimiČlánek Digestivní endoskopieČlánek KvízČlánek Bezbolestná kolonoskopieČlánek Srovnání dietních návyků pacientů s kolorektálními neoplaziemi a jejich příbuzných prvního stupněČlánek Projekt RISING STARSČlánek XVIII. hradecké gastroenterologické a hepatologické dny a VIII. mezinárodní endoskopický workshopČlánek Správná odpověď na kvíz
Článek vyšel v časopiseGastroenterologie a hepatologie
Nejčtenější tento týden
2014 Číslo 3- Itoprid v léčbě funkční dyspepsie
- Farmakokinetika a tolerance pantoprazolu v dětském věku
- Vliv podávání prokinetik na riziko syndromu bakteriálního přerůstání u pacientů užívajících inhibitory protonové pumpy
- Efekt itopridu na motilitu jícnu a funkci dolního jícnového svěrače
- Strava bohatá na arginin a prolin slibuje urychlení hojení ran u diabetických pacientů
-
Všechny články tohoto čísla
- Digestivní endoskopie
- Kvíz
- Bezbolestná kolonoskopie
- Vodou asistovaná kolonoskopie
- Srovnání dietních návyků pacientů s kolorektálními neoplaziemi a jejich příbuzných prvního stupně
- Kombinovaná endoskopická a laparoskopická terapie akutního krvácení z žaludečních metastáz renálního karcinomu – videokazuistika
- Neobvyklá komplikace ERCP
- Profesor Zdeněk Mařatka
- 100 let od narození profesora Zdeňka Mařatky
- Ideo centisimi
- Porovnání účinnosti kolonické kapslové endoskopie a kolonoskopie v detekci polypů a karcinomů tlustého střeva a konečníku – multicentrická, prospektivní, cross-over studie
- Perspektivy biologické léčby u idiopatických střevních zánětů
- Rifaximin v léčbě gastrointestinálních onemocnění
- Experimentální elektrogastrografie
- Akútne krvácanie do horného gastrointestinálneho traktu – zriedkavá manifestácia adenokarcinómu pankreasu
- Rostliny v terapii idiopatických střevních zánětů
- Kolorektální screening a projekt adresného zvaní – zpětná vazba z regionu
- Vyjádření ke zpětné vazbě na program adresného zvaní ke kolorektálnímu screeningu
- Projekt RISING STARS
- „Single endoscopist“ cholangioskopia (Spyglass) na Slovensku – zavedenie metódy vo Fakultnej nemocnici Trnava
- 4th Prague endoscopic day and 15th endoscopic day IKEM
- 87th congress of Japan Gastroenterological Endoscopy Society, Fukuoka, 15.–17. 5. 2014, Japan
- XVIIIth gastroenterology and hepatology days in Hradec Králové and VIIIth international endoscopic workshop
- Looking back at the 10th Congress EAGEN Postgraduate School in Prague
- Správná odpověď na kvíz
- Golimumab – nové biologikum v léčbě ulcerózní kolitidy
- K odchodu pana prof. MUDr. Bohumila Fixy, DrSc.
- Citrafleet® – jednoduchá a efektivní příprava tlustého střeva před vyšetřením
- Autodidaktický test: digestivní endoskopie
- Gastroenterologie a hepatologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Rifaximin v léčbě gastrointestinálních onemocnění
- Citrafleet® – jednoduchá a efektivní příprava tlustého střeva před vyšetřením
- Akútne krvácanie do horného gastrointestinálneho traktu – zriedkavá manifestácia adenokarcinómu pankreasu
- Neobvyklá komplikace ERCP
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Revma Focus: Spondyloartritidy
nový kurz
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Autoři: prof. MUDr. Pavel Horák, CSc., doc. MUDr. Ludmila Brunerová, Ph.D., doc. MUDr. Václav Vyskočil, Ph.D., prim. MUDr. Richard Pikner, Ph.D., MUDr. Olga Růžičková, MUDr. Jan Rosa, prof. MUDr. Vladimír Palička, CSc., Dr.h.c.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



