-
Články
Top novinky
Reklama- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
Top novinky
Reklama- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariérní portál
Doporučené pozice
Reklama- Praxe
Top novinky
ReklamaXXXVI. Umělá inteligence v onkologii
Vyšlo v časopise: Klin Onkol 2022; 35(Supplementum 1): 123-125
Kategorie: XXXVI. Umělá inteligence v onkologii
XXXVI/ 271. Umělá inteligence v onkologii – možnosti využití v praxi
Halámková J.1, Nováček V.2
1 Klinika komplexní onkologické péče LF MU a MOÚ Brno, 2 Fakulta informatiky, MU Brno
Východiska: Umělá inteligence (artificial intelligence – AI) je odvětví informatiky, které se zabývá simulací inteligentního chování v počítačích. Pomocí matematických operací lze tyto systémy učit novým informacím a schopnosti se na jejich základě rozhodovat. Podoblastí umělé inteligence je strojové učení (machine learning – ML), při němž je počítač schopen zlepšovat svůj vlastní výkon průběžným začleňováním nově generovaných dat do těch stávajících. Jedním z oborů strojového učení je hluboké učení (deep learning – DL), ve kterém jsou využívány matematické algoritmy připomínající lidské poznávání, jako jsou zejména neuronové sítě. Cíl: Cílem sdělení je nastínit možnosti využití AI v klinické praxi. Jedním ze směrů, kterým se využití umělé inteligence v onkologii ubírá, je zobrazování, ať už je to hodnocení jak radiologických obrazů, tak i histopatologických nálezů či přímo fotografií konkrétních lézí. Oborem, který se soustředí na extrakci velkého množství znaků nedetekovatelných člověkem, které vyplývají z medicínských obrazů, je radiomika. V radiologii se AI soustřeďuje na detekci lézí screeningových obrazů, např. mamografických, a pomáhá klasifikovat jednotlivé pixely podle orgánů nebo lézí vč. jejich objemu a velikosti, např. u gliomů mozku. Umělou inteligenci lze využít také k monitorování dynamiky patologických změn. Možnosti odhadnout riziko vzniku malignity a stanovit tak nejvhodnější screeningovou metodu či schopnost predikce léčebné toxicity či terapeutické odpovědi jsou dalšími relevantními příležitostmi, jak zapojit umělou inteligenci do klinické praxe. Hodnocení prognózy je v experimentálních modelech v současnosti přesnější než prostřednictvím dosud užívaných metod. Další velkou kapitolou je využití umělé inteligence ve výzkumu a vývoji nových léčiv pomocí prediktivních modelů efektivity či nových nástrojů náboru nemocných do klinických hodnocení. Využití velkého množství dat genomiky a k ní přidružených oborů povede k tomu, že se umělá inteligence stane zásadní pro rozvoj personalizované medicíny, a to jak prevence či diagnostiky, tak i léčby. Kromě toho má umělá inteligence také nezanedbatelný potenciál snížit náklady na zdravotní péči a zmenšit rozdíly v její dostupnosti v různých regionech. Závěr: Možnosti využití umělé inteligence v onkologii jsou v současné době velmi široké a její dosah v tuto chvíli ani nedokážeme odhadnout. Je jen otázka, jak se k jejímu zapojení do běžné klinické praxe postavíme my zdravotníci. Umělá inteligence bude totiž jen tak dobrá, jak dobře se ji naučíme využívat.
XXXVI/ 272. AIcope – personalizovaný prediktivní nástroj pro zvyšování informačního komfortu onkologických pacientek pomocí umělé inteligence
Nováček V.
Fakulta informatiky, MU Brno
V roce 2016 bylo v ČR registrováno více než půl milionu onkologických pacientů, z toho 96 500 nově diagnostikovaných. Každá taková nová diagnóza znamená více či méně radikální změnu života nejen pacientů, ale i jejich okolí. Jedním z nejefektivnějších způsobů, jak se s touto změnou vyrovnávat, je dostatečná informovanost o nemoci a zvoleném léčebném postupu. Lepší informovanost vede k vyšší motivaci a lepší adherenci k léčbě, zvýšení spokojenosti pacienta a jeho rodiny a v neposlední řadě ke snížení stresu ošetřujících lékařů. Uspokojivé naplnění optimální informovanosti je ovšem zřídkakdy možné. Jedním z hlavních důvodů je nedostatek časového prostoru pro zevrubnou komunikaci s pacienty v rámci stávající klinické praxe. Ne vždy se tedy potenciálně užitečné informace k onkologicky nemocným dostanou ve formě a množství, jež jsou schopni v dané situaci zpracovat. Problém informačního nedostatku řeší projekt AIcope, v němž extrahujeme údaje z elektronických lékařských záznamů o pacientkách s diagnózou C50 (karcinom prsu) a integrujeme je s informacemi z veřejných datových zdrojů o nemocech, intervencích a lécích. Následně počítáme podobnosti mezi pacientkami a získané vztahy využíváme k vytváření personalizovaných modelů pro predikci možného průběhu a komplikací onemocnění a léčby nově diagnostikovaných pacientek. Pro prezentaci těchto informací pacientkám citlivou a intuitivní formou rozvíjíme webová rozhraní pro dotazování a průzkum extrahovaných znalostí a vypočítaných predikcí. Tento proces probíhá dle zásad tzv. ko-kreace, tj. vývoje uživatelských rozhraní společně s lékaři, pacienty a klinickými psychology. Výsledný prototyp bude vyhodnocen jeho předběžným nasazením v klinickém prostředí a porovnáním se současnými postupy informování pacientů. Principem je vytvořit takové IT prostředí, které pomocí umělé inteligence zlepší informovanost pacientů o jejich onemocnění a v případě zájmu také potenciálně zjednoduší nemocnému výběr z více možných terapeutických postupů na podkladě biologického profilu jejich nádoru, klinického stavu, komorbidit a v neposlední řadě jejich preferencí, s plnou podporou ošetřujícího lékaře.
Podpořeno mezioborovým grantovým programem Masarykovy univerzity GAMU v rámci projektu AIcope.
XXXVI/ 273. Predikce průběhu onkologické léčby na základě podobností pacientek vypočítaných z jejich klinických zpráv
Zelina P., Nováček V.
MU Brno
Klinické zprávy obsahují spoustu užitečných informací, které ale většinou nejsou vhodné pro naivní algoritmické zpracování. Text má mnohdy volnou strukturu, obsahuje zkratky a někdy i překlepy. Naším cílem je využít různé metody zpracování přirozeného jazyka (NLP) k lepšímu strojovému porozumění volně formátovaných klinických zpráv a výpočtu podobností mezi pacientkami. Tato podobnost může být následně použita pro personalizaci informací dodávaných pacientkám (např. v systému AIcope), jako nástroj pro odborníky, který umožňuje organizaci a průzkum velkého množství pacientek, nebo ke shlukování podobných průběhů nemoci a následné predikci budoucího průběhu léčby (např. zákroky či možné komplikace). Přestože zatím pracujeme s daty pacientek s diagnózou C50 (karcinom prsu), vyvíjený systém je modulární a univerzální, takže by nemělo být těžké jej upravit pro jiná onemocnění či nahradit některé jeho části. Pro výpočet podobností používáme různé metody embeddingů jednotlivých zpráv (projekce zpráv do vektorového prostoru), které pak kombinujeme a porovnáváme mezi pacientkami. Zároveň provádíme validaci shody generovaných podobností s odborným lékařským posudkem ve spolupráci s lékaři z Masarykova onkologického ústavu.
Podpořeno mezioborovým grantovým programem Masarykovy univerzity GAMU v rámci projektu AIcope: MUNI/ G/ 1763/ 2020.
XXXVI/ 274. Segmentace a klasifikace nádorů mozku
Kozubek M.1, Lux F.1, Michálek J.1, Matula P.1, Kopřivová T.2, Dostál M.2,3, Vybíhal V.4, Keřkovský M.2
1 Centrum analýzy biomedicínského obrazu, MU Brno, 2 Klinika radiologie a nukleární medicíny LF MU a FN Brno, 3 Biofyzikální ústav LF MU a FN Brno, 4 Neurochirurgická klinika LF MU a FN Brno
V rámci Centra umělé inteligence v onkologii se ve spolupráci s Masarykovou univerzitou a Fakultní nemocnicí Brno zabýváme analýzou obrazů nádorů mozku, jejichž diagnostika je založená na zobrazení magnetickou rezonancí (MRI). Multimodální MRI zobrazovací techniky, v poslední době vč. difuze, mají ve spojení s pokročilou analýzou dat potenciál zpřesnit možnosti neinvazivní analýzy mozkových tumorů. Hlavním cílem spolupráce je vyvinout automatizované metodické postupy umožňující jak segmentaci, tak klasifikaci (diferenciaci) jednotlivých druhů mozkových nádorů. Do prospektivní studie jsou postupně zařazováni pacienti s mozkovým nádorem, kteří podstupují MRI zobrazení mozku a následně resekci či stereotaktickou biopsii patologického ložiska. S využitím metod hlubokého učení jsou vyvíjeny algoritmy automatizované segmentace v obrazech MRI a klasifikace jednotlivých druhů tumorů na základě jejich morfologických a difuzních charakteristik. U segmentace jsou stanovovány oblasti obrazu obsahující edém a samotný tumor s rozlišením jeho syticí a nesyticí části. Pro trénování algoritmů hlubokého učení a také pro vyhodnocování jejich přesnosti jsou všechny obrazy ručně segmentovány a pro diferenciaci jednotlivých druhů tumorů jsou k dispozici histopatologické nálezy. Pro začátek byly pro vývoj metod připraveny dvě datové sady, a to retrospektivně 100 pacientů s nádory vizuálně stejného typu (high-grade gliomy), kompatibilní s mezinárodním benchmarkem BRATS (BRAin Tumor Segmentation) a 134 doposud prospektivně nabraných pacientů s 6 různými druhy nádorů (high-grade gliomy, low-grade gliomy, meningeomy, lymfomy, metastáze a jiné). Cílový počet prospektivních pacientů je 240. Pro vývoj segmentačních metod jsme zvolili modifikaci známé architektury U-Net a dosáhli výsledků srovnatelných s publikovanými metodami, avšak pracujících nejenom pro high-grade gliomy, ale i pro dalších 5 výše uvedených druhů nádorů. Kromě vývoje vlastních metod byl na retrospektivní sadě vyzkoušen i přístup federovaného učení segmentace přes 71 pracovišť z 6 kontinentů v široké mezinárodní spolupráci [1], přičemž bylo dosaženo zlepšení v průměru o 19 % oproti standardnímu postupu. Momentálně zkoušíme ke standardní čtveřici modalit (T1, T2, T1 s kontrastem, T2-FLAIR) přidat i modalitu IVIM dostupnou pro prospektivní sadu, což by mělo dále zlepšit segmentační výsledky a umožnit klasifikaci.
Obr. 1. Ukázka vstupních dat nádoru mozku pořízených ve čtyřech modalitách MR: T1, T2, FLAIR a T1ce (T1 s kontrastní látkou). V pravém sloupci je srovnání ruční anotace správného výsledku segmentace postižené části mozku a výsledku automatizované počítačové analýzy. 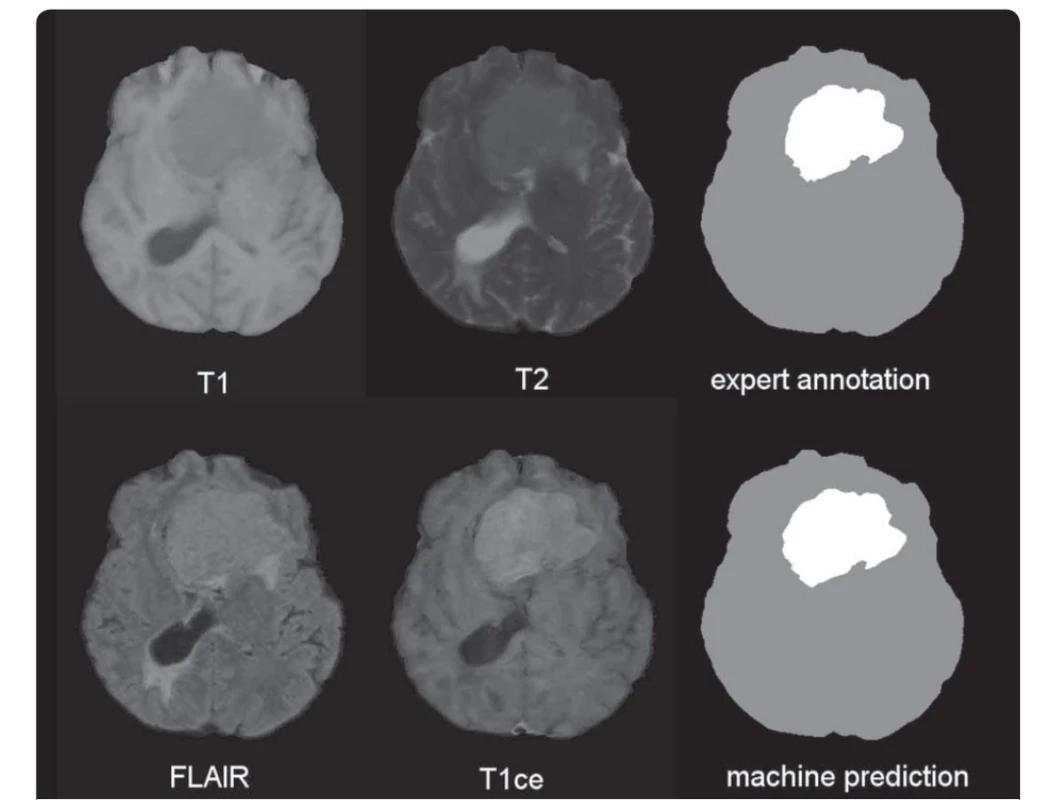
Podpořeno z programového projektu Ministerstva zdravotnictví ČR s reg. č. NU21-08-00359.
Literatura: [1] Pati S, Baid U, Edwards B, et al. Federated learning enables big data for rare cancer boundary detection. [online]. Available from: https:/ / arxiv.org/ abs/ 2204.10836arXiv.
XXXVI/ 276. AI metody v digitální patologii
Brázdil T.1, Nenutil R.2, Holub P.3, Gallo M.1, Krajňanský V.1, Horák J.1
1 Fakulta informatiky, MU Brno, 2 Oddělení onkologické patologie, MOÚ Brno, 3 Ústav výpočetní techniky, MU Brno
Cílem prezentace je představit aplikace metod strojového učení v digitální patologii. Konkrétně bude zaměřena na problém rozpoznávání nádorů v mikroskopických snímcích tkáně. V prezentaci bude představena aplikace učícího systému v rámci diagnostického procesu s využitím reálných dat pocházejících z Masarykova onkologického ústavu. Dále budou nastíněny možnosti interpretace výstupů učícího systému a představeny metody podporující vysvětlitelnost chování umělé inteligence v této oblasti. Přednášku uzavře souhrn výsledků našich experimentů s virtuálním obarvováním tkáně, jehož cílem je nahradit klasické postupy barvení (nedestruktivními) výpočetními modely.
XXXVI/ 277. Biosenzory a umělá inteligence jako nástroje pro odhalování signálních kódů řídících buněčné procesy
Sumbalová Koledová Z.1, Brezak M.1, Maška M.2
1 LF MU Brno, 2 Fakulta informatiky, MU Brno
Východiska: Signalizace ERK (kináza regulovaná extracelulárními signály) hraje zásadní roli v regulaci klíčových buněčných procesů, jako jsou proliferace, diferenciace, migrace, přežívání a smrt. Tím je signalizace ERK esenciální pro vývoj tkání a deregulace signalizace ERK vede k nádorům. Dosavadní výzkumy naznačují, že různé signální procesy jsou kódovány komplexními časoprostorovými vzory aktivity molekul ERK, a to oscilacemi rozličné amplitudy, frekvence a trvání, které teprve začínáme odhalovat. Pořád zůstává nejasné, jak signalizace ERK vykonává tolik rozličných funkcí během komplexních procesů vývoje orgánů a vzniku nádorů. Cílem našeho výzkumu je rozluštění signálního kódu ERK řídícího chování normálních a neoplastických buněk prsu. Materiál a metody: Používáme primární organoidy epitelu mléčné žlázy nesoucí ERK biosenzor EKAREV-NLS, kultivujeme je ve 2D a 3D podmínkách a zobrazujeme pomocí nejpokročilejších mikroskopovacích technik, včetně konfokální a light sheet mikroskopie, abychom odčítali vzory signálu ERK na úrovni jednotlivých buněk v odpovědi na rozličné signální vstupy. Umělou inteligenci využíváme pro analýzu obrazových dat. Výsledky: Náš výzkum odhalil rozličné signální vzory ERK buněk epitelu mléčné žlázy ve 2D a 3D podmínkách. Závěr: Naše práce přináší bezprecedentní vhled do regulace rozličného buněčného chování prostřednictvím ERK a má potenciál zlepšit cílenou terapii nádoru prsu určením specifické citlivosti nádorových buněk pacientky na specifické inhibitory ERK kaskády.
Tato práce byla umožněna díky grantové podpoře projektů MUNI/ G/ 1446/ 2018 a MUNI/ G/ 1775/ 2020 Interní grantové agentury Masarykovy univerzity. MB je držitelkou stipendia Brno PhD Talent, financovaného městem Brno.
Štítky
Dětská onkologie Chirurgie všeobecná Onkologie
Článek XXVII. UroonkologieČlánek XXX. HematoonkologieČlánek XXXIV. Biologie nádorůČlánek EditorialČlánek XI. ImunoonkologieČlánek XVI. Psychosociální péčeČlánek XVIII. Nádory prsuČlánek XX. Nádory jícnu a žaludkuČlánek XXIV. Nádory hlavy a krkuČlánek XXXVII. Covid-19
Článek vyšel v časopiseKlinická onkologie
Nejčtenější tento týden
2022 Číslo Supplementum 1- Prognostický vliv hodnoty CRP před léčbou u pacientů s metastatickým karcinomem ledviny léčených inhibitory tyrozinkinázy
- Nová šance pro pacientky s metastatickým karcinomem prsu
- I „pouhé“ doporučení znamená velkou pomoc. Nasměrujte své pacienty pod křídla Dobrých andělů
- Když se ve střevech děje něco nepatřičného...
- Perorální antivirotika jako vysoce efektivní nástroj prevence hospitalizací kvůli COVID-19 − otázky a odpovědi pro praxi
-
Všechny články tohoto čísla
- XXVII. Uroonkologie
- XXVIII. Neuroendokrinní a endokrinní nádory
- XXIX. Nádory nervového systému
- XXX. Hematoonkologie
- XXXI. Nádory dětí, adolescentů a mladých dospělých
- XXXII. Vývoj nových léčiv, farmakoekonomika, klinická farmacie v onkologii
- XXXIII. Základní, aplikovaný a klinický výzkum v onkologii
- XXXIV. Biologie nádorů
- XXXV. Integrativní přístupy v onkologii
- XXXVI. Umělá inteligence v onkologii
- XXXVII. Covid-19
- XXXVIII. Varia (ostatní, jinde nezařazené příspěvky)
- MikroRNA jako potenciální prognostické a prediktivní biomarkery u pacientů s atypickým meningeomem
- Pilotní analýza exprese PD-L1 u pacientek s ovariálním karcinomem léčených chemoterapií na bázi platiny
- Sekvenování dlouhých nekódujících RNA v exozomech u pacientů s kolorektálním karcinomem
- Využití analýzy fúzních genů metodou cíleného RNA sekvenování jako nástroje pro diagnostiku a terapeutické plánování u dětských pacientů se solidními nádory
- Sekvenování mikroRNA v mozkových metastázách jako nový diagnostický nástroj
- Retrospektivní studie případů pacientek s tuboovariálními karcinomy (n = 510) s analýzou hlavních faktorů vlivu na PFS a OS – zkušenost komplexního onkologického centra z období 2010–2019
- I. Onkologická prevence a screening
- II. Organizace a financování zdravotní péče
- III. Epidemiologie nádorů, klinické registry, zdravotnická informatika
- IV. Follow-up, sledování onkologických pacientů
- V. Vzdělávání, kvalita a bezpečnost v onkologické praxi
- VI. Diagnostické metody v onkologii a biobanking
- VII. Onkochirurgie, rekonstrukční chirurgie
- VIII. Radioterapeutické metody a radiofarmaka
- IX. Systémová protinádorová léčba
- X. Precizní medicína a personalizovaný přístup v onkologii
- Editorial
- XI. Imunoonkologie
- XII. Nežádoucí účinky protinádorové léčby a podpůrná léčba
- XIII. Paliativní péče a symptomatická léčba
- XIV. Nutriční podpora v onkologii
- XV. Ošetřovatelská péče a rehabilitace
- XVI. Psychosociální péče
- XVII. Hereditární nádorové syndromy
- XVIII. Nádory prsu
- XIX. Nádory kůže a maligní melanom
- XX. Nádory jícnu a žaludku
- XXI. Nádory tlustého střeva a konečníku
- XXII. Nádory slinivky, jater a žlučových cest
- XXIII. Nádory skeletu a sarkomy
- XXIV. Nádory hlavy a krku
- XXV. Nádory hrudníku, plic, průdušek a pleury
- XXVI. Gynekologická onkologie
- Klinická onkologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- VIII. Radioterapeutické metody a radiofarmaka
- IV. Follow-up, sledování onkologických pacientů
- XXVIII. Neuroendokrinní a endokrinní nádory
- XXII. Nádory slinivky, jater a žlučových cest
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Revma Focus: Spondyloartritidy
nový kurz
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



