-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Enterohemoragické kmeny Escherichia coli – nebezpečné novější patogeny
Enterohaemorrhagic Escherichia coli – dangerous new pathogens
Enterohaemorrhagic Escherichia coli first described in the United States in 1983, are important, worldwide spread zoonotic pathogens with a significant outbreak potential. Besides uncomplicated diarrhoea, they can cause severe complications in children and adults including haemolytic – uremic syndrome and rarely thrombotic thrombocytopenic purpura. Haemolytic – uremic syndrome is the most frequent cause of acute renal failure in children. In this article we review present knowledge about etiology, epidemiology, clinic, treatment and prevention of these infections including new data from National Reference Laboratory for Escherichia coli and shigella in Prague about the occurrence of enterohaemorrhagic Escherichia coli in the Czech Republic.
Key words:
Shiga toxin producing Escherichia coli, enterohaemorrhagic Escherichia coli, Shiga toxin, haemolytic-uremic syndrome.
Autoři: Helena Ambrožová 1; Monika Marejková 2
Působiště autorů: I. infekční klinika 2. LF UK a Nemocnice Na Bulovce, Praha 1; Národní referenční laboratoř pro Escherichia coli a shigely, Státní zdravotní ústav Praha 2
Vyšlo v časopise: Čas. Lék. čes. 2012; 151: 514-518
Kategorie: Přehledové články
Souhrn
Enterohemoragické kmeny Escherichia coli, které byly poprvé popsány v USA v roce 1983, jsou důležitými, celosvětově rozšířenými zoonotickými patogeny s významným epidemickým potenciálem. Vedle nekomplikovaného průjmu mohou vyvolávat u dětí i dospělých závažné komplikace, a to hemolyticko-uremický syndrom a vzácně trombotickou trombocytopenickou purpuru. Hemolyticko-uremický syndrom je nejčastější příčinou akutní renální insuficience v dětském věku. V článku jsou vedle etiologie, epidemiologie, klinického obrazu, komplikací, léčby a prevence zmíněna i nejnovější data z Národní referenční laboratoře pro Escherichia coli a shigely v Praze o výskytu a komplikacích této infekce v České republice.
Klíčová slova:
Shiga toxin produkující Escherichia coli, enterohemoragická Escherichia coli, Shiga toxin, hemolyticko-uremický syndrom.Úvod
Escherichia coli (E. coli) je nejen běžným komensálem lidského střeva, ale může být i vyvolavatelem střevních infekcí. Kmeny E. coli, které gastrointestinální onemocnění vyvolávají, se rozdělují do pěti skupin, z nichž některé mohou vyvolávat velmi těžké, někdy i smrtelné komplikace, nebo zanechávat dlouhodobé následky. Podle mechanismu účinku se jedná o enterotoxigenní E. coli (ETEC), které jsou nejčastější příčinou průjmu cestovatelů, enteroinvazivní E. coli (EIEC) vyvolávající onemocnění podobné bacilární úplavici, enteropatogenní E. coli (EPEC) způsobující v minulosti rozsáhlé epidemie průjmů u kojenců a v současné době méně časté sporadické průjmy u dětí, dále enteroagregativní kmeny (EAEC) způsobující průjmy cestovatelů a chronické průjmy malých dětí v rozvojových zemích (1). Poslední skupinou, která je příkladem vývoje a nebezpečnosti patogenních E. coli, jsou kmeny produkující dva typy toxinu nazývaného verotoxin, nebo Shiga toxin (Stx1 a 2) – odtud název verotoxigenní (VTEC) nebo Shiga toxin produkující E. coli (STEC) (2). STEC vyvolávající závažná lidská onemocnění, a to hemoragickou kolitidu, hemolyticko-uremický syndrom (HUS) a vzácně zřejmě i trombotickou trombocytopenickou purpuru (3), pak tvoří podskupinu známou jako enterohemoragické E. coli (EHEC) (4) (obr. 1, 2). Tyto kmeny jsou známé relativně krátce, od počátku osmdesátých let 20. století, kdy byly popsány v Kanadě, USA a v Evropě. V dalších částech světa byly diagnostikovány později (5). První případy v České republice byly zaznamenány již v roce 1988 (6). Nejzávažnější komplikací, někdy i smrtelnou, je HUS, který je vyvoláván především kmeny EHEC produkujícími Stx2 (7, 8). EHEC jsou celosvětově rozšířené a vzhledem k malé infekční dávce a vysoké nakažlivosti mají i významný epidemický potenciál. Lidská onemocnění se vyskytují jak sporadicky, tak epidemicky; ve světě byly popsány již stovky epidemií (9).
Obr. 1. EHEC v elektronovém mikroskopu (Foto: RNDr. Lenka Šípková, SZÚ-CEM) 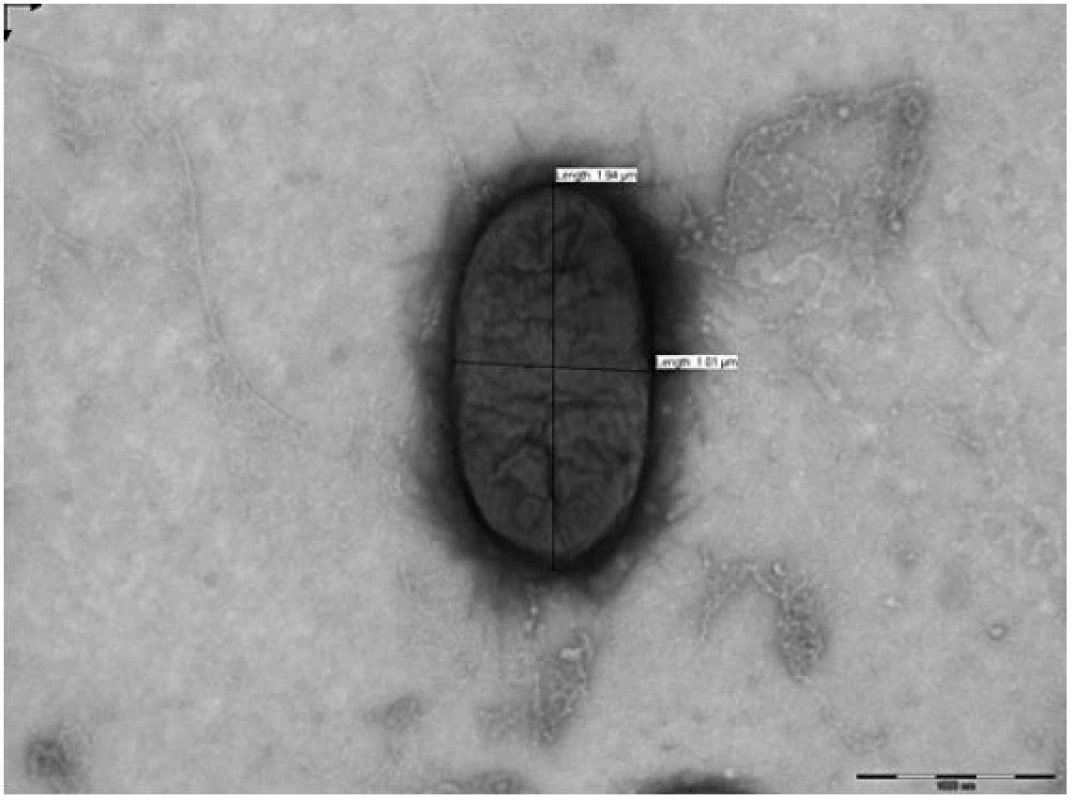
Obr. 2. Kmen <em>E. coli</em> z laboratorní sbírky NRL pro <em>E. coli</em> a shigely (SZÚ-CEM) 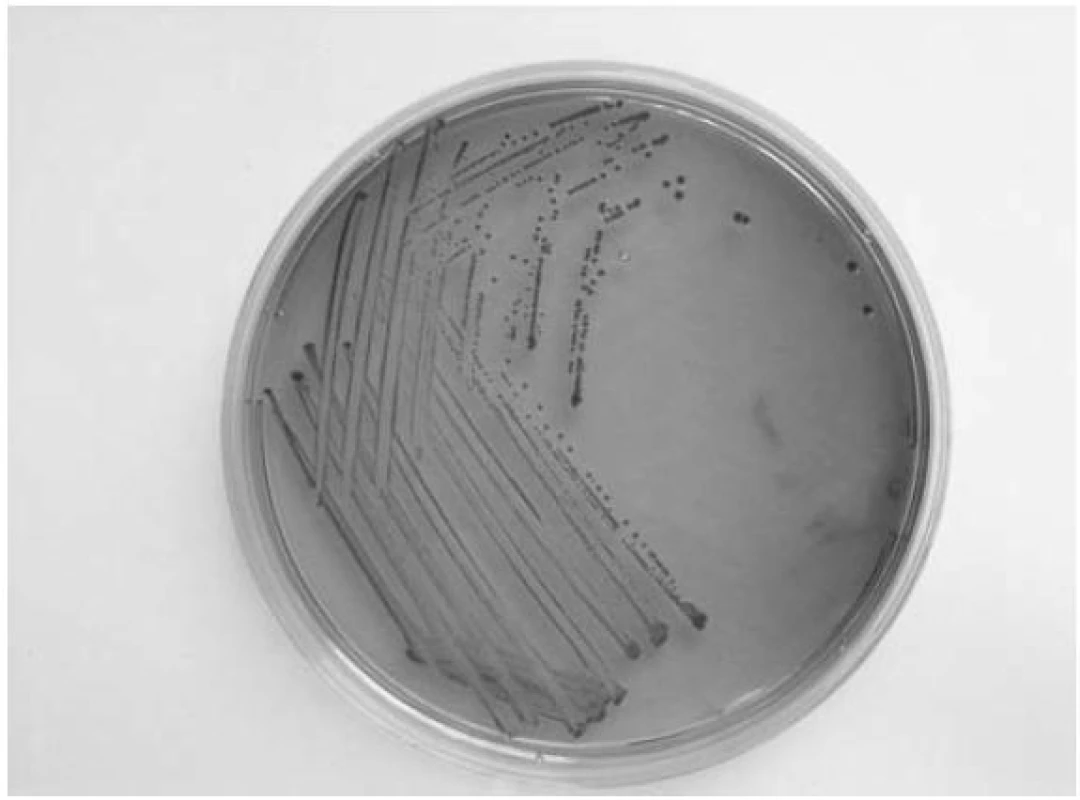
Etiologie, patogeneze
Je známa celá řada sérotypů EHEC, z nichž celosvětově nejčastěji izolovaným je O157:H7 (somatický antigen O, bičíkový antigen H) (10), který je také nejčastějším sérotypem izolovaným od pacientů s HUS (4). Kromě EHEC O157:H7 vyvolává lidská onemocnění řada non-O157:H7 sérotypů, z nichž nejčastější jsou O26:H11/H - (nepohyblivé kmeny), O103:H2/H-, O111:H8/H-, O145:H25/H28/H - a sorbitol-fermentující kmeny sérotypu O157:H - (4). V patogenezi onemocnění vyvolaných EHEC se uplatňuje několik faktorů virulence, z nichž nejdůležitější jsou již zmiňované Shiga toxiny (11). Stx1 je sekvencí nukleotidů velmi podobný Stx produkovanému Shigella dysenterie, zatímco Stx2 sdílí pouze asi 50 % podobnost s Stx1 (12). Shiga toxiny jsou produkovány EHEC kolonizujícími kolon, vstřebávají se ze střeva do krevního oběhu a jsou transportovány do cílových orgánů, kterými jsou v případě HUS primárně ledviny, eventuálně další orgány jako centrální nervový systém či pankreas (13). V cílových orgánech se toxin váže na povrchové receptory mikrovaskulárních endotelových buněk zejména v ledvinných glomerulech a mozku (14, 15) pomocí B podjednotky, zatímco enzymaticky aktivní podjednotka A vstupuje do buněk, kde inhibuje proteosyntézu (5). Toto vede k buněčné smrti různými mechanismy (nejčastěji nekróza či apoptóza). Kromě toho působí toxin na buňky bílé krevní řady (monocyty a leukocyty), kde stimuluje produkci a uvolnění zánětlivých cytokinů, které dále přispívají k patogenezi HUS a hemoragické kolitidy (14). Vedle Shiga toxinů se v patogenezi uplatňují i další faktory jako kolonizace střevní sliznice pomocí adhezinu intiminu, která rezultuje v tzv. attaching and effacing (A-E) léze a další, tzv. non-Stx toxiny (především EHEC hemolysin, cytoletální distendující toxin a serinová proteáza EspP) (2, 16–20). Výsledkem je endoteliální dysfunkce a následná mikroangiopatie (5, 14) s mikrovaskulární trombózou v různých orgánech.
Epidemiologie, přenos, výskyt
Rezervoárem kmenů EHEC je především hovězí dobytek, který vylučuje asymptomaticky bakterie stolicí. Dále jsou to především další přežvýkavci – ovce a kozy, ale vyskytují se i u prasat, koní, kuřat a krůt (10). U divokých zvířat je výskyt vzácnější, popsán byl např. u jelenů a daňků, sporadicky mohou být nosiči i synantropní hlodavci a ptáci. EHEC byly zjištěny dokonce i u obojživelníků, ryb a bezobratlých (10). Nejvyšší výskyt je u telat, která však na rozdíl od člověka neonemocní (21); z mnoha bovinních kmenů jsou pro člověka nebezpečné jen některé z nich (10). U prasat má infekce EHEC i klinický korelát v podobě edémové nemoci, projevující se u selat edémy podkoží, víček, žaludku a zejména edémem mozku, který vede k poruchám pohybu, křečím a úhynu. Vylučování u zvířat bývá obvykle jen krátkodobé, ale u tzv. „supervylučovatelů“ (supershedders), u kterých jsou počty bakterií ve střevě vysoké, trvá i déle (10, 22). Prevalence EHEC v chovech je zřejmě vyšší, než je známo, na některých farmách se mohou udržovat i měsíce až léta. Nejvyšší výskyt se objevuje v létě (8).
Přenos EHEC na člověka je fekálně – orální cestou, nejčastěji kontaminovanými potravinami, z nichž je rizikové hlavně nedostatečně tepelně upravené hovězí maso (hamburgery, tatarský biftek, kebab, sušené maso, salám) a zvěřina (5, 21), nepasterizované kravské a kozí mléko a mléčné výrobky – jogurt, máslo, sýry aj. (5, 23). V poslední době je stále častější přenos sekundárně kontaminovanou syrovou zeleninou a ovocem, a to především špenátem, hlávkovým a zelným salátem, ředkvičkovými výhonky, zeleninovými klíčky používanými do salátů aj. (24, 25), ale i jablečným džusem či melouny. K nákaze ve světě dochází i kontaminovanou vodou z veřejných i malých zdrojů pitné vody, často v souvislosti s dešti či povodněmi, které vedou k fekální kontaminaci vody, ale i z plováren či bazénů, jezer či rybníků (5, 26). Zdrojem může být i kontaminovaný led (5). Další možností je přímý kontakt s hospodářskými zvířaty, koňmi, chlévskou mrvou, hnojem ap. (10), ke kterému může dojít např. i při stále oblíbenější agroturistice (8). Podobně může dojít k nákaze i v zoo pro děti, kde je možné hladit zvířata (23); popsána byla i onemocnění laboratorních pracovníků. Protože infekční dávka je velmi nízká (jen kolem 10 bakterií), může docházet i k interpersonálnímu přenosu a vzniku sekundárních infekcí, které tvoří v epidemiích až 20 % případů (5). Vylučování EHEC u lidí je většinou krátkodobé, u nekomplikovaného onemocnění se udává průměrně 13 dnů, u případů s HUS 21 dnů (5). Známé jsou i nákazy z prostředí a asi u třetiny případů není zdroj nalezen (5).
Vysoký výskyt a nízká infekční dávka vede ve světě ke vzniku mnoha epidemií s různými zdroji, počtem případů i tíží klinického průběhu. Popsána jich byla celá řada, známé jsou americké epidemie vyvolané požitím hamburgerů z řetězců rychlého občerstvení (5) nebo syrového, omytého a ke konzumaci připraveného špenátu (27). Jedna z největších světových epidemií, která vypukla v roce 1986 v japonském městě Sakai po konzumaci ředkvičkových výhonků, postihla téměř 8000 lidí, a to především děti ve školním věku (28). Dobře známá a v odborném i laickém tisku široce komentovaná byla i loňská velká evropská epidemie, která zasáhla celkem 13 evropských států s maximem případů v Německu a Francii. Onemocnělo celkem 3842 lidí, komplikace (HUS) se vyskytly u 23 % z nich (5). Tato epidemie, jejíž příčinu se dlouho nedařilo najít (zdrojem nákazy byly mylně označeny např. španělské okurky), měla určitá specifika. Od ostatních se lišila vyšším věkem postižených lidí (zejména dospělí), vyšším počtem žen a svou závažností s vysokým počtem komplikací; HUS se vyskytl u více než 20 % případů (33). V České republice byl zaregistrován v souvislosti s touto epidemií jen jeden případ u 62leté americké turistky, která se před příjezdem do České republiky nakazila v severním Německu (30). Takto neobvykle závažný průběh epidemie mohl souviset s vlastnostmi vyvolávajícího kmene E. coli O104:H4, který pravděpodobně vznikl kombinací enteroagregativního afrického kmene E. coli O104 a EHEC, od kterého získal schopnost produkovat Stx2. Jednalo se tedy o „enteroagregativní hemoragické“ E. coli („EAHEC“), jehož zdrojem byly s největší pravděpodobností klíčky z kontaminovaných semen pískavice dovezené z Egypta, které byly použity do zeleninových salátů (31). Tuto teorii podporuje i vyšší počet postižených žen, které konzumují podobné zeleninové saláty častěji než muži. Na rozdíl od typických EHEC, epidemický kmen neobsahoval geny eae a EHEC-hlyA, kódující adherenční faktor intimin a EHEC hemolysin. Podobně, jako je tomu u klasické EHEC O157:H7, i německý epidemický kmen nesl klastr ter genů, zodpovědných za rezistenci k telluritu. EAHEC O104:H4 obsahoval klastr genů aggABCD, kódujících schopnost adherovat agregativním způsobem na střevní epitelové buňky, což je vlastnost, která je typická pro kmeny EAEC (32). Největší epidemií z kontaminované vody byla epidemie v kanadském Walkertonu z kontaminované vody ve veřejném vodovodu, která postihla 2300 lidí (26). V poslední době je sice zaznamenáván pokles počtu epidemií vyvolaných nákazou z masa, ale naopak se zvyšuje počet epidemií, jejichž zdrojem je syrová zelenina (33).
Výskyt STEC je celosvětový, incidence se liší podle kontinentů i jednotlivých států. Národní referenční laboratoř (NRL) pro E. coli a shigely při Státním zdravotním ústavu v Praze se zabývá podrobnou analýzou kmenů EHEC i následky těchto infekcí od roku 2006. Nelze však vyloučit, že následující čísla o výskytu EHEC v České republice nejsou úplně přesná, protože do Národní referenční laboratoře se obvykle dostává materiál hlavně od komplikovaných případů.
V České republice je frekvence záchytu infekcí vyvolaných EHEC nízká, v průměru asi šest případů za rok. Od roku 2006 do srpna 2012 bylo v NRL pro E. coli a shigely zaznamenáno 38 případů onemocnění vyvolaných kmeny EHEC, z toho 21 případů HUS a 17 případů nekomplikovaného průjmu či hemoragické enterokolitidy. Více než polovina EHEC izolovaných z těchto případů (celkem 23) produkovala Shiga toxin 2, čtyři kmeny byly producenty Shiga toxinu 1 a 11 kmenů bylo pozitivních na oba typy, Stx1 + Stx2.
Nejčastěji se jednalo o EHEC sérotypu O26:H11 (16 kmenů) a O157:H7 klasických, tj. sorbitol-nefermentujících (NSF) (13 kmenů). Dále to bylo po třech kmenech sorbitol-fermentujících (SF) O157:H - a séroskupiny O111, 2 izoláty O145 a jeden již výše zmíněný importovaný kmen STEC O104:H4 z velké německé epidemie z loňského roku. Se dvěma výjimkami se vždy jednalo o děti do 7 let věku, nejmladšímu bylo 10 měsíců. Bohužel i v tomto malém souboru skončily tři případy úmrtím. V červnu 2009 zemřela po velice těžkém průběhu onemocnění přes veškerou intenzivní snahu lékařů po týdenní hospitalizaci 2,5letá dívka. Původcem byla EHEC O26:H11 s produkcí Shiga toxinu 2 (34).V letošním roce zemřel jednoroční chlapec (agens EHEC SF O157:NM pozitivní na Stx2) a jednoroční dívka (agens EHEC O26:H11 pozitivní na Stx2). Ve všech případech se jednalo o velice těžký průběh HUS. Z literárních údajů je známé, že kmeny EHEC s produkcí Shiga toxinu 2 jsou obvykle původci závažnějších průběhů onemocnění (7).
V naší republice je dlouhodobá tradice průkazu EHEC. První hromadný výskyt byl popsán v roce 1989 (35), 5 let po první informaci prof. M. A. Karmaliho (Kanada) o E. coli – jako původci onemocnění HUS (36). V okrese Česká Lípa tehdy onemocnělo HUS pět dětí ve věku od 4 do 20 měsíců, jeden pacient zemřel. Původcem byla „klasická“ (tj. sorbitol nefermentující) EHEC O157:H7. Jako suspektní vehikulum byla uvedena kontaminovaná pitná voda (6,35). Další epidemie HUS byla zaznamenána roku 1995 v okresech Ústí nad Labem a Teplice. Po požití nepasterizovaného kozího mléka onemocněly čtyři děti ve věku od 10 měsíců do 3 let věku, původcem byla EHEC O157:H7 (37).
Klinický obraz, komplikace a následky
EHEC mohou vyvolat širokou škálu onemocnění a komplikací. Pro vývoj onemocnění a případný vznik komplikací jsou důležité jak faktory virulence patogena, tak faktory ze strany hostitele. U původce je důležitý především typ Shiga toxinu (kmeny produkující Stx2 vyvolávají HUS signifikantně častěji než kmeny produkující pouze Stx1) (38, 39) a přítomnost dalších non-Stx faktorů virulence, dále velikost inokula aj. Z faktorů ze strany hostitele záleží na jeho věku, imunitě, žaludeční aciditě, léčbě antibiotiky a antimotiliky aj. (7, 33). V okolí diagnostikovaného případu se často vyskytují i asymptomatičtí nosiči (16, 40), v proběhlých epidemiích tvořili 12–50 % nakažených (5). Nejčastějším klinickým obrazem je zpočátku nekomplikovaný průjem, ale později se většinou objeví příměs krve ve stolici (41). Po inkubační době 3–9 dnů dochází k rozvoji průjmu, kdy stolice jsou zpočátku bez příměsi krve, ale obvykle během 1–5 dnů, maximálně do týdne dochází k rozvoji hemoragické kolitidy, kdy krev je přítomna až v 80 % případů (15, 42) a příměs může být i masivní. Krev je přítomna zejména u infekcí vyvolaných E. coli O157:H7, u ostatních sérotypů je její výskyt menší (5). Počet stolic za den je obvykle pět a více. Na rozdíl od ostatních průjmů s přítomností krve ve stolici vyvolaných invazivními bakteriálními patogeny (shigely, kampylobaktery, yersinie, EIEC aj.) a koronaviry, pro které je typická horečka, se u infekcí vyvolaných EHEC setkáváme obvykle s afebrilním průběhem onemocnění, subfebrilie či febrilie se nevyskytují často. Zvracení není typické, pacienti obvykle udávají křečovité bolesti břicha (42).
K rozvoji komplikací dochází většinou během akutního stadia nemoci či krátce po něm (5–13 dní po začátku onemocnění), a to zejména u dětí mladších 5 let a u starších osob (14). Nejčastější je HUS, a to tzv. typický, D+ HUS („diarrhoea-associated“ HUS), který vzniká asi u 10–15 % nemocných (13, 43), v případě antibiotické léčby to však může být až v 50 % (44). Postiženy jsou více děti než dospělí, a to v poměru 90 % : 10 % (30). Histopatologickým podkladem HUS je mikroangiopatie vyvolaná působením toxinu na endotel kapilár především v glomerulech (7); onemocnění je charakterizováno triádou mikroangiopatické hemolytické anémie, trombocytopenie a renální insuficience (14). Musíme na něj myslet tehdy, jestliže je pacient správně rehydratován, a přesto laboratorně stoupá urea a kreatinin, bilirubin, LDH a v krevním obrazu se objevuje anémie, trombocytopenie a atypické deformované erytrocyty zvané schistocyty, v moči hematurie a proteinurie. V klinickém obrazu je typický bledý až subikterický kolorit kůže, vzácně i krvácivé projevy do kůže a oligurie až anurie. Pacienta s těmito příznaky a laboratorními nálezy je nutné předat na pracoviště, kde je možné provést dialýzu. Velký význam v prevenci anurie má dostatečné zavodnění pacienta izotonickými roztoky hned v počátečním stadiu HUS („volume expansion“) (45). STEC jsou ve světě hlavní příčinou postižení ledvin u dětí a velké morbidity a mortality u starších pacientů (15). HUS je u dětí hlavní příčinou akutní renální insuficience a velmi častou příčinou chronické renální insuficience (15, 29, 42, 46–48). U D+ HUS u dětí se v 90 % případů funkce ledvin upraví, 10 % (některé prameny uvádějí až 20 %) má pozdní následky či na HUS zemře (49, 50). Následkem může být postižení ledvin ve formě hypertenze, tubulopatie, reziduálních nálezů v moči. Dle literárních údajů z Kanady byla během 5 let po známé kanadské vodní epidemii zjištěna souvislost mezi hypertenzí v těhotenství a expozicí E. coli O157:H7 během této epidemie. Předpokládá se, že hypertenze vznikla jako následek subklinického postižení ledvin (51). Zejména u dospělých se může vzácně vyskytnout také trombotická trombocytopenická purpura – závažné onemocnění se řadou možných příčin obvykle neinfekčních; z infekcí není vyloučena souvislost s EHEC a HIV. Onemocnění je charakterizováno podobně jako HUS trombocytopenií, hemolytickou anémií a postižením ledvin, mohou být i horečky. Kromě toho se objevují projevy orgánové dysfunkce, a to vedle ledvin zejména CNS. Neurologické postižení se může projevit kvalitativní či kvantitativní poruchou vědomí až komatózním stavem, pacient může mít bolesti hlavy a křeče. Vzácně byly popsány i další extrarenální komplikace HUS jako pankreatitida, rhabdomyolýza, nekróza stěny tlustého střeva a myokarditida (5). Dle dalších literárních údajů mají pacienti, kteří prodělali HUS vyvolaný E. coli O157:H7, signifikantně vyšší incidenci diabetu 2. typu (40).
Diagnostika
Rutinní diagnostika STEC se provádí pomnožením a kultivací stolice na specifických a selektivních diagnostických půdách následovaných průkazem genů kódujících Shiga toxiny metodou polymerázové řetězové reakce (PCR)/RT PCR (Real Time PCR), případně fenotypovým průkazem Shiga toxinů (např. metodou reverzní pasivní latexové aglutinace či ELISA). V každém případě je třeba věnovat maximální úsilí izolaci kmene EHEC ze stolic pozitivních ve screeningových testech a fenotypové a genotypové charakterizaci izolátů (přinejmenším sérotypizaci metodou sklíčkové aglutinace nebo PCR (38), určení typu stx genu, což je důležité pro určení rizika rozvoje HUS u infikovaného jedince).
Terapie
Kauzální léčba neexistuje. Základem terapie je proto symptomatická léčba, především včasné zavodnění a úprava vnitřního prostředí (45). Vzhledem ke zvýšenému riziku vzniku HUS jsou kontraindikována antibiotika a antimotilika. V případě, že se onemocnění již rozvine, neexistuje mechanismus, který by zabránil rozvoji komplikací (5). Pokud se komplikace objeví, je nutné se zaměřit na jejich léčbu. Podávají se transfuze erytrocytů a trombocytů, u těžké renální insuficience při HUS je nutná hemodialýza, případně peritoneální dialýza, a to u 30–60 % dětí s HUS (15). U pacientů s reziduálním renálním postižením se uplatňují ACE inhibitory. V poslední době se vyvíjejí nové metody léčby zaměřené proti toxinu, které působí vazbou toxinu či jeho neutralizací – jako např. monoklonální protilátky neutralizující toxin, malé molekuly blokující Stx indukovanou cestou buněčné aktivace a apoptózy aj. (11, 15, 52).
Prevence
Vzhledem k léčbě s nejistým výsledkem a nemožnosti zabránit komplikacím při již rozvinutém onemocnění je velmi důležitá prevence. Řadě onemocnění, úmrtí, dlouhodobých následků i epidemií by bylo vzhledem k fekálně-orálnímu přenosu možné zabránit dodržováním preventivních opatření týkajících se správného zacházení s potravinami a vodou a dodržováním osobní hygieny. Právě jejich selhání vedlo v minulosti ve světě často k rozvoji velkých epidemií, např. ve Velké Británii, Kanadě či v USA (5). Je nutná zejména dostatečná tepelná úprava masa, pasterizace mléka, úprava pitné vody chlorováním stejně jako dostatečná osobní hygiena (důkladné mytí rukou) při návštěvě farem, kontaktu se zvířaty či jejich exkrety, chlévskou mrvou, hnojem, ale také u lidí kempujících v přírodě. U lidí, kteří si před jídlem neumyli ruce, je riziko nákazy EHEC v rizikovém prostředí až 9krát vyšší než u lidí dodržujících osobní hygienu (5). K šíření patogenů včetně EHEC přispívá i současná zvyšující se globalizace zdrojů potravin, jak názorně ukázala německá epidemie, a proto se EHEC stávají globální hrozbou (14). Na tomto poli je proto nutná i mezinárodní spolupráce na surveillance EHEC infekcí (53). Zatím neexistují metody, které by trvale redukovaly vylučování a nosičství STEC u zvířat. Nadějně se zatím jeví vývoj vakcín proti Stx, které by mohly vylučování u zvířat, bohužel ale většinou pouze přechodně, omezit (15).
Zkratky
- CNS – centrální nervový systém
- E. coli – Escherichia coli
- DNA – kyselina desoxyribonukleová
- HUS – hemolyticko-uremický syndrom
- D+HUS – „diarrhoea – associated“ hemolyticko – uremický syndrom
- EAEC – enteroagregativní kmen Escherichia coli
- EAHEC – enteroagregativní hemoragický kmen Escherichia coli
- EHEC – enterohemoragický kmen Eschericha coli
- EIEC – enteroinvazivní kmen Escherichia coli
- EPEC – enteropatogenní kmen Escherichia coli
- ETEC – enterotoxigenní kmen Escherichia coli
- HIV – virus lidské imunodeficience
- NRL – Národní referenční laboratoř
- NSF – sorbitol nefermentující
- PCR – polymerázová řetězová reakce
- SF – sorbitol fermentující
- STEC – Shiga toxin produkující kmen Escherichia coli
- Stx – Shiga toxin
- VTEC – verotoxin produkující Escherichia coli
Autoři děkují doc. MUDr. Martině Bielaszewské, Ph.D. z Institut für Hygiene und Konsiliarlaboratorium für Hämolytisch-Urämisches Syndrom, Universität Münster, Německo, za přečtení a kritické připomínky při přípravě tohoto rukopisu.
Adresa pro korespondenci:
MUDr. Helena Ambrožová, PhD.
I. infekční klinika 2. LF UK a Nemocnice Na Bulovce
Budínova 2, 180 00 Praha 8
fax: +420 283 840 517, e-mail: h.ambrozova@seznam.cz
Zdroje
1. Kaper JB, Nataro JP, Mobley HL. Pathogenic Escherichia coli. Nat Rev Microbiol 2004; 2(2): 123–402.
2. Bolton DJ. Verocytotoxigenic (Shiga toxin – producing) Escherichia coli: virulence factors and pathogenicity in the farm to fork paradigm. Foodborne Pathog Dis 2011; 8(3): 357–365.
3. Epidemiologic Notes and Reports. Thrombotic Thrombocytopenic Purpura Associated with Escherichia coli O157:H7-Washington. MMWR Weekly 1986; 35(34): 549–551.
4. Karch H, Tarr PI, Bielaszewska M. Enterohaemorrhagic Escherichia coli in human medicine. Int J Med Microbiol 2005; 295 : 405–418.
5. Pennington H. Escherichia coli O157. Lancet 2010; 376(23): 1428–1435.
6. Lhotová H, Bielaszewska M, Kopalová E, Štolbová M. Haemolyticko-uremický syndrom – mikrobiologické šetření. Čs. epid. microb. imunol. 1990; 39 : 13–20.
7. Friedrich AW, Bielaszewska M, Zhang WL, et al. Escherichia coli harboring Shiga toxin 2 gene variants: frequency and association with clinical symptoms. The Journal of Infectious Diseases 2002; 185 : 74–84.
8. Orth D, Würzner R. Complement in typical hemolytic uremic syndrome. Semin Tromb Hemost 2010; 366 : 620–624.
9. Money P, Kelly AF, Gould SW, et al. Cattle, weather and water: mapping Escherichia coli O157:H7 infections in humans in England and Scotland. Environ Microbiol 2010; 12(10): 2633–2644.
10. Ferens WA, Hovde CJ. Escherichia coli O157:H7: animal reservoir and sources of human infection. Foodborne Pathog Dis 2011; 8(4): 465–487.
11. Nishikawa K. Recent progress of Shiga toxin neutralizer for treatment of infections by Shiga toxin – producing Escherichia coli. Arch Immunol Ther Exp 2011; 59(4): 239–247.
12. Jackson MP, Neill RJ, O´Brien AD, et al. Nucleotide sequence analysis and comparison of the structural genes for Shiga-like toxin I and Shiga-like toxin II encoded by acteriophages from Escherichia coli 933. FEMS Microbiology letters 1987; 44(1): 109–114.
13. Tarr PI, Gordon CA, Chandler WL. Shiga toxin-producing Escherichia coli and the haemolytic uremic syndrome. Lancet 2005; 365 : 1073–1086.
14. Zoja C, Buelli S, Morici M. Shiga toxin – associated hemolytic uremic syndrome: Pathophysiology of endothelial dysfunction. Pediatr Nephrol 2010; 25(11): 2231–2240.
15. Bitzan M. Treatment options for HUS secondary to Escherichia coli O157:H7. Kidney Int Suppl 2009; 112: S2–6.
16. Karch H, Mellmann A, Bielaszewska M. Epidemiology aand pathogenesis of enterohaemorrhagic Escherichia coli. Berl Munch Tierarztl Wochenschr 2009; 122(11–12): 417–424.
17. Lim JY,Yoon J, Hovde C. A brief overview of Escherichia coli O157:H7 and its plastid O157. J Microbiol Biotechnol 2010; 20(1): 5–14.
18. Bielaszewska M, Sinha B, Kuczius T, Karch H. Cytolethal distending toxin from Shiga toxin-producing Escherichia coli O157 causes irreversible G2/M arrest, inhibition of proliferation, and death of human endothelial cells. Infect. Immun 2005; 73 : 552–562.
19. Aldick T, Bielaszewska M (shared first authorship), Zhang W, Brockmeyer J, et al. Hemolysin from Shiga toxin-negative Escherichia coli O26 strains injures microvascular endothelium. Microbes Infect 2007; 9 : 282–290.
20. Brockmeyer J, Bielaszewska M, Fruth A, et al. Subtypes of the plasmid-encoded serine protease EspP in Shiga toxin - producing Escherichia coli: Distribution, secretion, and proteolytic activity. Appl. Environ. Microbiol 2007; 73 : 6351–6359.
21. Garcia A, Fox JG, Besser TE. Zoonotic enterohemorrhagic Escherichia coli: A One Heath perspective. ILAR J 2010; 51(3): 221–232.
22. Chase-Topping M, Gally D, Low C, et al. Super – shedding and the link between human infection and livestock carriage of Esherichia coli O157. Nat Rev Microbiol 2008; 6(12): 904–912.
23. La Ragione RM, Best A, Woodward MJ, et al. Escherichia coli O157:H7 colonization in small domestic ruminants. FEMS Microbiol Rev 2009; 33(2): 394–410.
24. Berger CN, Sodha ASV, Shaw RK, et al. Fresh fruit and vegetables as vehicle for the transmission of human pathogens. Environ Microbiol 2010; 12(9): 2385–2397.
25. Franz E, van Bruggen AH. Ecology of E. coli 0157:H7 and Salmonella enterica in the primary vegetable production Chin. Crit Rev Microbiol 2008; 34(3–4): 143–161.
26. Matsell DG, White CT. An outbreak of diarrhoea – associated childhood hemolytic uremic syndrome: the Walkerton epidemic. Kidney Int Suppl 2009; 112: S35–37.
27. Wendel AM, Johnson DH, Sharapov U, et al. Multistate Outbreak of Escherichia coli O157:H7 Infection Associated with Consumption of Packaged Spinach, August September 2006: The Wisconsin Investigation. CID 2009; 48 : 1079–1086.
28. Watanabe Y, Ozasa K, Mermin JH, et al. Factory Outbreak of Escherichia coli O157:H7 Infection in Japan. Emerg Infect Dis 1999; 5(3): 424–428.
29. Malina M, Roumenina LT, Seeman T, et al. Genetics of hemolytic uremic syndromes. Presse Med 2012; 41(3): 105–114.
30. Marejková M, Roháčová H, Reisingerová M, Petráš P. An imported case of hemorrhagic colitis in Czech Republic caused by a Shiga toxin-producing Escherichia coli O104:H4 strain associated with the large German outbreak, May 2011 Folia Microbiol 2012; published on-line 19 January 2012; doi 10.1007/s12223-011-0095-0
31. Beutin L, Martin A. Outbreak of Shiga toxin-producing Escherichia coli (STEC) O104:H4 infection in Germany causes a paradigm shift with regard to human pathogenicity of STEC strains. J Food Prot 2012; 75(2): 408–418.
32. Bielaszewska M, Mellmann A, Zhang W, et al. Characterization of the Escherichia coli strain associated with an outbreak of hemolytic uremic syndrome in Germany, 2011: a microbiological study. Lancet Infect Dis 11; (9): 671–676.
33. Karmali MA. Host and pathogen determinants of verocytotoxin – producing Escherichia coli – associated hemolytic uremic syndrome. Kidney Int Suippl 2009; 112: S4–7
34. Marejková M, Zieg J, Dušek J, et al. Smrtelný případ diareapozitivního hemolyticko – uremického syndromu vyvolaného enterohemoragickým kmenem Escherichia coli O26. Zprávy epidemiologie a mikrobiologie 2009; 18(6): 212–214.
35. Bielaszewska M, Janda J. Mikrobiologické aspekty infekce kmeny E. coli produkujícími verotoxin u dětí s hemolyticko-uremickým syndromem. Epid mikrob imunol 1989; 38 : 237–244.
36. Karmali MA, Steele BT, Petric M, Lim C. Sporadic cases of Haemolytic-uraemic syndrome associated with faecal cytotoxin and cytotoxin-producing Escherichia coli in stools. Lancet 1983; 1 : 619–620.
37. Bielaszewska M, Janda J, Bláhová K, et al. Human Escherichia coli O157:H7 infection associated with the consumption of unpasteurized goat’s milk. Epidemiol Infect 1997; 119 : 299–305.
38. Friedrich AW, Bielaszewska M, Zhang WL, et al. Escherichia coli harboring Shiga toxin 2 gene variants: frequency and association with clinical symptoms. J Infect Dis 2002; 185 : 74–84.
39. Bielaszewska M., Friedrich AW, Aldick T, Schurk-Bulgrin R, Karch H. Shiga toxin activatable by intestinal mucus in Escherichia coli isolated from humans: predictor for a severe clinical outcome. Clin Infect Dis 2006; 43 : 1160–1167.
40. Suri RS, Mahon JL, Clark WF, et al. Relationship between Eschrichia coli O157:H7 and diabetes mellitus. Kidney Int Suppl 2009; 112: S44–46.
41. Müthing J, Schweppe CH, Karch H, et al. Shiga toxins, glycosphingolipid diversity, and endothelial cell injury. Tromb Haemost 2009; 101(2): 252–264.
42. Tarr PI. Shiga toxin - associated hemolytic učenic syndrome and thrombotic thrombocytopenic purpura: distinct mechanisms and pathogenesis. Kidney Int Suppl 2009; 112: S29–32.
43. Werber D, Behnke SC, Fruth A, et al. Shiga toxin-producing Escherichia coli infection in Germany: different risk factors for different age groups. Am J Epidemiol 2007; 165 : 425–434.
44. Serna A 4th, Boedeker EC. Pathogenesis and treatment of Shiga toxin – producing Escherichia coli infections. Curr Opin Gastroenterol 2008; 24(1): 38–47.
45. Ake JA, Jelacic S, Ciol MA, et al. Relative nephroprotection during Escherichia coli O157:H7 infections: Association with intravenous volume expansion. Pediatrics 2005; 115 : 673–680.
46. Palermo MS, Exeni RA, Fernández GC. Hemolytic-uremic syndrome: pathogenesis and update of interventions. Expert Rev Anti Infect Ter 2009; 7(6): 697–707.
47. Zieg J, Bláhová K, Dušek J, et al. Hemolyticko – uremický syndrom. Pediatrie pro praxi 2011; 12(2): 102–104.
48. Khanna R, Waechter L, Sargeant J, et al. Environmental prevention of human disease from verocytotoxin – producing Escherichia coli. Nephrol Dial Transplant 2008; 23(6): 1819–1822.
49. Malina M, Janda J, Seeman T. Hemolyticko-uremický syndrom – nejčastější příčina akutního renálního selhání u dětí. Komplexnost patofyziologie a nové možnosti diagnostiky a terapie atypických forem. Čsl. Pediatrie 2010; 65(11): 648–653.
50. Rosales A, Hofer J, Zimmerhackl LB, et al. Need for long - term follow-up in enterohemorrhagic Escherichia coli-associated hemolytic uremic syndrome due to late-emerging sequelae. Clin Infect Dis 2012; 54(10): 1413–1421.
51. Moist LM, Sontrop JM, Garg AX. Risk of preghnancy-related hypertension within five years of exposure to bacteria - contaminated drinking water. Kidney Int Suppl 2009; 112: S47–49.
52. Bitzan M, Schaefer F, Reymond D. Treatment of typical (enteropathic) hemolytic uremic syndrome. Semin Thromb Hemost 2010; 36(6): 594–610.
53. Wegener HC. Danish initiatives to improve the safety of meat products. Meat Sci 2010; 84(2); 273–283.
Štítky
Adiktologie Alergologie a imunologie Angiologie Audiologie a foniatrie Biochemie Dermatologie Dětská gastroenterologie Dětská chirurgie Dětská kardiologie Dětská neurologie Dětská otorinolaryngologie Dětská psychiatrie Dětská revmatologie Diabetologie Farmacie Chirurgie cévní Algeziologie Dentální hygienistka
Článek George Emil PaladeČlánek Lymphogranuloma venereum
Článek vyšel v časopiseČasopis lékařů českých
Nejčtenější tento týden
- Jak a kdy u celiakie začíná reakce na lepek? Možnou odpověď poodkryla čerstvá kanadská studie
- Doc. Jitka Fricová: V USA nasazovali fentanyl poměrně nekriticky, v Česku je situace jiná
- Trombóza portální žíly jako komplikace infekce COVID-19 – kazuistika
- Takrolimus v terapii atopické dermatitidy a analýza jeho nákladové efektivity ve srovnání s kortikosteroidní léčbou
- Sympozium věnované péči o pacienty s ALS jako odrazový můstek pro zlepšení kvality jejich života
-
Všechny články tohoto čísla
- Principy pro zacházení s lidským genetickým materiálem a genotypizační informací
- David B. Agus: KONEC NEMOCEM? (THE END OF ILLNESS)
- Enterohemoragické kmeny Escherichia coli – nebezpečné novější patogeny
- K štruktúre a funkcii lymfatických kapilár v synoviálnom kĺbe
- Lymphogranuloma venereum
- Papiledém a ischemický edém terče optiku
- Náhlé zhoršení renálních funkcí u staršího pacienta na léčbě vancomycinem pro endokarditidu
- Biomedicínský výzkum se třetími zeměmi v 7. rámcovém programu EU na roky 2007–2013
- Spolek českých lékařů v Praze
- Výročí Josefa Thomayera – 85 let od smrti, 160 let od narození
-
Krajský dermatovenerologický seminář
Rytířsko u Jihlavy, 11. září 2012 -
Etické, duchovní, právní a sociální aspekty paliativní medicíny
Rajhrad, 13. a 14. září 2012 -
Pediatrický den
Ostrava, 22. září 2012 -
35. den průmyslové neurologie
Praha, 10. října 2012 - Úpravy v Lékařském domě – sídla České lékařské společnosti J. E. Purkyně (ČLS JEP)
- Plánované akce odborných složek ČLS JEP
- Odešel zakladatel moderní laseroterapie prof. Isaac Kaplan (1919–2012)
- George Emil Palade
- Časopis lékařů českých
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Papiledém a ischemický edém terče optiku
- Enterohemoragické kmeny Escherichia coli – nebezpečné novější patogeny
- Lymphogranuloma venereum
- Principy pro zacházení s lidským genetickým materiálem a genotypizační informací
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



