-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Testování exprese claudinu 18.2 u adenokarcinomu žaludku a gastroesofageální junkce: Současný stav a výhled do blízké budoucnosti
Testing Claudin 18.2 Expression in Gastric and Gastroesophageal Junction Adenocarcinoma: Current Status and Near‑Future Outlook
Claudin 18.2 (CLDN18.2) represents one of the newest biomarkers expected to enter routine testing in the near future and expanding the spectrum of available predictive markers. It is currently a clinically relevant predictor for adenocarcinomas of the stomach and the gastroesophageal junction, although its use will likely extend also to other diagnoses. The aim of this report is to provide an overview of selected aspects of CLDN18.2 expression testing, including the choice of appropriate tissue, the issue of tumor heterogeneity, antibodies suitable for testing and their evaluation, where such testing can be performed, and the prospects for the future.
Keywords:
gastric adenocarcinoma – claudin 18.2 – adenocarcinoma of the gastroesophageal junction
Autoři: Pavel Dundr 1; Radoslav Matěj 1,2,3
Působiště autorů: Ústav patologie 1. LF UK a VFN v Praze 1; Ústav patologie 3. LF UK a Fakulní nemocnice Královské Vinohrady 2; Oddělení patologie, 3. LF UK a Fakultní Thomayerova nemocnice 3
Vyšlo v časopise: Čes.-slov. Patol., 62, 2026, No. 1, p. 13-16
Kategorie: Přehledový článek
Souhrn
Claudin 18.2 (CLDN18.2) představuje jeden z nejnovějších biomarkerů, jehož rutinní testování lze očekávat v brzké době a doplní tak spektrum dostupných prediktivních markerů. V současné době se jedná o prediktor významný pro adenokarcinomy žaludku a gastroesofageální junkce, lze však předpokládat rozšíření i na další diagnózy. Cílem stávajícího sdělení je podat přehled týkající se vybraných aspektů testování exprese CLDN18.2, zahrnujících výběr vhodné tkáně, problematiku nádorové heterogenity, protilátky použitelné pro testování a způsobu hodnocení, kde lze testovat a jaké jsou vyhlídky do budoucna.
Klíčová slova:
adenokarcinom žaludku – claudin 18.2 – adenokarcinom gastroesofageální junkce
Claudin 18.2 (CLDN18.2) představuje jeden z nejnovějších biomarkerů a terapeuticky ovlivnitelných molekulárních cílů. Na podkladě výsledků klinických studií, zejména GLOW a SPOTLIGHT, je v současné době pro adenokarcinom žaludku a gastroesofageální junkce (GEJ) na úrovni Food and Drug Administration (FDA) a European Medicines Agency (EMA) schválená léčba monoklonální protilátkou (zolbetuximab) (1, 2). Probíhají studie zaměřené i na další solidní nádory včetně karcinomu pankreatu (u kterého však recentně uveřejněné výsledky studie GLEAM vyzněly negativně) a do budoucna lze očekávat, že se léčebné možnosti a tím i nutnost testování rozšíří na další diagnózy. Indikace léčby je navázána na splnění indikačních omezení, které u karcinomu žaludku a GEJ zahrnují pacienty s neresekovatelným nebo metastazujícím adenokarcinomem, kteří nejsou vhodní pro jinou cílenou léčbu, tedy jsou HER2 negativní a nevhodní pro léčbu imunoterapií (ať už z důvodů nízkého PD-L1 CPS, nebo z jiných důvodů kontraindikujících imunoterapii). S ohledem na indikaci léčby je tedy nutné komplexní vyšetření prediktivních biomarkerů, které zahrnuje vyšetření stavu HER2, exprese PD-L1 (CPS), vyšetření mikrosatelitové instability (MSI) a vyšetření exprese CLDN18.2. V České republice probíhají jednání o úhradě léčby z prostředků zdravotního pojištění. V souvislosti s úhradou léčby je nutné řešit i prediktivní testování exprese CLDN18.2, které není aktuálně v ČR na úrovni standardních úhrad z prostředků zdravotního pojištění dostupné. Kromě aspektů týkajících se úhrad testování je také nutné řešit celou logistiku testování a další technické aspekty související s testováním.
CLAUDIN 18 (CLDN18)
CLDN18 je člen rodiny klaudinů, kterých se u člověka podle současných poznatků vyskytuje celkem 26 (3). Jedná se o protein kódovaný genem CLDN18 umístěným na dlouhém raménku chromozomu 3 (3q22.3), který má významnou roli v soudržnosti epitelových buněk v oblasti těsných vazeb („tight junction“), čímž přispívá k plnění ochranné bariérové funkce epitelu. Exprese jednotlivých typů klaudinů je tkáňově specifická, což hraje významnou roli s ohledem na jejich možné terapeutické ovlivnění, ale i na hodnocení exprese klaudinu jakožto prediktivního markeru (4). CLDN18 má dvě sestřihové varianty, CLDN18.1 a CLDN18.2 (3). První izoforma (CLDN18.1) je exprimována v normálních pneumocytech (zejména 2. typu) plicního parenchymu a plicních nádorech, oproti tomu v oblasti žaludku je exprimována zcela minimálně, nebo vůbec. Druhá izoforma (CLDN18.2) je exprimována fyziologicky v oblasti žaludečního epitelu, a to v povrchovém epitelu i ve žlázkách. Za patologických okolností může být tato izoforma exprimována nádorovými buňkami adenokarcinomu jícnu, plic, žaludku, GEJ a pankreatu (5-8). Obě izoformy mají velmi podobnou strukturu, liší se pouze v 69 aminokyselinách poblíž N konce. CLDN18.2 má dvě cytoplazmatické domény, 4 transmembránové domény, a dvě extracelulární kličky (3). Chimerická monoklonální IgG1 protilátka zolbetuximab se selektivně váže na první extracelulární kličku, která má sekvenci aminokyselin odlišnou od CLDN18.1. Monoklonální protilátka 43-14A, která je v současné době jediná vhodná pro prediktivní testování exprese CLDN18.2 však cílí na C konec CLDN18 a neumožňuje tedy rozlišení mezi CLDN18.1 a CLDN18.2. To s ohledem na stávající indikaci testování a fakt, že exprese CLDN18 je tkáňově specifická, proto nepředstavuje problém. Při rozšíření léčebné indikace i na nádory jiných oblastí by tento fakt však mohl hrát roli a pak by bylo zapotřebí použití specifické protilátky umožňující rozlišení mezi CLDN18.1 a CLDN18.2.
IMUNOHISTOCHEMICKÉ VYŠETŘENÍ EXPRESE CLDN18
Protilátky
V klinických studiích Spotlight a Glow byla použita protilátka VENTANA CLDN18 (43-14A) Assay. Tato protilátka je CE-IVDR a v říjnu 2024 byla schválena FDA jakožto „companion diagnostics“ pro účely testování exprese CLDN18 u adenokarcinomů žaludku a GEJ (1, 2). Na trhu jsou dostupné i další protilátky, ať už ve formě „ready-to-use“ nebo koncentrátů, klon 43-14 i jiné klony. Problémem v dané situaci je shoda mezi jednotlivými protilátkami, která byla do určité míry ověřována ve dvou studiích. První studie zahrnovala 27 laboratoří z 11 zemí a srovnávala tři protilátky (Ventana, LSBio a Novus) na třech platformách (Ventana, Dako, Leica) (9). Jako vysokou míru shody autoři nastavili 85 %, což je statisticky jistě přijatelné, ale pro praxi s ohledem na klinický význam diskutabilní. Zlatým standardem bylo centrální testování pomocí VENTANA CLDN18 (43-14A) kitu. Autoři studie vyhodnotili, že kromě VENTANA CLDN18 (43-14A) kitu je ještě vhodnou protilátkou LSBio při použití platformy Dako, která měla s centrálním hodnocením shodu přesahující 85 % ve všech hodnocených parametrech (senzitivita, specificita, přesnost, preciznost) a shodu mezi laboratořemi (Cohenova kappa) 0.84. Nutno zmínit, že ze dvou laboratoří, které byli s touto protilátkou hodnoceny v posledním kole NordiQC uspěla pouze jedna (https://www.nordiqc.org/downloads/assessments/206_123. pdf). Druhá práce popsala výsledky externího hodnocení kvality (EQA - QuIP GmbH) se zapojením 53 laboratoří z Německa, Rakouska a Švýcarska (10). Zúčastnilo se 53 laboratoří, které hodnotily 10 vzorků, jako úspěšné bylo bráno i chybné vyhodnocení jednoho vzorku. Všechny vzorky správně vyhodnotilo 68 % laboratoří, jednu chybu (tedy stále úspěšné) mělo 11 % laboratoří. Nejčastější bylo použití kitu VENTANA CLDN18 (43-14A), kde bylo úspěšných 27/28 laboratoří (96 %), druhá nejčastěji používaná protilátka byla ZR451 (Zeta, Zytomed), kde bylo úspěšných 5/9 laboratoří (55 %). Jako nejčastější příčinu neúspěchu autoři udávají falešnou negativitu, což dle nich byl nejčastější problém u ZR451 (Zeta, Zytomed) a EPR19202 (Abcam) (použilo 5 laboratoří, neuspěla žádná). Podle posledního kola NordiQC hodnotícího claudin bylo z laboratoří používajících certifikovaný kit VENTANA CLDN18 (43-14A) úspěšných 100 % (9/9), ready - -to-use protilátky 94 % (65/75) a koncentráty 46 % (6/13). U koncentrátů uspěly zejména klony protilátek 43-14 (https://www. nordiqc.org/downloads/assessments/206_123.pdf).
Doporučení v České republice
V roce 2025 proběhlo několik setkání zástupců Společnosti českých patologů a České onkologické společnosti ČLS JEP, jehož cílem bylo stanovit pravidla budoucího testování. Jako povinné bylo stanoveno používání certifikovaného kitu VENTANA CLDN18 (43-14A). Důvodem jsou sporné výsledky srovnávacích studií a zejména výsledky EHK, kdy se jako jednoznačně spolehlivé ukázaly být pouze certifikované kity. Dalším důvodem je fakt, že aktuálně není kromě kitu VENTANA CLDN18 (43-14A) dostupná žádná jiná protilátka, která by plnila požadovaná kritéria týkající se certifikace, tedy byla CE-IVDR, nebo alespoň CE-IVD. Jediná protilátka, která kromě protilátky kitu firmy Ventana, měla ještě v roce 2023 IVD, byla ZR451 (Zeta, Zytomed). To však už v roce 2025 neplatí, protože s „nástupem“ IVDR došlo ze strany firmy k přesunu protilátky do kategorie research-use-only (RUO). To je, a hlavně bude zásadní problém, se kterým se potýkáme v souvislosti s implementací (šíleného) konceptu IVDR čím dále častěji.
Způsob hodnocení imunohistochemické exprese
Způsob hodnocení musí vycházet z konkrétní indikace. V současné době je hodnocení definováno pro účely predikce odpovědi na léčbu zolbetuximabem, lze však předpokládat, že pro jiné léky mohou být v budoucnu kritéria pozitivity odlišná. Stejně tak je nutné zdůraznit, že literární data jsou s ohledem na výskyt exprese CLDN18.2 u různých nádorů zatížena odlišným způsobem skórování a bez podrobnější analýzy nejsou studie často vzájemně srovnatelné.
Pro účely léčby zolbetuximabem je hodnocení exprese CLDN18.2 binární. Jako pozitivní se bere středně a/nebo silně intenzivní membránová pozitivita (skóre 2+ a 3+) v ≥ 75 % nádorových buněk. Exprese může být kompletní, nebo pouze částečná (apikální, basolaterální, laterální, luminální). Cytoplazmatická exprese může být přítomna, pro účely hodnocení se však nebere jako pozitivní, hodnotí se výlučně pozitivita membránová. Příklady pozitivního a negativního výsledku jsou uvedeny na obrázku 1. Hodnotí se pouze vitální nádorové buňky, buňky v oblasti nekrózy by měly být z hodnocení vyloučeny. Celkově by mělo být jako minimum přítomno alespoň 50 vitálních nádorových buněk, jinak se test neprovádí. V normálním žaludečním epitelu je přítomna silná exprese, což může být použito jako vnitřní kontrola (obrázek 1A). Pokud je přítomna sliznice s intestinální metaplazií, v té se může vyskytovat celé spektrum intenzity exprese CLDN18.2 od negativní po silně pozitivní, což může být opět použito jako interní kontrola.
Obr. 1. Imunohistochemická exprese claudinu 18.2 (certifikovaný kit Ventana). Silně intenzivní pozitivita v epitelu nenádorové sliznice žaludku (100x) (A). Fokální pozitivita v adenokarcinomu žaludku - s ohledem na interpretační kritéria je nález negativní (100x) (B). Středně a silně intenzivní pozitivita v metastáze adenokarcinomu žaludku (hodnoceno jako pozitivní) (100x) (C). Difúzní silně intenzivní pozitivita žaludečního adenokarcinomu (100x) (D). 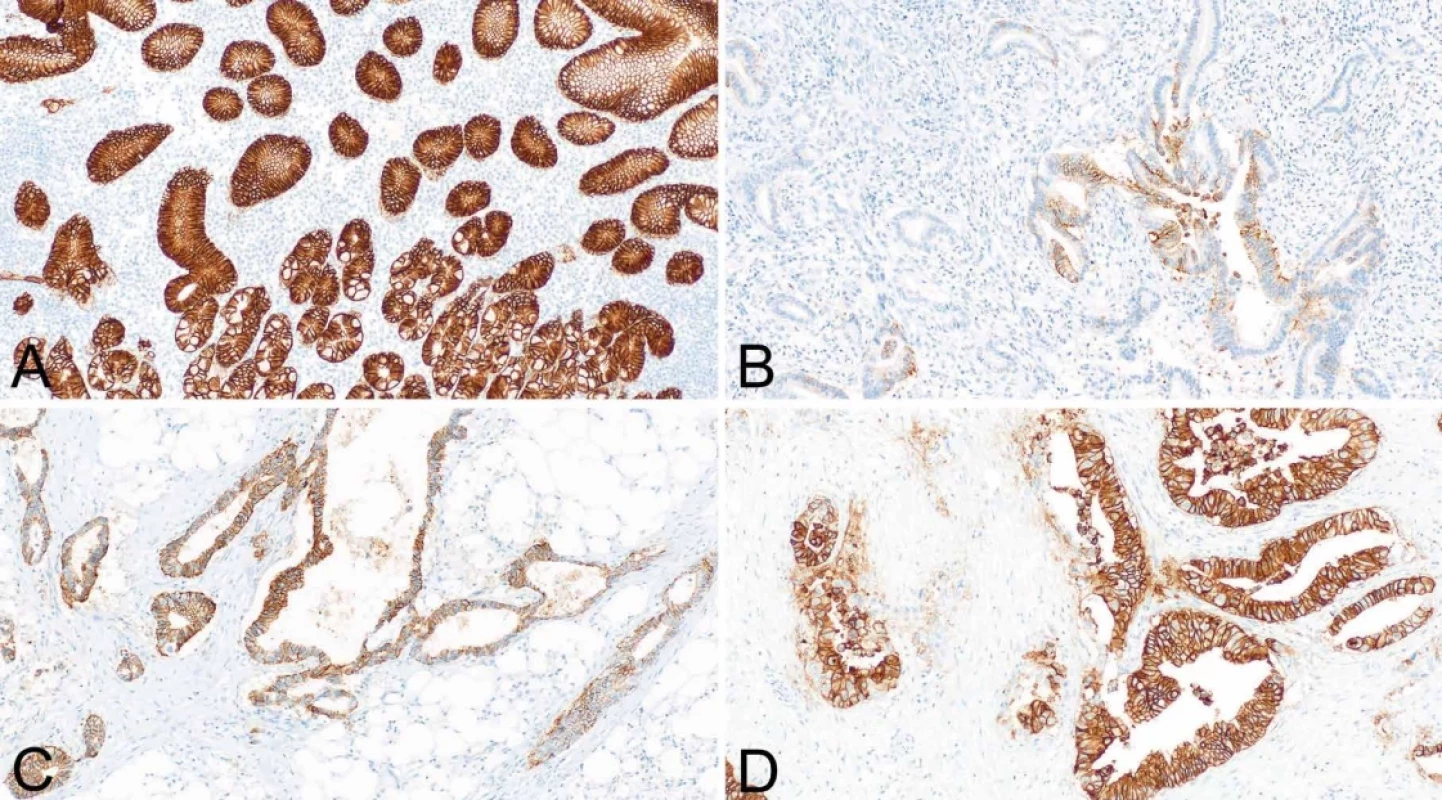
Rozsah exprese claudinu 18
Exprese claudinu 18.2 se liší mezi jednotlivými diagnózami. U karcinomu žaludku se podle literárních údajů při použití uvedeného způsobu skórování, tedy střední a/nebo silná pozitivita u ≥ 75 % nádorových buněk, pohybuje v rozmezí asi 30-45 % nádorů s tím, že vyšší exprese je u adenokarcinomů difúzního typu a HER2+ (11). Zajímavé je, že podle amerických autorů dosahuje pozitivita claudinu 18.2 52 % ve skupině tzv. „triple negative“ (tedy HER-2 negativní, PD-L1 negativní a MMR proficientní) (12). I přes poměrně limitovaná literární data se ukazuje, že exprese CLDN18 je heterogenní a jsou poměrně výrazné rozdíly nejen mezi hodnocením z biopsie a resekátu, ale i mezi primárním nádorem a metastázou. V jedné studii zaměřené na srovnání primárních a metastatických nádorů (102 případů) byla celková neshoda 16,7 % (13). V této studii bylo pozitivních 32,4 % primárních nádorů a 27,5 % metastáz. Změna výsledku u primárního nádoru ve srovnání s metastázou byla u 10,8 % z pozitivního na negativní, a u 5,9 % z negativního na pozitivní. Jiná studie analyzovala 166 případů (u 135 s dostupnou metastázou) (14). V této studii byla pozitivita u primárních nádorů 47 % a u metastáz 40 %. Celková neshoda byla 25,2 %, z toho byla u 10,3 % změna z pozitivního primárního nádoru na negativní v metastáze a u 14,9 % z negativního na pozitivní v metastáze. Třetí studie na 84 případech (s pouze peritoneálními metastázami) ukázala nižší procento pozitivity u primárních nádorů (28,6 %) i metastáz (20,2 %), jinak však byly výsledky podobné s celkovou
diskrepancí 25 % a změnou z pozitivního výsledku na negativní u 16,7 % případů a z negativního na pozitivní u 8,3 % případů (15). V této studii byla hodnocena i neshoda mezi biopsií a resekátem, která byla celkově 18,7 % případů. Na druhou stranu studie autorů z Bostonu udává relativně nízkou intratumorózní heterogenitu exprese claudinu 18.2, to zejména ve skupinách hodnocených jako negativní (méně jak 10 % pozitivních elementů) a difúzně pozitivních (více jak 90 % pozitivních elementů). Ve skupině nádorů hodnocených jako pozitivní (tedy více jak 75 %) jevilo homogenní pozitivitu 84 % hodnocených nádorů. I tak je však zřejmé, že heterogenní exprese může hrát roli při hodnocení pozitivity claudinu 18.2 v nádorových vzorcích roli.
Z dalších diagnóz je častá exprese udávána u karcinomu pankreatu (asi 30 % případů), to zejména u lépe diferencovaných duktálních adenokarcinomů (16). U cholangiocelulárního karcinomu je exprese nižší, liší se do určité míry u intrahepatálního, hilového a distálního typu, data jsou však poměrně limitovaná a celkově je u tohoto typu nádoru exprese asi u 13 % případů (17, 18).
Kde testovat
Aktuální testování exprese CLDN18 probíhá mimo úhrady z prostředků zdravotního pojištění pouze v rámci programu podporovaného společností Astellas Pharma Inc. na vybraných pracovištích. Cílem je však zavedení standardního testování hrazeného plátci, které by mělo být realizováno v souvislosti se schválením úhrady léčby z prostředků zdravotního pojištění. V tomto ohledu probíhají na úrovni SČP jednání s plátci, jejichž cílem je tvorba nového kódu zařazeného do seznamu zdravotních výkonů. Testování by pak jako všechna ostatní prediktivní testování probíhalo na pracovištích patologie zařazených do sítě referenčních laboratoří pro prediktivní diagnostiku. Nutno zdůraznit, že očekávané počty testů v celé ČR nebudou nijak vysoké a každá z referenčních laboratoří si pak musí vyhodnotit, jestli testování CLDN18.2 bude provádět.
ZÁVĚR
Exprese claudinu 18 představuje další z prediktivních markerů, který rozšiřuje spektrum prediktivního testování a doplňuje aktuální možnosti prediktivního testování u karcinomu žaludku a GEJ. Pro klinickou indikaci je zásadní interpretace v kontextu dalších prediktorů u karcinomů žaludku zahrnujících expresi HER2, PD-L1 a vyšetření MSI. V tuto chvíli je testování dostupné pouze ve vybraných pracovištích a není hrazeno z prostředků zdravotního pojištění. Až bude schválena úhrada léčby, bude testování možné ve všech laboratořích ze sítě referenčních laboratoří pro prediktivní diagnostiku, které toto vyšetření s ohledem na očekávaný spíše limitovaný počet vzorků testovaných v ČR budou chtít provádět. I přes nádorovou heterogenitu a určitý stupeň neshody mezi primárním nádorem testovaných z biopsie, nálezem v resekátu a v případné metastáze, nelze preferovat vyšetření konkrétního bioptického materiálu před jiným, spíše jde o to, jaký materiál bude pro testování vůbec dostupný. Možné je testování z recentní biopsie, v případě její nedostupnosti však i z biopsie archivní.
PODĚKOVÁNÍ
Práce byla podpořena MZČR, projekt VFN-RVO 64165
PROHLÁŠENÍ
Autor práce prohlašuje, že v souvislosti s tématem, vznikem a publikací tohoto článku není ve střetu zájmů a vznik ani publikace článku nebyly podpořeny žádnou farmaceutickou firmou. Toto prohlášení se týká i všech spoluautorů.
Zdroje
1. Shitara K, Lordick F, Bang YJ, et al. Zolbetuximab plus mfolfox6 in patients with cldn18. 2-positive, her2-negative, untreated, locally advanced unresectable or metastatic gastric or gastro-oesophageal junction adenocarcinoma (spotlight): A multicentre, randomised, double-blind, phase 3 trial. Lancet 2023; 401(10389): 1655-1668.
2. Shah MA, Shitara K, Ajani JA, et al. Zolbetuximab plus capox in cldn18.2-positive gastric or gastroesophageal junction adenocarcinoma: The randomized, phase 3 glow trial. Nat Med 2023; 29(8): 2133-2141.
3. Nakayama I, Qi C, Chen Y, et al. Claudin 18.2 as a novel therapeutic target. Nat Rev Clin Oncol 2024; 21(5): 354-369.
4. Hashimoto T, Iida N, Nakamura Y, et al. Landscape analysis of cldn18 expression and isoform distribution in solid tumors: Insights from monstar-screen-2 study. Cancer Sci 2025; 116(8): 2218-2231.
5. Angerilli V, Sacchi D, Rizzato M, et al. Claudin 18.2: A promising actionable target in biliary tract cancers. ESMO Open 2025; 10(5): 105049.
6. Arseneau RJ, Kempster E, Bekkers C, et al. Claudin 18 (43-14a clone) expression in pancreatic ductal adenocarcinoma: Assessment of a potential clinical biomarker for zolbetuximab therapy. Transl Oncol 2025; 55(102362.
7. Coati I, Lotz G, Fanelli GN, et al. Claudin-18 expression in oesophagogastric adenocarcinomas: A tissue microarray study of 523 molecularly profiled cases. Br J Cancer 2019; 121(3): 257-263.
8. Kim M, Woo HY, Kim J, Seo AN. Claudin 18.2 expression in gastric tumors and other tumor types with gastric epithelium-like differentiation. In Vivo 2025; 39(3): 1540-1553.
9. Jasani B, Taniere P, Schildhaus HU, et al. Global ring study to investigate the comparability of total assay performance of commercial claudin 18 antibodies for evaluation in gastric cancer. Lab Invest 2024; 104(1): 100284.
10. Rocken C, Hohn AK, Neumann J, et al. Concordance of laboratory assays for claudin 18.2 in gastric cancer tissue samples: Independent proficiency testing and a descriptive non - -interventional study. Virchows Arch 2025; 487(5):1117-1125.
11. Baek JH, Park DJ, Kim GY, et al. Clinical implications of claudin18.2 expression in patients with gastric cancer. Anticancer Res 2019; 39(12): 6973-6979.
12. Liu BL, Cleary JM, Shi J, Hornick JL, Zhao L. Claudin 18.2 and other therapeutic biomarkers in gastric and gastroesophageal junction adenocarcinomas. Am J Surg Pathol 2025; 49(12): 1233-1244.
13. Son SM, Woo CG, Lee OJ, et al. Discordance in claudin 18.2 expression between primary and metastatic lesions in patients with gastric cancer. J Gastric Cancer 2025; 25(2): 303 - 317.
14. Choi E, Shin J, Ryu MH, Kim HD, Park YS. Heterogeneity of claudin 18.2 expression in metastatic gastric cancer. Sci Rep 2024; 14(1): 17648.
15. Ogawa H, Abe H, Yagi K, Seto Y, Ushiku T. Claudin-18 status and its correlation with her2 and pd-l1 expression in gastric cancer with peritoneal dissemination. Gastric Cancer 2024; 27(4): 802-810.
16. Luchini C, Matkowskyj KA, Kuwata T, et al. Claudin-18.2 immunohistochemical evaluation in pancreatic cancer specimens: Review and recommendations for routine testing and scoring. Virchows Arch 2025; 487(3): 487 - 499.
17. Desai N, Ko HM, Lee M, et al. Claudin 18 immunohistochemistry in cholangiocarcinoma. J Gastrointest Oncol 2025; 16(2): 671 - 678.
18. Kinzler MN, Gretser S, Schulze F, et al. Expression of claudin-18.2 in cholangiocarcinoma: A comprehensive immunohistochemical analysis from a german tertiary centre. Histopathology 2025; 86(4): 640-646.
Štítky
Patologie Soudní lékařství Toxikologie
Článek vyšel v časopiseČesko-slovenská patologie

2026 Číslo 1-
Všechny články tohoto čísla
- Testování exprese claudinu 18.2 u adenokarcinomu žaludku a gastroesofageální junkce: Současný stav a výhled do blízké budoucnosti
- Castlemanova choroba – jedno jméno, mnoho tváří
- Lymfatická tkáň v souvislostech: od nenápadných změn k zásadním diagnózám
- Přednosti a limitace nového stagingového systému karcinomu endometria FIGO 2023 z pohledu klinika a patologa
- Od archeologické brigády k americké rezidentuře: proč je patologie „nejlepší obor medicíny“
- Cílené profilování genové exprese jako nástroj pro diagnostické určení buněčného subtypu a prognostickou stratifikaci u difuzního velkobuněčného B-lymfomu
- Castleman-like lymfadenopatie u pacienta se smíšenou chorobou pojiva: kazuistika a přehled literatury
- EBV-asociovaná plazmocelulární varianta Castlemanovy choroby: více než deset let trvající diagnostická odysea – kazuistika pacienta
- MONITOR, aneb nemělo by vám uniknout, že…
- Česko-slovenská patologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Castlemanova choroba – jedno jméno, mnoho tváří
- Testování exprese claudinu 18.2 u adenokarcinomu žaludku a gastroesofageální junkce: Současný stav a výhled do blízké budoucnosti
- Přednosti a limitace nového stagingového systému karcinomu endometria FIGO 2023 z pohledu klinika a patologa
- Cílené profilování genové exprese jako nástroj pro diagnostické určení buněčného subtypu a prognostickou stratifikaci u difuzního velkobuněčného B-lymfomu
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Revma Focus: Spondyloartritidy
nový kurz
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Autoři: prof. MUDr. Pavel Horák, CSc., doc. MUDr. Ludmila Brunerová, Ph.D., doc. MUDr. Václav Vyskočil, Ph.D., prim. MUDr. Richard Pikner, Ph.D., MUDr. Olga Růžičková, MUDr. Jan Rosa, prof. MUDr. Vladimír Palička, CSc., Dr.h.c.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



