-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Cílené profilování genové exprese jako nástroj pro diagnostické určení buněčného subtypu a prognostickou stratifikaci u difuzního velkobuněčného B-lymfomu
Targeted gene expression profiling as a tool for diagnostic cell-of-origin determination and prognostic stratification in diffuse large B-cell lymphoma
Classification of diffuse large B-cell lymphoma (DLBCL) according to cell-of-origin (COO) distinguishes two main biological subtypes: activated B-cell-like (ABC) and germinal center B-cell-like (GCB). Although this distinction reflects different pathogenetic mechanisms, its prognostic impact diminishes in the context of evolving therapeutic strategies. Molecular subtyping of DLBCL, which is based on the spectrum of affected genes and aims to personalize treatment approaches, is currently gaining importance. In the study, we applied targeted gene expression profiling (GEP) using a custom Lympho-qPCR panel, enabling rapid and practically applicable ABC/GCB classification together with risk stratification of patients. RNA isolated from a cohort of 89 DLBCL tissue samples was analyzed using three GEP-based classification models. Model A compared the expression profile with immunohistochemical (IHC) COO determination and showed the expected lower correlation (62 %). Model B employed the expression scores of selected genes to predict COO regardless of IHC classification. Model C was developed as a new IHC-independent prognostic tool allowing patient stratification based on expected survival. Patients identified as high-risk by Model C had significantly worse outcomes, regardless of existing clinical prognostic indicators. In patients with early progression, parallel DNA sequencing analysis (integrative LYNX panel) confirmed complex chromosomal aberrations and defects in BCL2, TP53 and CDKN2A/B. Our results demonstrate that targeted GEP testing represents a robust, rapid, and clinically applicable method for COO determination and risk stratification in DLBCL patients. In the near future, the predictive value of ABC/GCB classification is expected to increase in relation to novel targeted therapeutic regimens. Integration of transcriptomic and genetic data will be essential for independent and individualized risk assessment in the molecular diagnostics of DLBCL.
Keywords:
gene expression profiling – DLBCL – ABC/GCB subtype – prognostic stratification – molecular diagnostics
Autoři: Veronika Navrkalová 1,2,3; Andrea Marečková 1; Lenka Radová 2,3; Klára Činátlová 1; Václav Kubeš 4; David Šálek 1; Michael Doubek 1,2; Šárka Pospíšilová 1,2,3; Leoš Křen 4; Jana Kotašková 1,3
Působiště autorů: Interní hematologická a onkologická klinika, Fakultní nemocnice Brno a Lékařská fakulta Masarykovy univerzity, Brno 1; Centrum molekulární medicíny, Středoevropský technologický institut, Masarykova univerzita, Brno 2; Ústav lékařské genetiky a genomiky, Lékařská fakulta Masarykovy univerzity a Fakultní nemocnice Brno 3; Oddělení patologie, Fakultní nemocnice Brno 4
Vyšlo v časopise: Čes.-slov. Patol., 62, 2026, No. 1, p. 43-49
Kategorie: Původní práce
Souhrn
Klasifikace difuzního velkobuněčného B-lymfomu (DLBCL) podle buněčného původu (cell-of-origin, COO) rozlišuje dva základní biologické podtypy, ABC (activated B-cell-like) a GCB (germinal center B-cell-like). Ačkoli toto rozdělení odráží odlišnou patogenezi, jeho prognostický význam přestává být v kontextu vyvíjejících se léčebných postupů relevantní. Nově nabývá na významu molekulární subtypizace DLBCL, která vychází ze spektra postižených genů a cílí na personalizaci léčebného přístupu. V této studii jsme použili cílené profilování genové exprese (GEP) pomocí námi sestaveného panelu Lympho-qPCR, který umožňuje rychlou a v praxi využitelnou ABC/GCB klasifikaci a současně stratifikaci pacientů podle rizika progrese. RNA izolovaná z 89 vzorků tkání od pacientů s DLBCL sloužila k vytvoření tří klasifikačních modelů. Model A porovnával expresní profil s imunohistochemickým (IHC) stanovením COO a ukázal očekávanou nižší korelaci (62 %). Model B využívá skórování exprese vybraných genů k určení COO bez ohledu na IHC klasifikaci. Model C byl vyvinut jako nový, na IHC nezávislý prognostický nástroj umožňující stratifikaci pacientů podle očekávaného přežití. Významně horší prognózu měli pacienti identifikovaní jako vysoce rizikoví dle modelu C, bez ohledu na stávající klinické prognostické ukazatele. U pacientů s časnou progresí potvrdila paralelní sekvenační analýza DNA (integrativní panel LYNX) přítomnost komplexních chromozomových změn a defektů v genech BCL2, TP53 a CDKN2A/B. Naše výsledky ukazují, že cílený GEP test představuje robustní, rychlý a tedy rutinně využitelný nástroj pro určení COO subtypu a rizikovou stratifikaci DLBCL pacientů. V blízké budoucnosti lze očekávat narůstající prediktivní význam ABC/GCB typizace v souvislosti s novými cílenými terapeutickými režimy. Integrace transkriptomických a genetických dat bude klíčová pro nezávislé a individuální posouzení rizika pacientů v molekulární diagnostice DLBCL.
Klíčová slova:
DLBCL – ABC/GCB subtyp – profilování genové exprese – prognostická stratifikace – molekulární diagnostika
Pacienti s difuzním velkobuněčným B-lymfomem (DLBCL) obvykle vyžadují rychlé zahájení léčby, což omezuje možnosti podrobnější rizikové stratifikace pomocí pokročilých a časově náročných molekulárních metod. V důsledku toho je většina pacientů zpočátku léčena standardním režimem R-CHOP, přestože DLBCL představuje značně geneticky, fenotypově a klinicky heterogenní onemocnění. Přibližně u třetiny nemocných dochází i přes tuto léčbu k časné progresi nebo refrakteritě onemocnění (1,2). Klinicky významného zlepšení výsledků bylo v posledních dvaceti letech dosaženo pouze u režimu Pola-R-CHP (3). Pro zavedení nových, personalizovaných léčebných přístupů je proto nezbytná rychlá a spolehlivá identifikace rizikových pacientů, kterou dnes umožňují moderní a vysoce výkonné technologie molekulární biologie.
Profilování genové exprese (GEP) pomocí čipových technologií bylo první metodou, která rozdělila DLBCL do dvou kategorií podle buněčného původu (COO): podtyp podobný aktivovaným B-buňkám (ABC) a podtyp podobný B-buňkám germinálního centra (GCB) (4–6). Nedávno byla navíc popsána podskupina tzv. „dark-zone“ GCB lymfomů, která je asociována s agresivnějším průběhem (7,8). Protože původní čipová analýza nebyla vhodná pro rutinní praxi, byl pro diagnostické účely zaveden imunohistochemický (IHC) algoritmus dle Hansové (9), který využívá tři proteinové markery (CD10, BCL6, MUM1) k rozlišení ABC a GCB subtypu. Tento přístup však naráží na omezenou přesnost, reprodukovatelnost a obtížnou identifikaci ABC případů. Novější technologie, například platforma NanoString, nabízí spolehlivější určení COO pomocí cíleného GEP. Scott a kol. (10) navrhli panel 20 genů (Lymph2X assay), který byl úspěšně validován v prospektivních klinických kohortách (11). Nicméně jeho širší implementaci brání vysoké náklady a omezená dostupnost.
Metody založené na sekvenování nové generace (NGS) odkryly hlubší molekulární heterogenitu DLBCL nad rámec dvou buněčných subtypů a vedly k definici několika genetických podtypů s odlišnou prognózou a odpovědí na imunochemoterapii (12–14). Algoritmus LymphGen umožňuje jejich klasifikaci, avšak vyžaduje komplexní molekulární data zahrnující mutace, translokace BCL2/BCL6 i změny počtu chromozomových kopií, což výrazně omezuje praktické využití tohoto přístupu v diagnostice a managementu DLBCL.
V současné době se pozornost soustřeďuje na integraci transkriptomických a genetických dat pro predikci efektivity léčby první linie (15,16). Například přidání Ibrutinibu, inhibitoru BTK, k režimu R-CHOP prokázalo účinnost u ABC-DLBCL a genetických podtypů MCD a N1 (17). Slibné výsledky vykazují cílené léky také u relabovaných či refrakterních pacientů (18). I přes snahy vyvinout zjednodušené algoritmy pomocí cílené analýzy (19,20) zůstává široké využití molekulárních markerů v rutinní diagnostice a multicentrických studiích omezené, zejména kvůli nákladům, dostupnosti technologií a absenci standardizace.
Cílem této práce bylo vyvinout efektivní a zejména rychlý nástroj pro identifikaci vysoce rizikových pacientů s DLBCL na základě cíleného profilování genové exprese, který lze snadno začlenit do běžných diagnostických pracovních postupů molekulárně-patologických laboratoří.
MATERIÁL A METODY
Soubor pacientů a vzorky
Do studie bylo zařazeno 89 diagnostických vzorků pacientů s lymfomem (88 DLBCL a jeden HGBL) diagnostikovaných a léčených v letech 2006-2023 na Interní hematologické a onkologické klinice Fakultní nemocnice Brno. Všichni pacienti podepsali informovaný souhlas, který je v souladu s Helsinskou deklarací a byl schválen etickou komisí (číslo 23-090621-EK).
Vzorky byly vybrány retrospektivně podle dostupnosti čerstvě zmražené tkáně z diagnostických biopsií. Značný počet pacientů byl ze studie vyloučen z důvodu dostupnosti pouze rutinní fixované tkáně (FFPE bloky), která obecně není vhodná pro GEP kvůli nízké kvalitě RNA. Přítomnost lymfomových buněk byla ověřena hematopatologem. U 65 pacientů bylo provedeno IHC určení COO (z diagnostických FFPE řezů), které sloužilo pro sestavení tréninkové (26 ABC, 19 GCB) a validační kohorty (10 ABC, 10 GCB). Zbývajících 24 případů tvořilo experimentální soubor. Klinické a biologické údaje shrnuje Tabulka č.1.
Tab. 1. Základní klinické a laboratorní parametry souboru DLBCL pacientů (n=89). 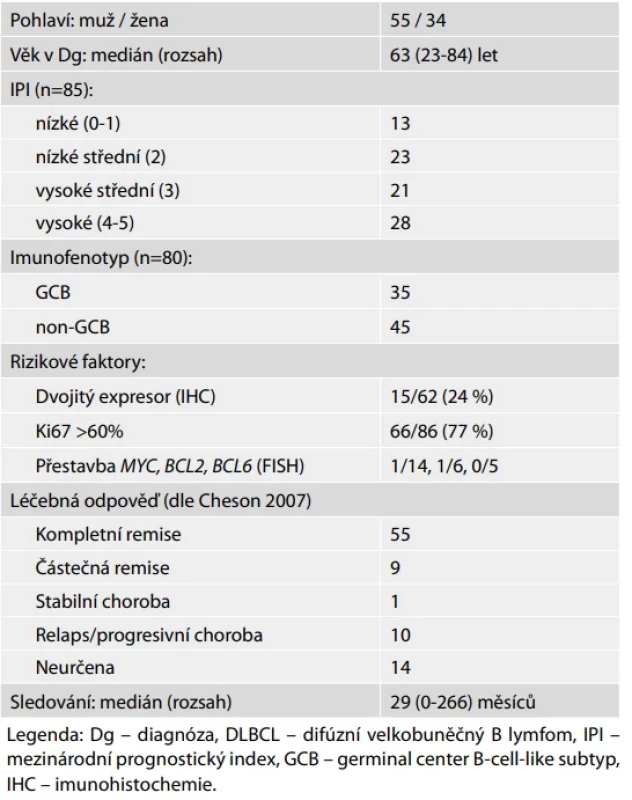
Celková RNA byla izolována z čerstvě zmražené tkáně (mirVana™ RNA Isolation Kit , Thermo Fisher Scientific) a její integrita a množství byly posouzeny pomocí systému TapeStation (Agilent); k další analýze genové exprese byly použity pouze vzorky s dostatečnou kvalitou RNA.
Návrh a provedení cíleného testu Lympho-qPCR
Pro rutinně využitelnou analýzu genové exprese byl vyvinut test Lympho-qPCR, založený na cíleném hodnocení exprese vybraných genů pomocí qPCR. Výběr cílových genů byl založen na důkladném prozkoumání zásadních studií definující podtypy ABC/GCB (4,6,10,21–26). Panel zahrnoval 28 genů spojených s COO podtypy a 3 referenční (housekeeping) geny. Primery a sondy byly syntetizovány společností Generi Biotech (Česká republika) a lyofilizovány v tripletech do 96jamkových destiček (obr. 1A), z nichž každá byla určena pro jeden vzorek. Jeden µg RNA byl pomocí reverzní transkripce přepsán do cDNA, která byla kvantifikována pomocí přístroje qTower³ (Analytik Jena). Relativní exprese genů byla stanovena metodou 2^-ΔCt, normalizovaná buď na každý jednotlivý housekeeping gen, nebo na jejich geometrický průměr. Tento přístup umožnil robustní a reprodukovatelnou kvantifikaci genové exprese v celé kohortě.
Obr. 1. Souhrn pracovního postupu studie. Vybrané geny pro Lympho-qPCR test (A) a metodický postup od sběru vzorků po analýzu dat (B). 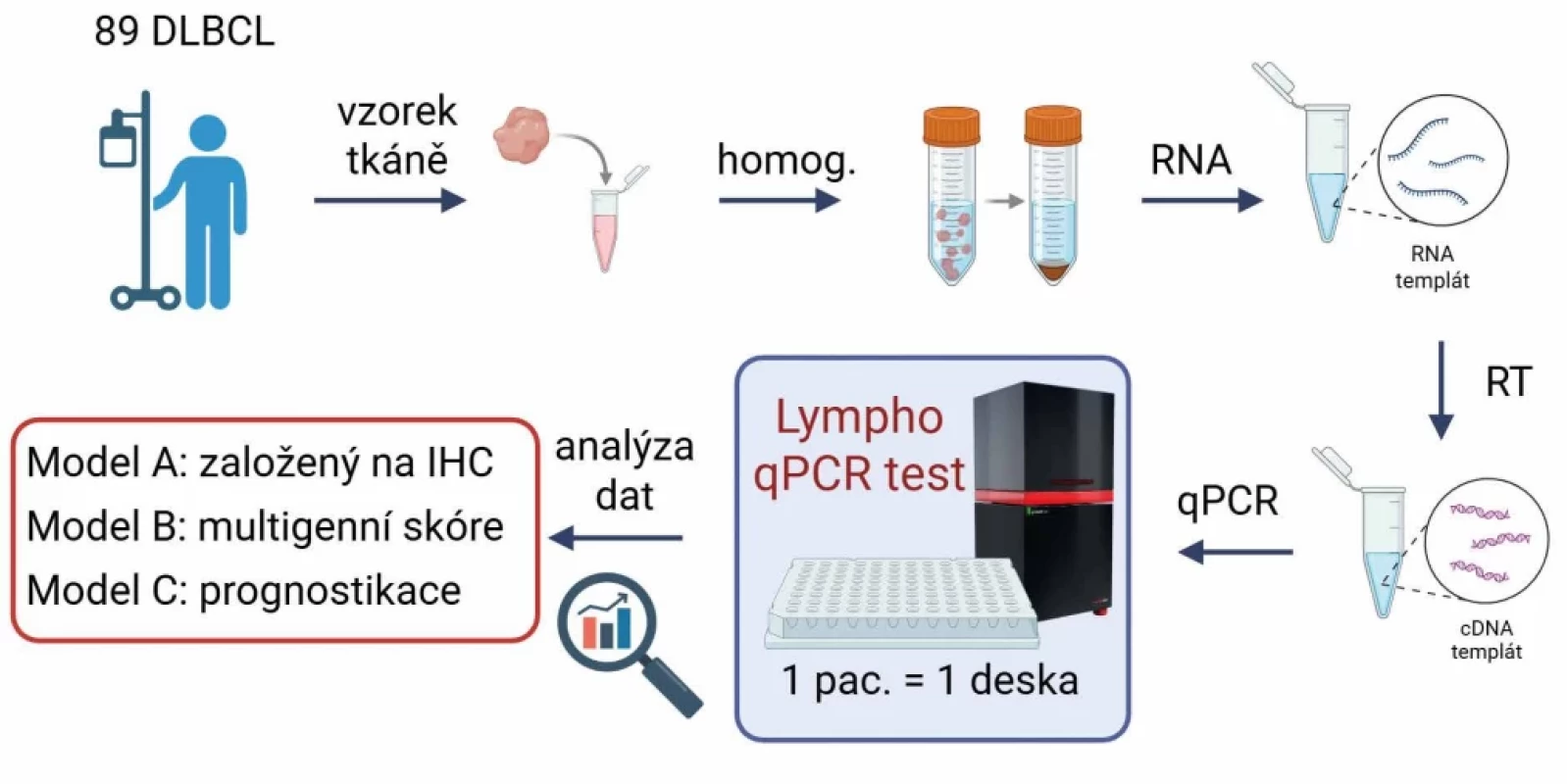
Genetická analýza pomocí NGS panelu LYNX
U 34 pacientů s nepříznivou prognózou (přežitím bez progrese (PFS) kratší než jeden rok) bylo provedeno NGS profilování pomocí panelu LYNX, rutinně používaného na našem pracovišti (27). Ten umožňuje integrativní genomické profilování u lymfoproliferativních onemocnění zahrnující detekci genových variant, chromozomálních změn, přestaveb antigenních receptorů a typických translokací.
DNA byla izolována ze vzorků tkání pomocí MagCore Genomic DNA Tissue kit 401 (RBC Bioscience, Tchaj-wan) a kvantifikována pomocí fluorometru Qubit (Thermo Fisher Scientific, MA, USA). Příprava NGS knihoven a bioinformatická analýza byly provedeny podle publikovaných postupů (27,28). Nalezené aberace byly korelovány s klasifikačními GEP modely pro odhalení potenciální asociace genotyp-fenotyp související s agresivitou onemocnění.
Statistická analýza dat
Na základě hodnot exprese 2^-ΔCt byly vyvinuty tři modely: i) model A pro určení ABC/GCB trénovaný podle IHC klasifikace, optimální kombinace prediktivních genů byla nalezena pomocí mnohorozměrné logistické regrese a obousměrné krokové selekce; ii) model B pro nezávislou klasifikaci ABC/GCB pomocí multigenního expresního skóre (součet hodnot ΔCt vynásobený +1 pro ABC geny a -1 pro GCB geny). Medián skóre byl použit jako dělící hodnota; iii) prognostický model C hodnotící individualizované rizikové skóre pro celkové přežití (OS) a PFS, založený na Coxově regresi zahrnující genovou expresi a věk.
Přežití (OS a PFS) bylo hodnoceno dle kritérií Cheson a kol. (29). Výsledky byly vizualizovány pomocí Kaplan-Meierových křivek a rozdíly ověřovány log-rank testem. Statistická významnost byla stanovena na hladině p ≤ 0,05. Všechny analýzy byly provedeny v programu R.
VÝSLEDKY
Soubor pacientů a zpracování qPCR dat
Studie zahrnovala 89 pacientů s převahou mužů a mediánem věku 63 let. Soubor obsahoval pacienty s vysokým rizikem: 58 % pacientů mělo vysoké IPI skóre, 56 % bylo imunofenotypu ABC a 77 % vykazovalo proliferační index Ki-67 nad 60 %. Medián sledování činil 29 měsíců (tabulka 1). Většina vzorků pocházela z biopsií lymfatických uzlin (94 %), menší část z extranodálních lokalit (kůže, varlata, slezina).
Izolovaná RNA vykazovala uspokojivou kvalitu (RNA Integrity Number (RIN) >7 u 76 vzorků, RIN >6 u 13 vzorků). Gen SERPINA9 byl z analýz vyloučen kvůli trvale nízké expresi. Variační koeficienty (CV) referenčních genů HPRT1, GAPDH a B2M byly 6,3 %, 6,3 % a 8,8 %, což potvrzuje dobrou technickou reprodukovatelnost. Hodnoty relativní kvantifikace (2^-ΔCt) byly použity pro vytvoření tří GEP klasifikačních modelů (obr. 1B): i) model A byl natrénován na základě stanoveného subtypu non-GCB/ GCB podle IHC, ii) model B byl založen čistě na expresi genů pro klasifikaci podtypu COO a iii) model C je prognostický model pro stratifikaci rizika přežití.
Obr. 2. Schematický přehled GEP modelů poskytující nejspolehlivější výsledky. (A) Model A odvozený od IHC stanovení COO subtypu, (B) model B založený na expresi genů a výpočtu multigenního skóre (tečky představují jednotlivé pacienty seřazené podle skóre) a (C) model C předpovídající individuální rizikové skóre pro přežití pacientů. 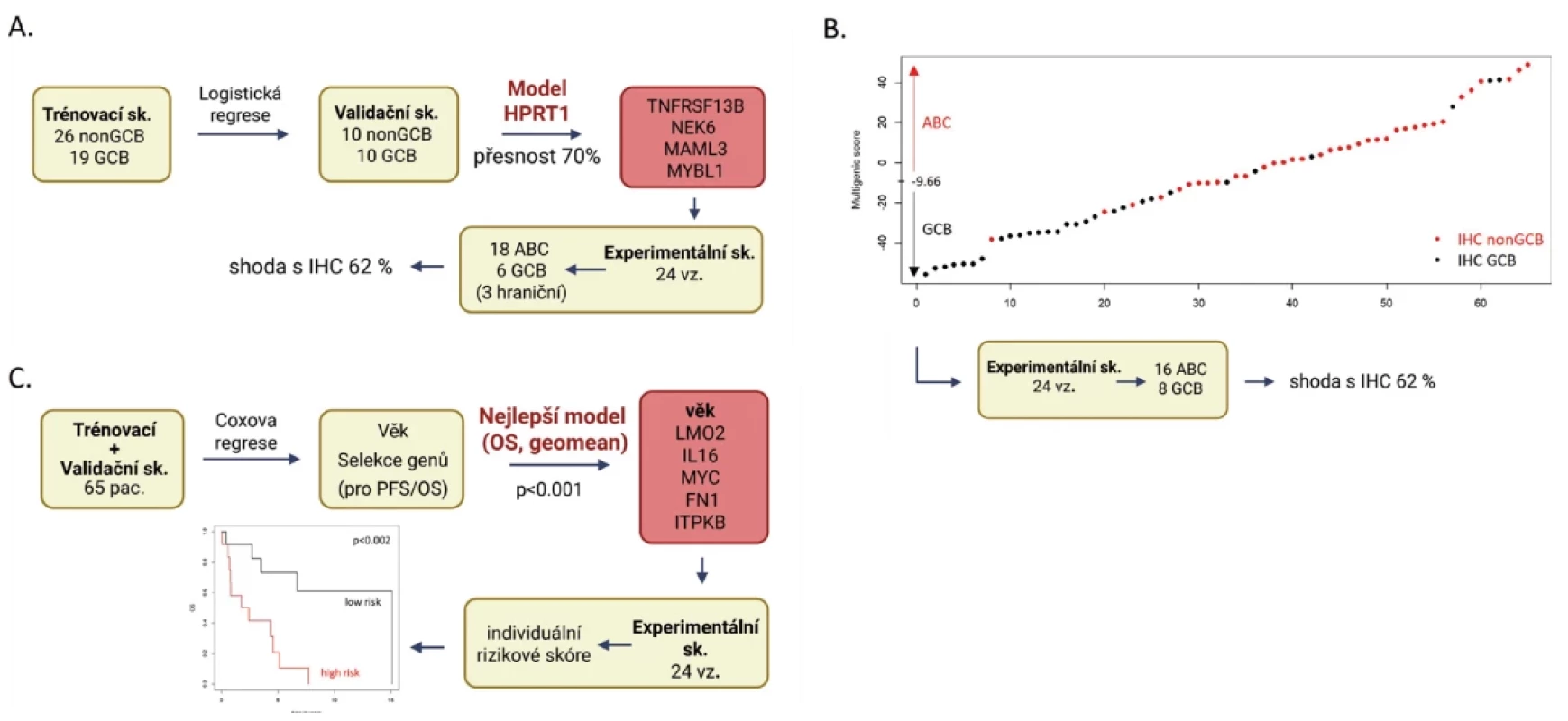
Model A: COO klasifikátor postavený na základě IHC
Model A byl vytvořen na tréninkové kohortě 26 non-GCB a 19 GCB případů, přičemž nezávislá validační kohorta zahrnovala 10 non-GCB a 10 GCB pacientů. Normalizace exprese byla testována zvlášť pro každý referenční gen i pro jejich geometrický průměr. Nejlepších výsledků pro rozlišení podtypů ABC/GCB bylo dosaženo při použití B2M a HPRT1, kdy oba shodně vykazovaly 70% přesnost klasifikace. Vzhledem ke stabilnější expresi byl jako hlavní normalizační gen zvolen HPRT1 (CV 6,3 % vs. 8,8 % u B2M). V experimentální kohortě model klasifikoval 18 vzorků jako ABC a 6 jako GCB. Z nich pouze tři vzorky spadaly do nejistého prahového rozmezí pravděpodobnosti 30-70 %. Porovnání s výsledky IHC ukázalo 62% shodu (8/13) s klasifikací dle Hansové (obr. 2A).
Model B: Predikce COO dle multigenního skóre exprese
S ohledem na limity IHC jsme vytvořili model nezávislý na IHC, vycházející výhradně z GEP hodnot ze sloučené trénovací a validační kohorty (n=65). Testovány byly dva skórovací přístupy: skóre 1 zahrnovalo všechny geny v panelu se stejnou váhou významu, zatímco skóre 2 bylo omezeno na geny IRF4, BCL6 a MME analogicky k Hans algoritmu. Prahová hodnota pro klasifikaci byla nastavena na medián skóre (ABC skóre > medián, GCB skóre
Po analýze experimentální kohorty vykazovalo dle očekávání nejvyšší shodu s IHC skóre 2 (77 %). Avšak jako preferovaný model bylo vybráno skóre 1, které zachycuje širší biologickou variabilitu než IHC (obr. 2B)
Následně jsme zkoumali schopnost identifikovat fenotyp tzv. dvojitých expresorů (DE) a jejich prognózu. Testovali jsme tři hranice exprese: 25., 50. a 75. percentil ΔCt hodnot genů MYC a BCL2, které umožnily identifikaci 39, 22 a 10 případů DE. Pacienti klasifikovaní jako DE podle 50. percentilu vykazovali trend ke kratšímu OS (p=0,08), PFS nedosáhlo statistické významnosti (p=0,1). Při porovnání s identifikací DE dle IHC (n=51) byla nejvyšší shoda 76% pozorována při použití vyšší hranice 75. percentilu. To ukazuje na potřebu dosažení vyšších hladin mRNA pro přiblížení se prahovým hodnotám stanovení proteinů pomocí IHC (MYC >40 %, BCL2 >50 %).
Model C: prognostický model nezávislý na COO
V naší kohortě jsme nepozorovali významný rozdíl v přežití ABC a GCB pacientů, ať už podle IHC nebo GEP. Proto byl vytvořen model C, který integruje věk, úroveň genové exprese a přežití (OS a PFS). Věk se ukázal jako silný prognostický faktor, který významně ovlivňuje OS (p < 0,001) i PFS (p < 0,002). Po testování různých způsobů normalizace byla jako nejspolehlivější zvolena kombinace věk a exprese genů LMO2, IL16, MYC, FN1 a ITPKB (normalizovaná na geometrický průměr housekeeping genů) asociující s OS (obr. 2C). Tento model má silnou prediktivní sílu pro pětileté přežití (AUC 78,6 % v ROC analýze přežití) a spolehlivě rozlišil v experimentální kohortě vysoce rizikové pacienty s kratším OS (p < 0,002; obr. 2C). Tito pacienti měli špatné výsledky bez ohledu na COO subtyp (2 ABC, 4 GCB, 6 nemá IHC údaj). Multivariační analýza potvrdila nezávislost modelu C na klasických prognostických kritériích ECOG, klinické stadium a skóre IPI (p < 0,001).
Genetické pozadí časné progrese u pacientů s nízkým rizikem dle GEP
U většiny pacientů s brzkou progresí (PFS < 1 rok; n=34) jsme detekovali četné nepříznivé genetické změny a značnou genomickou komplexitu (obr. 3). Zvláště časté byly komplexní chromozomální aberace (> 5 změn), které byly pozorovány u 82 % těchto pacientů (n=28). Nejčastější genetické změny zahrnovaly geny BCL2 (n=19), TP53 (n=18) a CDKN2A/B (n=16), následované mutacemi v signální dráze BCR (MYD88, CD79B). Častá byla bialelická inaktivace TP53 a CDKN2A/B přítomná u 13 a 8 pacientů. Naopak očekávané změny genu MYC byly vzácné (jedna mutace, jedna translokace, šest zisků 8q) a nebyly detekovány žádné případy tzv. double - nebo triple-hit lymfomů. Fenotyp DE byl zaznamenán u 8 pacientů.
Obr. 3. Nepříznivé genetické defekty identifikované pomocí integrativního NGS profilování u pacientů s časnou progresí onemocnění. Pacienti jsou seřazeni podle délky přežití bez progrese (PFS) do jednoho roku. 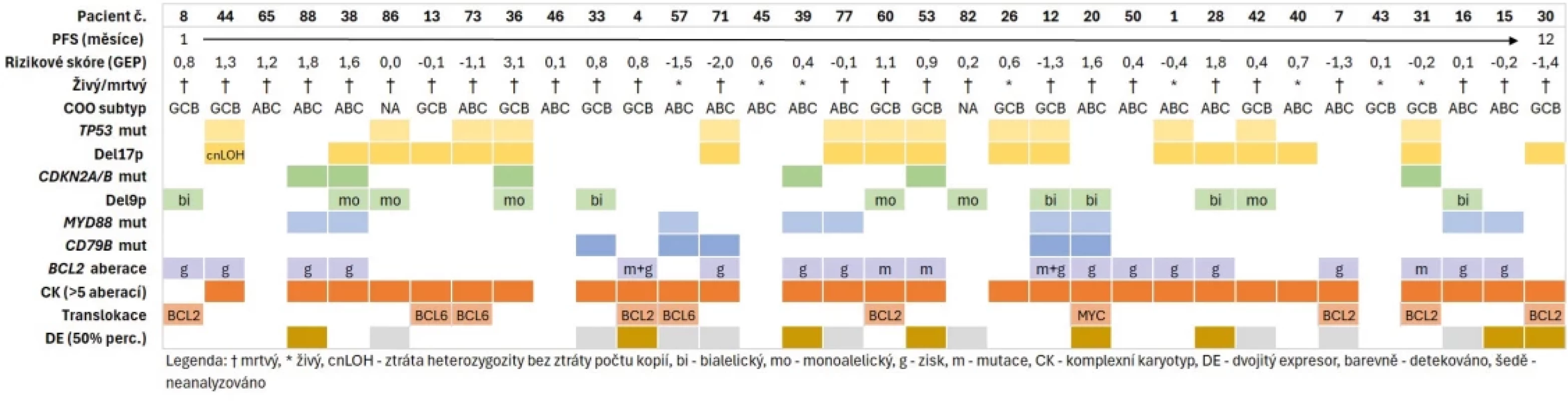
Zvláštní pozornost byla věnována pacientům s časnou progresí, kteří měli podle prognostického modelu C nízké riziko (PFS < 1 rok a skóre rizika < -1; pacienti č. 7, 12, 30, 57, 71, 73
na obrázku 3). Všichni měli komplexní karyotyp a čtyři z nich nesli aberace TP53 a/nebo BCL2, což naznačuje možnou příčinu progrese onemocnění. Pacienti bez detekovatelných molekulárních defektů (č. 43, 45, 46, 65) měli ve třech případech nepříznivý podtyp ABC a pouze jeden byl GCB se středním skóre rizika GEP.Integrace výsledků cíleného GEP a NGS ukazuje, že časná progrese je často i u pacientů s nízkým GEP-rizikem spojena s komplexními genetickými aberacemi. Jejich vyšetření je časově náročnější, ale může zlepšit rizikovou stratifikaci pacientů stanovenou pomocí rychlého GEP testu.
DISKUZE
Klasifikace pacientů podle COO hraje již téměř dvacet let důležitou roli v diagnostice DLBCL. Starší studie před zavedením rituximabu a rovněž v éře R-CHOP léčby jednoznačně prokazovaly horší prognózu u subtypu ABC oproti GCB (4,6). Novější prospektivní studie (30,31) u pacientů léčených jednotně moderní imunochemoterapií však tento rozdíl zpochybňují. Například studie GOYA (30) nezjistila významný rozdíl v přežití mezi oběma subtypy pacientů léčených R-CHOP, což naznačuje, že COO rozdělení dnes již nemusí mít samostatnou prognostickou hodnotu.
Naopak s rozvojem cílených terapií roste prediktivní význam COO klasifikace. Inhibitor BTK, ibrutinib, má vyšší účinnost u ABC-DLBCL v důsledku chronicky aktivní BCR signalizace (17), zatímco lenalidomid prokázal efektivitu u ABC relabovaných či refrakterních případů (32). Podobně studie Polarix a REMoDL-B potvrdily přínos režimu polatuzumab-R-CHP (3) a bortezomib - -R-CHOP (33) především v podskupině ABC. COO klasifikace se tedy stává důležitým prediktivním biomarkerem pro personalizovaný výběr léčby.
Navzdory své klinické hodnotě stanovení COO stále naráží na technické překážky. IHC algoritmus dle Hansové je rychlý, ale vykazuje omezenou reprodukovatelnost a přibližně 70% shodu s referenčním („gold standard“ metoda) profilováním genové exprese (9,20,34). Další metody jako je sekvenování RNA nebo mikročipové technologie jsou nákladné, časově náročné a nejsou běžně dostupné pro rutinní použití. V reakci na tato omezení jsme vyvinuli vlastní Lympho-qPCR test, který umožňuje rychlou, ekonomickou a spolehlivou klasifikaci COO na úrovni RNA. Navrhli jsme tři modely různé úrovně klinické použitelnosti. Model A, trénovaný na IHC, sdílí její omezení a dosahuje nižší přesnosti. Model B, založený čistě na expresních datech, umožňuje nezávislé určení COO a zároveň identifikaci dvojitých expresorů MYC/BCL2. Je však třeba připomenout, že hladiny mRNA těchto genů nejsou přímo srovnatelné s proteinovou expresí v IHC (35,36), díky rozdílné stabilitě a subcelulární lokalizaci. Naše data ukazují, že 75% práh GEP odpovídá běžně užívaným mezním hranicím IHC (MYC >40 %, BCL2 >50 %).
Model C rozšiřuje použití GEP nad rámec klasifikace COO a představuje samostatný prognostický nástroj, který kombinuje expresi vybraných genů a věk pacienta. Tento model předpovídá přežití nezávisle na standardním IPI indexu a tím doplňuje klinické hodnocení o biologické aspekty nádoru. Podobně jako jiné studie (34,37–40) i naše výsledky podporují integraci transkriptomických dat pro vylepšení rizikové stratifikace pacientů, které přesahuje binární zařazení do ABC/GCB subtypu. Jejich kombinace s genetickými a klinickými parametry umožňuje přesněji vytipovat pacienty s agresivním průběhem nemoci vhodných pro úpravu terapie.
Molekulární profilování se stává důležitou součástí precizní onkologie u DLBCL. Popsané molekulární subtypy mají různou prognózu a potenciál cílené léčby (12,14–18), např. podtyp MCD (typický s mutacemi MYD88) profituje z léčby ibrutinibem plus R-CHOP. Naše molekulární analýzy ukázaly v souladu s dostupnou literaturou (36,41–43), že časná progrese je spojena s defekty v TP53, CDKN2A/B a BCL2 a komplexními chromozomálními aberacemi. Tyto nepříznivé změny se objevují i u pacientů, kteří byli podle GEP hodnoceni jako nízké riziko (model C), což naznačuje, že kombinovaný přístup může zpřesnit rizikovou stratifikaci pacientů. Zajímavým zjištěním je absence genetických aberací MYC, která ukazuje, že samotná zvýšená exprese může postačovat k identifikaci vysoce rizikových pacientů. Do budoucna lze předpokládat, že význam tradičního dělení na ABC/ GCB postupně ustoupí přesnější molekulární klasifikaci založené na genetických a transkriptomických znacích.
Z praktického pohledu náš Lympho-qPCR test nabízí rychlou, modulární a diagnosticky využitelnou metodu pro současné určení COO subtypu a stratifikaci DLBCL pacientů dle rizika. Krátká doba vyšetření do dvou dnů umožňuje včasné rozhodnutí o léčbě a výběr pacientů vhodných pro intenzivnější režimy nebo klinické studie. Cílené doplnění o molekulární testy (FISH, Sangerovo sekvenování nebo NGS) dále zlepšuje prognostifikaci, zejména při cílené detekci defektů BCL2, TP53 a CDKN2A/B, které byly v našem souboru i v nezávislých studiích (36,41,43–45) konzistentně spojeny s časnou progresí. Dalším přínosem je analýza komplexních chromozomálních přestaveb, která ale prozatím vyžaduje přijetí náročných celogenomových metod (jako je WGS nebo optické mapování).
Naše práce nese také svá omezení, neboť byla provedena na vzorcích s vysoce kvalitní RNA z čerstvě zmrazené tkáně (bez zahrnutí běžněji dostupného FFPE materiálu), je retrospektivní a postrádá externí validační kohortu. Přesto tato studie odráží dlouhodobou zkušenost jednoho hematoonkologického centra, což zvyšuje její translační potenciál. Navazující práce směřují na rozšíření metody na FFPE vzorky a validaci v prospektivních multicentrických kohortách.
Závěrem lze shrnout, že cílené profilování genové exprese založené na qPCR umožňuje rychlou COO klasifikaci a prognostickou stratifikaci DLBCL pacientů v rámci jednoho diagnostického vyšetření. V kombinaci s malým, ale informativním souborem genetických markerů představuje praktický krok k implementaci personalizované medicíny u DLBCL. Víceúrovňové hodnocení rizika, které zachycuje transkriptomický fenotyp i genetickou nestabilitu, může podpořit časnější identifikaci pacientů s vysokým rizikem a zhodnocení léčebné strategie.
PODĚKOVÁNÍ
Tato práce byla podpořena projekty AZV NU22-08-00227 a FNBr 65269705 poskytnutými Ministerstvem zdravotnictví ČR. Za podporu při získávání vědeckých dat uvedených v tomto článku děkujeme pracovišti sdílené laboratoře genomiky a bioinformatiky z CEITEC MU, které je podporováno výzkumnou infrastrukturou NCMG (LM2018132 a LM2023067 financované MŠMT ČR).
PROHLÁŠENÍ
Autor práce prohlašuje, že v souvislosti s tématem, vznikem a publikací tohoto článku není ve střetu zájmů a vznik ani publikace článku nebyly podpořeny žádnou farmaceutickou firmou. Toto prohlášení se týká i všech spoluautorů.
Zdroje
1. Crump M, Neelapu SS, Farooq U, Van Den Neste E, Kuruvilla J, Westin J, et al. Outcomes in refractory diffuse large B-cell lymphoma: results from the international SCHOLAR-1 study. Blood 2017; 130(16): 1800–1808.
2. Farooq U, Maurer MJ, Thompson CA, Thanarajasingam G, Inwards DJ, Micallef I, et al. Clinical heterogeneity of diffuse large B cell lymphoma following failure of front-line immunochemotherapy. Br J Haematol 2017; 179(1): 50–60.
3. Tilly H, Morschhauser F, Sehn LH, Friedberg JW, Trněný M, Sharman JP, et al. Polatuzumab Vedotin in Previously Untreated Diffuse Large B-Cell Lymphoma. N Engl J Med 2022; 386(4): 351–363.
4. Alizadeh AA, Eisen MB, Davis RE, Ma C, Lossos IS, Rosenwald A, et al. Distinct types of diffuse large B-cell lymphoma identified by gene expression profiling. Nature 2000; 403(6769): 503–511.
5. Lenz G, Wright GW, Emre NCT, Kohlhammer H, Dave SS, Davis RE, et al. Molecular subtypes of diffuse large B-cell lymphoma arise by distinct genetic pathways. Proc Natl Acad Sci U S A 2008; 105(36): 13520–13525.
6. Rosenwald A, Wright G, Chan WC, Connors JM, Campo E, Fisher RI, et al. The use of molecular profiling to predict survival after chemotherapy for diffuse large-B-cell lymphoma. N Engl J Med 2002; 346(25): 1937–1947.
7. Alduaij W, Collinge B, Ben-Neriah S, Jiang A, Hilton LK, Boyle M, et al. Molecular determinants of clinical outcomes in a real-world diffuse large B-cell lymphoma population. Blood 2023; 141(20): 2493–2507.
8. Tripodo C, Zanardi F, Iannelli F, Mazzara S, Vegliante M, Morello G, et al. A Spatially Resolved Dark - versus Light-Zone Microenvironment Signature Subdivides Germinal Center-Related Aggressive B Cell Lymphomas. iScience 2020; 23(10): 101562.
9. Hans CP, Weisenburger DD, Greiner TC, Gascoyne RD, Delabie J, Ott G, et al. Confirmation of the molecular classification of diffuse large B-cell lymphoma by immunohistochemistry using a tissue microarray. Blood 2004; 103(1): 275–282.
10. Scott DW, Wright GW, Williams PM, Lih CJ, Walsh W, Jaffe ES, et al. Determining cell-of - -origin subtypes of diffuse large B-cell lymphoma using gene expression in formalin-fixed paraffin-embedded tissue. Blood 2014; 123(8): 1214–1217.
11. Zamò A, Gerhard-Hartmann E, Ott G, Anagnostopoulos I, Scott DW, Rosenwald A, et al. Routine application of the Lymph2Cx assay for the subclassification of aggressive B-cell lymphoma: report of a prospective real-world series. Virchows Arch 2022; 481(6): 935–943.
12. Chapuy B, Stewart C, Dunford AJ, Kim J, Kamburov A, Redd RA, et al. Molecular subtypes of diffuse large B cell lymphoma are associated with distinct pathogenic mechanisms and outcomes. Nat Med 2018; 24(5): 679–690.
13. Schmitz R, Wright GW, Huang DW, Johnson CA, Phelan JD, Wang JQ, et al. Genetics and Pathogenesis of Diffuse Large B-Cell Lymphoma. N Engl J Med 2018; 378(15): 1396–1407.
14. Wright GW, Huang DW, Phelan JD, Coulibaly ZA, Roulland S, Young RM, et al. A Probabilistic Classification Tool for Genetic Subtypes of Diffuse Large B Cell Lymphoma with Therapeutic Implications. Cancer Cell 2020; 37(4): 551-568.
15. Abrisqueta P. New Insights into First-Line Therapy in Diffuse Large B-Cell Lymphoma: Are We Improving Outcomes? J Clin Med 2024; 13(7): 1929.
16. Zhang MC, Tian S, Fu D, Wang L, Cheng S, Yi HM, et al. Genetic subtype-guided immunochemotherapy in diffuse large B cell lymphoma: The randomized GUIDANCE-01 trial. Cancer Cell 2023; 41(10): 1705-1716.
17. Wilson WH, Wright GW, Huang DW, Hodkinson B, Balasubramanian S, Fan Y, et al. Effect of ibrutinib with R-CHOP chemotherapy in genetic subtypes of DLBCL. Cancer Cell 2021; 39(12): 1643-1653.
18. Shen YG, Shi Q, Tang W, Xu PP, Cao YW, Ji MM, et al. Genetic subtype-guided immunochemotherapy in relapsed and refractory diffuse large B cell lymphoma: a phase 2 investigator-initiated nonrandomized clinical trial (GUIDANCE-06). Sig Transduct Target Ther 2025; 10(1): 232.
19. Shen R, Fu D, Dong L, Zhang MC, Shi Q, Shi ZY, et al. Simplified algorithm for genetic subtyping in diffuse large B-cell lymphoma. Signal Transduct Target Ther 2023; 8(1): 145.
20. Yan WH, Jiang XN, Wang WG, Sun YF, Wo YX, Luo ZZ, et al. Cell-of-Origin Subtyping of Diffuse Large B-Cell Lymphoma by Using a qPCR-based Gene Expression Assay on Formalin-Fixed Paraffin-Embedded Tissues. Front Oncol 2020; 10 : 803.
21. Bobée V, Ruminy P, Marchand V, Viailly PJ, Abdel Sater A, Veresezan L, et al. Determination of Molecular Subtypes of Diffuse Large B-Cell Lymphoma Using a Reverse Transcriptase Multiplex Ligation-Dependent Probe Amplification Classifier: A CALYM Study. J Mol Diagn 2017; 19(6): 892–904.
22. Barrans SL, Crouch S, Care MA, Worrillow L, Smith A, Patmore R, et al. Whole genome expression profiling based on paraffin embedded tissue can be used to classify diffuse large B-cell lymphoma and predict clinical outcome. Br J Haematol 2012; 159(4): 441 – 453.
23. Lossos IS, Czerwinski DK, Alizadeh AA, Wechser MA, Tibshirani R, Botstein D, et al. Prediction of survival in diffuse large-B-cell lymphoma based on the expression of six genes. N Engl J Med 2004; 350(18): 1828–1837.
24. Rimsza LM, Leblanc ML, Unger JM, Miller TP, Grogan TM, Persky DO, et al. Gene expression predicts overall survival in paraffin-embedded tissues of diffuse large B-cell lymphoma treated with R-CHOP. Blood 2008; 112(8): 3425–3433.
25. Shipp MA, Ross KN, Tamayo P, Weng AP, Kutok JL, Aguiar RCT, et al. Diffuse large B-cell lymphoma outcome prediction by gene-expression profiling and supervised machine learning. Nat Med 2002; 8(1): 68–74.
26. Wright G, Tan B, Rosenwald A, Hurt EH, Wiestner A, Staudt LM. A gene expression - -based method to diagnose clinically distinct subgroups of diffuse large B cell lymphoma. Proc Natl Acad Sci U S A 2003; 100(17): 9991 – 9996.
27. Navrkalova V, Plevova K, Hynst J, Pal K, Mareckova A, Reigl T, et al. LYmphoid NeXt-Generation Sequencing (LYNX) Panel: A Comprehensive Capture-Based Sequencing Tool for the Analysis of Prognostic and Predictive Markers in Lymphoid Malignancies. J Mol Diagn 2021; 23(8): 959–974.
28. Navrkalova V, Mareckova A, Hricko S, Hrabcakova V, Radova L, Kubes V, et al. Reliable detection of CNS lymphoma-derived circulating tumor DNA in cerebrospinal fluid using multi-biomarker NGS profiling: insights from a real-world study. Biomark Res 2025; 13(1): 71.
29. Cheson BD, Pfistner B, Juweid ME, Gascoyne RD, Specht L, Horning SJ, et al. Revised response criteria for malignant lymphoma. J Clin Oncol 2007; 25(5): 579–586.
30. Sehn LH, Martelli M, Trněný M, Liu W, Bolen CR, Knapp A, et al. A randomized, open - -label, Phase III study of obinutuzumab or rituximab plus CHOP in patients with previously untreated diffuse large B-Cell lymphoma: final analysis of GOYA. J Hematol Oncol 2020; 13(1): 71.
31. Staiger AM, Ziepert M, Horn H, Scott DW, Barth TFE, Bernd HW, et al. Clinical Impact of the Cell-of-Origin Classification and the MYC/ BCL2 Dual Expresser Status in Diffuse Large B-Cell Lymphoma Treated Within Prospective Clinical Trials of the German High-Grade Non-Hodgkin’s Lymphoma Study Group. J Clin Oncol 2017; 35(22): 2515–2526.
32. Hernandez-Ilizaliturri FJ, Deeb G, Zinzani PL, Pileri SA, Malik F, Macon WR, et al. Higher response to lenalidomide in relapsed/ refractory diffuse large B-cell lymphoma in nongerminal center B-cell-like than in germinal center B-cell-like phenotype. Cancer 2011; 117(22): 5058–5066.
33. Davies AJ, Barrans S, Stanton L, Caddy J, Wilding S, Saunders G, et al. Differential Efficacy From the Addition of Bortezomib to R-CHOP in Diffuse Large B-Cell Lymphoma According to the Molecular Subgroup in the REMoDL-B Study With a 5-Year Follow-Up. J Clin Oncol 2023; 41(15): 2718–2723.
34. Abdulla M, Hollander P, Pandzic T, Mansouri L, Ednersson SB, Andersson PO, et al. Cell-of-origin determined by both gene expression profiling and immunohistochemistry is the strongest predictor of survival in patients with diffuse large B-cell lymphoma. Am J Hematol 2020; 95(1): 57–67.
35. Valera A, López-Guillermo A, Cardesa-Salzmann T, Climent F, González-Barca E, Mercadal S, et al. MYC protein expression and genetic alterations have prognostic impact in patients with diffuse large B-cell lymphoma treated with immunochemotherapy. Haematologica 2013; 98(10): 1554–1562.
36. Qin Y, Chen H, Liu P, Zhang C, Yang J, Gui L, et al. Prognostic value of BCL2 and TP53 genetic alterations for diffuse large B-cell lymphoma patients treated with R-CHOP. Cancer Biol Med 2021; 19(6): 893–909.
37. Merdan S, Subramanian K, Ayer T, Van Weyenbergh J, Chang A, Koff JL, et al. Gene expression profiling-based risk prediction and profiles of immune infiltration in diffuse large B-cell lymphoma. Blood Cancer J 2021; 11(1): 2.
38. Mosquera Orgueira A, Díaz Arías JÁ, Cid López M, Peleteiro Raíndo A, López García A, Abal García R, et al. Prognostic Stratification of Diffuse Large B-cell Lymphoma Using Clinico-genomic Models: Validation and Improvement of the LymForest-25 Model. Hemasphere 2022; 6(4): e706.
39. Ren W, Wan H, Own SA, Berglund M, Wang X, Yang M, et al. Genetic and transcriptomic analyses of diffuse large B-cell lymphoma patients with poor outcomes within two years of diagnosis. Leukemia 2024; 38(3): 610–620.
40. Yan J, Yuan W, Zhang J, Li L, Zhang L, Zhang X, et al. Identification and Validation of a Prognostic Prediction Model in Diffuse Large B-Cell Lymphoma. Front Endocrinol (Lausanne) 2022; 13 : 846357.
41. Bolen CR, Klanova M, Trneny M, Sehn LH, He J, Tong J, et al. Prognostic impact of somatic mutations in diffuse large B-cell lymphoma and relationship to cell-of-origin: data from the phase III GOYA study. Haematologica 2020; 105(9): 2298–2307.
42. Cutmore NH, Krupka JA, Hodson DJ. Genetic Profiling in Diffuse Large B-Cell Lymphoma: The Promise and the Challenge. Mod Pathol 2023; 36(1): 100007.
43. Karube K, Enjuanes A, Dlouhy I, Jares P, Martin-Garcia D, Nadeu F, et al. Integrating genomic alterations in diffuse large B-cell lymphoma identifies new relevant pathways and potential therapeutic targets. Leukemia 2018; 32(3): 675–684.
44. de Leval L, Alizadeh AA, Bergsagel PL, Campo E, Davies A, Dogan A, et al. Genomic profiling for clinical decision making in lymphoid neoplasms. Blood 2022; 140(21): 2193–227.
45. Walker JS, Wenzl K, Novak JP, Stokes ME, Hopper MA, Dropik AR, et al. Integrated genomics with refined cell-of-origin subtyping distinguishes subtype-specific mechanisms of treatment resistance and relapse in diffuse large B-cell lymphoma. Blood Cancer J 2025; 15(1): 120.
Štítky
Patologie Soudní lékařství Toxikologie
Článek vyšel v časopiseČesko-slovenská patologie

2026 Číslo 1-
Všechny články tohoto čísla
- Testování exprese claudinu 18.2 u adenokarcinomu žaludku a gastroesofageální junkce: Současný stav a výhled do blízké budoucnosti
- Castlemanova choroba – jedno jméno, mnoho tváří
- Lymfatická tkáň v souvislostech: od nenápadných změn k zásadním diagnózám
- Přednosti a limitace nového stagingového systému karcinomu endometria FIGO 2023 z pohledu klinika a patologa
- Od archeologické brigády k americké rezidentuře: proč je patologie „nejlepší obor medicíny“
- Cílené profilování genové exprese jako nástroj pro diagnostické určení buněčného subtypu a prognostickou stratifikaci u difuzního velkobuněčného B-lymfomu
- Castleman-like lymfadenopatie u pacienta se smíšenou chorobou pojiva: kazuistika a přehled literatury
- EBV-asociovaná plazmocelulární varianta Castlemanovy choroby: více než deset let trvající diagnostická odysea – kazuistika pacienta
- MONITOR, aneb nemělo by vám uniknout, že…
- Česko-slovenská patologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Castlemanova choroba – jedno jméno, mnoho tváří
- Testování exprese claudinu 18.2 u adenokarcinomu žaludku a gastroesofageální junkce: Současný stav a výhled do blízké budoucnosti
- Přednosti a limitace nového stagingového systému karcinomu endometria FIGO 2023 z pohledu klinika a patologa
- Cílené profilování genové exprese jako nástroj pro diagnostické určení buněčného subtypu a prognostickou stratifikaci u difuzního velkobuněčného B-lymfomu
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Revma Focus: Spondyloartritidy
nový kurz
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Autoři: prof. MUDr. Pavel Horák, CSc., doc. MUDr. Ludmila Brunerová, Ph.D., doc. MUDr. Václav Vyskočil, Ph.D., prim. MUDr. Richard Pikner, Ph.D., MUDr. Olga Růžičková, MUDr. Jan Rosa, prof. MUDr. Vladimír Palička, CSc., Dr.h.c.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



