-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Přednosti a limitace nového stagingového systému karcinomu endometria FIGO 2023 z pohledu klinika a patologa
The advantages and limitations of the new FIGO 2023 staging system for endometrial carcinoma from the perspective of the clinician and pathologist
The Czech Republic is one of the countries with the highest incidence of endometrial cancer in the world. In June 2023, the Women’s Cancer Committee of the International Federation of Gynaecology and Obstetrics (FIGO) introduced a new staging system for endometrial cancer, FIGO 2023, which replaced the 2009 version. The FIGO 2023 staging system differs significantly from the previous version by incorporating the result of molecular classification of the tumour and some histopathological parameters - histological type of tumour, tumour grade and presence of substantial lymphovascular invasion - into the definitions of stage I and stage II. For stage I and II tumours, specific separate stages are reserved when the molecular profile of POLEmut or TP53mut is detected. Stages III and IV have also been modified, but the result of the molecular classification of the tumour and other histopathological parameters do not influence the staging. However, the molecular classification result should be reported for all stages. These changes have further strengthened the role of the pathologist in staging. The changes, which are partly based on the recommendations of the three European professional societies ESGO/ESTRO/ESP for the diagnosis and treatment of endometrial cancer, better reflect the biological behaviour of the tumour and significantly refine the prognosis of the patient at a given stage. On the other hand, the FIGO 2023 staging system is quite complex and requires expensive tests, which may pose a problem for its routine use in a global context. The implementation of the FIGO 2023 endometrial cancer staging system in daily practice requires the full involvement of all stakeholders.
Keywords:
endometrial cancer – staging – molecular classification – staging system – FIGO 2023 – LVSI – controversies
Autoři: Martin Hruda 1; Radoslav Matěj 2,3,4; Borek Sehnal 1; Jana Drozenová 2; Helena Robová 1; Tomáš Pichlík 1; Michael J. Halaška 1; Lukáš Rob 1; Pavel Dundr 4
Působiště autorů: Gynekologicko-porodnická klinika, Fakultní nemocnice Královské Vinohrady a 3. lékařská fakulta Univerzity Karlovy, Praha 1; Ústav patologie, Fakultní nemocnice Královské Vinohrady a 3. lékařská fakulta Univerzity Karlovy, Praha 2; Ústav patologie a molekulární medicíny, Fakultní Thomayerova nemocnice a 3. lékařská fakulta Univerzity Karlovy, Praha 3; Ústav patologie, Všeobecná fakultní nemocnice a 1. lékařská fakulta Univerzity Karlovy, Praha 4
Vyšlo v časopise: Čes.-slov. Patol., 62, 2026, No. 1, p. 35-42
Kategorie: Přehledový článek
Souhrn
Česká republika patří celosvětově k zemím s nejvyšší incidencí karcinomu endometria. V červnu 2023 představila Komise pro ženské malignity (Women’s Cancer Committee) mezinárodní organizace FIGO (The International Federation of Gynaecology and Obstetrics, Mezinárodní federace gynekologie a porodnictví) nový stagingový systém karcinomu endometria FIGO 2023, který nahradil verzi z roku 2009. Stagingový systém FIGO 2023 se výrazně liší od předchozí verze, protože do definic stádia I a stádia II implementoval nově výsledek molekulární klasifikace nádoru a některé histopatologické parametry – histologický typ nádoru, grade nádoru a přítomnost podstatné lymfovaskulární invaze. Pro nádory ve stádiu I a II jsou při průkazu molekulárního profilu POLEmut nebo TP53mut vyhrazena specifická samostatná stádia. Stádia III a IV byla také upravena, ale výsledek molekulární klasifikace nádoru a další histopatologické parametry nemají na stanovení stádia vliv. Výsledek molekulární klasifikace by měl být ale u všech stádií uveden. Tyto úpravy dále posílily roli patologa při určení stádia. Zahrnuté změny, které částečně vycházejí z doporučení tří evropských odborných společností ESGO/ESTRO/ESP pro diagnostiku a léčbu karcinomu endometria, lépe odráží biologické chování nádoru a výrazně zpřesňují prognózu pacientky v konkrétním stádiu. Na druhou stranu, stagingový systém FIGO 2023 je dosti složitý a vyžaduje nákladná vyšetření, což může způsobit problém při jeho rutinním používání v celosvětovém kontextu. Implementace stagingového systému pro karcinom endometria FIGO 2023 do každodenní praxe vyžaduje plné zapojení všech zúčastněných stran.
Klíčová slova:
karcinom endometria – staging – molekulární klasifikace – stagingový systém – FIGO 2023 – LVSI – kontroverze
Přednosti a limitace nového stagingového systému karcinomu endometria FIGO 2023 z pohledu klinika a patologa buje mezi 34–37 novými případy na 100 tisíc žen (1 800 – 2 000 nových onemocnění za rok) (3). Poslední data z roku 2021 uvádí incidenci 33,9 nových karcinomů endometria na 100 000 žen, což odpovídá mírnému poklesu o 200 případů (3). Vzhledem k časné symptomatologii jsou téměř dvě třetiny pacientek s karcinomem endometria diagnostikovány v časných stádiích s možností primární chirurgické léčby (3–7). Poslední revize stagingového systému FIGO karcinomu endometria byla uvedena do praxe v roce 2009 (8,9). V červnu 2023 Komise pro ženské malignity (Women‘s Cancer Committee) Mezinárodní federace gynekologie a porodnictví FIGO (Fédération Internationale de Gynécologie et d´Obstétrique, The International Federation of Gynecology and Obstetrics) oficiálně představila nový aktualizovaný stagingový systém pro karcinom endometria, který vznikl za spolupráce předních představitelů mezinárodních společností ESGO (European Society of Gynaecological Oncology – Evropská společnost pro gynekologickou onkologii), ESTRO (European Society for Radiotherapy and Oncology – Evropská společnost pro radioterapii a onkologii) a ESP (European Society of Pathology – Evropská společnost patologie) (7). Nový stagingový systém se výrazně liší od předchozích verzí, protože do definice jednotlivých stadií mimo tradičně anatomického rozsahu tumoru zahrnul i další histopatologické parametry. V současném stagingovém systému FIGO 2023 mění (sub)stádium i histologický typ nádoru (agresivní vs. neagresivní histologický typ), přítomnost podstatné (v originále substantial, extensive) lymfovaskulární invaze (LVSI, lymphovascular space invasion) a v některých případech také výsledek molekulární klasifikace nádoru. Stagingové systémy FIGO 2009 a FIGO 2023 zobrazuje tabulka 1. Stagingový systém pro karcinosarkom zůstává identický se stagingem karcinomu endometria.
Tab. 1. Staging karcinomu endometria (nová stadia vytvořena na základě výsledku molekulární testace jsou zvýrazněna). 
Pozn.: 1 Low-grade (LG) endometroidní karcinom (grade 1 a 2) s postižením endometria a jednoho vaječníku má velmi dobrou prognózu a žádná adjuvantní léčba se nedoporučuje, pokud jsou splněna všechna dále uvedená kritéria: 1) není přítomna hluboká myometriální invaze ( max. < 50 % stěny dělohy); 2) není přítomna masivní lymfangioinvaze (LVSI); 3) nejsou přítomné další metastázy; 4) nádor omezený na jeden vaječník bez známek invaze a prasknutí pouzdra (ekvivalentní pT1a). 2 LVSI podle definice WHO 2020: podstatná LVSI odpovídá ≥ 5 postižených cév. 3 Non-endometroidní (serózní, světlobuněčný, mezonefrický typ, mucinózní gastrointestinální typ, nediferencovaný, karcinosarkom) + high-grade (HG, grade 3) endometroidní karcinom; jedná se o prognosticky, klinicky a molekulárně heterogenní skupinu. 4 Mikrometastázy jsou považovány za metastatické postižení (pN1[mi]). Prognostický význam ITC (isolated tumour cells, izolované nádorové buňky) je nejasný. Přítomnost ITC by měla být zdokumentována a je považována za pN0(i+). Makrometastáza znamená postižení lymfatické uzliny velikosti > 2 mm, mikrometastáza velikosti 0,2–2 mm a/nebo počet > 200 postižených buněk a ITC jsou velikosti ≤ 0,2 mm a počtu ≤ 200 postižených buněk. Stádium I
Stádium IA, které bylo původně vyčleněno pro nádory s invazí < 50 % tloušťky myometria kteréhokoliv histologického typu, nyní zahrnuje karcinomy endometria pouze tzv. neagresivního histologického typu, tzn. LG (low-grade, grade 1 a 2) endometroidní karcinomy bez průkazu podstatné LVSI. Stádium IA se dělí na další tři podstádia: IA1 - neagresivní histologický typ bez invaze do myometria; IA2 - neagresivní histologický typ s invazí < 50 % myometria; IA3 – neagresivní histologický typ s invazí < 50 % myometria se současným postižením jednoho vaječníku. Nádory zařazené do stadia IB jsou neagresivní histologické typy bez průkazu podstatné lymfangioinvaze s invazí ≥ 50 % myometria. Stádium IC je vyhrazeno pouze pro nádory omezené na polyp nebo na endometrium agresivních histologických typů, tzn. high-grade (HG, grade 3) endometroidní a non-endometriodní karcinomy (serózní, světlobuněčný, nediferencovaný, karcinosarkom, mezonefrický typ, mucinózní gastrointestinální typ).
Komentář
U pacientek s postižením endometria i ovaria byl v minulosti kladen velký důraz na rozlišení mezi metastázami a dvěma synchronními primárními karcinomy endometria a ovaria. Podle recentních studií je původ souběžného LR (low-risk, nízce rizikového) endometroidního karcinomu endometria a ovaria v naprosté většině případů ze shodné klonální buněčné linie, což naznačuje, že se primární tumor z endometria sekundárně šíří na ovarium (7,10,11). Tyto pacientky se zařazují do nového stadia IA3 při splnění následujících kritérií: 1) LG endometroidní karcinom; 2) myometriální invaze <50 %; 3) není přítomna podstatná LVSI; 4) nejsou přítomny jiné metastázy; 5) nádor je omezený pouze na jeden vaječník a není přítomna invaze/porušení pouzdra (ekvivalent pT1a). Při postižení obou ovarií nebo nesplnění ostatních kritérií by karcinomy měly být klasifikovány jako Stádium IIIA1 (metastáza karcinomu endometria do vaječníků). To je rozdíl od doposud obecně používané verze FIGO 2009, kde tato kategorie vyčleněna není. Také WHO klasifikace nádorů ženského genitálu z roku 2020 nedefinuje postižení jednoho ovaria jako závazný parametr a existují případy, kdy mohou být postižena obě ovaria a přesto se jedná o lézi biologicky indolentní (12). Zvláště problematické se jeví klasifikovat jako metastatické onemocnění incipientní LG endometroidní karcinom (bez invaze nebo s minimální invazí) a s oboustrannými ovariálními LG nádory vzniklými v borderline tumorech.
Stádium II
Stádium II původně zahrnovalo všechny karcinomy endometria s infiltrací do stromatu děložního hrdla, nyní musí být splněna alespoň jedna ze tří podmínek: 1/ invaze do stromatu děložního hrdla bez extrauterinního šíření nebo 2/ přítomnost podstatné LVSI u neagresivního histologického typu nebo 3/ agresivní histologický typ s invazí do myometria. Stádium IIA nově zahrnuje nádory s neagresivním histotypem bez podstatné LVSI, které infiltrují stroma děložního hrdla. Stádium IIB nyní představují případy s neagresivním histotypem, ale s přítomností podstatné LVSI bez nebo s infiltrací do myometria jakékoliv hloubky a/nebo s infiltrací do stromatu hrdla (neagresivní histotyp bez podstatné LVSI a bez invaze do myometria odpovídá stádiu IA, s invazí do myometria stádiu IB a s invazí do stromatu hrdla stádiu IIA). Stádium IIC je vyhrazeno pro agresivní histologické typy s infiltrací do myometria a/nebo do stromatu hrdla (agresivní histotyp bez invaze do myometria odpovídá stádiu IC).
Komentář
Do stadia II patří nově některé nádory omezené pouze na endometrium a také nádory s infiltrací stromatu děložního hrdla. Díky těmto změnám se počet pacientek s karcinomem endometria ve stádiu II pravděpodobně zvýší. Na druhou stranu, při retrospektivní analýze, která srovnávala PFS (progression-free survival, přežití bez progrese) u pacientek s karcinomem endometria podle stagingových systémů FIGO 2009 a 2023, byl 5letý PFS u pacientek ve stádiu II (na rozdíl od stadia I) v obou skupinách srovnatelný (70,2 % vs. 71,2%) (13).
Stádium III
Základní definice stádia III zůstala beze změny: lokální a/nebo regionální šíření nádoru jakéhokoliv histologického typu. Stádium IIIA nově rozlišuje mezi infiltrací adnex (IIIA1) a děložní serózy (IIIA2). Stádium IIIB1 udává postižení pochvy a/nebo parametrií, což odpovídá předchozímu stádiu FIGO 2009 IIIB. Postižení pánevní pobřišnice je nyní klasifikováno jako IIIB2 (předchozí stádium FIGO 2009 IVB). Stádium IIIC s identickou definicí pro staging FIGO 2009 i FIGO 2023 (metastáza do pánevních a/nebo paraaortálních lymfatických uzlin) nově rozlišuje mikrometastázy (IIIC1i, IIIC2i) a makrometastázy (IIIC1ii, IIIC2ii) do lymfatických uzlin.
Komentář
Nádorové postižení vejcovodu se vždy řadí do stádia IIIA1, na rozdíl od LR endometroidních karcinomů se synchronním postižení endometria a jednoho ovaria (viz stádium IA3). U serózního karcinomu by se mělo vždy odlišit sekundární postižení vejcovodů od paralelní přítomnosti primárního serózního intraepiteliálního karcinomu vejcovodu (STIC). V těchto případech je vhodné vyšetřit tuby histologicky podle protokolu SEE-FIM, a také imunohistochemicky (7). Přítomnost volných fragmentů tumoru uvnitř vejcovodu je kontroverzní a není rozhodující pro stanovení stádia. Totéž platí pro pozitivní cytologii z laváže (7). Rozlišení postižení uzlin na makrometastázy (velikost > 2 mm) a mikrometastázy (0,2 – 2 mm a/nebo počet > 200 postižených buněk) v souladu s přístupem přijatým AJCC (American Joint Committe on Cancer, Americký společný výbor pro malignity) výrazně zpřesní prognózu. Změna vyjadřuje lepší prognózu u pacientek s mikrometastázami do lymfatických uzlin (5,7). Prognostický význam ITC (isolated tumour cells, izolované nádorové buňky) zůstává nejasný a nepovažuje se za metastázu (pN0(i+)) (7).
Stádium IV
Základní definice stádia IV se nemění (postižení sliznice močového měchýře a/nebo střeva nebo vzdálené metastázy), bylo ale přidáno další podstádium pro pacientky s peritoneálními metastázami nad úrovní pánve (stádium IVB), pacientky s peritoneálním postižením v oblasti pánve patří do stádia IIIB2. Stádium IVC znamená přítomnost vzdálených metastáz.
Komentář
Peritoneální karcinomatóza (nově stádium IIIB2) je relativně vzácná (přibližně u 2 % ze všech pacientek s karcinomy endometria) a tyto pacientky je třeba odlišit od pacientek se vzdálenými metastázami, protože na rozdíl od karcinomu endometria ve stádiu IV jsou většinou indikovány k primární operační léčbě (5,7,14). Při postižení lymfatických uzlin zůstává hranice mezi stádiem III a IV identická. Jako vzdálené metastázy se hodnotí postižení lymfatických uzlin nad úrovní odstupu renálních cév a/nebo jakýchkoliv extraabdominálních lymfatických uzlin.
Staging FIGO 2023 s molekulární klasifikací
Molekulární vyšetření umožňuje klasifikovat karcinom endometria do čtyř prognostických skupin: POLEmut, MMRd, NSMP a TP53mut (2,5,7,15).
1. POLEmut (inaktivace DNA polymerázy ε POLE); typický je velký počet somatických mutací (tzv. ultramutované endometriální karcinomy). Zastoupení této skupiny v karcinomech endometria se pohybuje mezi 6–12 % (2,16–18).
2. MMRd (mismatch repair deficient, synonymum mikrosatelitově instabilní); zahrnuje karcinomy s mikrosatelitovou nestabilitou (MSI) s vysokým počtem mutací (tzv. hypermutované endometriální karcinomy). Zastoupení těchto karcinomů se odhaduje na 30–35 % (2,16–18).
3. NSMP (no specific molecular profile); tyto endometriální karcinomy s nespecifickým molekulárním profilem vykazují nízký počet somatických alterací s nízkým počtem variací kopií genů (copy number variation (CNV) low, somatic copy - -number alteration low, SCNA-low). Tato skupina je největší (30–60 %), geneticky velmi heterogenní a výhledově bude nejspíše dále rozčleněna (2,16–19). Do této skupiny se také řadí endometriální karcinomy s mutací β-cateninu, z kterých část má zřejmě horší prognózu (20).
4. TP53mut (mutace/abnormalita genu TP53, označovaná také jako p53abn nebo p53mut); kromě definující aberace genu TP53 je přítomno vysoké množství početních změn genů (copy number high, somatic copy-number alteration high/ serous like, SCNA-high). Tyto nádory tvoří 12–25 % všech karcinomů endometria (2,16–18).
Podle doporučení CGA (The Cancer Genome Atlas) by pro správné vyhodnocení molekulární klasifikace měly být provedeny alespoň tři imunohistochemické markery (p53, MSH6 a PMS2) a jeden molekulární test (analýza patogenních POLE mutací), provedení pouze jednoho testu je nedostatečné (16–19). Stádium I a II se mění pouze při průkazu POLEmut (IAmPOLEmut) nebo TP53mut (IICmp53abn), při průkazu MMRd nebo NSMP se FIGO stádium nemění (tab. 1). Stádia III a IV zůstávají zachována i při průkazu kteréhokoliv markeru molekulární klasifikace, ale výsledek by měl být vždy do stádia zaznamenán pro účely sběru a vyhodnocování dat (např. IA3mMMRd, IIBmNSMP, IIIA2mPOLEmut, IVCmp53abn a podobně). Pokud bylo molekulární testování provedeno, označení stádia by se vždy mělo doplnit písmenem „m“ (např. IA3m nebo IVCm). Pokud není výsledek molekulární analýzy k dispozici, stádium by mělo být přiřazeno podle tradičních histopatologických kritérií, která zůstávají důležitými prognostickými parametry k indikaci adjuvantní terapie (5,7). V České republice se molekulární vyšetření podle společného doporučení českých odborných společností provádí vždy na žádost klinika z Komplexního onkologického centra (KOC) či Onkogynekologického centra a doporučuje se testovat až po vyšetření definitivního resekátu, nikoliv hned v rámci odběru biopsie (materiál z diagnostického odběru však může být také použit) (15).
Kontroverze stagingového systému FIGO 2023
Začlenění výsledků molekulární klasifikace je hlavní, nejdiskutovanější a tím i nejkontroverznější změnou nového stagingového systému. Molekulární klasifikace karcinomu endometria a její klinický význam se velmi rychle vyvíjí, což by mohlo v budoucnu vést k určitým rozporům a zapříčinit relativně rychlou neaktuálnost současného stagingového systému FIGO 2023 (5,7,21–23). Integrace molekulární klasifikace do stagingu FIGO 2023 není ani podpořena výsledky prospektivních studií. Navíc, metodika stanovení molekulárního subtypu není v aktualizaci FIGO z roku 2023 specifikována, což může způsobit rozdíly v interpretaci výsledků mezi laboratořemi. Na druhou stranu, WHO podrobně specifikovala a schválila metodiku provádění imunohistochemie (12). Na základě současných důkazů se jako preferovaný přístup jeví kombinace imunohistochemie (IHC) a samostatného vyšetření POLE (2,5,7,15–19,21). Výsledky testování POLE mutací metodou PCR však nejsou optimální a vykazují v 5-10 % případů diskrepantní výsledky. Nicméně podle závěrů recentních studií může tento problém vyřešit využití sekvenování nové generace (next-generation sequencing, NGS), pokud je k vyšetření poskytnut adekvátní vzorek nádorové tkáně (24). Zavedení nových sekvenčních panelů NGS pro rozšíření testování POLE mutací poskytlo na jedné straně informace o nových patogenních nebo pravděpodobně patogenních POLE mutacích, ale na druhé straně identifikovalo nové varianty neznámého významu. V současnosti je známo dvanáct mutací genu POLE, které jsou prokazatelně patogenní (25). Toto spektrum se bude nepochybně dále rozšiřovat. Rozdíl mezi patogenní a nepatogenní POLE mutací nemusí být v budoucnosti jednoznačný. Nepatogenní POLE mutace se díky vysoké mutační zátěži nacházejí většinou ve skupině hypermutovaných MMRd nádorů jako sekundární genetická událost a biologické chování je v souladu s charakteristikou této skupiny. Vzhledem k tomu, že pozitivní výsledek POLE mutace mění stádium onemocnění a tím i indikaci adjuvantní terapie, je znalost jednoznačných patogenních POLE mutací nezbytná pro správnou klasifikaci karcinomu endometria (21). Kromě vyšší citlivosti pro detekci POLE mutace přináší NGS možnost spolehlivější detekce mutací v genu TP53 a dalších potenciálně užitečných genetických alterací, například v heterogenní skupině NSMP karcinomů (26).
Podle některých expertů není imunohistochemické vyšetření p53 dokonalou náhradou průkazu mutačního stavu genu TP53 (27). Studie o ovariálních karcinomech prokázala, že při správné validaci má IHC s ohledem na detekci mutace TP53 100 % specificitu a 95,9 % senzitivitu (28). Na rozdíl od karcinomu ovaria však karcinom endometria může mít abnormální, většinou subklonální typ exprese, který je častý zejména u pacientek s MMRd nebo POLE mutací (28). Jako hranice pro subklonální imunohistochemické barvení je doporučována hodnota ≥10 %, protože tumory s hodnotou vyšší vykazují vyšší mortalitu (29). Pacientky s časným TP53mut karcinomem endometria jsou jediné ze čtyř molekulárních skupin, které mají prospěch z adjuvantní chemoradioterapie (18). Nesprávná klasifikace nádoru jako TP53mut má tedy pro pacientku významné negativní důsledky.
Jedním z problematických aspektů zůstávají také kritéria hodnocení a definice normálního a abnormálního typu exprese mikrosatelitní instability - imunohistochemického vyšetření exprese mismatch repair (MMR) proteinů. Výsledek MMRd sice nemění stádium onemocnění, ale měl by být u stadia uveden. V USA je abnormální exprese na doporučení CAP (College of American Pathologists) definována jako úplná ztráta exprese, tedy jakákoliv pozitivita bez ohledu na její rozsah a intenzitu je podle této definice normální. V praxi jsou však často používány hranice pozitivity s ohledem na její rozsah (obvykle jde o 5 %). Oproti tomu jiná doporučení, zejména britských gynekopatologů, doporučují zohledňovat nejen přítomnost exprese, ale i její rozsah a intenzitu ve srovnání s interní kontrolou (30).
Navíc, 3 až 6 % všech karcinomů endometria má více než jednu molekulární charakteristiku (označovanou jako „multiple classifier“) (16–19,23,31). Tyto karcinomy jsou vystaveny vyššímu riziku, že budou klasifikovány do jiné molekulární skupiny s odlišným odhadem prognózy. Nejběžnější je „dvojitý klasifikátor“ („double classifier“, např. POLEmut a TP53mut nebo MMRd a TP53mut), ale existují také „trojité klasifikátory“ („triple classifiers“, POLEmut a MMRd a TP53mut současně). V těchto případech je TP53mut sekundárním projevem ultramutovaného stavu u POLE mutace nebo v rámci mikrosatelitní nestability u MMRd. Prognóza těchto nádorů se pak odvíjí od mutace POLE nebo MMRd a podle toho je přiřazeno příslušné stádium (15,31). Pacientky s karcinomem endometria ve stádiu I asociovaným pouze s TP53mut vykazovaly 5leté přežití bez recidivy v 70,8 % na rozdíl od pacientek ve stejném stádiu s MMRd-TP53mut (92,2 %, p=0,024) a POLEmut-TP53mut (94,1 %, p=0,050) (18). Autoři jiné prospektivní studie s délkou sledování 24,7 měsíce uvádějí, že „multiple classifier“ karcinomy endometria mají potenciál chovat se agresivně, a jejich kategorizace jako POLEmut s deeskalací léčby proto nemusí být bezpečná (23). K podobnému závěru dospěla také skupina plzeňských autorů v jejich recentní studii na kohortě 270 pacientek. V daném souboru byly celkem 4 případy s POLEmut klasifikovány jako „multiple classifier“ a 3 z nich se chovaly agresivně (32). Toto ale nepotvrdila nedávná kohortová studie, ve které nebyla u žádné „multiple classifier“ pacientky s karcinomem endometria potvrzena recidiva onemocnění, pokud byla přítomna i POLEmut (33). Během sledování po dobu 17 měsíců nebyla u 15 pacientek s POLEmut-TP53mut, u 2 pacientek s POLEmut-MMRd a u 3 pacientek s POLEmut-MMRd-TP53mut zaznamenána žádná recidiva na rozdíl od 7,1 % (2/28) případů s „double classifier“ MMRd-TP53mut za 5 a 7 měsíců po operaci. Navíc, pacientky asociované pouze s MMRd zrecidivovaly ve 4,0 % (4/99) a pacientky asociované pouze s TP53mut dokonce ve 34,2 % (25/73) případů s mediánem doby do recidivy 8–9 měsíců (33). V současnosti tedy existuje konsenzus, že patogenní mutace genu POLE je nadřazena nad ostatní abnormality a takové nádory by měly být klasifikovány jako POLEmut (15,18,31). V každém případě, k vyhodnocení prognostického významu více klasifikátorů jsou zapotřebí další kolaborativní prospektivní multiinstitucionální studie, protože současné výsledky jsou založeny na omezeném počtu pacientek.
Ačkoli molekulárního klasifikace není povinnou součástí nového stagingu FIGO 2023, její zařazení se zdá problematické z různých důvodů, včetně obtížné až nemožné dostupnosti
v mnoha chudších zemích světa. Kromě toho existují některé další imunohistochemické markery (hlavně exprese estrogenových (ER) a progesteronových receptorů (PR), které jsou cenově dostupnější a významně zlepšují prognózu (34), ale nebyly do stagingu FIGO 2023 ale ani do ESGO/ESTRO/ESP guidelines z roku 2021 zahrnuty. To prokázala např. prospektivní studie na 132 pacientkách s karcinomem endometria (35). Do předoperační stratifikace pacientek s nízkým nebo vysokým rizikem autoři vedle standardních kritérií (věk, stádium, histologický typ, grade, lymfovaskulární invaze) zahrnuli přítomnost některých imunohistochemických biomarkerů (L1CAM, ER, PR a p53). Využití imunohistochemických markerů významně zlepšilo senzitivitu pro stanovení vysoce rizikové skupiny (48,4 % vs. 75,8 %, p <0,001) se statisticky nevýznamným poklesem specificity na 80 % (p=0,238). Pozitivní prediktivní hodnota (PPV) byla pro obě metody podobná, zatímco negativní prediktivní hodnota (NPV) (tj. pravděpodobnost extrémně nízkého rizika u negativních testovacích případů) se statisticky významně zlepšila (66,0 % vs. 78,9 %, p < 0,001) (35). Jiná studie na 763 pacientkách s karcinomem endometria rovněž potvrdila, že abnormální exprese p53, L1CAM, ER nebo PR je významně spojena s vyšším rizikem. Navíc, negativita ER a PR (HR 2,74; 95 % CI 1,48–5,07; p=0,001) a průkaz TP53mut (HR 1,88; 95 %CI 1,00–3,51; p=0,048) měly významný vliv na přežití pacientek (36). V současnosti se často diskutuje i o prognostickém a prediktivním významu exprese onkoproteinu HER2 u pacientek s HG endometrioidními karcinomy, které by mohly profitovat z anti-HER2 cílené terapie. Retrospektivní analýza 143 pacientek s HG endometrioidním karcinomem ve stadiu FIGO III prokázala přítomnost HER2 exprese, resp. amplifikace genu HER2 až u 73 pacientek (51 %) (37).Další limitací nového stagingového systému karcinomu endometria FIGO 2023 je zahrnutí charakteristik, jejichž definice se stále vyvíjejí, a také charakteristik, které podléhají značné interobservační variabilitě při jejich hodnocení. Přítomnost podstatné LVSI hraje v prognóze nádoru významnou roli, a proto byl tento parametr do stagingu implementován (7,34,38,39). Problémem zůstává, že je používáno několik různých definic pro kvantifikaci LVSI. FIGO 2023, stejně jako WHO Classification of Female Genital Tumors (12) a ESGO/ESTRO/ESP guidelines (5) definují jako podstatnou (neboli extenzivní) LVSI při postižení ≥ 5 lymfovaskulárních struktur (fokální LVSI je při postižení < 5 cév, negativní LVSI je bez postižení cév). Jiné organizace ovšem využívají odlišné definice. NCCN (National Comprehensive Cancer Network) definuje jako podstatnou LVSI při postižení ≥ 4 lymfovaskulárních struktur na jednom řezu obarveném hematoxylin-eosinem (40) a organizacím ICCR (International Collaboration on Cancer Reporting) (41), ISGyP (The International Society of Gynecological Pathologists, Mezinárodní společnost gynekologických patologů) (42) a CAP (College of American Pathologists) (43), DGGG (Deutsche Gesellschaft für Gynäkologie und Geburtshilfe, Německá společnost pro gynekologii a porodnictví) a DKG (Deutsche Krebsgesellschaft, Německá společnost pro rakovinu) (44) postačuje k definici podstatné LVSI postižení pouze ≥ 3 cév (tab. 2). Většina definic (včetně FIGO 2023) také nespecifikuje, zda je rozsah LVSI založen na maximálním postižení v jednom tkáňovém řezu nebo na kumulativním postižení ve všech vyšetřených řezech postižené tkáně. Tato nejednoznačnost může vést k přidělení rozdílných stadií u onkologicky identických pacientek s odlišnými výsledky identické terapie (21).
Tab. 2. Definice pro diagnózu podstatné lymfangioinvaze podle jednotlivých odborných společností (5, 12, 35-39). 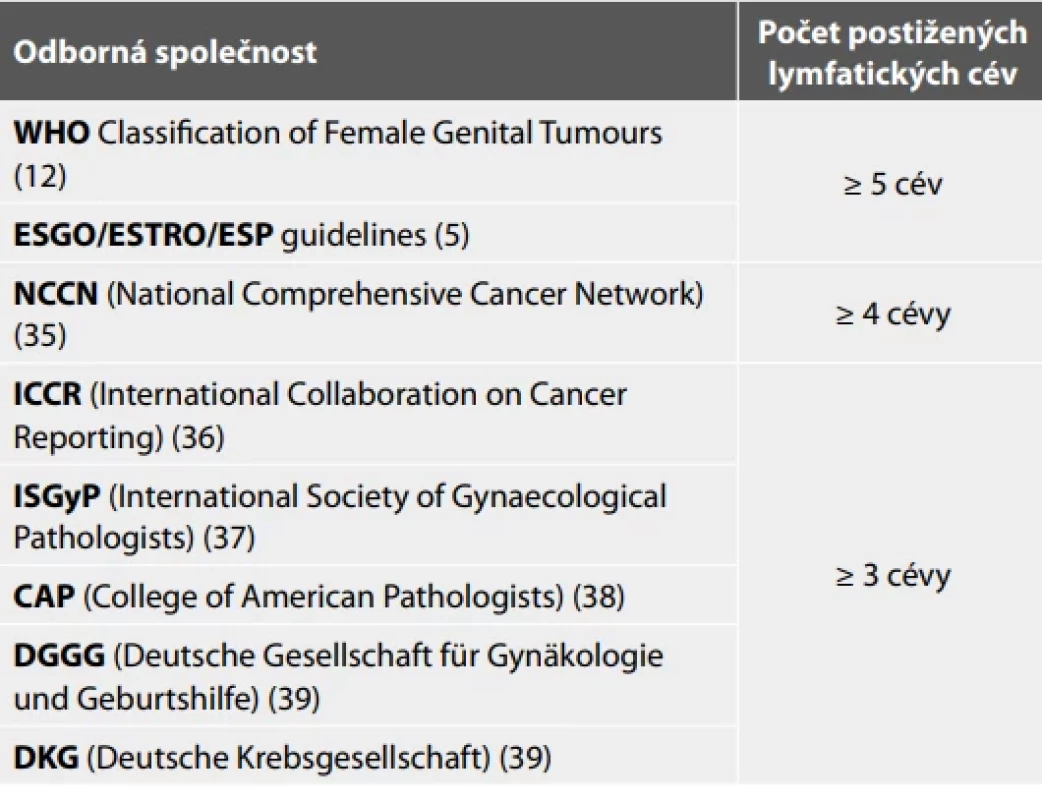
Dalším příkladem je obnovený požadavek na histologické rozlišení mezi nádorem omezeným na endometrium a nádorem s minimální invazí do myometria. Toto rozlišení je problematické zejména u neagresivních (low-grade endometrioidních) karcinomů. Přesné histologické zhodnocení je často obtížné pro přítomnost adenomyózy a nepravidelné rozhraní mezi endometriem a myometriem. V důsledku této limitace se může popis nádorové invaze do myometria mezi jednotlivými pracovišti značně lišit (21,42). Další otázkou je histopatologické určení nádorového postižení děložní serózy uvedené jako „uterine subserosa“ pro definici stadia IIIA2. ISGyP zahrnuje submezoteliální vazivovou tkáň jako součást definice serózní invaze (42). Definice subserózní (na rozdíl od serózní) invaze nemá jasně definovaná histopatologická kritéria a není zahrnuta v žádných odborných guidelines a ani v jiných zdrojových dokumentech a nelze ji jednoznačně interpretovat (21).
Mnoho implementovaných změn a doporučení je uvedeno bez jakýchkoliv citací na původní recenzovanou literaturu. Jako příklad lze uvést zařazení endometroidních karcinomu grade 3 do skupiny „agresivních“ histologických typů spolu s jinými non-endometroidními karcinomy, přestože se jedná o skupinu nádorů výrazně molekulárně a klinicky heterogenních. Tato stratifikace nemá zásadní oporu v citované literatuře a také ESGO/ ESTRO/ESP guidelines z roku 2021 oddělují endometroidní karcinom grade 3 od ostatních agresivních non-endometroidních karcinomů (5,21,45).
DISKUZE
Poslední změna systému stagingu karcinomu endometria byla přijata společností FIGO v roce 2008 a zveřejněna v roce 2009. O dva roky později byly podobné změny implementovány v systému TNM (8,9). Tradiční pojetí stagingového systému je založeno na popisu anatomického rozsahu onemocnění v době diagnózy na podkladě výsledků klinického, radiologického a případně histopatologického vyšetření. Stagingový systém FIGO 2023 je prezentován jako pokus o definování jednotlivých stadií s přesnější prognózou zahrnutím dalších důležitých prognostických faktorů, které prosté anatomické šíření nemůže definovat. Společná doporučení ESGO/ESTRO/ESP z roku 2021 jsou založena na stejném principu a kategorizují pacientky s karcinomem endometria do několika rizikových skupin (nízké, střední, středně vysoké a vysoké riziko). Definice rizikových skupin se liší podle toho, zda je znám výsledek molekulárního klasifikace nádoru (5).
Nový stagingový systém karcinomu endometria FIGO 2023 má oproti minulé verzi nesporně některé přednosti. Stagingový systém FIGO 2023 reflektuje, že karcinom endometria není jedno onemocnění. Neoddiskutovatelných faktem zůstává, že implementací nových histopatologických parametrů a výsledku molekulární klasifikace se výrazně zpřesní prognóza konkrétní pacientky v konkrétním stádiu (7,16–19). Srovnáním stagingových systémů FIGO 2009 a FIGO 2023 se zabývala mezinárodní studie tří evropských onkogynekologických center (13). V této studii všechny aplikované statistické testy potvrdily přesnější predikci PFS („progression-free survival“, období bez progrese) a OS („overall survival“, celkové přežití) pomocí stagingového systému FIGO 2023 ve srovnání s FIGO 2009 (13). Při retrospektivní analýze 519 pacientek s karcinomem endometria byl prokázán významně vyšší 5letý PFS ve stádiu I podle stagingového systému FIGO 2023 ve srovnání s FIGO 2009 (93,0 % vs. 87,4 %). Dvě nová molekulárně definovaná podstádia IAmPOLEmut a IICmp53abn podle 2023 FIGO vykazovala zcela odlišné onkologické výsledky (13).
Výsledek molekulární klasifikace umožňuje definovat pacientky s vynikající (POLEmut) a špatnou prognózou (TP53mut) (2,5,7,17,18). Jedná se o nejvýznamnější posun v diagnostice a léčbě karcinomů endometria za posledních 10 let (7). Testování MMRd také představuje u pokročilých nádorů prediktor imunoterapie pomocí tzv. check point inhibitorů a je důležité i s ohledem na roli ve screeningu Lynchova syndromu, který ale není v současnosti v ČR organizován (15).
Navíc, provedení molekulární klasifikace je u všech pacientek s karcinomem endometria v běžné praxi v českých podmínkách proveditelné a neprodlužuje dobu nutnou pro rozhodnutí o adjuvantní terapii (46). Vzhledem k časné symptomatologii jsou téměř dvě třetiny pacientek s karcinomem endometria diagnostikovány v časných stádiích s možností primární chirurgické léčby a pouze relativně malá část pacientek je poté indikována k adjuvantní terapii, někdy na základě pouze výsledků molekulární klasifikace (2,7,17,18,40,44,45). Molekulární klasifikace má zvláště význam u agresivních histologických typů. Nejvíce profituje z molekulární klasifikace high-grade endometroidní karcinom, protože se jedná o klinicky, molekulárně a prognosticky velmi heterogenní onemocnění (45). Bez molekulární klasifikace nelze HG endometroidní karcinom endometria stratifikovat do správné rizikové skupiny. Pacientky s karcinomy skupiny POLEmut významně profitují z redukce pooperační adjuvantní radioterapie ve smyslu eliminace nežádoucích účinků při zachování stejné prognózy (5,7,17,18,45). Na druhou stranu, podle našich zkušeností z klinické praxe někteří kliničtí onkologové mají problém spolehnout se výhradně na výsledek patogenní POLE mutace a indikují adjuvantní léčbu i u POLEmut karcinomů, které jsou podle jiných kritérií považovány za agresivní. Využití molekulární klasifikace pravděpodobně najde také uplatnění pro stanovení rizika nemoci v případě fertilitu zachovávajících postupů u mladých žen s karcinomem endometria splňujících předepsaná kritéria (47). Velká studie z České republiky zahrnula celkem 270 molekulárně klasifikovaných karcinomů endometria (23). Celkem 6,6 % (18/270) subjektů mělo POLE mutaci, 31,5 % (85/270) bylo MMRd, 11,1 % (30/270) mělo TP53 mutaci a 50,7 % (137/270) nemělo žádný specifický molekulární profil. Třináct případů (4,8 %) bylo klasifikováno jako „multiple classifier“ (23).
Mnohé změny byly přijaty odbornou veřejností pozitivně. Experti přivítali vytvoření stadia IA3 pro LR karcinom se synchronním postižením endometria a jednoho ovaria, protože tyto karcinomy mají dobrou prognózu, pokud není přítomna podstatná LVSI (7,10,19,38,39). Podle WHO klasifikace z roku 2020 (12) a také podle ESGO/ESTRO/ESP guidelines (5) se u těchto pacientek doporučuje konzervativní postup bez adjuvantní terapie (7,10,19,38,39). Naproti tomu, u agresivních typů nádoru (hlavně serózní karcinom), je velký rozdíl v prognóze pacientky mezi nádory omezené na polyp a nádory postihujícími i přilehlé endometrium (48,49). Vytvoření nových stadii IC a IIC (tab. 1) je tedy z tohoto pohledu odůvodněné. Také rozšíření definic stadií II, III a IV s přesnějším rozlišením různých typů šíření nádoru mimo dělohu a tím zpřesnění prognózy jednotlivých substádií byly přijaty odbornou veřejností vesměs příznivě. Stejně tak i rozlišení postižení uzlin na mikro - a makrometastázy v souladu s AJCC bylo dobře akceptováno (21,40–43). Různé techniky detekce sentinelové uzliny s podrobným histologickým vyšetřením pomocí ultrastagingu jsou dnes v České republice standardem (4,50,51).
V roce 2021 ISGyP provedla dotazníkový průzkum mezi členy ISGyP a International Gynecologic Cancer Society a získala odpovědi od 172 patologů a 135 onkogynekologů (52). Jen relativně málo otázek vyvolalo konsensuální odpověď, definovanou jako alespoň 75 % shodu. Konsensuální shody bylo dosaženo v rozlišení postižení uzlin na mikro a makrometastázy, definování kritérií pro rozdělení případů simultánního postižení děložního těla a karcinomu vaječníku a význam exprese LVSI jako nezávislého rizikového faktoru. Ale pouze polovina patologů (48 %) a 2/3 onkogynekologů (61 %) souhlasila s implementací výsledku LVSI do stagingového systému a podobnou podporu mělo také začlenění molekulární klasifikace (48 % patologů a 63 % onkogynekologů) nebo histologického typu nádoru (52 % patologů a 65 % onkogynekologů) do stagingu (52). Se změnami implementovanými do stagingového sytému FIGO 2023 tedy souhlasily přibližně dvě třetiny klinických onkologů, ale pouze polovina patologů. To odráží současné názory na staging karcinomu endometria FIGO 2023. Zatímco patologové mají tendenci staging FIGO 2023 kritizovat (21,27), většina klinických onkologů tyto změny přijala, i když mají připomínky a kladou doplňující otázky (53). Parametry potřebné ke stanovení konkrétního stadia s indikací vhodné terapie do značné míry závisí na histopatologických parametrech. Někteří experti se domnívají, že nedostatečné zastoupení patologické komunity s nemožností odborných společností formulovat své námitky byl hlavní nedostatek při návrhu stagingu FIGO 2023 (21).
Stanovení stádia podle systému FIGO 2023 se jeví příliš složité s nemožností přímého srovnání pacientek s karcinomem endometria podle stagingů FIGO 2009 a FIGO 2023 (27). Stagingový systém FIGO 2023 je velmi odlišný a komplikovanější než předchozí verze, což může výrazně ztížit jeho širší přijetí v regionech s různou úrovní zdravotní péče. Začlenění výsledků molekulárního klasifikace v podstatě vylučuje staging v oblastech s nedostatečnými zdroji. Tato limitace zásadně zkomplikuje sběr zdravotních dat pro klinické, epidemiologické a výzkumné účely, včetně provádění klinických studií (21). Stádium onemocnění se navíc může u jednoho pacienta změnit několikrát během relativně krátké doby. Podle histopatologického výsledku z hysterektomie může být například stanoveno stádium IIC (agresivní histologický typ s myometriální invazí), ale po kontrole v onkogynekologickém centru se výsledné stádium může změnit např. na IAmPOLEmut (průkaz patogenní POLE mutace). Je stále předmětem diskuse, zda by stádium onemocnění mělo být pomocnou složkou při výpočtu stratifikace rizika pacienta, nebo zda by stádium začleněním dalších prognostických parametrů mělo odrážet co nejpřesnější prognózu konkrétního pacienta. Fáze zpřesňování prognózy konkrétního stadia začleněním různých histopatologických a molekulárních proměnných stanovení tohoto stadia výrazně komplikuje. Celosvětově se proto jako lepší řešení jeví zachování definic jednotlivých stádií na základě anatomického šíření. Paradoxně náhlý přechod na úplný systém stagingu FIGO 2023, jak jej navrhuje FIGO, může bránit pokroku směrem k přesnější prognóze pro jednotlivá stadia (21,52).
ZÁVĚR
Nový stagingový systém pro karcinom endometria FIGO 2023 se výrazně liší od předchozích verzí, protože kromě tradičního anatomického rozsahu nádoru zahrnuje v definici jednotlivých stádií další histopatologické parametry a také molekulární klasifikaci nádoru. Tyto změny dále posílily roli patologa při určení stadia. Zahrnutí těchto parametrů významně zpřesnilo odhad prognózy konkrétní pacientky s přiřazeným stadiem. Na druhou stranu, stagingový systém FIGO 2023 je dosti složitý a vyžaduje nákladná vyšetření, což může způsobit problém při jeho rutinním používání v celosvětovém kontextu. Implementace stagingového systému pro karcinom endometria FIGO 2023 do každodenní praxe vyžaduje plné zapojení všech zúčastněných stran.
PODĚKOVÁNÍ
Práce byla podpořena Ministerstvem zdravotnictví České republiky [programový projekt, Gynekologicko-porodnická klinika Fakultní nemocnice Královské Vinohrady (č. NW24-09-00505) a koncepce rozvoje výzkumné organizace, Všeobecná fakultní nemocnice v Praze (VFN 00064165) a Fakultní Thomayerova nemocnice (FTN 00064190)] a programem Cooperatio č. 207035, Maternal and Childhood Care, Univerzity Karlovy v Praze.
PROHLÁŠENÍ
Autor práce prohlašuje, že v souvislosti s tématem, vznikem a publikací tohoto článku není ve střetu zájmů a vznik ani publikace článku nebyly podpořeny žádnou farmaceutickou firmou. Toto prohlášení se týká i všech spoluautorů.
Zdroje
1. Sung H, Ferlay J, Siegel RL, et al. Global Cancer Statistics 2020: GLOBOCAN Estimates of Incidence and Mortality Worldwide for 36 Cancers in 185 Countries. CA A Cancer J Clin 2021; 71(3): 209–249.
2. Presl J, Vaněček T, Michal M, et al. Molekulární klasifikace endometriálních karcinomů převedená do praxe. Ceska Gynekol 2021; 86(4): 258–262.
3. Krejčí D, Mužík J, Šnábl I, Gregor J, Komenda M, Dušek L. Portál epidemiologie novotvarů v ČR [online]. Masarykova univerzita, Brno, 2024. [cit. 2025-01-05]. Dostupný z: https://www.svod.cz.
4. Vinklerová P, Minář L, Weinberger V, Felsinger M, Koblížková M. Změna trendu operační léčby a stagingu lymfatických uzlin u karcinomu endometria – výsledky Onkogynekologického centra Gynekologicko-porodnické kliniky FN Brno a LF MU v letech 2012 – 2021. Ceska Gynekol 2022; 87(5): 308–316.
5. Concin N, Matias-Guiu X, Vergote I, et al. ESGO/ESTRO/ESP guidelines for the management of patients with endometrial carcinoma. Int J Gynecol Cancer 2021; 31(1): 12–39.
6. Koblížková M, Bretová P, Felsinger M, et al. Faktory zvyšující riziko malignity při nálezu endometriálního polypu v ultrazvukovém obraze. Ceska Gynekol 2024; 89(1): 44–51.
7. Berek JS, Matias‐Guiu X, Creutzberg C, et al. FIGO staging of endometrial cancer: 2023. J Gynecol Oncol 2023; 34(5): e85.
8. Creasman W. Revised FIGO staging for carcinoma of the endometrium. Int J Gynaecol Obstet 2009; 105(2): 109.
9. Sehnal B, Benková K, Kmoníčková E, et al. Současný staging zhoubných nádorů děložního těla a jeho význam pro klinickou praxi Cesk Patol 2014; 50(2): 100–105.
10. Anglesio MS, Wang YK, Maassen M, et al. Synchronous Endometrial and Ovarian Carcinomas: Evidence of Clonality. J Natl Cancer Inst 2016; 108: djv428.
11. Hájková N, Tichá I, Hojný J, et al. Synchronous endometrioid endometrial and ovarian carcinomas are biologically related: A clinico - -pathological and molecular (next generation sequencing) study of 22 cases. Oncol Lett 2019; 17(2) :2207–2214.
12. Cree IA, White VA, Indave BI, et al. Revising the WHO classification: female genital tract tumours. Histopathology 2020; 76(1): 151 - 156.
13. Schwameis R, Fanfani F, Ebner C, et al. Verification of the prognostic precision of the new 2023 FIGO staging system in endometrial cancer patients - An international pooled analysis of three ESGO accredited centres. Eur J Cancer Oxf Engl 2023; 193 : 113317.
14. Burg L, Timmermans M, van der Aa M, et al. Incidence and predictors of peritoneal metastases of gynecological origin: a population-based study in the Netherlands. J Gynecol Oncol 2020; 31: e58.
15. Dundr P, Cibula D, Doležel M, et al. Molekulární testování u karcinomu endometria (společné doporučení ČOS, onkogynekologické sekce ČGPS, SROBF a SČP ČLS JEP). Cesk Patol 2021; 57(3): 181–187.
16. Kandoth C, Schultz N, Cherniack AD, et al. Cancer Genome Atlas Research Network. Integrated genomic characterization of endometrial carcinoma. Nature 2013; 497(7447): 67–73.
17. Stelloo E, Nout RA, Osse EM, et al. Improved risk assessment by integrating molecular and clinicopathological factors in early-stage endometrial cancer-combined analysis of the PORTEC cohorts. Clin Cancer Res 2016; 22(16): 4215–4224. 18. León-Castillo A, de Boer SM, Powell ME, et al. Molecular classification of the PORTEC-3 trial for high-risk endometrial cancer: impact on prognosis and benefit from adjuvant therapy. J Clin Oncol 2020; 38(29): 3388–3397. 19. Piulats JM, Guerra E, Gil-Martín M, et al. Molecular approaches for classifying endometrial carcinoma. Gynecol Oncol 2017; 145(1): 200–207. 20. De Leo A, de Biase D, Lenzi J, et al. ARID1A and CTNNB1/β-Catenin Molecular Status Affects the Clinicopathologic Features and Prognosis of Endometrial Carcinoma: Implications for an Improved Surrogate Molecular Classification. Cancers (Basel) 2021; 13(5): 950.
21. McCluggage WG, Bosse T, Gilks CB, et al. FIGO 2023 endometrial cancer staging: too much, too soon? Int J Gynecol Cancer 2024; 34 : 138–143.
22. Dvořák O, Slavíčková M, Laco J, et al. DNA hypermetylace tumor supresorových genů TWIST1, GATA4, MUS81 a NTRK1 u hyperplázie endometria. Ceska Gynekol 2024; 89(4): 261–268.
23. Michalová K, Presl J, Straková-Peteříková A, et al. Výhody genetického sekvenování nové generace (NGS) v molekulární klasifikaci endometriálních karcinomů: Naše zkušenosti s 270 případy. Ceska Gynekol 2024; 89 : 349–359.
24. Smithgall MC, Remotti H, Hsiao SJ, et al. Investigation of discrepant mismatch repair immunohistochemistry and microsatellite instability polymerase chain reaction test results for gynecologic cancers using next-generation sequencing. Hum Pathol 2022; 119 : 41–50.
25. Cui J, Chen X, Zhai Q, et al. A novel somatic mutation in POLE exonuclease domain associated with ultra-mutational signature and MMR deficiency in endometrial cancer: a case report. Diagn Pathol 2023; 18 : 19.
26. Ondič O, Michalová K, Švajdler M, et al. Molecular substratification of endometrial carcinomas with no special molecular profile (NSMP) by using a limited NGS custom panel may facilitate effective patient selection for the PIK3CA-targeted therapy. Virchows Arch. In press 2024.
27. Espinosa I, D’Angelo E, Prat J. Endometrial carcinoma: 10 years of TCGA (the cancer genome atlas): A critical reappraisal with comments on FIGO 2023 staging. Gynecol Oncol 2024; 186 : 94–103.
28. Köbel M, Ronnett BM, Singh N, et al. Interpretation of P53 Immunohistochemistry in Endometrial Carcinomas: Toward Increased Reproducibility. Int J Gynecol Pathol 2019; 38 (Suppl 1): 123–131.
29. Huvila J, Thompson EF, Vanden Broek J, et al. Subclonal p53 immunostaining in the diagnosis of endometrial carcinoma molecular subtype. Histopathology 2023; 83(6): 880–890. 30. Dundr P, Němejcová K, Bártů M, et al. Význam imunohistochemických metod v diagnostice karcinomu endometria. Cesk Patol 2021; 57(2): 73–85.
31. León-Castillo A, Gilvazquez E, Nout R, et al. Clinicopathological and molecular characterisation of „multiple-classifier“ endometrial carcinomas. J Pathol 2020; 250 : 312–322.
32. Michalová K, Straková-Peteříková A, Ondič O, et al. Next-generation sequencing in the molecular classification of endometrial carcinomas: Experience with 270 cases suggesting a potentially more aggressive clinical behavior of multiple classifier endometrial carcinomas. Virchows Arch 2025; 487(1): 141-152.
33. De Vitis LA, Schivardi G, Caruso G, et al. Clinicopathological characteristics of multiple - -classifier endometrial cancers: a cohort study and systematic review. Int J Gynecol Cancer 2024; 34 : 229–238.
34. Visser NCM, van der Wurff AAM, IntHout J, et al. Improving preoperative diagnosis in endometrial cancer using systematic morphological assessment and a small immunohistochemical panel. Hum Pathol 2021; 117 : 68–78.
35. Weinberger V, Bednaříková M, Hausnerová J, et al. A novel approach to preoperative risk stratification in endometrial cancer: the added value of immunohistochemical markers. Front Oncol 2019; 9 : 265.
36. Vrede SW, van Weelden WJ, Visser NCM, et al. Immunohistochemical biomarkers are prognostic relevant in addition to the ESMO - -ESGO-ESTRO risk classification in endometrial cancer. Gynecol Oncol 2021; 161 : 787–794.
37. Abada E, Kim S, Jang H, et al. Human epidermal growth factor receptor-2 (HER2) expression in FIGO3 high-grade endometrial endometrioid carcinoma: Clinicopathologic characteristics and future directions. Gynecol Oncol 2024; 185 : 25–32.
38. Veade AE, Foote J, Ehrisman J, et al. Associations between lymphovascular space invasion, nodal recurrence, and survival in patients with surgical stage I endometrioid endometrial adenocarcinoma. World J Surg Oncol 2019;17(1): 80.
39. Tortorella L, Restaino S, Zannoni GF, et al. Substantial lymph-vascular space invasion (LVSI) as predictor of distant relapse and poor prognosis in low-risk early-stage endometrial cancer. J Gynecol Oncol 2021; 32(2): e11.
40. Abu-Rustum N, Yashar C, Arend R, et al. Uterine Neoplasms, Version 1.2023, NCCN Clinical Practice Guidelines in Oncology. J Natl Compr Canc Netw 2023; 21(2): 181–209.
41. Matias-Guiu X, Selinger CI, Anderson L, et al. Data Set for the Reporting of Endometrial Cancer: Recommendations From the International Collaboration on Cancer Reporting (ICCR). Int J Gynecol Pathol 2022; 41(Suppl 1): 90–118.
42. Singh N, Hirschowitz L, Zaino R, et al. Pathologic Prognostic Factors in Endometrial Carcinoma (Other Than Tumor Type and Grade). Int J Gynecol Pathol 2019; 38 (Suppl 1): 93–113.
43. Cancer Protocol Templates. College of American Pathologists (cap.org). 2023. Dostupné z: https://www.cap.org.
44. Emons G, Steiner E, Vordermark D, et al. Endometrial Cancer. Guideline of the DGGG, DKG and DKH. Part 1 with Recommendations on the Epidemiology, Screening, Diagnosis and Hereditary Factors of Endometrial Cancer, Geriatric Assessment and Supply Structures. Geburtshilfe Frauenheilkd 2023; 83 : 919–962.
45. Bosse T, Nout RA, McAlpine JN, et al. Molecular classification of grade 3 endometrioid endometrial cancers identifies distinct prognostic subgroups. Am J Surg Pathol 2018; 42(5): 561–568.
46. Bednaříková M, Hausnerová J, Minář L, et al. Molekulární testování karcinomu endometria – analýza prvních zkušeností z klinické praxe. Klin Onkol 2023; 36(3): 215–223.
47. Hejl Z, Hanáček J, Pilka R. Fertilitu zachovávající postupy u mladých žen s karcinomem endometria. Ceska Gynekol 2022; 87(3): 202 – 205.
48. Assem H, Rottmann D, Finkelstein A, et al. Minimal uterine serous carcinoma and endometrial polyp: a close clinicopathological relationship. Hum Pathol 2021; 118 : 1–8.
49. Dundr P. MONITOR aneb nemělo by vám uniknout, že... Cesk Patol 2022; 58(2): 72.
50. Michal M, Valha P, Velemínský M. Detekce sentinelové lymfatické uzliny u karcinomu endometria – porovnání účinnosti robotického a laparoskopického detekčního systému. Ceska Gynekol 2023;88(3):157–161.
51. Brych O, Drozenová J, Pichlík T, et al. Předoperační a pooperační staging u karcinomu endometria - prospektivní studie. Ceska Gynekol 2024; 89(1): 5–10.
52. Kayraklioglu N, Katsakhyan L, Cohen PA, et al. Perceptions of Controversies and Unresolved Issues in the 2014 FIGO Staging System for Endometrial Cancer: Survey Results From Members of the International Society of Gynecological Pathologists and International Gynecologic Cancer Society. Int J Gynecol Pathol 2024; 43 : 242–252.
53. Betella I, De Vitis LA, Calidona C, et al. Letter to the editor-The new FIGO staging system for endometrial cancer: Is the paradigm shift clinically feasible? Int J Gynaecol Obstet 2024; 164 : 364–365.
Štítky
Patologie Soudní lékařství Toxikologie
Článek vyšel v časopiseČesko-slovenská patologie

2026 Číslo 1-
Všechny články tohoto čísla
- Testování exprese claudinu 18.2 u adenokarcinomu žaludku a gastroesofageální junkce: Současný stav a výhled do blízké budoucnosti
- Castlemanova choroba – jedno jméno, mnoho tváří
- Lymfatická tkáň v souvislostech: od nenápadných změn k zásadním diagnózám
- Přednosti a limitace nového stagingového systému karcinomu endometria FIGO 2023 z pohledu klinika a patologa
- Od archeologické brigády k americké rezidentuře: proč je patologie „nejlepší obor medicíny“
- Cílené profilování genové exprese jako nástroj pro diagnostické určení buněčného subtypu a prognostickou stratifikaci u difuzního velkobuněčného B-lymfomu
- Castleman-like lymfadenopatie u pacienta se smíšenou chorobou pojiva: kazuistika a přehled literatury
- EBV-asociovaná plazmocelulární varianta Castlemanovy choroby: více než deset let trvající diagnostická odysea – kazuistika pacienta
- MONITOR, aneb nemělo by vám uniknout, že…
- Česko-slovenská patologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Castlemanova choroba – jedno jméno, mnoho tváří
- Testování exprese claudinu 18.2 u adenokarcinomu žaludku a gastroesofageální junkce: Současný stav a výhled do blízké budoucnosti
- Přednosti a limitace nového stagingového systému karcinomu endometria FIGO 2023 z pohledu klinika a patologa
- Cílené profilování genové exprese jako nástroj pro diagnostické určení buněčného subtypu a prognostickou stratifikaci u difuzního velkobuněčného B-lymfomu
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Revma Focus: Spondyloartritidy
nový kurz
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Autoři: prof. MUDr. Pavel Horák, CSc., doc. MUDr. Ludmila Brunerová, Ph.D., doc. MUDr. Václav Vyskočil, Ph.D., prim. MUDr. Richard Pikner, Ph.D., MUDr. Olga Růžičková, MUDr. Jan Rosa, prof. MUDr. Vladimír Palička, CSc., Dr.h.c.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



