-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
EBV-asociovaná plazmocelulární varianta Castlemanovy choroby: více než deset let trvající diagnostická odysea – kazuistika pacienta
EBV-associated plasmacytic variant of Castleman disease: more than a decade-long diagnostic odyssey – a case report
Background: Castleman disease is a rare and heterogeneous lymphoproliferative disorder with variable clinical presentation. The plasma cell variant, particularly when associated with Epstein–Barr virus (EBV), is uncommon and diagnostically challenging. We present a complex and long-lasting case of EBV-associated plasma cell variant Castleman disease with fluctuating systemic symptoms, multiorgan involvement, and delayed definitive diagnosis.
Case presentation: A 35year old man (born 1974) first presented in 2009 with high-grade fever, diarrhea, elevated inflammatory markers, hepatomegaly and biochemical signs of liver injury. Initial findings were attributed to rotavirus infection. Over the following years, he developed recurrent episodes of fever, night sweats, fatigue, arthralgias, hepatosplenomegaly, lymphadenopathy, and progressive laboratory abnormalities including persistent elevation of CRP, leukocytosis, hyperfibrinogenemia and polyclonal hypergammaglobulinemia. Extensive diagnostic workup repeatedly ruled out infectious, rheumatologic and malignant causes. Imaging eventually demonstrated retroperitoneal lymphadenopathy, hepatosplenomegaly, spinal lesions (Th5 – Th8), narrowing and occlusion of the inferior vena cava, and multiorgan inflammatory changes. Multiple biopsies (lymph nodes, spleen, liver, pancreas, bone lesions) initially showed only nonspecific reactive changes. Repeated PET/CT scans revealed multifocal FDG-avid lesions of low to moderate metabolic activity. In 2023, after multidisciplinary reassessment, lymph node tissue demonstrated EBV positivity in the absence of peripheral viremia, leading to a diagnosis of EBV-associated plasma cell variant Castleman disease. The patient was initiated on targeted therapy. During the third-line treatment, a sustained clinical and laboratory remission was achieved.
Conclusion: This case illustrates the diagnostic complexity of EBV-associated plasma cell variant Castleman disease, especially when presenting with longstanding systemic inflammation, nonspecific multiorgan involvement, and repeatedly inconclusive histopathology. Early consideration of Castleman disease in chronic inflammatory syndromes with lymphadenopathy may reduce diagnostic delay and improve outcome.
Keywords:
lymphadenopathy – Castleman disease – case report – chronic inflammation – plasma cell variant – EBV-associated lymphoproliferative disorder
Autoři: Ivanna Boichuk; Zdeněk Adam
Působiště autorů: Interní hematologická a onkologická klinika LF MU a FN Brno
Vyšlo v časopise: Čes.-slov. Patol., 62, 2026, No. 1, p. 58-61
Kategorie: Původní práce
Souhrn
Úvod: Castlemanova choroba (CD) je vzácné a klinicky heterogenní lymfoproliferativní onemocnění. Plazmocelulární varianta, zvláště asociovaná s EBV, představuje diagnostickou výzvu.
Kazuistika: Popisujeme případ 35letého muže (nar. 1974), u něhož se v roce 2009 objevily febrilie, průjem, hepatomegalie a zvýšené jaterní enzymy. Nálezy byly původně uzavřeny jako rotavirová infekce. V následujících letech pacient opakovaně trpěl subfebriliemi, artralgiemi, postupnou lymfadenopatií, hepatosplenomegalií, zvýšenými zánětlivými markery a variabilními orgánovými projevy. Po řadě hospitalizací, opakovaných zobrazovacích a histologických vyšetření, která byla dlouho nespecifická, byla teprve v roce 2023 na základě přítomnosti EBV v uzlinách (při negativitě v periferní krvi) stanovena diagnóza EBV-asociované plazmocelulární varianty Castlemanovy choroby. Pacient byl následně léčen cílenou terapií a při třetí linii léčby dosáhl klinické a laboratorní remise.
Závěr: Tento případ dokumentuje extrémně komplikovaný diagnostický proces u plazmocelulární Castlemanovy choroby s atypickým průběhem a víceetážovým orgánovým postižením. Včasné pomyšlení na CD u pacientů s chronickým zánětlivým syndromem a lymfadenopatií může vést ke zkrácení diagnostického prodlení a ovlivnit prognózu.
Klíčová slova:
Castlemanova choroba – kazuistika – lymfadenopatie – plazmocelulární varianta – EBV – chronický zánětlivý syndrom
EBV-asociovaná forma Castlemanovy choroby je vzácná a může imitovat infekční, autoimunitní i maligní onemocnění (1,2). Diagnostika vyžaduje opakované histologické ověření, korelaci s klinickým stavem a vyloučení diferenciálních diagnóz (2,3). Castlemanova choroba (Castleman disease, CD) představuje vzácný, nejednotný a klinicky vysoce variabilní syndrom charakterizovaný benigní, avšak často systémovou lymfoproliferací (2-4). Podle klasifikace se rozlišuje unicentrická (UCD) a multicentrická forma (MCD), přičemž MCD má dramaticky širší spektrum klinických projevů a horší prognózu (3,4). Plazmocelulární varianta, často provázená výraznou systémovou zánětlivou aktivitou, patří k nejkomplexnějším diagnostickým jednotkám v hematopatologii (2,3).
Předkládáme případ více než deset let trvajícího diagnostického procesu u pacienta s postupně rozvíjející se plazmocelulární CD, jejíž definitivní diagnóza byla možná až při prokázání EBV v uzlinách v roce 2023.
Obr. 1. 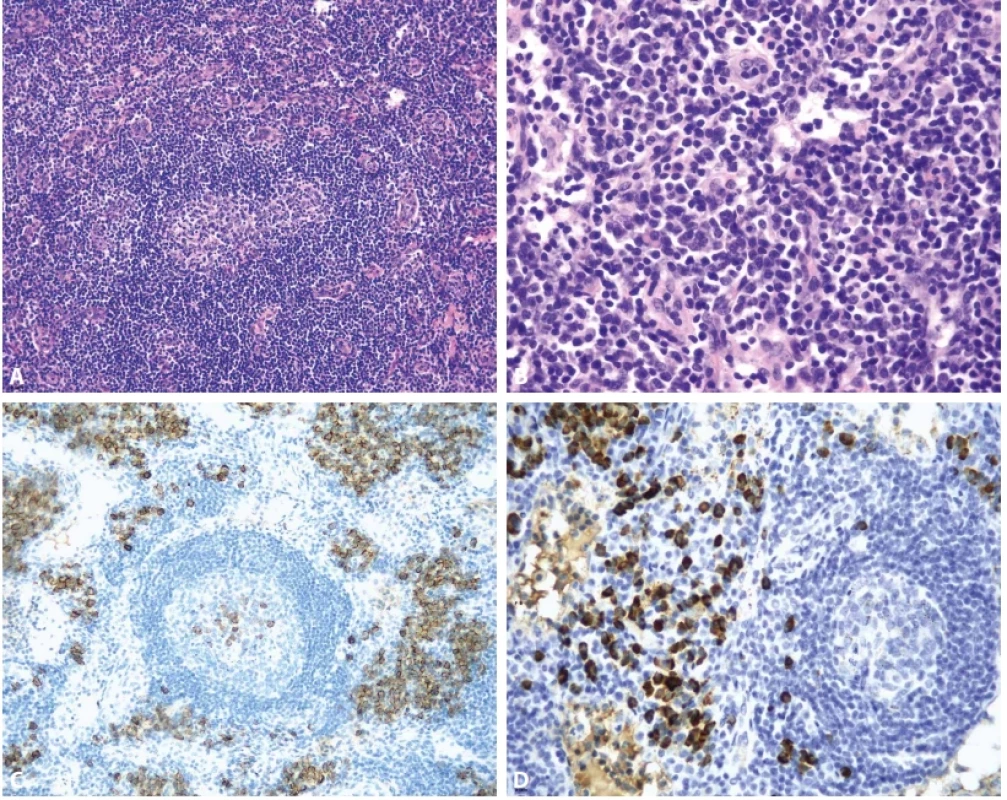
Histopatologické změny v lymfatické uzlině Smíšené změny s regresivně změněným naznačeně zdvojeným zárodečným centrem, zvýšenou vaskularitou interfolikulární oblasti (A - hematoxylin-eosin, 100x) a s plachtovitou plazmocytózou (B - hematoxylin-eosin, 400x). Interfolikulárně zmnožené plazmocyty jsou pozitivní v imunohistochemickém průkazu CD138 (C, zvětšení 100x), bez známek restrikce lehkých řetězců imunoglobulinů, zde pozitivita v průkazu kappa (D, zvětšení 200x), lambda není zobrazena. (Fotodokumentace MUDr. Kateřina Kamarádová Ph.D., Fingerlandův ústav patologie, FN Hradec Králové) POPIS PŘÍPADU
Počáteční obtíže (2009)
Muž narozený v roce 1974 se poprvé dostavil k lékaři v březnu 2009 pro febrilie přes 38 °C a průjem. Obtíže přičítal interpersonální infekci od svého syna. Laboratorně byla při přijetí zjištěna elevace ALT a AST, CRP 118 mg/l, leukocytóza a fibrinogen 7,6 g/l. Vyšetření stolice prokázalo rotavirus. Klinicky byly přítomny petechie na hrudníku a obličeji, hyperemie sklér a hepatomegalie. Infekční hepatitidy, CMV, malárie, leptospiróza i střevní bakteriální patogeny byly vyloučeny. Pacient byl propuštěn s diagnózou středně těžké rotavirové infekce.
Rekurence obtíží (2009–2015)
V květnu 2009 se pacient znovu dostavil pro subfebrilie, zimnici a stěhovavé artralgie velkých kloubů. Trvala elevace CRP, ALT a leukocytózy. Proběhlo vyšetření očním lékařem, který popsal subakutní konjunktivitidu. Tehdy bylo poprvé vyjádřeno podezření na Reiterův syndrom, ale nebyla splněna kriteria. Pacient zahájil léčbu chlorochinem (Delagil), který vedl ke zlepšení stavu. Pro léčbu přetrvávajících obtíží jej užíval přibližně jeden rok, následně ho samovolně vysadil a po dobu čtyř let byl bez obtíží.
Progrese choroby (2015–2016)
Od dubna 2015 se opět objevily večerní subfebrilie. Samoléčba Delagilem již neměla efekt. Na břišní stěně se vytvořila podkožní žilní pleteň odpovídající caput medusae, nadměrné pocení a zimnice. CT trupu prokázalo retroperitoneální lymfadenopatii, hepatosplenomegalii, hemangiomy jater, cystu levé ledviny a stenózu dolní duté žíly. CT angiografie potvrdila neplnění dolní duté žíly kontrastní látkou (vzhledem k tomu že vyšetření proběhlo v zahraniční, nemáme k dispozici celý popis CT).
Pro podezření na malignitu proběhla splenektomie, resekce kaudy pankreatu, lymfadenektomie a biopsie jater. Pooperační průběh komplikován abscesem v lůžku sleziny. Histologie byla nespecifická, spíše reaktivní, bez známek malignity.
V říjnu 2015 CT prokázalo vlající trombus pravé femorální žíly, přetrvávající hepatomegalii a retroperitoneální lymfadenopatii. Hematolog doporučil suplementaci železa, kyseliny listové a methylprednisolonu – došlo ke zlepšení celkového stavu, avšak subfebrilie přetrvávaly.
Revmatolog pro rozvoj diabetu 1. typu vysadil kortikoidy a nasadil azathioprin, který byl po několika měsících pro neefektivitu a trvající febrilie ukončen.
CT v listopadu 2016 prokázalo nová ložiska v Th7–Th8, včetně osteolýzy Th8. Biopsie popsala pouze fragmenty chrupavčité tkáně, bez diagnostického přínosu. Vyšetření kostní dřeně ukázalo zvýšené množství malých lymfocytů a počáteční známky myeloproliferace, JAK2 byl negativní.
Relativní stabilizace a nové zhoršení (2017–2020)
Relativní stabilizace a nové zhoršení (2017–2020) Následně pacient propuštěn domu, v mezidobí podstoupil chirurgický zákrok pro paraproktitidu. Dále trvaly subfebrilie, ale nebyly až tak limitující.
V roce 2020 hospitalizace pro celkové zhoršení pacienta – subfebrilie, únava, zácpa, elevace CRP, FW alfa. Za hospitalizace proběhlo další došetření CT trupu 2/2020 - chronická segmentální okluze intrarenální části dolní duté žily, známky nefritidy pravé ledviny, kapilární hemangiomy SIV a SVII.
MR mozku: intrakraniálně bez známek patologie. Doplněno ECHO srdce a kolonoskopií, ale bez patologie. Při dimisi doporučeno Metotrexat 15mg tbl 1x za 3 měsice.
Výrazná systémová aktivita (2021–2023)
V roce 2021 se opět rozvinuly každodenní teploty, exantém na obličeji a trupu. Pacient opětovně absolvoval široké spektrum vyšetření. (poznámka: do roku 2022 celý diagnostický proces probíhal mimo ČR, od roku 2022 došetření v ČR). Na začátku roku 2022 došlo k progresi zhoršení celkového stavu, febrilie, únava, občas noční pocení, od srpna 2022 nově bolesti v zádech s maximální intenzitou v noci. Revmatologem byla navýšena dávka metotrexátu, přidány kortikoidy. Po zavedené léčbě pacient pociťoval úlevu, ale vzhledem k přítomnosti normocytární anemie a trombocytózy, polyklonální hypergamaglobulinemie bylo doporučeno ještě vyšetření hematologem. Následně hematologem indikováno doplnění CT hrudníku, kde byla popsána patologická lymfadenopatie v oblastí pravého podpaží, proběhla biopsie lymfatické uzliny, kde bez záchytu nádorových buněk, pouze reaktivní změny. Pacient nadále užíval analgetika s částečným efektem.
V lednu 2023 doplněno PET/CT, se závěrem: víceetážová patologická aktivita s nízkou metabolickou aktivitou (pravá axila, retroperitoneum, parailicky), uzlina v zadním mediastinu s intenzivní aktivitou, patologický infiltrát v pravé axile kolem cévního svazku, patologická infiltrace obou ledvin, patologické ložisko Th5 (SUV max 6,82) (5).
Vzhledem k tomu, že pacient pořád měl bolesti zad a byla přítomna patologická infiltrace Th5, proběhla diagnostická biopsie pod CT kontrolou z Th5, která byla bohužel nevýtěžná (5,6).
Laboratorně nadále trvá elevace zánětlivých parametrů, hepatopatie, elevace interleukinu 6, nespecifická aktivita ANA protilátek, vyloučeno infekční onemocnění (hepatitidy, HIV, negativní CMV a EBV). Proto po kolektivní rozvaze pacient podstoupil opakovanou biopsii axilární uzliny vpravo se závěrem: nález nespecifický, mírná folikulární hyperplázie s reaktivní sinusovou histiocytózou a plazmocytózou, v dif. dg. revmatoidní lymfadenopatie, plazmocelulární Castlemanova nemoc nevyloučena (2,3). Revmatologem bylo vyloučeno systémové onemocnění pojiva.
Proběhlo druhé čtení histologie, kde průkaz EBV pozitivity v lymfatické tkání (při negativitě v periferní krvi). Po korelaci klinického, radiologického a laboratorního obrazu byla stanovena diagnóza: EBV-asociovaná plazmocelulární varianta multicentrické Castlemanovy choroby (MCD) (2-4).
Léčba a stav pacienta
Od roku 2023 je pacient léčen na našem pracovišti. 1. linie léčby – kombinace Rituximabu (antiCD20 protilátky) a Cyklofosfamidu od 5/2023. Pacient tuto léčbu toleroval dobře, ale týden po podání Rituximabu už měl subfebrilie, také pozoroval zmenšení lymfatické uzliny v pravé axile. Po podání 4 cyklu léčby efekt hodnoceno jako progrese, potvrzeno i dle PET/CT.
2. linie léčby – podání Kineretu (inhibitor interleukinu 1) od 9/2023, léčba podávána denně formou podkožní injekce. Klinicky se pacient cítil dobře, několikrát do týdne měl zvýšenou teplotu, rezistence v oblasti pravé axily zůstávala stacionární. V červnu 2024 nově hmatná rezistence v oblasti levého nadklíčku.
3. linie léčby – podán Siltuximab (inhibitor interleukinu 6), léčba podávána původně á 2 týdny, po 4 měsících léčby již v režimu á 21 dní. Již od začátku léčby ústup teplot, zmenšení až postupné vymizení hmatných periferních uzlin, laboratorně normalizace zánětlivých parametrů. Doplněno kontrolní PET/CT 12.2.2025: parciální regrese sledovaných patologických Infiltrátů a LU v oblasti pravé axily a subpektorálně. Kompletní morfometabolická regrese LU v podkoží pravé lopatky. V této léčbě pacient pokračuje doposud, nemá žádné potíže. Má dobrou kvalitu života. Laboratorní hodnoty jsou v normě.
DISKUZE
Tento případ představuje mimořádně obtížnou diagnostickou situaci, způsobenou: relativní vzácností onemocnění, nespecifickými projevy (které imitují infekce, autoimunitní choroby či malignity), opakovaně nediagnostickými biopsiemi, kolísavým průběhem s obdobími relativní stabilizace (1,2,4).
Plazmocelulární varianta Castlemanovy choroby bývá spojena se systémovou zánětlivou aktivitou, vysokými hladinami CRP, hypergammaglobulinémií a multiorgánovým postižením (2,3). Histologicky jde o proliferaci folikulů s nápadnou plazmocelulární infiltrací v interfolikulární oblasti (3). EBV-asociace je vzácnější, ale může hrát zásadní roli v patogenezi (2).
Diagnostické prodlení v našem případě přesáhlo 13 let, což v literatuře není běžné, avšak je u CD popsáno v případech s atypickým nebo slabě vyjádřeným histologickým profilem (4). PET/ CT bývá užitečné k určení nejaktivnějšího ložiska, nicméně ani opakované biopsie nemusí být průkazné (5).
Tento případ ukazuje nutnost opakovaného klinicko-patologického přehodnocení a mezioborové spolupráce. Prokázání EBV v uzlině bylo klíčové pro stanovení finální diagnózy.
ZÁVĚR
Předkládaná kazuistika ukazuje mimořádně komplexní průběh EBV-asociované plazmocelulární Castlemanovy choroby. Prodloužené diagnostické období vyplývalo z nespecifických projevů a opakovaně nediagnostických biopsií. Teprve kombinace PET/CT, histopatologické revize a detekce EBV umožnila stanovit správnou diagnózu. Pacient dobře odpověděl na cílenou léčbu a je v dlouhodobé remisi.
PODĚKOVÁNÍ
Podpořeno projektem BBMRI-CZ LM2023033, programem Cooperatio, vědní oblasti DIAG a projektem MZ ČR – RVO (FNHK, 00179906).
PROHLÁŠENÍ
Autor práce prohlašuje, že v souvislosti s tématem, vznikem a publikací tohoto článku není ve střetu zájmů a vznik ani publikace článku nebyly podpořeny žádnou farmaceutickou firmou. Toto prohlášení se týká i všech spoluautorů.
Zdroje
1. Adam Z, Mayer J, Pour L. et al. Autoinflamatorní choroby se symptomy, které připomínají maligní krevní choroby - syndrom Schnitzlerové, Stillova choroba dospělých, SAPHO a VEXAS syndrom. Transfuze a hematologie dnes 2024; 30(3): 151-168.
2. Schmalzing M, Sander O, Seidl M, et al. Castleman‘s disease in the rheumatological practice. Z Rheumatol 2024; 83(Suppl 3): 289-298.
3. Alaggio R, Amador C, Anagnostopoulos I, et al. The 5th edition of the World Health Organization Classification of Haematolymphoid Tumours: Lymphoid Neoplasms. Leukemia 2022; 36(7): 1720-1748.
4. Pierson SK, Brandstadter JD, Torigian DA, et al. Characterizing the heterogeneity of Castleman disease and oligocentric subtype: findings from the ACCELERATE registry. Blood Adv 2025; 9(8): 1952-1965.
5. Romano Gargarella E, Vocaturo F, Guarneri A, et al. Role of 18F FDG-PET-CT in Fever and Inflammation of Unknown Origin. J Clin Med 2025; 14(16): 5861.
6. Řehák Z, Šprláková-Puková A, Kazda T, et al. 18F-FDG PET/CT in polymyalgia rheumatica-a pictorial review. Br J Radiol 2017; 90(1076): 20170198.
Štítky
Patologie Soudní lékařství Toxikologie
Článek vyšel v časopiseČesko-slovenská patologie

2026 Číslo 1-
Všechny články tohoto čísla
- Testování exprese claudinu 18.2 u adenokarcinomu žaludku a gastroesofageální junkce: Současný stav a výhled do blízké budoucnosti
- Castlemanova choroba – jedno jméno, mnoho tváří
- Lymfatická tkáň v souvislostech: od nenápadných změn k zásadním diagnózám
- Přednosti a limitace nového stagingového systému karcinomu endometria FIGO 2023 z pohledu klinika a patologa
- Od archeologické brigády k americké rezidentuře: proč je patologie „nejlepší obor medicíny“
- Cílené profilování genové exprese jako nástroj pro diagnostické určení buněčného subtypu a prognostickou stratifikaci u difuzního velkobuněčného B-lymfomu
- Castleman-like lymfadenopatie u pacienta se smíšenou chorobou pojiva: kazuistika a přehled literatury
- EBV-asociovaná plazmocelulární varianta Castlemanovy choroby: více než deset let trvající diagnostická odysea – kazuistika pacienta
- MONITOR, aneb nemělo by vám uniknout, že…
- Česko-slovenská patologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Castlemanova choroba – jedno jméno, mnoho tváří
- Testování exprese claudinu 18.2 u adenokarcinomu žaludku a gastroesofageální junkce: Současný stav a výhled do blízké budoucnosti
- Přednosti a limitace nového stagingového systému karcinomu endometria FIGO 2023 z pohledu klinika a patologa
- Cílené profilování genové exprese jako nástroj pro diagnostické určení buněčného subtypu a prognostickou stratifikaci u difuzního velkobuněčného B-lymfomu
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



