-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Vliv dárcovství krve na zásoby železa u dárců: porovnání dvojité erytrocytaferézy a dárcovství plné krve
Blood donation and iron stores – comparison of double erythrocytapheresis and whole blood donation
Background:
Repeated double erythrocytapheresis and whole blood donation could be accompanied by loss of iron and anemisation. The aim was to evaluate long-term effects of blood donation on iron stores and to find useful parameter for monitoring of them. Methods: Using separator Haemonetics MCS+, we completed double erythrocytaphereses in 30 donors who meet European donor criteria. Hb, Ht and levels of serum iron, transferin, ferritin, sTfR and qTfRi were analyzed on day 0, 30, 90, 180 after the 1th and 2nd apheresis and on day 90, 180 after the 3th collection. In donors without Hb value restoration, we measured occult bleeding. The results were compared with the same parameters in whole blood donors with history of 4 donations per year. P-valueResults:
In 30 men, 98 double erythrocytaphereses were performed. Initial values in donors: Hb 152 ± 7 g/l, Ht 0.43 ± 0.02, ferritin 47.3 ± 20.4 μg/l, sTfR 2.92 ± 0.73 mg/l, qTFRi 0.78 ± 0.20. Significant decrease in Hb (147 ± 7 g/l), Ht (0.41 ± 0.02), ferritin (22.1 ± 10.5 μg/l) and increase of values sTfR (4.88 ± 1.03 mg/l) and qTfRi (1.73 ± 0.57) (pConclusions:
Repeated double erythrocytaphereses had comparable influence on donor iron status as frequent whole blood donation. The decrease of iron stores in several double erythrocytapheresis donors was found. Thus, we recommend ferritin plasma level > 40 μg/l as preselection criterium for repeated double erythrocytapheresis donors and as a useful parameter for monitoring of iron stores. Oral iron supplementation should be judged on individual bases, the cause of iron deficiency should looked for.Key words:
double erythrocytapheresis, iron stores, ferritin
Autoři: R. Procházková, (STL)
Působiště autorů: Transfuzní oddělení, Krajská nemocnice Liberec, a. s.
Vyšlo v časopise: Transfuze Hematol. dnes,16, 2010, No. 4, p. 224-229.
Kategorie: Souhrnné práce, původní práce, kazuistiky
Souhrn
Úvod:
Opakované odběry metodou dvojité erytrocytaferézy anebo plné krve mohou být spojeny se ztrátou zásobního železa anebo anemizací dárců krve. Cílem studie bylo zhodnotit dlouhodobý efekt dárcovství krve na zásoby železa a stanovit vhodný parametr pro jejich monitorování.Metoda:
Odběry dvou jednotek erytrocytů byly provedeny u dárců plazmy na separátoru Haemonetics MCS+ dle vstupních kritérií Doporučení Rady Evropy. U dárců jsme hodnotili hodnoty hemoglobinu, hematokritu a parametry metabolismu železa v den 0, 30, 90, 180 po 1. a 2. odběru a v den 90 a 180 po 3. odběru. Preparáty železa jsme preventivně nepodávali. Výsledky jsme porovnali se souborem dárců plné krve, darujících 4 odběry ročně. K hodnocení byl použit dvouvýběrový t-test a párový test, statistická významnost byla posouzena na hladině pVýsledky:
U 30 mužů bylo provedeno 98 dvojitých erytrocytaferéz. Vstupní hodnoty u dárců: Hb 152 ± 7 g/l, Ht 0,43 ± 0,02, feritin 47,3 ± 20,4 μg/l, sTfR 2,92 ± 0,73 mg/l a qTFRi 0,78 ± 0,20. Za 30 dnů po erytrocytaferéze bylo zaznamenáno statisticky významné snížení hodnot Hb (147 ± 7 g/l), Ht (0,41 ± 0,02), feritinu (22,1 ± 10,5 μg/l) a vzestup hodnot sTfR (4,88 ± 1,03 mg/l) a qTfRi (1,73 ± 0,57), vše pZávěr:
Dvojitá erytrocytaferéza a časté dárcovství plné krve představují pro dárce srovnatelnou zátěž. U některých dárců může docházet k deficitu zásob železa, substituce přípravky železa by měla být individuální, s ohledem na další možné příčiny jeho deficitu. U dvojitých erytrocytaferéz je vhodné výběrová kritéria doplnit o stanovení feritinu (> 40 μg/l), u opakovaných odběrů je třeba hladinu feritinu sledovat.Klíčová slova:
dvojitá erytrocytaferéza, zásoby železa, feritinÚvod
Erytrocytové přípravky je možné získávat klasickými odběry plné krve a jejím zpracováním, anebo aferetickou technikou – dvojitou erytrocytaferézou. K výběru dárců obou typů odběrů jsou používána kritéria stanovená Vyhl. 143/2008 Sb. (1) a Doporučením Společnosti pro transfuzní lékařství (2) (tab. 1). Při odběru plné krve se dárci odebírá 400–500 ml krve.
Dvojitá erytrocytaferéza je odběr dvou jednotek erytrocytů na krevním separátoru (3, 4) od jednoho dárce. Krev se odebírá speciálním odběrovým setem, extrakorporálně se antikoaguluje a vede do přístroje, v němž se v gravitačním poli centrifugy rozdělí podle specifické hmotnosti jednotlivých složek. Odebírané erytrocyty se sbírají do sběrného vaku, plazma se vrací zpět dárci. Nutná je objemová náhrada (5). Výhodou tohoto typu odběru je možnost přípravy dvou transfuzních jednotek (T.U.) erytrocytů (RBC), zejména při nedostatku dárců a stoupajícím nárokům na jejich výběr (6). Erytrocytové přípravky získané aferézou jsou vysoké jakosti, obsahují standardní terapeutickou dávku hemoglobinu. Výhodou aplikace více T.U. od jednoho dárce je snížení počtu dárců, jimž je pacient exponován. Tím lze snížit riziko možnost imunizace hemoterapií a přenosu infekce (3, 7), zejména u polytransfundovaných pacientů. Metodu lze využít i u autotransfuzí (8, 9). Dvojitá erytrocytaferéza je dárci dobře snášena, vzhledem k izovolemickému odběru je incidence přímých vedlejších účinků obdobná nebo menší než u odběrů plné krve (10). U zdravých dárců se po odběru 2 T.U. RBC nedostavují symptomy anémie (11), odběry však mohou vést k depleci zásob železa nebo k anemizaci dárce (12).
Cílem studie bylo zhodnotit vliv odběru 2 T.U. RBC na zdravotní stav dárce krve, zaměřit se na hodnoty krevního obrazu a parametry metabolismu železa a vybrat vhodné parametry pro sledování zdravotního stavu dárce v případě potřeby.
Materiál a metodika
Prospektivní studie sledovala určené parametry dárců 2 T.U. RBC a porovnávala je s odpovídajícími parametry alikvotního počtu dárců plné krve. Projekt byl schválen Etickou komisí KN Liberec. Součástí studie byl přijatý a obhájený výzkumný projekt IGA MZ ČR č. NR/8015–3.
Krevní separátory a odběrové protokoly
Odběry 2 jednotek erytrocytů byly provedeny na separátoru Haemonetics MCS+ (Haemonetics Corp., Braintree, USA). Použili jsme antikoagulační roztok CPD a odběrový set LN 948 F (Haemonetics Corp., Braintree, USA). Odběry byly kompenzovány kontinuální infuzí 400 ml fyziologického roztoku. Odebrané erytrocyty byly resuspendovány ve 100 ml roztoku SAGM na jednotku a následně deleukotizovány integrovanými filtry RC 2H PALL za 2 hodiny po odběru bez předchlazení.
Soubor dárců a hodnocené parametry
Do studie byli zařazeni dobrovolní bezplatní dárci plazmy na základě informovaného souhlasu, dle kritérií v tabulce 1. Zkoumaný soubor tvořilo 30 mužů, u kterých bylo provedeno 98 odběrů 2 T.U. RBC, žádná žena nevyhověla vstupním kritériím. U dárců jsme hodnotili bezprostřední nežádoucí projevy výkonů a změnu hodnot Hb a hematokritu (Ht) ihned po erytrocytaferéze. Dále jsme sledovali hodnotu Hb, Ht a parametry metabolismu železa (Fe) (hladina plazmatického Fe, transferin, feritin, solubilní transferinový receptor (sTfR) a index qTFRi v den 0, 30, 90, 180 po 1. a 2. erytrocytaferéze, a v den 90 a 180 po 3. a 4. erytrocytaferéze. Základní charakteristiku souboru uvádí tabulka 2.
Tab. 1. Výběrová kritéria dárců krve. 
Legenda: T.U.: transfuzní jednotka, RBC: erytrocyty, TBV: celkový objem krve, * minimální hodnota po odběru Tab. 2. Parametry souborů dárců krve. 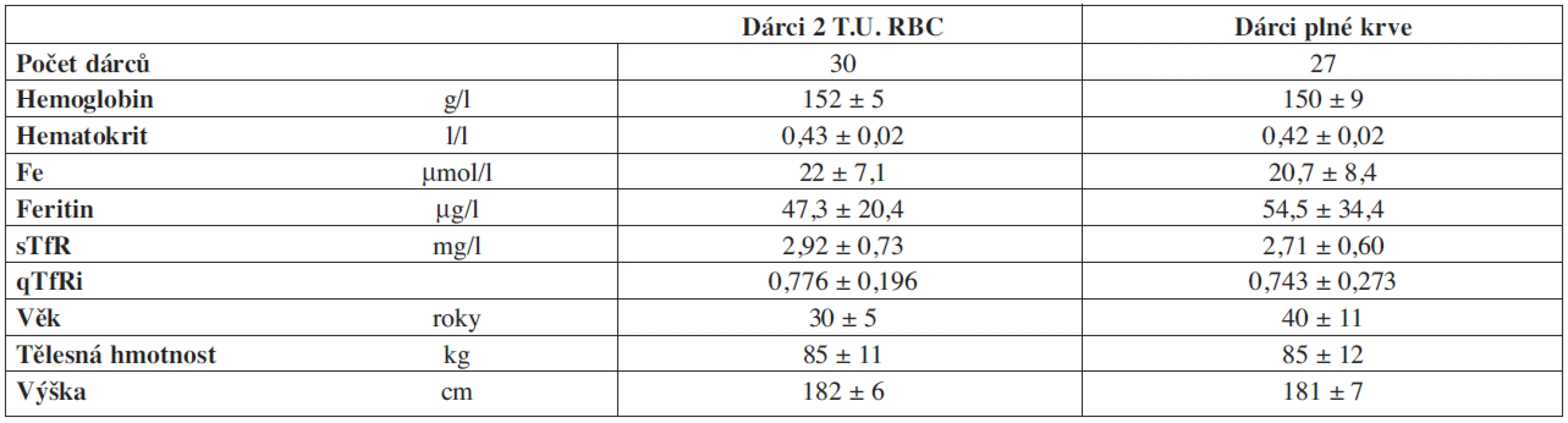
Legenda: T.U.: transfuzní jednotka, RBC: erytrocyty, Fe: plazmatické železo, sTfR: solubilní transferinový receptor, qTfRi: index sTfR Před každým odběrem byl dárce vyšetřen lékařem a zhodnocena vstupní kritéria.
Kontrolní soubor dárců plné krve tvořilo 27 mužů. Odběry 450 ± 10 ml krve byly prováděny 4x ročně v intervalu 90 dnů. Sledování odpovídajících parametrů zdravotního stavu dárců krve bylo prováděno paralelně se zkoumaným souborem. Preparáty železa jsme preventivně nepodávali dárcům ani jednoho souboru.
Laboratorní analýza:Krevní obraz byl měřen na přístroji Coulter STKS (Beckman Coulter, Florida, USA). Biochemická vyšetření byla provedena na Oddělení klinické biochemie KN Liberec na analyzátoru Modular EVO Roche. Plazmatická hladina železa byla vyšetřena kolorimetricky (kit FerroZin, kat. č. 1876996, Roche Diagnostics), feritin imunochemicky soupravou Elecsys Feritin (kat. č. 03737551, Roche Diagnostics, SRN), transferin imunoturbidimetricky (Transferin ver. 2, kat. č. 3015084, Roche Diagnostics, SRN), solubilní transferinový receptor latexem usnadněnou turbidimetrií (sTfR, kat. č. 218315, Roche Diagnostics, SRN), index qTfRi byl stanoven dle vzorce qTfRi = sTfR/ln feritin.
Statistické metody: Cílem statistického hodnocení bylo hodnocení určených parametrů u zkoumaných souborů dárců v časové ose a hodnocení parametrů mezi hodnoceným a kontrolním souborem navzájem. Pro prezentaci dat byly použity základní grafické nástroje (spojnicové a sloupcové grafy) a přehledové tabulky (průměr, medián, směrodatná odchylka, range). K statistickému hodnocení byl použit statistický software Excel 4.0. Byl použit Studentův t-test, F-test, párový test, Pearsonův a Spearmanův korelační koeficient. Statistická významnost byla posouzena na hladině p < 0,05.
Výsledky
Dvojité erytrocytaferézy trvaly 36–47 (med. 40) min., odebíraný objem byl 374–397 (med. 384) ml a 5,7–8,2 (med. 7,0) % TBV. V porovnání s objemem odebírané jednotky plné krve byl odebírán objem menší o 66 ml (p < 0,001). Při hodnocení přímého vlivu procedury jsme nezaznamenali žádné závažné klinické vedlejší účinky, jedenkrát jsme zaznamenali rupturu žíly u dárce.
Poodběrové hodnoty Hb a Ht (tab. 3) ve všech případech vyhovovaly doporučeným limitům a odpovídaly hodnotám predikovaným software separátoru. Ke změně počtu trombocytů nedošlo (p = 0,85).
Tab. 3. Změny hemoglobinu a hematokritu po dvojité erytrocytaferéze. 
Vývoj hemoglobinu a parametrů metabolismu Fe po dvojité erytrocytaferéze uvádí tabulka 4 a graf 1. Za 30 dnů po odběru jsme zaznamenali statisticky významné změny všech sledovaných parametrů, tzn. snížení hodnot Hb, Ht, Fe, saturace transferinu, feritinu a vzestup hodnot transferinu, sTfR a indexu qTfRi. U většiny dárců tohoto typu odběru došlo ke spontánní úpravě Hb, Ht a některých parametrů metabolismu železa na předodběrové hodnoty. U hodnot Hb, Ht, plazmatického železa a saturace transferinu tomu tak bylo již za 90 dnů po odběru u 25 dárců ze 30, u 2 dárců za 180 dnů a u 3 dárců za 270 dnů. Úprava hladiny feritinu na hodnoty před odběrem trvala 180 dnů u 22 dárců, u 3 dárců 270 dnů a u 2 dárců 360 dnů po odběru. U 3 dárců jsme pro pokles hodnoty feritinu pod 12 μg/l indikovali preparát železa (Sorbifer durules), u jednoho z nich bylo zjištěno okultní krvácení ve stolici, u dvou nesprávná životospráva. K úpravě hodnot transferinu, sTfR a qTfRi za 180 dnů nedošlo, vývoj hodnot měl však tendenci k úpravě.
Tab. 4. Vývoj hemoglobinu a parametrů Fe po dvojité erytrocytaferéze. 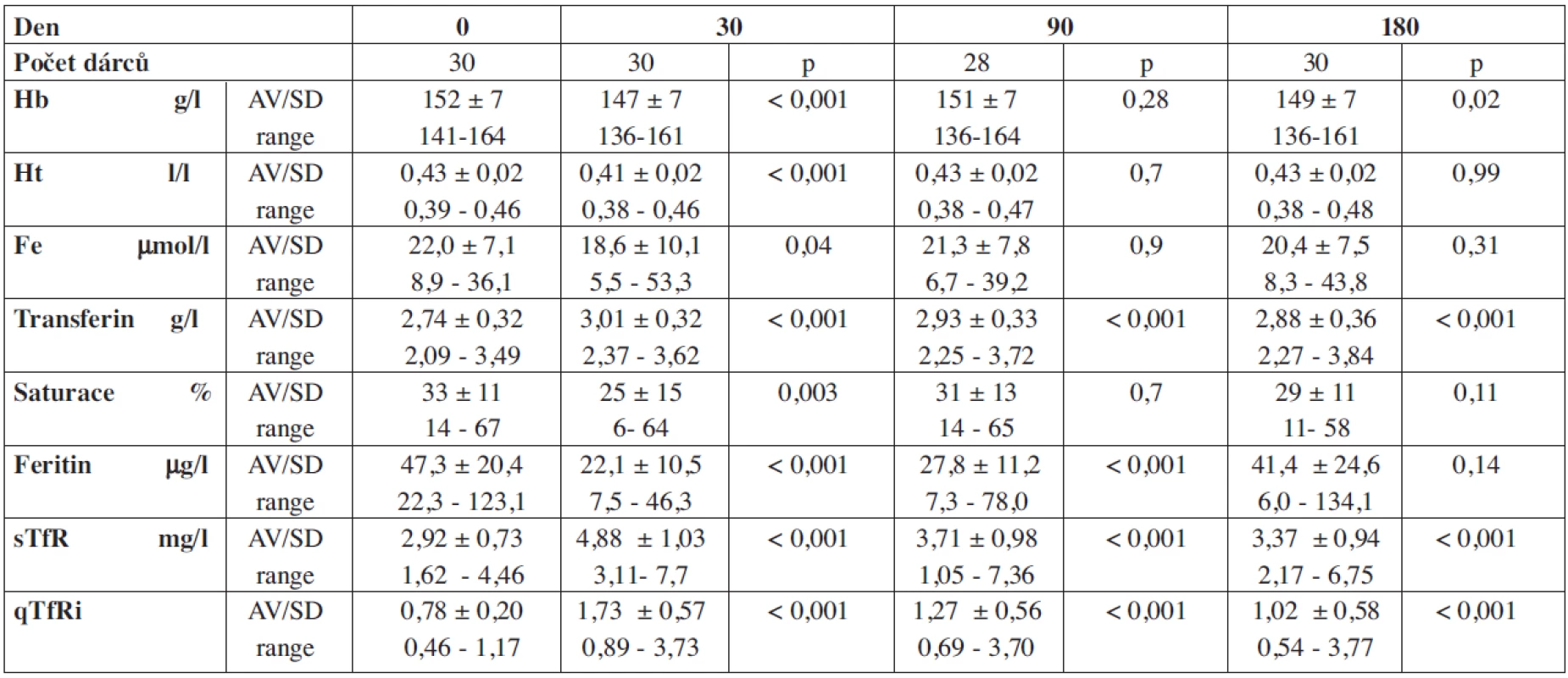
Legenda: saturace transferinu, p: statistická významnost ke dni 0, sTfR: solubilní transferinový receptor, qTfRi: index sTfR (= sTfR/ln feritin) Graf 1. Vývoj parametrů metabolismu Fe po dvojité erytrocytaferéze. Legenda: Fe: plazmatické železo, sTfR: solubilní transferinový receptor, qTfRi: index sTfR 
Dárci, u kterých došlo k doplnění zásob železa za 180 dnů, měli průměrnou vstupní hodnotu feritinu vyšší (50,8 ± 21,3 μg/l) (p = 0,004) nežli dárci, u kterých k doplnění zásob na hodnotu před odběrem nedošlo (34,2 ± 8,3 μg/l) (graf 2). U 22 dárců byla provedena 2. erytrocytaferéza (med. 210 dnů po 1. odběru), zde k úpravě Hb, Ht, Fe, transferinu, jeho saturace a feritinu došlo u 19 dárců za 180 dnů, u tří dárců úprava hladiny transferinu, jeho saturace a feritinu trvala 270 dnů. Třetí erytrocytaferézu bylo možno provést u 21 dárců (med. 420 dnů po 1. odběru). Po 3. erytrocytaferéze bylo hodnoceno 19 dárců. U 16 dárců trvala úprava transferinu, jeho saturace a feritinu 180 dnů, opět tři dárci potřebovali ke spontánní obnově zásob železa interval 270 dnů. Při hodnocení vývoje hodnot sTfR a indexu qTfRi jsme zjistili statisticky významné rozdíly proti dnu 0 i po 1., 2. i 3. erytrocytaferéze (p < 0,001) (tab. 5).
Graf 2. Porovnání vstupních hodnot feritinu u dárců erytrocytaferézy. Legenda: hodnota feritinu: 1: 50,8 ± 21,3 μg/l (dárci, kteří za 180 dnů doplnili zásoby železa na hodnoty před odběrem), 2: 34,2 ± 8,3 μg/l (dárci, kteří za 180 dnů nedoplnili zásoby železa na hodnoty před odběrem). 
Tab. 5. Vývoj parametrů metabolismu železa po 2. a 3. dvojité erytrocytaferéze. 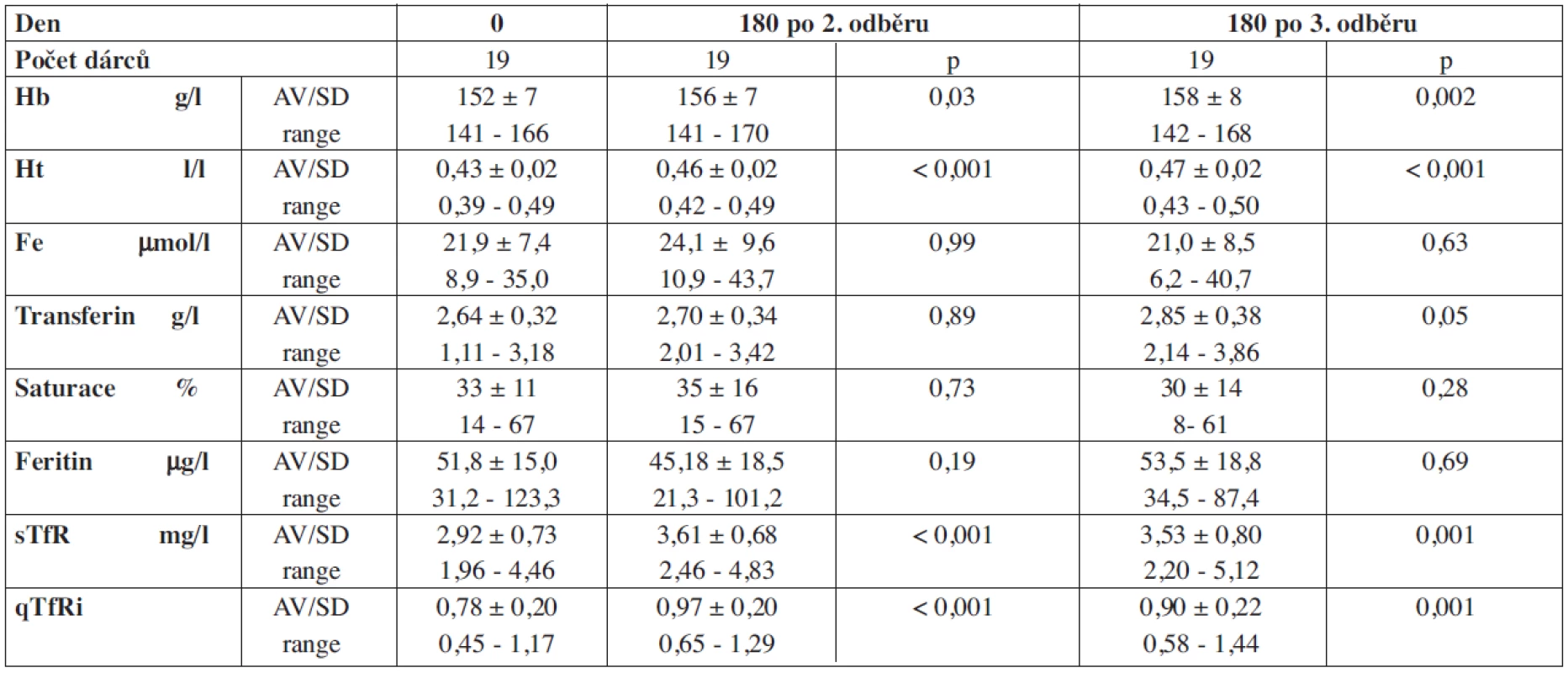
Legenda: saturace transferinu, p: statistická významnost ke dni 0, sTfR: solubilní transferinový receptor, qTfRi: index sTfR (= sTfR/ln feritin) Výsledky sledování Hb, Ht a parametrů metabolismu Fe u kontrolního souboru dárců plné krve uvádí tabulka 6 a graf 2. U hodnot Hb, Ht, hladiny železa a saturace transferinu nedocházelo ke statisticky významnému snížení. V den 360 byly hodnoty Hb a Ht v porovnání s hodnotami v den 0 dokonce vyšší. Zvýšení hladiny transferinu bylo v den 180 na hladině statistické významnosti a v den 360 po čtyřech odběrech plné krve bylo statisticky významné. Hladina feritinu byla v den 90 a 180 statisticky významně snížena v porovnání s jeho hodnotou v den 0, v den 360 nebyl zaznamenán statisticky významný rozdíl. Hodnoty sTfR a qTfRi byly statisticky významně zvýšeny po celou dobu sledování. Přípravek železa jsme museli podat u tří dárců, z toho u dvou dárců jsme zjistili pozitivní okultní krvácení. Druhý rok sledování jsme zjistili obdobné výsledky.
Tab. 6. Vývoj hemoglobinu a parametrů Fe u dárců plné krve. 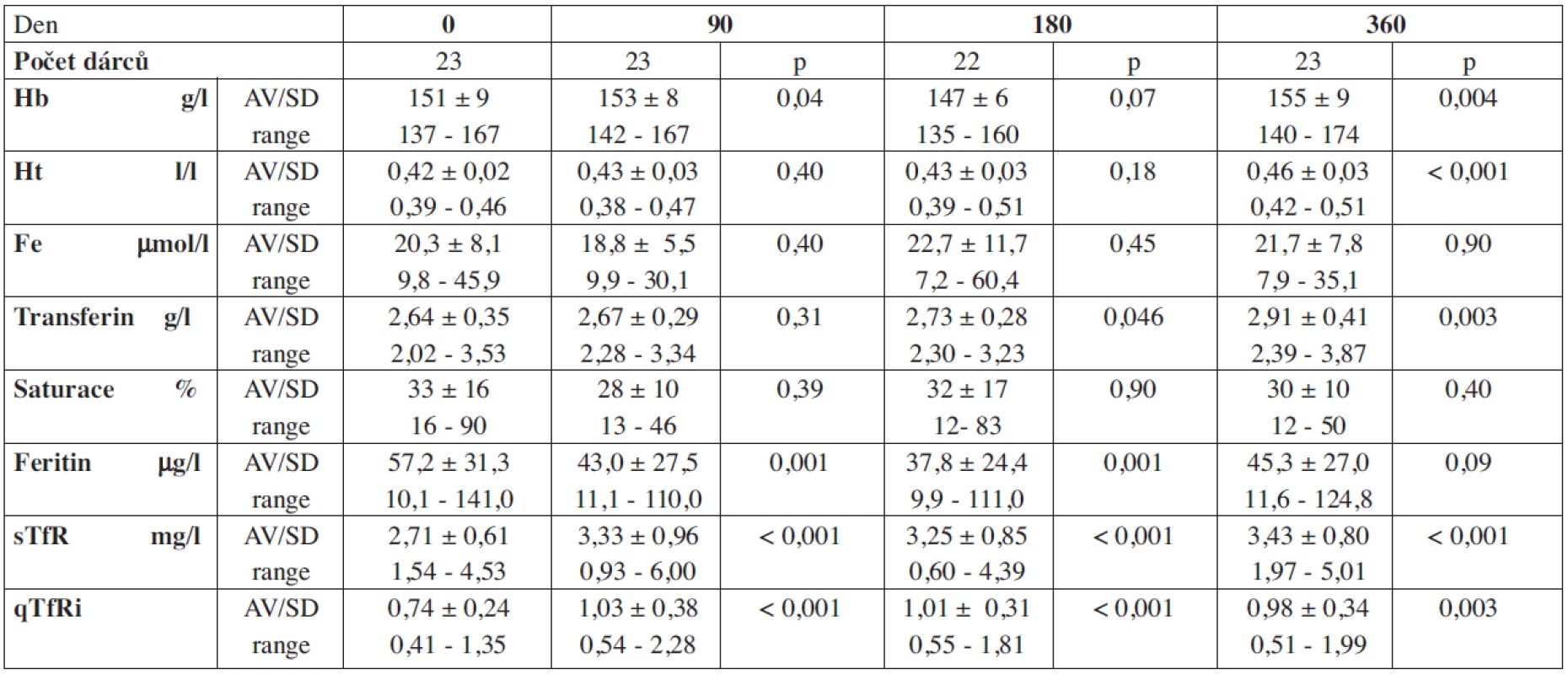
Legenda: saturace transferinu, p: statistická významnost ke dni 0, sTfR: solubilní transferinový receptor, qTfRi: index sTfR (= sTfR/ln feritin) Diskuse
Ztráta železa při dvojitém odběru erytrocytů je cca 320–420 mg (11). Tato ztráta je obdobná i u dárcovství plné krve, kde při jednom odběru dochází k ztrátě cca 200 mg železa (13). Řada autorů považuje za známku sideropenie u dárců krve hladinu feritinu pod 12 μg/l (14, 15). Vyšetření hladiny feritinu je proto některými autory doporučeno i jako parametr monitorování dárce dvojitých erytrocytaferéz (12, 15). Obecná doporučená hodnota zatím stanovena nebyla, italští autoři doporučují hladinu feritinu > 50 μg/l (15). Citlivým parametrem latentního nedostatku železa je stanovení solubilního transferinového receptoru v séru (sTfR) (16, 17, 18, 19), které je některými autory doporučováno i u dárců plné krve (20) či u pacientů podstupujících předoperační odběr autotransfuze (21).
Dvouleté sledování souboru dárců dvou jednotek erytrocytů v souladu s literaturou (14, 22) prokázalo, že k významným změnám v zásobách železa nedochází u všech dárců. Po odběrech došlo ke statisticky významnému poklesu hladiny Hb, Ht, Fe a feritinu, avšak u většiny dárců jsme nalezli spontánní úpravu uvedených parametrů. U hodnot Hb, Ht a Fe tomu tak bylo za 90 dnů, u feritinu za 180 dnů, podobně jako zjistili i jiní autoři (11, 12). U dárců s hladinou feritinu nad 40 μg/l nedošlo k poklesu feritinu pod 12 μg/l a obnova zásob Fe nastala dříve. Proto jsme mezi výběrová kritéria zařadili hodnotu feritinu 40 μg/l. Bonomo a spol., 2004 (15) doporučuje hodnotu feritinu nad 50 μg/l, takto se však počet vhodných dárců může významně snížit. Z našeho souboru tomuto kritériu vyhovělo pouze 9 dárců.
Dlouhodobě přetrvával statisticky významný vzestup sTfR a indexu qTfRi. Uvedené změny sTfR a qTfRi jsme zaznamenali i při dvouletém sledování dárců plné krve, což může signalizovat obdobně se snižující zásoby železa u obou typů odběrů (13). Porovnání souboru dárců 2 T.U. RBC se souborem dárců plné krve tak prokázalo, že dvojitá erytrocytaferéza a časté dárcovství plné krve představují pro dárce srovnatelnou zátěž.
Pro praxi bude u opakovaných dárců nejen dvojitých erytrocytaferéz, ale i plné krve důležité doplnit monitorování metabolismu železa (23), jak bylo doporučeno již ve 12. vydáním Doporučení Rady Evropy (24). Sledování zásob Fe vytipuje jedince ohrožené sideropenií, zamezí neindikovanému podávání přípravků železa. Feritin se ukazuje jako vhodný vstupní parametr pro výběr dárců 2 T.U. RBC a pro sledování opakovaných dárců 2 T.U. RBC i plné krve. Stanovení sTfR jako citlivějšího parametru nedostatku železa je třeba vzhledem k vysoké ceně vyšetření indikovat individuálně.
Diskutováno je preventivní podávání preparátů železa, při kterém dochází k doplnění zásob Fe dříve než u dárců, kteří tuto substituci nedostávají (11, 12). Dvojitá erytrocytaferéza je proto považována řadou autorů za bezpečnou při preventivním podávání preparátů železa (11). Doporučení nejsou jednotná, protože ztráta železa je obdobná jako u častých dárců plné krve, kde preventivní substituce v řadě případů není doporučována vůbec, anebo je indikována na podkladě jasných pravidel (informovaný souhlas, informace praktického lékaře o medikaci preparáty Fe, nad 40 let preparáty Fe preventivně nepodávat vzhledem k riziku přehlédnutí nádorů) (25). Lze najít doporučení podávat Fe v dávce cca 15 mg denně formou dietetických či vitaminových přípravků (26) anebo minidávek preparátů Fe (20), které mohou kompenzovat ztráty železa při častém dárcovství plné krve (13). Je třeba zdůraznit nutnost pečlivého hodnocení zdravotního stavu dárců zejména dvojitých erytrocytaferéz, s důrazem na stanovení příčiny deficitu železa (27, 28, 29, 30). Důležité je identifikovat dárce krve s latentní sideropenií (20) a zvažovat i vedlejší efekt medikace.
Preventivní aplikace preparátů Fe tak, jak ji doporučují někteří autoři (11, 31), by jistě urychlila regeneraci jeho zásob. Naše výsledky však ukazují, že při současných intervalech mezi odběry není paušální indikace přípravků železa nutná u dárců dvojité erytrocytaferézy ani u dárců plné krve. Domníváme se, že je k ní nutno přistupovat individuálně, s vědomím nutnosti diferenciálně diagnostické rozvahy i nad jinými možnými příčinami nedostatku železa (25, 26, 30, 32) a monitorovat zásoby Fe při opakovaných odběrech.
V některých státech, např. USA nebo SRN je interval mezi dvěma erytrocytaferézami stanoven na 4 měsíce, či je povoleno 6 odběrů plné krve ročně (11, 12, 13, 27). Z naší práce pro praxi vyplývá, že při zkrácení intervalu mezi dvěma erytrocytaferézami se zásoby železa u dárců s vysokou pravděpodobností spontánně nedoplní a bude nutné je substituovat u vyššího počtu dárců nežli dosud.
MUDr. Renata Procházková, Ph.D.
Transfuzní oddělení
Krajská nemocnice Liberec, a.s.
Baarova 15
460 63 Liberec
Zdroje
1. Vyhl. 143/2008 Sb. o stanovení bližších požadavků pro zajištění jakosti a bezpečnosti lidské krve a jejích složek (vyhláška o lidské krvi).
2. Doporučení STL č. 20072_03 Posuzování způsobilosti k dárcovství krve a krevních složek.
3. Leitner GC, Stohlawetz PJ, Stiegler G, et al. Quality of packed red blood cells and platelet concentrates by multicomponent collection using the MCS Plus device. Journal of Clinical Apheresis 2003; 18 : 21–25.Seghatchian J, Krailadsiri P. The quality of MCS + version C2 double dose platelet concentrate with leucodepletion through a continuos filtration process. Transfus Apher Sci 2002; 26 : 37-41.
5. Guide to the preparation, use and quality assurance of blood components. 9th ed. Strasburg, Council of Europe Publishing, 2003.
6. Goodnough LT, Shander A, Brecher ME. Transfusion medicine: looking to the future. The Lancet 2003; 361 : 161–188.
7. Urbánek P, Mareček Z, Brodanová M, et al. Rizikové faktory přenosu viru hepatitidy C (HCV) v české populaci. Čas Lék Čes 2002; 6 : 185–188.
8. Garcia Gala JM, Vincente PR, Gonzales Muniz S, et al. Utility of red blood cell apheresis in autologous blood donation. Transfus Sci 2000; 23 : 69–73.
9. Höcker P. Red cell apheresis in autologous preoperative blood donation. Transfus Apher Sci 2001; 24 : 75–78.
10. Moog R, Bartsch R, Muller N. Concurrent collection of in-line filtered platelets and red blood cells by apheresis. Ann Haematol 2002; 81 : 322–325.
11. Shi PA, Ness PM. Two-unit red cell apheresis and its potential advantages over traditiional whole-blood donation. Transfusion 1999; 39 : 218–225.
12. Hogler W, Mayer W, Messmer Ch, et al. Prolonged iron depletion after allogenetic 2-unit apheresis. Transfusion 2001; 41 : 602–605.
13. Popovsky MA. Safety of RBC apheresis and whole blood donation in allogeneic and autologous blood donors. Transfus Apher Sci 2006; 34 : 205–211.
14. Bedchtloff S, Tran-Mi B, Haubelt H, et al. A prospective trial on the safety of long term intensive plasmapheresis in donors. Vox Sanq 2005; 88 : 189–195.
15. Bonomo P, Garozzo G, Bennardello F. The selection of donors in multicomponent collection management. Transfus Apher Sci 2004; 30 : 55–59.
16. Čermák J, Brabec V. Klinický význam vyšetření hladiny cirkulujících transferinových receptorů v séru. Vnitř lék 1999; 45 : 468–472.
17. Čermák J, Brabec J. Transferin receptor – ferritin index: a useful parameter in differential diagnosis of iron deficiency and hyperplastic erythropoesis. European Journal of Haematology 1998; 61 : 210–212.
18. Chrobák L. Mikrocytární a hypochromní anémie. Vnitř lék 2001; 47 : 166–174.
19. Pácal L, Kaňková K. Novější poznatky o metabolismu železa a jeho poruchách. Čas Lék čes 2004; 143 : 9–14.
20. Flesland O, Eskelund AK, Flesland AB, et al. Transferrin receptor in serum. A new toll in the diagnosis and prevention of iron deficiency in blood donors. Transfus Apher Sci 2004; 31 : 11–16.
21. Dimonte D, Pepe M, Silletti I, et al. Serum transferin receptor is a marker of iron deficiency in patients included in programs for preoperative autologous blood donation. Transfus Apher Sci 2002; 27 : 211–216.
22. Tran-Mi B, Storch H, Seidel K, et al. The impact of different intensities of regular donor plasmapheresis on humoral and cellular imunity, red cell and iron metabolism, and cardiovaskular risk markers. Vox Sang 2004; 86 : 189.
23. Smith JW, Gilcher RO. The future of automated red blood cell collection. Transfus Apher Sci 2006; 34 : 219–226.
24. Guide to the preparation, use and quality assurance of blood components. 12th ed. Strasburg, Council of Europe Publishing, 2006.
25. Simon TL. Iron, iron ewerywhere but not enough to donate. Transfusion 2002; 42 : 664–665.
26. Boulton F. Managing donors and iron deficiency. Vox Sang 2004; 87 (suppl. 2): 22–24.
27. Matthes GA. Options and cost effectiveness of multicomponent blood collection. Transfus Apher Sci 2002; 27 : 115–121.
28. Moore SB, Winters JL. Multiple blood donations and iron deficiency in patients with restless legs syndrome. Mayo Clin Proc 2003; 78 : 654.
29. Straub J, Kolešková E, Haber J. Sideropenická anémie jako projev selektivní malabsopce železa. Vnitř lék 2001; 7 : 493–495.
30. Ščudla V, Adam Z, Ščudlová M. Současné možnosti diagnostiky a léčby anémie vnitřních chorob. Vnitř lék 2001; 47 : 400–406.
31. Radtke H, Mayer B, Rocker, et al. Iron supplementation and 2-unit red blood cell apheresis: a randomized, double blind, placebo – controlled study. Transfusion 2004; 44 : 1463–1467.
32. Špičák J. Screening kolorektálního karcinomu – realita a perspektivy. Prakt Lék 2006; 96 : 254–259.
Štítky
Hematologie a transfuzní lékařství Interní lékařství Onkologie
Článek vyšel v časopiseTransfuze a hematologie dnes
Nejčtenější tento týden
2010 Číslo 4- Aktuální doporučení pro diagnostiku von Willebrandovy choroby
- Trombóza portální žíly jako komplikace infekce COVID-19 – kazuistika
- Steroidní a nesteroidní inhibitory aromatázy v léčbě rakoviny prsu u postmenopauzálních žen
- Ibrance® – nová šance pro pacientky s HR+/HER2– karcinomem prsu
-
Všechny články tohoto čísla
- Súčasná klasifikácia, diagnostika a prognóza primárnych monoklonových gamapatií (paraproteinémií)
- Výsledky liečby pacientov v chronickej fáze chronickej myelocytovej leukémie na HOK v Olomouci v rokoch 2000-2009: prognostický význam Sokalovho indexu a ELN kritérií
-
Radioterapie u folikulárního lymfomu.
Stará historie v nové perspektivě? - Proteomická analýza solubilních proteinů důležitých u dětské leukemie
- Vliv dárcovství krve na zásoby železa u dárců: porovnání dvojité erytrocytaferézy a dárcovství plné krve
- Výběr z tisku a zpráv o knihách
- Česká asociace zdravotních laborantů - co je a proč vznikla
- Zpráva o XX. konferenci dětských hematologů a onkologů České a Slovenské republiky konané ve dnech 8.–10. října 2010 v Praze
-
Vybrané odborné akce v roce 2011
ČESKÁ REPUBLIKA - OBSAH ROČNÍKU 16/2010 Transfuze a hematologie dnes
- Transfuze a hematologie dnes
- Archiv čísel
- Aktuální číslo
- Pouze online
- Informace o časopisu
Nejčtenější v tomto čísle- Súčasná klasifikácia, diagnostika a prognóza primárnych monoklonových gamapatií (paraproteinémií)
- Vliv dárcovství krve na zásoby železa u dárců: porovnání dvojité erytrocytaferézy a dárcovství plné krve
- Česká asociace zdravotních laborantů - co je a proč vznikla
-
Radioterapie u folikulárního lymfomu.
Stará historie v nové perspektivě?
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



