-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Serrated adenomy a karcinomy tlustého střeva
Serrated adenomas and carcinomas of the colon
Approximately 5 – 35 % of colorectal carcinomas arise through serrated carcinogenesis. The precursor of such carcinomas are serrated adenomas, which differ from conventional adenomas morphologically as well as genetically. Herein, we provide a basic overview of serrated lesions of the large intestine with the focus on histological diagnosis and molecular biology.
Keywords:
hyperplastic polyp – sessile serrated adenoma – traditional serrated adenoma – serrated carcinoma – serrated carcinogenesis
Autoři: Alena Chlumská 1,2; Petr Martínek 2; Petr Mukenšnabl 1; Michael Michal 1,2; Michal Zámečník 3,4
Působiště autorů: Šiklův ústav patologie FN, Univerzita Karlova v Plzni, Česká republika 1; Bioptická laboratoř s. r. o., Plzeň, Česká Republika 2; Agel a. s., Laboratoř patologie, Nový Jičín, Česká republika 3; Medirex Group Academy n. o., Bratislava, Slovenská republika 4
Vyšlo v časopise: Čes.-slov. Patol., 52, 2016, No. 1, p. 11-14
Kategorie: Přehledový článek
Souhrn
Přibližně 5 – 35 % kolorektálních karcinomů vzniká tzv. „serrated“ karcinogenezí. Prekurzorem těchto karcinomů jsou serrated adenomy, které se od konvenčních adenomů tlustého střeva liší morfologicky a geneticky. V článku podáváme základní přehled serrated lézí tlustého střeva se zaměřením na histologickou diagnózu a molekulární biologii.
Klíčová slova:
hyperplastický polyp – sesilní serrated adenom – tradiční serrated adenom – serrated karcinom – serrated karcinogeneze
Většina kolorektálních karcinomů vzniká maligním zvratem konvenčních tubulárních, tubulovilózních a vilózních adenomů. Jejich vývoj a nádorová progrese jsou charakterizovány chromozomální nestabilitou a postupnou kumulací genetických alterací, mezi něž patří zejména mutace genu APC (adenomatózní polypózy tlustého střeva), beta-cateninu (CTNNB1) a následně genu KRAS. Přibližně 5 – 35 % karcinomů tlustého střeva má ale odlišný vývoj, označovaný jako „serrated karcinogeneze“ (serrated pathway) (1-8). Prekurzorem těchto nádorů jsou serrated adenomy, které se od konvenčních adenomů liší nejen histologicky, ale i typem genetických mutací.
Serrated adenomy většinou vznikají z hyperplastických polypů (HPy), které se běžně nacházejí v celém tlustém střevě, zvláště v jeho distální části a v rektu. HPy se vyskytují ve třech variantách: mikrovezikulární, z pohárkových buněk a variantě chudé na hlen. Přestože vykazují mutace genů BRAF a KRAS (4), nepovažují se za prekancerózní léze. V současné době se rozlišují dva typy serrated adenomů: sesilní serrated adenom a tradiční serrated adenom.
Sesilní serrated adenom (SSA), v britské literatuře sesilní serrated léze (SSL)
SSA je většinou plochý, široce přisedlý polyp nažloutlé barvy. Vyskytuje se převážně v pravé polovině tračníku, častěji u starších žen a obvykle dosahuje velikosti 5 a více mm (6,8-14). Histologicky se vyznačuje serrated (zoubkovaným) uspořádáním povrchové zóny a abnormální proliferací bazální části krypt (obr. 1 – 3). Projevuje se dilatací, větvením a deformací krypt do tvaru písmene L nebo T, někdy diferenciací bazálních buněk do pohárkových a foveolárních gastrických epitelií (2,4,5,9 - 11,13,15). Přítomnost proliferujících krypt odlišuje SSA od HP. Výskyt SSA v jednotlivých sestavách kolísá podle použitých diagnostických kriterií, která vycházejí z počtu abnormálních krypt. V poslední, tj. 4. edici WHO klasifikace nádorů zažívacího traktu se pro diagnózu SSA vyžadují dvě až tři abnormální krypty (4,14). Jiné studie navrhují jakýkoliv počet deformovaných krypt, dostačující je i jediná abnormální krypta (6,10). Při užití těchto kritérií se výskyt SSA v sestavě Bettingtona a spol. zvýšil z původních 12,1 % na 14,4 % (10). Požadavek většího počtu abnormálních krypt má naopak za následek podhodnocení části SSA a zvýšené riziko vývoje tzv. intervalových karcinomů (6,8,10). Z prognostického hlediska je důležité rozlišovat SSA bez cytologických dysplazií a SSA s dysplazií. Geneticky se SSA většinou vyznačuje mutací BRAF (podobně jako jeho prekruzor - mikrovesikulární HP), hypermetylací promotoru MLH1, mikrosatelitní nestabilitou (MSI-H) a fenotypem obecně zvýšené metylace CpG ostrovů (CpG island methylator phenotype - high, CIMP-H) (6,15).
Obr. 1. Sesilní serrated adenom s abnormálními kryptami – přehled (HE, objektiv x10). 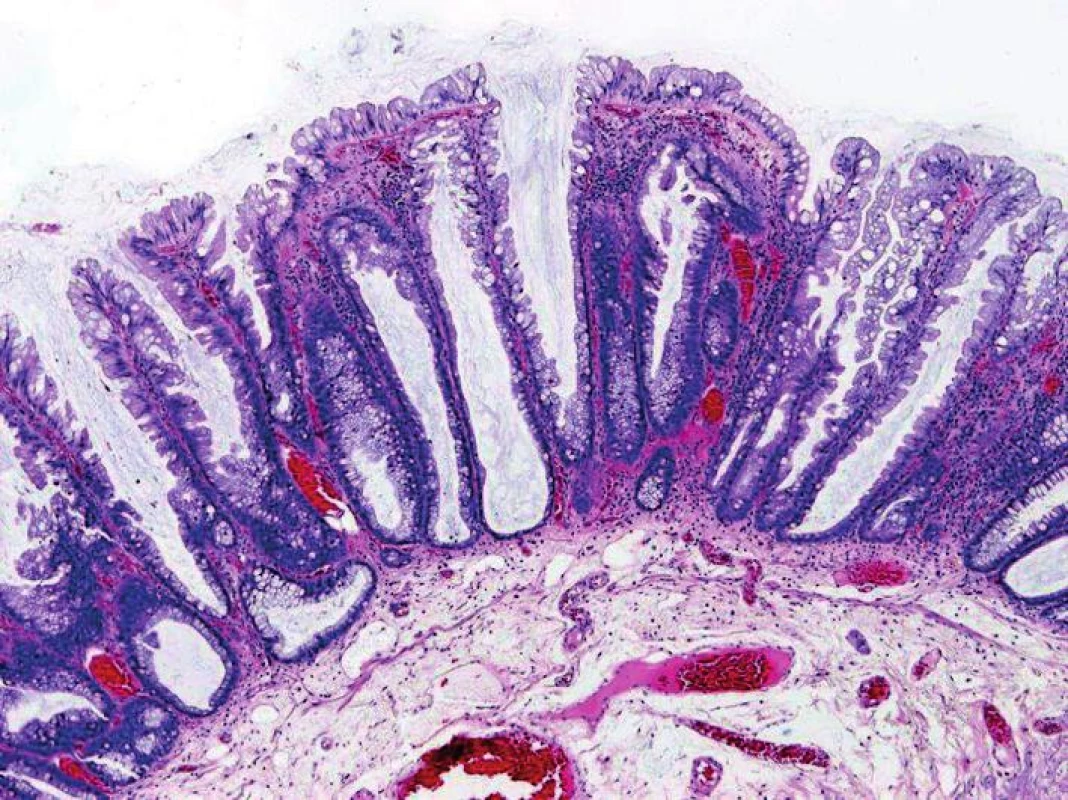
Obr. 2. Sesilní serrated adenom. Serrated uspořádání povrchové části léze (HE, objektiv x40). 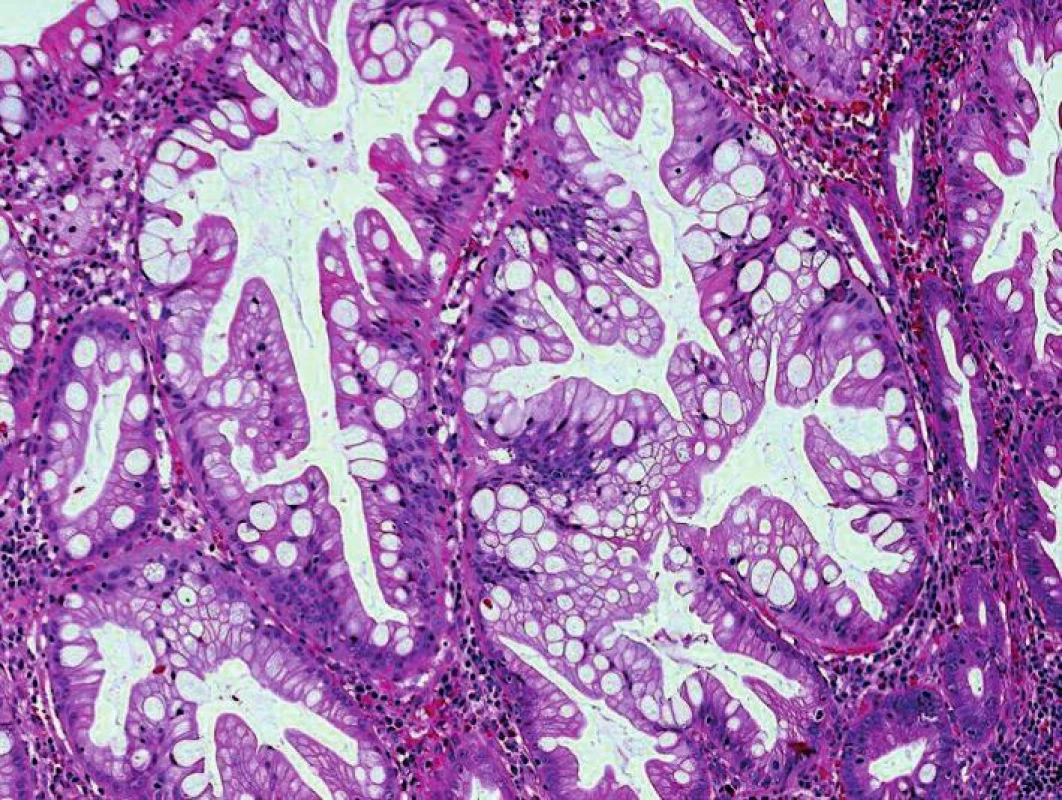
Obr. 3. Sesilní serrated adenom. Absence cytologických dysplazií, v bazální části léze zřetelné abnormální krypty (HE, objektiv x20). 
Tradiční serrated adenom (TSA)
Na rozdíl od SSA má polypózní tvar a většinou se nachází v levém tračníku. V proximálních úsecích tlustého střeva bývá plochý (1,9,16,18). Histologicky (obr. 4 – 8) má tubulovilózní nebo vilózní uspořádání vystupňované v tzv. viliformní variantě (9,17). Povrch adenomu je krytý vysokým cylindrickým epitelem s eozinofilní cytoplazmou a s úzkými centrálně uloženými jádry. Pod povrchovým epitelem se nacházejí malé tubuly označované jako ektopické krypty. Odpovídají skupinám proliferujících buněk, které vyrůstají z povrchového epitelu kolmo do přilehlého stromatu, ale nedosahují k muscularis mucosae (8). Ektopické krypty se dlouho považovaly za příznačné pro TSA, ale vyskytují se také v konvenčních tubulovilózních a vilózních adenomech (9,16,19). Rovněž eozinofilní cylindrické buňky nejsou pro TSA typické, protože se běžně pozorují v konvenčních adenomech, SSA, HP a dokonce i v regenerujícím epitelu sliznice tlustého střeva (8,9,19). Nízká proliferační aktivita eozinofilních buněk vylučuje jejich dysplastickou povahu (8,17). Pravděpodobně odpovídají metaplastickým nebo stárnoucím epiteliím. Jediným uznávaným morfologickým znakem TSA zatím zůstává zvláštní deformace luminálního povrchu označovaná jako štěrbinovitá serace (slite-like serration) podmíněná hlubokými zářezy v povrchovém epitelu a štěrbinami v místě odstupu ektopických krypt (1,9,13,16,19).
Obr. 4. Tradiční serrated adenom – přehled (HE, objektiv x10). 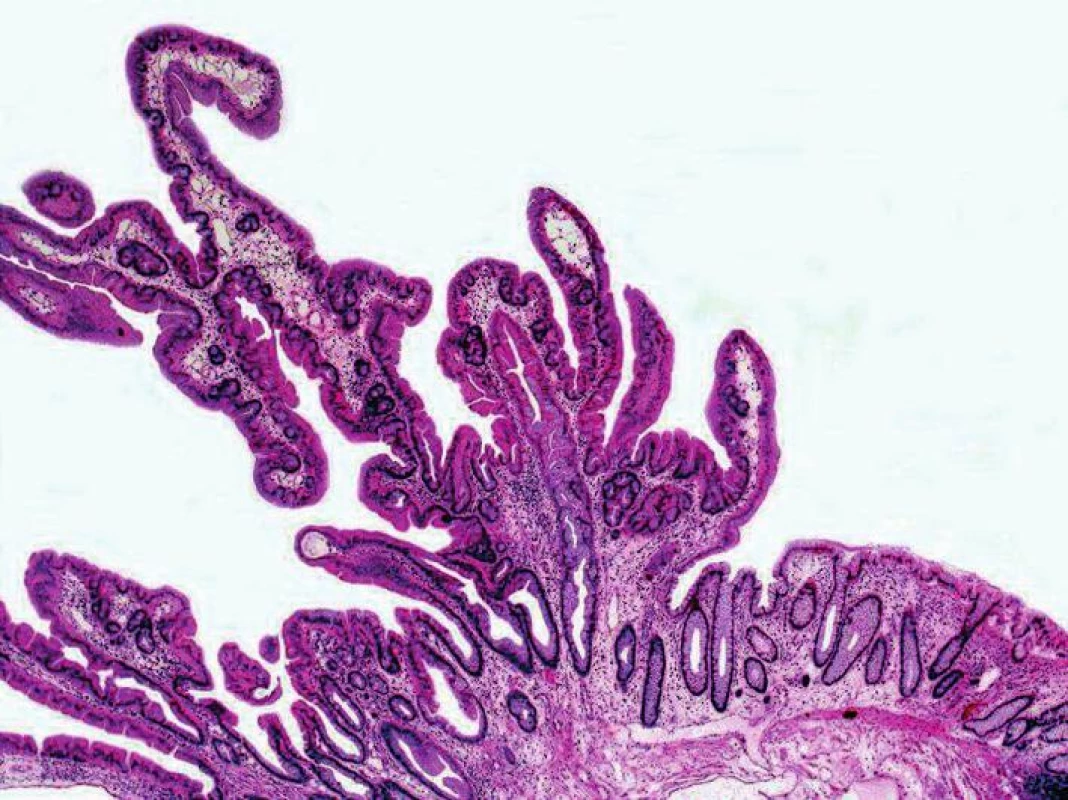
Obr. 5. Tradiční serrated adenom. Povrchový epitel s eozinofilní cytoplazmou a s centrálně uloženými protáhlými jádry (HE, objektiv x20). 
Obr. 6. Tradiční serrated adenom. Zřetelné slite-like serace epitelu. Fokálně je přítomná low-grade dysplazie (části s tmavšími jádry), ve které jsou slite-like struktury redukované (HE, objektiv x20). 
Obr. 7. Tradiční serrated adenom, s low-grade dysplázií a četnými ektopickými kryptami (HE, objektiv x20). 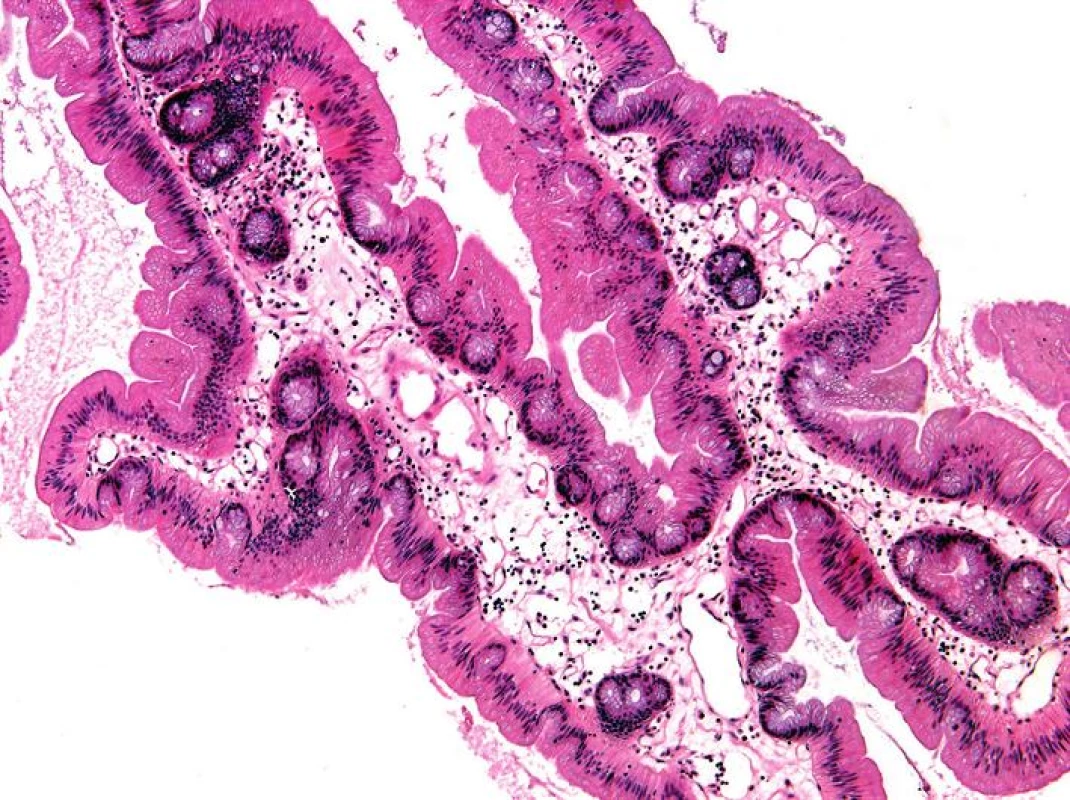
Obr. 8. Tradiční serrated adenom. Povrchový epitel s eozinofilní cytoplazmou a protáhlými jádry. (HE, objektiv x20). 
Morfologie TSA může být značně variabilní a diagnostické znaky málo vyjádřené. V malých adenomech obvykle chybí ektopické krypty a velké adenomy do značné míry připomínají konvenční tubulovilózní adenomy. K diagnóze velkých TSA doporučuje Bettington se spol. (20) přítomnost nejméně dvou základních znaků, z toho jednoho alespoň v 50 % polypu. Při menším zastoupení těchto znaků se doporučuje označení tubulovilózní adenom s rysy tradičního serrated adenomu (9,10,16,19). Nelze vyloučit, že tyto adenomy odpovídají TSA s pokročilou konvenční dysplazií. Molekulárně geneticky lze TSA rozdělit na dvě podskupiny podle aktivující mutace buď genu BRAF nebo KRAS.
Přibližně dvě třetiny TSA vykazují mutaci BRAF a jsou častěji fenotypu CIMP-H. BRAF mutované TSA jsou obvykle lokalizované proximálně, mají plochý tvar a ve 30 – 50 % rudimentárně zachovanou prekurzorovou lézi (HP nebo SSA). Naopak podskupina KRAS mutovaných TSA (cca 20 %) se nachází téměř výlučně v distálním tračníku, zvláště v rektu (9). Tyto adenomy jsou většinou fenotypu CIMP-L. Velmi důležitým nálezem v dysplastických TSA s mutací BRAF nebo KRAS je zachovaný MLH1 (mismatch repair funkce) (9,15,16). Tím se TSA s mikrosatelitovou stabilitou liší od mikrosatelit-nestabilních sesilních serrated adenomů.
Syndrom serrated polypózy
Výskyt většího počtu serrated polypů se označuje jako syndrom serrated polypózy, původně popsané jako hyperplastická polypóza (14). Kritéria tohoto syndromu zahrnují:
- nejméně 5 serrated polypů proximálně od sigmoidea, z toho alespoň dvou větších než 10 mm;
- jakýkoliv počet serrated polypů bez ohledu na velikost proximálně od sigmoidea u jedinců se serrated polypózou příbuzných první linie;
- více než 20 serrated polypů různé velikosti v průběhu celého tlustého střeva.
Polypy histologicky odpovídají HP, SSA bez cytologických dysplazií, SSA s dysplazií, TSA a konvenčním adenomům (7,9). Syndrom serrated polypózy představuje zvýšené riziko výskytu kolorektálních karcinomů, které bývají geneticky heterogenní (3,7-9,12).
Dysplastické změny v serrated adenomech
Dysplazie v serrated adenomech mohou napodobovat dysplazii konvenčních adenomů (tzv. konvenční dysplazie) nebo odpovídají serrated typu (5,6,9). Serrated dysplazie je cytologicky charakterizovaná okrouhlými buňkami s eozinofilní cytoplazmou a zvětšenými, bazálně uloženými vezikulárními jádry. Buňky si zachovávají serrated uspořádaní, které je patrné i v karcinomech (obr. 9) (1,12). Serrated karcinomy vznikající konvenční dysplazií není možné histologicky odlišit od konvenčních kolorektálních karcinomů. Předpokládá se, že SSA s dysplazií progredují do kolorektálního karcinomu častěji a pravděpodobně také v kratším časovém intervalu než konvenční adenomy (2,5,8,9,12,13). Z tohoto důvodu se u dysplastických SSA doporučuje kompletní polypektomie a při postupném odstraňování adenomů zkrácení intervalů kontrolních vyšetření na 2 – 6 měsíců (13).
Obr. 9. Serrated karcinom invazivně rostoucí do muscularis propria (HE, objektiv x20). 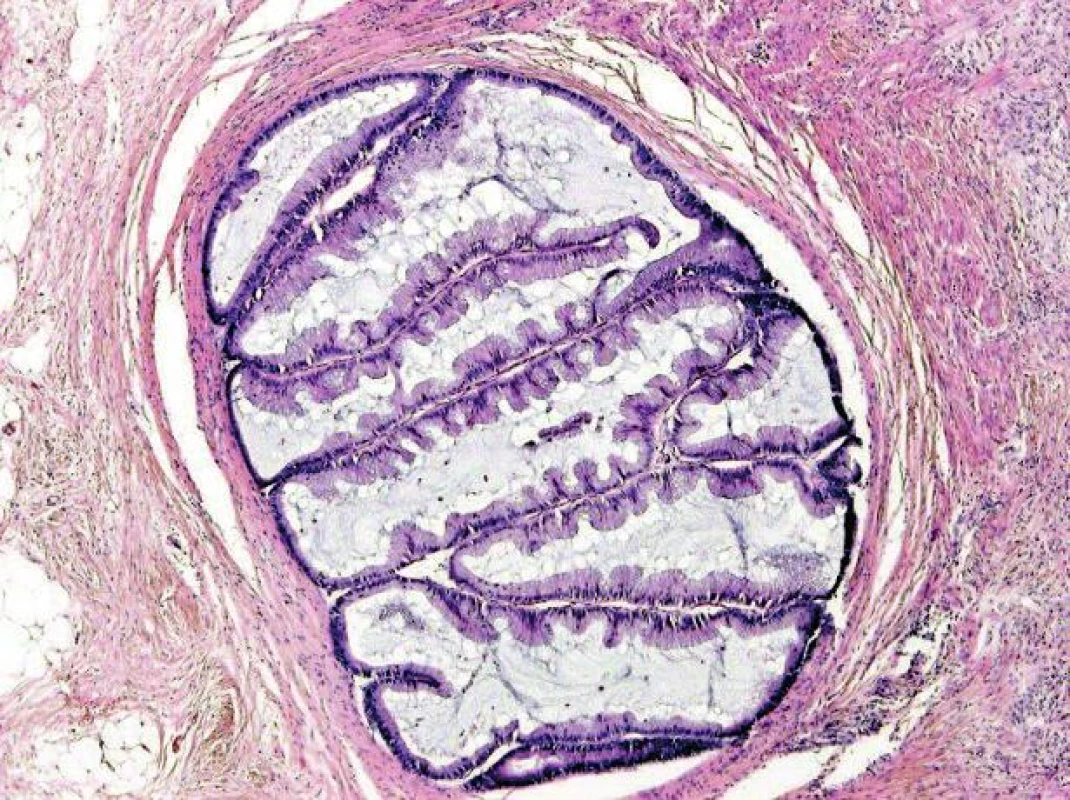
Serrated karcinom
Více než polovina serrated karcinomů se vyskytuje v céku a ve vzestupném tračníku – tzv. proximální serrated karcinomy, a přibližně jedna třetina v distálním tračníku a v rektu – tzv. distální serrated karcinomy. Prognóza karcinomů se v obou lokalizacích liší. Zatímco u proximálních karcinomů přežívá 5 let více než 70 % nemocných, u distálních serrated karcinomů je topouze 30 % (9,12). Prognóza serrated karcinomů souvisí s jejich molekulárně genetickým typem. Proximální serrated karcinomy vznikají převážně maligním zvratem SSA a odpovídají MSI-H fenotypu s MLH1 hypermetylací. Naproti tomu distální serrated karcinomy většinou vycházejí z TSA, jsou MSI-L/MSS (tj. mikrosatelitně stabilní) a jejich prognóza je méně příznivá (1,12). Makroskopicky se serrated karcinomy neliší od konvenčních kolorektálních karcinomů.
Histologicky se rozlišují 3 typy serrated karcinomů se serrated dysplazií (9,12):
- dobře nebo středně diferencovaný karcinom se serrated uspořádáním nádorových buněk s eozinofilní cytoplazmou a s mucinózní diferenciací (obr. 9). Tento typ představuje téměř 60% serrated karcinomů;
- mucinózní karcinom, který tvoří přibližně 20 % serrated nádorů. Extracelulární hlen zaujímá nejméně 50 % plochy nádoru, fokálně jsou patrné serrated struktury;
- špatně diferencovaný trabekulární, někdy mikropapilárně uspořádaný karcinom se serrated cytologií, rudimentárními serrated strukturami a s tendencí k lymfatické invazi (přibližně 7% serrated karcinomů).
Závěrem je možno říci, že serrated karcinogeneze tlustého střeva zahrnuje nově vymezené jednotky, které se od konvenčních adenomů a karcinomů liší nejen histologicky, ale i typem genetických mutací. Zatímco sesilní serrated adenom představuje poměrně přesně vymezenou lézi, tradiční serrated adenom je morfologicky a molekulárně geneticky značně variabilní. Diagnózu serrated karcinomu umožňuje přítomnost serrated struktur a vzhled nádorových buněk, odlišný od konvenční dysplazie.
PROHLÁŠENÍ
Autor práce prohlašuje, že v souvislosti s tématem, vznikem a publikací tohoto článku není ve střetu zájmů a vznik ani publikace článku nebyly podpořeny žádnou farmaceutickou firmou. Toto prohlášení se týká i všech spoluautorů.
Adresa pro korespondenci:
doc. MUDr. Alena Chlumská, CSc.
Bioptická lab., s.r.o.
Mikulášské nám. 4
32600 Plzeň,
Česká Republika
e-mail: chlumska@medima.cz
tel: +420 737 220 403
Zdroje
1. Bettington ML, Walker N, Rosty Ch, et al. A clinicopathological and molecular analysis of 200 traditional serrated adenomas. Mod Pathol 2015; 28 : 414-427.
2. Bordacahar B, Barret M, Terris B, et al. Sessile serrated adenoma: from identification to resection. Dig Liver Dis 2015; 47 : 95-102.
3. Crowder CD, Sweet K, Lehman A, Frankel WL. Serrated polyposis is an underdiagnosed and unclear syndrome. The surgical pathologist has a role in improving detection. Am J Surg Pathol 2012; 36 : 1178-1185.
4. Kwon HJ, Cho NY, Chang MS, Kim YS, Kang GH. Intermediate serrated polyp as an intermediate lesion of hyperplastic polyp and sessile serated polyp/adenoma in terms of morphological and molecular features. Hum Pathol 2014; 45 : 1759-1765.
5. Lash RH, Genta RM, Schuler CM. Sessile serrated adenomas: prevalence of dysplasia and carcinoma in 2139 patients. J Clin Pathol 2010; 63 : 681-686.
6. O´Brien MJ, Zhao Q, Yang S. Colorectal serrated pathway cancers and precursors. Histopathology 2015; 66 : 49-65.
7. Rosty Ch, Buchanan DD, Walsh MD, et al. Phenotype and polyp landscape in serrated polyposis syndrome: A series of 100 patients from genetics clinics. Am J Surg Pathol 2012; 36 : 876-822.
8. Snover DC. Update on the serrated pathway to colorectal carcinoma. Hum Pathol 2011; 42 : 1-10.
9. Bettington M, Walker N, Clouston A, Brown I, Leggett B, Whitehall V. The serrated pathway to colorectal carcinoma: current concepts and challenges. Histopathology 2013; 62 : 367-386.
10. Bettington M, Walker N, Rosty C, et al. Critical appraisal of the diagnosis of the sessile serrated adenoma. Am J Surg Pathol 2014; 38 : 158-166.
11. Chlumská A, Boudová L, Zámečník M. Sessile serrated adenomas of the large bowel. Clinicopathologic and immunohistochemical study including comparison with common hyperplastic polyps and adenomas. Cesk Patol 2006; 42 : 133-138.
12. Mäkinen MJ. Colorectal serrated adenocarcinoma.Histopathology 2007; 50 : 131-150.
13. Salaria SN, Streppel MM, Lee LA, Iacobuzio - Donahue CA, Montgomery EA. Sessile serrated adenomas: high-risk lesions? Hum Pathol 2012; 43 : 1808-1814.
14. Snover DC, Ahnen DJ, Burt RW, Odze RD. Serrated polyps of the colon and rectum and serrated polyposis. In: Bosman FT, Carneiro F, Hruban RH, Thiese ND, eds. WHO Classification of Tumors of the Digestive System (4th ed). Lyon: IARC; 2010 : 160-165.
15. Yang HM, Mitchell JM, Sepulveda JL, Sepulveda AR. Molecular and histologic considerations in the assessment of serrated polyps. Arch Pathol Lab Med 2015; 139 : 730-741.
16. Bettington ML, Chetty R. Traditional serrated adenoma: an update. Hum Pathol 2015; 46 : 933-938.
17. Kim MJ, Lee EJ, Suh JP, et al. Traditional serrated adenoma of the colorectum. Clinicopathologic implications and endoscopic findings of the precursor lesions. Am J Clin Pathol 2013; 140 : 898-911.
18. Wiland HO, Shadrach B, Allende D, et al. Morphologic and molecular characterization of traditional serrated adenomas of the distal colon and rectum. Am J Surg Pathol 2014; 38 : 1290-1297.
19. Hafezi-Bakhtiari S, Wang LM, Colling R, Serra S, Chetty R. Histological overlap between colorectal villous/tubulovillous and traditional serrated adenomas. Histopathology 2015; 66 : 308-313.
20. Bettington M, Walker N, Rosty C, et al. Serrated tubulovillous adenoma of the large intestine. Histopathology. In press 2016.
Štítky
Patologie Soudní lékařství Toxikologie
Článek Jaká je Vaše diagnóza?
Článek vyšel v časopiseČesko-slovenská patologie

2016 Číslo 1-
Všechny články tohoto čísla
- Serrated adenomy a karcinomy tlustého střeva
- Morfologie gastroezofageálního refluxu
- MONITOR aneb nemělo by vám uniknout, že
- Patologická diagnostika nerefluxních ezofagitid
- Zaostrené na gastrointestinálny trakt
- MONITOR aneb nemělo by vám uniknout, že
- Folikulový lymfóm a lymfóm z plášťových buniek v biopsiách orgánov žalúdočno-črevnej oblasti
- O teórii „tripolárneho života“
- Jaká je Vaše diagnóza?
- Hypoglykémie u solitárního fibrózního tumoru jater
- Jaká je Vaše diagnóza? Odpověď
- MONITOR aneb nemělo by vám uniknout, že
- Klinicko-patologická korelace imunoprofilu u difúzního velkobuněčného lymfomu, NOS - zkušenost z jednoho pracoviště
- MONITOR aneb nemělo by vám uniknout, že
- Kožná bunková reakcia po popálení medúzou
- MONITOR aneb nemělo by vám uniknout, že
- Postinfekční glomerulonefritida u dospělých: skrytá tvář dlouho známého onemocnění
- Česko-slovenská patologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Serrated adenomy a karcinomy tlustého střeva
- Morfologie gastroezofageálního refluxu
- Folikulový lymfóm a lymfóm z plášťových buniek v biopsiách orgánov žalúdočno-črevnej oblasti
- Kožná bunková reakcia po popálení medúzou
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: MUDr. Petr Výborný, CSc., FEBO
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



