-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Alkoholová choroba jater v terénní praxi
Alcohol-related liver disease in medical practice
The Czech Republic is still one of the European countries with above-average alcohol consumption. Excessive consumption has a dual effect – it affects the soul and body, leads to the development of alcohol dependence, withdrawal symptoms, psychosocial problems, significantly contributes to the damage of multiple organs. The "tolerable" dose is up to 20 g of pure alcohol per day for women and 30 g of alcohol per day for men. Regular use of higher doses leads to liver damage of varying severity. The first stage of damage is clinically insignificant steatosis, which progresses to steatohepatitis and liver fibrosis as abuse continues. The end stage is irreversible liver cirrhosis. Alcoholic hepatitis is also a serious condition. The basic therapeutic measure is absolute abstinence. The treatment of these patients is long, complicated and a multidisciplinary approach seems to be the most effective. The only treatment modality in patients with liver cirrhosis and long-term abstinence is liver transplantation.
Keywords:
alcohol – abuse – Cirrhosis – Steatosis – fibrosis – alcoholic hepatitis
Autoři: Jiří Hlušička; Radan Brůha
Působiště autorů: 4. interní klinika – klinika gastroenterologie a hepatologie 1. LF UK a VFN v Praze
Vyšlo v časopise: Čas. Lék. čes. 2022; 161: 84-89
Kategorie: Přehledový článek
Souhrn
Česko stále patří k evropským zemím s nadprůměrnou spotřebou etanolu, což má negativní vliv jak na somatické, tak mentální funkce jejích obyvatel. Vede to u nich k rozvoji syndromu závislosti na alkoholu, odvykacím stavům, psychosociálním problémům a prokazatelně se to podílí na poškození mnoha orgánů. Jako denní „tolerovaná“ dávka je považováno do 20 g čistého alkoholu u žen a do 30 g téhož u mužů. Pravidelné užívání jeho vyšších dávek vede k různě závažnému poškození jater. Jeho prvním stupněm je klinicky nezávažná steatóza, která při pokračujícím abúzu progreduje ve steatohepatitidu a jaterní fibrózu. Jeho konečným stádiem je ireverzibilní jaterní cirhóza. Závažným stavem je i alkoholová hepatitida. Základním terapeutickým opatřením je v těchto případech absolutní abstinence. Léčba těchto nemocných je dlouhá, komplikovaná a jako nejúčinnější se jeví multidisciplinární přístup. Jedinou léčebnou modalitou u pacientů s pokročilou jaterní cirhózou a prokazatelnou dlouhodobou abstinencí je transplantace jater.
Klíčová slova:
alkohol – cirhóza – fibróza – abúzus – steatóza – alkoholová hepatitida
ÚVOD
Alkohol, přesněji řečeno etanol nebo také etylalkohol, je nejstarší používanou psychoaktivní látkou na světě, jeho konzumace je ve většině zemí legální a veřejností akceptována (1). Kromě krátkodobého euforického účinku má při chronickém užívání na lidský organismus řadu dalších efektů. Ovlivňuje psyché – od syndromu závislosti na alkoholu, po změny a rozpad osobnosti; i tělo – způsobuje choroby kardiovaskulárního systému, pankreatu, je prokázaným karcinogenem. Jeho nadměrné užívání nemá efekt jen na jednotlivce, ale ovlivňuje i okolí postižených osob a je tedy problémem celospolečenským (2).
Tento příspěvek je zaměřen na problematiku alkoholové jaterní choroby (ALD – alcoholic liver disease, případně ARLD – alcohol-related liver disease). Nadměrná konzumace alkoholu může indukovat široké spektrum jaterních lézí, které zahrnují steatózu, steatohepatitidu, jaterní fibrózu, cirhózu a hepatocelulární karcinom. Klinicky významná je i alkoholová hepatitida (3).
Podle dat Světové zdravotnické organizace (WHO) z roku 2014 způsobuje každoročně škodlivé užívání alkoholu skoro 3,5 milionu úmrtí. Mezi muži se alkohol podílí na 7,6 % úmrtí; u žen na 4 % (4). Morbidita a mortalita související s nadměrným užíváním alkoholu má širokou geografickou variabilitu. Nejvíce případů je hlášeno v evropském regionu. Ačkoliv je průměrná světová spotřeba alkoholu 6,2 litru čistého alkoholu na osobu a rok, spotřeba v Evropě dosahuje 10,9 litrů na osobu a rok (4). Podle Českého statistického úřadu (ČSÚ) bylo v Česku v roce 2020 spotřebováno 166,7 l alkoholických nápojů na jednoho obyvatele. To odpovídá 9,7 l čistého lihu, z toho nejvíce v pivu (4,6 l), dále v lihovinách (2,8 l) a vínu (2,3 l). Alarmující je také skutečnost, že s konzumací alkoholu a opilostí mají u nás zkušenosti i děti a mladiství (5). Za posledních 25 let došlo k mírnému poklesu konzumace alkoholu ve středozápadních a středomořských státech Evropské unie. U středoevropských států, které jsou součástí Evropské unie, je spotřeba alkoholu stabilní (6). I nadále roste v zemích východní a jihovýchodní Evropy. Významný nárůst v posledních 20 letech byl pozorován i ve Finsku a Velké Británii (7). Ačkoli v rozvinutých zemích západního světa probíhají kampaně proti nadměrné spotřebě alkoholu, přijímají se opatření jako razantní zdražování, zákaz reklam na alkoholické nápoje v televizi, v naší zemi se i přes šokující spotřebu alkoholu nic podobného neděje. A i nadále platí bonmot uváděný v zahraničních turistických průvodcích, že v českých restauracích je pivo levnější než voda.
Alkohol souvisí se vznikem více než 200 onemocnění a různých typů zranění. Největší počet úmrtí je spojen s rozvojem kardiovaskulárních chorob. Následují úrazy, choroby gastrointestinálního traktu (zejména jaterní cirhóza) (4). Jaterní cirhóza toxonutritivní etiologie je u pacientů s jaterní chorobou v Evropské unii ve 41 % případech příčinou smrti (7). Těžký abúzus alkoholu je asociován s vysokým rizikem kardiomyopatie, arteriální hypertenze, síňových arytmií, cévní mozkové příhody (8). Alkohol je prokazatelný karcinogen (9).
METABOLISMUS ALKOHOLU
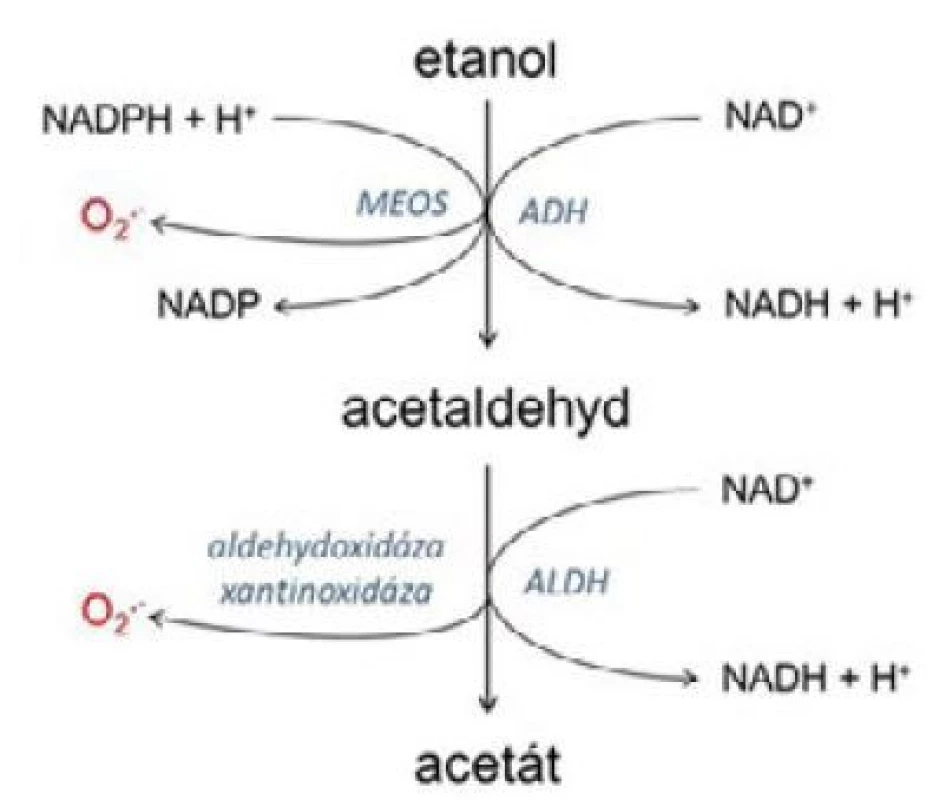
Etanol se vstřebává již v dutině ústní, nejvíce v tenkém střevě (10), je metabolizován hlavně v játrech, kde probíhá dvoustupňová oxidace. Účinkem alkoholdehydrogenázy se etylalkohol oxiduje na acetaldehyd, aldehyddehydrogenáza jej oxiduje na acetát (kyselinu octovou). Při této reakci je nezbytný koenzym nikotinamidadenindinukleotid NAD+, který je redukován na NADH. U osob s chronickým abúzem alkoholu je významná i alternativní jaterní metabolická dráha MEOS (mikrosomový etanol oxidující systém). Koenzymem je v tomto případě nikotinamidadenindinukleotidfosfát NADPH. Při jeho oxidaci se uvolňují volné kyslíkové radikály, které se mimo jiné mohou podílet na poškození hepatocytů. Metabolismus alkoholu je znázorněn na obr. 1 (11).
HODNOCENÍ ABÚZU, SCREENING
V souvislosti v poškozením jater není rozhodující druh alkoholického nápoje, ale množství čistého etanolu. Při každodenní konzumaci více než 30 g je zvýšené riziko jaterního poškození. Při dlouhodobé konzumaci více než 80 g/den je rozvoj jaterního poškození téměř jistý (12, 13). Ke zhodnocení příjmu alkoholu byl zaveden praktický termín „drink“ – dle různých autorů se jedná o množství nápoje s 10–16 g čistého alkoholu (12, 14). V našich podmínkách si tak pod pojmem jeden „drink“ můžeme představit přibližně 1/3 litru piva, 1 dcl vína, nebo 0,4 dcl destilátu. „Tolerovaná“ dávka alkoholu by neměla přesáhnout 2 „drinky“ denně u žen a 3 „drinky“ denně u mužů (přičemž počítáno je 10 g alkoholu na jeden drink). Toto množství alkoholu ještě nebylo ve studiích spojeno s významným rizikem vzniku jaterní cirhózy (15). Co se týče rizikovosti režimu pití – dle Askgaardové et al. je každodenní pití alkoholu spojeno s vysokým rizikem jaterní cirhózy (16). Nárazové pití se některými autory jeví jako méně rizikové (12, 17).
Alkoholovou jaterní chorobu lze tedy očekávat u žen a mužů konzumujících více než 20 a 30 g čistého alkoholu denně. Klinický stav nekoreluje s histologickým nálezem, a tak pacienti s pokročilými změnami jaterní tkáně nemusí mít žádné klinické symptomy ani laboratorní abnormality. Screening ARLD provádíme u všech osob s rizikovou mírou konzumace alkoholu (18). Na pracovištích pracujících s osobami se syndromem závislosti na etanolu by měl probíhat u všech pacientů, stejně tak u pacientů, kteří vykazují extrahepatální manifestaci jaterních chorob nebo známky dalších chorob asociovaných s nadměrnou konzumací alkoholu – pankreatitida, kardiomyopatie atd. (19). Jako laboratorní známky abúzu a nastupujícího jaterního onemocnění lze použít střední objem erytrocytu MCV, koncentraci jaterních transamináz nebo poměr aktivity enzymů aspartátaminotransferázy/alaninaminotransferázy (AST/ALT). Abúzus dále můžeme hodnotit pomocí anamnestických a psychologických dotazníků. Na celém světě se používá dotazník AUDIT (20), uvedený v tab. 1. Existují i další dotazníky, zájemci se s nimi mohou seznámit například na stránkách www.adiktologie.cz. U pacientů konzumujících alkohol v rizikovém množství nebo při pozitivním nálezu v laboratorních vyšetřeních bychom měli zvážit zobrazovací metody, které jsou schopny odhalit pokročilou jaterní chorobu, ultrasonografii, a především jaterní elastografii. V případě jasných známek ARLD bychom měli pacienta odeslat ke specialistovi (na screening portální hypertenze, specifickou terapii, psychologickou/psychiatrickou péči).
Tab. 1. Dotazník AUDIT – C 
(kompletní dotazník dostupný na www.adiktologie.cz, 20) Při posuzování konzumace alkoholu využíváme přímé a nepřímé markery. Jelikož stanovení gama-glutamyltransferázy (GGT), alaninaminotransferázy (ALT), aspartátaminotransferázy (AST) a středního objemu erytrocytů (MCV) je snadné a levné, zůstávají tyto nepřímé markery nejčastěji používanými pro časnou detekci ARLD. Jejich senzitivita a specifita je však velmi nízká (21). Dalším nepřímým markerem je karbohydrát deficientní transferin (CDT). CDT je pozitivní jen u těžkých pijáků konzumujících 50–80 g alkoholu denně po dobu alespoň 2 týdnů, navíc pacienti s jaterní cirhózou mají často falešně negativní výsledek (22).
Mezi přímé markery konzumace etanolu patří hojně užívaný etylglukuronid. Zůstává v moči až 80 hodin po požití alkoholu. Toto vyšetření má vysokou senzitivitu i specifitu. Prokáže tedy i požití menšího množství alkoholu (23). K přímým metodám logicky řadíme i stanovení koncentrace etanolu v krvi a stanovení alkoholu ve vydechovaném vzduchu. Dlouhodobé nadužívání alkoholu vede rovněž k sekundární dyslipoproteinemii, ke zvýšení hodnot kyseliny močové (24).
JATERNÍ POŠKOZENÍ Z NADMĚRNÉHO UŽÍVÁNÍ ALKOHOLU
Steatóza a steatohepatitida
Konzumace etylalkoholu může vést k lehkým změnám ve smyslu steatózy a přecházet dál ve steatohepatitidu, fibrózu, v cirhózu až hepatocelulární karcinom. Mimo alkohol se na urychlení těchto patologických změn mohou podílet i další faktory – obezita, diabetes mellitus, kouření, virové infekce, hepatotoxické léky, přetížení organismu železem a samozřejmě i vlivy genetické. S vyšším rizikem alkoholového poškození jater je asociován polymorfismus v genu PNPLA3 (25).
Nejčastějším typem jaterního poškození u pacientů s abúzem alkoholu je steatóza, „ztukovatění“ jater. Jde o cytoplazmatické nahromadění triacylglycerolů v hepatocytech, přičemž by v nich mělo být uloženo více než obvyklých 5 % tuku. Při pokračujícím abúzu alkoholu změny progredují ve steatohepatitidu. Jak název napovídá, hromadění tuku doprovázejí zánětlivé změny vedoucí k zániku hepatocytů (v biopsii kromě ložisek zánětu často pozorujeme tzv. balónovitých /ballooning/ hepatocytů).
V tomto stádiu onemocnění mohou být pacienti zcela asymptomatičtí, jediným jejich steskem může být „tlak“ v pravém podžebří, nadýmání, únava. V diagnostice steatózy, kromě neinvazivních ukazatelů, hraje hlavní roli ultrasonografické vyšetření. K její kvantifikaci lze použít nové metody, o nichž je pojednáno v jiném textu tohoto vydání ČLČ (viz článek „Možnosti diagnostiky jaterní steatózy“). V terapii je zásadní absolutní abstinence. Hepatoprotektiva mají sporný efekt (24, 25).
Alkoholová hepatitida
Alkoholová hepatitida (AH) je klinický syndrom charakterizovaný zánětlivou reakcí/steatohepatitidou u osob užívajících > 80 g alkoholu denně, častější je u mužů (26). Není výjimkou, že se obtíže s ní spojené dostaví dny až týdny po posledním alkoholovém excesu. Klinicky je AH charakterizovaná ikterem, únavou, nevolností, nechutenstvím či teplotou. V těžších případech mohou pacienti vyvinout encefalopatii či koagulopatii. Tyto stavy jsou zatíženy vysokou mortalitou (25).
V úvodu je vždy nutné v rámci diferenciální diagnostiky vyloučit ostatní možné příčiny jaterní léze, zejména virové hepatitidy, toxické poškození (vč. léků) a autoimunitní onemocnění. Diagnóza je stanovena na základě klinické symptomatiky, laboratorního vyšetření (neutrofilie, hyperbilirubinémie, elevace transamináz) a anamnézy abúzu alkoholu. Někdy je nezbytné doplnit i jaterní biopsii. K posouzení závažnosti onemocnění bylo vypracováno několik skórovacích systémů. Jejich přehled podává tab. 2. Nejčastěji využívaným je Maddrey’s discriminant function, v modifikované podobě (mDF) se používá od roku 1989. Vypočte se následovně: mDF = [4,6 x (rozdíl protrombinového času pacienta a normálu)] + sérový bilirubin (mg/dl). Jeho cut-off hodnota je 32 (25, 27).
Tab. 2. Nejčastěji užívané prognostické skórovací systémy u alkoholové hepatitidy (25) 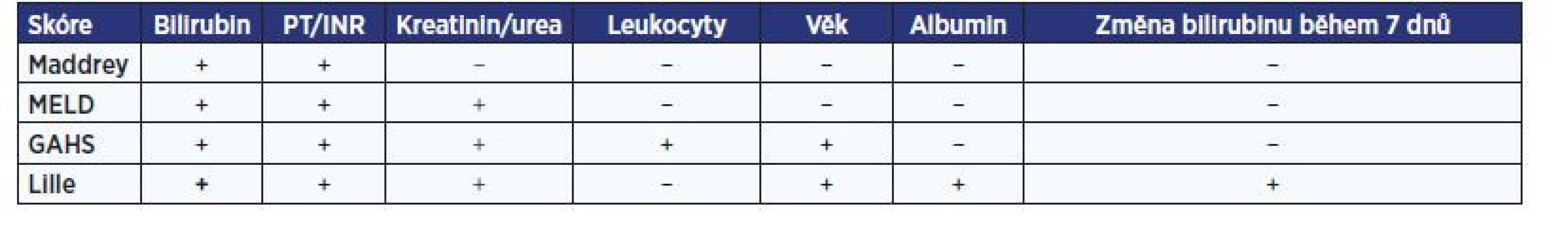
Základem terapie alkoholové hepatitidy je pochopitelně absolutní alkoholová abstinence. Pro riziko Wernickeho encefalopatie je doporučováno podávání vitaminů skupiny B. Důležitá je hydratace a přiměřená výživa. Denní doporučený energetický příjem je 150–165 kJ/kg, denní příjem proteinů 1,2–1,5 g/kg (28). U jaterní encefalopatie podáváme laktulózu a rifaximin. Aktivně pátráme po infekcích, u alkoholové hepatitidy se mohou vyskytnou i ty atypické. Nedílnou součástí terapie je aktivní mikrobiologická surveillance a časné zahájení antibiotické terapie. Při těžkém průběhu je indikován prednison. Glukokortikoidy jsou indikovány při Maddrey skóre ≥ 32 a GAHS (Glasgow Alcoholic Hepatitis Score) ≥ 9. Terapeutický postup u alkoholové hepatitidy podle Evropské asociace pro studium jater (EASL) z roku 2018 je znázorněn na obr. 2 (24, 25).
Obr. 2. Nejčastěji užívané prognostické skórovací systémy u alkoholové hepatitidy (25) 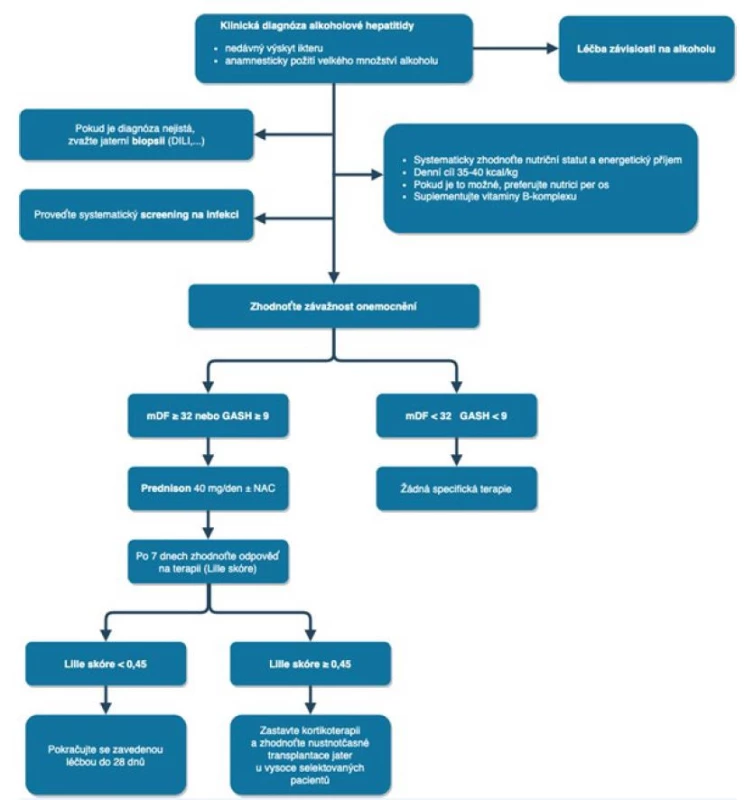
Velmi závažná je prognóza, pokud alkoholová hepatitida nasedne na již preexistující chronické onemocnění jater (ACLF – acute on chronic liver failure). To často vede k orgánovému selhání a systémové zánětlivé odpovědi organismu. Terapeuticky se zde uplatňují extrakorporální systémy podpory jater. Definitivní léčbou je transplantace jater (29, 30).
Jaterní fibróza a cirhóza způsobená alkoholem
Jaterní fibróza je definována jako nadměrné ukládání vazivové hmoty v játrech. Mimo to při ní dochází i k zánětlivým změnám, nekrózám hepatocytů, a hlavně k poruše mikrocirkulace krve a rozvoji portální hypertenze. Fibróza je stav ještě zvrátitelný. Účinná v léčbě je pouze abstinence. Pokud však abúzus pokračuje dál, stav progreduje do jaterní cirhózy. Diagnostika jaterní fibrózy se dnes dominantně opírá o neinvazivní metody, ať již sérové markery či skóre, především o sonografii a jaterní elastografii, metodu založenou na měření tuhosti jaterní tkáně. Jako levná a snadno dostupná metoda posouzení pokročilosti jaterní fibrózy slouží např. skóre FIB-4 (24, 25).
U jaterní cirhózy jsou již přítomné pokročilé změny jaterní architektoniky – extenzivní fibrotická přestavba, formace uzlů, abnormální průtok krve orgánem. V počátečních stádiích může být cirhóza i klinicky němá, bývají přítomny pouze nespecifické projevy jako únava, nechutenství. Později se objevují znaky typické pro pokročilé onemocnění – hepatomegalie a splenomegalie, ascites, sarkopenie, endokrinní projevy (gynekomastie, vymizení ochlupení u mužů, impotence, testikulární atrofie), palmární erytém, pavoučkové névy, projevy koagulopatie. Při dekompenzaci se objevuje ikterus, ascites, krvácení z jícnových varixů, hepatorenální syndrom, encefalopatie, kachexie, infekce.
K posouzení závažnosti jaterní cirhózy se používá několik skórovacích systémů – nejběžnější jsou Childovo-Pughovo skóre a skóre MELD (Mayo End-stage Liver Disease) (25). Alkoholová jaterní cirhóza je spojena s vyšší pravděpodobností vzniku hepatocelulárního karcinomu (31). Klinická péče o pacienty s ARLD cirhózou se zaměřuje na alkoholovou abstinenci, nutriční podporu, primární a sekundární profylaxi cirhotických komplikací. Pacienty zařazujeme do screeningu hepatocelulárního karcinomu, každých 6 měsíců se u nich provádí ultrasonografické vyšetření. Terapie jaterní cirhózy přesahuje rámec tohoto článku. Je důležité uvést, že u pacientů s ARLD cirhózou se jedná o duální patologii – léčíme komplikace jaterní cirhózy, ale také závislost na alkoholu. Řada studií se snažila ověřit účinek hepatoprotektiv, avšak žádná ze zkoušených látek (sylimarin, propyltiouracil) zlepšení jaterních funkcí neprokázala (25). U nemocných s pokročilou jaterní cirhózou, kteří abstinují alespoň 6 měsíců, lze uvážit transplantaci jater (24, 25). Roční přežití s touto diagnózou je 89 %, pětileté 75 % (32). Histologický obraz jaterní steatózy a cirhózy je uveden na obr. 3.
Obr. 3. Histologický obraz jaterní steatózy a cirhózy 
Léčba závislosti na alkoholu je multioborová, dlouhodobá a komplikovaná. Hlavní slovo při ní má adiktolog. Využívá se k ní jak farmakoterapie, tak psychoterapie, kognitivně-behaviorální metody. Dobře známý disulfiram je ovšem hepatotoxický. Dnes je na trhu celá řada látek s anticravingovým účinkem, které snižují „bažení“ (naltrexon, nalmefen, akamprosát, topiramát, baklofen aj.). Baklofen (agonista GABA-B receptorů) byl zatím jako jediný z uvedených preparátů hodnocen u pacientů s významným jaterním postižením (25, 33). K léčbě syndromu z odnětí se využívají benzodiazepiny, hlavně molekuly s delším poločasem (diazepam), u geriatrických pacientů a pacientů s jaterními chorobami jsou preferovány molekuly s kratším eliminačním poločasem (oxazepam). Užívání těchto léčiv je opět spojeno s rizikem vzniku tolerance a syndromu závislosti (25).
ZÁVĚR
Nadměrná konzumace alkoholu prokazatelně vede k poškození organismu. Jeho chronické užívání je toxické pro centrální i periferní nervový systém, játra, kardiovaskulární aparát, slinivku. V játrech vyvolává změny od relativně benigní steatózy až po ireverzibilní cirhózu, která nemocným výrazně zkracuje život. Závažným stavem je i alkoholová hepatitida. Dlouhodobé užívání alkoholu vede k rozvoji psychosociálních problémů.
Terapie je komplexní, dlouhodobá a komplikovaná. Probíhá ve spolupráci gastroenterologa/hepatologa a adiktologa. Jejím základem je absolutní abstinence. Při ireverzibilním poškození jater je jediným možným řešením transplantace. Spotřeba alkoholu v Česku je stále nad průměrem států Evropské unie. Zatímco u našich západních sousedů probíhají účinné kampaně za snížení spotřeby etanolu, u nás tomu tak bohužel není.
Čestné prohlášení
Autoři nedeklarují žádný střet zájmů. Text nebyl vytvořen v rámci žádného grantového projektu.
Zkratky
ACLF akutní selhání jater nasedající na chronické poškození jater
ADH alkoholdehydrogenáza
AH alkoholová hepatitida
ALD/ARLD alkoholová jaterní choroba
ALDH aldehyddehydrogenáza
ALT alaninaminotransferáza
AST aspartátaminotransferáza
AUDIT Alcohol Use Disorders Identification Test
CDT karbohydrát-deficientní transferin
GAHS Glasgow Alcoholic Hepatitis Score
GGT gama-glutamyltransferáza
MCV střední objem erytrocytu
mDF modified Maddrey’s discriminant function
MELD Mayo End-stage Liver Disease
MEOS mikrosomový etanol oxidující systém
NAD/NADH nikotinamidadenindinukleotid
NADPH nikotinamidadenindinukleotidfosfát
NAFLD nealkoholová tuková jaterní choroba
Adresa pro korespondenci:
MUDr. Jiří Hlušička, Ph.D.
4. interní klinika 1. LF UK a VFN
U Nemocnice 499/2, 128 08 Praha 2
Tel.: 774 124 909
e-mail: jiri.hlusicka@vfn.cz
Zdroje
- Hunt S, Climer J. Encyclopedia of Substance Abuse Prevention, Treatment, and Recovery. Sage, Thous and Oaks, 2009.
- World Health Organization. Global status report on alcohol and health 2018. WHO Library Cataloguing in Publication Data, Ženeva, 2019.
- Gao B, Bataller R. Alcoholic liver disease: pathogenesis and new therapeutic targets. Gastroenterology 2011; 141(5): 1572–1585.
- World Health Organization. Global status report on noncommunicable diseases 2014. WHO Library Cataloguing in Publication Data, Ženeva, 2014.
- Mravčík V, Chomyová P, Černíková T a kol. Zpráva o alkoholu v České republice 2021. Úřad vlády ČR, Praha, 2021.
- Shield KD, Rylett M, Rehm J. Public health successes and missed opportunities. Trends in alcohol consumption and attributable mortality in the WHO European Region 2014. Centre for Addiction and Mental Health, Ontario, 2016, 1990 : 20–22.
- Sheron N. Alcohol and liver disease in Europe–Simple measures have the potential to prevent tens of thousands of premature deaths. J Hepatol 2016; 64(4): 957–967.
- Klatsky AL. Alcohol and cardiovascular diseases: where do we stand today? J intern Med 2015; 287(3): 238–250.
- Bagnardi V, Rota M, Botteri E et al. Alcohol consumption and site-specific cancer risk: a comprehensive dose–response meta-analysis. Brit J Cancer 2015; 112(3): 580–593.
- Waszkiewicz N, Zalewska A, Szulc A et al. The influence of alcohol on the oral cavity, salivary glands and saliva. Pol Merkur Lekarski 2011; 2011 : 69–74.
- Racek J, Rajdl D. Klinická biochemie. Základy toxikologie. Galén, Praha, 2021.
- Brůha R, Dvořák K, Petrtýl J a kol. Alkoholové poškození jater. Medicína pro praxi 2009; 6(3): 144–146.
- Bellentani S, Saccoccio G, Costa G et al. Drinking habits as cofactors of risk for alcohol induced liver damage. Gut 1997; 41(6): 845–850.
- Dietary Guidelines for Americans. US Department of Health and Human Services and US Department of Agriculture, Des Moines, 2015; 7.
- World Health Organization. Food-based dietary guidelines in the WHO European Region. No. EUR/03/5045414. WHO Regional Office for Europe, Ženeva, 2003.
- Askgaard G, Grønbæk M, Kjær MS et al. Alcohol drinking pattern and risk of alcoholic liver cirrhosis: a prospective cohort study. J Hepatol 2015; 62(5): 1061–1067.
- Åberg F, Helenius-Hietala J, Puukka P et al. Binge drinking and the risk of liver events: a population-based cohort study. Liver Int 2017; 37(9): 1373–1381.
- Askgaard G, Leon DA, Kjaer MS et al. Risk for alcoholic liver cirrhosis after an initial hospital contact with alcohol problems: a nationwide prospective cohort study. Hepatology 2017; 65(3): 929–937.
- Torruellas C, French SW, Medici V et al. Diagnosis of alcoholic liver disease. World J Gastroenterol 2014; 20(33): 11684.
- Babor TF, de la Fuente JR, Saunders J. Test pro identifikaci poruch působených užíváním alkoholu, WHO, Ženeva, 1989. Dostupné na: www.adiktologie.cz/test-pro-identfikaci-poruch-pusobenych-uzivanim-alkoholu-audit
- Seitz HK. Additive effects of moderate drinking and obesity on serum g-glutamyl transferase. Am J Clin Nutr 2006; 83(6): 1252–1253.
- Helander A, Wielders J, Anton R et al. Standardisation and use of the alcohol biomarker carbohydrate-deficient transferrin (CDT). Clin Chim Acta 2016; 459 : 19–24.
- Wurst FM, Wiesbeck GA, Metzger JW et al. On sensitivity, specificity, and the influence of various parameters on ethyl glucuronide levels in urine – results from the WHO/ISBRA study. Alcohol Clin Exp Res 2004; 28(8): 1220–1228.
- Ehrmann J, Aiglová K, Urban O a kol. Onemocnění jater související s alkoholem (ALD). Vnitřní lékařství 2020; 66(5): e3–e15.
- European Association for the Study of the Liver. EASL Clinical Practice Guidelines: Management of alcohol-related liver disease. J Hepatol 2018; 69(1): 154–181.
- Naveau S, Giraud V, Borotto E et al. Excess weight risk factor for alcoholic liver disease. Hepatology 1997; 25(1): 108–111.
- Phillips M, Curtis H, Portmann B et al. Antioxidants versus corticosteroids in the treatment of severe alcoholic hepatitis – a randomised clinical trial. J Hepatol 2006; 44(4): 784–790.
- Plauth M, Cabre E, Riggio O et al. ESPEN guidelines on enteral nutrition: liver disease. Clin Nutr 2006; 25(2): 285–294.
- Michelena J, Altamanirano J, Abraldes JG et al. Systemic inflammatory response and serum lipopolysaccharide levels predict multiple organ failure and death in alcoholic hepatitis. Hepatology 2015; 62(3): 762–772.
- Kjaergard LL, Liu J, Als-Nielsen B et al. Artificial and bioartificial support systems for acute and acute-on-chronic liver failure: a systematic review. JAMA 2003; 289(2): 217–222.
- Mancebo A, Gonzalez-Dieguez ML, Cadahia V et al. Annual incidence of hepatocellular carcinoma among patients with alcoholic cirrhosis and identification of risk groups. Clin Gastroenterol Hepatol 2013; 11(1): 95–101.
- Kim WR, Lake JR, Smith JM et al. OPTN/SRTR 2016 annual data report: liver. Am J Transplant 2018; 18(Suppl. 1): 172–253.
- Routhu M, Hosák L. Alkoholismus a abúzus alkoholu. In: Hůlek P, Urbánek P (eds.). Hepatologie (3. vyd.). Grada, Praha, 2018.
Štítky
Adiktologie Alergologie a imunologie Angiologie Audiologie a foniatrie Biochemie Dermatologie Dětská gastroenterologie Dětská chirurgie Dětská kardiologie Dětská neurologie Dětská otorinolaryngologie Dětská psychiatrie Dětská revmatologie Diabetologie Farmacie Chirurgie cévní Algeziologie Dentální hygienistka
Článek ÚVODEMČlánek EDITORIALČlánek Jaterní testyČlánek Elastografie jaterČlánek Statiny a játraČlánek Současná léčba hepatitidy C
Článek vyšel v časopiseČasopis lékařů českých
Nejčtenější tento týden
2022 Číslo 2- Takrolimus v terapii atopické dermatitidy a analýza jeho nákladové efektivity ve srovnání s kortikosteroidní léčbou
- Trombóza portální žíly jako komplikace infekce COVID-19 – kazuistika
- Sympozium věnované péči o pacienty s ALS jako odrazový můstek pro zlepšení kvality jejich života
- Doc. Jitka Fricová: V USA nasazovali fentanyl poměrně nekriticky, v Česku je situace jiná
- Protilátky anti-IgE v léčbě mnohočetných potravinových alergií
-
Všechny články tohoto čísla
- ÚVODEM
- EDITORIAL
- Jaterní testy
- Možnosti diagnostiky jaterní steatózy
- Elastografie jater
- Ztukovatění jater spojené s metabolickou dysfunkcí (MAFLD) jako přesnější název pro NAFLD – společné aspekty patogeneze
- Diagnostika nealkoholové tukové nemoci jater a její aktivní screening v rizikových skupinách
- Současné možnosti léčby nealkoholového ztukovatění jater (NAFLD)
- Statiny a játra
- Alkoholová choroba jater v terénní praxi
- Současná léčba hepatitidy C
- Klinická obezitologie – nejen Základy
- Nutriční návyky studentů lékařských fakult
- Za profesorem Peterem Krištúfkem, čestným prezidentem SLS
- Časopis lékařů českých
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Revma Focus: Spondyloartritidy
nový kurz
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Autoři: prof. MUDr. Pavel Horák, CSc., doc. MUDr. Ludmila Brunerová, Ph.D., doc. MUDr. Václav Vyskočil, Ph.D., prim. MUDr. Richard Pikner, Ph.D., MUDr. Olga Růžičková, MUDr. Jan Rosa, prof. MUDr. Vladimír Palička, CSc., Dr.h.c.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání