-
Články
Top novinky
Reklama- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
Top novinky
Reklama- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Top novinky
ReklamaRabdomyolýza – kdy na ni myslet?
Autoři: V. Černý
Vyšlo v časopise: Anest. intenziv. Med., 26, 2015, č. 4, s. 236-238
Kategorie: Postgraduální vzdělávání - Kapitoly z klinické fyziologie
Rabdomyolýza (RM) je definována jako „komplexní porucha organismu v důsledku rychlé dezintegrace kosterního svalstva způsobené poškozením tohoto svalstva“.
Destrukce svalové tkáně vede k vyplavení intracelulárních součástí svalů – myoglobin, kreatin kináza (CK), aldoláza, laktát dehydrogenáza (LDH), elektrolyty – do krevního oběhu a extracelulárního prostoru. Projevy RM mohou být na straně jedné zcela bez klinických příznaků, pouze se vzestupem hodnot CK, až po život ohrožující stav vyúsťující v multiorgánové selhání.
Vznik RM
V klinické praxi oboru anesteziologie a intenzivní medicína dominují jednoznačně mechanismy přímého poškození svalů, nelze však zde zapomínat na netraumatické mechanismy vzniku RM, jako jsou např.:
- nehybnost, upoutání na lůžko;
- febrilní stav (včetně jednotek typu maligní hypertermie nebo neuroleptický maligní syndrom).
Diagnostika RM
Základní klinické příznaky bez ohledu, zda jde o traumatickou nebo netraumatickou RM) jsou:
- svalová slabost (lze-li ji u pacienta posoudit),
- myalgie různého stupně,
- tmavá moč (pigmenturie).
V anglosaské literatuře se uvedené příznaky popisují jako „klasická klinická triáda“ (myalgia, weakness, myoglobinuria), nicméně uvedenátriáda se vyskytuje v méně než 10 % případů RM a více než 50 % pacientů s později diagnostikovanou RM neudává ani myalgie, ani svalovou slabost. Nejvíce senzitivním diagnostickým nástrojem je vyšetření hladiny kreatinfosfokinázy (CK), za předpokladu absence jiných příčin vzestupu CK jako je např. ischémie myokardu nebo mozku). Přestože neexistuje jednoznačná a přímá korelace mezi hladinami CK a závažností RM, hodnoty CK nad 5 000 IU/l jsou považovány za známku závažné RM.
Vztah RM a vzniku renálního poškození
Odhaduje se, že u 10–40 % pacientů s RM dojde k rozvoji renální dysfunkce až selhání (ARF) a že cca 15 % případů ARF je ve vazbě na RM. U dětí je riziko vzniku ARF při RM pravděpodobně vyšší (42–50%).
Patofyziologie
Jakkoliv bývá etiologie RM často rozpoznatelná, přesné mechanismy rozvoje nekrózy svalů a následných změn nejsou známy. Bez ohledu na povahu iniciálního inzultu jsou hlavními mechanismy výsledného poškození: přímé poranění svalů a energetické selhání na úrovni myocytů. Sodíková-draslíková pumpa při svém selhání nestačí udržet koncentraci sodíku intracelulárně, dochází k akumulaci sodíku, vápníku a následně vody, výsledkem je strukturální destrukce myocytu. Akumulace vápníku vede rovněž k udržování myofibril v kontraktilním stavu, což dále zvyšuje spotřebu energie a prohlubuje nepoměr mezi dodávkou a potřebou ATP. Jako klíčové „koncové“ mechanismy RM jsou zmiňovány:
- peroxidace lipidů, proteinů a DNA;
- mitochondriální dysfunkce;
- excesivní kontraktibilita myocytů.
Příčiny RM
Teoreticky, jakákoliv zátěž svalů může inicio-vat RM. V klinické medicíně u dospělých je RM spojována nejčastěji s:
- požitím alkoholu,
- požitím farmak,
- neuroleptickým maligním syndromem (MNS),
- traumatem,
- imobilitou jakékoliv etiologie.
U dětí je RM spojována nejčastěji s:
- virovou myozitidou (literárně až 1/3 dětí s RM),
- traumatem,
- fyzickou námahou,
- předávkováním farmaky.
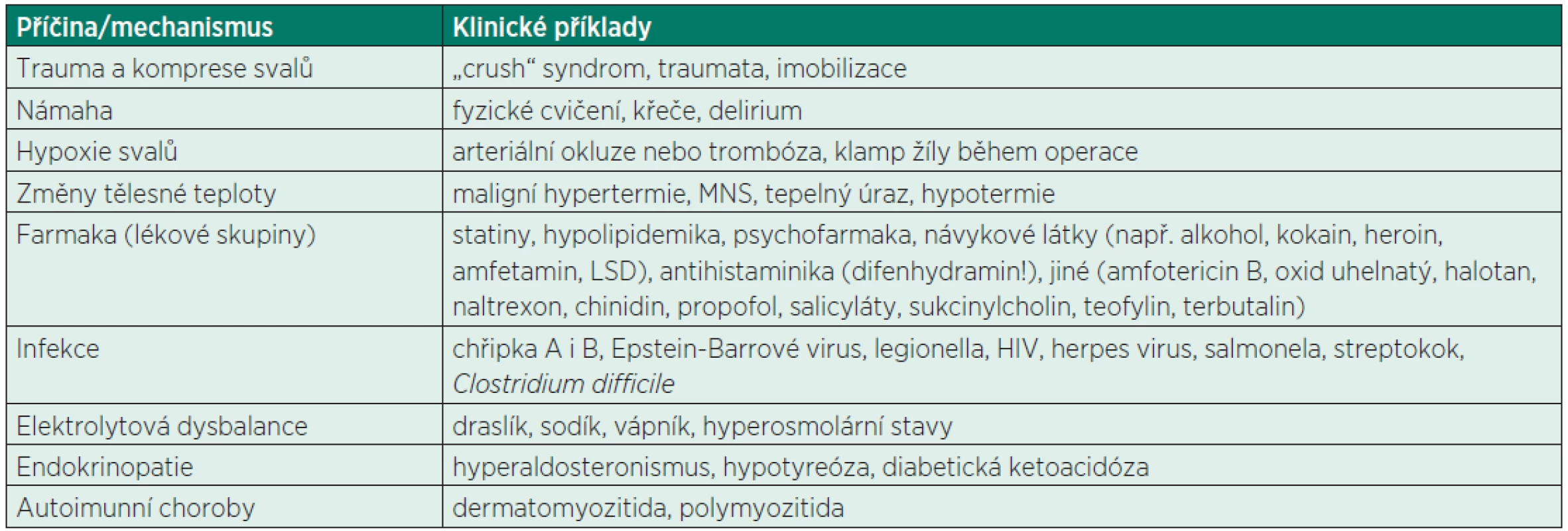
Tabulka 1 ukazuje přehled nejčastějších možných příčin RM.
Statiny a RM
Statiny indukovaná myopatie/myalgie (SIM) je reálně se vyskytující komplikace, na kterou by měli být všichni pacienti užívající statiny upozorněni. Incidence je udávána v randomizovaných studiích 1,5–5%, v klinické praxi je výskyt odhadován až na 33 % všech pacientů se statiny. Mezi hlavní rizikové faktory SIM patří:
- vysoké dávky statinů,
- vyšší věk,
- ženské pohlaví,
- jaterní dysfunkce,
- renální dysfunkce,
- diabetes mellitus.
The FDA Adverse Events Reporting System udává výskyt RM v souvislosti se statiny 1,07 na milion pacientů, za statin s nejnižším rizikem RM je považován pravastatin. Výskyt RM je udáván u simvastatinu 36%, cerivastatinu 32%, atorvastatinu 12%, pravastatinu 12%, lovastatinu 6%, fluvastatinu 2%.
Fyzická námaha/zátěž a RM
Odlišení vzestupu CK jako známky RM nebo „fyziologické reakce“ organismu/svalů na námahu je obtížné. Fyzická námaha může zvýšit i u zdravého člověka hladiny CK až na 10násobek normy. Riziko vzniku RM se zvyšuje, pokud zátěž probíhá současně za vyšší okolní teploty a zvýšené vlhkosti vzduchu.
Teplota, maligní hypertermie a NMS
Prolongovaná expozice vyšším teplotám je jednoznačným rizikovým faktorem vzniku RM, zejména ve spojení s námahou. Vyšší výskyt RM ve spojení s námahou a horkem se vyskytuje převážně u mužů, u žen existuje pravděpodobně protektivní efekt vyšší hladiny estrogenů. Výskyt RM v kontextu horka a fyzické námahy u žen by měl vést k aktivnímu hledání svalového onemocnění u těchto žen.
Svalová ischémie a RM
Prolongovaná lokální nebo systémová hypoxie mohou vést k rozvoji RM, vzácně i hypotermie (mechanismem redukce perfuze) může iniciovat RM.
Propofol a RM
Tzv. propofol infusion syndrome (PRIS) byl původně popsán u dětí, vyskytuje se ale i dospělých pacientů v intenzivní péči. Jeho výskyt byl popsán i u zdravých jedinců po podání i jednorázové, extrémně vysoké dávky propofolu. PRIS je podle současných názorů definován jako metabolická acidóza nebo kardiální dysfunkce s jedním nebo více dalšími příznaky, mezi které patří RM, zvýšená hladina triglyceridů anebo renální selhání. Za zmínku stojí, že u kriticky nemocných pacientů, u nichž byl popsán PRIS (výskyt je udáván cca u 1 % všech pacientů s podávaným propofolem pro sedaci) jich bylo 91 % na vazopresorech. Prediktorem rozvoje PRIS se zdá spíše celková dávka propofolu než rychlost jeho podávání.
Možné závažné komplikace RM
- Akutní renální selhání (myoglobinové válce a hypovolémie).
- Kompartment syndrom.
- Hypovolémie (sekvestrace tekutiny do svalů).
- Hyperkalémie.
- Hypokalcémie (časně).
- Hyperkalcémie (pozdně).
- Hyperfosfatémie.
- Diseminovaná intravaskulární koagulace (poškození svalů vede k vyplavení tromboplastinu).
Základní principy „léčby“ RM
- Eliminace inzultu.
- Obnovení normovolémie a korekce případné elektrolytové dysbalance.
- Alkalizace moči.
- Udržení svalové integrity odstraněním kompartment syndromu, je-li přítomen.
- Reverze abnormální vazodilatace, zejména korekcí kalémie a acidózy.
Body k zapamatování
- Lékaři by měli mít „high index of suspicion“ u všech pacientů v rizikovém kontextu pro RM a s triádou myalgie, weakness a pigmenturie.
- Pacienti v kritickém stavu bez ohledu na vyvolávající inzult mají vyšší riziko RM.
- Zvýšení hladiny CK nad 5násobek normy je považováno nejčastěji za práh pro diagnózu RM odpovídající klinickému kontextu:
- CK (poločas cca 1,5 dne) zůstává při RM zvýšena déle než hladiny myoglobinu (poločas 2–4 hodiny),
- plazmatická koncentrace myoglobinu není tak senzitivní jako hodnoty CK,
- myoglobin v moči vede k pozitivitě testu na erytrocyty v moči.
- Hlavní součástí léčby RM jsou:
- eliminace příčiny RM,
- normovolémie,
- alkalizace moči.
Prof. MUDr. Vladimír Černý, Ph.D., FCCM
Klinika anesteziologie, perioperační a intenzivní medicíny
Univerzita J. E. Purkyně v Ústí nad Labem
Masarykova nemocnice v Ústí nad Labem
Institut postgraduálního vzděláváníve zdravotnictví
Centrum pro výzkum a vývoj
Fakultní nemocnice Hradec Králové
Dept. of Anesthesia, Pain Managementand Perioperative Medicine
Dalhousie University, Halifax, Canada
Klinika anesteziologie, resuscitacea intenzivní medicíny
Univerzita Karlova v Praze
Lékařská fakulta v Hradci Králové
e-mail: cernyvla1960@gmail.com
Zdroje
1. Mirrakhimov AE, Voore P, Halytskyy O, Khan M, Ali AM. Propofol infusion syndrome in adults: a clinical update. Crit Care Res Pract. 2015;2015 : 260385.
2. Torres PA, Helmstetter JA, Kaye AM, Kaye AD. Rhab-domyolysis: pathogenesis, diagnosis, and treatment. Ochsner J. 2015 Spring;15(1):58–69. Review.
3. Ayach T, Nappo RW, Paugh-Miller JL, Ross EA. Postoperative hyperkalemia. Eur J Intern Med. 2015 Mar;26(2):106–111.
4. Magni P, Macchi C, Morlotti B, Sirtori CR, Ruscica M. Risk identification and possible countermeasures for muscle adverse effects during statin therapy. Eur J Intern Med. 2015 Mar;26(2):82–88.
5. Chan EK, Kornberg AJ, Ryan MM. A diagnostic approach to recurrent myalgia and rhabdomyolysis in children. Arch Dis Child. 2015 Jan 29; pii: archdischild-2014-307663.
6. Feng Q. Approach to clinical and genetic characterization of statin-induced myopathy. Methods Mol Biol. 2014;1175 : 67–90.
7. Sharp LJ, Haller RG. Metabolic and mitochondrial myopathies. Neurol Clin. 2014 Aug;32(3):777–799, ix.
8. Pasnoor M, Barohn RJ, Dimachkie MM. Toxic myopathies. Neurol Clin. 2014 Aug;32(3):647–670, viii.
Štítky
Anesteziologie a resuscitace Intenzivní medicína
Článek vyšel v časopiseAnesteziologie a intenzivní medicína
Nejčtenější tento týden
2015 Číslo 4- Aktuální pohled na využití myorelaxancií a jejich antidot v moderní anesteziologii a intenzivní medicíně
- Perorální antivirotika jako vysoce efektivní nástroj prevence hospitalizací kvůli COVID-19 − otázky a odpovědi pro praxi
- Neodolpasse účinně snižuje pooperační bolest
- Neodolpasse jako ideální volba tam, kde je bolest provázena spasmem kosterního svalstva
- Optimalizace léčby pooperační bolesti snižuje nároky na zdravotní péči
-
Všechny články tohoto čísla
- Několik poznámek k budoucnosti vzdělávání v našem oboru
- Tančit v páru, na to musí být dva…
- Slučování kongresů ČSIM a ČSARIM – existuje jen jedno správné řešení? (aneb “the best solution takes time ...“ )
- Jaký může být potenciál mezinárodní studie OBAAMA-INT ve světle projektu OBAAMA-CZ?
- Zapojení interaktivní výuky do pregraduálního studia akutní medicíny: virtuální pacient, pokročilé simulace a přenosy z operačních sálů
- Výsledky léčby pomocí extrakorporální membránové oxygenace (ECMO) v souboru novorozenců a dětí
- Evropský diplom v anesteziologii a intenzivní medicíně (EDAIC)
- Vazopresin a jeho role v anesteziologii a intenzivní medicíně
- Echokardiografie – měření srdečního výdeje u kriticky nemocných
- Akutní respirační distress syndrom (ARDS)
- Rabdomyolýza – kdy na ni myslet?
- Doporučení pro perioperační péči o obézní chirurgické pacienty 2015
- Kongres ČSARIM
- MUDr. Dimitrij Miloschewsky
- Legendární anesteziolog…
- Zápis z jednání výboru č. 2/2015
- Zápis z jednání výboru č. 3/2015
- Anesteziologie a intenzivní medicína
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Vazopresin a jeho role v anesteziologii a intenzivní medicíně
- Echokardiografie – měření srdečního výdeje u kriticky nemocných
- Akutní respirační distress syndrom (ARDS)
- Doporučení pro perioperační péči o obézní chirurgické pacienty 2015
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Revma Focus: Spondyloartritidy
nový kurz
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Autoři: prof. MUDr. Pavel Horák, CSc., doc. MUDr. Ludmila Brunerová, Ph.D., doc. MUDr. Václav Vyskočil, Ph.D., prim. MUDr. Richard Pikner, Ph.D., MUDr. Olga Růžičková, MUDr. Jan Rosa, prof. MUDr. Vladimír Palička, CSc., Dr.h.c.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání