-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Úspěšná léčba sepse způsobené multirezistentní Pseudomonas aeruginosa pomocí cefi derokolu u hematoonkologické imunokompromitované pacientky po alogenní transplantaci krvetvorby
Successful treatment of sepsis caused by multidrug-resistant Pseudomonas aeruginosa using cefi derocol in an immunocompromised hematological cancer patient fol lowing allogeneic hematopoietic stem cell transplantation
Background: In present days we have the possibility to use new antibiotic drug cefiderocol for the treatment of multiple drug resistant bacterial infections. This infections are the result of preceding and repeating antibiotic therapy mainly in immunocompromised patients. Case: In our case report we present a young woman with acute leukemia with complicated infection in the perianal and rectal area with sepsis development caused by Pseudomonas aeruginosa with lower sensitivity for carbapenems at the early time of allogeneic transplantation of hematopoiesis due to acute leukemia, when she is under the negative influence of chemotherapy and immunosuppressive drugs. We emphasize the adverse effects of colimycine type antibiotics and their interactions with other drugs with the organ toxicity development. Conclusion: The newly available antibiotic cefiderocol with low potential of adverse events and drug interactions demonstrates a benefit in the treatment of the patient described.
Keywords:
Pseudomonas aeruginosa – sepsis – cefiderocol
Autoři: M. Navrátil
Působiště autorů: Klinika hematoonkologie LF OU a FN Ostrava
Vyšlo v časopise: Klin Onkol 2025; 38(3): 209-212
Kategorie: Kazuistiky
doi: https://doi.org/10.48095/ccko2025209Souhrn
Východiska: V současné době máme k dispozici nové antibiotikum cefiderokol k léčbě infekcí způsobených multirezistentními gramnegativními bakteriemi. Tyto infekce bývají výsledkem předchozí opakované antibiotické terapie zvláště pak u pacientů imunokompromitovaných. Případ: V kazuistice ukazujeme případ mladé pacientky s akutní leukemií s komplikující infekcí v oblasti rekta a anu s rozvojem sepse způsobené Pseudomonas aeruginosa se sníženou citlivostí ke karbapenemům v časné době po alogenní transplantaci krvetvorby pro akutní leukemii, kdy je vystavena navíc vedlejšímu účinku chemoterapie a imunosupresiv. Zároveň poukazujeme na nežádoucí účinky doposud používaných antibiotik typu kolimycin a jejich interakce s dalšími léky s rozvojem orgánové toxicity. Závěr: Nově dostupné antibiotikum cefiderokol s nízkým potenciálem nežádoucích účinků a lékových interakcí prokázalo u popisované pacientky benefit v léčbě závažné pseudomonádové infekce.
Klíčová slova:
sepse – Pseudomonas aeruginosa – cefiderokol
Úvod
Infekce multirezistentními bakteriemi v současné době představují vážný problém a podílí se na zvyšování morbidity i mortality u hospitalizovaných pacientů. U pacientů, kteří mají z nějakého důvodu kompromitovanou imunitu, jsou pak tyto infekce život ohrožující a mohou výrazně zhoršovat celkové přežití u této skupiny pacientů. U hematoonkologických pacientů je dána porucha imunity nejen samotným onemocněním, ale i léčbou, která je imunosupresivní. U této skupiny pacientů jsou opakovaně používána širokospektrá antibiotika pro zvládnutí infekčních komplikací po absolovování chemoterapie nebo jiné moderní biologické léčby, kdy negativním důsledkem je selekce multirezistentních kmenů bakterií, které jsou pak jen omezeně citlivé na antibiotika. V neposlední řadě pak právě hematoonkolgičtí pacienti po alogenní transplantaci krvetvorby užívají ještě další léky, které mohou kromě imunosuprese i negativně ovlivňovat funkci jednotlivých orgánů a v kombinaci s antibiotikem pak mohou ještě prohlubovat svůj organotoxický potenciál, jako např. nefrotoxicitu, hepatotoxicitu a jiné. V poslední době se v klinickém používání objevují nová antibiotika, která vykazují velmi dobrý efekt na léčbu multirezistentních bakterií a zároveň nemají tak výrazně vyjádřeny nežádoucí účinky. Patří k nim např. cefiderokol, imipenem/cilastatin/relebaktam nebo azteronam/avibaktam. Jejich použití by mělo být vyhrazeno pouze pro specializovaná pracoviště se zvážením všech skutečností, ze kterých může pacient profitovat. Cefiderokol je nové antibiotikum schválené k používání v Evropě v roce 2020. Je ze skupiny cefalosporinů a je určeno k léčbě infekcí způsobených multirezistentními bakteriemi vč. Pseudomonas aeruginosa. Jeho mechanizmus účinku je specifický, váže se na železo, a transportem pro železo tak vniká přímo do bakterií, kde působí baktericidně. Profil nežádoucích účinků je velmi příznivý [1–3].
Popis případu
Osmnáctiletá žena bez komorbidit s diagnózou akutní nediferencované leukemie po standardní indukční léčbě (daunorubicin, cytosinarabinosid, venetoklax) nedosáhla 20. den od zahájení dostatečné blastoredukce, a proto byla následně léčena reindukční chemoterapií (fludarabin, cytosinarabinosid, idarubicin a venetoklax). Následovalo období dlouhého dřeňového útlumu s absolutní neutropenií trvající 38 dní, kdy měla pacientka opakovaně epizody febrilní neutropenie zaléčené širokospektrými antibiotiky. U pacientky dominuje od počátku hospitalizace sklon k zácpě a po cíleném zjišťování vyšlo najevo, že mívala tyto problémy dlouhodobě i před hospitalizací. V polovině této dlouhodobé neutropenie se u pacientky objevuje bolestivost konečníku, defekt kůže a sliznice v oblasti rekta a rozvoj flegmony perianálně. Ze stěru z rekta byla vykultivována karbapenemáza rezistentní Pseudomonas aeruginosa, současně byla pacientka na empirické kombinaci antibiotik ceftazidim/avibaktam, amikacin a vankomycin. Dle předběžných výsledků bylo známo, že Pseudomonas je citlivá jen na kolimycin, a proto jsme nahradili ceftazidim/avibaktam a amikacin monoterapií kolimycinem. Nadále však přetrvávaly febrilie a vysoký stovkový CRP, navíc třetí den od nasazení kolimycinu došlo k elevaci kreatininu i močoviny a velmi rychle se snižovala diuréza. Následovala změna antibiotik za dostupný imipenem/cilastatin/relebaktam, přičemž v té době jsme ještě neměli standardně dostupné citlivosti pro toto nové širokospektré antibiotikum. Od jeho nasazení došlo k poklesu CRP a klinickému zlepšení stavu, pomohla i aplikace granulocytárních růstových faktorů (filgrastim) a vzestup neutrofilních granulocytů, což bývá mnohdy zásadní faktor v boji proti bakteriální infekci. Stran základního onemocnění (leukemie) pacientka dosáhla kompletní remise. Od počátku diagnózy leukemie bylo jasné, že pacientka je pro rizikovost relapsu leukemie indikována k alogenní transplantaci krvetvorby, což bylo paralelně organizováno vyhledáváním vhodného dárce v registrech dárců krvetvorných buněk po dosažení kompletní remise. Na překlenutí doby do transplantace byly pacientce podány dva cykly konsolidační léčby 5-azacytidinem a venetoklaxem v intervalech 4–5 týdnů s cílem co nejmenší hematologické i slizniční toxicity vzhledem k prodělané život ohrožující závažné infekční komplikaci. Pravidelně byly prováděny i screeningové mikrobiologické stěry z rekta, z dutiny ústní a kontroly moči, vše nadále s negativním nálezem. Pět týdnů od poslední konsolidační terapie jsme přistoupili k alogenní transplantaci krvetvorby od nepříbuzného dárce, muže, HLA shoda 9 z 10. Jako přípravný režim byl na našem pracovišti použit standardní nemyeloablativní režim fludarabin a melfalan a jako imunosuprese cyklosporin ode dne −1, mykofenolát mofetil ode dne +1 a potransplantační cyklofosfamid v den +3 a +5. Podání samotného přípravného režimu vč. převodu štěpu nativních alogenních krvetvorných hematopoetických buněk proběhlo bez komplikací. Screeningové mikrobiologické odběry (stěry z rekta a dutiny ústní a moč) byly kultivačně negativní. V den převodu štěpu (den 0) již byla pacientka neutropenická s absolutním počtem neutrofilů pod 0,1 × 109/l. Třetí den po transplanataci se objevuje mírný průjem jako projev aborální mukozitidy. Pátý den se pak objevuje epizoda febrilní neutropenie a mírná bolestivost v oblasti podrážděného konečníku, i když zevně nebylo žádné zánětlivé postižení patrné. Nasadili jsme standardní empirickou kombinaci používanou na našem pracovišti – fosfomycin a amikacin. V ten samý den byl odebrán screeningový odběr – stěr z rekta – a kultivačně (výsledek byl znám až za další 2 dny) je ve výsledku Pseudomonas aeruginosa se sníženou citlivostí ke karbapenemům. Postupně se u pacientky v těchto 2 dnech zhoršuje bolestivost konečníku a objevuje se perianálně kožní defekt s flegmonou, který přechází i na sliznici rekta (obr. 1). Pacientka byla proto převedena na bezezbytkovou stravu, která byla následně pro nechutenství a snížený perorální příjem stravy doplněna přechodně i parenterální výživou. Úvodní kombinace fosfomycin a amikacin jsme nahradili kolimycinem a vzhledem k anamnéze závažné a v podstatě podobné komplikace před 4 měsíci v době po reindukční chemoterapii jsme následně nasadili i imipenem/cilastatin/relebaktam v kombinaci s vankomycinem [4,5]. Zároveň jsme požádali mikrobiologickou laboratoř o provedení testu citlivosti na imipenem/cilastatin/relebaktam a cefiderokol. Toto vše proběhlo v den +10 a +11 po transplantaci. Stav pacientky se horšil, velmi rychle došlo k oligurii, elevaci renálních parametrů, retenci tekutin, pacientka byla hemodynamicky normotenzní, ale byla výrazná sinusová tachykardie 130/min a rozvíjela se i klidová dušnost při retenci tekutin. Zároveň bolestivost konečníku vyžadovala aplikaci kontinuálního opiátu intravenózně. Zavedena byla i podpora granulocyty stimulujícími faktory (filgrastim) ve standardním dávkování. Kontinuální diuretická podpora však nevedla k dostatečné diuréze, a proto i když ještě parametry urey a kreatininu nedosahovaly dialyzačních hodnot, ode dne +12 byla pacientka napojena na kontinuální náhradu renálních funkcí. Zároveň v den +12 nám mikrobiologická laboratoř sděluje, že má pacientka pozitivní hemokultury, ve kterých je Pseudomonas aeruginosa se sníženou citlivostí ke karbapenemům a že kmen není citlivý na imipenem/cilastatin/relebaktam, ale je citlivý na cefiderokol. Vzhledem k progredujícímu renálnímu selhávání a mikrobiologickým výsledkům jsme upravili antibiotickou terapii na kombinaci cefiderokol a linezolid – vankomycin nahrazujeme linezolidem (snížení potenciálně další renální toxicity vankomycinu). Stav pacientky se ode dne +13 začíná zlepšovat s poklesem CRP (graf 1) a rozvojem spontánní diurézy. V den +14 je ukončena kontinuální náhrada renálních funkcí, renální parametry se postupně upravují, zároveň se v krevním obraze začínají restituovat leukocyty i krevní destičky jako známky přihojování alogenní krvetvorby (graf 2). Klinicky ustupuje retence tekutin, dušnost, bolestivost v oblasti konečníku. V následujících dnech je již pacientka afebrilní, při narůstajících leukocytech se demarkuje poměrně rozsáhlý defekt v oblasti konečníku s postupnou granulací spodiny a hojením. Neutrofily pak nad 0,5 × 109/l již v den +15, což jistě významně přispělo ke zvládnutí této závažné infekční komplikace. Velmi rychle byly vysazeny i opiáty a analgetika. Linezolid byl po úpravě neutrofilů a leukocytů vysazen po 5 dnech a cefiderokol byl podáván do dne +23 (tedy celkem 11 dní). Pacientka je postupně převedena na perorální medikaci vč. imunosupresiv, defekt v oblasti konečníku je ošetřován lokálně a pacientka je propuštěna do domácího ošetřování v den +27 po alogenní transplantaci krvetvorby.
Obr. 1. Perianální afekce v důsledku infekce Pseudomonas aeruginosa. 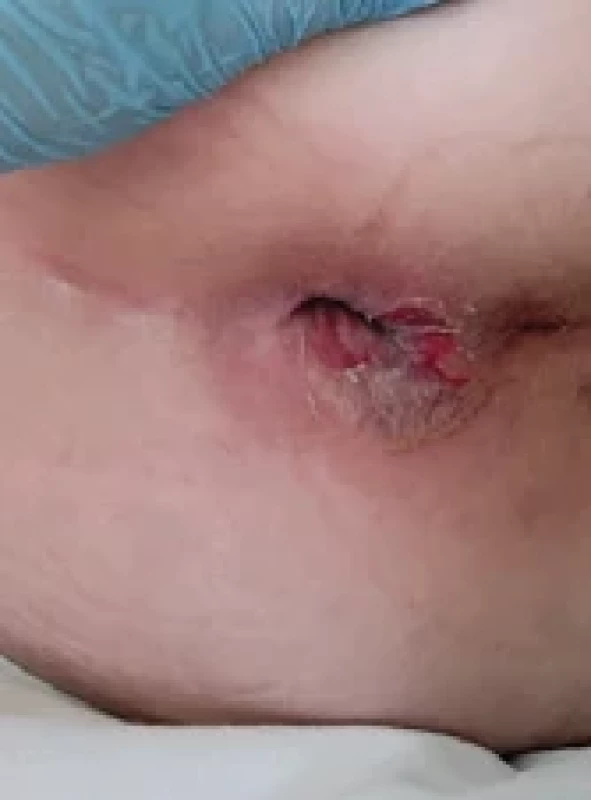
Graf 1. Vývoj denních hodnot CRP během hospitalizace. 
den 0 = den transplantace Graf 2. Vývoj denních hodnot leukocytů během hospitalizace. 
den 0 = den transplantace Závěr
Uvedená kazuistika ukazuje nové možnosti léčby závažných infekcí způsobených gramnegativními multirezistent - ními bakteriemi u imunokompromitovaných pacientů. Velikou výhodou je příznivý profil nežádoucích účinků i lékových interakcí cefiderokolu u této skupiny pacientů, protože právě tito pacienti chronicky užívají další léky vč. imunosupresiv, které jsou potenciálně toxické. Jedinou ze současných nevýhod této léčby je její ekonomická náročnost – cena denní dávky se v současné době pohybuje okolo 20 000 Kč. S infekcemi multirezistentními bakteriemi se budeme jistě setkávat i nadále, i když se jednotlivá pracoviště snaží racionalizovat svou antibiotickou politiku tak, aby nedocházelo k nárůstu rezistencí. Na druhé straně moderní hematoonkologická léčba se nyní rozšiřuje napříč diagnózami i stran věkového složení pacientů s cílem kurability základního onemocnění, což je ovšem spojeno s nárůstem infekčních komplikací jako nežádoucího účinku této moderní léčby. Cefiderokol nyní představuje další součást arzenálu, který je možno v takových případech nasadit. Jeho použití musí být vždy jasně opodstatněné i z toho důvodu, abychom zabránili šíření rezistence i na toto antibiotikum [6], a musí být vždy pod přísným dohledem nejen specialistů léčících základní onemocnění, ale i v těsné spolupráci s mikrobiology, epidemiology a antibiotickými centry při mikrobiologických laboratořích.
Zdroje
1. Bassetti M, Echols R, Matsunaga Y et al. Efficacy and safety of cefiderocol or best available therapy for the treatment of serious infections caused by carbapenem-resistant Gram-negative bacteria (CREDIBLE--CR): a randomised, open-label, multicentre, pathogen-focused, descriptive, phase 3 trial. Lancet Infect Dis 2021; 21 (2): 226–240. doi: 10.1016/S1473-3099 (20) 30796-9.
2. Sato T, Yamawaki K. Cefiderocol: Discovery, chemistry, and in vivo profiles of a novel siderophore cephalosporin. Clin Infect Dis 2019; 69 (Suppl 7): S538–S543. doi: 10.1093/cid/ciz826.
3. Zhanel GG, Golden AR, Zelenitsky S et al. Cefiderocol: a siderophore cephalosporin with activity against carbapenem-resistant and multidrug-resistant gram-negative bacilli. Drugs. 2019; 79 (3): 271–289. doi: 10.1007/s40265-019-1055-2.
4. Lasarte-Monterrubio C, Fraile-Ribot PA, Vázquez-Ucha JC et al. Activity of cefiderocol, imipenem/relebactam, cefepime/taniborbactam and cefepime/zidebactam against ceftolozane/tazobactam - and ceftazidime/avibactam-resistant Pseudomonas aeruginosa. J Antimicrob Chemother 2022; 77 (10): 2809–2815. doi: 10.1093/jac/dkac241.
5. Santerre Henriksen A, Jeannot K, Oliver A et al. In vitro activity of cefiderocol against European Pseudomonas aeruginosa and Acinetobacter spp., including isolates resistant to meropenem and recent b-lactam/b-lactamase inhibitor combinations. Microbiol Spectr 2024; 12 (4): e0383623. doi: 10.1128/spectrum.03836-23.
6. Teran N, Egge SL, Phe K et al. The emergence of cefiderocol resistance in Pseudomonas aeruginosa from a heteroresistant isolate during prolonged therapy. Antimicrob Agents Chemother 2024; 68 (1): e0100923. doi: 10.1128/aac.01009-23.
Štítky
Dětská onkologie Chirurgie všeobecná Onkologie
Článek Influencer trendů
Článek vyšel v časopiseKlinická onkologie
Nejčtenější tento týden
2025 Číslo 3- Trombóza portální žíly jako komplikace infekce COVID-19 – kazuistika
- Ibrance® – nová šance pro pacientky s HR+/HER2– karcinomem prsu
- Vliv alkoholu na riziko vzniku karcinomu prsu, nově podle histologického typu nádoru a jeho senzitivity k estrogenovým receptorům
- Exemestan zlepšuje interval bez relapsu při karcinomu prsu
-
Všechny články tohoto čísla
- Influencer trendů
- Současný management gastrointestinálních stromálních tumorů
- Zhubné nádory u seniorov na Slovensku
- Současná komplexní léčba karcinomu hrdla děložního
- Testování PD-L1 v reálné praxi, první linie léčby pokročilého NSCLC a výsledky a využití první linie léčby metastatického NSCLC pembrolizumabem v monoterapii v České republice
- Totální mezometriální resekce pro léčbu karcinomu děložního čípku – exploratorní studie proveditelnosti, bezpečnosti a onkologických výsledků v rozvojových zemích
- Úspěšná léčba sepse způsobené multirezistentní Pseudomonas aeruginosa pomocí cefi derokolu u hematoonkologické imunokompromitované pacientky po alogenní transplantaci krvetvorby
- Účinnost dlouhodobé léčby u rychle rostoucího maligního nediferencovaného nádoru plic
- Praktická doporučení pro indikace inhibitorů PARP v léčbě ovariálního karcinomu
- Extravazace (paravazace) protinádorových léčiv – aktualizované doporučení (2025) pro standardní péči v rámci České republiky vycházející z multioborové spolupráce
- Pemigatinib v léčbě FGFR2+ cholangiokarcinomu – zázraky se dějí
- Aktuality z Národního ústavu pro výzkum rakoviny
- Klinická onkologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Testování PD-L1 v reálné praxi, první linie léčby pokročilého NSCLC a výsledky a využití první linie léčby metastatického NSCLC pembrolizumabem v monoterapii v České republice
- Extravazace (paravazace) protinádorových léčiv – aktualizované doporučení (2025) pro standardní péči v rámci České republiky vycházející z multioborové spolupráce
- Současná komplexní léčba karcinomu hrdla děložního
- Současný management gastrointestinálních stromálních tumorů
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Revma Focus: Spondyloartritidy
nový kurz
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Autoři: prof. MUDr. Pavel Horák, CSc., doc. MUDr. Ludmila Brunerová, Ph.D., doc. MUDr. Václav Vyskočil, Ph.D., prim. MUDr. Richard Pikner, Ph.D., MUDr. Olga Růžičková, MUDr. Jan Rosa, prof. MUDr. Vladimír Palička, CSc., Dr.h.c.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



