-
Články
Top novinky
Reklama- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
Top novinky
Reklama- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Top novinky
ReklamaXV. Nádory tlustého střeva a konečníku
Vyšlo v časopise: Klin Onkol 2021; 34(Supplementum 2): 53-57
Kategorie: XV. NÁDORY TLUSTÉHO STŘEVA A KONEČNÍKU
XV/ 76. ZVLÁŠTNOSTI ONKOLOGICKÉ LÉČBY MLADÝCH PACIENTŮ
OBERMANNOVÁ R.
Klinika komplexní onkologické péče LF MU a MOÚ Brno
Východiska: Nádory zažívacího traktu, zvláště kolorektální karcinom (KRK), jsou vážným zdravotním problém nejen u starší populace. Ačkoliv v poslední dekádě dochází k poklesu mortality tohoto onemocnění, některé epidemiologické studie ukazují významný vzestup výskytu kolorektálního karcinomu v populaci starší 50 let. Recentní SEER studie (založena na datech the Surveillance, Epidemiology and End Result) udává, že v letech 1992–2013 došlo ke kontinuálnímu vzestupu počtu kolorektálního karcinomu CRC u mladých nemocných, konkrétně u mužů o 1,5 % ročně a u žen o 1,6 % s nejvýznačnějším navýšením mezi 20. a 29. rokem života (muži 5,2 % ročně; ženy 5,6% ročně). S narůstající incidencí v mladších věkových kategoriích čelíme nejen jiným klinicko-patologickým charakteristikám onemocnění ale i jiným socioekonomickým dopadům. Mladí pacienti jsou typicky zdraví, bez závažných komorbidit, avšak jejich onemocnění je v době diagnózy charakterizováno větším rozsahem onemocnění a vyšší agresivitou. Vážnější průběh nemoci může být výsledkem odlišné nádorové biologie. Neméně závažným problém jsou i komplikace a vedlejší účinky protinádorové terapie, jmenovitě zachování fertility a řešení pozdních nežádoucích účinků onkologické léčby. Kombinace narůstajícího počtu pacientů ve fertilním věku, vyšší efektivity onkologické terapie vedoucí k prodloužení celkového přežití pacientů s onkologickým onemocněním a tendence odkládat mateřství přináší naléhavou potřebu pojmenovat specifika mladých nemocných a upravit léčebný a poléčebný algoritmus dle jejich potřeb. Závěr: Přednáška shrnuje charakteristiky a specifika diagnostiky, léčby i řešení nežádoucích účinků onkologické terapie mladých nemocných.
XV/ 80. SOUČASNÉ MOŽNOSTI ENDOSKOPICKÉHO ŘEŠENÍ PREMALIGNÍCH A ČASNÝCH MALIGNÍCH LÉZÍ GIT
TRNA J., NOVOTNÝ I., ŠACHLOVÁ M.
Gastroenterologické oddělení, MOÚ Brno
Mezi potenciálně endoskopicky řešitelné léze patří adenomy s low a high grade dysplazií, intramukózní karcinomy a některé T1 karcinomy. Mezi možnosti endoskopické resekce patří endoskopická polypektomie (EPE), endoskopická mukózní resekce (EMR), endoskopická submukózní disekce (ESD) a endoskopická transmurální resekce (full thickness resection – FTR). EPE je nejběžnější, určena primárně k resekci polypů, tj. stopkatých či polopřisedlých lézí. Jedná se o přerušení stopky léze mechanickou silou (většinou v kombinaci s elektrokoagulačním proudem) za pomoci polypektomické kličky. U malých lézí (≤ 9 mm) je v poslední době doporučována resekce kličkou bez použití proudu (cold snare polypectomy), která vykazuje mj. nižší riziko opožděného krvácení. U větších lézí je použití proudu vhodné až nutné. Při EMR je různými principy (nejčastěji submukózním podpichem) vytvořen z ploché nepolypoidní léze pseudopolyp, který je následně možné odstranit kličkou. Pokud lze (většinou léze velikosti do 30 mm) je preferováno odstranění vcelku (en bloc), větší léze je nutné odstranit po částech (piecemeal). Pokud nedochází při podpichu ke zvedání léze (příznak non-liftingu), může se jednat mj. o hlubší invazi léze a jedná se o kontraindikaci EMR. ESD je schopná „en bloc“ odstranění i větších lézí v kolonu. Metoda je efektivní, ale technicky a fi nančně náročná, vyžaduje dlouhý čas a je zatížena vyšším rizikem komplikací než EPE a EMR. Výkon je prováděn s průhledným nástavcem (capem) nasazeným na konec přístroje. Po označení okrajů léze a jejím podpichu je provedena incize a následná preparace v submukózní vrstvě za pomoci speciálních ESD nožů. V průběhu výkonu dochází k odtlačování (disekci) léze od zbylé stěny střeva za pomoci capu. Pozice ESD není zatím jednoznačná. Lze o ní uvažovat u lézí ≥ 20 mm se silným podezřením na submukózně invadující karcinom, především v oblasti rekta, kde chirurgický výkon vede k výraznému zhoršení kvality života. FTR je za pomoci speciálního instrumentária schopna resekovat celou stěnu kolon. Je tak možno resekovat i non-lifting léze (obtížně řešitelné jak EMR tak ESD) a léze vycházející z hlubších vrstev stěny. Výkon je prováděn za pomoci capu, který obsahuje kličku a velký OTS (over the scope) klip. Speciálními kleštěmi (grasperem) je léze vtažena do capu, následně uvolněn klip, který tak vytvoří duplikaturu střevní stěny a kličkou je odstraněna část nad klipem. I pozice FTR je ve stadiu ověřování. Za vhodné bývají považovány léze s příznakem non-liftingu, případně léze subepiteliální. FTR umožňuje precizní lokální staging vyšetřením celé stěny.
XV/ 179. CAN WE ACHIEVE LONG-TERM SURVIVAL WITH MAINTENANCE THERAPY IN METASTATIC COLORECTAL CANCER? – A CASE REPORT
PAZDEROVÁ N.
Second Department of Oncology, Faculty of Medicine, Comenius University, National Cancer Institute, Bratislava, Slovak Republic
Colorectal cancer is the second leading cause of cancer-related death worldwide. Approximately 20–25% of patients suff er from metastatic disease at the time of diagnosis. Within these patients, an accurate staging allows to plan adequate treatment strategy. Patient's clinical features, tumour characteristics and molecular profile should be considered during the treatment choice. In case of unresectable tumours, disease control is the best treatment approach for long term survival. For metastatic colorectal cancer, induction chemotherapy combined with a targeted agent is considered the mainstay of treatment. After objective response to active therapy, several local ablative methods can be included to treatment strategy. Here we report the case of a 71-year-old man aff ected by right-sided colorectal cancer with multiple liver metastases who achieved a complete radiological response after receiving capecitabine, oxaliplatine and bevacizumab for 8 months with regression of liver metastasis. Then he continued with maintenance capecitabine plus bevacizumab for 4 years until one liver metastasis reoccurred. Based on MDT decision, patient underwent radiofrequency ablation and continued with maintenance therapy for other 4 months until the progression of liver metastasis. We have decided to reintroduce oxaliplatin. The patient now continues with CAPOX plus bevacizumab with mild pulmonary toxicity and low grade neuropathy. Six years after the beginning of first-line treatment, the patient remains in good condition with disease stabilization.
XV/ 180. MULTIMODAL THERAPY CONSISTING OF CONCURRENT CHEMO-RADIOTHERAPY, SURGERY AND SYSTEMIC CHEMOTHERAPY IS BENEFICIAL IN PATIENTS WITH STAGE II/ III RECTAL CANCER – A CASE REPORT
HORVÁTHOVÁ B., NĚMEČEK R.
Department of Comprehensive Cancer Care, MMCI Brno, Czech Republic
Patients with locally advanced, node-positive, T3/ T4 rectal tumors could benefit from the concept of total neoadjuvant therapy (TNT) in which the equivalent of standard adjuvant chemotherapy is given preoperatively. It is still a matter of debate whether chemotherapy should be used as induction therapy before the beginning of chemo-radiotherapy (CHRT) or after it. Furthermore, based on the randomized RAPIDO trial, short-course radiotherapy (RT) is considered as an appropriate alternative for patients with locally advanced rectal cancer undergoing TNT treatment. Here we present a case of a 56-year-old woman with MSI-high, locally advanced rectal cancer, initially stage IIIc (T4bN2M0). Respecting the high volume of the tumor, anatomic proportions and suspected significant inflammatory component of the lesion, we started systemic chemotherapy (FOLFOX regimen). Given the circumstances, the whole treatment strategy at the beginning could have been neoadjuvant as well as palliative. After a good clinical response to the chemotherapy, proven by promising results of imaging methods, we decided to continue with long-course chemo-RT with capecitabine followed by surgery; thus, the applied preoperative therapy equaled to a TNT. Despite the good clinical response, the extensive surgery in a form of pelvic exenteration resulted in R1 resection and the histological analyses showed no regression at all (Mandard 5). After a short period of time, the progression of the disease to stage IV was evident. The patient received standard systemic chemotherapy and then, given the MSI-high status of the tumor, the immunotherapy with checkpoint inhibitors as well. The role of neoadjuvant therapy (TNT in our case) and potential benefit of RT in locally advanced MSI-high rectal cancer remain highly controversial.
XV/ 190. ENDOSKOPICKÉ ŘEŠENÍ DYSPLASTICKÝCH LÉZÍ A ČASNÝCH KARCINOMŮ V DOLNÍM GIT
TRNA J., NOVOTNÝ I., ŠACHLOVÁ M.
Gastroenterologické oddělení, MOÚ Brno
Mezi potenciálně endoskopicky řešitelné léze patří adenomy s low a high grade dysplazií, intramukózní karcinomy a ně kte ré T1 karcinomy (s postižením horní 1/ 3 submukózy). Mezi současné možnosti endoskopické resekce patří endoskopická polypektomie (EPE), endoskopická mukózní resekce (EMR), endoskopická submukózní disekce (ESD) a endoskopická transmurální resekce (full thickness resection – FTR). EPE je nejběžnější metodou, určenou k resekci stopkatých či polopřisedlých lézí. Jedná se o odstranění léze mechanickou silou (většinou v kombinaci s elektrokoagulačním proudem) za pomoci polypektomické kličky. U malých lézí (≤ 9 mm) je v poslední době doporučována resekce bez použití proudu (cold snare polypectomy), která vykazuje mj. nižší riziko opožděného krvácení. U větších lézí je použití proudu vhodné až nutné. Při EMR je různými principy (nejčastěji submukózním podpichem) vytvořen z ploché nepolypoidní léze pseudopolyp, který je následně odstraněn kličkou. Pokud lze (léze velikosti do 30 mm) je preferováno odstranění vcelku (en bloc), větší léze je nutné odstranit po částech (piecemeal). Pokud nedochází při submukózním podpichu ke zvedání léze (příznak non-liftingu), může se jednat mj. o hlubší invazi léze a jedná se o kontraindikaci EMR. ESD je schopná en bloc odstranění i větších lézí v kolonu. Metoda je efektivní, ale je technicky a finančně náročná, vyžaduje dlouhý čas a je zatížena vyšším rizikem komplikací než EPE a EMR. Výkon je prováděn s průhledným nástavcem (capem) nasazeným na konec přístroje. Po označení okrajů léze a jejím podpichu je provedena incize a následná preparace v submukózní vrstvě za pomoci speciálních ESD nožů. V průběhu výkonu dochází k odtlačování (disekci) léze od zbylé stěny střeva za pomoci capu. O ESD lze uvažovat u lézí ≥ 20 mm se silným podezřením na submukózně invadující karcinom, především v oblasti rekta, kde chirurgický výkon vede k výraznému zhoršení kvality života. FTR je za pomoci speciálního instrumentária schopna resekovat celou stěnu kolon. Je tak možno resekovat i non-lifting léze (obtížně řešitelné jak EMR tak ESD) a léze vycházející z hlubších vrstev stěny. Výkon je prováděn za pomoci capu, který obsahuje integrovanou kličku a velký OTS (over the scope) klip. Speciálními kleštěmi (grasperem) je léze vtažena do capu, pak je uvolněn klip, který vytvoří duplikaturu střevní stěny a kličkou je odstraněna část nad klipem. FTR je vhodná u lézí s příznakem non-liftingu, případně léze subepiteliální. FTR umožňuje precizní lokální staging vyšetřením celé stěny. Velikost léze nesmí přesahovat velikost capu (15–30 mm).
XV/ 223. VYUŽITIE ŽELATÍNOVEJ ZYMOGRAFIE PRI DIAGNOSTIKE KOLOREKTÁLNEHO KARCINÓMU
VEČURKOVSKÁ I., MAŠLANKOVÁ J., STUPÁK M., TOMEČKOVÁ V.
Ústav lekárskej a klinickej biochémie, LF UPJŠ Košice, Slovenská republika
Úvod: Na Slovensku je najvyššia mortalita na kolorektálny karcinóm (CRC) z celej EÚ, a to 82,7 % mužov a 42,9 % žien. Mnoho publikácií popisuje procesy súvisiace s karcinogenézou rôznych typov nádorov, pričom značná pozornosť sa zameriava na aktivitu matrixových metaloproteínáz (MMP) v extracelulárnom matrix (ECM). Táto skupina enzýmov hrá dôležitú úlohu v progresii nádoru tým, že degradáciou ECM odstraňuje fyzické bariéry a umožňuje inváziu nádorových buniek do krvných a lymfatických ciev. Dochádza tým k rastu nádoru, neoangiogenéze a extravazácii. Ciele: Cieľom predkladanej práce bolo posúdenie vhodnosti využitia želatínovej zymografie pri stanovení neaktívnych a aktívnych foriem vybraných MMP v sére a tkanive pacientov v rôznych štádiách CRC. Materiál: Biologický materiál (sérum, tkanivo) bol odobratý na I. chirurgickej klinike UNLP v Košiciach od 100 pacientov, z ktorých 32 bolo benígnych. Metódy: Na stanovenie aktivity vybraných MMP sme využili želatínovú zymografiu, ktorá prebiehala v 10% polyakrylamidovom géli kopolymerizovanom s 1 mg/ ml želatínou pri 150 V. Po elektroforéze bol gél premývaný v 2,5% Triton X-100 (2x) a následne inkubovaný pri 37 °C vo vyvíjacom (renaturačnom) roztoku obsahujúcom ióny Zn2+ a Ca2+. Po inkubácii bol gél farbený 0,5 % roztokom Coomassie Brilliant Blue G-250 a následne odfarbovaný v odfarbovacom roztoku I a II. Enzymatické aktivity jednotlivých foriem MMP boli rozoznané ako biele pásy na modrom pozadí. Výsledky: Výsledný zymogram sme spracovali pomocou programu ImageJ. V sére pacientov s CRC (obr. 1) sme detekovali iba neaktívne formy MMP-2 a MMP-9, zatiaľ čo v tkanivách pacientov boli prítomné aj ich aktívne formy, pričom v nižších štádiách neboli prítomné aktívne formy MMP-2. Záver: Želatínová zymografia vo vzorkách tkaniva pacientov s CRC sa zdá byť vhodnou metodikou na monitorovanie progresie CRC a následnej úspešnosti liečby.
Táto práca bola podporená projektom VEGA 1/ 0333/ 20.
Obr. 1. Zymogram séra pacientov s CRC. 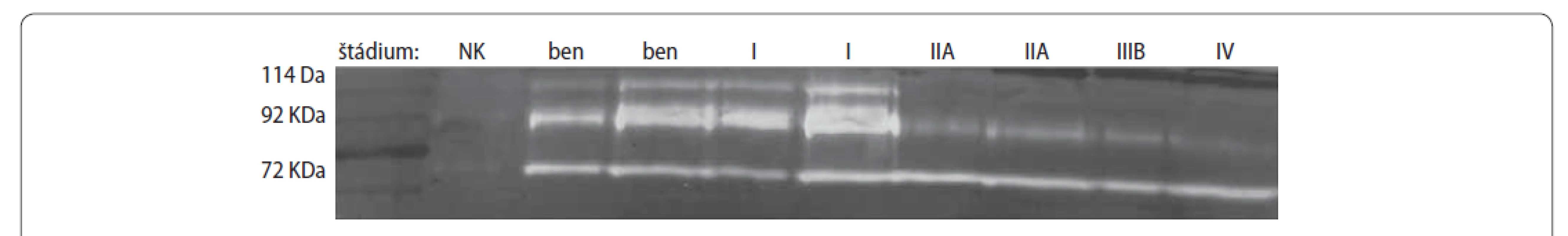
114 kDa – MMP-2 dimér, 92 kDa – pro-MMP-9, 72 kDa – pro-MMP-2; NK – negatívna kontrola XV/ 225. LAZARŮV EFEKT ANEB KOMBINOVANÁ IMUNOTERAPIE (NIVOLUMAB PLUS IPILIMUMAB) VSTUPUJE DO LÉČBY KOLOREKTÁLNÍHO KARCINOMU S FENOTYPEM MSI-H/ MMR-D
OSTŘÍŽKOVÁ L.1, KOSÍKOVÁ I.1, ANDRAŠINA T.2, KALA Z.3, MAN M.4, PAVLOVSKÝ Z.5
1Interní hematologická a onkologická klinika LF MU a FN Brno, 2Klinika zobrazovacích metod LF MU a FN Brno, 3Chirurgická klinika LF MU a FN Brno, 4Chirurgické oddělení, NTGM Hodonín, 5Ústav patologie, FN Brno
Úvod: Léčba checkpoint inhibitory nastartovala imunoterapeutickou tsunami nejprve u pokročilého melanomu, ale její vliv se začíná uplatňovat napříč celou řadou nádorů. V tuto chvíli je léčba anti-PD1 či anti-PD-L1 inhibitory schválena nejméně u 15 indikací, přičemž poslední schválenou léčbou nivolumabu (v kombinaci s nízkou dávkou ipilimumabu) je předléčený kolorektální karcinom (KRK) vykazující vysokou mikrosatelitovou instabilitu (MSI-H) či deficit v „mismatch-repair genech“ (MMR-D). Pacienti s tímto fenotypem vykazují sníženou schopnost opravovat mutace v DNA a výsledkem je vysoký počet mutací v nádoru a větší „atraktivita“ těchto nádorů pro imunitní systém. Pacienti s MSI-H/ MMR-D KRK mají také nádor s vyššími počty tumor-infiltrujících lymfocytů (TILs). Tito pacienti tvoří 4–5 % pacientů s metastatickým KRK a mají horší prognózu po léčbě konvenční chemoterapií. Cíl práce: Tato práce si dává za cíl diskutovat aktuální klinická data pro kombinaci nivolumabu s ipilimumabem u předléčených pacientů s MSI-H/ MMR-D KRK a vysvětlit, proč tyto nádory odpovídají tak výrazně na léčbu anti-PD1 terapií. Budeme také prezentovat naše zkušenosti s anti-PD1 léčbou u těchto pacientů. Výsledky: Kombinace anti-PD1 a anti-CTLA-4 byla schválena na základě studie CM-142, která sledovala bezpečnost a účinnost nivolumabu 3 mg/ kg Q3W spolu s ipilimumabem (1 mg/ kg) ve 4 dávkách s následným podáváním nivolumabu 3 mg/ kg Q2W. Celkem bylo ve studii léčeno 119 pacientů. S metastazujícím KRK s MSI-H/ MMR-D. Celkem 36 % pacientů mělo za sebou minimálně 2 systémové chemoterapie a 40 % pacientů mělo za sebou ≥ 3 linie léčby. Při mediánu sledování 51,1 měsíce byla odpověď dosažena u 65 % pacientů (CR 13 %, PR 52 %). Medián doby do nástupu odpovědi byl 2,8 měsíce a medián trvání odpovědi nebyl dosažen. Medián PFS byl odhadnut na 56 měsíce a celkově přežívalo po 3 a 4 letech 71,4 a 70,5 % pacientů. V přednášce budou prezentována data našich KRK pacientů s MSI-H/ MMR-D fenotypem a na 2 klinických případech ukážeme tzv. Lazarův efekt imunoterapie, kdy bylo pacientům s tímto fenotypem predikováno přežití v řádu několika týdnů. Diskuze a závěry: Analýza vlastních pacientů s MSI-H/ MMR-D fenotypem ukázala vysokou účinnost léčby i samotným nivolumabem. Tito pacienti mají z léčby imunoterapií výrazný efekt, o čemž svědčí data PFS a OS a naše osobní zkušenosti s léčbou nivolumabem. Důležité bude otestovat ve spolupráci s patology na tento biomarker každého pacienti s KRK, protože benefit z imunoterapie se zdá být mezi solidními nádory ještě výraznější než v případě melanomu či Hodgkinova lymfomu.
XV/ 244. MIKROBIOM PACIENTŮ S RAKOVINOU KOLOREKTA A JEHO KORELACE S KLINICKÝMI PROMĚNNÝMI
BUDINSKÁ E.1, ZWINSOVÁ B.2, PETROV V.2, HRIVŇÁKOVÁ M.2, ŠEFR R.3, BENCSIKOVA B.4, ZDRAŽILOVÁ DUBSKÁ L.5, NENUTIL R.6, VÍDEŇSKÁ P.2
1Institut biostatistiky a analýz LF MU a FN Brno, 2RECETOX, MU Brno, 3Klinika operační onkologie LF MU a MOÚ Brno, 4Klinika komplexní onkologické péče LF MU a MOÚ Brno, 5Oddělení klinické mikrobiologie a imunologie, FN Brno, 6Úsek diagnostické bioptické patologie, MOÚ Brno
Východiska: Nejnovější výzkumy dokazují, že mikrobiom ovlivňuje vznik a vývoj kolorektálního karcinomu (KRK) a to porovnáním mikrobiomu zdravých jedinců a pacientů s KRK. Studií, které se věnují asociaci mikrobiomu s klinickými parametry KRK, je málo a jsou provedeny na malém počtu pacientů a obvykle jednom typu vzorku. Metody: U 178 pacientů diagnostikovaných s KRK ve stadiu 0–IV jsme korelovali mikrobiální složení stěrů z nádorové mukózy, mukózy přilehlé zdravé tkáně a stolice s klinickými a molekulárními charakteristikami (grade, stadium, přítomnost metastáz, lokalizace nádoru, MSI, přítomnost KRAS a BRAF mutace). Mikrobiální složení bylo zhodnoceno na základě sekvenace genu pro 16S rRNA. Výsledky: Analýza β-diverzity ukázala, že lokalizace nádoru byla faktorem s největším vlivem na celkové složení mikrobiomu pro všechny typy vzorků, zatímco histologický grade nádoru ovlivňoval pouze mikrobiom nádorové mukózy. Ve vzorcích z mukózy nádoru bylo nalezeno 31 rodů významně asociovaných s grade nebo lokalizací, z toho 15 s významnou interakcí mezi těmito dvěma proměnnými. Rody Fusobacterium, Campylobacter a Leptotrichia se významně zvyšovaly se zvyšujícím se grade nádoru bez ohledu na jeho lokalizaci (FDR < 0,1). Mukóza pravostranných nádorů grade 3 byla obohacena o bakterie rodu Prevotella a Selenomonas a Selenomonas 3. U pokročilých (III–IV) stadií nádorů jsme identifikovali zvýšenou abundanci Akkermansie. Přítomnost lokálních metastáz byla asociována se zvýšeným výskytem bakterií rodu Akkermansia ve stolici pacientů, přítomnost vzdálených metastáz zas se zvýšeným výskytem rodů Porphyromonas, Streptococcus and Ruminococcaceae UCG-005 na nádorové mukóze a Akkermansia na vizuálně zdravé mukóze. Závěr: V naší studii jsme identifikovali bakteriální rody, které dříve nebyly spojeny s nádorovou mukózou KRK, klinickými proměnnými nebo vůbec s kolorektálním karcinomem. Tyto rody by měly být podrobněji studovány, aby bylo možné popsat jejich mechanizmus interakce s onemocněním. Naše studie dále ukázala, že asociace bakterií na nádorové mukóze nebo přilehlé zdravé mukóze s klinickými proměnnými jsou v mikrobiálním složení stolice zřídka zachovány a naopak. Zdá se, že mikrobiom sliznice a stolice se komplementuje s ohledem na modulaci jejich účinků na progresi onemocnění. Pro efektivní využití mikrobiomu pro screeningové nebo diagnostické účely bude zřejmě nutné kombinovat vzorky biopsie nádorů se vzorkováním stolice. Tento výzkum byl podpořen grantem AZV 16-31966A.
XV/ 245. STRATIFIKACE PACIENTŮ S KOLOREKTÁLNÍM KARCINOMEM NA ZÁKLADĚ NÁDOROVÉHO MIKROBIOMU
ZWINSOVÁ B.1, PETROV V.2, HRIVŇÁKOVÁ M.1, MICENKOVÁ L.1, ŠEFR R.3, BENCSIKOVÁ B.4, ZDRAŽILOVÁ DUBSKÁ L.1, NENUTIL R.5, VÍDEŇSKÁ P.1, BUDINSKÁ E.1
1PřF MU Brno, 2MU Brno, 3Klinika operační onkologie LF MU a MOÚ Brno, 4Klinika komplexní onkologické péče LF MU a MOÚ Brno, 5Oddělení onkologické patologie, MOÚ Brno
Východiska: Kolorektální karcinom (KRK) je velmi heterogenní onemocnění, které se projevuje i v prognóze a rozdílné odpovědi pacientů na protinádorovou léčbu. Molekulární profilování zatím přineslo pouze dílčí úspěchy. Střevní mikrobiom, v poslední době často asociovaný se vznikem a vývojem KRK, by mohl být chybějícím dílkem v komplexní charakteristice heterogenity KRK. Cílem naší studie bylo identifikovat skupiny pacientů na základě mikrobiálního složení mukózy jejich nádorů, přilehlé normální tkáně a stolice. Metody: Mikrobiální složení stěrů z nádorů a přilehlé zdravé tkáně u 178 pacientů diagnostikovaných s KRK ve stadiu 0–IV bylo provedeno na základě sekvenace genu pro 16S rRNA. U 127 pacientů bylo navíc k dispozici mikrobiální složení stolice. Výsledky: Porovnáním mikrobiálního složení stěrů z nádorů, přilehlé zdravé tkáně a stolice u 127 pacientů bylo identifikováno 57 druhů bakterií specifických pro tumorovou tkáň. Zajímavostí bylo, že část těchto bakterií byly patogeny orálního původu. Na základě výskytu či absence těchto bakterií byli pacienti stratifikování do tří podtypů. Pro první podtyp (TMS1) byla charakteristická zvýšená abundance patogenních bakterií jako Fusobacterium, Campylobacter, Leptotrichia, Peptoclostridium a Selenomonas a nižší abundance typicky komenzálních bakterií stolice (Bifidobacterium, Ruminococcus 2, Anaerostipes a Coprococcus 1). V tomto podtypu převažovaly pravostranné nádory (60,9 %), nádory stupně 3 (58,7 %), pT3 a pT4 (95,6 %). V porovnání s ostatními podtypy navíc obsahoval významně více nádorů s mikrosatelitovou nestabilitou (34,8 %) a mutací genu BRAF (15,2 %). Druhý podtyp (TMS2) byl definovaný chybějícím výskytem bakterií ze skupiny Selenomonas. Tento podtyp obsahuje levostranné nádory a nádory rektosigmoidea nebo rekta (70,9 %). Poslední podtyp (TMS3) byla charakteristická absence patogenu Fusobacterium u nejméně poloviny nádorů, dále absencí bakterií specifických pro vyšší stupně nádorů a zvýšeným podílem nádorů stupně 1 (15,6 %). V TMS3 byly rovnoměrně zastoupené pravostranné a levostranné nádory. Tyto podtypy se navíc signifikantně lišily v mediánu proporci výskytu bakteriálních patogenů orálního původu (TMS1 15,8 %, TMS2 12,3 % a TMS3 5,3 %). Závěr: Při detailní analýze 57 bakterií specifických pro nádory se nám podařilo identifikovat tři hlavní mikrobiální podtypy pacientů s KRK, které korelují s klinickými proměnnými, jako je stupeň nádoru, lokalizace a TNM stadia. Nádorově specifické bakterie pak obsahují patogeny orálního původu.
Práce byla podpořena projektem AZV 16-31966A
XV/ 246. KONSENZUÁLNÍ MOLEKULÁRNÍ PODTYPY KOLOREKTÁLNÍHO KARCINOMU SE LIŠÍ S MORFOLOGICKOU VARIABILITOU NÁDORU
BUDINSKÁ E.1, POPOVICI V.2, IVKOVIČ T.3, HRIVŇÁKOVÁ M.2, NENUTIL R.4, NĚMEČEK M.4, ZDRAŽILOVÁ DUBSKÁ L.5, SLABÝ O.6, BENCSIKOVÁ B.6
1Institut biostatistiky a analýz LF MU Brno, 2RECETOX, MU Brno, 3CEITEC, MU Brno, 4Úsek diagnostické bioptické patologie, MOÚ Brno, 5Oddělení klinické mikrobiologie a imunologie, FN Brno, 6Klinika komplexní onkologické péče LF MU a MOÚ Brno
Východiska: Konsenzuální molekulární podtypy (CMS) [1] kolorektálního karcinomu (KRK), definují čtyři odlišné skupiny KRK s klinickým významem. Souvislost mezi morfologií nádoru a CMS byla dříve popsána kvalitativně [2] i kvantitativně [3,4]. Vnitřní morfologická heterogenita nádorů a různé strategie odběrů vzorků pro molekulární profilování významně ovlivňují CMS klasifikaci [5]. Pro lepší charakterizaci této heterogenity a nalezení stabilních oblastí pro extrakci RNA, jsme porovnali CMS klasifikaci celonádorových řezů a jejich morfologických regionů. Metody: Do studie bylo zařazeno 100 KRK nádorů stadia II a III z MOÚ. Morfologické regiony (komplexní tubulární, desmoplastický, mucinózní, papilární, zoubkovaný – serrated, solidní trabekulární a normální a stromální oblasti sousedící s nádorem) byly ručně anotovány a makro-disekovány. Z regionů byla extrahována RNA a pro transkriptomické profilování byl použit mikročip human Clariom™ D Assay. Pro klasifikaci podtypů byl použit R balík CMScaller. Výsledky: Celkem bylo získáno 100 transkriptomických celonádorových profilů a 152 profilů morfologických regionů. Pokud byl celonádorový profil klasifikován jako CMS1 až 3, většinou (73, 62 a 78 %) byl stejně klasifikován alespoň jeden z jeho morfologických regionů. Výjimkou byl celonádorový podtyp CMS4 (44 %). Komplexní tubulární regiony byly většinou označeny jako CMS1 (41 %) a CMS2 (32 %), desmoplastické regiony jako CMS4 (54 %) a CMS1 (31 %). Podtyp desmoplastického regionu (i v kombinaci s jinými typy regionů) určoval podtyp celonádorového profilu. Zoubkované regiony byly většinou označeny jako CMS2 (42 %) a CMS3 (32 %). Stroma sousedící s nádorem bylo označeno jako CMS4 a překvapivě také většina mucinózních regionů (60 %). Geny kanonické Wnt dráhy měli vyšší expresi v mucinózních, zoubkovaných a stromálních regionech, geny epiteliální mesenchymální tranzice zas v desmoplastických, mucinózních a stromálních regionech. Závěr: Morfologické regiony nádoru mohou mít odlišný CMS podtyp než profily odvozené z celonádorového řezu. Morfologické vyhodnocení nádoru v kombinaci s výběrem reprezentativních oblastí je nezbytné pro zlepšení stability klasifikace CMS. Multiregionální vzorkování zároveň otevírá možnosti upřesnění stávající CMS klasifikace. Molekulární charakterizace CMS4 jako EMT je důsledkem přítomnosti desmoplastické reakce.
Tento výzkum byl podpořen grantem GAČR 19-08646S.
Literatura: [1] Guinney J, Dienstmann R, Wang X. The consensus molecular subtypes of colorectal cancer. Nat Med 2015; 21(11): 1350–1356. doi: 10.1038/ nm.3967. [2] Dunne PD, McArt DG, Bradley CA et al. Challenging the cancer molecular stratification dogma: intratumoral heterogeneity undermines consensus molecular subtypes and potential diagnostic value in colorectal cancer. Clin Cancer Res 2016; 22(16): 4095–4104. doi: 110.1158/ 1078-0432.CCR-16-0032. [3] Budinska E, Popovici V, Tejpar S et al. Gene expression patterns unveil a new level of molecular heterogeneity in colorectal cancer. J Pathol 2013; 231(1): 63–76. doi: 10.1002/ path.4212. [4] Popovici V, Budinska E, Dušek L et al. Image-based surrogate biomarkers for molecular subtypes of colorectal cancer. Bioinformatics 2017; 33(13): 2002–2009. doi: 10.1093/ bioinformatics/ btx027. [5] Kim DH, Choi SH, Park SH et al. Meta-analysis of the accuracy of Liver Imaging Reporting and Data System category 4 or 5 for diagnosing hepatocellular carcinoma. [online]. Available from: https:/ / gut.bmj.com/ content/ 68/ 9/ 1719.
XV/ 247. SUBPOPULACE T-LYMFOCYTŮ, REGULAČNÍ T-LYMFOCYTY, U PACIENTŮ S KOLOREKTÁLNÍM KARCINOMEM
ZDRAŽILOVÁ DUBSKÁ L.1, BENCSIKOVÁ B.2, BUDINSKÁ E.3, SELINGEROVÁ I.4, PILÁTOVÁ K.5, GREPLOVÁ K.6, VALÍK D.7, NENUTIL R.8, GESCHEIDTOVÁ L.6, OBERMANNOVÁ R.9
1Oddělení klinické mikrobiologie a imunologie, FN Brno, 2Klinika komplexní onkologické péče LF MU a MOÚ Brno, 3RECETOX PřF MU Brno, 4MOÚ Brno, 5Farmakologický ústav, LF MU Brno, 6Úsek laboratorní medicíny, MOÚ Brno, 7Katedra laboratorních metod, LF MU Brno, 8RECAMO, MOÚ Brno, 9Klinika komplexní onkologické péče LF MU a MOÚ Brno
Východiska: V prospektivní studii s dlouhodobým sledováním jsme analyzovali subpopulace cirkulujících T-lymfocytů u pacientů s metastatickým kolorektálním karcinomem (mCRC) a to v kontextu stranovosti primárního nádoru, mutačního stavu KRAS a odpovědi na léčbu. Naším primárním cílem bylo zjistit, zda hladiny cirkulujících subpopulací T-lymfocytů před zahájením systémové onkologické léčby s anti-VEGF mohou sloužit jako ukazatel klinické odpovědi na léčbu u pacientů s mCRC. Hodnocená skupina se skládala z 36 pacientů s kolorektálním adenokarcinomem, kteří zahájili první linii chemoterapie s bevacizumabem pro metastazující onemocnění. Před zahájením léčby jsme v periferní krvi kvantifikovali subsety T-lymfocytů včetně regulačních (T-reg) a CD8+ cytotoxických T-lymfocytů. Klinický benefit byl hodnocen jako přežití bez progrese (PFS), celkové přežití (OS) a míra objektivní odpovědi (ORR). Výsledky: 1) pacienti s mCRC s KRAS wt měli vyšší proporci cirkulujících CD8+ cytotoxických T-lymfocytů, ale také vyšší hodnoty T-reg, a to jak absolutní počet, tak proporci v CD4+; 2) nízký podíl cirkulujících T-reg mezi CD4+ buňkami a vysoký poměr CD8/T-reg při zahájení léčby s anti-VEGF byly spojeny s příznivým klinickým výsledkem; 3) u podskupiny pacientů s mCRC s primárním tumorem v pravé straně kolorekta byly v případě vysokého poměru CD8/T-reg pozorovány vyšší PFS a OS. Závěry: Hladiny cirkulujících imunitních buněk před zahájením léčby mohou přispět k predikci klinického benefitu z léčby anti-VEGF bevacizumbem. U pacientů s mCRC s primem v pravé části kolorekta bylo možné identifikovat podskupinu s lepší léčebnou odpovědí na základě poměru CD8/T-reg.
XV/ 250. ROZSÁHLÝ TUMOR REKTA – PŘEKVAPUJÍCÍ ETIOLOGIE
BARKMANOVÁ J.1, MAŠEK T.2
1Onkologická klinika 1. LF UK a VFN v Praze, 2Centrum chirurgie střevních onemocnění, Nemocnice Milosrdných sester sv. Karla Boromejského v Praze
Úvod: Pacienti s defekačními obtížemi nebo s krvácením z GIT bývají v první době vyšetřeni gastroenterologem nebo chirurgem. Všechny nálezy pacienta by měly být zhodnoceny multidisciplinárním týmem, který doporučí posloupnost jednotlivých terapeutických modalit dle charakteru a rozsahu onemocnění. Popis případu: Jednatřicetiletý pacient byl odeslán pro 2týdenní krvácení z konečníku do koloproktologické ambulance. V osobní anamnéze neměl nic pozoruhodného, byl kuřák, pracoval jako sociální pracovník. Otec pacienta byl léčen pro polypózu tlustého střeva kolem 50. roku a absolvoval 2x polypektomii. Při endoskopii byl na polovině obvodu patrný rozsáhlý tumor spíše měkké konsistence, velikosti 7 x 7 cm, nasedající těsně na svěrač, od anu do 9 cm téměř cirkulárně exulcerovaná infiltrace stěny rekta. Endosonograficky (EUS) také podezření na tumor rekta rozsahu T3, NO, s infiltrací horního okraje svěrače. Histologicky popsány jen zánětlivé změny. Na CT břicha a malé pánve i magnetické rezonanci (MR) pánve nález nízkého tumoru rekta T3 s metastázami do uzlin mezorektálních a mezosigmatických. Vzhledem k negativní biopsii multidisciplinární seminář zamítl možnost neoadjuvantní léčby nebo operace bez řádné verifikace procesu. Druhá histologie byla uzavřena jako chronický transmurální zánět rekta nejasné etiologie. Při podrobnější osobní anamnéze bylo zjištěno, že pacient je homosexuál. Pro podezření na venerologickou etiologii tumoru byl pacient odeslán na dermatovenerologickou ambulanci VFN v Praze. Ze stěru z rekta byly prokázány: lymphogranuloma venereum, Chlamydia trachomatis, Mycoplasma hominis. Ve smyslu Neisseria gonorrhoe, Ureaplasma urealyticum, Ureaplasma parvum a sérologie na syfilis a HIV byl nález negativní. Uzavřeno jak lymphogranuloma venereum. Výsledky: Pacientovi byl aplikován Doxyhexal 100 mg tbl à 12 hod po dobu 4 týdnů. Po léčbě nález výrazně ustoupil, těsně za svěračem bylo ještě zánětlivé reziduum zaujímající plochu 30 x 30 mm. Po 2 měsících v anu ještě několik reziduálních polypózních útvarů. Koloskopická kontrola po 5 měsících byla již bez patologických změn, histologicky bez zánětu. Celková doba léčby trvala 5,5 měsíce se zhojením afekce v rektu ad integrum. Závěr: Kazuistika dokazuje nutnost multidisciplinárního přístupu k patologickým afekcím v rektu. Histologická verifikace, osobní a epidemiologická anamnéza jsou nezbytné. Doporučením neoadjuvantní chemoradioterapie nebo operace pouze na základě velmi sugestivních výsledků zobrazovacích vyšetření bychom pacienta výrazně poškodili.
Štítky
Dětská onkologie Chirurgie všeobecná Onkologie
Článek VI. Radioterapeutické metodyČlánek XI. Psychosociální péčeČlánek XIII. Nádory prsuČlánek EditorialČlánek XIV. Nádory jícnu a žaludkuČlánek XXVII. COVID-19Článek XVIII. Nádory hlavy a krkuČlánek XX. Gynekologická onkologieČlánek XXI. UroonkologieČlánek XXIV. Hematoonkologie
Článek vyšel v časopiseKlinická onkologie
Nejčtenější tento týden
2021 Číslo Supplementum 2- Ibrance® – nová šance pro pacientky s HR+/HER2– karcinomem prsu
- Vliv alkoholu na riziko vzniku karcinomu prsu, nově podle histologického typu nádoru a jeho senzitivity k estrogenovým receptorům
- Ženy s falešně pozitivním nálezem na mamografii pociťují zvýšenou úzkost a sníženou kvalitu života
- Exemestan zlepšuje interval bez relapsu při karcinomu prsu
- Přítomnost genetické mutace BRCA vede k častějšímu výskytu rakoviny i ve druhém prsu
-
Všechny články tohoto čísla
- XXVII. COVID-19
- XXVIII. Varia (ostatní, jinde nezařazené příspěvky)
- Predikce odpovědi na léčbu imunoterapií checkpoint inhibitory u pacientů s pokročilými solidními nádory
- Protektivní faktory prožívaného stresu u pacientů s mnohočetným myelomem
- I. Onkologická prevence a screening
- II. Epidemiologie nádorů, klinické registry, zdravotnická informatika
- III. Vzdělávání, kvalita a bezpečnost v onkologické praxi
- IV. Diagnostické metody v onkologii
- V. Onkochirurgie, rekonstrukční chirurgie
- VI. Radioterapeutické metody
- VII. Nežádoucí účinky protinádorové léčby
- VIII. Paliativní péče a symptomatická léčba
- IX. Nutriční podpora v onkologii
- X. Ošetřovatelská péče a rehabilitace
- XI. Psychosociální péče
- XII. Hereditární nádorové syndromy
- XIII. Nádory prsu
- Editorial
- XIV. Nádory jícnu a žaludku
- XV. Nádory tlustého střeva a konečníku
- XVI. Nádory slinivky, jater a žlučových cest
- XVII. Nádory skeletu a sarkomy
- XVIII. Nádory hlavy a krku
- XIX. Nádory hrudníku, plic, průdušek a pleury
- XX. Gynekologická onkologie
- XXI. Uroonkologie
- XXII. Neuroendokrinní a endokrinní nádory
- XXIII. Nádory nervového systému
- XXIV. Hematoonkologie
- XXV. Vývoj nových léčiv, farmakoekonomika, klinická farmacie v onkologii
- XXVI. Základní a aplikovaný výzkum v onkologii
- Klinická onkologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- XVI. Nádory slinivky, jater a žlučových cest
- VII. Nežádoucí účinky protinádorové léčby
- XV. Nádory tlustého střeva a konečníku
- VIII. Paliativní péče a symptomatická léčba
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Revma Focus: Spondyloartritidy
nový kurz
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Autoři: prof. MUDr. Pavel Horák, CSc., doc. MUDr. Ludmila Brunerová, Ph.D., doc. MUDr. Václav Vyskočil, Ph.D., prim. MUDr. Richard Pikner, Ph.D., MUDr. Olga Růžičková, MUDr. Jan Rosa, prof. MUDr. Vladimír Palička, CSc., Dr.h.c.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



