-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Podtlaková terapie hojení ran v onkogynekologii – současné poznatky a klinické využití
Autoři: Klára Balcárová 1
; Petra Bretová 1
; M. O. Ndukwe 1,2
; Daniel Leško 1; Martin Štěpán 1
; Jiří Špaček 1
Působiště autorů: Porodnická a gynekologická klinika LF UK a FN Hradec Králové 1; Klinika onkologie a radioterapie LF UK a FN Hradec Králové 2
Vyšlo v časopise: Ceska Gynekol 2025; 90(6): 495-502
Kategorie: Přehledová práce
doi: https://doi.org/10.48095/cccg2025495Souhrn
Podtlaková terapie ran představuje moderní a účinnou metodu prevence a léčby komplikací hojení operačních ran, jejíž využití v posledních letech narůstá také v gynekologii, zejména v oblasti gynekologické onkologie. Mechanizmus účinku této metody zahrnuje zajištění efektivní drenáže, redukci edému, podporu angiogeneze a stimulaci tvorby granulační tkáně, což ve svém důsledku přispívá k rychlejšímu hojení a nižšímu riziku infekce, vzniku seromu či dehiscence rány. Účinnost podtlakové terapie byla prokázána při léčbě komplikovaných, infikovaných nebo dehiscentních ran po onkogynekologických operacích. Novější studie rovněž naznačují, že profylaktická aplikace podtlakové terapie na primárně uzavřené incize po laparotomii či vulvektomii může významně snížit výskyt chirurgických komplikací, zkrátit dobu hospitalizace a urychlit rekonvalescenci, což je obzvláště významné u pacientek, které mají podstoupit adjuvantní léčbu. Vzhledem k tomu, že většina dostupných důkazů vychází z retrospektivních studií, je třeba dalších prospektivních randomizovaných studií, které by potvrdily účinnost této metody jak v léčbě, tak v prevenci a umožnily její zařazení do standardní perioperační péče v onkogynekologii.
Klíčová slova:
hojení ran – podtlaková terapie – gynekologické operace – dehiscence operační rány – gynekologické malignity
Úvod
Podtlaková terapie (NPWT – negative-pressure wound therapy) nebo také vakuový systém (VAC – vacuum assisted closure) představuje efektivní přístup v léčbě akutních i chronických ran. Podtlakový systém je velice často užíván k terapii operačních ran, a to zejména ran infikovaných a dehiscentních, u nichž jiné postupy léčby nevedou ke zdárnému hojení [1,2]. Podtlaková terapie hojení ran prošla výrazným vývojem od svých historických počátků, které sahají až do 19. století. Moderní koncept NPWT, jak jej známe dnes, byl zásadně rozvinut Argentou a Morykwasem, kteří v roce 1997 publikovali průlomovou práci prokazující její klinickou účinnost. Jejich výzkum zahrnoval nejen aplikaci v klinické praxi, ale také experimenty in vivo v laboratorních podmínkách s cílem optimalizovat hodnotu podtlaku pro co nejefektivnější hojení [2].
Vzhledem k prevalenci komorbidit u současné populace lze předpokládat, že incidence zhoršeného hojení chirurgických ran a výskyt infekcí v operačních ranách zůstane i v následujícím období vysoká. Běžné rizikové faktory, jako jsou obezita, diabetes mellitus, kardiovaskulární onemocnění, anemie, kouření, imunosuprese a malnutrice, jsou spojeny s prolongovaným hojením ran a zvýšenou náchylností k infekci. Tyto stavy mohou narušovat perfuzi a okysličení tkání, imunitní odpověď a syntézu kolagenu, čímž ohrožují integritu hojení rány [3]. Infekce v místě chirurgického výkonu (SSI – surgical site infection) přispívá k prodloužení hospitalizace, zvyšuje riziko dalších komplikací a zátěž ošetřovatelské péče, což se významně promítá do ekonomických nákladů zdravotnického systému [4].
Z těchto důvodů je žádoucí hledat účinné preventivní i terapeutické přístupy, které by mohly snížit riziko komplikací spojených s hojením operačních ran, zejména u rizikových skupin pacientek. Velký potenciál má metoda NPWT v rámci primárně uzavřených chirurgických ran (ciNPWT – closed-incision negative-pressure wound therapy), která může přispět ke snížení výskytu infekcí v místě chirurgického výkonu, dehiscencí, tvorby seromů a hematomů, a tím zkrátit dobu hospitalizace, urychlit rekonvalescenci a potenciálně zlepšit celkové onkologické výsledky u pacientek, u nichž je plánována adjuvantní terapie [4].
Cílem přehledové práce je shrnout aktuální poznatky z publikované literatury o podtlakové terapii ran v gynekologické onkologii se zaměřením na terapeutické i profylaktické využití. Článek zároveň popisuje principy a mechanizmy účinku NPWT, zabývá se klinickými indikacemi a praktickým zavedením této metody a přináší podrobný přehled alternativních a doplňkových strategií pro ošetřování ran.
Princip metody podtlakové terapie
Současné systémy NPWT využívají porézní polyuretanovou pěnu aplikovanou do rány, na niž je prostřednictvím elektronického přístroje připojen podtlak buď v kontinuálním, nebo intermitentním režimu. Tím je dosaženo subatmosferického tlaku, který příznivě ovlivňuje proces hojení. Mechanizmus účinku NPWT zahrnuje mechanické zpevnění a sblížení okrajů, odstranění extracelulární tekutiny a stabilizaci prostředí v ráně, což vede ke snížení edému a bakteriální kolonizace, zvýšení prokrvení, podpoře angiogeneze, tvorbě granulační tkáně a rychlejšímu hojení rány [5]. Konstantní podtlak zároveň výrazně zvyšuje lokální mikrocirkulaci krve a rozšiřuje průměr kapilár, arteriol a venul. Tato technika se využívá k podpoře tvorby granulační tkáně v otevřených ranách, čistých chirurgických incizích a při překrytí kožních štěpů. Benefitem NPWT je zkrácení doby hojení rány a snížení rizika chirurgických komplikací, včetně infekce v místě chirurgického výkonu, tvorby seromu, hematomu a dehiscence rány [6,7].
Optimální nastavení negativního tlaku při NPWT by mělo být přizpůsobeno typu rány, stavu okolní tkáně a riziku komplikací. Zatímco tradičně používaný tlak –125 mmHg je efektivní pro drenáž a kontrakci rány, novější studie ukazují, že maximálního biologického účinku, včetně tvorby granulační tkáně a regionální perfuze, lze často dosáhnout již při tlaku –80 mmHg [8]. Experimentální studie použití NPWT na otevřenou operační ránu prokázaly, že tlak v rozmezí –50 až –170 mmHg způsobuje signifikantní pokles průtoku krve ve střevních kličkách přímo pod krytím. Efekt byl lokalizovaný a rostl s intenzitou podtlaku, přičemž hlubší kličky negativním tlakem ovlivněny nebyly. Prolongovaná hypoperfuze může vést k ischemii a následné nekróze střevní stěny, což zvyšuje riziko vzniku enterokutánních a enteroatmosferických píštělí. Vložení neadhezivní ochranné bariéry mezi střeva a zdroj podtlaku bylo spojeno s nižší mírou petechiálního krvácení, a tedy nižším rizikem ischemického poškození [9].
Nové experimentální poznatky navíc ukazují, že NPWT nejen odsává tekutinu, ale také vyvíjí pozitivní tlak na okolní měkké tkáně, a tím zvyšuje lokální tkáňový tlak, což může paradoxně vést ke snížení perfuze. Důležitou roli hraje nejen intenzita podtlaku, ale i velikost a umístění pěnového krytí – větší plocha pěny přenáší vyšší celkový tlak na okolní měkké tkáně, zejména v jejích okrajových částech, kde bývá tlak nejvyšší (v experimentálním modelu naměřeno až 187 mm Hg). Naopak menší pěnové krytí při zachování stejné sací jednotky vyvíjí nižší kompresní síly na okolní tkáň, a může být proto výhodnější v situacích, kde hrozí ischemie, například u pacientů se zhoršeným periferním prokrvením. Navíc při aplikaci pěny mimo samotnou ránu nebo při překrytí okrajů rány jen částečně může být distribuce tlaku zcela odlišná, a může tak významně ovlivnit výsledný účinek i bezpečnost terapie. To podporuje potřebu nejen volit vhodnou výši podtlaku, ale také pečlivě přizpůsobit rozměr a umístění pěnové výplně konkrétní anatomické lokalitě a stavu měkkých tkání [10].
Podtlaková terapie hojení ran prochází v současnosti dynamickým vývojem provázeným řadou technologických inovací. Nové modifikace této metody nacházejí uplatnění také v aseptické chirurgii, kde jsou využívány k profylaktické aplikaci podtlakové terapie na primárně uzavřené chirurgické rány [11]. Byla rovněž vyvinuta zařízení umožňující instilaci, tedy cílenou aplikaci irigačních roztoků, včetně antibiotik, přímo do rány [2,12].
Přenosné jednorázové systémy podtlakové terapie hojení ran (suNPWT – single-use negative pressure wound therapy), zejména systémy s rezervoárem (CB – canister-based), se v posledních letech staly atraktivní volbou v rámci pooperační péče. Umožňují pacientům zachovat mobilitu, a tím přispívají ke zlepšení kvality života díky možnosti návratu k běžným denním aktivitám [13]. Ve srovnání s konvenčními NPWT systémy přinášejí také ekonomické výhody, jelikož vyžadují menší míru odborné intervence, což vede k lepším klinickým výsledkům, kratší době hojení a snížení délky hospitalizace [5,14].
Inovace se týkají také materiálů na rozhraní mezi systémem NPWT a povrchem rány, což umožňuje individualizovat biologickou odpověď podle charakteru defektu. Například velikost pórů ve výplňovém materiálu hraje zásadní roli v rychlosti tvorby granulační tkáně. Moderní NPWT systémy lze navíc kombinovat s dalšími chirurgickými technologiemi, jako jsou dermální nosiče (scaffolds) či zpracované alogenní nebo xenogenní materiály, které rozšiřují terapeutické možnosti v oblasti regenerativní chirurgie [15].
Obr. 1. Zhodnocení rozsahu dehiscence, hloubky defektu, přítomnosti nekrotické tkáně a exsudátu. Fig. 1. Evaluation of the extent of dehiscence, defect depth, and the presence of necrotic tissue and exudate. 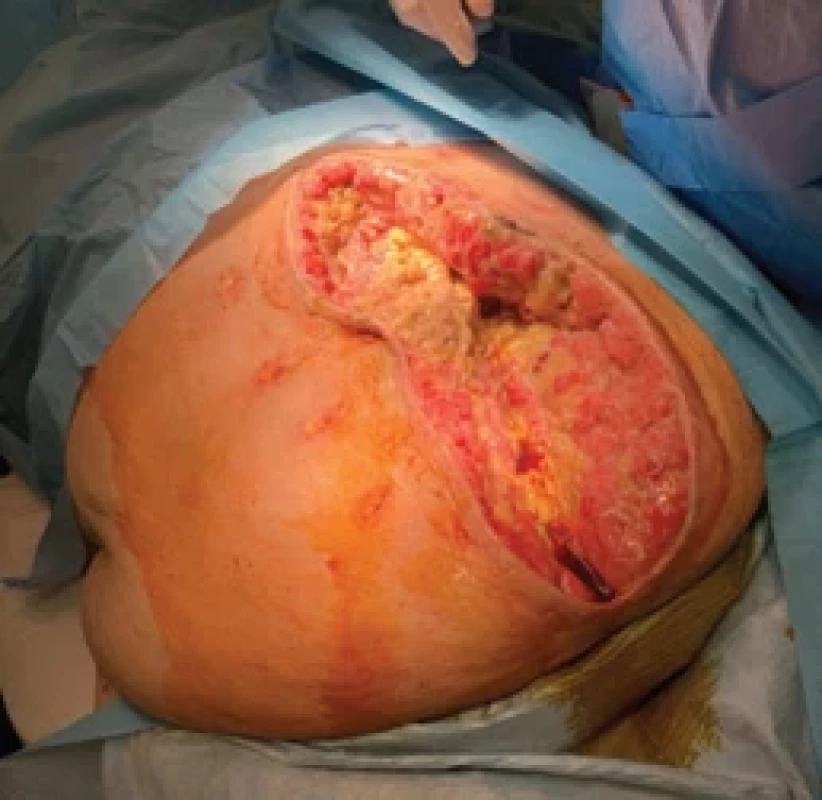
Obr. 2. Odstranění nekrotických tkání a koagul k dosažení čisté a dobře prokrvené spodiny rány. Fig. 2. Removal of necrotic tissue and coagula to achieve a clean and well-perfused wound bed. 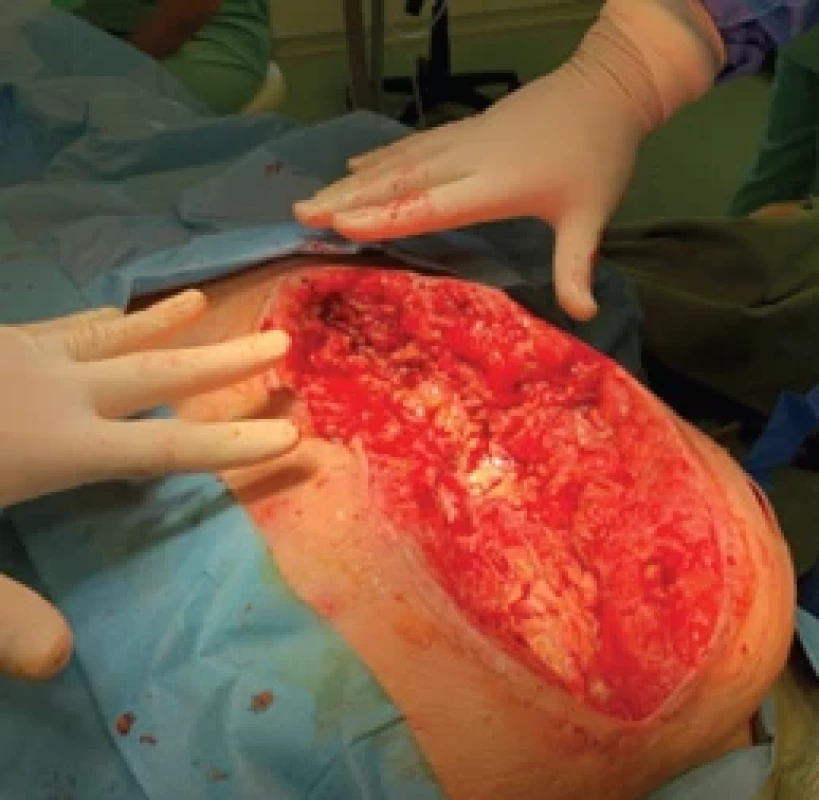
Využití podtlakové terapie v onkogynekologii
Minimálně invazivní přístupy, zejména laparoskopie a robotická chirurgie, jsou v současnosti preferovanými metodami pro řadu gynekologických výkonů včetně onkologických operací. Umožňují kratší hospitalizaci, nižší výskyt pooperačních komplikací a rychlejší návrat k běžné aktivitě [16]. Nicméně existuje skupina pacientek, u nichž je laparotomie i nadále nejvhodnějším nebo nezbytným operačním přístupem [17].
K laparotomii se přistupuje zejména v případech rozsáhlého pokročilého onkologického postižení, u nějž je cílem radikální cytoredukce a miniinvazivní přístup neumožňuje dostatečnou vizualizaci nebo bezpečné provedení resekcí a rekonstrukcí [18,19]. Dále se laparotomie preferuje u pacientek s mnohočetnými adhezemi po předchozích operacích, při urgentních stavech (např. masivní krvácení, perforace) nebo v situacích, kdy je laparoskopický přístup do dutiny břišní kontraindikován či neproveditelný [20].
V onkogynekologické praxi se NPWT etablovala zejména v léčbě komplikovaných operačních ran, například po abdominálních operacích (obr. 1–5) nebo vulvektomii [16]. Komplikace hojení operační rány, jako jsou infekce, dehiscence, hematom či serom, představují závažný klinický problém [21]. Jejich vznik ovlivňují faktory na straně pacientky, jako jsou například obezita, diabetes mellitus, vyšší věk, anemie nebo malnutrice, stejně jako intraoperační okolnosti včetně délky výkonu, operace na zažívacím traktu, krevní ztráty nebo způsobu primární sutury [22]. Hematomy a seromy vznikající při nedostatečné hemostáze či absenci drenáže zvyšují riziko infekce a zhoršují hojení. V tomto kontextu se NPWT uplatňuje jako metoda, která podporuje drenáž, snižuje otok a bakteriální kontaminaci, a tím zlepšuje proces hojení i u pacientek s vyšším rizikem komplikací [4,23].
NPWT se tedy v posledních letech stává slibnou metodou v prevenci a léčbě komplikací hojení ran i v oblasti onkogynekologie. Přestože většina dostupných důkazů pochází z oblasti všeobecné chirurgie, počet studií zaměřených specificky na onkogynekologické výkony je stále omezený a tyto případy bývají často součástí heterogenních souborů chirurgických výkonů.
Studie Argenta et al. představuje jednu z prvních kazuistických sérií, která popisuje využití NPWT u pacientek v gynekologické onkologii. Autoři referují kazuistickou sérii tří pacientek s komplikovaným hojením ran po onkogynekologických výkonech, u nichž použití NPWT vedlo k výraznému klinickému zlepšení. U všech pacientek došlo během 48–72 hod k poklesu exsudace a během 5–7 dnů k tvorbě robustní granulační tkáně. Průměrná doba potřebná k dosažení stavu vhodného k sekundárnímu uzavření rány nebo pokračující epitelizaci byla 10 dnů. U jedné z pacientek byla NPWT úspěšně aplikována i přes přítomnost enterokutánní píštěle a u jiné při obnažené polypropylenové síťce (MESH), přičemž nebyly zaznamenány žádné závažné komplikace. Autoři uzavírají, že NPWT představuje bezpečnou a efektivní metodu léčby hlubokých a infikovaných ran u onkogynekologických pacientek, zejména v případech, kde selhala konvenční terapie [24].
Schimp et al. ve své retrospektivní studii analyzovali 27 pacientek s gynekologickými malignitami a komplikovaným hojením ran, u nichž byla použita terapie negativním podtlakem. Výsledky ukázaly 96% mediánové zmenšení objemu rány (z 330 cm³ na 14 cm³) po mediánové době terapie 32 dnů. U 26 z 27 pacientek (96 %) došlo k úplnému zhojení rány. Většina pacientek (74 %) byla léčena ambulantně bez komplikací. Jediná komplikace byla mírné krvácení z rány. Tato studie potvrzuje bezpečnost a efektivitu NPWT u pacientek s onkogynekologickým onemocněním a podporuje její využití při léčbě komplikovaných ran po rozsáhlých chirurgických výkonech [25].
V posledních letech se zvyšuje zájem o využití NPWT u pacientek po chirurgické léčbě karcinomu vulvy. Recentní studie se zaměřují především na její efektivitu v prevenci a léčbě komplikací hojení ran po radikální vulvektomii, často kombinované s inguinofemorální lymfadenektomií a plastickými výkony. Vzhledem k anatomické lokalizaci, vysokému napětí operačních ran a častému výskytu infekcí, seromů či dehiscencí představují tyto výkony významné riziko pro poruchy hojení, které mohou vést ke zpoždění adjuvantní terapie a zhoršení prognózy [26]. NPWT se v této souvislosti ukazuje jako slibná metoda zajišťující drenáž exsudátu, snižující bakteriální kontaminaci a podporující tvorbu granulační tkáně.
Quercia et al. ve své retrospektivní kohortové studii hodnotili 18 pacientek po radikální vulvektomii s inguinofemorální lymfadenektomií, přičemž sedm z nich bylo léčeno NPWT a jedenáct tvořilo kontrolní skupinu. Skupina s NPWT měla signifikantně kratší délku hospitalizace (14,2 ± 4,7 vs. 17,1 ± 6,1 dne; p < 0,05) a rychlejší kompletní zhojení rány (zkrácení o 31,9 dne; 95% CI −43,5 až −20,3). Výskyt infekce, nekrózy ani dehiscence se mezi skupinami významně nelišil [27].
V jiné retrospektivní studii bylo zahrnuto 17 pacientek po operaci karcinomu vulvy, z nichž 16 podstoupilo NPWT. U všech došlo k úplnému zhojení rány, přičemž průměrná doba hojení byla 43,5 ± 17,9 dne. Terapie vedla k podpoře hojení laloku, redukci exsudace, zmírnění edému a snížení frekvence výměny krytí. Autoři zároveň popsali specifické technické přístupy, jak překonat anatomické výzvy perinea při aplikaci NPWT [28].
Obě studie tedy podporují využití NPWT jako účinného prostředku ke zlepšení výsledků hojení a k potenciálnímu zkrácení rekonvalescence po chirurgické léčbě vulvárního karcinomu.
Obr. 3. Aplikace ochranné silikonové kontaktní vrstvy Mepitel na exponované struktury. Fig. 3. Application of the Mepitel silicone contact layer to exposed structures. 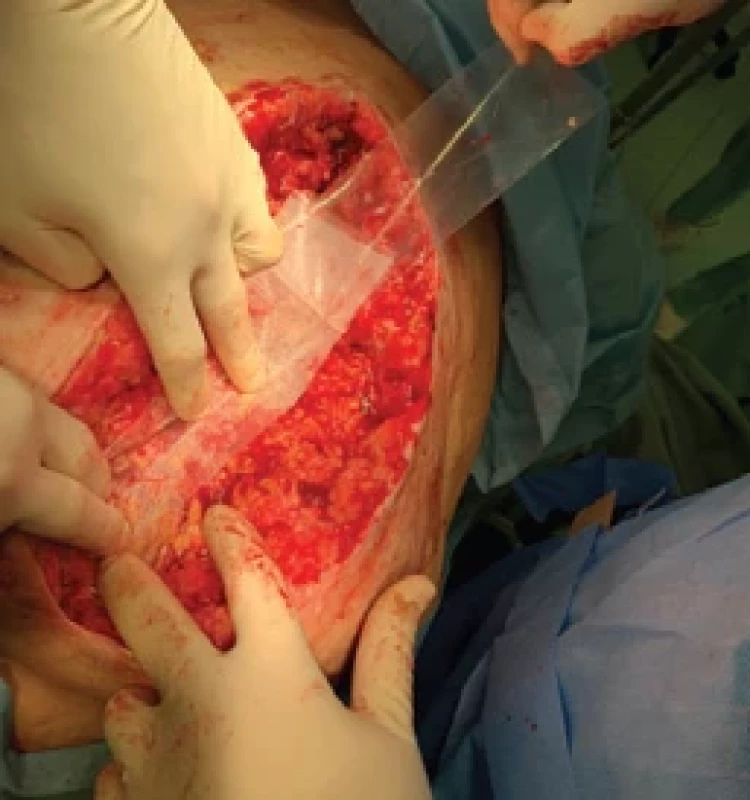
Obr. 4. Vložení polyuretanové pěny upravené podle tvaru rány a vyplnění defektu. Fig. 4. Insertion of polyurethane foam trimmed to the wound shape to fi ll the defect. 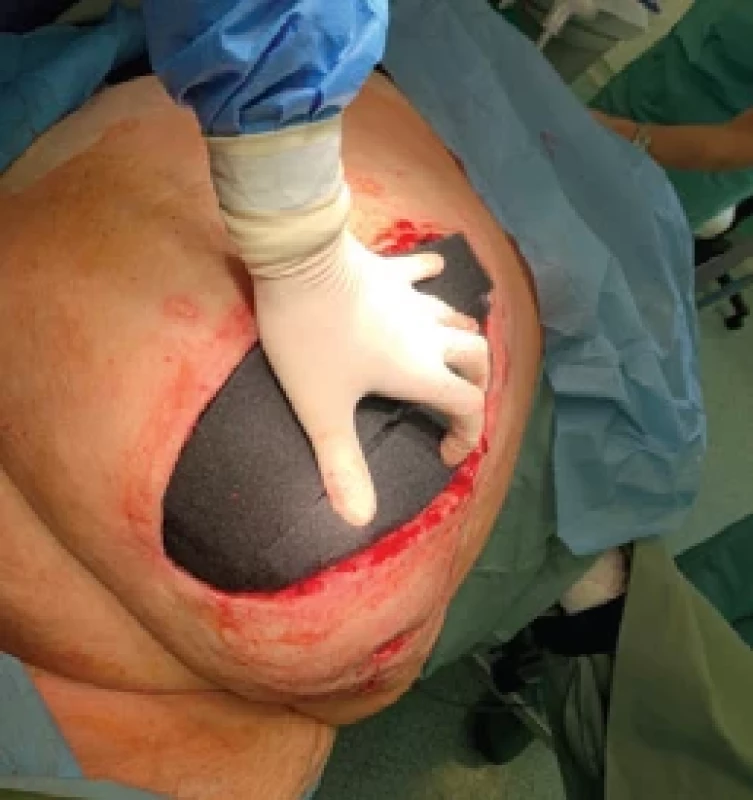
Obr. 5. Hermetické překrytí pěny okluzivní fólií, napojení sacího portu a spuštění podtlaku s kontrolou těsnosti systému. Fig. 5. Hermetic sealing of the foam with an occlusive drape, connection of the suction port, and initiation of negative pressure with system leak check. 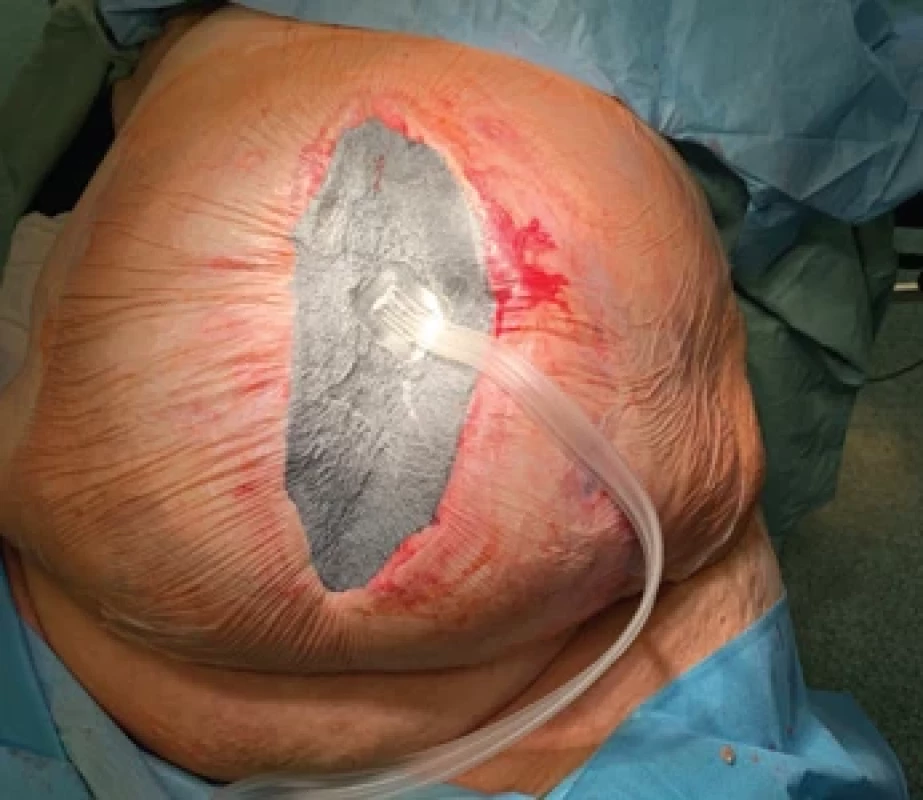
Profylaktické využití podtlakové terapie v onkogynekologii
Profylaktické využití ciNPWT v onkogynekologii představuje slibnou strategii v prevenci komplikací hojení operačních ran u vysoce rizikových pacientek. Recentní studie naznačují, že aplikace NPWT na primárně uzavřené incize po rozsáhlých abdominálních výkonech, jako je cytoreduktivní chirurgie či radikální hysterektomie, může významně snížit výskyt SSI, seromů a dehiscencí.
V recentní systematické přehledové studii a metaanalýze zahrnující 57 randomizovaných kontrolovaných studií s celkem 13 744 pacienty bylo prokázáno, že NPWT významně snižuje výskyt infekcí v místě chirurgického výkonu (RR 0,66; 95% CI 0,59–0,74), dehiscence rány (RR 0,72; 95% CI 0,60–0,87), seromu (RR 0,67; 95% CI 0,54–0,83) a hematomu (RR 0,68; 95% CI 0,53–0,88) u ran hojených per primam ve srovnání s konvenčním krytím. Největší přínos byl zaznamenán u pacientů se zvýšeným rizikem komplikací, například při přítomnosti obezity, diabetu či kardiovaskulárního onemocnění. Výsledky byly konzistentní napříč různými chirurgickými obory, včetně gynekologických výkonů, a potvrzují význam profylaktického využití NPWT jako účinného nástroje v prevenci raných pooperačních komplikací [5].
Martí et al. v retrospektivní kohortové studii porovnávali výskyt komplikací hojení operačních ran u 143 pacientek podstupujících laparotomii pro gynekologické malignity. Skupina s konvenčním krytím (n = 85) byla srovnávána se skupinou, u níž bylo po uzavření rány použito profylaktické podtlakové krytí (ciNPWT; n = 58). Výsledky ukázaly statisticky významné snížení výskytu komplikací ve skupině s ciNPWT (6,9 vs. 31,8 %; p < 0,001). Konkrétně došlo ke snížení výskytu povrchových infekcí (1,7 vs. 18,8 %), seromů (3,4 vs. 18,8 %) a dehiscencí rány (1,7 vs. 18,8 %). Průměrná délka hospitalizace byla ve skupině s ciNPWT zkrácena téměř o 3 dny (6,2 vs. 8,9 dne; p < 0,05). Tento efekt byl potvrzen i u obézních pacientek (BMI ≥ 30 kg/m²), u nichž se při použití ciNPWT komplikace vyskytovaly významně méně často [29].
Další studie zaměřená na využití ciNPWT u žen podstupujících operaci pro gynekologické malignity zkoumala její efekt na výskyt komplikací hojení ran. Retrospektivní analýza zahrnula 103 pacientek, z nichž 48 bylo léčeno pomocí ciNPWT a 55 tvořilo kontrolní skupinu. Výsledky ukázaly, že ve skupině s NPWT byl signifikantně nižší výskyt infekce v místě chirurgického výkonu (2 vs. 15 %; p = 0,03), nižší výskyt seromu (2 vs. 15 %; p = 0,03) i dehiscence (4 vs. 18 %; p = 0,04). Tato data podporují profylaktické použití NPWT jako efektivního nástroje ke snížení pooperačních komplikací v gynekologické onkologii [23].
Studie tedy naznačují, že profylaktická aplikace ciNPWT po laparotomii může významně snížit pooperační morbiditu a zároveň přinést potenciální úspory díky nižším nákladům na léčbu komplikací a kratší hospitalizaci. Profylaktická aplikace NPWT tak může představovat účinnou intervenci ke zlepšení perioperačních výsledků a snížení potřeby reintervencí v této specifické populaci.
Alternativy podtlakové terapie
Přestože je negativní podtlaková terapie považována za jednu z nejefektivnějších metod podpory hojení komplikovaných ran, její využití není vždy vhodné nebo dostupné [16]. V mnoha klinických situacích může být indikováno použití alternativních metod, které jsou jednodušší, ekonomicky méně náročné a méně invazivní. Mezi tyto alternativy patří zejména moderní formy vlhkého hojení, antimikrobiální krytí nebo biologické materiály. Výběr konkrétního postupu by měl vždy vycházet z individuálního posouzení typu rány, celkového klinického stavu pacientky a dostupnosti zdravotnických prostředků [30].
Tradiční krycí materiály, jako jsou gáza, sterilní savá vata či textilní obvazy, patří mezi nejběžněji používané prostředky v klinické praxi. Jejich hlavní výhodou je nízká cena a široká dostupnost. Na druhé straně však tyto materiály vykazují řadu omezení, jako nízkou absorpční kapacitu, nedostatečnou schopnost udržet vlhké prostředí a omezenou schopnost zabránit mikrobiální kontaminaci [31]. Také často přilnou ke spodině rány, což při převazech vede k sekundárnímu poškození tkáně a bolesti [30,32].
Mezi nejčastěji používané typy vlhkého krytí v moderní léčbě ran patří hydrokoloidy, algináty a hydrogely, které se liší svými vlastnostmi a indikacemi [33]. Hydrokoloidní krytí sestává z adhezivní matrice obsahující karboxymetylcelulózu, pektin a želatinu, která při kontaktu s exsudátem vytváří gel podporující autolytické čištění rány. Jsou vhodná pro mírně exsudující rány, dobře přiléhají k pokožce a umožňují pacientům běžné denní aktivity včetně koupání. Jejich účinnost byla potvrzena v několika metaanalýzách, které prokázaly lepší výsledky hojení ve srovnání se sterilní gázou [30,34]. Algináty získávané z mořských řas vynikají vysokou absorpční kapacitou a mírným hemostatickým účinkem, a proto se uplatňují u silně exsudujících ran. Naopak nejsou vhodné pro suché rány [35]. Hydrogely tvořené převážně vodou v hydrofilní polymerní síti jsou indikovány zejména u suchých a nekrotických ran, u nichž podporují hydrataci tkáně a zároveň mají chladivý a analgetický efekt [35,36]. Vhodný výběr konkrétního typu krytí umožňuje optimalizovat prostředí rány a urychlit proces hojení podle jejího aktuálního stavu [30–32].
Další alternativou NPWT je krytí s antimikrobiálními složkami, jako je stříbro, jód, polyhexanid či med (např. Manuka honey) [33]. Tato krytí snižují mikrobiální zátěž, minimalizují zánětlivou odpověď a mohou být indikována u kolonizovaných nebo infikovaných ran. Jejich použití by mělo být cílené a časově omezené, aby se předešlo cytotoxicitě a rozvoji bakteriální rezistence [32,37].
Mezi nové a stále více studované alternativy patří růstové faktory, terapie krevními deriváty a tkáňové inženýrství (bioaktivní matrice, kolagenová krytí, xenogenní transplantáty) [37–39]. Tyto postupy se zaměřují na stimulaci buněčné proliferace, angiogeneze a urychlení reepitelizace. Přestože je jejich využití v rutinní klinické praxi zatím omezené, představují slibný směr v personalizované terapii chronických ran [40,41].
Kombinace podtlakové terapie s krytím obsahujícím antimikrobiální složky je předmětem řady recentních studií [15,42,43]. Ali et al. ve své randomizované kontrolované studii prokázali, že spojení NPWT se stříbrným alginátovým krytím významně urychluje tvorbu granulační tkáně, snižuje intenzitu bolesti a je účinnější proti infekci ve srovnání s krytím bez obsahu stříbra [44]. Rovněž kombinace moderního vlhkého krytí s antimikrobiálními nebo biologicky aktivními látkami vykazuje potenciál ke zlepšení hojení i u klinicky náročných typů ran [32].
Závěr
Závěrem lze konstatovat, že podtlaková terapie představuje účinnou a bezpečnou metodu v prevenci a léčbě komplikací hojení operačních ran u pacientek po onkogynekologických výkonech. Dostupná data, včetně recentních studií zaměřených na vulvektomie, cytoreduktivní operace a jiné rozsáhlé operační výkony, ukazují na signifikantní snížení výskytu infekcí, seromů a dehiscencí při použití NPWT, a to jak v léčebném, tak profylaktickém kontextu.
Nicméně i přes pozitivní výsledky je třeba si uvědomit, že celá řada informací pochází z retrospektivních nebo observačních studií s omezenou velikostí souboru. Stále tedy existuje potřeba vysoce kvalitních prospektivních a randomizovaných studií, které by popsaly skutečnou účinnost NPWT v gynekologické onkologii a stanovily standardizované postupy týkající se načasování, délky aplikace, nastavení tlaku a optimálního výběru pacientek. Chybějí také údaje o dlouhodobých výsledcích, jako je oddálení adjuvantní léčby, onkologická prognóza a kvalita života udávaná pacientkami. Dále je třeba podrobněji zkoumat nákladovou efektivitu NPWT v různých zdravotnických systémech a její srovnatelnou hodnotu oproti jiným moderním strategiím hojení ran. Rozšíření evidence v těchto oblastech je nezbytné pro informované a na důkazech založené používání NPWT v gynekologické onkologii a pro jeho začlenění do rutinní perioperační péče.
Zdroje
1. Bastawisy KA, Hassan BD, Loon MM et al. Negative pressure wound therapy in the prevention of surgical site infections following abdominal surgery: a systematic review. Cureus 2025; 17 (4): e82237. doi: 10.7759/cureus.82237.
2. Zaver V, Kankanalu P. Negative Pressure wound therapy. In: StatPearls. Treasure Island (FL): StatPearls Publishing. 2025 [online]. Available from: http: //www.ncbi.nlm.nih.gov/books/NBK576388/.
3. Taliento C, Scutiero G, Milano C et al. Surgical site infections and sepsis in gynecological surgery. Int J Gynaecol Obstet 2025. doi: 10.1002/ijgo.70356.
4. Moreno Gijón M, Suárez Sánchez A, de Santiago Álvarez I et al. The efficacy of negative-pressure wound therapy (NPWT) in the prevention of surgical site occurrences in open abdominal surgery: a randomized clinical trial. Surgery 2025; 178 : 108920. doi: 10.1016/j.surg.2024.10.011.
5. Norman G, Shi C, Goh EL et al. Negative pressure wound therapy for surgical wounds healing by primary closure. Cochrane Database Syst Rev 2022; 2022 (4): CD009261. doi: 10.1002/14651858.CD009261.
6. Putri IL, Adzalika LB, Pramanasari R et al. Negative pressure wound therapy versus conventional wound care in cancer surgical wounds: a meta‐analysis of observational studies and randomised controlled trials. Int Wound J 2022; 19 (6): 1578–1593. doi: 10.1111/iwj.13756.
7. Agarwal P, Kukrele R, Sharma D. Vacuum assisted closure (VAC) /negative pressure wound therapy (NPWT) for difficult wounds: a review. J Clin Orthop Trauma 2019; 10 (5): 845–848. doi: 10.1016/j.jcot.2019.06.015.
8. Borgquist O, Ingemansson R, Malmsjö M. Individualizing the use of negative pressure wound therapy for optimal wound healing: a focused review of the literature. Ostomy Wound Manage 2011; 57 (4): 44–54.
9. Lindstedt S, Hlebowicz J. Blood flow response in small intestinal loops at different depths during negative pressure wound therapy of the open abdomen. Int Wound J 2013; 10 (4): 411–417. doi: 10.1111/j.1742-481X.2012.00998.x.
10. Biermann N, Geissler EK, Brix E et al. Pressure distribution and flow characteristics during negative pressure wound therapy. J Tissue Viability 2020; 29 (1): 32–36. doi: 10.1016/j.jtv.2019.12.004.
11. Hrubovčák J, Jelínek P, Žídek R et al. Profylaktické použití podtlakové terapie (Ci-NPWT) v aseptické chirurgii – přehled literatury. Cas Lek Cesk 2023; 162 (5): 207–211.
12. Kim PJ, Attinger CE, Crist BD et al. Negative pressure wound therapy with instillation: review of evidence and recommendations. Wounds 2015; 27 (12): S2–S19.
13. Henriksson AS. Single use negative pressure wound therapy (suNPWT) system with controlled fluid management technology – an evaluation of performance. Wounds 2021; 12 (4): 62–68.
14. Orlov A, Gefen A. The potential of a canister‐based single‐use negative‐pressure wound therapy system delivering a greater and continuous absolute pressure level to facilitate better surgical wound care. Int Wound J 2022; 19 (6): 1471–1493. doi: 10.1111/iwj.13744.
15. Huang C, Leavitt T, Bayer LR et al. Effect of negative pressure wound therapy on wound healing. Curr Probl Surg 2014; 51 (7): 301–331. doi: 10.1067/j.cpsurg.2014.04.001.
16. Frountzas M, Karavolias I, Nikolaou C et al. The Impact of Prophylactic Negative Wound Pressure Treatment (NWPT) on surgical site occurrences after gynecologic cancer surgery: a meta-analysis of randomized controlled and observational cohort studies. Cancers (Basel) 2025; 17 (10): 1717. doi: 10.3390/cancers17101717.
17. Aarts JW, Nieboer TE, Johnson N et al. Surgical approach to hysterectomy for benign gynaecological disease. Cochrane Database Syst Rev 2015; 2015 (8): CD003677. doi: 10.1002/14651858.CD003677.
18. Concin N, Matias-Guiu X, Vergote I et al. ESGO/ESTRO/ESP guidelines for the management of patients with endometrial carcinoma. Int J Gynecol Cancer 2021; 31 (1): 12–39. doi: 10.1136/ijgc-2020-002230.
19. Querleu D, Planchamp F, Chiva L et al. European Society of Gynaecological Oncology (ESGO) Guidelines for Ovarian Cancer Surgery. Int J Gynecol Cancer 2017; 27 (7): 1534–1542. doi: 10.1097/IGC.0000000000001041.
20. Wong JM, Arlandson M, Milad M. Use of negative pressure wound therapy in benign gynecologic surgery: a review. Am J Obstet Gynecol 2018; 218 (2): S947–S948. doi: 10.1016/j.ajog.2017.12.108
21. Hagedorn C, Dornhöfer N, Aktas B et al. Risk factors for surgical wound infection and fascial dehiscence after open gynecologic oncologic surgery: a retrospective cohort study. Cancers (Basel) 2024; 16 (24): 4157. doi: 10.3390/cancers16244157.
22. Gillispie-Bell V. Prevention of surgical site infections in gynecologic surgery: a review of risk factors and recommendations. Ochsner J 2020; 20 (4): 434–438. doi: 10.3148/toj.20. 0044.
23. Chambers LM, Morton M, Lampert E et al. Use of prophylactic closed incision negative pressure therapy is associated with reduced surgical site infections in gynecologic oncology patients undergoing laparotomy. Am J Obstet Gynecol 2020; 223 (5): 731.e1–731.e9. doi: 10.1016/j.ajog.2020.05.011.
24. Argenta P, Rahaman J, Gretz H et al. Vacuum-assisted closure in the treatment of complex gynecologic wound failures. Obstet Gynecol 2002; 99 (3): 497–501. doi: 10.1016/s0029-7844 (01) 01752-5.
25. Schimp V, Worley C, Brunello S et al. Vacuum-assisted closure in the treatment of gynecologic oncology wound failures. Gynecol Oncol 2004; 92 (2): 586–591. doi: 10.1016/j.ygyno. 2003.10.055.
26. Cebolla-Verdugo M, Cassini-Gomez de Cadiz VA, Velasco-Amador JP et al. Multidisciplinary vulvar cancer management: the dermatologist’s perspective. Life (Basel) 2025; 15 (1): 19. doi: 10.3390/life15010019.
27. Quercia V, Saccone G, Raffone A et al. Use of negative pressure wound therapy systems after radical vulvectomy for advanced vulvar cancer. Cancer Invest 2020; 38 (8–9): 531–534. doi: 10.1080/07357907.2020.1817484.
28. Qiu L, Wu X, Wang X. Application of negative-pressure wound therapy in patients with wound complications after flap repair for vulvar cancer: a retrospective study. Adv Skin Wound Care 2025; 38 (3): 142–147. doi: 10.1097/ASW.0000000000000247.
29. Martí MT, Fernandez-Gonzalez S, Martí MD et al. Prophylactic incisional negative pressure wound therapy for gynaecologic malignancies. Int Wound J 2022; 19 (2): 272–277. doi: 10.1111/iwj.13628.
30. Britto EJ, Nezwek TA, Popowicz P et al. Wound dressings. In: StatPearls. Treasure Island (FL): StatPearls Publishing. 2025 [online]. Available from: http: //www.ncbi.nlm.nih.gov/books/NBK470199/.
31. Obagi Z, Damiani G, Grada A et al. Principles of wound dressings: a review. Surg Technol Int 2019; 35 : 50–57.
32. Gou Y, Hu L, Liao X et al. Advances of antimicrobial dressings loaded with antimicrobial agents in infected wounds. Front Bioeng Biotechnol 2024; 12 : 1431949. doi: 10.3389/fbioe. 2024.1431949.
33. Powers JG, Higham C, Broussard K et al. Wound healing and treating wounds: chronic wound care and management. J Am Acad Dermatol 2016; 74 (4): 607–625. doi: 10.1016/j.jaad. 2015.08.070.
34. Liang Y, He J, Guo B. Functional hydrogels as wound dressing to enhance wound healing. ACS Nano 2021; 15 (8): 12687–12722. doi: 10.1021/acsnano.1c04206.
35. Zhang M, Zhao X. Alginate hydrogel dressings for advanced wound management. Int J Biol Macromol 2020; 162 : 1414–1428. doi: 10.1016/j.ijbiomac.2020.07.311.
36. Peng W, Li D, Dai K et al. Recent progress of collagen, chitosan, alginate and other hydrogels in skin repair and wound dressing applications. Int J Biol Macromol 2022; 208 : 400–408. doi: 10.1016/j.ijbiomac.2022.03.002.
37. Yousefian F, Hesari R, Jensen T et al. Antimicrobial wound dressings: a concise review for clinicians. Antibiotics (Basel) 2023; 12 (9): 1434. doi: 10.3390/antibiotics12091434.
38. Stanirowski PJ, Wnuk A, Cendrowski K et al. Growth factors, silver dressings and negative pressure wound therapy in the management of hard-to-heal postoperative wounds in obstetrics and gynecology: a review. Arch Gynecol Obstet 2015; 292 (4): 757–775. doi: 10.1007/s00404-015-3709-y.
39. Han G, Ceilley R. Chronic wound healing: a review of current management and treatments. Adv Ther 2017; 34 (3): 599–610. doi: 10.1007/s12325-017-0478-y.
40. Li R, Liu K, Huang X et al. Bioactive materials promote wound healing through modulation of cell behaviors. Adv Sci (Weinh) 2022; 9 (10): e2105152. doi: 10.1002/advs.2021 05152.
41. Mullin JA, Rahmani E, Kiick KL et al. Growth factors and growth factor gene therapies for treating chronic wounds. Bioeng Transl Med 2024; 9 (3): e10642. doi: 10.1002/btm2. 10642.
42. Abu-Baker A, Țigăran AE, Peligrad T et al. Exploring an innovative approach: integrating negative-pressure wound therapy with silver nanoparticle dressings in skin graft procedures. J Pers Med 2024; 14 (2): 206. doi: 10.3390/jpm14020206.
43. Veale RW, Kollmetz T, Taghavi N et al. Influence of advanced wound matrices on observed vacuum pressure during simulated negative pressure wound therapy. J Mech Behav Biomed Mater 2023; 138 : 105620. doi: 10.1016/j.jmbbm.2022.105620.
44. Ali M, Ali H, Akhlaq F et al. A comparative study of negative pressure dressing with and without silver alginate to promote faster wound healing in chronic wounds. Pak Armed Forces Med J 2022; 72 (3): 913–916. doi: 10.51253/pafmj.v72i3.7489.
ORCID autorů
K. Balcarová 0009-0007-9197-2073
P. Bretová 0000-0003-1082-433X
M. I. Ndukwe 0000-0001-8900-8057
M. Štěpán 0000-0002-5976-2291
Doručeno/ Submitted: 4. 8. 2025
Přijato/ Accepted: 5. 8. 2025
MU Dr. Petra Bretová, Ph.D.
Porodnická a gynekologická klinika
LF UK a FN Hradec Králové
Sokolská 581
500 05 Hradec Králové
petra.bretova1@fnhk.cz
Štítky
Dětská gynekologie Gynekologie a porodnictví Reprodukční medicína
Článek Mechanizmy navigace spermií
Článek vyšel v časopiseČeská gynekologie
Nejčtenější tento týden
2025 Číslo 6- Aktuální doporučení pro diagnostiku von Willebrandovy choroby
- Postabortivní syndrom – symptomy, dopady a možnosti léčby
- Trombóza portální žíly jako komplikace infekce COVID-19 – kazuistika
- Romosozumab zlepšuje kostní mikroarchitekturu u postmenopauzálních žen s osteoporózou
- S MUDr. Janem Rosou o problematice osteoporózy u revmatologických pacientů: Kdy začít s osteoanaboliky a jak minimalizovat selhání léčby?
-
Všechny články tohoto čísla
- Vliv vybraných imunohistochemických a klinicko-patologických markerů na prognózu pacientek se zhoubným nádorem dělohy
- HLA-C a KIR interakce jako možná příčina reprodukčních neúspěchů
- Který způsobuje menší bolest? Srovnání misoprostolu a dinoprostonu při indukci porodu
- Pooperační analgezie při operacích karcinomu prsu – anestetické techniky a role cytokinů
- Vliv produktů akumulace lipidů, triglyceridového/ glukózového indexu a viscerálního adipozitního indexu na kardiometabolické rizikové faktory u mladých pacientek se syndromem polycystických ovarií
- Dvojčetné těhotenství v jizvě po císařském řezu – kazuistika a literární přehled terapeutických přístupů
- Arteriovenózní malformace vznikající v jizvě po císařském řezu po ukončení těhotenství – kazuistika a přehled literatury
- Ne každý záchvat je eklampsie – vzácný případ mozkového abscesu u těhotné ženy způsobeného Streptococcus pneumoniae z dentálního zdroje
- Atypický uzlík v placentární oblasti detekovaný hysteroskopií – první kazuistika z Brazílie
- Mechanizmy navigace spermií
- Podtlaková terapie hojení ran v onkogynekologii – současné poznatky a klinické využití
- Česká gynekologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- HLA-C a KIR interakce jako možná příčina reprodukčních neúspěchů
- Vliv vybraných imunohistochemických a klinicko-patologických markerů na prognózu pacientek se zhoubným nádorem dělohy
- Podtlaková terapie hojení ran v onkogynekologii – současné poznatky a klinické využití
- Který způsobuje menší bolest? Srovnání misoprostolu a dinoprostonu při indukci porodu
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



