-
Články
Top novinky
Reklama- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
Top novinky
Reklama- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Top novinky
ReklamaPrognostický význam Pgp, MRP1 a MRP3 u pacientek s karcinomem ovaria
Prognostic significance of Pgp, MRP1, and MRP3 in ovarian cancer patients
Objective:
To evaluate the correlation of resistance proteins Pgp (P-glycoprotein), MRP1 (Multidrug Related Protein, Multidrug Resistance–Associated Protein) and MRP3 with clinical – pathological factors and to find the clinical outcome of these data in ovarian cancer patients.Design:
Prospective study.Setting:
Department of Gynecology and Obstetrics, Charles University in Prague, Faculty of Medicine in Hradec Králové, University Hospital Hradec Králové.Methods:
133 patients with epithelial ovarian cancer who underwent primary surgery from 2006–2010 had specimens stained with imunohistochemistry for Pgp, MRP1, MRP3.Results:
The histological subtype of epithelial ovarian cancer correlated with the expression of PgP, MRP1, and MRP3. The lowest incidence of Pgp and MRP1 expression was documented in endometrioid ovarian cancers (P = 0.151, P = 0.013). Patients with advanced ovarian cancer (FIGO III+IV) had higher MRP1 expression than those with early stage ovarian cancer (Med MRP1 FIGO I+II 80%; CI: 60–100; FIGO III+IV 100%; CI: 90–100; P = 0.100). An association was observed between MRP1 and tumor grade (Med MRP1 G1 80% (CI: 0–100), G2 80% (CI: 30–100), G3 100% (CI: 90–100); P < 0.001). There was no relationship between the size of the residual tumor after primary surgery and any resistance proteins. Patients with complete response after primary treatment had lower levels of LRP, Pgp, and MRP1 expression than other patients. Patients with higher Pgp and MRP1 expression had relapse of disease during the following 24 months more often than patients with lower Pgp and MRP1 expression. FIGO stage, histological type, debulking efficiency, and Pgp and MRP1 expression correlated with poor patient survival (P < 0.001, P < 0.001, P < 0.001, P = 0.040, P = 0.026).Conclusion:
We found prognostic significance of Pgp, MRP1 and MRP3 expression in ovarian cancer patients. MRP1 have some additional prognostic value for the clinical outcome of patients with ovarian carcinoma.Keywords:
ovarian carcinoma, Pgp/ABCB1, MRP1/ABCC1, MRP3/ABCC3, drug resistance
Autoři: I. Sedláková 1; J. Laco 2; J. Tošner 1; J. Špaček 1
Působiště autorů: Porodnická a gynekologická klinika LF UK a FN, Hradec Králové, přednosta doc. MUDr. J. Špaček, PhD., IFEPAG 1; Fingerlandův ústav patologie LF UK a FN, Hradec Králové, přednosta prof. MUDr. A. Ryška, Ph. D. 2
Vyšlo v časopise: Ceska Gynekol 2015; 80(6): 405-413
Souhrn
Cíl studie:
Cílem této práce je stanovení proteinů rezistence Pgp (P-glykoprotein) , MRP1 (Multidrug Related Protein, Multidrug Resistance – Associated Protein) a MRP3 a zjištění jejich prognostického významu u ovariálního karcinomu.Typ studie:
Prospektivní klinická studie.Název a sídlo pracoviště:
Porodnická a gynekologická klinika LF UK a FN Hradec Králové.Metodika:
Stanovení proteinů rezistence (Pgp, MRP1, MRP3) jsme provedli u 133 vzorků ovariálních karcinomů u pacientek operovaných na Porodnické a gynekologické klinice FN Hradec Králové v letech 2006–2013. Proteiny rezistence jsme stanovili metodou dvoustupňové imunohistochemie.Výsledky:
Pgp, MRP1 a MRP3 vykazovaly výrazné rozdíly hodnot v závislosti na histologickém typu ovariálního karcinomu. Nejnižší hodnoty Pgp a MRP1 jsme zjistili u endometroidního ovariálního karcinomu (p = 0,151, p = 0,013). Stupeň diferenciace významně ovlivnil pouze hodnoty MRP1, které narůstaly směrem od dobře diferencovaného ke špatně diferencovanému karcinomu ovaria (G1 80 % (CI 0–100), G2 80 % (CI 30–100), G3 100 % (CI 90–100), p < 0,001). Zaznamenán byl nárůst MRP1 od časných stadií (I+II) k pokročilému onemocnění (III+IV) (I+II 80 % (CI 60–100), III+IV 100 % (CI 90–100), p = 0,100). Peroperační velikost nádoru ani velikost nádorového rezidua po primární operaci nevykazovaly vztah s žádným z námi sledovaných proteinů rezistence. Pacientky s kompletní odpovědí na primární léčbu měly nižší hodnoty MRP1 v porovnání s ostatními pacientkami. Pacientky s vyššími hodnotami Pgp, MRP1, MRP3 měly také vyšší riziko recidivy. Jako statisticky významné faktory mající vliv na délku přežití byly v univariantní analýze zjištěny: FIGO stadium (p < 0,001), histologický typ nádoru (p < 0,001), přítomnost reziduálního tumoru (p < 0,001), exprese Pgp (p = 0,040), exprese MRP1 (p = 0,026).Závěr:
Prokázali jsme prognostický význam stanovení Pgp, MRP1 a MRP3 u pacientek s karcinomem ovaria. MRP1 je z proteinů rezistence nejperspektivnější prognostický faktor u pacientek s karcinomem ovaria.Klíčová slova:
karcinom ovaria, Pgp/ABCB1, MRP1/ABCC1, MRP3/ABCC3, chemorezistenceÚVOD
Ovariální karcinom je šestým nejčastějším karcinomem u žen v České republice, reprezentuje 1,7 % ze všech nově diagnostikovaných neoplazmat (3,7 % u žen). Výsledky přežití pacientek se za posledních 20 let zlepšily minimálně [4]. Standardní primární léčba se skládá z chirurgického výkonu a chemoterapie (paklitaxel + karboplatina) u naprosté většiny pacientek s karcinomem ovaria. Hlavním klinickým problémem současné cytostatické léčby ovariálního karcinomu je léková rezistence na cytostatika (chemorezistence). Jejím následkem je selhání léčby [5].
Kompletní odpověd na primární chemoterapii je vysoká, mezi 50–70 %. Přesto 50–75 % pacientek s pokročilým ovariálním karcinomem onemocnění relabuje a dochází k vývoji lékové rezistence, zejména mnohočetné lékové rezistence (MDR). Maligní buněčné populace mohou být vůči chemoterapii rezistentní již v primární léčbě. V tomto případě jde o tzv. přirozenou (primární) rezistenci. Získaná (sekundární) rezistence vzniká až v průběhu cytostatické léčby, kdy se původně citlivé buňky stávají rezistentními a účinnost cytostatické léčby se snižuje. Pokud při ztrátě citlivosti k jednomu přípravku vzniká současně rezistence na jiné, většinou strukturálně příbuzné cytostatikum, hovoříme o rezistenci zkřížené. Byly však popsány případy zkřížené rezistence mezi protinádorovými léčivy lišícími se jak strukturálně, tak mechanismem účinku. Takové případy rezistence pak nazýváme mnohočetná léková rezistence (multidrug resistance, MDR). MDR vysvětluje případy necitlivosti některých nádorů k alternativním léčebným režimům, obsahujícím nové druhy cytostatik nepoužitých v původní léčbě. Typická (klasická) MDR je zapříčiněna membránovým P-glykoproteinem (Pgp), který je produktem MDR1 genu. Jako atypická MDR jsou souhrnně označovány všechny mechanismy mnohočetné lékové rezistence, na kterých se neúčastní Pgp [16].
Jedním ze základních mechanismů vzniku MDR je transportní funkce některých transmembránových proteinů ze skupiny tzv. ABC-transportérů (ATP binding cassette proteins). Jedním z nejvýznamnějších ABC-transportérů přispívajících k rozvoji MDR je právě P-glykoprotein. Jedná se o transmembránový glykoprotein o velikosti 170 kDa tvořený 1280 aminokyselinami [19]. Pgp/MDR je běžně exprimován v játrech, ledvinách, střevech, mozku, děloze, varlatech a placentě [14]. Z toho vyplývá i jeho fyziologická funkce, kterou je především řízení absorpce, distribuce a exkrece celé řady xenobiotik včetně řady klinicky významných léčiv. Brání také průniku xenobiotik do mozku či reprodukčních orgánů [18]. Pgp je kódován genem MDR1 (ABCB1). Exprese proteinu koreluje s expresí na úrovni genu [10]. Substráty Pgp je řada protinádorových léčiv, jako vinka-alkaloidy, antracykliny, taxany, kolchicin a aktinomycin D [14]. Taxany jsou standardní součástí chemoterapie první linie pokročilého ovariálního karcinomu. Při zvýšené expresi Pgp/MDR mohou být taková léčiva za účasti transportní funkce Pgp předčasně vylučována z nádorových buněk, což může způsobit pokles účinku dané léčby.
V roce 1992 byl objeven druhý ABC transportér nazývaný multidrug resistance-associated protein (MRP, MRP1/ABCC1). MRP1 byl následně rozpoznán jako prototyp nové podskupiny transportérů, ze kterých MRP1 zůstává zatím jako nejlépe charakterizovaný [3, 8]. Nejdůležitější geny ABC transportních proteinů podílející se na lékové rezistenci zahrnují MDR1/ABCB1 (Pgp), několik členů z podskupiny MRP/ABCC a ABCG2 [12]. Úloha ABC transportérů v klinické rezistenci a zejména rezistenci u chemonaivních pacientů se solidními nádory je stále předmětem mnoha diskusí.
Cílem této práce je zhodnocení prognostického významu proteinů rezistence Pgp (P-glycoprotein, ABCB1), MRP1 (Multidrug Related Proetin, ABCC1) a MRP3 (ABCC3) a jejich klinicko-patologického významu u pacientek s karcinomem ovaria.
METODIKA
Stanovení proteinů rezistence Pgp, MRP1, MRP3
Proteiny rezistence Pgp (P-glycoprotein), MRP1 (Multidrug Related Protein) a MRP3 jsme stanovili standardním postupem dvoustupňovou imunohistochemií ve Fingerlandově ústavu patologie ve Fakultní nemocnici Hradec Králové. Materiál získaný při operaci byl po odběru rutinně fixován v 10% formalinu. Ve všech případech byl proveden standardizovaný odběr tkáně na histologické (a následné imunohistochemické) vyšetření. Byly odebrány vždy nejméně tři vzorky z nádoru (zpravidla 1 bloček na 1 cm nádoru) se zaměřením na pouzdro, případně periferii tumoru. Tkáňové bločky byly dále zpracovány standardní histologickou technikou a zality do parafinu. Z každého bločku byly krájeny řezy o tloušťce 2–3 mm. Tyto řezy byly použity jednak k rutinnímu barvení hematoxylinem-eozinem, jednak k imunohistochemickému vyšetření. Stanoven byl histologický typ nádoru a stupeň jeho diferenciace.
Parafinové bločky byly imunohistochemicky vyšetřeny za použití těchto primárních protilátek: Pgp (klon C494, LabVision, Fremont, USA, ředění 1 : 50), MRP1 (klon 33A6, Novocastra, Newcastle upon Tyne, United Kingdom, ředění 1 : 100) a MRP3 (klon DTX 1, Novocastra, ředění 1 : 100). Antigen MRP1 byl demaskován inkubací v citrátovém pufru (pH 6) při teplotě 95 °C po dobu 30 minut (Pgp), resp. 60 minut (MRP1). Protein MRP3 byl demaskován v pufru S 3308 (DakoCytomation, Glostrup, Dánsko) (pH 6) při teplotě 95 °C po dobu 60 minut. K imunohistochemickému vyšetření byla užita nepřímá imunohistochemická metoda s použitím avidin-biotinového vizualizačního systému EnVision+ (DakoCytomation).
Ve světelném mikroskopu pak byla kvantitativně hodnocena pozitivita reakce, tj. procento pozitivních (hnědě zbarvených) nádorových buněk: Pgp – membránová, popř. i cytoplazmatická pozitivita, MRP1 – membránová, případně i cytoplazmatická pozitivita, MRP3 – membránová, popř. i cytoplazmatická pozitivita.
SOUBOR PACIENTEK
Stanovení proteinů rezistence (Pgp, MRP1, MRP3) jsme provedli u 133 vzorků epiteliálních ovariálních karcinomů u pacientek operovaných na Porodnické a gynekologické klinice FNHK v letech 2006–2013 (tab. 1). Pacientky před danou operací neprodělaly chemoterapii ani žádnou jinou léčbu pro ovariální karcinom. Jednalo se o pacientky s nově zjištěným karcinomem ovaria – chemonaivní. Žádná z těchto pacientek nebyla v minulosti léčena pro jiný karcinom. Všechny pacientky měly před operací podepsaný informovaný souhlas s odběrem vzorků tkáně schválený Etickou komisí FNHK. Sto pacientek z tohoto souboru dostalo podle současných doporučených standardů v rámci adjuvantní pooperační chemoterapie první linie šest cyklů kombinace paklitaxel (175 mg/m2) a karboplatina (AUC 5–6) a bylo možné od nich získat potřebné klinické údaje.
Tab. 1. Charakteristika souboru 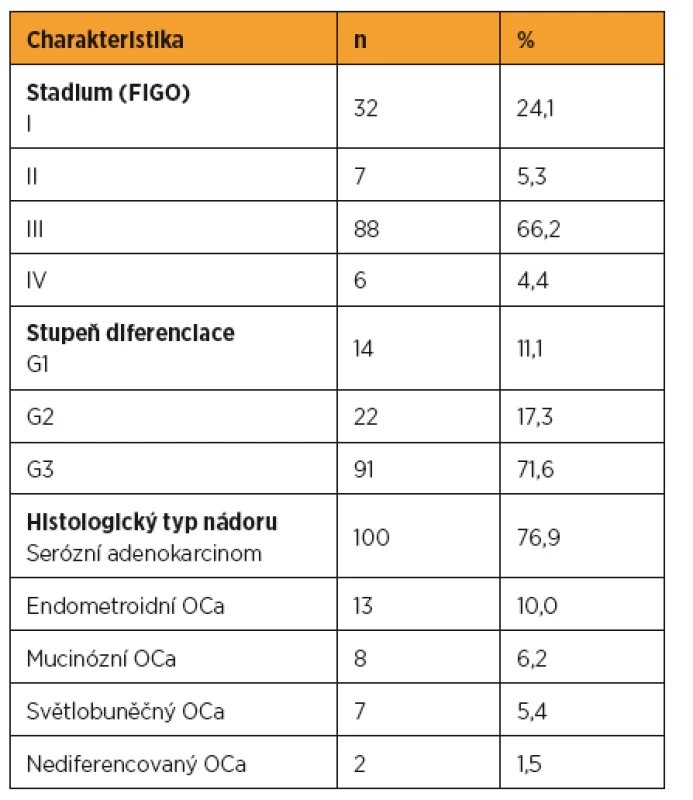
Průměrný věk testovaných pacientek byl 63,8 let (33–89 let). Stadium bylo stanoveno podle FIGO klasifikace (International Federation of Obstetrics and Gynecology). Za časné onemocnění jsme považovali stadium I+II a pokročilé onemocnění stadium III+IV. Jednalo se o 32 pacientek se stadiem I, 7 pacientek se stadiem II, 88 pacientek se stadiem III a 6 pacientek se stadiem IV. Histopatologický typ ovariálního karcinomu byl stanoven podle World Health Organization (WHO) klasifikace. Dobře diferencovaný ovariální karcinom v tomto souboru mělo 14 pacientek, 22 pacientek středně diferencovaný ovariální karcinom a 91 pacientek špatně diferencovaný karcinom ovaria. U dvou pacientek byl diagnostikován nediferencovaný ovariální karcinom. U tří pacientek nebyl stupeň diferenciace určen. Serózní ovariální karcinom mělo 100 žen, mucinózní ovariální karcinom osm pacientek, endometroidní ovariální karcinom mělo 13 pacientek a sedm žen mělo světlobuněčný ovariální karcinom. Pacientky s jinými histologickými typy ovariálního karcinomu ani borderline tumory jsme do této práce nezahrnuli.
Klinické údaje jsme zpětně dohledali z dokumentace pacientek. Minimální follow-up pro sledování klinických údajů bylo tři roky. Léčebnou odpověď na primární léčbu jsme hodnotili podle RECIST kritérií (RECIST 1.1). Typ léčebné odpovědi jsme stanovili na základě výsledků objektivního vyšetření, Ca 125, rtg plic a CT břicha po skončení chemoterapie první linie. Všechny pacientky s časným onemocněním (I+II) v našem souboru měly kompletní odpověď na primární léčbu. Kompletní odpověď na primární léčbu jsme zaznamenali celkem u 81 pacientek, částečnou odpověď na primární léčbu u osmi žen, „stable disease“ u tří pacientek a progresi onemocnění po skončení primární léčby u devíti žen z našeho souboru. Za délku PFS (progression free survival, bezpříznakové období) jsme považovali období od dosáhnutí kompletní remise onemocnění do objevení se recidivy potvrzené laboratorně i zobrazovacími metodami.
Pro popis souboru byly použity deskriptivní metody statistiky. Vzhledem k tomu, že byla u většiny případů zamítnuta normalita, použili jsme pro hodnocení prostřední hodnoty (medián, Med) a pro stanovení míry rozptylu jsme využili 95% interval spolehlivosti (CI – Confidence Interval). Porovnání jednotlivých skupin bylo provedeno neparametrickým Mannovým-Whitneyho testem případně Kolmogorovovým-Smirnovovým testem, v případě tří skupin byla použita Kruskalova-Walisova neparametrická analýza rozptylu. Log-rank test pro porovnání Kaplanových-Meierových křivek pro PFS a OS. Za statisticky významnou jsme považovali hladinu významnosti p < 0,05.
VÝSLEDKY
Proteiny rezistence Pgp a MRP1 vykazovaly výrazné rozdíly hodnot v závislosti na histologickém typu ovariálního karcinom. Nejvyšší hodnoty Pgp, MRP1 a MRP3 byly zjištěny u mucinózního ovariálního karcinomu v porovnání s ostatními histologickými typy. Nejnižší hodnoty jsme zjistili u endometroidního ovariálního karcinomu (tab. 2). Stupeň diferenciace významně ovlivnil pouze hodnoty MRP1, které narůstaly směrem od dobře diferencovaného ke špatně diferencovanému karcinomu ovaria (G1 80 % (CI 0–100), G2 80 % (CI 30–100), G3 100 % (CI 90–100), p < 0,001). Patrný je nárůst MRP1 od časných stadií (I+II) k pokročilému onemocnění (III+IV) (I+II 80 % (CI 60–100), III+IV 100 % (CI 90–100), p = 0,100). Peroperační velikost nádoru ani velikost nádorového rezidua po primární operaci nevykazovaly vztah s žádným z námi sledovaných proteinů rezistence.
Tab. 2. Proteiny rezistence Pgp, MRP1, MRP3 a histologický typ ovariálního karcinomu 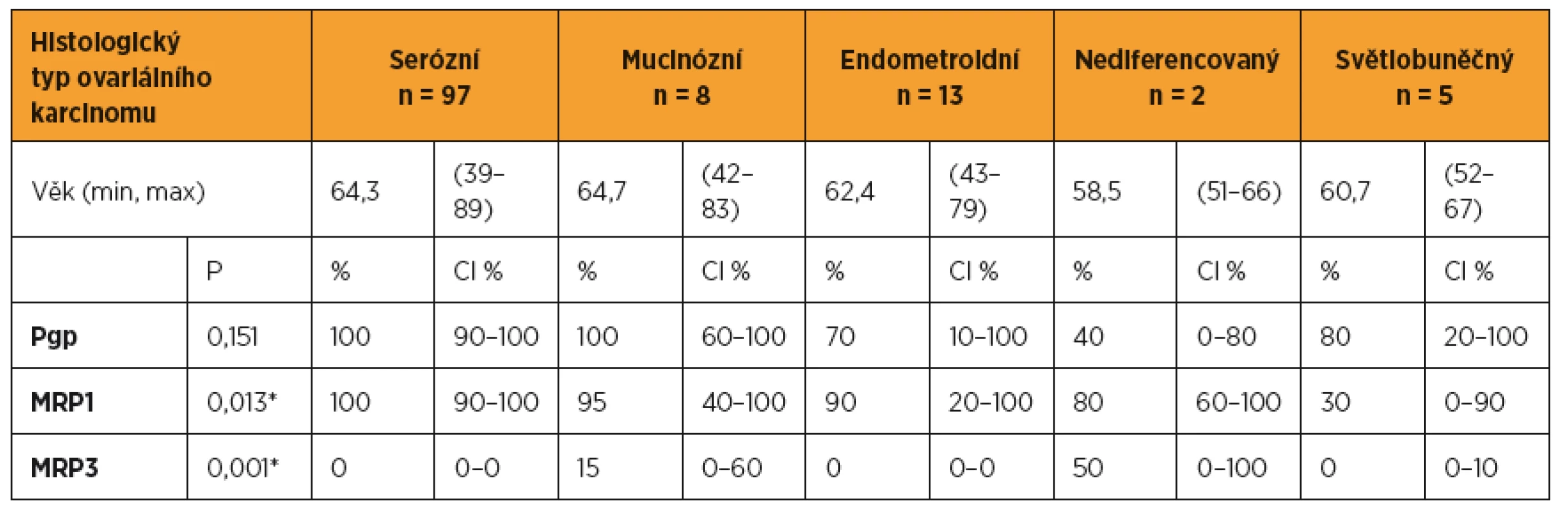
Pro posouzení vztahu proteinů rezistence s klinickým průběhem onemocnění jsme zařadili do studie pouze pacientky, které dostaly šest cyklů primární pooperační chemoterapie ve složení paklitaxel (175 mg/m2) a karboplatina (AUC 5–6). V této části jsme hodnotili pouze pacientky s dostatečným follow up, u kterých jsme mohli přesně dohledat data o klinickém průběhu onemocnění. Porovnávali jsme proteiny rezistence v jednotlivých kategoriích v závislosti na typu léčebné odpovědi (RECIST 1.1). Pacientky s kompletní odpovědí na primární léčbu měly nižší hodnoty MRP1 v porovnání s ostatními pacientkami (částečná odpověď, „stable disease“, progrese onemocnění) (tab. 3). U MRP3 jsme nezaznamenali významnější vztah k léčebné odpovědi u pacientek s ovariálním karcinomem. Pacientky s vyššími hodnotami Pgp, MRP1, MRP3 měly také vyšší riziko recidivy. Pacientky s vysokou expresí Pgp a MRP1(> 85 %) měly významně kratší období do objevení se recidivy v porovnání s pacientkami s nízkou expresí (≤ 85 %) těchto proteinů rezistence (tab. 4). Stejně tak pacientky s nižší expresí MRP1 a Pgp přežívaly déle v porovnání s ženami s vyšší expresí proteinů rezistence (tab. 5).
Tab. 3. Pgp, MRP1, MRP3 a typ léčebné odpovědi (RECIST 1.1) 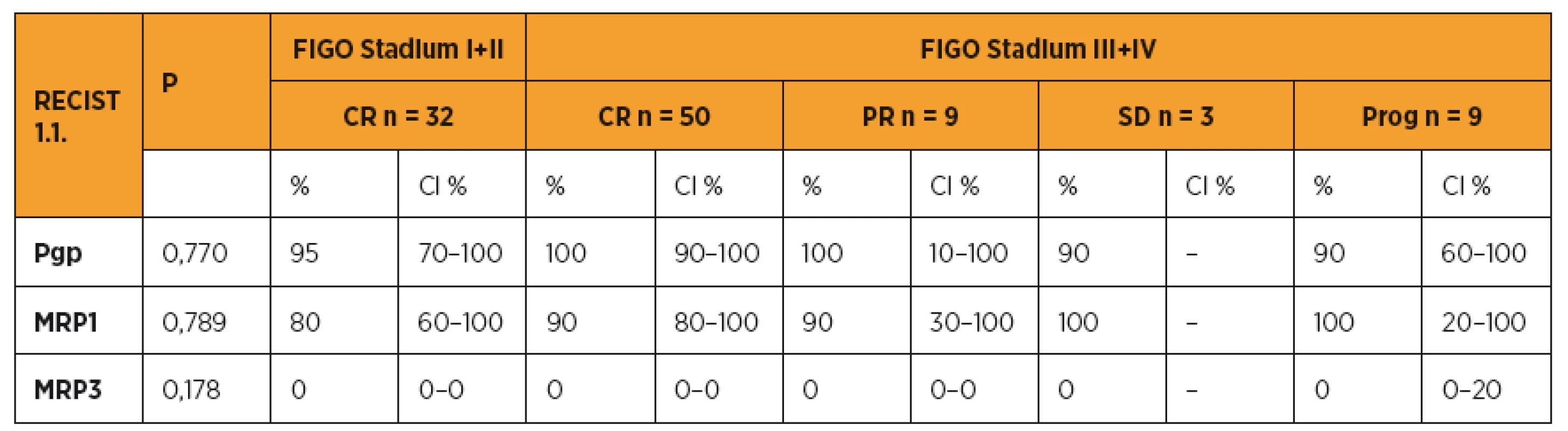
CR – kompletní odpověď, PR – částečná odpověď, SD – „stable disease“, Prog – progrese onemocnění. CI – confidence interval (interval spolehlivosti). Tab. 4. Pgp, MRP1, MRP3 a délka období PFS 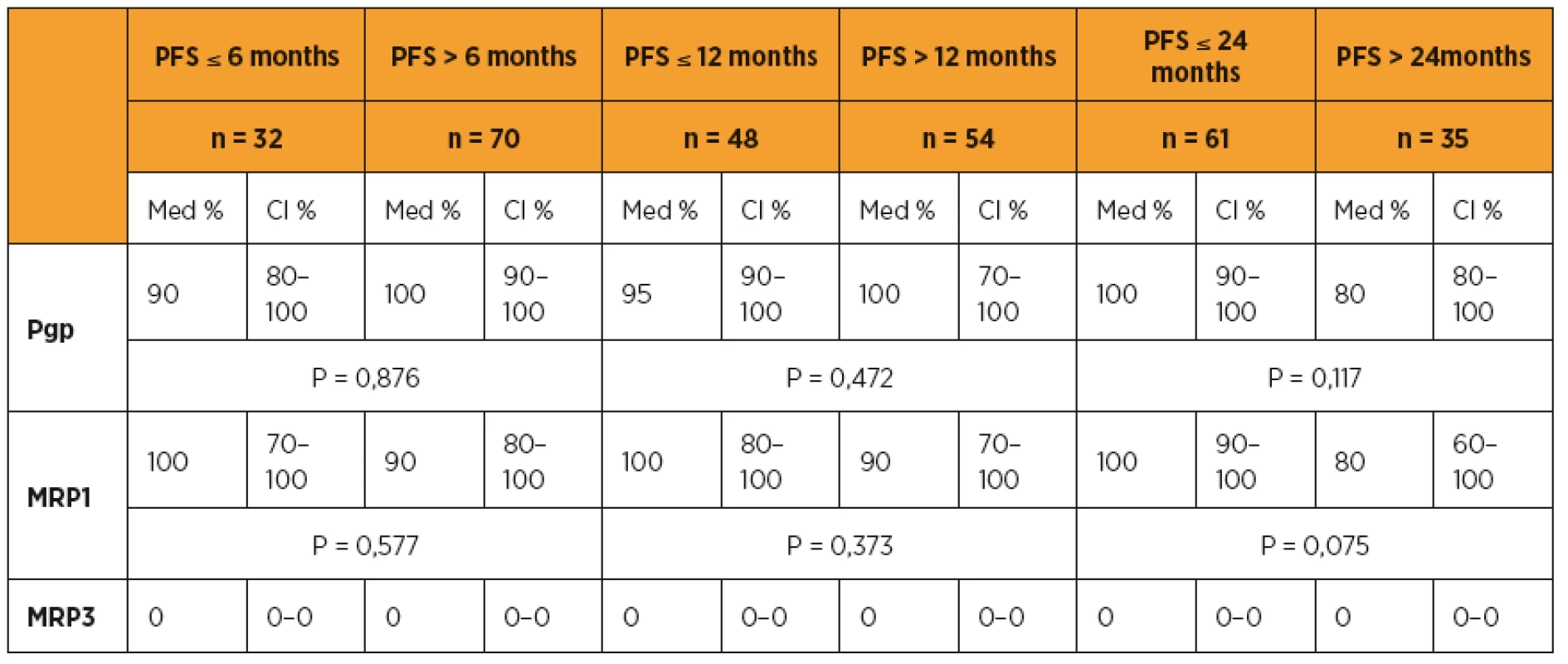
PFS – progression free survival; CI – confidence interval (interval spolehlivosti) Tab. 5. Pgp, MRP1, MRP3 a délka přežití (OS) 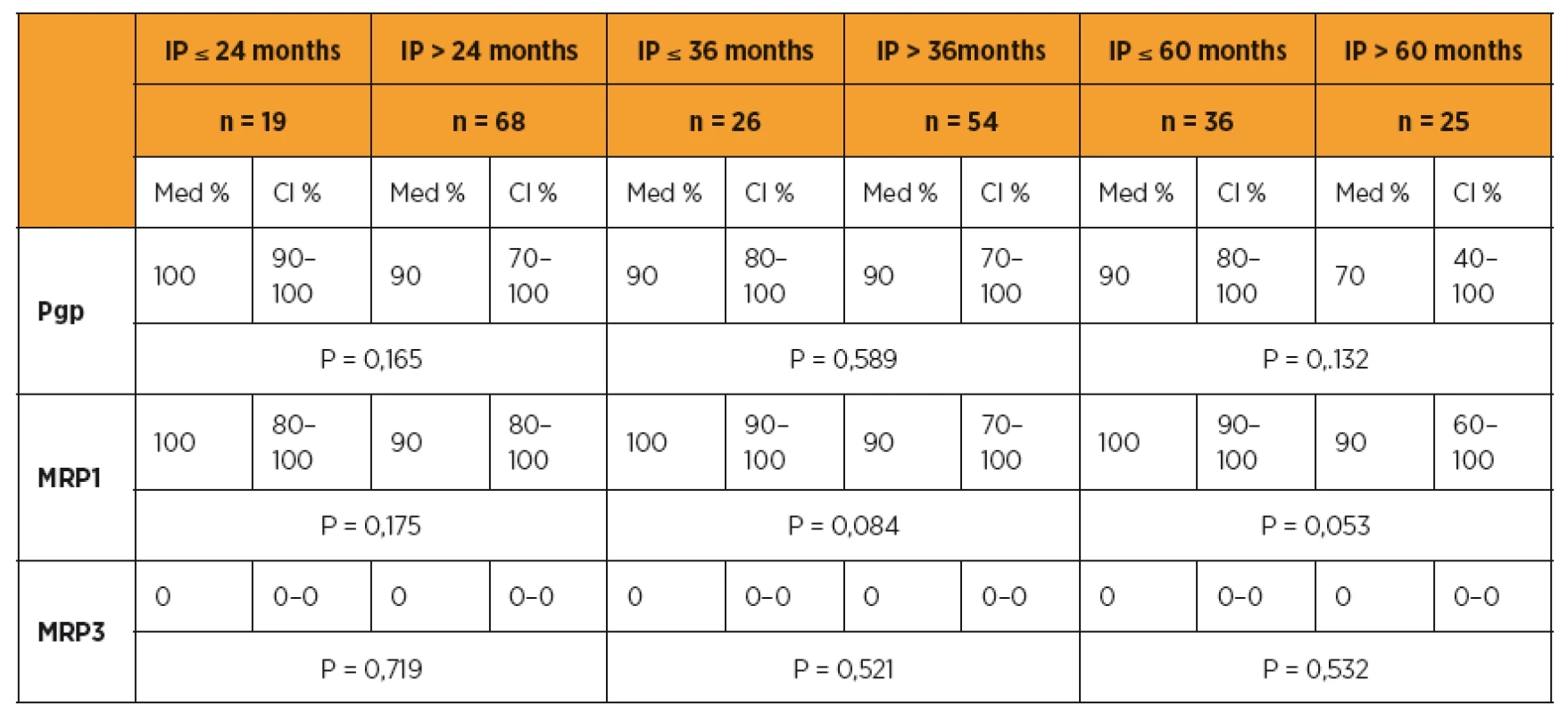
OS – overal survival; CI – confidence interval (interval spolehlivosti) Pro zhodnocení vztahu proteinů rezistence s délkou bezpříznakového období a celkovou dobou přežití pomocí Kaplanovy-Meierovy křivky jsme stanovili dvě kategorie pro Pgp a MRP1 ≤ 85 % versus > 85 % a pro MRP3 kategorii 0 % versus ostatní. Rozdělení jsme stanovili vlastní, na základě posouzených dat, protože v dosud publikovaných studiích věnovaných hodnocení klinického významu proteinů rezistence Pgp a MRP1 nejsou rozdělení jednotná a nalezení odpovídajících kategorií je stále předmětem výzkumu. Hodnotili jsme délku PFS a celkovou dobu přežití (OS) u skupiny pacientek s hodnotu Pgp a MRP1 nad 85 % se skupinou pacientek s hodnotou Pgp a MRP1 menší než 85 %. Medián délky PFS byl statisticky významně kratší u skupiny pacientek s Pgp a MRP1 nad 85 % v porovnání s pacientkami s hodnotami těchto proteinů rezistence pod 85 % (Kaplanův-Meierův test pro PFS, Pgp ≤ 85 % med. PFS 33 měs. (CI 16–64) vs > 85 % med. PFS 12 měs. (CI 10–18), p = 0,025), (MRP1 ≤ 85 % med. PFS 18 měs. (CI 10–43) vs > 85 % med. PFS 12 měs. (CI 9–19), p = 0,273). Medián délky celkového přežití (OS) byl statisticky významně kratší u skupiny pacientek s Pgp a MRP1 nad 85 % v porovnání s pacientkami s hodnotami těchto proteinů rezistence pod 85 % (Kaplanův-Meierův test pro OS, Pgp ≤ 85 % med. OS 96 měs. (CI 48–96) vs > 85 % med. PFS 49 měs. (CI 39–64), p = 0,040), (MRP1 ≤ 85 % med. OS 68 měs. (CI 48–68) vs > 85 % med. OS 49 měs. (CI 32–64), p = 0,026) (graf 1, 2).
Graf 1. Kaplanova-Meierova křivka přežití – P-glykoprotein (Pgp) Pgp ≤ 85 % versus > 85% (p = 0,040) 
Graf 2. Kaplanova-Meierova křivka přežití – Multidrug Related Protein 1 (MRP1) MRP1 ≤ 85 % versus > 85% (p = 0,026) 
V univariantní analýze byly jako statisticky významné faktory mající vliv na délku progression free survival (bezpříznakové období) zjištěny tyto parametry: FIGO stadium (p < 0,001), stupeň diferenciace (p = 0,034), histologický typ nádoru (p < 0,001), přítomnost reziduálního tumoru (p < 0,001), exprese Pgp (p = 0,025) a exprese MRP3 (p = 0,058) (tab. 6). Jako statisticky významné faktory mající vliv na délku přežití byly v univariantní analýze zjištěny tyto parametry: FIGO stadium (p < 0,001), histologický typ nádoru (p < 0,001), přítomnost reziduálního tumoru (p < 0,001), exprese Pgp (p = 0,040), exprese MRP1 (p = 0,026) (tab. 7). V multivariantní analýze jsme jako nezávislé prognostické faktory nalezli pouze: expresi MRP1 (p = 0,051) a FIGO stadium onemocnění (p = 0,016). Údaje získané multivariantní analýzou shrnuje tabulka 8.
Tab. 6. Univariantní analýza progression-free survival (log-rank test) 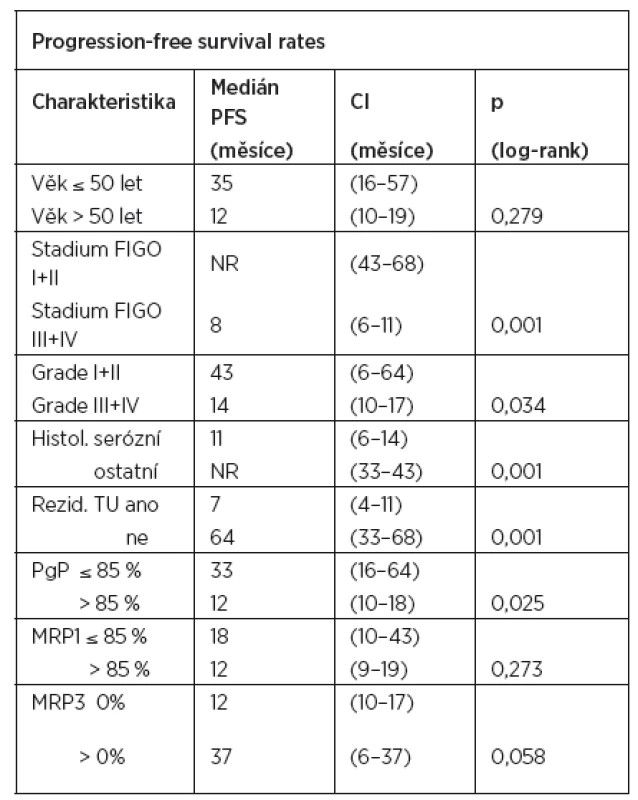
Tab. 7. Univariantní analýza přežití (log-rank test) 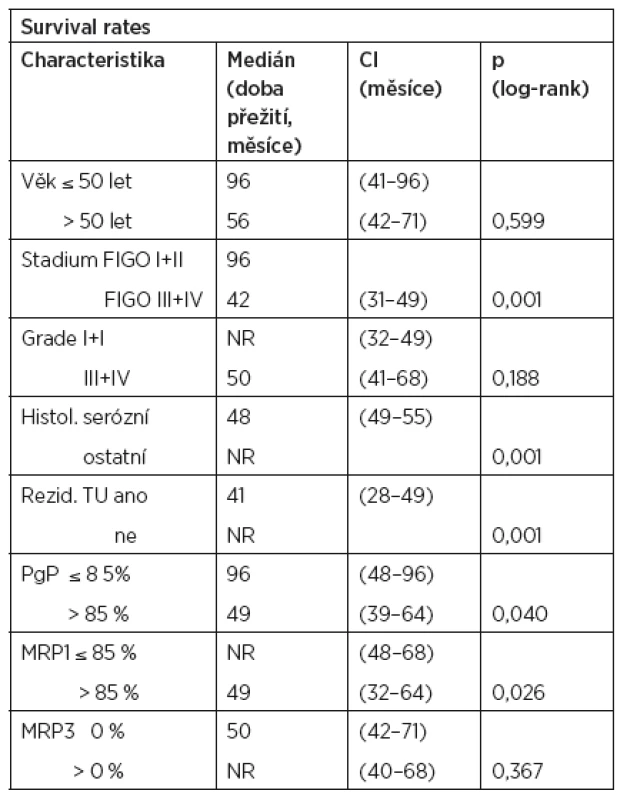
Tab. 8. Výsledky multivariantní analýzy 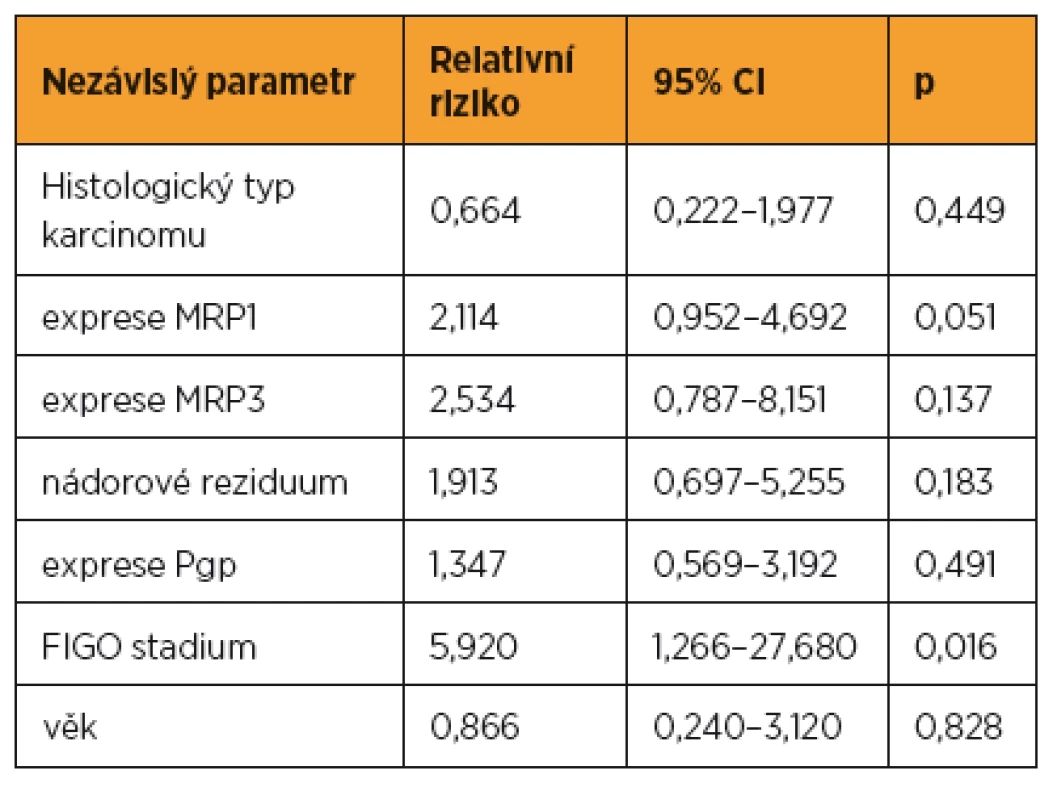
DISKUSE
Chemorezistence je hlavním klinickým problémem současné systémové léčby pacientek s karcinomem ovaria. Proteiny rezistence Pgp a MRP se podílejí na vzniku chemorezistence. Z dosud publikovaných prací věnovaných proteinům rezistence vyplývají nejednotná data. Problematika vzniku primární chemorezistence ovariálního karcinomu není stále jednoznačně objasněna. Z toho důvodu jsou velmi přínosné práce studující podstatu primární chemorezistence na konkrétních vzorcích nádorové tkáně od jednotlivých pacientek, a ne na vypěstovaných uniformních buněčných kulturách. Protože jedině tímto způsobem je možné posunout se dále k vysvětlení vzniku a průběhu chemorezistence.
Materna et al. prokázali prognostický význam Pgp a MRP2 u pacientek s karcinomem ovaria [15]. Pro posouzení významu míry exprese Pgp pro predikci úspěšnosti chemoterapie je rozhodujícím faktorem výběr cytostatika. V případě použití cytostatik, která jsou substráty Pgp, např. taxany, existuje předpoklad, že terapie může vést ke vzniku mnohočetné lékové rezistence. Díky případně zvýšené expresi Pgp mohou být taková léčiva za účasti transportní funkce Pgp předčasně vylučována z nádorových buněk, což může způsobit pokles účinku léčby [19]. Data o významu Pgp u ovariálního karcinomu jsou zatím nejvíce prozkoumána, ale jsou stále nejednotná. Při porovnání hodnot MDR v nádorové tkáni a párových vzorcích okolní přiléhající nenádorové tkáně bez morfologicky detekovaných nádorových buněk u pacientek s karcinomem prsu byla nalezena indukce exprese MDR po podání chemoterapie i v nenádorové tkáni [19]. Starší studie neprokázaly prognostický význam Pgp pro počáteční odpověď na chemoterapii [2, 11, 12]. Novější práce v souladu s našimi výsledky prokázaly negativní korelaci exprese Pgp s léčebnou odpovědí u pacientek s karcinomem ovaria [9, 15, 20].
Exprese MRP byla prokázána u více než dvou třetin epiteliálních ovariálních karcinomů [1, 12]. Izquierdo et al. nalezli expresi MRP u 68 % epiteliálních ovariálních karcinomů stadia III/IV a exprese byla limitována hlavně v cytoplazmatické membráně [12]. Goff et al. zjistili expresi MRP u 66 % epiteliálních ovariálních karcinomů [7], nezaznamenali však asociaci s chemorezistencí. Tyto výsledky potvrdily i další studie, které nenalezly významný vztah mezi expresí MRP a chemorezistencí ovariálního karcinomu [1, 2, 12]. Yakirevich et al. nalezli statisticky významnou korelaci mezi silnou expresí Pgp a kratším přežitím u pacientek s karcinomem ovaria. Delší interval přežití měly pacientky Pgp negativní v porovnání s ženami s Pgp pozitivními tumorem. MRP1 podle jejich výsledků neměl vliv na délku přežití [20].
V této studii jsme stanovili proteiny rezistence Pgp, MRP1 a MRP3. Opakovaně jsme zjistili velmi významné rozdíly hodnot Pgp, MRP1 a MRP3 u jednotlivých histologických typů ovariálního karcinomu. I přes malý počet pacientek s mucinózním ovariálním karcinomem jsme zaznamenali opět nejvyšší hodnoty Pgp, MRP1 a MRP3 v porovnání s ostatními histologickými typy. Přestože v našem souboru šlo o malou skupinu pacientek s mucinózním ovariálním karcinomem, potvrzuje se tím klinicky špatná odpověď pacientek s tímto histologickým typem ovariálního karcinomu na primární chemoterapii ve složení paklitaxel + karboplatina. Na druhé straně nejnižší hodnoty proteinů rezistence jsme zaznamenali u endometroidního ovariálního karcinomu. I zde můžeme najít korelaci s klinickým průběhem, protože endometroidní ovariální karcinom většinou dobře odpovídá na standardní chemoterapii první linie. Různé zastoupení proteinů rezistence u jednotlivých histologických typů ovariálního karcinomu potvrzuje různorodost chování jednotlivých histologických typů ovariálního karcinomu včetně odlišné odpovědi na jeden typ primární chemoterapie. Stále se potvrzuje, že ovariální karcinom je heterogenní onemocnění zahrnující různé typy nádorů, které mají velice odlišné klinicko-patologické vlastnosti a chování [13].
Histopatologické vyšetření je k dispozici u všech pacientek po chirurgické léčbě bez dalších finančních nákladů a bez zátěže pacientky. Přitom v současné době se v rozhodovacím algoritmu o následné systémové léčbě nezohledňuje ani histologický typ nádoru. Všechny pacientky s pokročilým ovariálním karcinomem dostávají v následné léčbě paklitaxel a platinový derivát. A to i přesto, že pacientky primárně chemorezistentní na daná cytostatika z této léčby neprofitují a jsou tímto léčebným postupem pravděpodobně poškozovány. Primárně chemorezistentní pacientky by chemoterapii v daném složení neměly vůbec dostávat. Jiný typ primární léčby by pro ně mohl znamenat lepší léčebnou odpověď i méně nežádoucích účinků.
Stanovení chemorezistence ze vzorků ovariálních karcinomů odebraných při operaci pomocí proteinů rezistence nebo prostřednictvím MTT testu (Sedláková, I., Česká gynekologie, 2011) umožňuje výběr pacientek vhodných pro určitý typ primární následné systémové léčby. Chemoterapie pravděpodobně zůstane ještě určitou dobu základem následné systémové léčby pro většinu pacientek s karcinomem ovaria a právě pooperační vyšetření chemorezistence by mohlo přispět k individualizaci léčby. Je třeba vymezit podmínky, kdy bude primární chemoterapie, popř. její kombinace s další systémovou léčbou, nejvhodnější pro danou pacientku s minimálními vedlejšími účinky. Pro primárně chemorezistentní pacientky by měl být ihned po precizním chirurgickém výkonu volen jiný typ následné léčby, např. imunoterapie, biologická léčba, nové metody radioterapie, nebo alespoň jiná kombinace cytostatik. Tak aby následná systémová léčba byla co nejúčinnější pro všechny ženy s karcinomem ovaria.
Z prognostického hlediska nás zajímal zejména vliv exprese proteinů rezistence na délku bezpříznakového období (PFS) a dobu přežití (overall survival, interval přežití, IP). Z našich výsledků je patrné ovlivnění délky PFS, a to zejména při porovnání delšího časového období PFS více nebo méně než 24 měsíců. Zajímavý je zejména vliv exprese proteinů rezistence na délku přežití pacientek s karcinomem ovaria, kde se jednotlivé hodnoty významně liší a statistická významnost exprese proteinů rezistence, zejména MRP1, narůstá směrem ke zvyšující se délce celkové doby přežití. Nižší hodnoty MRP1 u pacientek s karcinomem ovaria, které přežívají více než pět let v porovnání s vyššími hodnotami MRP1 u pacientek, jejichž interval přežití je kratší než 60 měsíců, jsou statisticky významné (p = 0,053). Z našich výsledků vyplývá prognostický význam proteinů rezistence, zejména MRP1 a Pgp, pro pacientky s karcinomem ovaria. V případě hodnot MRP3 se sice v našem hodnocení prostřední hodnoty nelišily v závislosti na jednotlivých sledovaných faktorech, ale jeho průměrné hodnoty vykazovaly významné rozdíly.
Prokázali jsme prognostický význam stanovení Pgp a MRP1 u pacientek s karcinomem ovaria. Z našich dat se ukazuje jako nejperspektivnější prognostický faktor u pacientek s karcinomem ovaria MRP1. Chemoterapie zůstává stále základem systémové léčby ovariálního karcinomu. Nové typy následné primární léčby (biologická léčba, imunoterapie) jsou podávány zatím „pouze“ v kombinaci s primární chemoterapií. Zohlednění histopatologických vlastností a stanovení chemorezistence před nasazením pooperační systémové léčby by mohlo přispět k predikci pacientek nevhodných k současné standardní primární chemoterapii a následné individualizaci systémové léčby u pacientek s karcinomem ovaria.
Tento projekt vznikl za podpory MZ ČR NT 14107-3/2013.
MUDr. Iva Sedláková, Ph.D.
Porodnická a gynekologická klinika
Sokolská 581
500 05 Hradec Králové
e-mail: iva.sedlakova@ fnhk.cz
Zdroje
1. Arao, S., Suwa, H., Mandai, M., et al. Expression of multidrug resistance gene and localization of P-glycoprotein in human primary ovarian cancer. Cancer Res, 1995, 54, p. 1355–1359.
2. Arts, HJ., Katsaros, D., de Vries, FG., et al. Drug resistance-associated markers P-glycoprotein, multidrug resistance-associated protein 1, multidrug resistance-associated protein 2, and lung resistance protein as prognostic factors in ovarian carcinoma. Clin Cancer Res, 1999, 5, p. 2798–2805.
3. Borst, P., Evers, P., Kool, M., Wijnholds, J. A family of drug transporters: the multidrug resistance-associated proteins. J Natl Cancer Inst, 2000, 92, p. 1295–1302.
4. Cibula, D., Petruželka, L., a kol. Onkogynekologieedition. Praha, Grada Publishing, 2009.
5. Fruehauf, PJ., Alberts, DS. In vitro drug resistance versus chemosensitivity: two sides of different coins. J Clin Oncol, 2005, 23, p. 3641–3643.
6. Glavinas, H., Krajcsi, P., Cserepes, J., et al. The role of ABC transporters in drug resistance, metabolism and toxicity. Curr Drug Deliv, 2004, 1, p. 27.
7. Goff, AB., Paley, JP., Greer, EB., Grown, MA. Evaluation of chemoresistance markers in women with epithelial ovarian carcinoma. Gynecol Oncol, 2001, 81, p. 18–24.
8. Gottesman, MM., Fojo, T., Bates, SE. Multidrug resistance in cancer: role of ATP-dependent transporters. NatRevCancer, 2002, 2, p. 48–58.
9. Holzmayer, TA., Hilsenbeck, S., Von Hoff DD., Roninson, IB. Clinical correlates of MDR1 (P-glycoprotein) gene expression in ovarian and small-cell lung carcinomas. J Natl Cancer Inst, 1992, 84, p. 1486–1491.
10. Charpin, C., Vielh, P., Duffaud, F., et al. Quantitative immunocytochemical assays of P-glycoprotein in breast carcinomas: correlation to messenger RNA expression and to immunohistochemical prognostic indicators. J Natl Cancer Inst, 1994, 86, p. 1539–1545.
11. Ikeda, K., Sakai, K., Yamamoti, R., et al. Multivariate analysis for prognostic significance of histologic sybtype, GST-pi, MDR-1, and p-53 in stages II-IV ovarian cancer. Int J Gynecol Cancer, 2003, 13, p. 776–784.
12. Izquierdo, MA., van der Zee, AG., Vermorken, JB., et al. Drug resistance-associated marker LRP for prediction of response to chemotherapy and prognosis in advanced ovarian carcinoma. J Natl Cancer Inst, 1995, 87, p. 1230–1237.
13. Kurman, JR., Shih, M. The origin and pathogenesis of epithelial ovarian cancer – a proposed unifying theory. Am J Surg Pathol, 2010, 34, p. 1–18.
14. Kuwano, M., Uchiumi, T., Hayakawa, H, et al. The basic and clinical implications of ABC transporters, Y-box-binding protein-1 and angiogenesis-related factors in human malignancies. Cancer Sci, 2003, 94, p. 9–14.
15. Materna, V., Pleger, J., Hoffmann, U., Lage, H. RNA-expression of MDR1/P-glycoprotein, DNA-topoisomerase I, and MRP2 in ovarian carcinoma patients: correlation with chemotherapeutic response. Gynecol Oncol, 2004, 94, p. 152–160.
16. Nosková, V., Hajdúch, M., Mihál, V., Cwiertka, K. Mechanismy mnohočetné lékové rezistence a jejich význam pro klinickou praxi. Klinická onkologie, 2000, 13, s. 4–9.
17. Scheffer, GL., Wijngaard, PL., Flens, MJ., et al. The drug resistance related protein LRP is the human major vault protein. Nat Med, 1995, 1, p. 578–582.
18. Schinkel, AH. P-Glycoprotein, a gatekeeper in the blood-brain barier. Adv Drug Deliv Rev, 1999, 36, s. 179–194.
19. Václavíková, R., Hubáčková, M., Kubala, E., et al. Exprese genu mnohočetné lékové rezistence 1 (MDR1) a její význam v rozvoji a terapii karcinomu prsu. Klinická onkologie, 2007, 3, s. 253–259.
20. Yakirevich, E., Sabo, E., Naroditsky, I., et al. Multidrug resistance-related phenotype and apoptosis-related protein expression in ovarian serous carcinomas. Gynecol Oncol, 2006, 100, p. 152–159.
Štítky
Dětská gynekologie Gynekologie a porodnictví Reprodukční medicína
Článek vyšel v časopiseČeská gynekologie
Nejčtenější tento týden
2015 Číslo 6- Postabortivní syndrom – symptomy, dopady a možnosti léčby
- Inosin pranobex v léčbě chřipky a dalších respiračních infekcí virové etiologie
- Fexofenadin – nesedativní a imunomodulační antihistaminikum v léčbě alergických projevů
- Trombóza portální žíly jako komplikace infekce COVID-19 – kazuistika
- Diagnostika osteoporózy v kontextu současných doporučení
-
Všechny články tohoto čísla
- Editorial
- Nonavalentní HPV vakcína – nová generace očkování proti HPV
- Spontánní antepartální RhD aloimunizace
- Prognostický význam Pgp, MRP1 a MRP3 u pacientek s karcinomem ovaria
- Cytologicko-energetický princip vyšetřování plodové vody po předčasném předtermínovém odtoku – dosavadní zkušenosti a perspektivy
- Trombofília v tehotenstve
- Spokojenost žen s perinatální péčí v Kraji Vysočina za období říjen 2013 až září 2014
- Pilotní studie pro využití samoodběrové soupravy a molekulární diagnostiky HPV infekce pro skrínink karcinomu děložního čípku
- Hypertyreóza v graviditě, méně častá porucha štítné žlázy komplikující těhotenství – kazuistika
- Těžký ovariální hyperstimulační syndrom – kazuistika
- Farmakologické ukončení gravidity mifepristonem a misoprostolem – zhodnocení úspěšnosti, komplikací a spokojenosti pacientek
- Závislost na tabáku – krátká intervence
-
ZÁSADY DISPENZÁRNÍ PÉČE VE FYZIOLOGICKÉM TĚHOTENSTVÍ
Doporučený postup -
GESTAČNÍ DIABETES MELLITUS
Doporučený postup - Rejstříky
- Česká gynekologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Farmakologické ukončení gravidity mifepristonem a misoprostolem – zhodnocení úspěšnosti, komplikací a spokojenosti pacientek
- Těžký ovariální hyperstimulační syndrom – kazuistika
- Trombofília v tehotenstve
- Hypertyreóza v graviditě, méně častá porucha štítné žlázy komplikující těhotenství – kazuistika
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Revma Focus: Spondyloartritidy
nový kurz
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Autoři: prof. MUDr. Pavel Horák, CSc., doc. MUDr. Ludmila Brunerová, Ph.D., doc. MUDr. Václav Vyskočil, Ph.D., prim. MUDr. Richard Pikner, Ph.D., MUDr. Olga Růžičková, MUDr. Jan Rosa, prof. MUDr. Vladimír Palička, CSc., Dr.h.c.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



