-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
DIAGNOSTIKA A LÉČBA MNOHOČETNÉHO MYELOMU
Vyšlo v časopise: Transfuze Hematol. dnes,24, 2018, No. Supplementum1, p. 7-23.
Kategorie: Souhrn doporučení
DIAGNOSTIKA A LÉČBA MNOHOČETNÉHO MYELOMU
B. ZÁPIS DIAGNÓZY
Správný a úplný zápis vstupní diagnózy mnohočetný myelom
Správným diagnostickým výstupem je dnes např. následný vzorový zápis:
Smoldering MM IgA-kappa; D-S IA, R-ISS 1 (event. ISS 1) datum dg.
- léčba není indikovaná
Mnohočetný myelom IgG-lambda (poškození ledvin, mnohočetná osteolytická ložiska);
D-S IIIB, ISS 3, R-ISS 2 (poz. del 13, translokace neg., del 17 neg., amplifikace 1q21 neg.); datum dg.
- indikováno zahájení léčby.
MGUS IgG-kappa, nízké riziko transformace
- doporučeny pravidelné kontroly á 12–18 měsíců od druhého roku sledování
MGUS IgG-kappa, nízké až střední riziko transformace
- doporučeny pravidelné kontroly á 6–12 měsíců od druhého roku sledování
MGUS IgG-kappa, střední až vysoké riziko transformace
- doporučeny pravidelné kontroly á 4–6 měsíců od druhého roku sledování
MGUS IgG-kappa, vysoké riziko transformace
- doporučeny pravidelné kontroly á 2–4 měsíce od druhého roku sledování
A. DIAGNOSTIKA
Tab. 1. Iniciální vyšetření u pacienta s mnohočetným myelomem 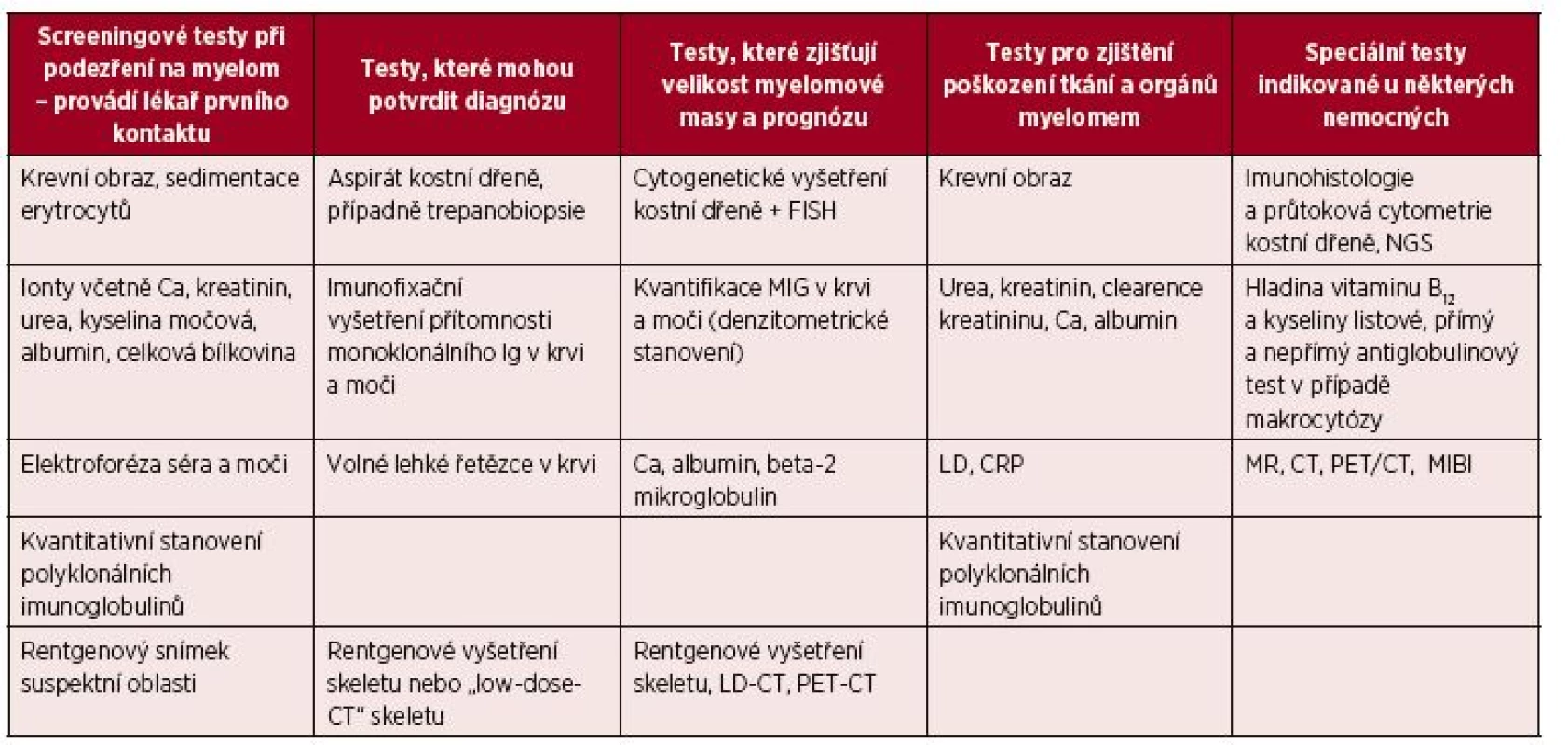
Upraveno a doplněno podle [Kumar, 2016; Munshi, 2017; Smith, 2005; Terpos, 2015] Vysvětlivky: FISH – fluorescenční in situ hybridizace; NGS – sekvenování další generace; Ig – imunoglobulin; MIG – monoklonální imunoglobulin; LD – laktátdehydrogenáza; CRP – C reaktivní protein; MR – magnetická rezonance; CT – počítačová tomografie; PET/CT – pozitronová emisní tomografie v kombinaci s počítačovou tomografii; MIBI – radionuklidové vyšetření pomocí technecia sestamibi. Tab. 2. Srovnání kritérií MGUS, asymptomatického a symptomatického mnohočetného myelomu 
Upraveno pro diagnostická doporučení 2018 podle [Doporučení International Myeloma Working Group] Tab. 3. Kritéria solitárního kostního plazmocytomu* 
[International Myeloma Working Group 2003] *Pro diagnózu solitárního kostního plazmocytomu musí být splněny všechny uvedené podmínky. Tab. 4. Kritéria solitárního mimokostního (extramedulárního) plazmocytomu* 
[International Myeloma Working Group, 2003] *Pro diagnózu solitárního mimokostního plazmocytomu musí být splněny všechny uvedené podmínky. Tab. 5. Kritéria plazmocelulární leukemie 
[International Myeloma Working Group 2003] Tab. 6. Revidovaná diagnostická kritéria mnohočetného myelomu 
[Rajkumar, 2014] 1Klonalita by měla být stanovena pomocí průkazu κ/λ restrikce lehkých řetězců při vyšetření pomocí průtokové cytometrie, imunohistochemie nebo imunofluorescence, počet plazmatických buněk by měl být přednostně stanoven z biopsie kostní dřeně; v případě rozdílu v procentuálním zastoupení plazmatických buněk zjištěném v aspirátu a bioptickém vzorku by měla být použita vyšší hodnota. 2Pokud je počet klonálních plazmatických buněk v kostní dřeni < 10 %, pak je nutná přítomnost více než jednoho ložiska k odlišení od solitárního plazmocytomu s minimálním postižením kostní dřeně. 3Při použití stanovení pomocí metody Freelite© (The Binding Site, Birmingham, UK). 4Velikost ložiska musí být minimálně 5 mm. Tab. 7. Revidovaná diagnostická kritéria „smoldering“ (doutnajícího, asymptomatického) mnohočetného myelomu Pro diagnózu je nutné splnění obou následujících kritérií: 
[Rajkumar, 2014] Tab. 8. Stanovení klinického stadia mnohočetného myelomu 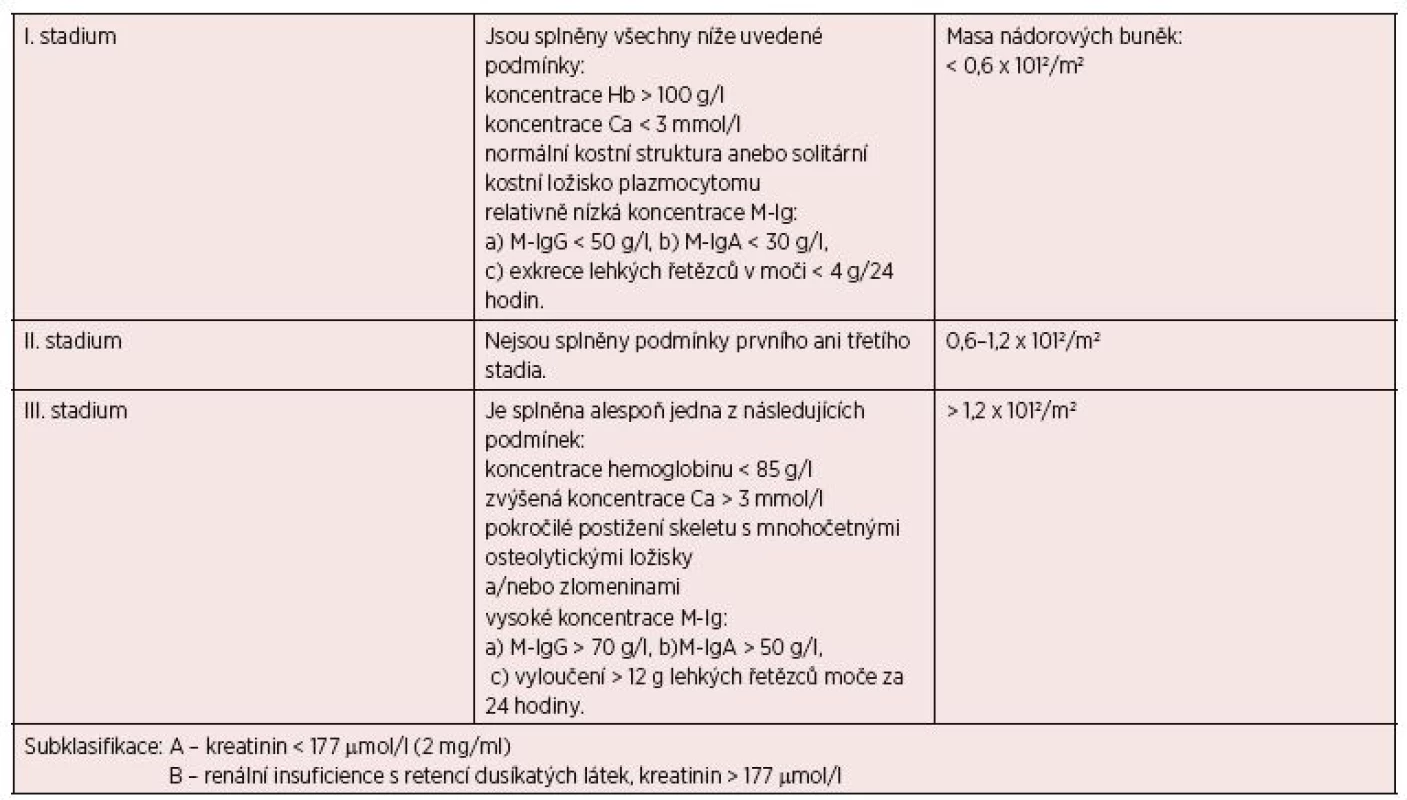
Podle [Durieho a Salmona, 1975] Tab. 9. Mezinárodní prognostický index (ISS) pro mnohočetný myelom 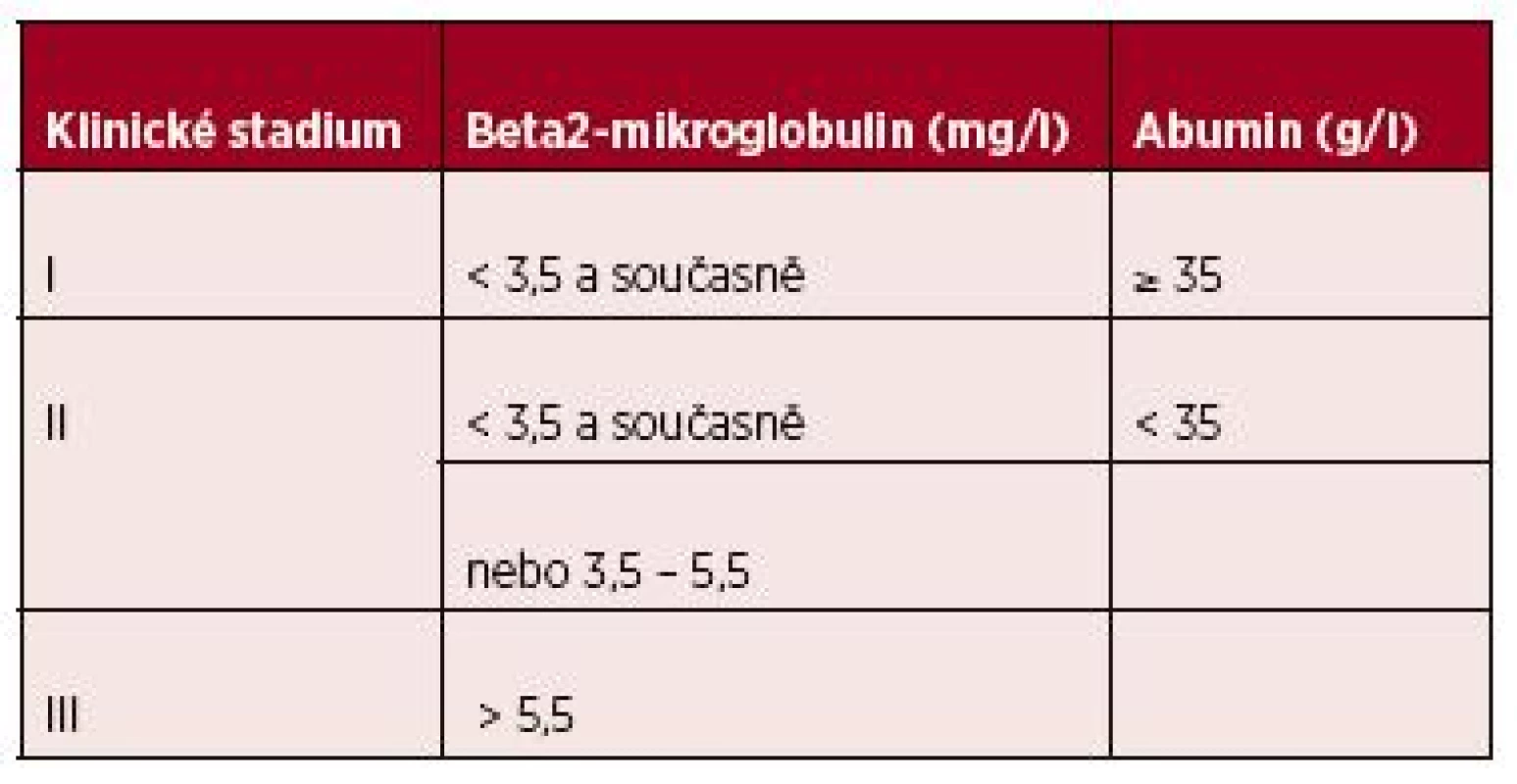
[Greipp, 2005] Tab. 10. Revidovaný mezinárodní prognostický index (R-ISS) mnohočetného myelomu 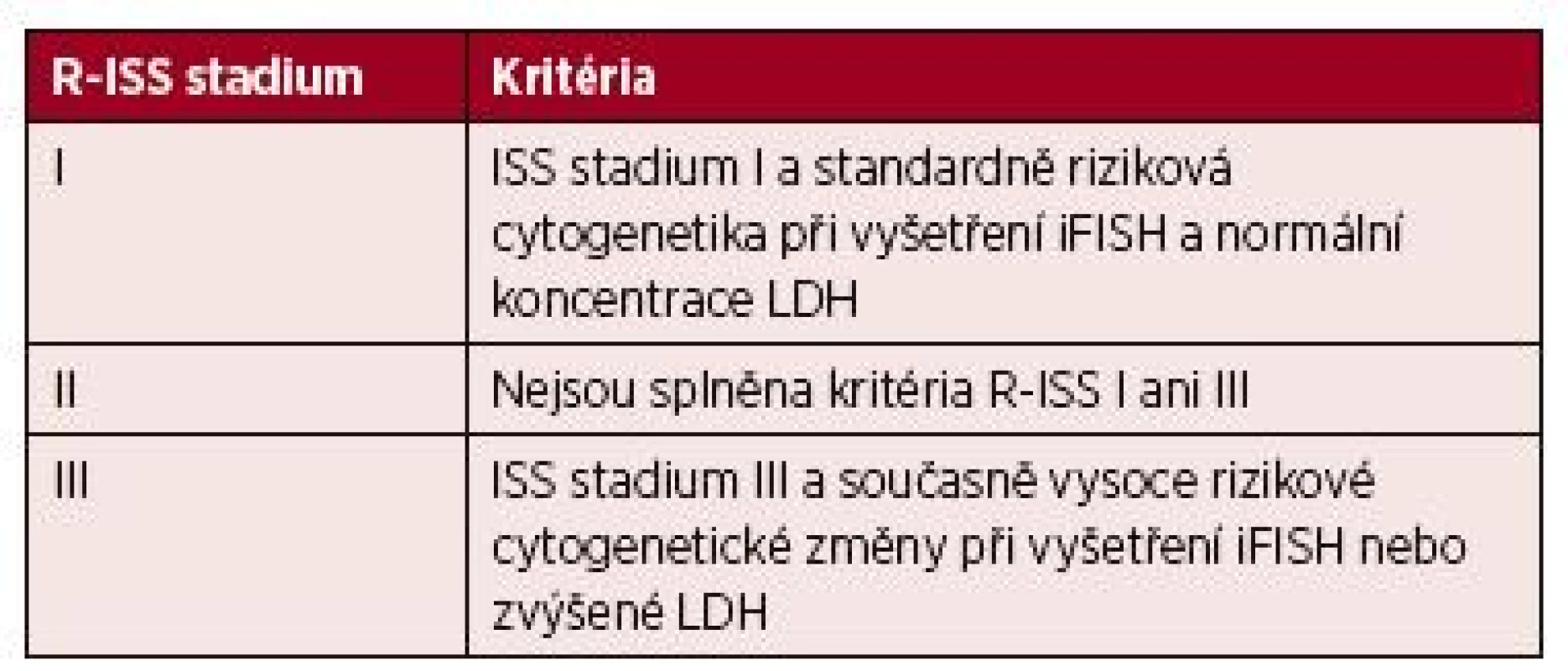
[Palumbo, 2015] Vysoce rizikové cytogenetické změny – přítomnost del(17p) a/nebo translokace t(4;14) a/ nebo translokace t(14;16) při iFISH; standardní riziko = nebyla prokázána žádná z uvedených změn. Tab. 11. Klasifikace monoklonálních gamapatií neurčeného významu 
[Kyle, 2010] Poznámka: Ve skupině nízkého rizika je pouze 5% riziko přechodu do obrazu maligní monoklonální gamapatie do 20 let od stanovení diagnózy MGUS, ve skupině vysokého rizika je pak výše tohoto rizika již 58 %! Vysvětlivka: FLC – volné lehké řetězce. C. KRITÉRIA PRO HODNOCENÍ LÉČEBNÉ ÚČINNOSTI A DLOUHODOBÉ ÚSPĚŠNOSTI LÉČBY
Tab. 12. Standardní definice dosažených léčebných odpovědí u MM podle IMWG 2006 a 2011 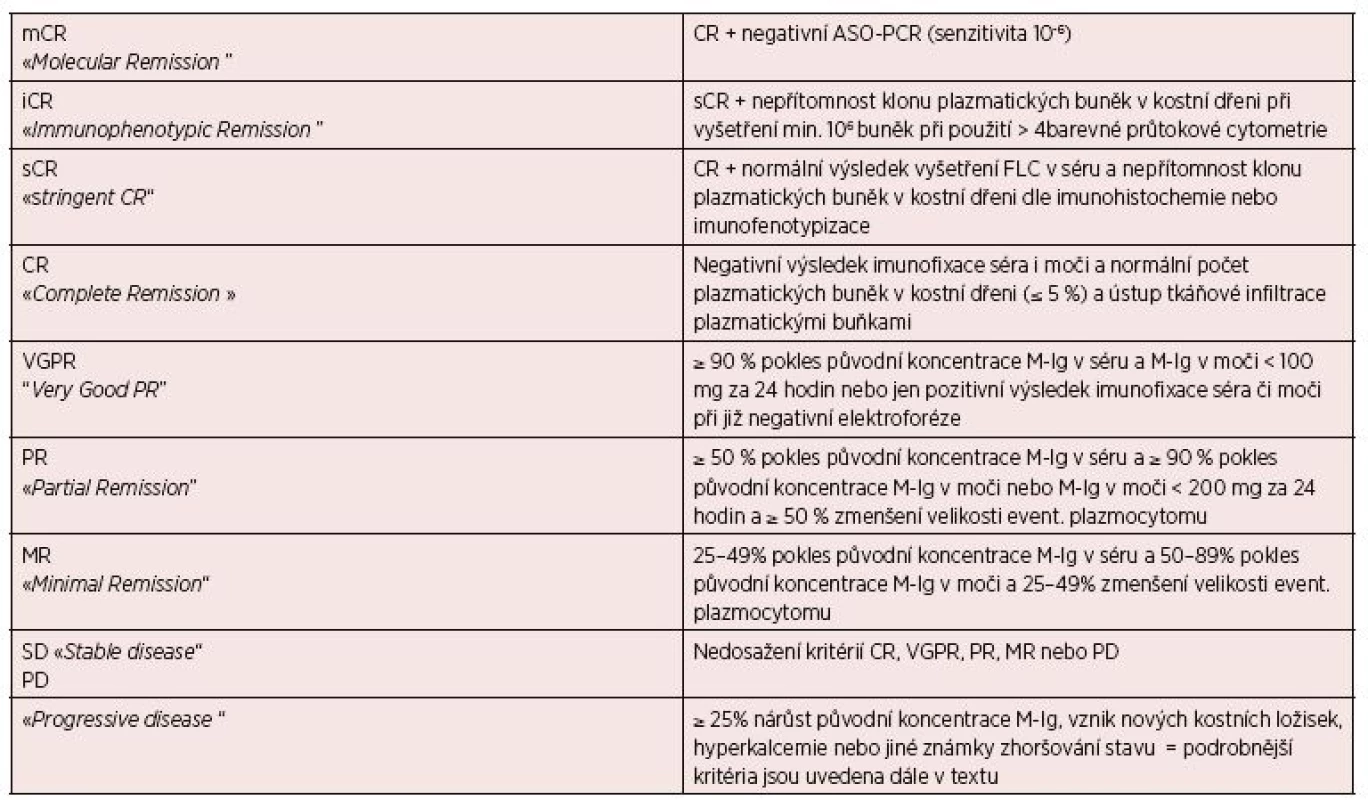
Vysvětlivky: ASO-PCR – polymerázová řetězová reakce; mCR – molekulární kompletní remise; iCR – kompletní remise potvrzena průtokovou cytometrií; sCR – přísná kompletní remise; FLC – volné lehké řetězce; CR – kompletní remise; VGPR – velmi dobrá parciální remise; PR – parciální remise; MR – minimální remise; SD – stabilní nemoc; PD – progresivní nemoc. Tab. 13. Definice minimální reziduální choroby podle IMWG 2016 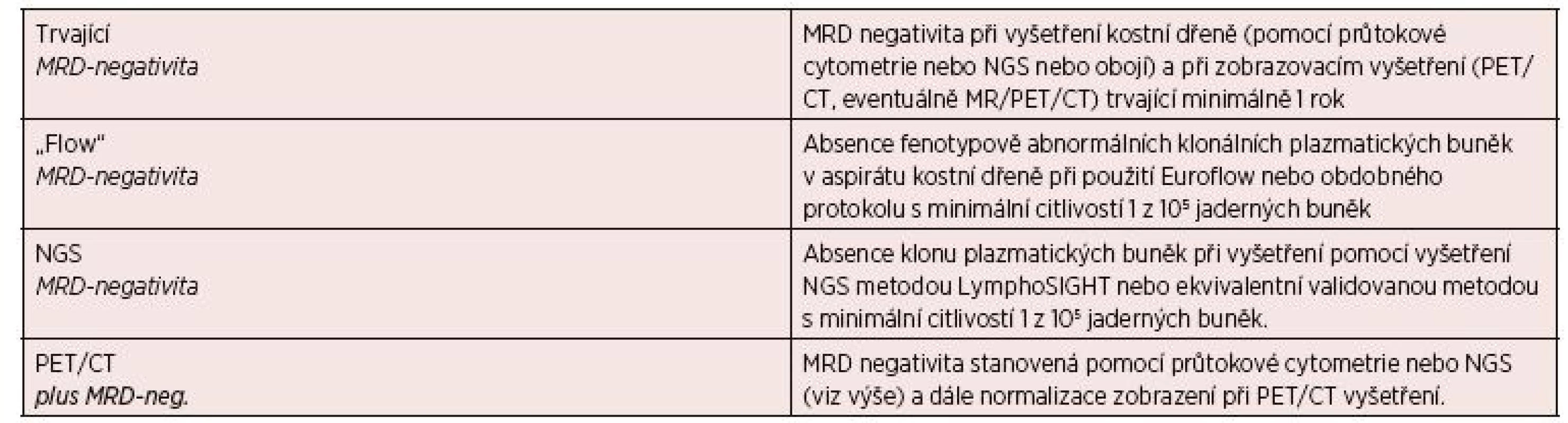
Vysvětlivky: MRD – minimální reziduální onemocnění; PET/CT – pozitronová emisní tomografie s kombinaci s počítačovou tomografií; MR – magnetická rezonance; flow MRD – MRD stanovena pomocí průtokové cytometrie; NGS – sekvenování další generace. Tab. 14. Současné definice léčebných intervalů doporučených pro hodnocení dosažené léčebné odpovědi podle IMWG 2006 
Vysvětlivky: PFS – přežití bez progrese; MM – mnohočetný myelom; EFS – přežití bez události; TTP – čas do progrese; DFS – přežití bez známek onemocnění; DOR – trvání odpovědi; OS – celkové přežití. D. HODNOCENÍ NOVÉ AKTIVITY ONEMOCNĚNÍ
Relaps onemocnění znamená novou aktivitu onemocnění po léčbě, kterou bylo dosaženo nejméně kompletní remise onemocnění (nutná negativní imunofixace).
Progrese onemocnění znamená novou aktivitu onemocnění po léčbě v případě, že maximální léčebná odpověď byla horší než kompletní remise, ale lepší než minimální léčebná odpověď (pokles o 25 % od původních hodnot). Jako progresi označujeme i stav vyžadující léčbu dříve neléčené tzv. „smoldering“ (dříve asymptomatické) formy onemocnění.
Pojem laboratorní relaps/progrese používáme pro případy, kdy nejsou splněna kritéria klinického relapsu, kterými jsou projevy CRAB symptomatologie nebo vzestup koncentrace původního monoklonálního imunoglobulinu o 25 %, minimálně však o 5 g/l, a to se současnou CRAB symptomatologií nebo bez ní.
Refrakterní myelom je definován jako onemocnění nereagující na léčbu nebo onemocnění progredující během 60 dnů od poslední léčby. Jako nereagující onemocnění přitom můžeme označit i stav, kdy pacient nedosáhne ani minimální léčebné odpovědi nebo stav, kdy dojde k progresi onemocnění v průběhu léčby. Refrakterní myelom má dvě kategorie: Relabující a refrakterní myelom (léčba relapsu či progrese) nebo primárně refrakterní v případě primoléčby [Rajkumar 2011].
Možnosti stanovení relapsu/progrese u nemocných s mnohočetným myelomem:
- vzestup koncentrace M-Ig v séru o 25 % vstupní hodnoty v případě neléčeného onemocnění, respektive nejnižší dosažené a potvrzené hodnoty po léčbě, minimálně musí však jít o nárůst koncentrace M-Ig o 5 g/l
- vzestup koncentrace lehkých řetězců u B-J typu MM ve sběru moči/24hod o 25 % vstupní hodnoty v případě neléčeného onemocnění, respektive nejnižší dosažené hodnoty po léčbě, minimálně však musí jít o nárůst koncentrace o více než 200 mg/24hod
- u oligosekreční, případně nesekreční formy MM, dnes můžeme při hodnocení využít stanovení koncentrace volných lehkých řetězců v séru, kdy je pro stanovení progrese nutný absolutní nárůst o více než 100 mg/l
- v případech, kdy není možné využít ani stanovení volných lehkých řetězců, je pak nutné pro průkaz relapsu/progrese provedení vyšetření kostní dřeně, kdy stanovení nové aktivity umožňuje průkaz ≥ 10 % infiltrace kostní dřeně MM buňkami
- relaps/progrese může být stanoven i na základě vzniku nového či zvětšení původního osteolytického ložiska nebo plazmocytomu měkkých tkání o více než 50 % (minimálně o 1 cm)
- nově lze aktivitu onemocnění posoudit i pomocí celotělové magnetické rezonance nebo PET/CT, které jsou zejména v případě čistě nesekreční formy spolu s vyšetřením kostní dřeně jedinými možnostmi zhodnocení, zde je však nutné mít pro srovnání výsledky vyšetření provedených po ukončení předchozí léčby.
E. LÉČEBNÁ STRATEGIE
Nejdůležitější změny oproti doporučením z roku 2012
- Lenalidomid a bortezomib jsou doporučeny používat i současně v indukční fázi onemocnění jak v primoléčbě, tak v relapsu onemocnění. Použití této kombinace k lednu 2018 nebylo registrováno a vyžaduje proto souhlas zdravotní pojišťovny.
- Posun v léčebném cíli zvláště u relapsu onemocnění. Rozhodovací algoritmy jasně definují první léčebné cíle – dosažení kompletní léčebné odpovědi (CR) potvrzené průtokovou cytometrii nebo metodami molekulární biologie v případě primoléčby a prvního relapsu onemocnění. Optimálním cílem je dosažení negativity MRD, protože tito nemocní mají nejlepší šanci na dlouhodobé bezpříznakové přežití.
- Zařazení 6 nových léků do léčby relapsu onemocnění.
- Poprvé existuje doporučení pro léčbu prognosticky nepříznivých myelomů na základě FISH analýzy.
Obr. 1. Základní algoritmus léčby mnohočetného myelomu od roku 2018 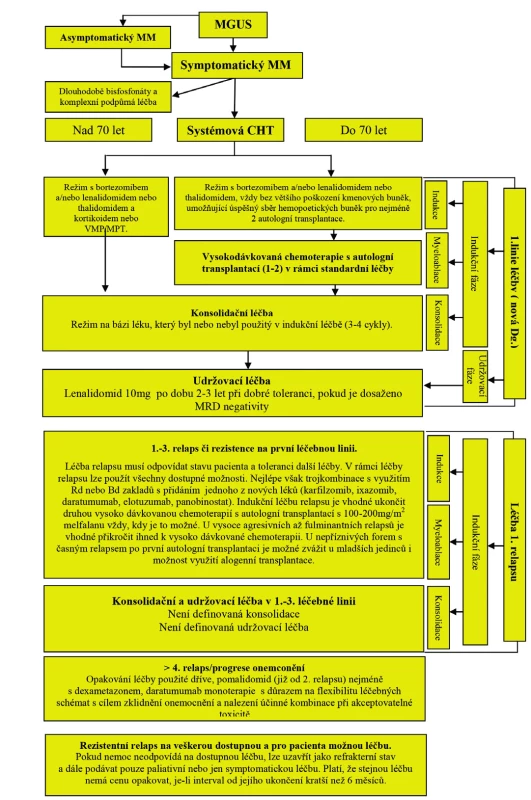
Vysvětlivky: MGUS – monoklonální gamapatie nejasného významu; MM – mnohočetný myelom; CHT – chemoterapie; VMP – bortezomib, melfalan, prednison; MPT – melfalan, prednison, thalidomid; MRD – minimální reziduální nemoc; Rd – lenalidomid, dexametazon; Bd – bortezomib, dexametazon. Doporučení: pro diagnostiku a léčbu vysoce prognosticky rizikové skupiny („high-risk“) nemocných s mnohočetným myelomem
- Pro identifikaci podskupiny nemocných s vysokým rizikem pro krátké celkové přežití (tzv. „high-risk“ MM) je vhodné vstupně vyšetřit na myelomových buňkách všechny dostupné rizikové translokace IgH (t(4;14), t(14;16), t(14;20), del(17p), zisk (1q21) a stanovit, zda jde o hyperdiploidní karyotyp. Za nezbytné minimum lze považovat (t(4;14), t(14;16) a del(17p) a zisk (1q21). (stupeň doporučení A, úroveň důkazu Ia)
- „Ultra-high-risk“ skupinu identifikují komplexní změny karyotypu.
- Změny se v čase vyvíjejí, proto je vhodné vyhodnotit tyto změny i před léčbou relapsu onemocnění.
- U „high-risk“ podskupiny nemocných s MM by neměly být používány dvojkombinace léků, naopak by měly být použity nejméně nejúčinnější dostupné trojkombinace. Toto platí pro novou diagnózu i relaps onemocnění. (stupeň doporučení A, úroveň důkazu Ia)
- V primoléčbě při přítomnosti t(4;14) by měl být součástí léčebné strategie bortezomib a v indikovaných případech tandemová autologní transplantace. (stupeň doporučení A, úroveň důkazu Ia)
Rozhodovací algoritmy léčby a léčebné protokoly
Na obrázku 2 a v tabulce 15 jsou základní možnosti léčby. V tabulce 16 redukční kroky v souvislosti s vybranými faktory nemocného. Jednotlivé léčebné protokoly, jejichž přehledy jsou pravidelně aktualizovány v souboru „Léčebné protokoly CMG “ na webových stránkách CMG. Stávající platná verze a aktualizace jsou ke stažení z www.myeloma.cz (sekce mnohočetný myelom/guidelines/aktuální protokoly).
Tab. 15. Přehled doporučených léčebných režimů 
*AT – autologní transplantace Tab. 16. Léčebný algoritmus pro nemocné s MM nad 65 let podle rizikových faktorů* 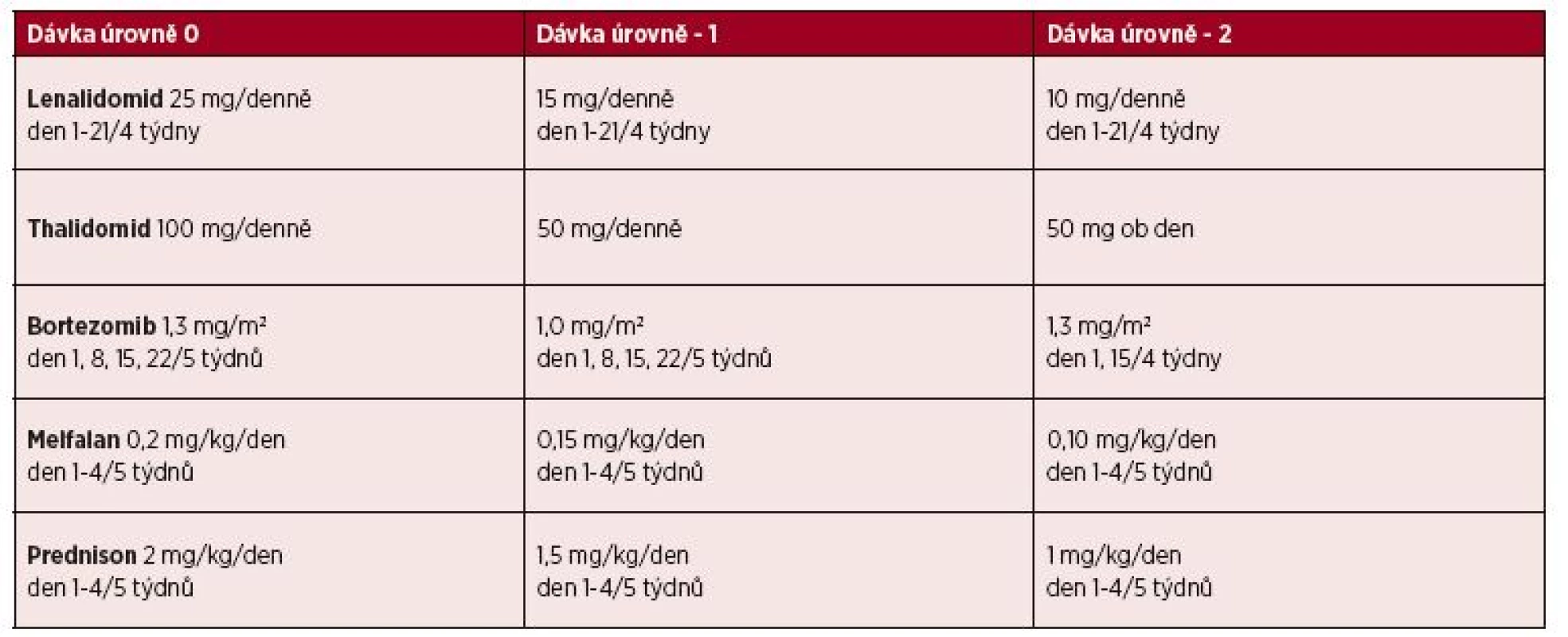
(modifikace podle [Palumbo, NEJM 2011]) *Rizikové faktory jsou mírná, střední nebo vysoká slabost či chatrnost vyžadující pomoc v běžném životě, v praxi i zhoršený status performace; další interní nemoci (porucha funkce některého z důležitých orgánů – srdce, ledviny, plíce, játra, jiné). Dávka úrovně 0 je standardní dávkou pro běžné nemocné bez rizikových faktorů. Dávka úrovně -1 je vstupní dávka u nemocných s jedním rizikovým faktorem. Dávka úrovně -2 je vstupní dávka u nemocných s jedním rizikovým faktorem a nežádoucími účinky léčby st. 3–4 mimo hematologické. Obr. 2. Primoléčba onemocnění u nemocných vhodných k autologní transplantaci* *Jak autologní transplantace, tak konsolidace jsou možné možnosti volby dalšího postupu, je-li cílem dosažení hluboké remise (kompletní remise potvrzena průtokovou cytometrií nebo metodami molekulární biologie v primoléčbě). 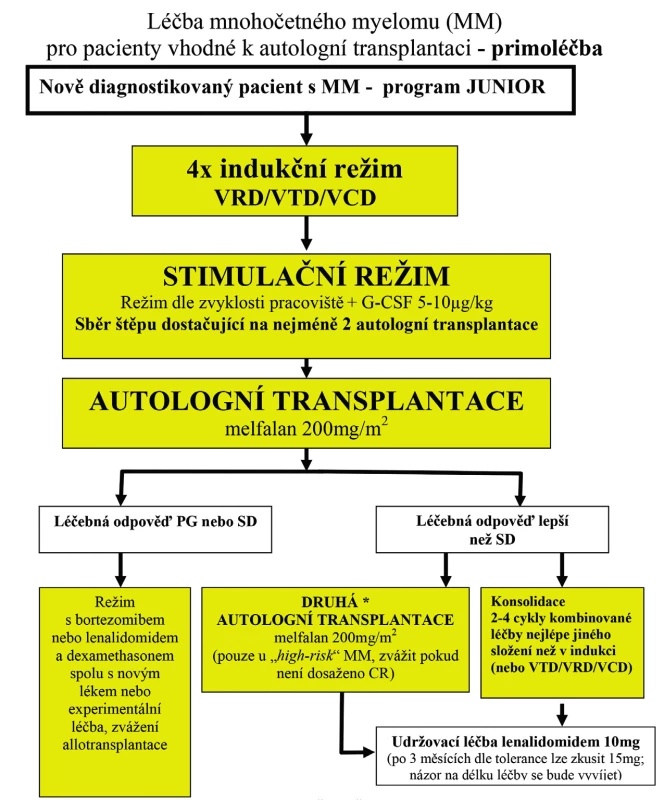
Vysvětlivky: MM – mnohočetný myelom; VRD – bortezomib, lenalidomid, dexametazon; VTD – bortezomib, thalidomid, dexametazon; VCD – bortezomib, cyklofosfamid, dexametazon; G-CSF – granulocytární kolonie stimulující růstový faktor; PG – progrese; SD – stabilní onemocnění; CR – kompletní remise. F. LÉČBA MNOHOČETNÉHO MYELOMU
Doporučení pro léčbu thalidomidem
- Thalidomid je účinným lékem s významnou toxicitou. V primoléčbě by léčebný režim výhradně na bázi thalidomidu neměl být první volbou, pokud jsou k dispozici účinnější a bezpečnější léčebné možnosti (stupeň doporučení A, úroveň důkazu Ia).
- Thalidomid je účinný lék u MM. Je indikován v primoléčbě i relapsu onemocnění (stupeň doporučení A, úroveň důkazu Ia).
- Kombinované režimy na bázi thalidomidu jsou účinnější než monoterapie a optimální je využití režimů s kombinací alkylační látky (melfalan, cyklofosfamid) a glukokortikoidu a případně bortezomibu (stupeň doporučení A, úroveň důkazu Ia), v budoucnosti případně novými léky na základě dostupným dat (stupeň doporučení C, úroveň důkazu IV).
- Je doporučeno používat thalidomid v běžné dávce 100 mg denně večer před spaním v indukční léčbě a v udržovací léčbě nebo lépe krátkodobé konsolidační léčbě. Minimální dávka není stanovena (stupeň doporučení A, úroveň důkazu Ia).
- Thalidomid nepřekonává negativní prognostický vliv tzv. nepříznivých chromozomálních aberací a neměl by tedy být lékem první volby u těchto nemocných (stupeň doporučení A, úroveň důkazu Ia).
- Mezi klíčová profylaktická opatření patří použití nízkomolekulárního heparinu nebo kyseliny acetylsalicylové jako profylaxe žilní trombózy po dobu léčby, použití laxativ a použití thalidomidu večer před spaním (stupeň doporučení A, úroveň důkazu Ia).
- Polyneuropatie je nejzávažnějším nežádoucím účinkem thalidomidu. Časná redukce dávky a časné zastavení léčby jsou vhodným opatřením. Rozvoj polyneuropatie do stupně dva by měl být signálem k zastavení léčby, existují-li jiné dostupné léčebné možnosti (stupeň doporučení A, úroveň důkazu Ib).
- Thalidomid je teratogenní lék a při jeho použití je nezbytné dodržet přesně stanovený bezpečnostní program daný regulačními úřady (stupeň doporučení A, úroveň důkazu Ia).
- Konsolidační léčba režimem s thalidomidem je účinná a měla by být jednou z léčebných modalit po provedení vstupní indukční a případně myeloablativní léčby (stupeň doporučení A, úroveň důkazu Ia).
DOPORUČENÍ PRO LÉČBU LENALIDOMIDEM
- Lenalidomid je vysoce účinný lék u MM. Je indikován k léčbě relapsu i k léčbě nově diagnostikovaného onemocnění nejméně v kombinaci s dexametazonem (stupeň doporučení A, úroveň důkazu Ia); je indikován k udržovací léčbě po provedení autologní transplantace (stupeň doporučení A, úroveň důkazu Ia).
- Základním režimem podle SPC přípravku u RRMM i NDMM je kombinovaný režim lenalidomidu s dexametazonem. Doporučené dávkování přípravku a počáteční dávka je 25 mg denně perorálně po dobu 21 dnů s týdenní pauzou v 28denním cyklu (stupeň doporučení A, úroveň důkazu Ia). V udržovací léčbě se podává lenalidomid v monoterapii, počáteční dávka je 10 mg denně perorálně po dobu 28 dnů v 28denním cyklu (stupeň doporučení A, úroveň důkazu Ia). Režim na bázi lenalidomidu by měl být podáván podle SPC a registračních studií až do progrese onemocnění nebo do nepřijatelné toxicity (stupeň doporučení A, úroveň důkazu Ib).
- Kombinované režimy na bázi lenalidomidu s přidáním nového léku s biologickým mechanismem účinku prokázaly u předléčených nemocných (karfilzomib, daratumumab, elotuzumab, ixazomib) i u nově diagnostikovaného onemocnění (bortezomib) zásadní zlepšení léčebného účinku i prognózy. Trojkombinace léků mají vyšší účinnost než dvojkombinace Len/Dex (stupeň doporučení A, úroveň důkazu Ib). Dle doporučení myelomové sekce ČHS by měly být proto kombinované režimy upřednostňovány.
- Užití nízké dávky dexametazonu v kombinaci s lenalidomidem vykazuje lepší toleranci léčby bez ztráty účinnosti ve srovnání s vysokou dávkou dexametazonu (480 mg/cyklus) (stupeň doporučení A, úroveň důkazu Ib).
- Tolerance léčby lenalidomidem závisí na stavu předléčenosti a tomu musí být upraveno dávkování lenalidomidu v průběhu léčby (stupeň doporučení C, úroveň důkazu 4).
- Neutropenie a trombocytopenie jsou nejčastější nežádoucí účinky, které jsou předvídatelné a zvládnutelné. Neutropenii je možné zvládnout kombinací podávání růstového faktoru pro granulocyty (G-CSF), modifikací dávek lenalidomidu či přerušením léčby. Trombocytopenii lze zvládnout transfuzemi destiček, modifikací dávek lenalidomidu či přerušením léčby.
- Mezi klíčová profylaktická opatření patří profylaxe žilní trombózy po celou dobu léčby. Profylaxe kyselinou acetylsalicylovou (100 mg/den) je vhodná u pacientů se standardním rizikem venozního tromboembolismu (VTE). Pro pacienty s vyšším rizikem je doporučeno použít LMWH v profylaktických dávkách (stupeň doporučení B, úroveň důkazu IIa).
- Před zahájením léčby lenalidomidem je doporučeno vyšetřit nemocného na přítomnost hepatitidy B. V případě pozitivního nálezu a rovněž u nemocných s předcházející infekcí v anamnéze je doporučeno realizovat monitorování příslušných antigenů a případně zvážit vhodnou profylaxi (stupeň doporučení C, úroveň důkazu IV).
- Použití lenalidomidu nezpůsobuje závažnou polyneuropatii. Je proto lékem volby u pacientů se závažnější formou polyneuropatie (stupeň doporučení C, úroveň důkazu IV).
- Kombinace lenalidomidu s perorálním melfalanem u pacientů s nově diagnostikovaným mnohočetným myelomem zvyšuje riziko vzniku sekundárních primárních malignit (stupeň doporučení A, úroveň důkazu Ia). Tato kombinace léků je relativně kontraindikovaná a to obecně u všech nemocných s mnohočetným myelomem.
- Lenalidomid je teratogenní lék a při jeho použití je nezbytné dodržovat Program prevence početí (stupeň doporučení C, úroveň důkazu IV).
DOPORUČENÍ PRO LÉČBU POMALIDOMIDEM
- Pomalidomid je v kombinaci nejméně s dexametazonem indikován k léčbě dospělých pacientů s relabovaným a refrakterním mnohočetným myelomem, kteří absolvovali alespoň dvě předchozí léčebná schémata, zahrnující jak lenalidomid, tak i bortezomib a jsou refrakterní na poslední podávanou léčbu (stupeň doporučení A, úroveň důkazu Ib).
- Pomalidomid se podává perorálně ve startovací dávce 4 mg jednou denně ve dnech 1–21 v 28denním cyklu. Léčba pokračuje do progrese onemocnění. (stupeň doporučení A, úroveň důkazu Ib).
- Přidání třetího léku k pomalidomidu a dexametazonu je možné, nezvyšuje toxicitu a zvyšuje počet léčebných odpovědí nejméně v případě bortezomibu a cyklofosfamidu (stupeň doporučení B, úroveň důkazu IIa).
- Pomalidomid lze bezpečně podávat u pacientů s renálním selháním bez nutnosti redukovat dávku (stupeň doporučení B, úroveň důkazu IIa).
- Mezi klíčová profylaktická opatření patří profylaxe žilní trombózy po celou dobu léčby a použití růstových faktorů v případě myelosuprese. Profylaxe kyselinou acetylsalicylovou (100 mg/den) je vhodná u pacientů se standardním rizikem venózního tromboembolismu (VTE). Je doporučeno použít LMWH v profylaktických dávkách pro pacienty s vyšším rizikem (stupeň doporučení B, úroveň důkazu IIa).
- Použití pomalidomidu nezpůsobuje ani nezhoršuje polyneuropatii související s předchozí neurotoxickou léčbou. Pomalidomid je možné podávat nemocným s preexistující polyneuropatií (stupeň doporučení A, úroveň důkazu Ia).
- Pomalidomid je teratogenní lék a při jeho použití je nezbytné dodržovat Program prevence početí (stupeň doporučení C, úroveň důkazu IV).
- Před zahájením léčby pomalidomidem je doporučeno vyšetřit nemocného na přítomnost hepatitidy B. V případě pozitivního nálezu a rovněž u nemocných s předcházející infekcí v anamnéze je doporučené realizovat monitorování příslušných antigenů a případně zvážit vhodnou profylaxi (stupeň doporučení C, úroveň důkazu IV).
DOPORUČENÍ PRO LÉČBU BORTEZOMIBEM
- Bortezomib je vysoce účinný lék u MM. Je indikován v primoléčbě i relapsu onemocnění, ve vstupní indukční a konsolidační části indukční fáze léčby u všech nemocných (stupeň doporučení A, úroveň důkazu Ib).
- Kombinované režimy na bázi bortezomibu s glukokortikoidem a imunomodulační látkou (především režim VRD) lze považovat za nejúčinnější dostupné režimy dobře tolerované nemocnými v primoléčbě v roce 2018. Jde současně o účinné režimy v relapsu onemocnění (stupeň doporučení A, úroveň důkazu Ib pro primoléčbu).
- Kombinované režimy na bázi bortezomibu s glukokortikoidem a alkylační látkou (melfalan, cyklofosfamid) patří mezi účinné režimy v primoléčbě (stupeň doporučení A, úroveň důkazu Ia). Použití monoterapie až na výjimky nelze považovat za správný postup.
- Optimální dávkování není stanoveno. Dle SPC produktu je bortezomib v dávce 1,3 mg/m2 s. c. nebo i. v. podáván v monoterapii či kombinaci ve dny 1, 4, 8, 11 v 21denním cyklu. Stávající doporučení však upřednostňují méně intenzivní režimy s prodloužením intervalu mezi dávkami (dny 1, 8, 15, 22 v 28denním cyklu) a podkožní aplikací bortezomibu, které dosahují podobných léčebných výsledků se zásadním snížením nežádoucích účinků. U vysoce fragilních nemocných může být dávkování výrazně individuální (stupeň doporučení A, úroveň důkazu Ib).
- Počet aplikací bortezomibu v případě dobré tolerance je regulován úhradovou vyhláškou – v kombinaci s melfalanem maximálně 52 aplikací (u dosud neléčených pacientů nevhodných k autologní transplantaci), u pacientů vhodných k autologní transplantaci pak v kombinaci s thalidomidem a dexametazonem 24 aplikací. Počet aplikací při progresi nemoci je limitován počtem 44 aplikací. V případě dobré tolerance může být režim podávaný až do následné progrese (stupeň doporučení C úroveň důkazu IV).
- Bortezomib v kombinovaném režimu je doporučen jako lék první volby u nemocných s renálním selháním, u kterých může být použit bez nutnosti redukce dávky (stupeň doporučení B, úroveň důkazu IIa).
- Bortezomib částečně překonává negativní prognostický vliv tzv. nepříznivých chromozomálních aberací, zvláště translokací IgH, a měl by proto být jedním z léků první volby u těchto nemocných (stupeň doporučení A, úroveň důkazu Ib).
- Bortezomib nezvyšuje riziko tromboembolické nemoci. U nemocných s anamnézou či vysokým rizikem tromboembolické nemoci je jeho aplikace upřednostněna (stupeň doporučení A, úroveň důkazu Ib).
- Mezi klíčová profylaktická opatření patří použití acykloviru v dávce nejméně 200–400 mg 1x denně, zvýšený pitný režim a antidiarhoická medikace večer a následující den ráno po aplikaci bortezomibu (stupeň doporučení A, úroveň důkazu Ib).
- Neuropatie je nejzávažnějším nežádoucím účinkem bortezomibu. Subkutánní aplikace, časná redukce dávky nebo prodloužení intervalů mezi dávkami na 1x týdně a případně časné zastavení léčby jsou vhodným opatřením. Rozvoj polyneuropatie do stupně dva by měl být signálem k zastavení léčby, existují-li jiné dostupné léčebné možnosti (stupeň doporučení A, úroveň důkazu Ib).
DOPORUČENÍ PRO LÉČBU KARFILZOMIBEM
- Karfilzomib je indikován k léčbě dospělých pacientů s relabovaným a refrakterním mnohočetným myelomem po nejméně 1 léčebné linii v kombinaci s lenalidomidem a dexametazonem nebo v kombinaci s dexametazonem (stupeň doporučení A, úroveň důkazu Ia).
- Karfilzomib nemá být používán v monoterapii (stupeň doporučení A, úroveň důkazu Ib), ale nejméně s dexametazonem (stupeň doporučení C, úroveň důkazu IIa).
- Karfilzomib se podává intravenózně den 1, 2, 8, 9, 15 a 16 v 28denních cyklech. V prvním cyklu je lék podáván nejprve v dávce 20 mg/m² i. v. V případě tolerance léku se následně od 8. dne prvního cyklu dávka zvyšuje na 27 mg/m² v případě režimu s lenalidomidem a dexametazonem (režim KRd) a na 56 mg/m2 v případě kombinace kombinace s dexametazonem (režim KD). Léčba pokračuje do progrese onemocnění podle SPC léku (pro režim KRd je podání karfilzomibu limitované na 18 měsíců) (stupeň doporučení A, úroveň důkazu Ia).
- U pacientů je doporučena profylaxe herpetických infekcí (stupeň doporučení A, úroveň důkazu Ia).
- Při použití karfilzomibu je doporučeno aktivně řešit problematiku hypertenze a hypervolemie vstupně i v průběhu léčby, neboť se mohou podílet na vzniku srdečního selhání u predisponovaných jedinců a starších nemocných (stupeň doporučení A, úroveň důkazu Ia).
DOPORUČENÍ PRO LÉČBU IXAZOMIBEM
- Ixazomib je indikován k léčbě dospělých pacientů s relabovaným a refrakterním mnohočetným myelomem po 1–3 léčebných liniích v kombinaci s lenalidomidem a dexametazonem (stupeň doporučení A, úroveň důkazu Ib).
- Ixazomib se podává perorálně jednu hodinu před jídlem nebo dvě hodiny po jídle ve vstupní dávce 4 mg jednou týdně (den 1, 8, 15) v 28denních cyklech. Léčba pokračuje do progrese onemocnění podle SPC léku (stupeň doporučení A, úroveň důkazu Ia).
- U pacientů je doporučena profylaxe herpetických infekcí (stupeň doporučení A, úroveň důkazu Ib).
- Ixazomib v kombinovaném režimu Ixa/Len/Dex významně zlepšuje výstupy u prognosticky nepříznivé skupiny nemocných (tzv. vysoké riziko na základě definice chromozomálních abnormalit včetně skupiny nemocných s amplifikací 1q21) a podle jedné randomizované studie tuto negativní prognózu překonává (stupeň doporučení A, úroveň důkazu Ib).
DOPORUČENÍ PRO LÉČBU DARATUMUMABEM
- Daratumumab v monoterapii je indikován u pacientů s relabovaným a refrakterním mnohočetným myelomem, kteří absolvovali léčbu obsahující jak proteasomový inhibitor, tak imunomodulační látku, a u kterých došlo k progresi onemocnění při poslední léčbě (stupeň doporučení B, úroveň důkazu IIA).
- Daratumumab v kombinaci s lenalidomidem a dexametazonem nebo v kombinaci s bortezomibem a dexametazonem je indikován u pacientů s mnohočetným myelomem, kteří absolvovali alespoň jednu předchozí léčebnou linii (stupeň doporučení A, úroveň důkazu Ib).
- Daratumumab se podává intravenózně v dávce 16 mg/kg:
- a) v případě monoterapie nebo kombinace s lenalidomidem a dexametazonem, kdy 1. cyklus léčby má 4 týdny, se daratumumab podává v prvních 2 cyklech každý týden (den 1, 8, 15, 22); v cyklech 3–6 pak každé 2 týdny (den 1, 15) a následně již jen každé 4 týdny (den 1) až do progrese onemocnění či neakceptovatelné toxicity.
- b) v případě kombinace s bortezomibem a dexametazonem, kdy 1 cyklus léčby má 3 týdny: cyklus 1 až 3 – každý týden (den 1, 8, 15), cyklus 4 až 8 – 1x za 3 týdny, cyklus 9 a dále 1x za 4 týdny až do progrese onemocnění či neakceptovatelné toxicity.
- Reakce spojené s infuzí (IRRs) jsou typickým a nejčastějším nežádoucím účinkem spojeným s podáním daratumumabu, vyskytující se přibližně u 50 % léčených. Je doporučeno aplikovat premedikaci v podobě kortikoidů, antihistaminik a paracetamolu 30–60 minut před zahájením infuze, stejně jako podat první infuzi velmi pomalu (cca 6 hodin) (stupeň doporučení A, úroveň důkazu Ib).
- Vzhledem k interferenci daratumumabu v rámci předtransfuzního vyšetření je doporučeno provést vstupní imunohematologická vyšetření ještě před zahájením léčby a tak dopředu zajistit dostupnost antigenně kompatibilních erytrocytových transfuzních přípravků (stupeň doporučení C, úroveň důkazu IV). Kompletní přehled edukačních materiálů k této probklematice je umístěn na stránkách SÚKLu (http://www.sukl.cz/leciva/rok-2016).
- Je doporučena profylaxe pomocí antivirotik v rámci prevence reaktivace herpes zoster, a to po dobu léčby a minimálně ještě 3 měsíce po ukončení léčby (stupeň doporučení A, úroveň důkazu Ib).
DOPORUČENÍ PRO LÉČBU ELOTUZUMABEM
- Elotuzumab v kombinaci s lenalidomidem a dexametazonem je indikován u pacientů s mnohočetným myelomem, kteří absolvovali 1–3 předchozí léčebné linie (stupeň doporučení A, úroveň důkazu Ib).
- Elotuzumab se podává intravenózně v dávce 10 mg/kg: v 1. a 2. cyklu – 1x týdně (den 1, 8, 15, 22), od 3. cyklu – dále 1x za 2 týdny (den 1, 15) až do progrese onemocnění nebo neakceptovatelné toxicity.
- Před zahájením infuze je doporučeno aplikovat premedikaci v podobě kortikoidů, antihistaminik a paracetamolu 30–60 minut v rámci prevence rozvoje IRRs. Doporučená rychlost infuze elotuzumabu je 5 ml/min (stupeň doporučení A, úroveň důkazu Ib).
- Elotuzumab lze bezpečně podávat u pacientů s mnohočetným myelomem a renálním selháním bez nutnosti redukovat dávku (stupeň doporučení B, úroveň důkazu IIa).
DOPORUČENÍ PRO LÉČBU PANOBINOSTATEM
- Panobinostat je v kombinaci s bortezomibem a dexametazonem indikován k léčbě dospělých pacientů s relabujícím a/nebo refrakterním mnohočetným myelomem, kteří dostávali nejméně dvě předchozí linie léčby včetně bortezomibu a imunomodulačního léku (stupeň doporučení A, úroveň důkazu Ib).
- Doporučená zahajovací dávka panobinostatu je 20 mg, podávaná perorálně jednou denně ve dnech 1, 3, 5, 8, 10 a 12 během 21denního cyklu. Pacienti by měli být nejdříve léčeni osmi cykly. Doporučuje se, aby pacienti profitující z léčby pokračovali v léčbě dalšími osmi cykly. Celkové trvání léčby je tedy až 16 cyklů (48 týdnů).
- Úprava zahajovací dávky u nemocných s lehkou až těžkou poruchou funkcí ledvin není nutná (stupeň doporučení B, úroveň důkazu IIa).
- U pacientů s lehkou poruchou jaterních funkcí by se měla léčba zahajovat sníženou dávkou panobinostatu, a to 15 mg během prvního cyklu léčby. Na základě snášenlivosti pacienta může být zvažováno zvýšení dávky z 15 mg na 20 mg. Pacienti se středně těžkou poruchou jaterních funkcí by měli zahájit léčbu panobinostatem během prvního cyklu léčby sníženou dávkou 10 mg. Při pacientově snášenlivosti je možné zvažovat zvýšení dávky z 10 mg na 15 mg. Panobinostat nemá být podáván pacientům s těžkou poruchou funkce jater z důvodu nedostatku zkušeností a bezpečnostních údajů u této populace (stupeň doporučení B, úroveň důkazu IIa).
DOPORUČENÍ PRO LÉČBU BENDAMUSTINEM
- Bendamustin je možné využít u nemocných nevhodných k autologní transplantaci s MM v primoléčbě při kontraindikaci thalidomidu či bortezomibu v případě přítomné neuropatie (stupeň doporučení C, úroveň důkazu IV).
- Jak v první linii, tak i v následných liniích je bendamustin indikován v kombinovaných režimech místo melfalanu a cyklofosfamidu u nemocných s renální insuficiencí. U nemocných s clearance kreatininu > 10 ml/min není úprava dávky nutná (stupeň doporučení B, úroveň důkazu IIa).
- U nemocných bez renální insuficience může být bendamustin indikován v kombinovaných režimech v případě rezistence na konvenční alkylační látky (melfalan, cyklofosfamid) (stupeň doporučení B, úroveň důkazu IIa).
- U nemocných se středně těžkou poruchou funkce jater (hodnoty sérového bilirubinu v rozmezí 20–50 μmol/l) je možné bendamustin bezpečně podávat s 30 % redukcí dávky (stupeň doporučení B, úroveň důkazu IIa).
- Optimální dávka bendamustinu není stanovena. Podle SPC je doporučeno dávkování v rozmezí 120–150 mg/m2 tělesného povrchu v den 1 a 2 každé 4 týdny. Dávkování 60 mg/m2 případně 75 mg/m2 v den 1 a 2 je doporučenou variantou v kombinovaných režimech na základě zkušeností z klinických studií (stupeň doporučení B, úroveň důkazu Ia).
DOPORUČENÍ – ALKYLAČNÍ A JINÁ CYTOSTATIKA, GLUKOKORTIKOIDY
- Léčba vysokými dávkami dexametazonu v monoterapii je vhodná pro iniciální léčbu pacientů, u nichž je jiná léčba kontraindikována, to znamená u pacientů s těžkou pancytopenií (stupeň doporučení C, úroveň důkazu IIa). Neprodleně, jak to stav nemocného umožní, by měl být režim doplněn na standardně používanou léčebnou kombinaci. Tato léčba je vhodná i pro pacienty s renální insuficiencí, nelze-li použít jiný silnější režim (stupeň doporučení B, úroveň důkazu IIa).
- Kombinace melfalanu s prednisonem nebo cyklofosfamidu s glukokortikoidy dnes nejsou optimální léčebnou volbou v primoléčbě ani v relapsu onemocnění, jejich možným využitím je paliativní léčba. Opatrnosti je třeba při podávání pacientům s renální insuficiencí.
DOPORUČENÍ PRO VYSOKODÁVKOVANOU CHEMOTERAPII S AUTOLOGNÍ TRANSPLANTACÍ KMENOVÝCH BUNĚK
- Vysokodávkovaná chemoterapie s autologní transplantací kmenových buněk (AT) by měla být součástí primární léčebné strategie u pacienta s nově diagnostikovaným onemocněním ve věku do 70 let či vhodného biologického věku (stupeň doporučení A, úroveň důkazu Ia).
- Optimálním předtransplantačním režimem je melfalan 200 mg/m2 (stupeň doporučení A, úroveň důkazu Ib).
- Nejvíce účinným postupem v současnosti (z hlediska četnosti kompletních remisí, PFS, OS) je kombinace zahrnující 1–2 nové léky v indukční fázi a AT (stupeň doporučení A, úroveň důkazu Ia).
- Opakovaná (tandemová) autologní transplantace může být použita jako konsolidace u nemocných s cílem dosáhnout maximální léčebné odpovědi a dlouhodobého trvání remise (stupeň doporučení A, úroveň důkazu Ia).
- Pacienti starší 70 let v dobrém celkovém stavu mohou být také vhodnými kandidáty pro tento postup s možností využí melfalanu v dávce redukované na 100 mg/m2 podané dvakrát krátce po sobě (stupeň doporučení A, úroveň důkazu Ib). V rozhodnutí o způsobu léčby musí být zvážena všechna možná rizika a přínosy tohoto postupu u konkrétního pacienta (stupeň doporučení C, úroveň důkazu IV).
- Vysokodávkovaná chemoterapie s autologní transplantací kmenových buněk (AT) by měla být vždy součástí léčebné strategie relapsu MM, pokud nebyla provedena z nějakého důvodu v primoléčbě (kontraindikace, nesouhlas nemocného a podobně) u nemocných vhodných pro provedení AT. Retransplantace v relapsu u nemocných s MM je možnou efektivní léčebnou strategií, zvláště pokud je použita v kombinaci s reindukcí zahrnující nové cílené léky (stupeň doporučení A, úroveň důkazu Ib).
- V současnosti dostupné metody čištění transplantátu (tzv. „purging“) nejsou přínosné, a proto nejsou doporučovány (stupeň doporučení A, úroveň průkazu Ib).
- Vysokodávkovaná chemoterapie u pacientů s těžkým poškozením ledvin (clearance < 50 ml/min) je proveditelná, ale vyžaduje vždy redukci dávky melfalanu a měla by být prováděna pouze ve specializovaných centrech (stupeň doporučení B, úroveň důkazu IIa).
DOPORUČENÍ PRO ALOGENNÍ TRANSPLANTACI
- Alogenní transplantace má omezenou roli v terapii mnohočetného myelomu, a to především z důvodů značné toxicity kombinované etiologie a také malého množství pacientů s myelomem, kterým lze tuto léčebnou alternativu nabídnout (stupeň doporučení A, úroveň důkazu Ib).
- Alogenní transplantace by měly být prováděny u nemocných s mnohočetným myelomem nejlépe v rámci klinických studií, v primoléčbě výhradně v rámci klinických studií (stupeň doporučení C, úroveň důkazu IV).
- Za možné kandidáty lze považovat nemocné ve věku do 55 let s HLA identickým sourozencem, kteří nejsou rezistentní na indukční léčbu před provedením alogenní transplantace. Pacient však musí být plně obeznámen s možnými riziky tohoto postupu (stupeň doporučení B, úroveň důkazu IIa).
- Za optimální indikaci v dnešní době lze považovat časný první senzitivní relaps onemocnění u vysoce rizikových nemocných, za optimální léčebný postup využití kombinace auto-allo transplantace s použitím RIC režimů (stupeň doporučení C, úroveň důkazu IV).
DOPORUČENÍ PRO UDRŽOVACÍ LÉČBU
- Lenalidomid je doposud nejúčinnějším lékem v udržovací léčbě mnohočetného myelomu (stupeň doporučení A, úroveň důkazu Ia).
- Udržovací léčba lenalidomidem je doporučena v dávce 10 mg denně (stupeň doporučení A, úroveň důkazu Ib).
- Délka udržovací léčby je doporučena až do relapsu či progrese onemocnění (stupeň doporučení A, úroveň důkazu Ia).
- Optimální délka podávání UL lenalidomidem není doposud známa, zvláště u nemocných v kompletní remisi s MRD negativitou je podávání léku delší než 3 roky jen obtížně zdůvodnitelné s ohledem na průměrnou délku udržovací léčby v klinických studiích a bezpečnost podávaní (doporučení C, úroveň důkazu IV).
- Thalidomid v udržovací léčbě je doporučen jen v případě nedostupnosti lenalidomidu nebo při jeho kontraindikaci či nesnášenlivosti, a to z důvodu menší účinnosti a vyšší toxicity (stupeň doporučení A, úroveň důkazu Ib).
- V udržovací léčbě je thalidomid doporučen ve vstupní dávce 100 mg denně u nemocných bez delece nebo monosomie chromozomu 13, translokace t(4;14), t14,16) a delece chromozomu 17 (stupeň doporučení A, úroveň důkazu Ib).
- Podávaní thalidomidu je doporučeno po dobu jednoho roku nezávisle na léčebné odpovědi. Pokračování udržovací léčby při výborné toleranci je na individuálním zvážení (stupeň doporučení C, úroveň důkazu IV).
- Kromě výše uvedených možností by jakákoliv udržovací a konsolidační léčba měla probíhat výhradně v rámci klinických studií (stupeň doporučení A, úroveň důkazu Ib).
DOPORUČENÍ PRO VOLBU CHEMOTERAPIE PŘI SELHÁNÍ LEDVIN
- Základní podmínkou pro úspěšnou záchranu funkcí ledvin je použití známých standardních opatření, jako jsou dostatečná hydratace a obrat tekutin s měřením centrálního žilního tlaku, řešení minerální dysbalance, zvláště pak hyperkalcemie.
- Pro iniciální léčbu mnohočetného myelomu u pacientů s poškozenou funkcí ledvin se doporučuje režim s rychlým nástupem účinku, s dobrou tolerancí a především s vysokou šancí na léčebnou odpověď s využitím plné dávky léku. Důležité je však především zahájit léčbu rychle, ať už je použit jakýkoliv léčebný režim (stupeň doporučení B, úroveň důkazu IIa).
- Režimy s proteasomovými inhibitory (nejlépe s bortezomibem) lze v současnosti považovat za optimální postup splňující v současnosti nejlépe výše uvedené parametry optimálního režimu pro záchranu ledvin (stupeň doporučení C, úroveň důkazu IV).
- Režim s imunomodulačním lékem thalidomidem nebo pomalidomidem v příslušné dávce lze použít v případě, kdy není vhodné podat režim s bortezomibem (stupeň doporučení C, úroveň důkazu IV.).
- Režimy s lenalidomidem (nejméně s dexametazonem) vyžadují redukci dávky podle SPC. Samotný dexametazon je možno podat okamžitě po stanovení diagnózy, aniž by byla ujasněna další strategie (stupeň doporučení C, úroveň důkazu IV).
- Kombinace protinádorové léčby současně s využitím nové dialyzační membrány (dialyzační HCO membrána) je indikovaným postupem v případě akutního renálního selhání zapříčiněného velkým množstvím volných lehkých řetězců – cast nephropathy (stupeň doporučení A, úroveň důkazu Ib).
- Nezbytné je důsledné monitorování nežádoucích účinků a včasné snížení dávky či následně vysazení léků (stupeň doporučení B, úroveň důkazu III).
- Je nezbytná opatrnost při používání nesteroidních antiflogistik a úprava dávek řady léků, např. derivátů morfinu a bisfosfonátů (stupeň doporučení B, úroveň důkazu III).
- Při renální insuficienci je nezbytné zvážit případnou souvislost selhání ledvin a léčby určitým typem bisfosfonátu podle jeho nefrotoxicity (stupeň doporučení B, úroveň důkazu III).
- Pacienti s chronickou nedostatečností ledvin a anémií by měli být léčeni rekombinantním erytropoetinem (stupeň doporučení A, úroveň důkazu I).
- Při rozvaze o vysokodávkované chemoterapii je nutno zvážit potenciální přínos a podstatně vyšší počet komplikací, než je obvyklé u pacientů s normální funkcí ledvin. Tento postup by proto měl být prováděn jen v centrech s dostatkem zkušeností se zvládáním závažných potransplantačních situací (stupeň doporučení C, úroveň důkazu IV).
G. PODPŮRNÁ LÉČBA U NEMOCNÝCH S MNOHOČETNÝM MYELOMEM
Doporučení z komplexní podpůrné léčby
- Radioterapie je standardní léčebnou metodou pro solitární plazmocytom i extramedularní plazmocytom (stupeň doporučení B, úroveň důkazu IIa).
- Adjuvantní chemoterapie není doporučena u solitárního plazmocytomu po provedení radioterapie nebo chirurgickém výkonu z důvodu nedostatečného množství dat k vyhodnocení účinnosti postupu. Výjimkou je stále aktivní ložisko po radioterapii zhodnocené PET/CT (stupeň doporučení C, úroveň důkazu IV).
Doporučení pro podávání bisfosfonátů
- Dlouhodobé léčebné podávání bisfosfonátů nebo denosumabu je doporučováno všem pacientům s nepochybnou diagnózou symptomatický mnohočetný myelom (stupeň doporučení A, úroveň důkazu Ia).
- Podávání bisfosfonátů je možné i u nemocných s mnohočetným myelomem v asymptomatické fázi nemoci. Neoddálí přechod v symptomatický mnohočetný myelom, ale v době diagnózy přechodu do symptomatického myelomu budou menší projevy kostního postižení. Je na ošetřujícím lékaři, aby individuálně vyhodnotil přínos časného nasazení bisfosfonátů oproti rizikům plynoucím z dlouhodobého podávání (stupeň doporučení A, úroveň důkazu Ia).
- Za účinnou léčbu lze považovat podávání perorální nebo parenterální formy klodronatu, parenterální formy pamidronatu a zoledronatu (stupeň doporučení A, úroveň důkazu Ib). Ibandronat je dalším účinným bisfosfonátem s průkazem u solidních nádorů, s jednou randomizovanou studií u mnohočetného myelomu
- Klodronat lze podávat perorálně, nejnižší denní dávka jakéhokoliv preparátu klodronatu s dokumentovanou účinností je 1 600 mg, při dobré toleranci lze podávat i 2 400 mg. Ekvivalentní nitrožilní dávka klodronatu je 900 mg i. v. infuze 1x za 14 dní (stupeň doporučení A, úroveň důkazu Ia).
- Pamidronat se podává v dávce 90 mg i.v. 1x za 3–4 týdny, případně 60 mg 1x za 14 dní) (stupeň doporučení A, úroveň důkazu Ib).
- Zoledronat se podává v dávce 4 mg i. v. infuzi 1x za 3–4 týdny (stupeň doporučení A, úroveň důkazu Ib). Intervaly lze prodloužit na 2–3 měsíce.
- Ibandronat se podává v dávce 6 mg v i. v. infuzi 1x za 3–4 týdny. Alternativou je 50 mg p. o. denně (stupeň doporučení C, úroveň doporučení IV).
- Denosumab se podává v dávce 120 mg s. c. 1x za 4 týdny (stupeň doporučení A, úroveň důkazu Ib).
- Výběr preparátu závisí na preferenci pacienta a lékaře a stavu organismu před léčbou, zvláště s ohledem na poškození ledvin a možnost vzniku osteonekrózy.
- Doba podávání bisfosfonátů u pacientů, kteří dosáhnou kompletní remise nebo velmi dobré parciální remise, by měla přesáhnout jeden rok od dosažení této léčebné odpovědi, ale neměla by být delší než dva roky od dosažení léčebných odpovědí (stupeň doporučení C, úroveň doporučení IV).
- V případě nedosažení ani velmi dobré parciální remise a trvání osteolytické aktivity nemoci může být podávání bisfosfonátů dlouhodobé.
- Opatrnost a úprava dávek těchto preparátů, zvláště pak zolendronatu, je nutná při středním a závažném selhání ledvin (stupeň doporučení A, úroveň důkazu Ib).
- Před zahájením léčby bisfosfonáty je vždy nutné zvážit riziko případné osteonekrózy. Zejména u pacientů s vyšším rizikem osteonekrózy čelisti, u kterých nelze očekávat možnost zajištění komplexní stomatologické péče, raději léčbu bisfosfonáty oddálit či vůbec nezahajovat. Tuto situaci je nutno vždy s pacientem individuálně prodiskutovat (stupeň doporučení C, úroveň doporučení IV).
DOPORUČENÍ PRO PREVENCI VZNIKU OSTEONEKRÓZY U NEMOCNÝCH S MNOHOČETNÝM MYELOMEM PŘI SOUČASNÉ LÉČBĚ DUSÍK OBSAHUJÍCÍMI BISFOSFONÁTY
Doporučení pro pacienty
- Je nezbytné informovat nemocné o možnosti vzniku osteonekrózy čelisti (ONČ) při léčbě dusík obsahující bisfosfonáty.
- Před zahájením léčby je nezbytné provedení panoramatického snímku čelisti, stomatologického vyšetření s výhledem na 2–3 roky a případné sanace fokusů infekce, či problémových zubů.
- Vhodné je informovat nemocné o nutnosti zvýšené hygieny dutiny ústní.
- Nemocný musí být poučen, že má vždy neprodleně informovat lékaře o jakémkoliv výkonu zubaře v dutině ústní, zvláště pak stomatochirurgickém výkonu (nejčastěji vytržení zubu).
- Před každým podáním bisfosfonátu obsahující dusík je vhodné, aby se zdravotnický personál přesvědčil, že nemocný neměl proveden stomatologický výkon nebo výkon není plánován. (stupeň doporučení C, úroveň důkazů IV)
Doporučení při stomatochirurgickém výkonu
- Stomatochirurgický výkon (prosté vytržení zubu) se doporučuje provádět s antibiotickou profylaxí (například Augmentin či Amoksilav á 1g – 2 tablety 2 hodiny před samotným výkonem a poté 2 x 1g á 12 hod. po dobu 10–14 dnů). Při alergii na peniciliny lze použít např. Rovamycin 1-0-1, nebo Dalacin. (stupeň doporučení B, úroveň důkazů III)
- Po 14 dnech je doporučeno provést kontrolní stomatologické vyšetření. Pokud není rána zhojena do 14 dnů, je vhodné provést mikrobiologické vyšetření, případně změnu antibiotika. (stupeň doporučení B, úroveň důkazů III)
- Je vhodné zvýšeně pečovat o hygienu dutiny ústní (například 3–4krát denně mezi jídly kloktat chlorhexidin (Corsodyl) do zhojení rány).
- Je doporučeno provedení plánovaného výkonu s určitým odstupem od poslední infuze dusík obsahujícího bisfosfonátu. Doba není přesně stanovena, pokud výkon není urgentní, doporučuje se 2–3 měsíce před plánovanou extrakcí přerušit podávání bisfosfonátů. (stupeň doporučení B, úroveň důkazů III)
- Je doporučeno znovu zahájit podávání dusík obsahujících bisfosfonátů po úplném zhojení rány. Rovněž zde není doba přesně stanovena, dva měsíce je doba dostatečná. (stupeň doporučení B, úroveň důkazů III)
Doporučení pro léčbu anémie
- U každého pacienta s anémií je třeba standardně provést diferenciální diagnostiku příčiny anémie.
- Pokud není nalezena jiná příčina anémie a anémie odpovídá anémii chronických chorob při mnohočetném myelomu, je v případě klinických příznaků (obvykle při hodnotách hemoglobinu nižších než 100 g/l) možné zvážit léčbu humánním rekombinantním erytropoetinem.
- Léčebný test s preparátem stimulujícím erytropoézu je na zvážení u všech nemocných s mnohočetným myelomem a symptomatickou anémií. Indikace musí korespondovat s obecnými indikacemi pro léčbu erytropoetinem vydanými Českou hematologickou společností (stupeň doporučení A úroveň důkazu 1b).
- Erytropoetin je indikovaný k léčbě anémie u pacientů s myelomem a chronickým renálním selháním (stupeň doporučení A úroveň důkazu 1b).
DOPORUČENÝ POSTUP PRO PROFYLAXI TROMBOTICKÝCH KOMPLIKACÍ U PACIENTŮ S MNOHOČETNÝM MYELOMEM
- U pacientů bez rizikových faktorů TEN*, kteří jsou léčeni režimy neobsahujícími IMiDy ani kombinaci anthracyklinu s vysoko dávkovaným dexametazonem, není nutná žádná farmakologická tromboprofylaxe, doporučena jsou jen režimová opatření (mobilizace, cvičení, řádná hydratace, kompresní punčochy) (úroveň důkazu IV, stupeň doporučení C).
- U všech ostatních pacientů je doporučena farmakologická tromboprofylaxe. Je u nich možné použít LMWH v profylaktické dávce (enoxaparin 40 mg, bemiparin 3500 j, dalteparin 5000 j, nadroparin u osob s hmotností do 50 kg 0,3 ml, u osob s hmotností 50–69 kg 0,4 ml, u osob s hmotností nad 70 kg 0,6 ml – vše 1x denně.)
- U pacientů bez dalších rizikových faktorů TEN* lze po dosažení parciální remise považovat za srovnatelně účinný postup ASA 100 mg denně nebo warfarin v terapeutické dávce (úroveň důkazu Ib, stupeň doporučení A pro 1. linii léčby, úroveň důkazu IV, stupeň doporučení C pro další linie léčby).
- U pacientů s velmi vysokým rizikem (TEN v anamnéze, nově diagnostikovaný MM léčený kombinací IMiDu nebo anthracyklinu s pulsním dexametazonem) je možné podat intermediární dávku LMWH (nadroparin, enoxaparin, dalteparin) 100 IU/kg 1x denně (úroveň důkazu IIa, stupeň doporučení B)
- U pacientů bez dalších rizikových faktorů TEN* léčených pro relaps MM IMiDy v kombinaci s nízkou dávkou kortikoidů nebo v monoterapii je možné od počátku podávat ASA místo LMWH.
- U pacientů léčených warfarinem nebo některým z přímých orálních antikoagulancií (dabigatran, rivaroxaban, apixaban, edoxaban) z jiné indikace je možné tuto léčbu ponechat, neboť lze předpokládat dostatečný tromboprofylaktický efekt těchto léků během léčby MM.
- Při léčbě warfarinem je třeba častěji kontrolovat INR, při léčbě přímými orálními antikoagulancii je třeba kontrolovat renální funkce a respektovat jejich kontraindikaci při renální insuficienci podle SPC.
- *Za rizikové faktory TEN jsou považovány: upoutání na lůžko, imobilizace končetiny, infekce, srdeční selhání NYHA III–IV, otoky DK, respirační insuficience, paréza nebo plegie končetiny, zavedený centrální žilní katétr, obezita, známá vrozená nebo získaná trombofilní laboratorní odchylka, duplicitní malignita, současná léčba estrogeny, současná léčba erytropoetinem nebo jeho deriváty.
PROFYLAKCE INFEKČNÍCH NEMOCÍ – DOPORUČENÍ
- Profylaktické podávání antibiotik s cílem snížit četnost infekčních komplikací není při běžné chemoterapii (CTD, VMP, RP) doporučeno.
- U režimů s vysokými dávkami kortikoidů (nad 20 mg prednisonu po déle než 4 týdny nebo ekvivalent podle NCCN) se doporučuje profylaxe pneumocystové pneumonie (stupeň doporučení B úroveň důkazu IIb).
- Při standardní chemoterapii mnohočetného myelomu není primárně profylaktické podávání antimykotik standardním postupem. V případě vzniku slizniční mykózy v průběhu léčby je však vhodné podávat v dalších cyklech profylakticky antimykotikum (flukonazol) (stupeň doporučení C, úroveň důkazu III pro redukci mortality při ASCT).
- Antivirová profylaxe acyklovirem je indikovaná u pacientů léčených inhibitory proteazomu a lenalidomidem (stupeň doporučení A, úroveň důkazu IIb). Dávku acykloviru je možné bezpečně zredukovat až na dávku 1x 200–400 mg s uspokojivým profylaktickým efektem (stupeň doporučení B, úroveň důkazu IIb)
- U dlouhodobě neutropenických pacientů (nad 7 dní očekávané neutropenie – u MM prakticky pouze u ASCT) je doporučena profylaxe fluorochinolonem a flukonazolem s přihlédnutím k lokální epidemiologické situaci daného pracoviště, u krátkodobě neutropenických pacientů s MM lze zvážit i bez profylaxe (stupeň doporučení A, úroveň důkazu Ia).
- Po autologní transplantaci je doporučena profylaxe acyklovirem a trimetoprim-sulfamethoxazol po dobu aspoň 30 dní (stupeň doporučení A, úroveň důkazu IIa podle NCCN).
- Vakcinace pacientů je možná neživými vakcínami, mimo standardní očkování (tetanus,...) není jiné očkování rutinně doporučeno, vhodné je každoroční očkování proti sezónní chřipce (stupeň doporučení C, úroveň důkazu obecně III, influenza IIa).
- Před nasazením léčby lenalidomidem (pomalidomidem) je nutné sérologické vyšetření viru hepatitidy B (stupeň doporučení C, úroveň důkazu III)
DOPORUČENÍ PRO SLEDOVÁNÍ PACIENTŮ S MGUS A PRO STRATIFIKACI RIZIKA PŘECHODU V MM
- Po vyloučení jiného typu MG musí být pro stanovení diagnózy MGUS splněna kritéria podle IMWG z roku 2016 (stupeň doporučení C, úroveň důkazu IV).
- Optimálním diagnostickým výstupem je zápis obsahující: typ Ig paraproteinu, určení rizika transformace s doporučenou frekvencí sledování (stupeň doporučení C, úroveň důkazu IV).
- Doporučený panel vyšetření v rámci sledování zahrnuje: krevní obraz, základní biochemické vyšetření zahrnující stanovení sérových koncentrací urey, kreatinu, vápníku, celkové bílkoviny, C - reaktivního proteinu, beta2-mikroglobulinu, albuminu, laktátdehydrogenázy, jaterních enzymů, glukózy, dále kvantitativní stanovení imunoglobulinů a FLC v séru včetně stanovení jejich poměru, elektroforézu, případně imunofixaci séra a moči. Vyšetření kostní dřeně je doporučeno u IgG MGUS v případě sérového M-proteinu ≥15 g/l a u všech IgA a IgM typů MGUS. Zobrazovací vyšetření není běžně doporučováno u pacientů s M-proteinem typu IgG ≤15 g/l a při M-proteinu typu IgA ≤10 g/l bez kostních bolestí. U všech ostatních pacientů je vhodné provedení RTG celého skeletu, resp. dnes spíše „low-dose“ CT, případně celotělového MRI, PET/CT či PET/MRI vyšetření (stupeň doporučení C, úroveň důkazu IV).
- Frekvence sledování v prvním roce upřesňuje dynamiku MGUS (interval 2-4 měsíce). Kontrolní vyšetření od druhého roku sledování jsou v intervalech od 2–4 měsíců do 12–18 měsíců v závislosti na míře rizika transformace. Minimální interval jednoho roku mezi kontrolami je optimální dobou z praktického hlediska (stupeň doporučení C, úroveň důkazu IV).
Štítky
Hematologie a transfuzní lékařství Interní lékařství Onkologie
Článek Úvodní slovoČlánek 7 LÉČEBNÉ STRATEGIE
Článek vyšel v časopiseTransfuze a hematologie dnes
Nejčtenější tento týden
2018 Číslo Supplementum1- Není statin jako statin aneb praktický přehled rozdílů jednotlivých molekul
- Magnosolv a jeho využití v neurologii
- Moje zkušenosti s Magnosolvem podávaným pacientům jako profylaxe migrény a u pacientů s diagnostikovanou spazmofilní tetanií i při normomagnezémii - MUDr. Dana Pecharová, neurolog
- Nejlepší kůže je zdravá kůže: 3 úrovně ochrany v moderní péči o stomii
- S prof. Vladimírem Paličkou o racionální suplementaci kalcia a vitaminu D v každodenní praxi
-
Všechny články tohoto čísla
-
8 Léčba mnohočetného myelomu
8. 9 Panobinostat -
8 Léčba mnohočetného myelomu
8. 10 Bendamustin -
8 Léčba mnohočetného myelomu
8. 11 Alkylační a jiná cytostatika, glukokortikoidy - 9 VYSOKODÁVKOVANÁ CHEMOTERAPIE S TRANSPLANTACÍ AUTOLOGNÍCH KMENOVÝCH BUNĚK
- 10 ALOGENNÍ TRANSPLANTACE KRVETVORNÝCH BUNĚK
- 11 UDRŽOVACÍ A KONSOLIDAČNÍ LÉČBA
- 12 LÉČBA MNOHOČETNÉHO MYELOMU U NEMOCNÝCH SE SELHÁNÍM FUNKCE LEDVIN
- 13 VYBRANÉ OBLASTI Z KOMPLEXNÍ PODPŮRNÉ LÉČBY MNOHOČETNÉHO MYELOMU
- 14 LÉKY INHIBUJÍCÍ OSTEOLÝZU U PACIENTŮ S MNOHOČETNÝM MYELOMEM V ROCE 2018
- 15 KOMPLEXNÍ PODPŮRNÁ LÉČBA – ANÉMIE
- 16 PROFYLAXE TROMBOEMBOLICKÉ NEMOCI U PACIENTŮ S MNOHOČETNÝM MYELOMEM
- 17 PROFYLAXE INFEKČNÍCH KOMPLIKACÍ
- 18 MONOKLONÁLNÍ GAMAPATIE NEJASNÉHO VÝZNAMU (MGUS): DOPORUČENÍ PRO SLEDOVÁNÍ A PRO STRATIFIKACI RIZIKA PŘECHODU V MNOHOČETNÝ MYELOM
- 19 REÁLNÁ DATA O LÉČBĚ Z REGISTRU MONOKLONÁLNÍCH GAMAPATIÍ
- 1 METODICKÉ POSTUPY TVORBY DOPORUČENÍ
- 2 EPIDEMIOLOGIE MNOHOČETNÉHO MYELOMU
- 3 NEJČASTĚJŠÍ PROJEVY NEMOCI A VYŠETŘENÍ VEDOUCÍ K ROZPOZNÁNÍ A KE STANOVENÍ ROZSAHU NEMOCI
- 4 KRITÉRIA PRO STANOVENÍ DIAGNÓZY MNOHOČETNÉHO MYELOMU A JEHO KLINICKÉHO STADIA, KRITÉRIA DALŠÍCH PLAZMOCELULÁRNÍCH CHOROB
- 5 KRITÉRIA PRO HODNOCENÍ LÉČEBNÉHO EFEKTU A DLOUHODOBÉ ÚSPĚŠNOSTI LÉČBY
- 6 OBECNÉ INFORMACE O LÉČBĚ MNOHOČETNÉHO MYELOMU
- 7 LÉČEBNÉ STRATEGIE
- Úvodní slovo
-
8 Léčba mnohočetného myelomu
8. 1 Thalidomid -
8 Léčba mnohočetného myelomu
8. 2 Lenalidomid - DIAGNOSTIKA A LÉČBA MNOHOČETNÉHO MYELOMU
-
8 Léčba mnohočetného myelomu
8. 3 Pomalidomid -
8 Léčba mnohočetného myelomu
8.4 BORTEZOMIB -
8 Léčba mnohočetného myelomu
8. 5 Karfilzomib -
8 Léčba mnohočetného myelomu
8. 6 Ixazomib -
8 Léčba mnohočetného myelomu
8. 7 Daratumumab -
8 Léčba mnohočetného myelomu
8. 8. Elotuzumab
-
8 Léčba mnohočetného myelomu
- Transfuze a hematologie dnes
- Archiv čísel
- Aktuální číslo
- Pouze online
- Informace o časopisu
Nejčtenější v tomto čísle- DIAGNOSTIKA A LÉČBA MNOHOČETNÉHO MYELOMU
- 3 NEJČASTĚJŠÍ PROJEVY NEMOCI A VYŠETŘENÍ VEDOUCÍ K ROZPOZNÁNÍ A KE STANOVENÍ ROZSAHU NEMOCI
- 11 UDRŽOVACÍ A KONSOLIDAČNÍ LÉČBA
- 18 MONOKLONÁLNÍ GAMAPATIE NEJASNÉHO VÝZNAMU (MGUS): DOPORUČENÍ PRO SLEDOVÁNÍ A PRO STRATIFIKACI RIZIKA PŘECHODU V MNOHOČETNÝ MYELOM
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



