-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Cirkulující nádorová DNA jako biomarker pro predikci minimální reziduální nemoci a individualizaci adjuvantní léčby kolorektálního karcinomu – přehled současných poznatků a perspektiv
Circulating tumor DNA as a biomarker for the prediction of minimal residual disease and the individualization of adjuvant therapy in colorectal cancer – a review of current evidence and perspectives
Background: Colorectal cancer (CRC) remains one of the most common malignancies in the Czech Republic. Despite advances in surgical treatment, the risk of recurrence persists, mainly due to minimal residual disease (MRD). Current surveillance strategies, including colonoscopy, CT imaging, and serum tumor markers (CEA, CA19-9), demonstrate limited sensitivity and specificity. In recent years, circulating tumor DNA (ctDNA) has emerged as a promising biomarker with significant prognostic and predictive potential. Methodology: This review was prepared based on a systematic literature search in PubMed, Web of Science, ScienceDirect, Scopus, and clinicaltrials.gov covering the period 2005–2025. Observational studies, retrospective analyses, and randomized clinical trials evaluating the prognostic and predictive role of ctDNA in patients with CRC were included. Results: Available studies confirm that the presence of ctDNA after curative resection of CRC is a strong predictor of early recurrence and worse survival, whereas ctDNA negativity reliably identifies patients at low risk. Prospective projects (VICTORI, GALAXY, COSMOS) demonstrated that ctDNA can predict relapse several months earlier than standard methods. The BESPOKE CRC study highlighted that only patients with positive ctDNA significantly benefit from adjuvant chemotherapy. The randomized DYNAMIC trial proved that a ctDNA-guided approach enables safe de-escalation of adjuvant therapy without compromising outcomes. Ongoing studies (PEGASUS, SAGITTARIUS, TRACC, DYNAMIC-III, ALTAIR, VEGA) are testing the efficacy of escalation and de-escalation strategies. Conclusions: ctDNA is a highly promising biomarker for early MRN detection, risk stratification, and the individualization of adjuvant therapy in CRC patients. Its implementation in routine clinical practice, however, requires confirmation from ongoing randomized trials and validation in the Czech setting, where the use of ctDNA currently remains limited primarily to research.
Keywords:
colorectal cancer – Adjuvant chemotherapy – Circulating tumor DNA – liquid biopsy – minimal residual disease – personalized oncology
Autoři: A. Pirshtuk 1; T. Büchler 1; V. Vymetálková 2
Působiště autorů: Onkologická klinika 2. LF UK a FN Motol a Homolka, Praha 1; Oddělení molekulární biologie nádorů, Ústav Experimentální medicíny AV ČR, Praha 2
Vyšlo v časopise: Klin Onkol 2026; 39(2): 105-111
Kategorie: Přehled
doi: https://doi.org/10.48095/ccko2026105Souhrn
Východiska: Kolorektální karcinom (KRK) zůstává jednou z nejčastějších malignit v ČR. Přes pokroky v chirurgické léčbě přetrvává vysoké riziko recidivy, zejména v důsledku minimální reziduální nemoci (MRN). Stávající postupy sledování, zahrnující kolonoskopii, CT vyšetření a sérové nádorové markery (CEA, CA19-9), vykazují omezenou senzitivitu a specificitu. Cirkulující nádorová DNA (ctDNA) se v posledních letech prosazuje jako perspektivní biomarker s významným prognostickým a prediktivním potenciálem. Metodologie: Článek byl zpracován na základě systematického vyhledávání literatury v databázích PubMed, Web of Science, ScienceDirect, Scopus a clinicaltrials.gov v období 2005–2025. Zahrnuty byly observační studie, retrospektivní analýzy a randomizovaná klinická hodnocení hodnotící prognostický a prediktivní význam ctDNA u pacientů s KRK. Výsledky: Dostupné studie potvrzují, že přítomnost ctDNA po kurativní resekci KRK je silným prediktorem časné recidivy a horšího přežití, zatímco její negativita identifikuje pacienty s nízkým rizikem. Prospektivní projekty (VICTORI, GALAXY, COSMOS) ukázaly, že ctDNA dokáže předpovědět relaps s několikaměsíčním předstihem oproti standardním metodám. Studie BESPOKE CRC zdůraznila, že z adjuvantní chemoterapie profitují zejména pacienti s pozitivní ctDNA. Randomizovaná studie DYNAMIC prokázala, že ctDNA řízený přístup umožňuje deeskalaci adjuvantní terapie bez negativního vlivu na výsledky. Probíhající studie (PEGASUS, SAGITTARIUS, TRACC, DYNAMIC-III, ALTAIR, VEGA) testují efektivitu eskalačních a deeskalačních strategií. Závěr: ctDNA představuje vysoce slibný biomarker pro časnou detekci MRN, stratifikaci rizika a individualizaci adjuvantní terapie u pacientů s KRK. Její zavedení do klinické praxe však vyžaduje potvrzení výsledků v probíhajících randomizovaných studiích a validaci v českých podmínkách, kde je využití ctDNA zatím omezeno převážně na výzkumnou sféru.
Klíčová slova:
kolorektální karcinom – cirkulující nádorová DNA – tekutá biopsie – minimální reziduální nemoc – adjuvantní chemoterapie – personalizovaná onkologie
Úvod
Kolorektální karcinom (KRK) patří dlouhodobě mezi nejčastější malignity v ČR, přičemž každoročně postihuje přibližně 7 200 pacientů [1]. Navzdory pokroku v chirurgických technikách, včetně zavedení robotické chirurgie, přetrvává riziko rekurence onemocnění po radikální resekci v rozmezí 14–35 % [2]. Zásadní výzvou se proto stává včasná identifikace pacientů s vysokým rizikem relapsu, a to i po kurativní operaci. Rekurence se nejčastěji objevuje v průběhu prvních 3 let po výkonu [3], což nasvědčuje přítomnosti tzv. minimální reziduální nemoci (MRN), která může perzistovat i po makroskopicky radikální resekci.
Současné doporučené postupy sledování pacientů po operaci KRK zahrnují pravidelné kolonoskopické kontroly, které však bývají pacienty odmítány z důvodu invazivity, náročné přípravy či komorbidit. Další metodou je pravidelné CT vyšetření, jehož opakované provádění však přináší potenciální radiační zátěž [4]. Doplněním sledování jsou sérové nádorové markery, jako např. karcinoembryonální antigen (carcinoembryonic antigen – CEA). Retrospektivní analýzy však ukazují, že senzitivita CEA u pacientů po resekci KRK stadia II se pohybuje v rozmezí 32–53 %, zatímco u stadia III dosahuje 46–59 % [5,6]. Senzitivita CA 19-9 je ještě nižší, 20–30 % [6,7]. Významná pozitivní prediktivní hodnota těchto markerů byla zaznamenána převážně u pacientů s jejich předoperační elevací [7,8].
Randomizovaná klinická studie FACS porovnávala různé sledovací strategie – izolované monitorování pomocí CEA, CT, jejich kombinaci a minimální sledování. Studie ukázala, že pravidelné CT vyšetření vedlo k vyšší detekci rekurencí (65 %) ve srovnání se samotným CEA (32,5 %), přičemž kombinace obou metod nepřinesla signifikantní přínos [9].
Uvedené skutečnosti zdůrazňují potřebu zavedení nových, spolehlivějších biomarkerů, které by umožnily časnou detekci rekurence. V této souvislosti nabývá na významu tzv. tekutá biopsie – detekce nádorových biomarkerů v periferní krvi nebo jiných tělesných tekutinách (moč, sliny, stolice, mozkomíšní mok) [10]. Mezi nejvýznamnější biomarkery patří cirkulující nádorová DNA (ctDNA), cirkulující nádorové buňky (CTCs), nekódující mRNA molekuly, např. mikroRNA a dlouhé nekódující RNA, extracelulární vezikuly a nádorové proteiny [11].
Ze zmíněných biomarkerů vykazuje právě ctDNA značný potenciál při detekci molekulární reziduální nemoci a predikci časné recidivy KRK. Jde o krátké fragmenty DNA uvolněné z nádorové tkáně do periferní krve, zejména u pokročilých stadií onemocnění. K detekci se využívají vysoce senzitivní molekulárně biologické metody – kvantitativní PCR (qPCR), digitální PCR (dPCR) a sekvenování nové generace (next generation sequencing – NGS), které umožňují zachytit i velmi nízké hladiny nádorové DNA [12].
Výsledky mezinárodních studií ukazují, že ctDNA umožňuje identifikaci pacientů s vysokým rizikem relapsu dříve než konvenční sledovací metody a zároveň usnadňuje deeskalaci terapie u MRN-negativních pacientů bez zhoršení klinických výsledků. Ve vybraných zahraničních centrech se tak ctDNA postupně začleňuje do algoritmů léčby a sledování. V ČR je však její využití zatím omezeno na výzkumnou úroveň, přesto její potenciál zůstává nesporný.
Cílem tohoto článku je podat souhrnný přehled aktuálních poznatků o využití ctDNA v managementu pacientů s KRK, se zvláštním důrazem na její prognostickou hodnotu a roli při rozhodování o adjuvantní terapii.
Metodologie
Tento přehledový článek byl zpracován na základě systematického vyhledávání relevantních prací v databázích PubMed, Web of Science, ScienceDirect, Scopus a clinicaltrials.gov, a to za období od ledna 2005 do srpna 2025. Přednost byla dána observačním studiím, randomizovaným klinickým studiím a retrospektivním analýzám zahrnujícím pacienty s lokálně pokročilým nebo metastatickým kolorektálním karcinomem. Zařazeny byly práce, které hodnotily detekci a měření ctDNA (pozitivita/negativita) v různých časových bodech, s použitím validovaných metod, publikované v anglickém jazyce.
Typy testů: tumor informovaný vs. tumor agnostický
V detekci MRN se uplatňují dva hlavní přístupy [13]:
Tumor informovaný (tumor-informed) vyžaduje počáteční sekvenování nádorové tkáně konkrétního pacienta k identifikaci somatických mutací, které se následně sledují v periferní krvi. Tento přístup vykazuje vyšší senzitivitu a specificitu pro predikci recidivy a disponuje silnější prognostickou hodnotou [13]. Nevýhodou je nutnost tkáňových vzorků, časová náročnost a vyšší cena.
Tumor agnostický (tumor-agnostic) vychází z předdefinovaných panelů genetických či epigenetických změn detekovaných přímo z plazmy. Jeho výhodou je širší použitelnost a nezávislost na dostupnosti původní nádorové tkáně. Nevýhodou bývá nižší senzitivita a prognostická hodnota [14].
Rozlišení těchto strategií je zásadní, protože volba metody má přímý dopad na interpretaci výsledků, srovnatelnost klinických studií a potenciální implementaci ctDNA testování do rutinní praxe.
Prognostická role detekce minimální reziduální nemoci
Otázka, zda ctDNA může být spolehlivým prognostickým markerem po kurativní resekci KRK, byla zkoumána již před více než 20 lety [15,16], avšak převážně v rámci retrospektivních studií [17]. Prospektivní práce Diehla et al. (2008) ukázala, že ctDNA byla zjistitelná u všech pacientů se stadii II–IV KRK před operací a že její přetrvávání po chirurgickém výkonu predikovalo rekurenci do jednoho roku. ctDNA se zároveň ukázala jako citlivější marker než CEA [18].
Na tento koncept navázala řada studií zaměřených na kvantitativní i kvalitativní hodnocení ctDNA a na identifikaci konkrétních mutací odrážejících heterogenitu nádorové populace (tab. 1) [12]. Klinicky významná studie IDEA, primárně zaměřená na stanovení optimální délky adjuvantní léčby pacientů se stadiem III KRK, navíc zahrnovala i analýzu ctDNA pomocí tumor informovaného panelu Signatera (Natera Inc.). ctDNA byla po resekci detekovatelná u 19,7 % pacientů. Pětileté přežití bez recidivy (disease-free survival – DFS) činilo 33,1 % u ctDNA pozitivních oproti 81,0 % u ctDNA negativních pacientů. Pětileté celkové přežití (overall survival – OS) bylo 52,7 % vs. 89,4 % (HR 5,31; 95% CI 3,75–7,51; p < 0,0001). Analýzy dále ukázaly, že délka chemoterapie měla významný vliv u pacientů s pozitivní ctDNA, zejména ve skupině s nízkým klinickým rizikem (T1-3/N1), kde 2leté DFS bylo dvojnásobně vyšší u pacientů, kteří podstoupili 6měsíční adjuvantní chemoterapie (ACT) oproti 3měsíční (66,7 % vs. 31,6 %) [19].
Tab. 1. Studie zaměřené na výzkum prognostické role detekce minimální reziduální nemoci u pacientů s kolorektálním karcinomem. 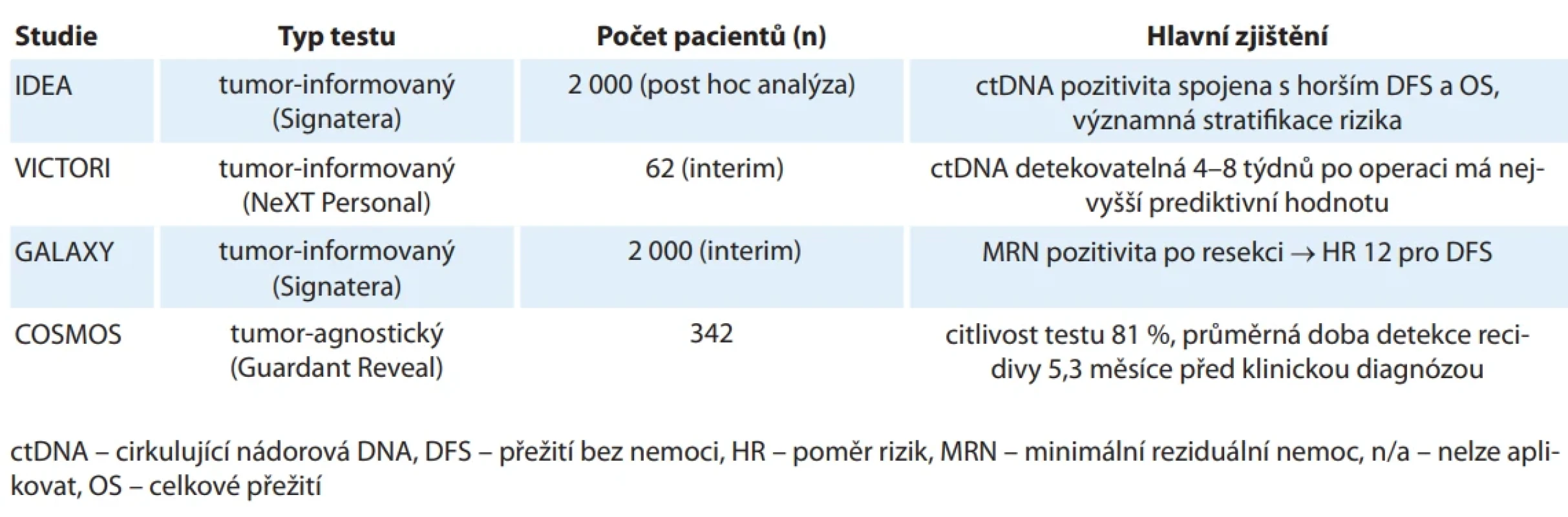
Z prospektivních studií, které se přímo věnují zkoumání prognostické role ctDNA, stojí za zmínku kanadská studie VICTORI a rozsáhlá japonská studie GALAXY. GALAXY je observační částí projektu CIRCULATE-Japan, v jehož rámci probíhají také dvě randomizované kontrolované studie fáze III – VEGA a ALTAIR – zkoumající efektivitu strategií eskalace a deeskalace adjuvantní léčby v závislosti na ctDNA statusu po radikálním chirurgickém výkonu [20].
V obou studiích, tedy VICTORI i GALAXY, je využíván tumor informovaný přístup k monitoraci ctDNA u pacientů s KRK stadia I–IV po kurativní resekci. Studie VICTORI používá panel NeXT Personal, který umožňuje analyzovat až 1 800 unikátních tumor specifických mutací zjištěných pomocí WGS z primárního nádoru konkrétního pacienta [21]. Analýza ctDNA se provádí před operací, poté každé 2 týdny v období 2–8 týdnů po resekci a následně v delších intervalech až do 3 let sledování. Díky tomu je možné extrémně citlivé monitorování ctDNA v periferní krvi. Metodologicky je tato studie zaměřena na detailní sledování kinetiky ctDNA s cílem stanovit optimální časový rámec pro detekci MRN po operaci a předvídání recidivy.
Ačkoliv studie stále probíhá, v lednu 2025 již byly publikovány interim výsledky po roce sledování kohorty 60 pacientů léčených ve Vancouver Cancer Centre. Tyto výsledky ukázaly, že detekce ctDNA v tzv. landmark okně mezi 4. a 8. týdnem po operaci měla nejvyšší prediktivní hodnotu pro následnou recidivu – HR 12,86 (95% CI 2,74–60,28, p = 0,0012) pro 4. týden; HR 16,14 (95% CI 3,52–74,09; p = 0,0004) pro 8. týden. U pacientů s prokázanou recidivou (15 z 60 hodnocených, tj. 25 %) byla přítomnost ctDNA detekovatelná v mediánu 194 dní (rozmezí 5–397) před radiologickým průkazem onemocnění. Koncentrace ctDNA při první detekci se u 64,3 % pacientů s recidivou pohybovala v ultra low rozmezí (< 100 ppm). Tyto výsledky potvrzují vysokou senzitivitu a prognostický význam testu a zároveň navrhují optimální landmark okno pro stanovení MRN v intervalu 4–8 týdnů po operaci [22].
Japonská studie GALAXY, jejíž nejaktuálnější předběžné výsledky byly publikovány na podzim 2024, na rozdíl od VICTORI využívá méně citlivý 16variantní panel Signatera. Vyniká však rozsáhlostí – zahrnuje kolem 6 000 pacientů z 157 center, převážně v Japonsku. Odběry jsou prováděny před neoadjuvantní léčbou a/nebo resekcí, dále 4 týdny po resekci a následně každé 3 měsíce. Cílem je vyhodnotit vliv pozitivity ctDNA po operaci na DFS a OS. Interim analýza zahrnula 2 109 pacientů s KRK stadia II–IV a mediánem sledování 23 měsíců. MRN status byl stanoven 4 týdny po resekci. MRN pozitivních bylo 15,93 % (336/2109). Z této MRN pozitivní skupiny recidivovalo 78,27 % pacientů (263/336), zatímco u MRN negativních (1 773 pacientů) zaznamenalo recidivu pouze 13,14 % pacientů (233/1773). V souladu s výsledky jiných studií tato data potvrzují, že přítomnost ctDNA v periferní krvi po operaci je silným prediktorem recidivy (HR 11,99; 95% CI 10,02–14,35; p < 0,0001). Dále se ukázalo, že ctDNA pozitivita byla významně spojena s kratším OS ve srovnání s ctDNA negativními pacienty (HR 9,68; 95% CI 6,33–14,82; p < 0,0001). Tříleté OS činilo 71,80 % (95% CI 63,40–78,60 %; p < 0,0001) oproti 96,0 % (95% CI 94,30–97,20 %; p < 0,0001). U pacientů, kteří prodělali recidivu, byla pozitivita ctDNA v době záchytu recidivy spojena s kratším OS (HR 2,71; 95% CI 1,64–4,47; p < 0,0001).
Studie zároveň sledovala prognostický význam clearance ctDNA po ACT. Trvalé vymizení ctDNA v reakci na ACT bylo spojeno s příznivější prognózou oproti přechodnému vymizení. Dvouleté DFS činilo 89,0 % oproti 3,3 % a 2leté OS 100,0 % oproti 82,3 % [23,24].
Další významné výsledky přinesla studie COSMOS, která využívá tumor agnostický test Guardant Reveal. Tento test je unikátní tím, že nevyžaduje analýzu primární nádorové tkáně, ale zaměřuje se na více než 20 000 epigenomických oblastí přímo v plazmě [25].
Studie zahrnovala longitudinální sledování 342 pacientů s KRK stadia I–III a analyzovala více než 1 900 vzorků plazmy odebraných po operaci. Výsledky ukázaly vysokou citlivost i specificitu pro predikci recidivy v různých časových bodech po chirurgickém zákroku. Průměrná doba předstihu detekce recidivy pomocí ctDNA činila 5,3 měsíce před klinickým potvrzením.
Senzitivita dosahovala 81 % u pacientů s KRK stadia II a vyššího. Nejvyšší byla při detekci jaterních metastáz (100 %), nižší u metastáz plicních (53 %) a peritoneálních (40 %). Tyto výsledky potvrzují, že i tumor agnostický přístup může poskytovat relevantní klinické informace a představuje dostupnější variantu monitorování MRN [26].
Výše zmíněné studie potvrzují slibný potenciál ctDNA jako neinvazivního biomarkeru, který umožňuje přesnější rizikovou stratifikaci, sledování účinnosti léčby a časnou detekci recidivy v reálném čase u pacientů s KRK po chirurgické léčbě. Tyto výsledky zároveň vytvořily základ pro další prospektivní studie zaměřené na hodnocení efektivity a bezpečnosti ctDNA řízených přístupů při rozhodování o strategii adjuvantní léčby (tab. 2).
Tab. 2. Studie zkoumající roli využití ctDNA v řízení léčby pacientů s kolorektálním karcinomem. 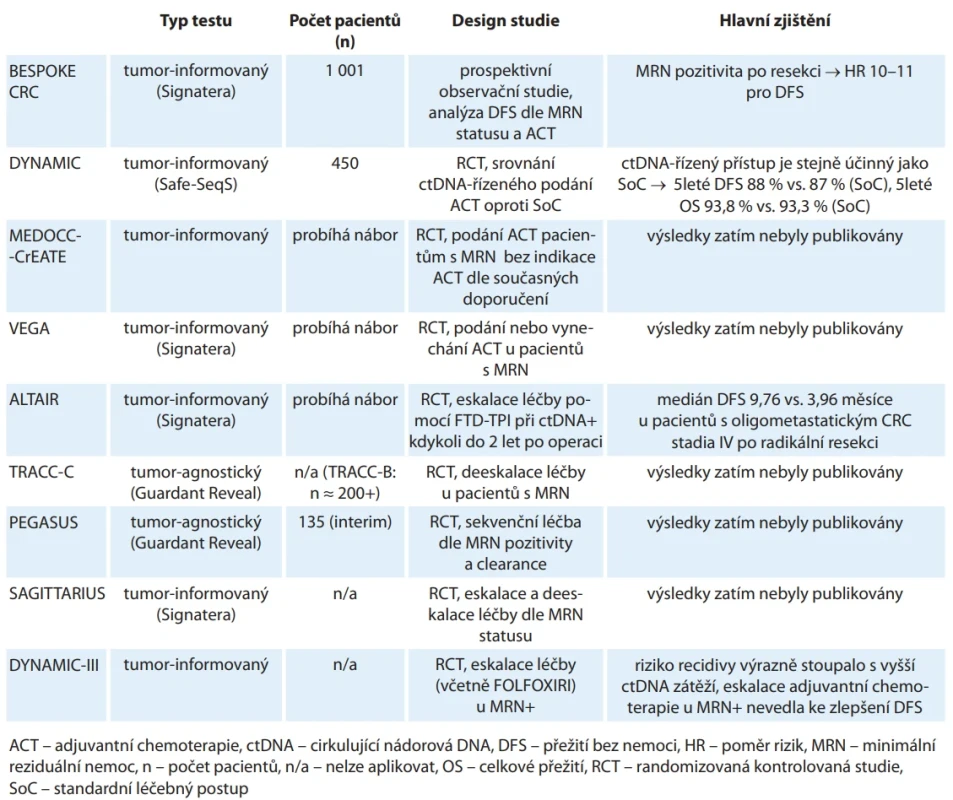
ctDNA řízené rozhodování o léčbě
V lednu 2025 byly prezentovány výsledky finální subanalýzy kohorty 1 001 pacientů s KRK stadia II–III americké prospektivní observační studie BESPOKE CRC, která hodnotila úlohu ctDNA při rozhodování o adjuvantní léčbě a při detekci recidivy onemocnění u pacientů. Pozitivita ctDNA po operaci byla detekována u 8,1 % nemocných ve stadiu II (34/420) a u 24,9 % ve stadiu III (126/505). V obou případech byla spojena s významně horším DFS (stadium II: HR 10,4; p < 0,0001; stadium III: HR 10,1; p < 0,0001).
Analýza přítomnosti ctDNA byla provedena odděleně u pacientů pouze sledovaných (n = 368) a u pacientů léčených ACT (n = 597). V observační kohortě byla pozitivita ctDNA v průběhu sledování zaznamenána u 6,8 % (22/323) pacientů stadia II a u 33,3 % (15/45) pacientů stadia III. V obou případech byla spojena s významně horším DFS (stadium II: HR 34,9; p < 0,0001; stadium III: HR 34,1; p = 0,0008).
V průběhu sledování kohorty léčené ACT se pozitivita ctDNA objevila u 10,9 % (12/110) pacientů stadia II a u 21,1 % (103/487) pacientů stadia III. I zde byla pozitivita spojena s horším DFS (stadium II: HR 131,4; p < 0,0001; stadium III: HR 54,6; p < 0,0001).
Pozoruhodným zjištěním studie BESPOKE CRC bylo, že z ACT profitovali pouze pacienti s prokázanou MRN. U ctDNA pozitivních nemocných, u nichž byla ACT podána do 6 týdnů od operace, došlo k významnému prodloužení DFS oproti samotnému sledování. Naproti tomu u pacientů MRN negativních byly výsledky DFS prakticky totožné bez ohledu na podání chemoterapie [27].
Hlavním omezením této studie je její design – jednalo se o prospektivní observační studii, nikoli o randomizovanou kontrolovanou studii (RCT). Právě výsledky z RCT jsou však nezbytné k tomu, aby se ctDNA mohla etablovat jako spolehlivý biomarker pro identifikaci MRN a aby byla zařazena do klinické praxe pro individualizaci pooperační léčby.
Tento deficit se snaží vyrovnat několik aktuálně probíhajících RCT realizovaných v mnoha centrech po celém světě [28]. Přestože se liší designem, všechny mají společný cíl – porovnat standardní postupy indikace a podání ACT s přístupy řízenými výsledky ctDNA.
První randomizovaná kontrolovaná studie, která hodnotila ctDNA řízený přístup, byla DYNAMIC. Pacienti se stadiem II KRK po resekci byli randomizováni do dvou skupin: v jedné byla léčba řízena podle výsledků ctDNA (ACT byla podávána pouze ctDNA pozitivním pacientům), zatímco druhá skupina podstoupila standardní management podle platných guidelines [29].
Při mediánu sledování 59,7 měsíce bylo 5leté DFS 88 % u pacientů řízených pomocí ctDNA a 87 % u pacientů se standardním přístupem. Pětileté OS činilo 93,8 % vs. 93,3 % (HR 1,05; 95% CI 0,47–2,37; p = 0,887). Studie zároveň prokázala, že clearance ctDNA během ACT byla silným prediktorem dobré prognózy: 5leté DFS dosáhlo 97 % u pacientů s clearance ctDNA po léčbě oproti 0 % u těch s přetrvávající pozitivitou ctDNA (p < 0,001) [30].
Na pacienty s KRK stadia II se zaměřila i nizozemská studie MEDOCC-CrEATE. V ní jsou pacienti, kteří podle guidelines nemají indikaci k ACT, randomizováni k podání či nepodání režimu CAPOX (kapecitabin, oxaliplatina) na základě pozitivity ctDNA [31]. Podobný design mají i dánská studie IMPROVE-IT a americká studie COBRA, která navíc podrobně zkoumá význam rychlosti clearance ctDNA u MRN pozitivní kohorty [32,33].
Intervenční ramena projektu CIRCULATE-Japan testují možnosti eskalace a deeskalace léčby. Studie VEGA randomizuje MRN negativní pacienty po kurativní resekci ke standardní 3měsíční chemoterapii CAPOX nebo k jejímu vynechání [20]. Studie ALTAIR testuje přínos eskalace léčby pomocí trifluridin/tipiracilu oproti placebu u pacientů s pozitivní ctDNA kdykoli do 2 let po operaci. Předběžné výsledky ukazují, že nejvíce profitovali pacienti s oligometastatickým KRK stadia IV po radikální resekci – medián DFS činil 9,76 vs. 3,96 měsíce (HR 0,53; p = 0,012) [34].
Britská multicentrická studie TRACC-C, používající tumor agnostický test Guardant Reveal, zařazuje pacienty s KRK stadia II–III. Cílem je prokázat, že deeskalace ACT na základě negativity ctDNA po resekci není horší než standardní léčba, a to měřeno 3letým DFS [35].
Výsledky předcházející observační části TRACC-B s mediánem sledování 30,3 měsíce ukázaly, že 2leté DFS dosáhlo 91,1 % u pacientů bez detekovatelné ctDNA po operaci oproti 50,4 % u pacientů s detekovanou ctDNA (HR 6,5; 95% CI 2,96–14,5; p < 0,0001). Longitudinální senzitivita a specificita tohoto tumor agnostického testu byly 62,1 % (95% CI 42,2–79,3) a 85,9 % (95% CI 78,9–91,3) [36].
Další evropská studie, PEGASUS, využívá stejný test Guardant Reveal u pacientů s KRK stadia III a T4N0 stadia II [37]. Design studie předpokládá 3měsíční chemoterapii CAPOX u MRN pozitivních pacientů a 6měsíční monoterapii kapecitabinem u MRN negativních. Po ukončení adjuvantní léčby je prováděna další analýza ctDNA, podle níž se terapie dále upravuje.
První výsledky této studie, prezentované na kongresu ESMO 2023, s mediánem sledování 20,8 měsíce ukázaly, že po operaci byla ctDNA detekována u 26 % pacientů (35/135). Z nich relabovalo 34 % (12/35). Ve skupině MRN negativní došlo k relapsu u 9 % (9/100), což představovalo případy falešné negativity. Po 3měsíčním CAPOX režimu došlo u 31 % MRN pozitivních (11/35) ke konverzi na MRN negativní status. U osmi z těchto pacientů se však ctDNA později znovu objevila nebo došlo k relapsu.
Z pacientů, kteří po CAPOX obdrželi eskalační léčbu v chemoterapeutickém režimu FOLFIRI, zůstalo 52 % (12/23) MRN pozitivních, z nichž polovina (6/12) relabovala. Zbývajících 48 % (11/23) dosáhlo konverze na MRN negativitu a zůstalo bez relapsu k datu analýzy. U 9 % MRN negativních pacientů došlo k relapsu navzdory deeskalaci léčby [38].
Limity senzitivity tumor agnostických testů a relativně malých souborů se snaží překonat evropská multicentrická studie SAGITTARIUS. Ta hodnotí efektivitu personalizované eskalace nebo deeskalace adjuvantní léčby na základě pooperační MRN pozitivity či pozdější konverze. Primárním cílem je 2leté DFS u ctDNA pozitivních pacientů, sekundárními cíli jsou OS, míra konverze ctDNA a nákladová efektivita [39].
Australská studie DYNAMIC-III zařadila pacienty s KRK stadia III indikované k ACT. Po stanovení MRN statusu byli randomizováni do dvou ramen: standardní léčba (SoC) bez využití výsledků ctDNA a ctDNA řízená léčba, kde se u MRN pozitivních eskalovalo z kapecitabinu na doublet s oxaliplatinou nebo z doubletu na triplet FOLFOXIRI (5-fluorouracil, leukovorin, oxaliplatina, irinotekan). U MRN negativních byla naopak terapie deeskalována.
Analýza MRN pozitivní kohorty prezentovaná na ASCO 2025 potvrdila prognostický význam detekce ctDNA po operaci. Riziko recidivy výrazně stoupalo s vyšší ctDNA zátěží: 3leté DFS činilo 78 %, 63 %, 36 % a 22 % v kvartilech < 0,06; 0,06–0,17; 0,18–1,31 a >1,31 mutantních molekul/ml (p < 0,01). Eskalace ACT, včetně režimu FOLFOXIRI, však nevedla ke zlepšení DFS. Tříleté DFS u ctDNA pozitivních pacientů léčených FOLFOXIRI bylo 47 % oproti 51 % při standardní léčbě FOLFOX (5-fluorouracil, leukovorin, oxaliplatina) / CAPOX (HR 1,09; 90% CI 0,78–1,53; p = 0,7) [40].
Konečně studie DYNAMIC-Rectal zkoumala využití ctDNA u pacientů s lokálně pokročilým karcinomem rekta (LARC). Předběžné výsledky potvrdily prognostickou hodnotu ctDNA a ukázaly, že ctDNA řízený přístup může snížit podávání ACT [41]. Studie však byla předčasně ukončena kvůli změnám v léčebných strategiích LARC (nástup totální neoadjuvantní léčby – TNT) a komplikacím spojeným s pandemií COVID-19.
Shrnutí a diskuze
ctDNA se v posledních dvou dekádách etablovala jako významný biomarker s potenciálem zásadně změnit přístup k monitoraci a individualizaci adjuvantní léčby u pacientů s KRK. Na rozdíl od tradičně používaných metod, jako je kolonoskopie, CT vyšetření nebo sledování sérových nádorových markerů (CEA, CA 19-9), umožňuje ctDNA časnou detekci minimální reziduální nemoci, přesnější stratifikaci rizika recidivy a predikci odpovědi na léčbu.
Dosavadní prospektivní i retrospektivní studie jednoznačně ukazují, že přítomnost ctDNA po kurativní resekci KRK je silně asociována s vyšším rizikem relapsu a kratším přežitím bez onemocnění i s celkovým přežitím. Naopak negativita ctDNA spolehlivě identifikuje pacienty s nízkým rizikem, kteří mohou profitovat z redukovaného sledování a deeskalace ACT. Tyto závěry potvrdila mimo jiné studie IDEA, prospektivní projekty VICTORI a GALAXY i rozsáhlá interim analýza studie COSMOS využívající tumor agnostický přístup.
Výsledky prvních randomizovaných kontrolovaných studií, zejména studie DYNAMIC, prokázaly, že ctDNA řízený přístup umožňuje bezpečně omezit indikaci ACT bez negativního vlivu na onkologické výsledky. Naopak data z projektů PEGASUS a DYNAMIC-III ukázala, že pouhá eskalace intenzity léčby u ctDNA pozitivních pacientů nemusí vést k očekávanému zlepšení prognózy. To podtrhuje potřebu dalšího výzkumu zaměřeného nejen na predikci rizika, ale i na optimalizaci terapeutických strategií u pacientů s přetrvávající pozitivitou ctDNA.
Zajímavým směrem je využití ctDNA u pacientů s LARC. Studie DYNAMIC-Rectal sice potvrdila prognostickou hodnotu ctDNA, avšak byla předčasně ukončena. Aktuální výzkum se zaměřuje na roli ctDNA při identifikaci pacientů s LARC s kompletní klinickou odpovědí na TNT, u nichž by bylo možné bezpečně vynechat chirurgický výkon. V tomto kontextu je citlivost stanovení ctDNA klíčová, aby se předešlo falešně negativním výsledkům a následnému podléčení.
Ekonomická efektivita ctDNA testování představuje další důležitý aspekt. Přestože testy zatím vykazují vyšší náklady, možnost vyhnout se zbytečnému podávání chemoterapie a s tím spojeným komplikacím může vést k významným finančním úsporám v systému zdravotní péče.
V českých reáliích se využití ctDNA dosud omezuje především na výzkumné projekty a pilotní klinické hodnocení. Klinická implementace zůstává zatím omezená, a to zejména z důvodu finančních nákladů, omezené dostupnosti testů a absence dat validovaných na české populaci. S ohledem na mezinárodní výsledky však lze očekávat, že ctDNA bude v budoucnu začleněna i do českých doporučených postupů pro sledování a léčbu pacientů s KRK. Zvlášť důležité bude ověřit, zda lze zahraniční výsledky plně aplikovat i na specifika české populace, kde incidence KRK patří k nejvyšším v Evropě.
Celkově lze shrnout, že ctDNA se stává klíčovým nástrojem personalizované onkologie. Umožňuje časnou identifikaci pacientů s vysokým rizikem relapsu, individualizaci rozhodování o ACT a efektivnější využití zdravotnických zdrojů. Definitivní zařazení ctDNA do standardní klinické praxe ale vyžaduje výsledky probíhajících randomizovaných studií a validaci v lokálních podmínkách, včetně českého prostředí.
Dedikace
Projekt Národní ústav pro výzkum rakoviny (Program EXCELES, ID: LX22NPO5102) – Financováno Evropskou unií – Next Generation EU.
Zdroje
1. SVOD. Portál epidemiologie novotvarů v ČR. 2024 [online]. Dostupné z: https: //www.svod.cz.
2. Yakabe T, Nakafusa Y, Sumi K et al. Clinical significance of CEA and CA19-9 in postoperative follow-up of colorectal cancer. Ann Surg Oncol 2010; 17 (9): 2349–2356. doi: 10.1245/s10434-010-1004-5.
3. Brenner H, Kloor M, Pox CP. Colorectal cancer. Lancet 2014; 383 (9927): 1490–1502. doi: 10.1016/S0140-6736 (13) 61649-9.
4. Smith-Bindman R, Chu PW, Azman Firdaus H et al. Projected lifetime cancer risks from current computed tomography imaging. JAMA Intern Med 2025; 185 (6): 710–719. doi: 10.1001/jamainternmed.2025.0505.
5. Ho Seung K, Ro Lee M. Diagnostic accuracy of elevated serum carcinoembryonic antigen for recurrence in postoperative stage II colorectal cancer patients: comparison with stage III. Ann Coloproctol 2013; 29 (4): 155–159. doi: 10.3393/ac.2013.29.4.155.
6. Yokota M, Morikawa A, Matsuoka H et al. Is frequent measurement of tumor markers beneficial for postoperative surveillance of colorectal cancer? Int J Colorectal Dis 2023; 38 (1): 75. doi: 10.1007/s00384-023-04356-2.
7. Okamura R, Hasegawa S, Hida K et al. The role of periodic serum CA19-9 test in surveillance after colorectal cancer surgery. Int J Clin Oncol 2017; 22 (1): 96–101. doi: 10.1007/s10147-016-1027-4.
8. Park IJ, Choi GS, Lim KH et al. Serum carcinoembryonic antigen monitoring after curative resection for colorectal cancer: clinical significance of the preoperative level. Ann Surg Oncol 2009; 16 (11): 3087–3093. doi: 10.1245/s10434-009-0625-z.
9. Primrose JN, Perera R, Gray A et al. Effect of 3 to 5 years of scheduled CEA and CT follow-up to detect recurrence of colorectal cancer: the FACS randomized clinical trial. JAMA 2014; 311 (3): 263–270. doi: 10.1001/jama.2013. 285718.
10. Mauri G, Vitiello PP, Sogari A et al. Liquid biopsies to monitor and direct cancer treatment in colorectal cancer. Br J Cancer 2022; 127 (3): 394–407. doi: 10.1038/s41416-022-01769-8.
11. Diaz LA, Bardelli A. Liquid biopsies: genotyping circulating tumor DNA. J Clin Oncol 2014; 32 (6): 579–586. doi: 10.1200/JCO.2012.45.2011.
12. Vymetalkova V, Cervena K, Bartu L et al. Circulating cell--free DNA and colorectal cancer: a systematic review. Int J Mol Sci 2018; 19 (11): 3356. doi: 10.3390/ijms19113356.
13. Martínez-Castedo B, Camblor DG, Martín-Arana J et al. Minimal residual disease in colorectal cancer. Tumor-informed versus tumor-agnostic approaches: unraveling the optimal strategy. Ann Oncol 2025; 36 (3): 263–276. doi: 10.1016/j.annonc.2024.12.006.
14. Nakamura Y, Tsukada Y, Matsuhashi N et al. Colorectal cancer recurrence prediction using a tissue-free epigenomic minimal residual disease assay. Clin Cancer Res 2024; 30 (19): 4377–4387. doi: 10.1158/1078-0432.CCR-24-1651.
15. Ryan BM, Lefort F, McManus R et al. A prospective study of circulating mutant KRAS2 in the serum of patients with colorectal neoplasia: strong prognostic indicator in postoperative follow up. Gut 2003; 52 (1): 101–108. doi: 10.1136/gut.52.1.101.
16. Lecomte T, Berger A, Zinzindohoué F et al. Detection of free-circulating tumor-associated DNA in plasma of colorectal cancer patients and its association with prognosis. Int J Cancer 2002; 100 (5): 542–548. doi: 10.1002/ijc.10526.
17. Mauri G, Vitiello PP, Sogari A et al. Liquid biopsies to monitor and direct cancer treatment in colorectal cancer. Br J Cancer 2022; 127 (3): 394–407. doi: 10.1038/s41416-022-01769-8.
18. Diehl F, Schmidt K, Choti MA et al. Circulating mutant DNA to assess tumor dynamics. Nat Med 2008; 14 (9): 985–990. doi: 10.1038/nm.1789.
19. Taieb J, Souglakos J, Boukovinas I et al. Combined analyses of circulating tumor DNA and immunoscore in patients with stage III colon cancer: a post hoc analysis of the PRODIGE-GERCOR IDEA-France/HORG-IDEA-Greece trials. J Clin Oncol 2025; 43 (13): 1234–1245. doi: 10.1200/JCO.24.00648.
20. Taniguchi H, Nakamura Y, Kotani D et al. CIRCULATE-Japan: circulating tumor DNA-guided adaptive platform trials to refine adjuvant therapy for colorectal cancer. Cancer Sci 2021; 112 (7): 2915–2920. doi: 10.1111/cas.14926.
21. Solar Vasconcelos JP, Titmuss E, Navarro F et al. Circulating tumor DNA (ctDNA) kinetics in colorectal cancer treated with curative intent in the VICTORI study with an ultrasensitive MRD assay. J Clin Oncol 2024; 42 (Suppl 16): e15625. doi: 10.1200/JCO.2024.42.16_suppl.e15625.
22. Solar Vasconcelos JP, Titmuss E, Navarro F et al. Identifying the optimal post-surgical timing of molecular residual disease (MRD) detection in colorectal cancer using an ultra-sensitive assay: interim results from the VICTORI study. J Clin Oncol 2025; 43 (Suppl 4): 275. doi: 10.1200/JCO.2025.43.4_suppl.275.
23. Nakamura Y, Watanabe J, Akazawa N et al. ctDNA-based molecular residual disease and survival in resectable colorectal cancer. Nat Med 2024; 30 (11): 3272–3283. doi: 10.1038/s41591-024-03254-6.
24. Kataoka K, Mori K, Nakamura Y et al. Survival benefit of adjuvant chemotherapy based on molecular residual disease detection in resected colorectal liver metastases: subgroup analysis from CIRCULATE-Japan GALAXY. Ann Oncol 2024; 35 (11): 1015–1025. doi: 10.1016/j.annonc.2024.08.2240.
25. Nakamura Y, Tsukada Y, Matsuhashi N et al. Colorectal cancer recurrence prediction using a tissue-free epigenomic minimal residual disease assay. Clin Cancer Res 2024; 30 (19): 4377–4387. doi: 10.1158/1078-0432.CCR-24-1651.
26. Tsukada Y, Matsuhashi N, Murano T et al. Impact of postoperative integrated genomic and epigenomic signatures of circulating tumor DNA on recurrence in resected colorectal cancer: initial report of a prospective ctDNA monitoring study COSMOS-CRC-01. J Clin Oncol 2022; 40 (Suppl 4): 168. doi: 10.1200/JCO.2022.40.4_suppl.168.
27. Aushev VN, Ensor J, Sanchez SA et al. Circulating tumor DNA for detection of molecular residual disease in patients with stage II/III colorectal cancer: final analysis of the BESPOKE CRC sub-cohort. Gastroenterology 2025; 169 (1): S127. doi: 10.1016/S0016-5085 (25) 01235-1.
28. Verschoor N, Bos MK, Oomen-de Hoop E et al. A review of trials investigating ctDNA-guided adjuvant treatment of solid tumors: the importance of trial design. Eur J Cancer 2024; 207 : 114159. doi: 10.1016/j.ejca.2024.114159.
29. Tie J, Cohen JD, Lahouel K et al. Circulating tumor DNA analysis guiding adjuvant therapy in stage II colon cancer. N Engl J Med 2022; 386 (24): 2261–2272. doi: 10.1056/NEJMoa2200075.
30. Tie J, Wang Y, Loree JM et al. ctDNA-guided adjuvant chemotherapy escalation in stage III colon cancer: primary analysis of the ctDNA-positive cohort from the randomized AGITG DYNAMIC-III trial (intergroup study of AGITG and CCTG). J Clin Oncol 2025; 43 (Suppl 16): 3503. doi: 10.1200/JCO.2025.43.16_suppl.3503.
31. Clinical Trials. Circulating tumor DNA based adjuvant chemotherapy in stage II colon cancer patients: the MEDOCC-CrEATE trial (CrEATE). 2025 [online]. Dostupné z: https: //clinicaltrials.gov/study/NCT06434896.
32. Clinical Trials. IMPROVE intervention trial implementing non-invasive circulating tumor DNA analysis to optimize the operative and postoperative treatment for patients with colorectal cancer (IMPROVE-IT). 2025 [online]. Dostupné z: https: //clinicaltrials.gov/study/NCT03748680.
33. Clinical Trials. Circulating tumor DNA testing in predicting treatment for patients with stage IIA colon cancer after surgery. 2025 [online]. Dostupné z: https: //clinicaltrials.gov/study/NCT04068103.
34. Bando H, Watanabe J, Kotaka M et al. A randomized, double-blind, phase III study comparing trifluridine/tipiracil (FTD/TPI) versus placebo in patients with molecular residual disease following curative resection of colorectal cancer (CRC): the ALTAIR study. J Clin Oncol 2025; 43 (Suppl 4): LBA22. doi: 10.1200/JCO.2025.43.4_suppl.LBA22.
35. Slater S, Bryant A, Chen HC et al. ctDNA guided adjuvant chemotherapy versus standard of care adjuvant chemotherapy after curative surgery in patients with high risk stage II or stage III colorectal cancer: a multi-centre, prospective, randomised control trial (TRACC Part C). BMC Cancer 2023; 23 (1): 257. doi: 10.1186/s12885-023-10699-4.
36. Slater S, Bryant A, Aresu M et al. Tissue-free liquid biopsies combining genomic and methylation signals for minimal residual disease detection in patients with early colorectal cancer from the UK TRACC part B study. Clin Cancer Res 2024; 30 (16): 3459–3469. doi: 10.1158/1078-0432.CCR-24-0226.
37. Clinical Trials. Post-surgical liquid biopsy-guided treatment of stage III and high-risk stage II colon cancer patients: the PEGASUS trial. 2025 [online]. Available from: https: //clinicaltrials.gov/study/NCT04259944.
38. Lonardi S, Pietrantonio F, Tarazona L et al. The PEGASUS trial: post-surgical liquid biopsy-guided treatment of stage III and high-risk stage II colon cancer patients. J Clin Oncol 2020; 38 (Suppl 15): TPS4124. doi: 10.1200/JCO.2020.38.15_suppl.TPS4124.
39. Montagut CO, Tamberi S, Leone F et al. A precision medicine trial leveraging tissue and blood-based tumor genomics to optimize treatment in resected stage III and high-risk stage II colon cancer (CC) patients: the SAGITTARIUS trial. J Clin Oncol 2025; 43 (Suppl 16): TPS3647. doi: 10.1200/JCO.2025.43.16_suppl.TPS3647.
40. Tie J, Wang Y, Loree JM et al. ctDNA-guided adjuvant chemotherapy escalation in stage III colon cancer: primary analysis of the ctDNA-positive cohort from the randomized AGITG DYNAMIC-III trial (intergroup study of AGITG and CCTG). J Clin Oncol 2025; 43 (Suppl 16): 3503. doi: 10.1200/JCO.2025.43.16_suppl.3503.
41. Tie J, Cohen J, Wang Y et al. Circulating tumor DNA analysis informing adjuvant chemotherapy in locally advanced rectal cancer: the randomized AGITG DYNAMIC-rectal study. J Clin Oncol 2024; 42 (Suppl 3): 12. doi: 10.1200/JCO.2024.42.3_suppl.12.
Štítky
Dětská onkologie Chirurgie všeobecná Onkologie
Článek Není ct jako CT
Článek vyšel v časopiseKlinická onkologie
Nejčtenější tento týden
2026 Číslo 2- Trombóza portální žíly jako komplikace infekce COVID-19 – kazuistika
- Ibrance® – nová šance pro pacientky s HR+/HER2– karcinomem prsu
- Exemestan zlepšuje interval bez relapsu při karcinomu prsu
- Význam a prognostická hodnota nádorových markerů
-
Všechny články tohoto čísla
- Cirkulující nádorová DNA jako biomarker pro predikci minimální reziduální nemoci a individualizaci adjuvantní léčby kolorektálního karcinomu – přehled současných poznatků a perspektiv
- Intravaskulárna propagácia adenomyózy v krvných cievach myometria a uterinného leiomyómu u pacientky s mutáciou génu fumaráthydratázy – zriedkavý nález imitujúci malígnu neopláziu
- Druhá rekurence karcinomu prsu 36 let po počátečním chirurgickém výkonu a 18 let po první rekurenci – extrémně vzácný případ
- FDG-PET/CT: metabolicky aktivní solitární ložisko podkožně gluteálně u pacientky s karcinomem prsu – granulom či metastáza?
- Cancer patients admitted to intensive care unit
- Nádory GIT – chemoterapie a precizní léčba se synergicky doplňují
- Snižování škod rizikového chování v onkologické prevenci
- AKTUALITY Z NÁRODNÍHO ÚSTAVU PRO VÝZKUM RAKOVINY
- Není ct jako CT
- Léčba Castlemanovy choroby z pohledu roku 2026
- Ewingův sarkom – současné diagnostické a terapeutické postupy
- Klinická onkologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Léčba Castlemanovy choroby z pohledu roku 2026
- Ewingův sarkom – současné diagnostické a terapeutické postupy
- Cirkulující nádorová DNA jako biomarker pro predikci minimální reziduální nemoci a individualizaci adjuvantní léčby kolorektálního karcinomu – přehled současných poznatků a perspektiv
- FDG-PET/CT: metabolicky aktivní solitární ložisko podkožně gluteálně u pacientky s karcinomem prsu – granulom či metastáza?
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Revma Focus: Spondyloartritidy
nový kurz
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Autoři: prof. MUDr. Pavel Horák, CSc., doc. MUDr. Ludmila Brunerová, Ph.D., doc. MUDr. Václav Vyskočil, Ph.D., prim. MUDr. Richard Pikner, Ph.D., MUDr. Olga Růžičková, MUDr. Jan Rosa, prof. MUDr. Vladimír Palička, CSc., Dr.h.c.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



