-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Problematika jodu u předčasně narozených novorozenců
Iodine status in premature newborns
Iodine is a micronutrient essential for normal thyroid function, growth and development of a child. Iodine deficiency remains an unresolved problem worldwide, where even in countries with adequate iodine supply certain population groups remain particularly at risk. Premature newborns comprise one such group as several factors including organic and functional developmental immaturity, a lower iodine reserve pool and insufficient postnatal iodine intake may contribute to iodine deficiency. However, such newborns are also more susceptible to autoregulatory thyroid inhibition upon excessive iodine supply. Several guidelines on the optimal daily iodine intake for preterm newborns exist in different parts of the world. Our article presents an overview of these guidelines and current data about iodine content in parenteral nutrition, breast milk and milk formulas.
Keywords:
Thyroid – Iodine – premature newborn – urinary iodine concentration
Autoři: Rana Ibrahim; Kateřina Krylová; David Neumann
Působiště autorů: Dětská klinika LF UK a FN Hradec Králové
Vyšlo v časopise: Čas. Lék. čes. 2021; 160: 230-232
Kategorie: Přehledový článek
Souhrn
Jod je mikronutrient nezbytný pro správnou funkci štítné žlázy a růst a vývoj dítěte. Deficit jodu zůstává nevyřešeným problémem u rizikových skupin populace i v zemích s dostatečným zásobením jodem. Předčasně narození novorozenci patří mezi tyto rizikové skupiny, protože mají nižší kapacitu ukládání jodu při jeho nedostatečném příjmu. Jsou současně náchylnější k útlumu štítné žlázy při nadbytku jodu. Doporučení pro ideální denní příjem jodu u předčasně narozených novorozenců se v různých zemích liší. V článku uvádíme přehled, jaký denní příjem jodu u nedonošených novorozenců doporučují různé odborné společnosti, a současné poznatky o obsahu jodu v parenterální výživě, mateřském mléce a umělých mléčných formulích.
Klíčová slova:
štítná žláza – jód – nedonošený novorozenec – jodurie
ÚVOD
Jod je esenciální pro tvorbu tyreoidálních hormonů. I přes významný pokrok při zvládání nedostatku jodu v posledních třech desetiletích a omezení zdravotních důsledků zůstává celosvětově deficit jodu jedním z nejčastějších deficitů stopových prvků. Ve více než polovině zemí Evropy přetrvává mírný nedostatek jodu, a jeho příjem navíc v několika posledních letech klesá (1).
Předčasně narození novorozenci jsou k nedostatku jodu zvlášť citliví. Mají nižší kapacitu jeho ukládání, což vysvětluje, proč jsou zásoby jodu, tyreoglobulinu a trijodthyroninu (T3) u dětí s extrémně nízkou porodní hmotností jen zhruba 30procentní ve srovnání s hodnotami u dětí narozených v termínu (na základě obsahu DNA a trijodthyroninu na 1 mol tyreoglobulinu) (2).
Problémem je také nedostatečný příjem jodu, ve skupině předčasně narozených novorozenců relativně častý. Enterální výživa formulí či fortifikovaným mateřským mlékem obvykle neobsahuje doporučené denní dávky jodu pro předčasně narozené novorozence (30–60 µg/kg za den) a v úplné parenterální výživě podávané u dětí na JIP se jod vyskytuje jen v nevýznamném množství (3, 4). Předpokládá se, že nedostatek jodu přispívá k výskytu hypothyroxinémie u asi 30 % enterálně krmených dětí narozených ve 27.–30. gestačním týdnu (GT) (5). Kromě toho studie ukazují, že u některých předčasně narozených (27.–37. GT) a nemocných novorozenců se na nedostatku jodu může spolupodílet jeho přechodně negativní bilance, neboť močí vylučují přibližně 1,5krát více jodu než zdravé donošené děti (6).
JOD VE VÝŽIVĚ PŘEDČASNĚ NAROZENÝCH NOVOROZENCŮ
Jod v parenterální výživě
V Severní Americe není jod běžně zahrnut do parenterální výživy, zatímco v Evropě, Austrálii a na Novém Zélandu jej roztoky obvykle v určitém množství obsahují (7–11). Doporučení ESPGHAN/ESPEN/ESPE/CPEN z roku 2018 uvádějí, že jod by měl být podáván v denní dávce 1–10 µg/kg/den u předčasně narozených dětí, které dostávají parenterální výživu. Některá doporučení se však kloní k vyšší denní dávce (10–30 µg/kg/den), a to na základě studie, která upozorňuje na negativní bilanci jodu u předčasně narozených dětí, pokud jejich příjem jodu činí průměrně 3 µg/kg/den (při dávce tekutin 150 ml/kg/den) (14). Přípravky parenterální výživy v Austrálii a na Novém Zélandu obsahují jod v dávkovém rozmezí 1–1,1 µmol/kg/den. Na druhé straně Výbor pro klinickou praxi Americké společnosti pro klinickou výživu (Committee on Clinical Practice Issues of the American Society of Clinical Nutrition) doporučuje při parenterálním příjmu jen 1 µg/kg/den. To je hluboko pod doporučeným denním příjmem jodu a důvodem je snaha zabránit potenciálnímu nadbytku tohoto mikroelementu a následnému potlačení funkce štítné žlázy.
Takovéto rozdíly v doporučeních plynou hlavně z obav z účinku mimonutričních zdrojů jodu, kterým může být dítě vystaveno. Proto by měl být sledován obsah jodu v antisepticích, intravenózních infuzích a dalších potenciálních zdrojích, aby se předešlo nadměrnému i nedostatečnému přívodu. Obecně je doporučeno jodový stav u předčasně narozených novorozenců dlouhodobě léčených parenterální výživou pravidelně kontrolovat, a to stanovením koncentrací hormonů štítné žlázy, aby bylo možné správně nastavit ev. substituci (11–14).
Jod v mateřském mléce
V oblastech s dostatečným zásobením jodem je průměrná koncentrace tohoto mikroelementu v mateřském mléce asi 150–180 µg/l (15). Přidání fortifikace do mateřského mléka zvyšuje jeho množství asi o 20–25 µg/l. Ghirri et al. uvádí, že obsah jodu v mléce matek předčasně narozených dětí je nižší než u matek dětí narozených v termínu (100–150 µg/l vs. 150–180 µg/l) (16), ale jiní autoři rozdíly v obsahu jodu v mateřském mléce nezjistili (17, 18).
Jod v mléčných formulích
Doporučený příjem jodu enterální výživou se u předčasně narozených dětí pohybuje od 10 do 55 µg/kg/den (10). Celkový denní příjem závisí na jeho obsahu ve formuli a na množství konzumovaného mléka, které je ovlivněno především postnatálním věkem a hmotností dítěte. Ve studii o obsahu jodu v dětské výživě a jeho příjmu u předčasně narozených dětí Aresová et al. zjistili (18), že děti narozené ve 27.–30. GT dostávaly mléko průměrně v množství asi 70 ml/kg šest dní po porodu, 105 ml/kg ve 3 týdnech, 150 ml/kg ve 2 měsících a asi 175 ml/kg ve 3 měsících postnatálního věku. Z této studie též vyplývá, že předčasně narozené děti obvykle nedostávají mléko v množství 150–200 ml/kg dříve než v měsíci věku. Méně nedonošené děti, narozené v 31.–36. GT, dostávaly průměrně 100 ml/kg šest dní po narození, 150 ml/kg do 3 týdnů a 150–200 ml/kg ve věku od 1 do 2 měsíců. Objemy požitého mléka souvisely hlavně s tělesnou hmotností a byly nižší než doporučené hodnoty, dokud dítě nevážilo kolem 2 kg (18).
Shromáždili jsme údaje o obsahu jodu v nejčastěji používaných formulích a přípravcích pro fortifikaci mateřského mléka (Human Milk Fortifiers) v Česku. Na základě údajů předložených Aresovou et al. o množství mléka a obsahu jodu v těchto formulích dostupné preparáty nesplňují doporučenou denní dávku jodu pro předčasně narozené děti (např. podle AAP 30–40 μg/kg denně) zejména v prvních týdnech života (19) (tab. 1).
Tab. 1. Obsah jodu v novorozeneckých umělých mléčných formulích a přípravcích* pro děti se specifickými výživovými potřebami 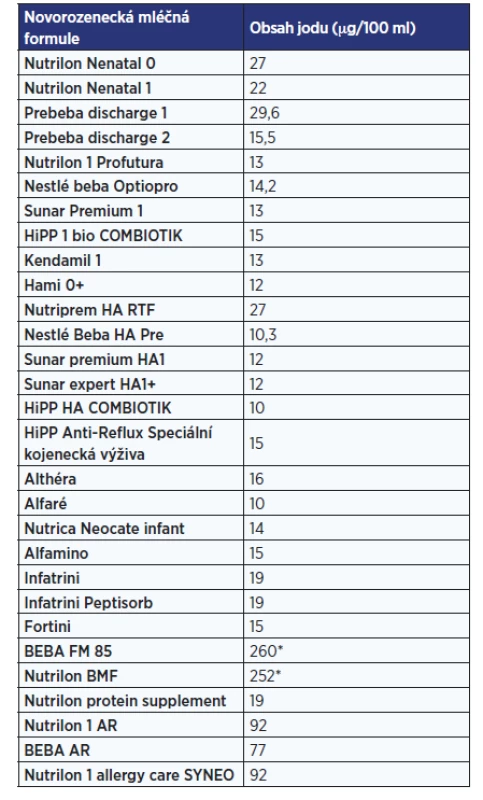
DŮSLEDKY NEDOSTATKU JODU
Těžký nedostatek jodu v těhotenství v kritické fázi vývoje plodu je spojen se zvýšeným výskytem potratů, poškození placenty, vrozených vad, novorozenecké a kojenecké úmrtnosti a s neurologicko-vývojovým syndromem, tzv. kretenismem. Nedostatek jodu, který nastane později v těhotenství, v tzv. vývojovém okně mozku, je spojen s myxedematózní formou poškození (20). Dlouhodobý vliv mírného nedostatku jodu během těhotenství není jednoznačně definován.
V literatuře byl popsán vliv na neuropsychologický vývoj. Bathová et al. prokázali, že mírný až střední nedostatek jodu ze vzorků moči matky v I. trimestru (jodurie < 150 µg/l) byl spojen s nižším verbálním IQ, horší přesností čtení a čtení s porozuměním u 8letých dětí (21). Podobně studie Hynesové et al. poskytla důkazy, že dysgrafie a problémy s anglickou gramatikou se u 9letých dětí vyskytují častěji, pokud jejich matky měly v graviditě jodurii < 150 µg/l, než u těch, jejichž matky měly jodurii > 150 µg/l. Tento rozdíl zůstal významný i po korekci na další biologické a socioekonomické faktory (22).
NADBYTEK JODU
Předčasně narození novorozenci jsou náchylnější k útlumu funkce štítné žlázy v důsledku nadbytku jodu než novorozenci narození v termínu. Obrana před Wolffovým-Chaikoffovým efektem se objevuje po 35. GT (23). Děti narozené před 32. GT jsou zvláště citlivé k útlumu štítné žlázy, pokud jsou vystaveny působení jodu z kožních antiseptik a dalších zdrojů, např. infuzí. Podobně expozice jeho nadměrnému množství v mateřském mléce může vést k subklinické hypotyreóze u předčasně narozených novorozenců (24–26). Z tohoto důvodu někteří odborníci nedoporučují suplementaci u předčasně narozených novorozenců, konkrétně u pacientů na JIP, kteří dostávají parenterální výživu (27).
V posledních letech se objevuje snaha vytvořit „prostředí bez nadbytku jodu“. Používají se antiseptika bez jodu (např. chlorhexidin), což by mohlo ohrozit novorozence, kteří mají malé, nebo dokonce nevýznamné zásoby jodu ve štítné žláze. Toto úsilí by však mohlo vést k celkovému nedostatku jodu (28).
ZÁVĚR
Jod je životně důležitý mikronutrient, který je nezbytný pro správnou funkci štítné žlázy a produkci jejích hormonů. Nedostatek jodu má mnoho známých závažných a trvalých následků. Předčasně narození novorozenci jsou náchylnější jak k nedostatku jodu, tak k jeho nadbytku a doporučení ohledně ideálního množství jodu, které by tyto děti měly dostávat, nejsou v současnosti jednoznačná. Proto je u této skupiny dětí nejvhodnější pravidelné sledování funkce štítné žlázy, aby se zabránilo nerovnováze zásobení jodem a péče o ně se optimalizovala. Cílem je dlouhodobý fyziologický neuropsychický vývoj těchto dětí.
Poděkování
Grantová dedikace – PERSONMED CZ.02.1.01/0.0/0.0/17_048/0007441.
Čestné prohlášení
Autoři nemají střet zájmů.
Adresa pro korespondenci:
MUDr. Kateřina Krylová, Ph.D.
Dětská klinika LF UK a FNHK
Sokolská 581, 500 05 Hradec Králové
Tel.: 495 832 666
e-mail: krylovak@lfhk.cuni.cz
Zdroje
- Eastman CJ, Zimmermann MB. The iodine deficiency disorders. In: Feingold KR, Anawalt B, Boyce A et al. (eds.): Endotext. MDText.com, Inc., South Dartmouth, 2018.
- van den Hove MD, Beckers C, Devlieger D et al. Hormone synthesis and storage in the thyroid of human preterm and term newborns: effect of thyroxine treatment. Biochemie 1999; 81 : 563–570.
- Paul DA, Mackley A, Yencha EM. Thyroid function in term and late preterm infants with respiratory distress and relation to severity of illness. Thyroid 2010; 20 : 189–94.
- Délange F. Optimal iodine nutrition during pregnancy, lactation and the neonatal period. Int J Endocrinol Metab 2004; 2 : 1–12.
- Ares S, Escobar–Morreale HF, Quero J et al. Neonatal hypothyroxinemia: Effects of iodine intake and premature birth. J Clin Endo Metab 1997; 82 : 1704–1712.
- Ares S, Quero J, Morreale de Escobar G. Iodine balance, iatrogenic excess, and thyroid dysfunction in premature newborns. Sem Perinatol 2008; 32 : 407–412.
- Jin J, Mulesa L, Carrilero Rouillet M. Trace elements in parenteral nutrition: considerations for the prescribing clinician. Nutrients 2017; 9 : 440.
- Clarridge KE, Conway EE, Bucuvalas J. Hypothyroidism and iodine deficiency in an infant requiring total parenteral nutrition. JPEN 2014; 38 : 901–904.
- Golekoh MC, Cole CR, Jones NY. Severe hypothyroidism from iodine deficiency associated with parenteral nutrition. JPEN 2016; 40 : 1191–1193.
- Domellöf M, Szitanyi P, Simchowitz V et al. ESPGHAN/ESPEN/ESPR guidelines on pediatric parenteral nutrition: iron and trace minerals. Clin Nutr 2018; 37 : 2354–2359.
- Osland EJ, Ali A, Isenring E et al. Australasian Society for Parenteral and Enteral Nutrition guidelines for supplementation of trace elements during parenteral nutrition. Asia Pac J Clin Nutr 2014; 23 : 545–554.
- Domellöf M. Nutritional care of premature infants: microminerals. World Rev Nutr Diet 2014; 110 : 121–139.
- Ibrahim M, de Escobar GM, Visser TJ et al. Iodine deficiency associated with parenteral nutrition in extreme preterm infants. Arch Dis Child Fetal Neonatal 2003; 88: F56–F57.
- Zimmermann MB, Crill CM. Iodine in enteral and parenteral nutrition. Best Pract Res Clin Endocrinol Metab 2010; 24 : 143–158.
- Zimmermann MB. Iodine deficiency. Endocr Rev 2009; 30 : 376–408.
- Ghirri P, Lunardi S, Boldrini A. Iodine supplementation in the newborn. Nutrients 2014; 6 : 382–390.
- Etling N, Padovani E, Fouque F, Taro L. First month variations in total iodine content of human breast milks. Early Hum Dev 1986; 13 : 81–85.
- Ares S, Quero J, Duran S et al. Iodine content of infant formulas and iodine intake of premature babies: High risk of iodine deficiency. Arch Dis Child Fetal Neonatal 1996; 71: F184–F191.
- Williams FLR, Ogston S, Hume R et al. Supplemental iodide for preterm infants and developmental outcomes at 2 years: An RCT. Pediatrics 2017; 139: e20163703.
- Boyages SC, Halpern JP, Maberly GF et al. A comparative study of neurological and myxedematous endemic cretinism in western China. J Clin Endocrinol Metab 1988; 67 : 1262–1271.
- Bath SC, Steer CD, Golding J et al. Effect of inadequate iodine status in UK pregnant women on cognitive outcomes in their children: results from the Avon Longitudinal Study of Parents and Children (ALSPAC). Lancet 2013; 382 : 331.
- Hynes KL, Otahal P, Hay I, Burgess JR. Mild iodine deficiency during pregnancy is associated with reduced educational outcomes in the offspring: 9-year follow-up of the Gestational Iodine Cohort. J Clin Endocrinol Metab 2013; 98 : 1954–1962.
- Melmed S, Polonsky KS, Larsen PR, Kronenberg HM. Williams Textbook of Endocrinology (13th ed.). Saunders Elsevier, Philadelphia, 2015 : 334–335.
- Smith VC, Svoren BM, Wolfsdorf JI. Hypothyroidism in a breast-fed preterm infant resulting from maternal topical iodine exposure. J Pediatr 2006; 49 : 566–567.
- Aitken J, Williams FL. A systematic review of thyroid dysfunction in preterm neonates exposed to topical iodine. Arch Dis Child Fetal Neonatal 2014; 99: F21–F28.
- Chung HR, Shin CH, Yang SW et al. Subclinical hypothyroidism in Korean preterm infants associated with high levels of iodine in breast milk. J Clin Endocrinol Metab 2009; 94 : 4444–4447.
- Harry L, Greene K, Hambidge M et al. Guidelines for the use of vitamins, trace elements, calcium, magnesium, and phosphorus in infants and children receiving total parenteral nutrition: report of the Subcommittee on Pediatric Parenteral Nutrient Requirements from the Committee on Clinical Practice Issues of the American Society for Clinical Nutrition. Am J Clin Nutr 1988; 48 : 1324–1342.
- Finch CW. Review of trace mineral requirements for preterm infants: What are the current recommendations for clinical practice? Nutr Clin Pract 2015; 30 : 44–58.
Štítky
Adiktologie Alergologie a imunologie Angiologie Audiologie a foniatrie Biochemie Dermatologie Dětská gastroenterologie Dětská chirurgie Dětská kardiologie Dětská neurologie Dětská otorinolaryngologie Dětská psychiatrie Dětská revmatologie Diabetologie Farmacie Chirurgie cévní Algeziologie Dentální hygienistka
Článek vyšel v časopiseČasopis lékařů českých
Nejčtenější tento týden
2021 Číslo 6- Jak a kdy u celiakie začíná reakce na lepek? Možnou odpověď poodkryla čerstvá kanadská studie
- Doc. Jitka Fricová: V USA nasazovali fentanyl poměrně nekriticky, v Česku je situace jiná
- Sympozium věnované péči o pacienty s ALS jako odrazový můstek pro zlepšení kvality jejich života
- Výhody kombinace olopatadinu a momethasonu v terapii alergické rinitidy
- Nedostatečné dávkování enoxaparinu je u pacientů po ortopedickém výkonu časté a zvyšuje riziko tromboembolické nemoci
-
Všechny články tohoto čísla
- ÚVODEM
- Jod a zdraví v Česku
- Čtvrtstoletí práce Meziresortní komise pro řešení jodového deficitu
- Význam jodu v graviditě – klinický pohled
- Problematika jodu u předčasně narozených novorozenců
- Monitorování jodového zásobení novorozenecké populace v Česku: alarmující výsledky za rok 2020
- Problematika jodového zásobení u dětí na veganské stravě
- Ryby – zdroj jodu, ale i dalších chemických látek
- Suplementy s obsahem jodu volně dostupné na českém trhu
- Jan Evangelista Purkyně a Napoleon Bonaparte
- Česká farmacie 150 let pod křídly odborné společnosti
- 100 let Sexuologického ústavu Univerzity Karlovy v Praze
- Léčba obezity – přehledně a prakticky
- Časopis lékařů českých
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Léčba obezity – přehledně a prakticky
- Suplementy s obsahem jodu volně dostupné na českém trhu
- Ryby – zdroj jodu, ale i dalších chemických látek
- Význam jodu v graviditě – klinický pohled
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: MUDr. Petr Výborný, CSc., FEBO
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



