-
Články
Top novinky
Reklama- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
Top novinky
Reklama- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Top novinky
ReklamaDetekce protein‑proteinových interakcí metodami FRET a BRET
Detection of Protein‑protein Interactions by FRET and BRET Methods
Nowadays, in vivo protein‑protein interaction studies have become preferable detecting methods that enable to show or specify (already known) protein interactions and discover their inhibitors. They also facilitate detection of protein conformational changes and discovery or specification of signaling pathways in living cells. One group of in vivo methods enabling these findings is based on fluorescent resonance energy transfer (FRET) and its bioluminescent modification (BRET). They are based on visualization of protein‑protein interactions via light or enzymatic excitation of fluorescent or bioluminescent proteins. These methods allow not only protein localization within the cell or its organelles (or small animals) but they also allow us to quantify fluorescent signals and to discover weak or strong interaction partners. In this review, we explain the principles of FRET and BRET, their applications in the characterization of protein‑protein interactions and we describe several findings using these two methods that clarify molecular and cellular mechanisms and signals related to cancer biology.
Key words:
FRET – BRET – imaging methods – protein‑protein interaction in vivo
This work was supported by the Czech Science Foundation projects P206/12/G151 and 13--00956S, by the European Regional Development Fund and the State Budget of the Czech Republic (RECAMO, CZ.1.05/2.1.00/03.0101) and by MH CZ – DRO (MMCI, 00209805).
The authors declare they have no potential conflicts of interest concerning drugs, products, or services used in the study.
The Editorial Board declares that the manuscript met the ICMJE “uniform requirements” for biomedical papers.Submitted:
20. 1. 2014Accepted:
31. 3. 2014
Autoři: E. Matoulková; B. Vojtěšek
Působiště autorů: Regionální centrum aplikované molekulární onkologie, Masarykův onkologický ústav, Brno
Vyšlo v časopise: Klin Onkol 2014; 27(Supplementum): 82-86
Souhrn
Studium protein‑proteinových interakcí in vivo se v současné době dostává do popředí zájmu – umožňuje prokázat nebo upřesnit již známé protein‑proteinové interakce a odhalit jejich inhibitory, zachytit konformační změny proteinů, objasnit nebo upřesnit signální kaskády v živé buňce s minimálním ovlivněním jejího buněčného prostředí. Jedním z možných přístupů umožňujících tuto charakteristiku jsou metody využívající rezonančního přenosu energie – fluorescenční (FRET) a jeho pozdější modifikace bioluminiscenční (BRET). Tyto metody jsou založeny na zviditelnění proteinových interakcí pomocí excitace fluorescenčních proteinů, ať už světelně nebo enzymaticky. Tyto přístupy umožňují nejen lokalizovat proteiny v buňce nebo jejich organelách (případně i v malých živočiších), ale i kvantifikovat intenzitu fluorescenčního nebo luminiscenčního signálu a odhalit pevnost vazby mezi interakčními partnery. V tomto příspěvku je objasněn princip metod FRET a BRET, jejich konkrétní aplikace při studiu protein‑proteinových interakcí a jsou popsány dosavadní poznatky získané s využitím těchto metod a upřesňující některé molekulární a buněčné mechanizmy a signalizace související s nádorovou biologií.
Klíčová slova:
FRET – BRET – zobrazovací metody – protein‑proteinové interakce in vivoÚvod
Od objevení primární struktury zeleného fluorescenčního proteinu (green fluorescent protein – GFP) v roce 1992 [1] se v posledních 20 letech fluorescenční proteiny a jejich různorodé aplikace stávají nepostradatelnými při zkoumání a popisování molekulárních buněčných dějů, buněčné fyziologie, buněčných interakcí a signalizací v živých buňkách a v malých organizmech. Významný potenciál fluorescenčních proteinů ve srovnání s fluorescenčními značkami tkví v jejich snadné manipulovatelnosti metodami genového inženýrství, která umožňuje jejich snadnou a stabilní expresi v buňkách a organizmech (příprava stabilních buněčných linií i transgenních organizmů) [2,3]. Fluorescenční proteiny je možné konjugovat nebo fúzovat s nejrůznějšími biomolekulami a je tak možné studovat různé typy vazeb – od protein‑proteinových interakcí (antigen ‑ protilátka, ligand ‑ receptor), přes DNA nebo RNA hybridizaci až po vazby proteinu s DNA anebo RNA [4]. Právě exprese fluorescenčních proteinů samotnou buňkou umožňuje sledovat jednotlivé interakce v intaktním buněčném prostředí a reálně tak hodnotit celkový vliv chemických sloučenin (např. léčiv) na živou buňku či organizmus. V současnosti je tento „in vivo“ trend stále častěji využíván farmaceutickými firmami při charakterizaci nových sloučenin s potenciálním terapeutickým účinkem.
Fluorescenční (Försterův) rezonanční přenos energie
Základní a poprvé popsanou metodou využívající fluorescenční proteiny v živých buňkách je fluorescenční (Försterův) rezonanční přenos energie (fluorescence resonance energy transfer – FRET) (obr. 1A). Metoda je založena na přenosu energie mezi dvěma sousedícími fluorescenčními molekulami (fluorofory) – z donoru na akceptor. Fluorofory se liší rozmezím vlnových délek svých emisních a excitačních spekter. Po excitaci donorové molekuly (externím zdrojem monochromatického světla o příslušné vlnové délce) dochází k emisi světla o vlnové délce charakteristické pro daný fluorofor. Takto uvolněná energie ve formě světla je zachycena akceptorovou molekulou a dochází tak k její excitaci a následně i k emisi světla o vlnové délce charakteristické pro akceptorovou molekulu. Světlo emitované akceptorem je finálně zachyceno a jeho intenzita je měřena detektorem, případně jej lze pozorovat mikroskopicky za využití příslušného světelného filtru [5].
Obr. 1. Znázornění mechanizmu rezonančního přenosu energie (proteinů v interakci a bez interakce). 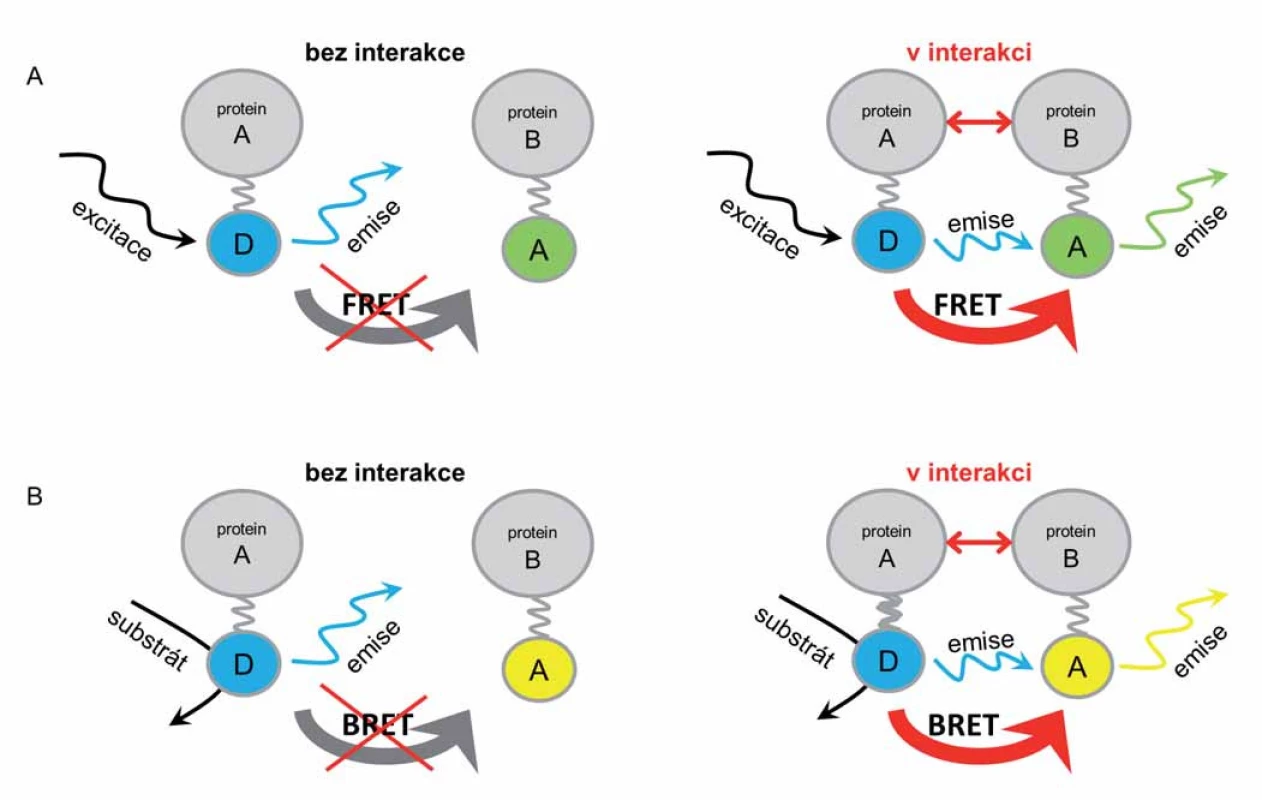
Pro přenos energie mezi dvěma fluorofory je vždy nezbytné dodržet dvě základní podmínky – donor a akceptor musí být v dostatečné vzdálenosti (1 – 10 nm) a musí docházet k částečnému překryvu emisního (donorového) a excitačního (akceptorového) spektra (nejméně z 30 %) [6]. Vzájemná využitelnost a kombinovatelnost jednotlivých fluoroforů je tedy vzhledem k jejich rozdílným emisním a excitačním spektrům omezená. Nejčastěji využívané donorové a akceptorové dvojice fluorescenčních molekul jsou: 1. modrý fluorescenční protein (cyan fluorescent protein – CFP) a žlutý fluorescenční protein (yellow fluorescent protein – YFP), 2. FITC a rhodamin, 3. CFP a červený fluorescenční protein DsRed, 4. modrý fluorescenční protein (blue fluorescent protein – BFP) a GFP, 5. Alexa488 a Cyanin 3 (Cy3), 6. GFP (nebo YFP) a DsRed, 7. Cy3 a Cyanin 5 (Cy5), 8. Alexa488 a Alexa555 [4].
Metodami genového inženýrství je možné jednotlivé fluorofory konjugovat s cílovými proteiny (případně s konkrétními vazebnými doménami) a navrhnout i vytvořit tzv. biosenzory umožňující studovat jednotlivé interakce a vazebné schopnosti těchto proteinů. Rozlišují se biosenzory dvojího typu: 1. intermolekulární (bimolekulární) a 2. intramolekulární (unimolekulární) [7].
Intermolekulární biosenzory jsou tvořeny dvěma molekulami – donorovou a akceptorovou molekulou, které jsou spojeny s vazebnou (donorovou) nebo senzorovou (akceptorovou) doménou (případně proteiny) (obr. 2A). Jsou využívány především při studiu a detekci protein‑proteinových interakcí v buňkách. Jejich výhodou je snadná příprava pomocí dvou plazmidů exprimujících proteiny fúzované s fluorofory, jejichž intenzita signálu je zachytitelná detektorem. Nejsou však vhodné pro rutinní využití, protože měření a kvantifikace FRET ‑ signálu vyžaduje citlivou a rychlou detekci fluorescenčního signálu, který rychle ztrácí svou intenzitu. Nadto dochází ke vzájemné excitaci akceptorových molekul fluoroforu, a tím vytváření falešně pozitivního signálu [6].
Obr. 2. Dva typy biosenzorů: intermolekulární (A) a itramolekulární (B) a schéma jejich přenosu energie. 
Druhým typem biosenzorů jsou intramolekulární biosenzory tvořené jednou molekulou sestávající z akceptorového a donorového fluoroforu navzájem propojených linkerem a konjugovaných s příslušnou vazebnou nebo senzorovou doménou (obr. 2B). Využití tohoto typu slouží ke snazší kvantifikaci v živých systémech než v případě intermolekulárních biosenzorů. Na druhou stranu je obtížnější a zdlouhavější jejich navržení, příprava a následná evaluace systému [5].
Doposud bylo vyvinuto množství intramolekulárních biosenzorů sledujících koncentraci iontů v buňce, sacharidy, fosfolipidy, aktivitu proteinkináz nebo GTPas a další. Byly také navrženy a vytvořeny biosenzory sledující aktivitu onkoproteinů, např. zvýšenou aktivitu Ras v lamelipodiích po stimulaci epidermálním růstovým faktorem (epidermal growth factor – EGF), začlenění c ‑ Raf do plazmatické membrány a vedlejší aktivaci c ‑ Raf po stimulaci EGF nebo zvyšující se fosforylaci CrkII (člen rodiny Crk) po stimulaci EGF [5]. S využitím biosenzorů byla rovněž potvrzena interakce estrogenového receptoru α a transkripčního faktoru Sp1 v živých buňkách. Interakce ERα/ Sp1 byla prokázána při regulaci řady genů asociovaných s buněčnou proliferací a buněčným cyklem [8].
První klinicky využitelný geneticky kódovaný biosenzor byl vyvinut a využit pro detekci kinázové aktivity Bcr ‑ Abl a s ní související citlivostí k terapeutickým inhibitorům u pacientů s chronickou myeloidní leukemií. Aktivita Bcr ‑ Abl byla sledována na základě zviditelnění fosforylace CrkL (nejcharakterističtějšího substrátu Bcr ‑ Abl) přímo v izolovaných BMC a PBMC buňkách z krve pacientů s CML. Tyto navržené biosenzory jsou schopné rozlišit již malé populace buněk rezistentních k terapeutickým inhibitorům, a predikovat tak citlivost pacientů k terapii [9].
Nevýhodou FRET je znesnadnění interpretace výsledků vlivem vzájemné excitace akceptorových fluoroforů a samotným monochromatickým světlem excitujícím donorový fluorofor. Dále dochází k rychlému slábnutí signálu donoru a k buněčné auto fluorescenci způsobené přítomností buněčných organel (mitochondrií a lysozomů) [4,10 – 12].
Bioluminiscenční rezonanční přenos energie
Bioluminiscenční rezonanční přenos energie (bioluminescence resonance energy transfer – BRET) je modifikací metody FRET (obr. 1B). BRET je oproti předchozí metodě zahájen enzymatickou reakcí katalyzovanou donorovou molekulou. To vede k až 10násobnému snížení nežádoucího měřeného signálu pozadí a tím umožňuje detekci až 40krát menšího množství proteinu při dosažení stejné intenzity signálu [13]. Jako donorová molekula není využíván fluorofor, a není tedy potřeba k aktivaci přenosu externí zdroj monochromatického světla. U BRET je donorovou molekulou enzym, který konvertuje specifický substrát a přitom uvolňuje světelnou energii, excitující vhodnou akceptorovou fluorescenční molekulu. Ta následně, stejně jako u FRET, emituje světlo o patřičné vlnové délce a to je finálně zachyceno detektorem [14].
Podmínky pro přenos energie jsou podobné jako u FRET – molekuly musí být v dostatečné vzdálenosti (méně než 10 nm) a emisní spektrum donoru a excitační spektrum akceptoru se musí překrývat. Pokud k interakci mezi sledovanými (fúzovanými proteiny s donorem a akceptorem) molekulami nedochází, je zachycováno pouze světlo vznikající při transformaci substrátu. Interagují‑li fúzované proteiny, dojde k přenosu energie z donoru na akceptor a následně k emisi světla akceptorem. Tak je možné detekovat interakce mezi různými nebo i stejnými proteiny či strukturní a konformační změny proteinu [12].
Metoda BRET byla poprvé popsána v roce 1999 [15] a od té doby bylo vyvinuto několik jejích variant využívajících různé substráty a kombinace donoru a akceptoru. Jednotlivé modifikace jsou označovány jako BRET1, BRET2, BRET3 (v pořadí podle popisu a charakterizace) a nejnovější QD ‑ BRET (tab. 1).
Tab. 1. Přehled různých variant BRET a jejich nejčastějších donorových a akceptorových fluoroforů [2,16−20]. ![Přehled různých variant BRET a jejich nejčastějších donorových a akceptorových fluoroforů [2,16−20].](https://pl-master.mdcdn.cz/media/cache/media_object_image_small/media/image/1e6b46ef2ad6345fffc591151779c539.png)
Původní popsaná varianta je označována jako BRET1 [15]. Donorovou molekulou je luciferáza Rluc (pocházející ze žahavce renila fialová), substrátem pak coelenterazine h (CLZ ‑ h) a jako akceptorová molekula je YFP nebo jeho varianty (topaz, citrine, venus, YPet) [12]. Později byla metoda pozměněna do podoby BRET2 [2], u které se místo CLZ ‑ h využívá jeho analog CLZ ‑ 400a nebo DeepBlueC a v některých případech se používá mutovaná varianta Rluc – Rluc8. Jako akceptor jsou využívány varianty GFP (GFP2 nebo GFP10). Výhoda BRET2 oproti BRET1 je větší vzdálenost emisních rozmezí donorové a akceptorové molekuly, ovšem DeepBlueC jako substrát má asi 100 – 300krát sníženou excitační schopnost (což je možné částečně nahradit mutantem Rluc8, který má přibližně 30krát zvýšenou emisní aktivitu).
Další varianta BRET je BRET3 využívající substrát D ‑ luciferin (D ‑ Luc). Donorovou molekulou je světluščí luciferáza (luc) nebo Rluc8 a akceptorovými molekulami pak DsRed, Cy3, Cy3.5 nebo mOrange [16 – 18]. Předpokládaná výhoda BRET3 je nižší buněčná autofluorescence a trvalejší světelná emise světluščí luciferázy ve srovnání s Rluc. To je ovšem limitováno extrémně nízkými emisními signály a podstatným překrytím donorového a akceptorového emisního maxima.
Nejnověji popsaná a v praxi vyzkoušená modifikace je tzv. QD ‑ BRET [19,20], využívající jako akceptorovou molekulu tzv. quantum dots. Quantum dots jsou polovodičové nanokrystaly excitovatelné v příslušných vlnových délkách. Vlnová délka jimi emitovaného světla pak závisí na jejich průměru a jsou tak schopny pokrýt emisní spektrum od modré až po infračervenou oblast. Nevýhoda této varianty je ovšem velikost nanokrystalů (1,5 – 6 nm) a fakt, že k fúzi sledované molekuly (proteinu) s nanokrystaly nemůže dojít geneticky – nanokrystaly nejsou geneticky kódované, a tak nemohou být produkovány v živých buňkách. Lze je ovšem využít pro značení cílových molekul při in vitro diagnostice. Velká výhoda této metody je bezesporu jasná separace donorových a akceptorových emisních spekter [12].
V dnešní době je BRET považována za jednu z nejuniverzálnějších metod pro studium protein‑proteinových interakcí v živých buňkách. Abnormální funkce (hyperaktivace nebo inhibice) proteinů je často pozorována u různých závažných onemocnění (např. nádorová nebo neurodegenerativní onemocnění). Řada studií tuto metodu využívá: 1. pro screening nových receptorových ligandů a jejich vliv na aktivitu receptoru; 2. pro sledování aktivity enzymů – proteázové, kinázové; 3. pro sledování a identifikace protein‑proteinových interakcí a jejich inhibitorů nebo 4. pro popsání signálních buněčných drah [12,21 – 23]. Slouží tak především k identifikaci bioaktivních sloučenin ovlivňujících buněčné vlastnosti.
Závěr
Metoda FRET a její modifikace BRET jsou v současné době intenzivně se rozvíjející metody a spolu s technickým pokrokem v oblastech mikroskopického zobrazování a vysoce citlivé i přesné detekce světelného záření o různých vlnových délkách umožňují sledovat protein‑proteinové interakce a konformační změny proteinů v živých buňkách nebo malých organizmech prostorově a v reálném čase s minimálním zásahem do buněčného prostředí [3]. Vzhledem k nutnosti genového inženýrství při přípravě jednotlivých FRET ‑ nebo BRET ‑ biosenzorů a při přípravě FRET ‑ nebo BRET ‑ fluoroforů fúzovaných se sledovanými proteiny je využití těchto metod v klinické praxi prozatím obtížné, i když první klinická aplikace již byla publikována [9]. Nicméně tyto přístupy studia proteinových interakcí in vivo začínají být hojněji využívány při sledování, testování a ověřování vlivu různých doposud necharakterizovaných chemických látek a sloučenin a jejich inhibitorů na buňku nebo živý organizmus (myši). Stejně tak začínají být tyto metody uplatňovány při sledování účinku potenciálních léčiv využitelných nejen ve farmaceutickém průmyslu [24].
Práce byla podpořena granty GA ČR P206/12//G151 a GA ČR 13-00956S, Evropským fondem pro regionální rozvoj a státním rozpočtem České republiky (OP VaVpI – RECAMO, Z.1.05/2.1.00/03.0101) a MZ ČR – RVO (MOÚ, 00209805).
Autoři deklarují, že v souvislosti s předmětem studie nemají žádné komerční zájmy.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
Mgr. Eva Matoulková
Regionální centrum aplikované molekulární onkologie
Masarykův onkologický ústav
Žlutý kopec 7
656 53 Brno
e-mail: eva.matoulkova@mou.cz
Obdrženo: 20. 1. 2014
Přijato: 31. 3. 2014
Zdroje
1. Prasher DC, Eckenrode VK, Ward WW et al. Primary structure of the Aequorea victoria green ‑ fluorescent protein. Gene 1992; 111(2): 229−233.
2. Bertrand L, Parent S, Caron M et al. The BRET2/ arrestin assay in stable recombinant cells: a platform to screen for compounds that interact with G protein‑coupled receptors (GPCRS). J Recept Signal Transduct Res 2002; 22(1−4): 533 – 541.
3. De A, Loening AM, Gambhir SS. An improved bioluminescence resonance energy transfer strategy for imaging intracellular events in single cells and living subjects. Cancer Res 2007; 67(15): 7175−7183.
4. Zadran S, Standley S, Wong K et al. Fluorescence resonance energy transfer (FRET)‑based biosensors: visualizing cellular dynamics and bioenergetics. Appl Microbiol Biotechnol 2012; 96(4): 895 – 902. doi: 10.1007/ s00253 - 012--4449 - 6.
5. Aoki K, Komatsu N, Hirata E et al. Stable expression of FRET biosensors: a new light in cancer research. Cancer Sci 2012; 103(4): 614 – 619. doi: 10.1111/ j.1349 - 7006.2011.02196.x.
6. Day RN, Davidson MW. Fluorescent proteins for FRET microscopy: monitoring protein interactions in living cells. Bioessays 2012; 34(5): 341 – 350. doi: 10.1002/ bies.201100098.
7. Kiyokawa E, Hara S, Nakamura T et al. Fluorescence (Förster) resonance energy transfer imaging of oncogene activity in living cells. Cancer Sci 2006; 97(1): 8 – 15.
8. Kim K, Barhoumi R, Burghardt R et al. Analysis of estrogen receptor alpha ‑ Sp1 interactions in breast cancer cells by fluorescence resonance energy transfer. Mol Endocrinol 2005; 19(4): 843 – 854.
9. Mizutani T, Kondo T, Darmanin S et al. A novel FRET‑based biosensor for the measurement of BCR ‑ ABL activity and its response to drugs in living cells. Clin Cancer Res 2010; 16(15): 3964 – 3975. doi: 10.1158/ 1078 – 0432.CCR ‑ 10 - 0548.
10. Boute N, Jockers R, Issad T. The use of resonance energy transfer in high‑throughput screening: BRET versus FRET. Trends Pharmacol Sci 2002; 23(8): 351 – 354.
11. Sturmey RG, O’Toole PJ, Leese HJ. Fluorescence resonance energy transfer analysis of mitochondrial: lipid association in the porcine oocyte. Reproduction 2006; 132(6): 829 – 837.
12. Bacart J, Corbel C, Jockers R et al. The BRET technology and its application to screening assays. Biotechnol J 2008; 3(3): 311−324. doi: 10.1002/ biot.200700222.
13. Arai R, Nakagawa H, Tsumoto K et al. Demonstration of a homogeneous noncompetitive immunoassay based on bioluminescence resonance energy transfer. Anal Biochem 2001; 289(1): 77 – 81.
14. Xia Z, Rao J. Biosensing and imaging based on bioluminescence resonance energy transfer. Curr Opin Biotechnol 2009; 20(1): 37−44. doi: 10.1016/ j.copbio.2009.01.001.
15. Xu Y, Piston DW, Johnson CH. A bioluminescence resonance energy transfer (BRET) system: application to interacting circadian clock proteins. Proc Natl Acad Sci USA 1999; 96(1): 151−156.
16. Arai R, Nakagawa H, Kitayama A et al. Detection of proteinprotein interaction by bioluminescence resonance energy transfer from firefly luciferase to red fluorescent protein. J Biosci Bioeng 2002; 94(4): 362 – 364.
17. Yamakawa Y, Ueda H, Kitayama A et al. Rapid homogeneous immunoassay of peptides based on bioluminescence resonance energy transfer from firefly luciferase. J Biosci Bioeng 2002; 93(6): 537 – 542.
18. Loening AM, Wu AM, Gambhir SS. Red ‑ shifted Renilla reniformis luciferase variants for imaging in living subjects. Nat Methods 2007; 4(8): 641 – 643.
19. De A, Ray P, Loening AM, Gambhir SS. BRET3: A red ‑ shifted bioluminescence resonance energy transfer (BRET)‑based integrated platform for imaging protein‑protein interactions from single live cells and living animals. FASEB J 2009; 23(8): 2702 – 2709. doi: 10.1096/ fj.08 - -118919.
20. Yao H, Zhang Y, Xiao F et al. Quantum dot/ bioluminescence resonance energy transfer based highly sensitive detection of proteases. Angew Chem Int Ed Engl 2007; 46(23): 4346−4349.
21. Boute N, Pernet K, Issad T. Monitoring the activation state of the insulin receptor using bioluminescence resonance energy transfer. Mol Pharmacol 2001; 60(4): 640 – 645.
22. Gavet O, Pines J. Progressive activation of Cyclin B1 - Cdk1 coordinates entry to mitosis. Dev Cell 2010; 18(4): 533 – 543. doi: 10.1016/ j.devcel.2010.02.013.
23. Couturier C, Deprez B. Setting up a bioluminescence resonance energy transfer high throughput screening assay to search for protein/ protein interaction inhibitors in mammalian cells. Front Endocrinol (Lausanne) 2012; 3 : 100. doi: 10.3389/ fendo.2012.00100.
24. Aoki K, Kamioka Y, Matsuda M. Fluorescence resonance energy transfer imaging of cell signaling from in vitro to in vivo: basis of biosensor construction, live imaging, and image processing. Dev Growth Differ 2013; 55(4): 515−522. doi: 10.1111/ dgd.12039.
Štítky
Dětská onkologie Chirurgie všeobecná Onkologie
Článek vyšel v časopiseKlinická onkologie
Nejčtenější tento týden
2014 Číslo Supplementum- Ibrance® – nová šance pro pacientky s HR+/HER2– karcinomem prsu
- Vliv alkoholu na riziko vzniku karcinomu prsu, nově podle histologického typu nádoru a jeho senzitivity k estrogenovým receptorům
- Ženy s falešně pozitivním nálezem na mamografii pociťují zvýšenou úzkost a sníženou kvalitu života
- Exemestan zlepšuje interval bez relapsu při karcinomu prsu
- Přítomnost genetické mutace BRCA vede k častějšímu výskytu rakoviny i ve druhém prsu
-
Všechny články tohoto čísla
- Analýza proteinů pomocí hmotnostní spektrometrie
- p‑ SRM, SWATH a HRM – cílené proteomické přístupy na hmotnostním spektrometru TripleTOF 5600+ a jejich aplikace v onkologickém výzkumu
- Analýza fosfoproteínov a signálnych dráh kvantitatívno‑ proteomickými metódami
- Nové trendy ve studiu glykosylace proteinů u onkologických onemocnění
- Současné trendy ve využívání PET radiofarmak k onkologické diagnostice
- „Techneciová krize“ – příčiny, možná řešení a dopad na diagnostiku planární scintigrafií a SPECT
- Vitamin D jako významný steroidní hormon u karcinomu prsu
- Využití průtokové cytometrie pro analýzu mitochondriální buněčné smrti
- Soutěž o nejlepší práci
- Metody studia buněčné migrace a invazivity nádorových buněk
- Možnosti studia transendoteliální migrace in vitro
- Editorial
- Mechanizmy lékové rezistence a nádorové kmenové buňky
- Funkční testy pro detekci nádorových kmenových buněk
- Mikroprostředí nádoru – možnosti výzkumu v podmínkách in vitro
- Elektrochemická analýza nukleových kyselin, bílkovin a polysacharidů v biomedicíně
- Sekvenování nové generace a možnosti jeho využití v onkologické praxi
- Vývoj metod založených na PCR a jejich aplikace v onkologickém výzkumu a praxi
- Programovaná buněčná smrt v nádorových buňkách
- Metody pro studium protein‑proteinových a protein‑ligandových interakcí
- Detekce protein‑proteinových interakcí metodami FRET a BRET
- Detekce proteinů, proteinových interakcí a modifikací s využitím „proximity ligation assay“ in situ
- Exprese a purifikace proteinů
- Kvantitativní hmotnostní spektrometrie a její využití v onkologii
- Klinická onkologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Exprese a purifikace proteinů
- Metody studia buněčné migrace a invazivity nádorových buněk
- Sekvenování nové generace a možnosti jeho využití v onkologické praxi
- Analýza proteinů pomocí hmotnostní spektrometrie
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Revma Focus: Spondyloartritidy
nový kurz
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Autoři: prof. MUDr. Pavel Horák, CSc., doc. MUDr. Ludmila Brunerová, Ph.D., doc. MUDr. Václav Vyskočil, Ph.D., prim. MUDr. Richard Pikner, Ph.D., MUDr. Olga Růžičková, MUDr. Jan Rosa, prof. MUDr. Vladimír Palička, CSc., Dr.h.c.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



