-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Kompresívne vertebrálne fraktúry u detí s Crohnovou chorobou: kazuistiky
Vertebral compression fractures in pediatric patients with Crohn´s disease: case reports
Alterations in bone metabolism are a common complication of inflammatory bowel disease. In pediatric patients, the changes present themselves as growth retardation, decrese in bones mass with changes of its microstructure. Pathological changes can be seen already at the time of diagnosis of primary disease. Pathogenesis of bone loss is multifactorial. Symptoms of skeletal involvement include severe bone pain, backache, kyphosis and fractures. In the article, we present two interesting case reports of adolescents with osteoporosis and vertebral compression fractures that have been manifested during Crohn’s disease.
Keywords:
body mass index – Crohn’s disease – vertebral compression fractures
Autoři: Čagalová Alžbeta 1; Čierna Iveta 1; Tichá Ľubica 1; Trepáč Martin 2; Podracká Ľudmila 1
Působiště autorů: Detská klinika LF UK a Národný ústav detských chorôb, Bratislava 1; Ortopedická klinika LF UK a Národný ústav detských chorôb, Bratislava 2
Vyšlo v časopise: Clinical Osteology 2018; 23(3): 126-131
Kategorie: Kazuistika
Souhrn
Porucha kostného metabolizmu je častou komplikáciou nešpecifického zápalového ochorenia čreva. U detí sa manifestuje poruchou rastu a úbytkom kostnej masy so zmenou mikroarchitektúry kosti už v čase diagnostiky primárneho ochorenia. Patogenéza straty kostnej hmoty je multifaktoriálna. K symptomatickým prejavom postihnutia skeletu patria úporné bolesti kostí, chrbta, kyfóza a fraktúry. V článku uvádzame dve zaujímavé kazuistiky mladistvých s výraznou osteoporózou a kompresívnymi vertebrálnymi fraktúrami, ktoré sa manifestovali v priebehu Crohnovej choroby.
Klíčová slova:
deti – kompresívne fraktúry stavcov – kostný metabolizmus
Úvod
Porucha kostného metabolizmu je častou komplikáciou nešpecifického zápalového ochorenia čreva (inflammatory bowel disease – IBD) u detí aj dospelých. Chronický zápal, malnutrícia a liečba systémovými glukokortikoidmi majú závažné dôsledky na rastúci skelet a potenciálne ohrozujú normálny telesný rast a pubertálny vývoj. Až 25 % všetkých prípadov IBD začína v detstve alebo v puberte, v ktorej vrcholí budovanie kostnej masy (Peak Bone Mass – PBM) a tvorí sa 40 % objemu celkovej kostnej hmoty [1]. Kosť v tomto období „naberá“ na lineárnej dĺžke aj objeme, preto neadekvátna tvorba zásadne ovplyvňuje celkové kostné zdravie jedinca. Prospektívne štúdie demonštrovali, že deti s IBD nedosiahnu optimálny PBM a čelia už v období dospievania vyššiemu riziku vzniku vertebrálnych fraktúr [2].
Patogenéza kostných strát asociovaných s IBD je multifaktoriálna. K primárnym faktorom patrí nadmerná tvorba zápalových cytokínov, ktorá inhibuje formáciu kosti a zvyšuje kostnú rezorpciu [3]. Nemenej dôležitú úlohu majú sekundárne dôsledky základného ochorenia, ako je slabý kalorický príjem a malabsorpcia, znížená fyzická aktivita, oneskorená puberta či rezistencia cieľových orgánov na anabolické rastové faktory, ako aj nepriaznivé účinky systémovej glukortikoidnej liečby [4]. Preto deti s IBD majú často poruchu rastu a úbytok kostnej masy so zmenou mikroarchitektúry už v čase diagnostiky primárneho ochorenia [5]. K symptomatickým prejavom postihnutia skeletu patria úporné bolesti kostí, chrbta, kyfóza a fraktúry. Z hľadiska anatomickej lokalizácie sú prekvapivo najčastejšie postihnuté stavce, potom femur a klavikula [6].
V článku uvádzame dve zaujímavé kazuistiky mladistvých s výraznou osteoporózou a kompresívnymi vertebrálnymi fraktúrami, ktoré sa manifestovali v priebehu Crohnovej choroby.
Kazuistika 1
V prvej kazuistike prezentujeme 15-ročné dievča s recidivujúcim vracaním a úpornými bolesťami v epigastriu, ktoré viedli k dramatickému hmotnostnému úbytku. Pacientka rapídne chradla a v priebehu 2 rokov schudla až 20 kg. Auxologické parametre pri prijatí na naše pracovisko zodpovedali kachexii. Telesná hmotnosť bola 36 kg (Z-skóre -2,24 SD) a BMI 13,55 kg/m2 (Z-skóre -2,92 SD), telesná výška 163 cm (50. percentil), prediktívna výška podľa výšky rodičov bola 166 cm (50. percentil). Sekundárne pohlavné znaky zodpovedali 4.–5. vývojovému štádiu podľa Tannera (prsníky 4. vývojové štádium, ochlpenie 5. štádium). Dievča malo sekundárnu amenoreu 48 mesiacov.
V krvnom obraze bola prítomná mikrocytová hypochrómna anémia: Hb 11,6 g/dl, MCV 73,3 fl, MCH 23,5 pg, v biochemických parametroch len mierna hypoalbuminémia 33,6 g/l.
Pri ezofagogastroduodenoskopii sa znázornil extrémne dilatovaný žalúdok s veľkým množstvom natrávenej potravy. V prepylorickej oblasti a v pylorickom kanáli boli hlboké plošné ulcerácie s pseudopolypóznou okolitou sliznicou obturujúcou celý pylorický kanál (obr. 1). Koloskopicky sa nepozorovali makroskopické patologické zmeny na sliznici hrubého čreva a terminálneho ilea, ale na MRI-enterografii sa v distálnej časti duodena, v jejune a proximálnom ileu zobrazilo rozsiahle zápalové postihnutie. Biopsia z ložísk potvrdila Crohnovu chorobu.
Obr. 1. Gastroskopický obraz – Crohnova choroba v oblasti pyloru 
Pre prekážku v pylorickom kanáli bola pacientke zavedená jejunálna sonda a podávaná výlučne oligomérna enterálna výživa. Po zabezpečení a tolerovaní výlučnej enterálnej výživy sme ukončili 3-mesačnú terapiu kortikoidmi a indikovali biologickú liečbu adalimumabom. Pacientka pribrala, ustúpili bolesti brucha, ale udávala pretrvávajúce bolesti v torakolumbálnej oblasti vyžadujúce analgetiká.
CT-vyšetrenie hrudnej chrbtice odhalilo difúznu porózu, dextrokonverznú kyfoskoliózu a kompresívne fraktúry stavcov Th6, Th7, Th9 a Th12 (obr. 2). Denzitometrickým vyšetrením (DXA) sa potvrdila nižšia hustota kostného minerálu v oblasti lumbálnej chrbtice, BMD Z-skóre -2,3 SD vzhľadom k veku, pohlaviu a výške pacientky. Z-skóre celotelovej denzity bolo signifikantne nízke -3,5 SD (tab. 1).
Obr. 2. CT-vyšetrenie chrbtice (kazuistika 1) 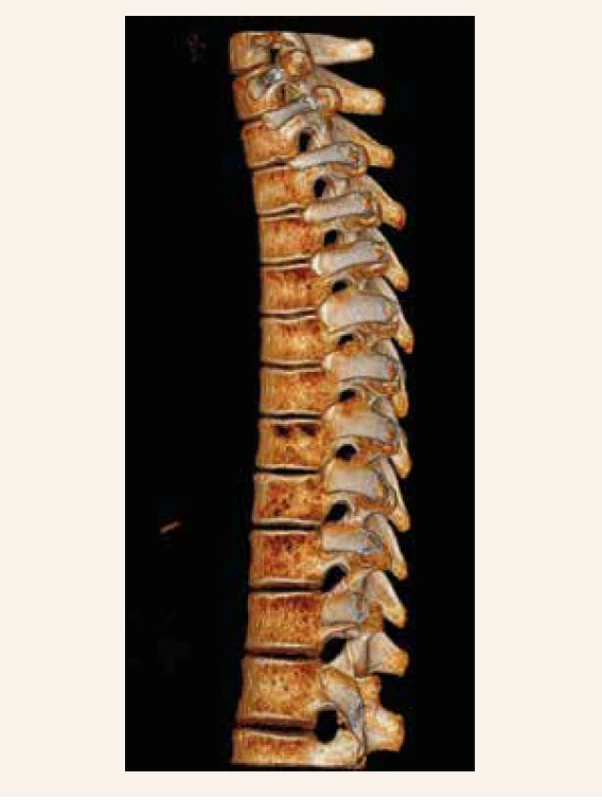
Tab. 1. Výsledky DXA (kazuistika 1) 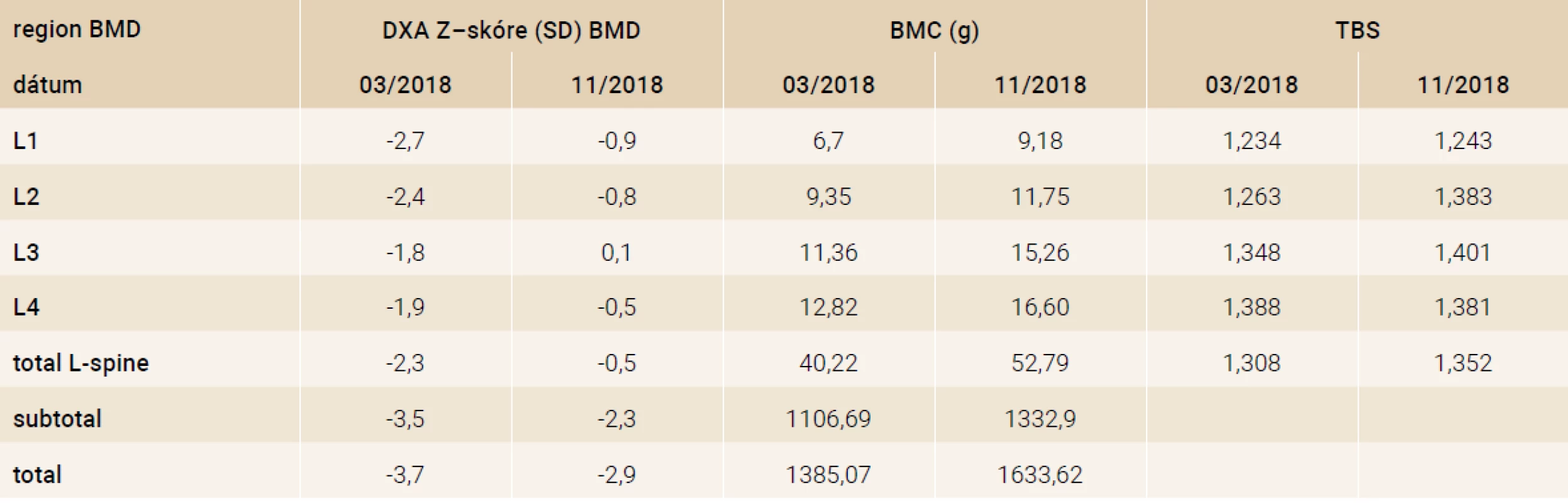
BMC – obsah kostného minerálu/Bone Mineral Content BMD – hustota kostného minerálu/Bone Minerel Density DXA – denzitometria/DXA (Dual-energy X-ray Absorptiometry) TBS – trabekulárne kostné skóre/Trabecular Bone Score SD – štandardná odchýlka/Standard Deviation Markery kostného metabolizmu (ALP 1,44 μkat/l, Ca 2,35 mmol/l, P 1,84 mmol/l, Mg 0,78 mmol/l, Ca/kreat v moči 0,41 mmol/mmol), koncentrácie 25-OH vitamínu D (34,4 ng/ml) a intaktného parathormónu (27,30 pg/ml) boli v referenčnom pásme (tab. 2). K celkovej liečbe sme indikovali ergokalciferol (300 tis IU i.m.), kalcium (4 × 250 mg denne) a bisfosfonáty (kyselina zolendrónová v dávke 0,05 mg/kg). Pravidelná rehabilitácia a korzet efektívne prispeli k spevneniu skeletu a čiastočnej úprave zakrivenia chrbtice. Pacientka v priebehu 6 mesiacov pribrala na hmotnosti (59,5 kg/ +23,5 kg), upravil sa klinický stav a ustúpili chronické bolesti chrbta.
Tab. 2. Laboratórne výsledky (kazuistika 1) 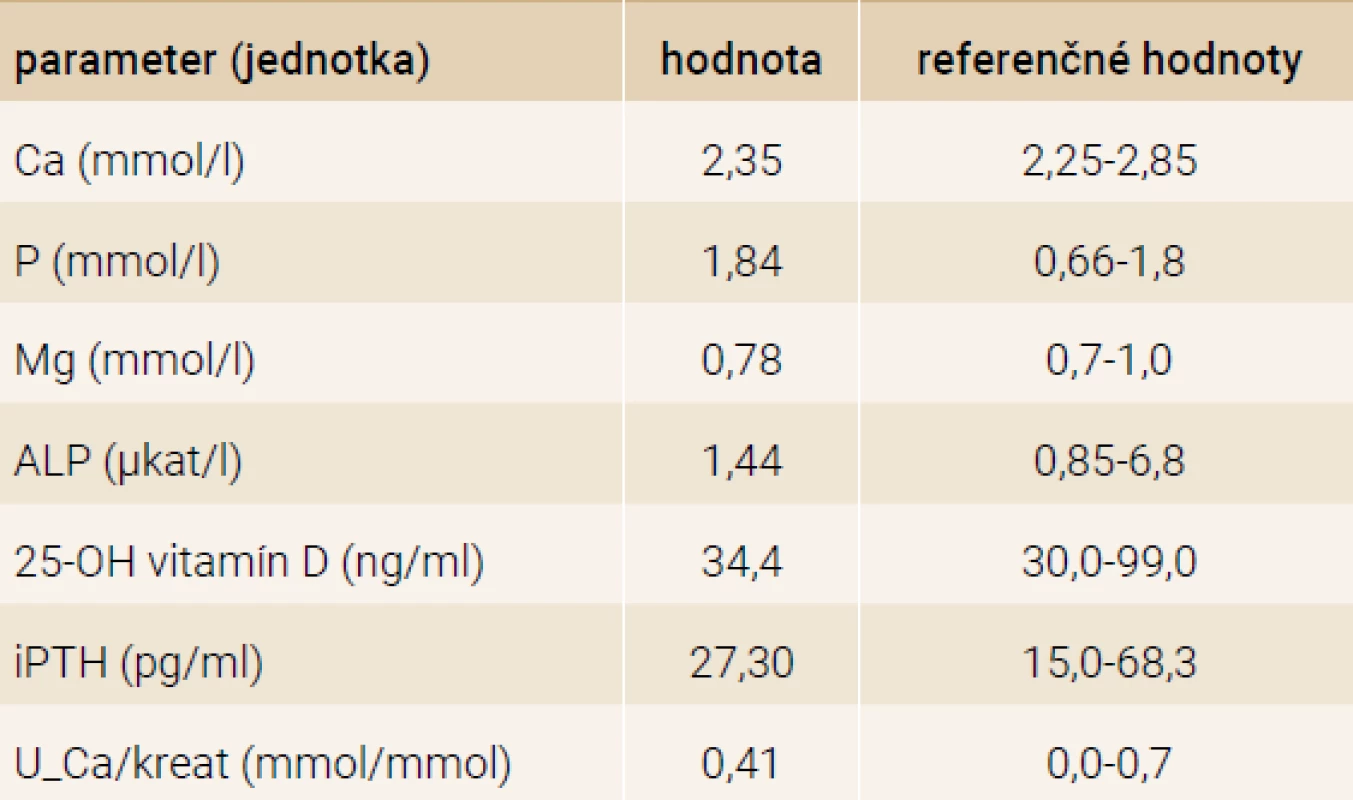
Kontrolné denzitometrické vyšetrenie potvrdilo zlepšenie BMD vo všetkých meraných oblastiach. Z-skóre lumbálnej chrbtice sa zvýšilo z -2,3 SD na -0,5 SD, Z-skóre celotelovej denzity z hodnoty -3,5 SD na -2,3 SD, čo zodpovedá nárastu kostnej hmoty v lumbálnej oblasti o 17 % a v celotelovej oblasti o 7 % (tab. 1).
Kazuistika 2
V druhej kazuistike opisujeme zaujímavý prípad 12-ročného chlapca, ktorý bol odoslaný na naše pracovisko pre dlhotrvajúce bolesti brucha, riedke stolice s prímesou hlienu, výrazný hmotnostný úbytok 10 kg a zvýšenú únavnosť. Chlapec bol vysoký 147 cm, čo v rastovom grafe predstavuje 3. percentil (Z-skóre výšky -0,85 SD), pričom predikcia jeho finálnej výšky podľa výšky rodičov bola 182,5 cm, čo zodpovedá 50. percentilu. Hmotnosť mal 41,8 kg, BMI 19,3 (-0,44SD). Sexuálny vývin podľa Tanera bol vo 4. štádiu.
V laboratórnom obraze dominovala vysoká zápalová aktivita (CRP 184 mg/l, fekálny kalprotektín > 1800 μg/g), anémia: Hb 109g/l, MCV 67 fl, MCH 21,3 pg a hypoalbuminémia 27mg/l.
Pre podozrenie na nešpecifický zápal čreva sme indikovali eozofagogastroduodenoskopiu a kolonoskopiu. Endoskopicky sa našli početné aftózne lézie na sliznici pažeráka a v prepylorickej oblasti, pri koloskopii sa pozorovali segmentálne zápalové zmeny s hlbokými nepravidelnými ulceráciami v oblasti rekta, kolon sigmoideum ako aj v céku a terminálnom ileu, čo je charakteristické pre Crohnovu chorobu, ktorá sa histologicky verifikovala.
U pacienta sme začali výlučnú enterálnu výživu polymérnou enterálnou diétou spolu s imunosupresívnou liečbou azatioprinom. Subjektívne sa cítil lepšie, ale pretrvávala zvýšená zápalová aktivita (CRP 34 mg/l), riedke stolice a vytvorila sa perianálna fistula. Pre nedostatočný efekt sa nasadili kortikosteroidy a následne biologická liečba infliximabom. Ani po mesiaci užívania kortikoidov nedošlo k úprave klinického stavu, naopak, pridružili sa úporné bolesti chrbta s obmedzenou hybnosťou, preto sme indikovali výpočtové tomografické vyšetrenie (Computed Tomography – CT).
CT-sken hrudnej a lumbálnej chrbtice (obr. 3) zobrazil výraznú porózu skeletu a viacpočetné kompresie tiel stavcov (najmä Th6-Th8, L1 a L3). Z-skóre denzity kostného minerálu lumbálnej chrbtice bolo -2,1 SD, a celotelová denzita -1,2 SD. Trabekulárne kostné skóre 1,322 nesvedčilo pre porušenú mikroarchitektúru kosti (tab. 3).
Obr. 3. CT-vyšetrenie chrbtice (kazuistika 2) 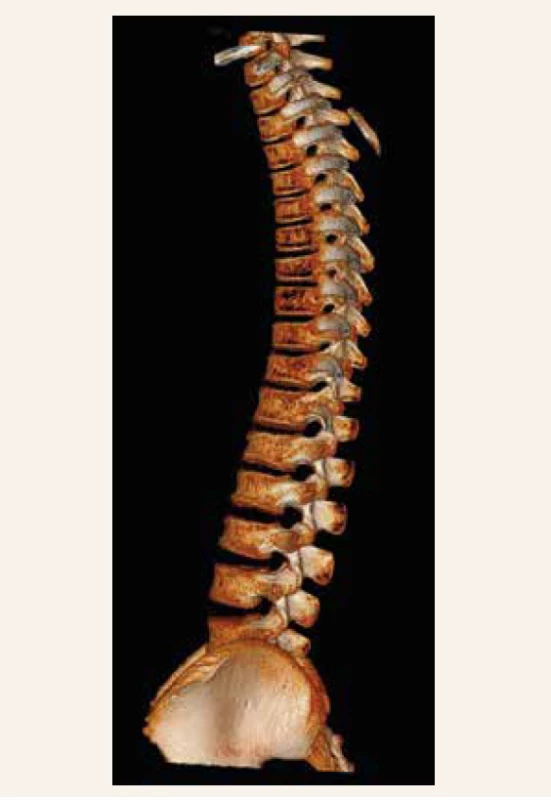
Tab. 3. Výsledky DXA (kazuistika 2) 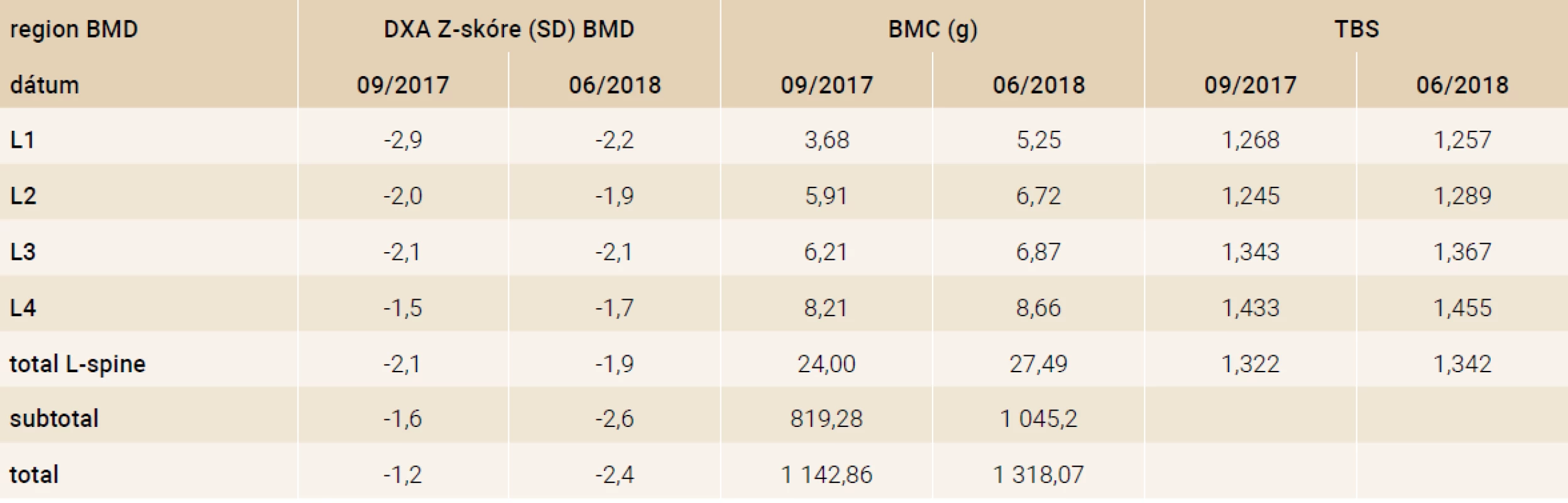
BMC – obsah kostného minerálu/Bone Mineral Content BMD – hustota kostného minerálu/Bone Minerel Density DXA – denzitometria/DXA (Dual-energy X-ray Absorptiometry) TBS –trabekulárne kostné skóre/Trabecular Bone Score SD – štandardná odchýľka/Standard Deviation V laboratórnych parametroch bola prítomná hypovitaminóza D (25-OH vitamín D 22,1 ng/ml) a znížený iPTH (11,00 pg/ml), ostatné markery kostného metabolizmu (Ca 2,26 mmol/l, P 1,45 mmol/l, ALP 1,74 μkat/l, Ca/kreat v moči 0,50 mmol/mmol) boli v referenčnom rozmedzí (tab. 4). V liečbe sme navýšili perorálnu substitúciu kalcia (2 x 250 mg denne), pridali vitamín D (1 200 IU denne) a indikovali bisfosfonát (kyselina zolendrónová v dávke 0,05 mg/kg).
Tab. 4. Laboratórne výsledky (kazuistika 2) 
Po roku sa stav pacienta výrazne zlepšil, nemá bolesti chrbta, pribral (62,7 kg/+20 kg), vyrástol 11 cm/rok, čo zlepšilo lineárny rast v rastovom grafe z 3. na 10. percentil. Kontrolné denzitometrické vyšetrenie v oblasti lumbálnej chrbtice preukázalo čiastočné zlepšenie hustoty kostného minerálu, Z-skóre sa zvýšilo z -2,1 na -1,9 SD (tab. 3).
Diskusia
Detstvo a dospievanie je pre tvorbu a mineralizáciu kosti kritické obdobie. Až 40 % z celkového objemu kostnej hmoty sa buduje do 18. roku života [1]. Preto narušenie dynamickej rovnováhy v procesoch tvorby kostnej hmoty zásadne ovplyvní kostné zdravie v krátkodobom aj dlhodobom horizonte.
Chronické zápalové ochorenia gastrointestinálneho traktu sú spojené s viacerými rizikovými faktormi, ktoré nepriaznivo interferujú s apozíciou kostnej matrix a remodeláciou kosti. Patogenéza straty kostnej hmoty u detí s IBD je komplexná. Dysregulácia medzi osteoformačnými a osteoresorpčnými mechanizmami môže spôsobiť poruchu vývoja lineárneho rastu kostí a úbytok kostnej hmoty. Nízka hustota kostného minerálu (Z-skóre ≤ -2 SD) u detí s IBD sa vyskytuje až v 40 % [7]. Hoci podľa epidemiologických dát prevalencia fraktúr dlhých kostí u detí s IBD starších ako 12 rokov nemusí byť zvýšená, títo jedinci sú vystavení signifikantne vyššiemu riziku vertebrálnych fraktúr ako ich zdraví rovesníci [6]. Dokumentujú to aj kazuistiky našich pacientov so symptomatickými viacpočetnými kompresiami stavcov.
Iniciálny etiologický inzult, ktorý spúšťa poruchu kostného metabolizmu u pacientov s IBD, je chronický intestinálny zápal s nadmernou produkciou proinflamatórnych cytokínov. TNFα stimuluje diferenciáciu a aktiváciu osteoklastov a inhibíciou apoptózy výrazne predlžuje ich viabilitu, čo signifikantne zvyšuje resorpciu kosti. Navyše, TNFα tlmí diferenciáciu osteoblastov a novotvorbu kosti [3]. Názorne to ilustruje klinický vývoj a torpídny priebeh základného ochorenia u našich pacientov. Výrazná gastrointestinálna symptomatológia pretrvávala niekoľko rokov, kým sa diagnostikovala Crohnova choroba. Dominantný vplyv chronického intenzívneho zápalu na rozvoj osteoporózy možno predpokladať najmä u nášho druhého pacienta s vysokou aktivitou špecifických diagnostických markerov (CRP, fekálny kalprotektín).
Silný dôkaz v prospech „osteotoxicity“ zápalového millieu na rastúci skelet demonštruje v literatúre publikovaný unikátny prípad 12-ročného chlapca, u ktorého bola kyfóza, progresívna netraumatická bolesť chrbta a extenzívna osteoporóza s viacpočetnými fraktúrami hrudných a driekových stavcov prítomná v čase diagnostikovania Crohnovej choroby [8]. To dokumentuje, že pri IBD môže dochádzať k masívnemu úbytku kostnej hmoty aj bez kortikoidnej liečby. Z tohto aspektu je pozoruhodné, že ani v americkej pediatrickej kohorte s IBD sa nezistila signifikantná asociácia medzi výskytom fraktúr a expozíciou kortikoidom [6].
Na druhej strane, škodlivý vplyv glukokortikoidov na kostný metabolizmus je roky dobre preštudovaný, hoci minimálna „prahová“ dávka kortikoidov, ktorá poškodzuje štruktúru kosti, nie je presne známa. Najzraniteľnejším obdobím, kedy glukokortikoidy môžu zapríčiniť ireverzibilnú stratu kosti, je puberta (Tanner štádium 2–4) [4]. Glukokortikoidy zvyšujú resorpciu kosti, vyvolávajú dysfunkciu osteoblastov a ich predčasnú apoptózu [9]. Tiež nezanedbateľný je ich zásah do endokrinnej regulácie metabolizmu kalcia v čreve a obličkách. Tieto patomechanizmy negatívne pôsobia najmä na trabekulárnu kosť, ktorá tvorí stavce chrbtice. Aj naši pre/pubertálni pacienti s osteoporózou a vertebrálnymi fraktúrami užívali systémové kortikoidy, čo mohlo potencovať stratu kostnej hmoty.
Pubertálny rastový špurt vyžaduje bohatý príjem energie. Deti s IBD trpia chronickým nechutenstvom so sprievodným úbytkom telesnej hmotnosti. Pacientka opísaná v prvej kazuistike schudla až 20 kg a mala sekundárnu amenoreu, kým sa diagnostikovalo základné ochorenie. Pri dlhom nutričnom „hladovaní“ nastupujú adaptačné hormonálne zmeny, vrátane dysbalancie pohlavných hormónov, ktoré sú dôležité pre normálnu mineralizáciu kosti. Estrogén inhibuje osteoklastami indukovanú resorpciu a má anabolický efekt na kosť. Pri hladovaní hladina estrogénu klesá, znižuje sa jeho osteoprotektívny účinok a stupňuje sa osteoresorpcia [10].
Kumulácia „skeleto-toxických“ faktorov asociovaných s IBD sa môže prejaviť buď včasne, čo vedie k zníženiu hustoty kostného minerálu, alebo sa manifestuje oneskorene, ak sa nedosiahne adekvátny PBM v období detstva a dospievania. Dospelí pacienti so začiatkom IBD v detstve majú podľa štúdií signifikantne vyššie riziko zlomenín (odds ratio 1,6) ako chorí s vývojom ochorenia v dospelosti [11]. Zaujímavý a prekvapivý je vyšší trend k fraktúram stavcov než dlhým kostiam [6]. Vyplýva to z obsiahlej epidemiologickej štúdie, ktorá mapovala incidenciu zlomenín vo veľkej kohorte 1 242 pediatrických pacientov s IBD. Vertebrálne fraktúry sú najčastejšou lokalizáciou osteoporotických zlomenín v pediatrickej populácií zrejme preto, že trabekulárna kosť je vulnerabilnejšia ako pevnejšie kostné tkanivo rastúcich dlhých kostí obklopené objemnou muskulatúrou. V súlade s týmto predpokladom sú aj výsledky denzitometrického vyšetrenia našich pacientov. Obaja pacienti mali patologickú odchýlku Z-skóre v oblasti lumbálnej chrbtice, a to ≤ -2 SD (-2,3; -2,1 SD). Trabekulárne kostné skóre (TBS 1,302; 1,322) poukazuje na normálnu kvalitu kosti. Príčinou fraktúr bola teda zhoršená denzita kostného minerálu, a nie zhoršená kvalita kosti [12]. Kompresívne fraktúry stavcov sa manifestovali krátko po diagnostikovaní Crohnovej choroby, čo podčiarkuje dôležitosť vyšetrenia kostných markerov a kostnej denzity už v úvode ochorenia.
Európska spoločnosť pre detskú gastroenterológiu, hepatológiu a výživu (European Society for Paediatric Gastroenterology Hepatology and Nutrition – ESPGHAN) odporúča u všetkých detí s IBD pravidelne monitorovať kostný metabolizmus vrátane denzitometrie a do liečebných protokolov IBD implementovala opatrenia na prevenciu kostných strát [13].
Potlačenie intenzívneho zápalu, dostatočný prísun mikronutrientov (vitamín D, K, vápnik a zinok) a vhodná fyzická aktivita môžu minimalizovať nepriaznivé účinky na kostný metabolizmus.
U detí s nízkou BMD a symptomatickými zlomeninami je indikovaná antiresorpčná liečba bisfosfonátmi [13]. Aká je optimálna voľba, dávka, či dĺžka terapie bisfosfonátmi u detí je stále predmetom diskusií a vyžaduje prospektívne longitudinálne štúdie. Avšak ako demonštrujú opísané kazuistické prípady, včasná komplexná liečba môže osteoporózu zmierniť už v relatívne krátkom čase, čo svedčí pre dobrú reštitučnú kapacitu „mladej“ rastúcej kosti v štádiu mineralizácie [8].
Záver
Deti s IBD sú obzvlášť vulnerabilné na negatívne vplyvy základného ochorenia a vedľajšie účinky chronickej liečby. Obavy pediatrov vyvoláva najmä postihnutie skeletu, ktoré z longitudinálneho hľadiska patrí k najzávažnejším sprievodným komplikáciám IBD. Prevalencia poruchy kostnej hmoty u detí s IBD je vysoká a môže byť prítomná už v čase diagnostikovania primárneho ochorenia. U všetkých detí a dospievajúcich s IBD je indikované vyšetrenie kostného metabolizmu a denzity kostného minerálu. Rastúca kosť má veľkú schopnosť remodelácie, preto včasná diagnostika a optimálna liečba zlepšujú kvalitu života detí a znižujú riziko rozvoja osteoporózy a zlomenín v neskoršom veku.
Práca bola podporená grantom VEGA V-17–016–00 a MZ SR 2018/36-LFUK-10
Received | Doručeno do redakce | Doručené do redakcie 17. 10. 2018
Accepted | Přijato po recenzi | Prijaté po recenzii 6. 11. 2018
MUDr. Alžbeta Čagalová
Zdroje
- Greer FR, Krebs NF. [American Academy of Pediatrics Committee on Nutrition].Optimizing bone health and calcium intakes of infants, children, and adolescents. Pediatrics 2006; 117(2): 578–585. Dostupné z DOI: <http://doi 10.1542/peds.2005–2822>.
- Laakso S, Valta H, Verkasalo M et al. Compromised peak bone mass in patients with inflammatory bowel disease – a prospective study. J Pediatr 2014; 164(4): 1436–1443. Dostupné z DOI: <http://doi 10.1016/j.jpeds.2014.01.073>.
- Gilbert L, He X, Farmer P, et al. Inhibition of osteoblast differentiation by tumor necrosis factor-alpha. Endocrinology 2000; 141(11): 3956–3964. Dostupné z DOI: <http://doi 10.1210/endo.141.11.7739>.
- Ward LM. Osteoporosis due to glucocorticoid use in children with chronic illness. Horm Res 2005; 64(5): 209–221. Dostupné z DOI: <http://doi 10.1159/000088976>.
- Hildebrand H, Karlberg J, Kristiansson B. Longitudinal growth in children and adolescents with inflammatory bowel disease. J Pediatr Gastroenterol Nutr 1994; 18(2): 165–173.
- Kappelman MD, Galako JA, Porter CQ et al. The Risk of Diagnosed Fractures in Children with Inflammatory Bowel Diseases. Inflamm Bowel Dis 2011; 17(5): 1125–1130. Dostupné z DOI: <http://doi 10.1002/ibd.21472>.
- Ahmed SF, Horrocks IA, Patterson T et al. Bone mineral assessment by dual energy X-ray absorptiometry in children with inflammatory bowel disease: evaluation by age or bone area. J Pediatr Gastroenterol Nutr 2004; 38(3): 276–280.
- Thearle M, Horlick M, Bilezikian JP et al. Osteoporosis: An anusual presentation of childhood Crohn’s disease. J Clin Endocrinol Metab 2000; 85(6): 2122–2126. Dostupné z DOI: <http://doi 10.1210/jcem.85.6.6640>.
- Patschan D, Loddenkemper K, Buttgereit F. Molecular mechanisms of glucocorticoid-induced osteoporosis. Bone 2001; 29(6): 498–505.
- Tichá Ľ, Payer J, Killinger Z et al. Kostný metabolizmus u pacientok s mentálnou anorexiou. Osteologický bulletín 2016; 21(2): 73–74.
- Wong SCh, Catto-Smith AGA, Zacharin M. Pathological fractures in paediatric patients with inflammatory bowel disease. Eur J Pediatr 2014; 173 (2): 141–151. Dostupné z DOI: <http://doi 10.1007/s00431–013–2174–5>.
- Payer J, Killinger Z. Osteoporóza. Herba: Bratislava 2012. ISBN 978–80–89171–94–1.
- Pappa H, Thayu M, Sylvester F et al. Skeletal health of children and adolescents with inflammatory bowel disease. J Pediatr Gastroenterol Nutr 2011; 53(1): 11–25. Dostupné z DOI: <http://doi 10.1097/MPG.0b013e31821988a3>.
Štítky
Biochemie Dětská gynekologie Dětská radiologie Dětská revmatologie Endokrinologie Gynekologie a porodnictví Interní lékařství Ortopedie Praktické lékařství pro dospělé Radiodiagnostika Rehabilitační a fyzikální medicína Revmatologie Traumatologie Osteologie
Článek vyšel v časopiseClinical Osteology
Nejčtenější tento týden
2018 Číslo 3- Aktuální doporučení pro diagnostiku von Willebrandovy choroby
- Na inkontinenční pomůcky nově dosáhne více pacientů
- Postabortivní syndrom – symptomy, dopady a možnosti léčby
- Trombóza portální žíly jako komplikace infekce COVID-19 – kazuistika
- EGb 761: extrakt z Ginkgo biloby s definovaným složením
-
Všechny články tohoto čísla
- Kostné prejavy porúch štítnej žľazy
- Vyšetrovacie metódy u sarkopénie
- Prevence a léčba osteoporózy u postmenopauzálních žen s karcinomem prsu léčených inhibitory aromatázy
- Diabetes mellitus 2. typu a kvalita kosti
- Kompresívne vertebrálne fraktúry u detí s Crohnovou chorobou: kazuistiky
- Odešel pan prof. MUDr. Jaroslav Blahoš, DrSc. (30. 6. 1930 – 27. 11. 2018)
- Teriparatid v liečbe ťažkej osteoporózy u starších pacientok: výsledky multicentrickej prospektívnej štúdie
- Porovnanie mortality pacientov po zlomenine proximálneho femoru 1995–2002 a 2003–2010
- Clinical Osteology
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Teriparatid v liečbe ťažkej osteoporózy u starších pacientok: výsledky multicentrickej prospektívnej štúdie
- Diabetes mellitus 2. typu a kvalita kosti
- Porovnanie mortality pacientov po zlomenine proximálneho femoru 1995–2002 a 2003–2010
- Prevence a léčba osteoporózy u postmenopauzálních žen s karcinomem prsu léčených inhibitory aromatázy
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



