-
Články
Top novinky
Reklama- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
Top novinky
Reklama- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Top novinky
ReklamaTransplantace jater pro akutní selhání jater
Liver transplantation for acute liver failure
Acute liver failure is a rare, highly devastating, potentially reversible condition characterised by the sudden onset of severe liver dysfunction in individuals without pre-existing liver disease and with a poor prognosis. In recent decades, advances in the diagnosis of the disease, a better understanding of its pathophysiology and the development of supportive care have improved the prognosis of patients with acute liver failure. However, despite the success of conservative therapy, urgent liver transplantation remains the only chance of survival for a large proportion of patients with acute liver failure. Early diagnosis of the disease, implementation of supportive care and identification of patients indicated for urgent liver transplantation are essential measures in the management of patients with acute liver failure.
Keywords:
acute liver failure – transplantation – supportive therapy – prognostic criteria
Autoři: E. Kieslichová 1,2
Působiště autorů: Klinika anesteziologie, resuscitace a intenzivní péče, Institut klinické a experimentální medicíny, Praha 2 1. LF Univerzity Karlovy, Praha 1
Vyšlo v časopise: Gastroent Hepatol 2024; 78(2): 95-100
Kategorie: Hepatologie
doi: https://doi.org/10.48095/ccgh202495Souhrn
Akutní selhání jater je vzácné, vysoce devastující, potenciálně reverzibilní onemocnění, které je charakterizované náhlým nástupem závažné jaterní dysfunkce u jedinců bez předchozího onemocnění jater. V průběhu posledních desetiletí došlo díky pokrokům v diagnostice onemocnění, lepšímu porozumění patofyziologii a rozvoji podpůrných opatření ke zlepšení prognózy pacientů s akutním selháním jater. Přes úspěchy konzervativní léčby ale pro velkou část pacientů s akutním selháním jater zůstává urgentně provedená transplantace jater jedinou šancí na přežití. Časné rozpoznání onemocnění, zavedení podpůrné terapie a identifikace pacientů indikovaných k urgentní transplantaci jater představují základní opatření v přístupu k pacientům s akutním selháním jater.
Klíčová slova:
akutní selhání jater – transplantace – podpůrná terapie – prognostická kritéria
Úvod
Transplantace jater (TJ) byla zavedena do klinické praxe v 60. letech 20. století jako terapeutická metoda pro pacienty se závažným, jinak neléčitelným onemocněním jater. Od té doby se TJ stala standardní a úspěšnou terapií jaterních onemocnění. Míra přežití v prvním roce po TJ přesahuje 95 % a po 10 letech 70 % [1]. Přežívání po TJ pro akutní selhání jater (ASJ) je nižší než u elektivních transplantací kvůli rizikovému operačnímu výkonu u pacienta v kritickém stavu a vyšší četnosti perioperačních komplikací.
Akutní selhání jater je kritický stav. Pro přežití pacienta s AJS je zcela zásadní časná identifikace onemocnění, stanovení prognózy a včasné nasazení terapie vč. rozvahy o indikaci k transplantaci. Jedná se o onemocnění zatížené vysokou letalitou, která před zavedením urgentní TJ přesahovala 80 % [2]. Přestože se díky lepšímu pochopení patofyziologie ASJ a pokrokům v léčbě kritických stavů míra přežití při konzervativní léčbě výrazně zlepšila, je pro mnoho pacientů s ASJ urgentní TJ život zachraňujícím zákrokem. Všechny pacienty s ASJ je tedy třeba považovat za potenciální kandidáty TJ.
Transplantace jater pro ASJ je léčba s náročným chirurgickým zákrokem, specifickou perioperační péčí a celoživotní imunosupresí; realizace TJ závisí na aktuální dostupnosti štěpu jater.
Definice akutního selhání jater
Akutní selhání jater je náhle vzniklé, rychle progredující a život ohrožující onemocnění. Je charakterizováno náhlým nástupem závažné jaterní dysfunkce u jedinců bez předchozího onemocnění jater, kdy do 26 týdnů od počátečních příznaků dochází k rozvoji koagulopatie (protrombinový čas > 15 s nebo mezinárodní normalizační poměr [INR] > 1,5) a jaterní encefalopatie. Pro definici ASJ u dětí není přítomnost jaterní encefalopatie nezbytná; nemusí být vyjádřena, vyvíjí se později nebo není dobře rozpoznatelná. ASJ u dětí je tedy definováno:
- jaterní koagulopatií (protrombinový čas > 15 s nebo INR > 1,5) nereagující na podání vitaminu K a jaterní encefalopatií nebo
- koagulopatií (protrombinový čas 20 s nebo INR 2,0) bez ohledu na přítomnost jaterní encefalopatie; podmínkou je absence předchozího onemocnění jater.
Tab. 1. Klasifi kace akutního selhání jater [5,27]. Tab. 1. Classification of acute liver failure [5,27]. ![Klasifi kace akutního selhání jater [5,27]. Tab. 1. Classification of acute liver failure [5,27].](https://pl-master.mdcdn.cz/media/cache/media_object_image_small/media/image/b0c3e793cdb89be1faec3d09f4dd7f64.png)
Vzhledem k vysoké regenerační schopnosti jater je onemocnění potenciálně reverzibilní [3]. ASJ je vzácné onemocnění; odhadovaná incidence na základě publikovaných studií a transplantačních registrů je v Evropě a Severní Americe kolem 6 případů na 1 mil. obyvatel/rok. ASJ postihuje spíše mladší pacienty s mírnou převahou žen.
Diagnóza ASJ se opírá o neexistenci předchozího onemocnění jater. V určitých případech, kdy se jedná o dosud asymptomatický stav a de novo se vyvine jaterní encefalopatie spolu s příslušnými abnormalitami v jaterních testech a koagulačním profilu a s přítomností ikteru, není absence již dříve existujícího onemocnění jater závazná. K těmto výjimkám patří Wilsonova choroba, akutní prezentace autoimunitní hepatitidy, Buddův-Chiariho syndrom a reaktivace hepatitidy B.
Na základě intervalu mezi ikterem a nástupem encefalopatie jsou rozlišovány tři subkategorie ASJ:
- „hyperakutní“ (< 7 dní);
- „akutní“ (7–28 dní) a
- „subakutní“ (4–24 týdnů) (tab. 1).
Klasifikace je důležitá, protože klinický obraz, léčba a prognóza se mezi jednotlivými kategoriemi podstatně liší. Hyperakutní selhání má rychlý nástup, je běžně spojováno s rozvojem edému mozku a nitrolební hypertenzí; jeho prognóza při konzervativní léčbě je však lepší než u akutního a subakutního typu [4,5].
Diferenciální diagnóza
Základem diagnostiky ASJ je pečlivá anamnéza, laboratorní vyšetření, toxikologické, sérologické vyšetření a zobrazovací metody. Je nutno pomýšlet na metabolické poruchy a geneticky podmíněná onemocnění [6]. Biopsie jater má v případě ASJ omezenou výpovědní hodnotu a je potenciálně rizikovým výkonem; jejím hlavním přínosem je vyloučení chronického onemocnění jater, malignity a alkoholového poškození jater. Na základě charakteristického histologického obrazu může biopsie pomoci v objasnění etiologie ASJ.
V diferenciální diagnostice ASJ je nutno vyloučit chronické onemocnění jater a akutní selhání jater nasedající na chronické (ACLF – acute on-chronic liver failure) [3,7]. Je třeba se zaměřit na trvání onemocnění, existenci spouštěcí příčiny, známky chronického selhání jater a portální hypertenze (jícnové varixy, pavoučkové névy, splenomegalie, ascites, svalová slabost, malnutrice). Vyloučení chronického onemocnění jater může být v některých případech problematické vzhledem k podobnosti klinických nálezů i nálezů na zobrazovacích metodách.
Patofyziologie a klinický obraz
Při ASJ dochází k úbytku masy funkčních jaterních buněk na podkladě masivní nekrózy hepatocytů, je redukována funkční kapacita jater; současně se rozvíjí masivní zánětlivá reakce. Spolu se ztrátou funkce jater se rozvíjí multiorgánové selhání (kardiovaskulární systém, nervový systém, respirační systém, ledviny, metabolické procesy, koagulační rovnováha a imunitní systém).
Akutní selhání jater je onemocnění s rychlou progresí v řádu dnů a týdnů. Typickými příznaky jsou encefalopatie, koagulopatie a ikterus. Další příznaky jsou často nespecifické a mohou se lišit v souvislosti s etiologií onemocnění a rozvojem systémové zánětlivé reakce [7].
Charakteristická je hemodynamická nestabilita v důsledku snížené vaskulární rezistence a relativní hypovolemie spolu s adrenokortikální insuficiencí, poškozením myokardu a iontovou dysbalancí. Vyvíjí se porucha vědomí, respirační insuficience, metabolické abnormality a akutní poškození ledvin. Příčinou úmrtí pacientů s ASJ je otok mozku a nitrolební hypertenze, sepse nebo multiorgánové selhání. Prognóza je horší u pacientů s těžším stupněm jaterní dysfunkce, selháním extrahepatálních orgánů a příp. při subakutní prezentaci.
Etiologie a průběh onemocnění
Akutní selhání jater vyvolává řada hepatálních i exrahepatálních příčin, které vedou k hepatocelulárnímu poškození a nekróze hepatocytů a které modifikují průběh onemocnění (tab. 2). Příčina ASJ určuje histologický typ jaterního poškození a ovlivňuje progresi klinického průběhu a prognózu; je nezávislým prediktorem úmrtí na čekací listině k TJ [8,9]. Celosvětově nejčastější příčinou ASJ jsou virové hepatitidy, které jsou rovněž dominantní etiologií v tzv. rozvojových zemích. V Evropě a v Severní Americe převládá polékové a toxické poškození. Etiologii se nedaří objasnit přibližně u 17–33 % všech případů ASJ (některé prameny uvádějí až 70 %), u dětí je tento podíl vyšší.
Identifikace příčiny ASJ je zcela zásadní pro zavedení specifické terapie a má význam pro odhad prognózy i pro zvažování zařazení k TJ. Přibližně 60 % pacientů s ASJ v důsledku intoxikace paracetamolem, hepatitidy typu A, ischemické hepatitidy nebo ASJ v těhotenství může přežít bez následků, zatímco v případě autoimunitní etiologie nebo idiosynkratické lékové reakce přežívá bez TJ pouze 30 % pacientů; akutně probíhající Wilsonova choroba má bez TJ 100% letalitu.
Tab. 2. Příčiny akutního jaterního selhání. Tab. 2. Causes of acute liver failure. 
Terapie
Pacienty s ASJ je nutno hospitalizovat na jednotce intenzivní péče, neprodleně zahájit specifickou a podpůrnou terapii a současně zvažovat TJ [10]. Při prvních známkách progrese onemocnění je doporučeno kontaktovat transplantační centrum a pacienta přeložit na jednotku intenzivní péče specializovaného pracoviště, kde je možné případnou transplantaci provést [11].
Ve všech případech ASJ je třeba zahájit podpůrnou terapii vč. přístrojové podpory dle stavu pacienta [12,13]. Pro vybrané etiologie ASJ je k dispozici terapie specifická (tab. 3). Podpůrná terapie zahrnuje resuscitaci oběhu (volumoterapie, vazopresory, inotropika), péči zaměřenou na respirační systém vč. umělé plicní ventilace, podporu a náhradu funkce ledvin, úpravu metabolických poruch (udržování normoglykemie, korekce iontové a metabolické dysbalance), výživu, profylaxi stresového vředu, profylaxi a léčbu infekce, korekci koagulopatie v případě aktivního krvácení, prevenci a terapii nitrolební hypertenze [14]. Včasné zavedení kontinuální náhrady funkce ledvin (kontinuální venovenózní hemodialýza – CVVHD) u pacientů s ASJ s hyperamonemií, metabolickou a iontovou dysbalancí a s akutním poškozením ledvin je spojeno se zlepšeným přežíváním pacientů. Standardní součástí podpůrné terapie všech typů ASJ je podávání N-acetylcysteinu, a to pro jeho antioxidační účinky a příznivý vliv na mikrocirkulaci; jeho užití ale není podloženo spolehlivými klinickými důkazy [15].
Přístrojová podpora jaterního selhání představuje možnost překlenovací terapie pacienta s jaterním selháním do doby reparace jaterních funkcí nebo do provedení TJ [16]. K dispozici jsou systémy biologické (s užitím hepatocytů), nebiologické a hybridní (bioartificiální). Informací ohledně dopadu těchto systémů na přežití pacientů s ASJ je jen málo, což je dáno nízkou incidencí ASJ v populaci, aplikací různých podpůrných systémů a rozdílným designem jednotlivých studií. Alternativou přístrojové podpory je výměna plazmy, která sice není léčbou ve smyslu mimotělní podpory jater, jejím přínosem je odstranění toxických metabolitů, doplnění potenciálně prospěšných faktorů a eliminace mediátorů selhání vícečetných orgánových systémů [17].
Kdy odeslat pacienta do transplantačního centra
Vzhledem k rychlé progresi ASJ je třeba realizovat transport na speciální jednotku intenzivní péče s možností provedení transplantace jater, dokud je pacient schopen převozu. Překlad by měl být zvažován s nástupem encefalopatie, při INR > 1,5; nebo při přítomnosti jiných známek špatné prognózy (hypoglykemie, metabolická acidóza).
Transportovat: by se měl pacient s encefalopatií maximálně 1.–2. stupně, s lékařským doprovodem, za pečlivé monitorace stavu a s vědomím, že ke zhoršení stavu (hypotenze, hypoglykemie, progrese encefalopatie) může dojít kdykoli během transportu, a to i u dosud stabilního pacienta [18].
Transplantace jater pro ASJ
Urgentní TJ je léčebná metoda, která významně změnila přežívání pacientů s ASJ. V současnosti tvoří ASJ v Evropě a USA přibližně 8–12 % indikací k TJ. Transplantace se provádí štěpem celým, redukovaným (použití části jater) nebo parciálním (split: rozdělení jater dárce na dvě a více plnohodnotných částí a jejich užití pro více příjemců), je možné provést i transplantaci AB0 nekompatibilní. Je možné provést i auxiliární transplantaci jako přemosťující terapii k regeneraci vlastních jater, např. u některých typů intoxikací [1,3].
Orgán k transplantaci pochází většinou od zemřelého dárce s diagnózou smrti mozku nebo po nevratné zástavě cirkulace. Vzhledem k urgentní indikaci a omezenému času, kdy lze transplantaci provést s nadějí na úspěch, jsou často akceptovány i štěpy jater hraniční kvality od dárců s rozšířenými kritérii. Ve výjimečných případech může být dárcem i žijící příbuzný pacienta, a to na základě pečlivé rozvahy a za podmínky minimalizace rizika u dárce s perspektivou významného benefitu pro příjemce.
Výkon se provádí v celkové anestezii s intubací a umělou plicní ventilací. V průběhu operace je nutná volumoterapie a podpora oběhu vazopresory a inotropiky. U nestabilních pacientů s akutním poškozením ledvin se sklonem k hyperamonemii je zapotřebí pokračovat v podpoře funkce ledvin (kontinuální venovenózní hemodialýza) i během operačního výkonu. Je zapotřebí vyvarovat se hypotenze, hypo - i hypervolemie, hypoxie, výkyvům nitrolebního tlaku. Vzhledem k vysokému riziku infekčních komplikací se podává antibiotická a antimykotická profylaxe.
Monitorace v průběhu výkonu odpovídá kritickému stavu, monitorují se parametry hemodynamiky, ventilace a oxygenace i laboratorní parametry, neurologický stav pacienta vč. nitrolebního tlaku a cerebrálního perfuzního tlaku; k monitoraci koagulace jsou vhodné viskoelastické metody, které podávají přesnější informaci o koagulačních poměrech než laboratorní vyšetření.
Problémy spojené s TJ u pacientů s ASJ se týkají nejen indikace k výkonu, omezené spolehlivosti prognostických modelů a komplikovaného perioperačního managementu, ale i rozhodování v časové tísni. Příliš brzká indikace TJ s sebou nese potenciální možnost provedení TJ u pacientů, u nichž může ještě dojít ke spontánnímu zotavení s kompletní reparací jaterních funkcí, což znamená nejen riziko spojené s urgentní TJ a celoživotní imunosupresí, ale i zbytečné použití orgánu. Na druhou stranu oddalování rozhodnutí o TJ zvyšuje riziko infekce, nevratného poškození mozku, multiorgánového selhání nebo úmrtí pacienta.
Výběr pacientů s ASJ, kteří potřebují LT, by proto měl být založen na včasné identifikaci faktorů, které předpovídají špatný klinický výsledek, na použití prognostických modelů kombinujících různé parametry a na klinickém odhadu erudovaného týmu. Pacienty s ASJ je nutno průběžně hodnotit zkušeným týmem specialistů z hlediska indikace k TJ i aktuální schopnosti transplantaci podstoupit [19].
Transplantace jater pro ASJ je urgentní operační výkon u pacienta v kritickém stavu, zatížený řadou perioperačních komplikací, který vyžaduje zkušený tým transplantačních chirurgů, zkušený anesteziologický tým a specifickou perioperační péči. Je třeba počítat s rizikem rozvoje edému mozku, progresí oběhové nestability u pacienta s rozvinutou systémovou zánětlivou reakcí, respirační insuficiencí, akutním poškozením ledvin se sklonem k hyperamonemii a s metabolickým rozvratem.
Některé etiologie ASJ vyžadují speciální perioperační přístup; např. pacienti transplantovaní pro akutní HBV infekci musí mít imunoprofylaxi a virostatika k potlačení replikace viru, pacienti transplantovaní pro Buddův-Chiariho syndrom účinnou antikoagulaci.
Prognostická kritéria a identifikace kandidátů urgentní TJ
Velmi důležitý pro úspěch výkonu je co nejpřesnější výběr pacientů, kteří mohou mít z transplantace prospěch; tj. identifikovat pacienty, kteří bez urgentně provedené TJ s vysokou pravděpodobností zemřou, zároveň ale jsou schopni transplantaci přežít a z výkonu profitovat. Navíc oproti jiným operačním výkonům u rizikových pacientů v případě TJ je nutno pomýšlet nejen na benefit a riziko u konkrétního pacienta, ale i na možnou ztrátu štěpu v případě neúspěchu transplantace nebo nesprávně indikovaného výkonu.
O zařazení k TJ v urgentním pořadí rozhoduje multidisciplinární tým (hepatolog, anesteziolog-intenzivista a chirurg) na základě etiologie, klinické prezentace a hodnocení prognostických kritérií, pacienti s ASJ jsou na čekacích listinách prioritizováni. Kontraindikací TJ pro ASJ je nekontrolovaná sepse, refrakterní nitrolební hypertenze, těžká extrahepatální komorbidita (malignity) a refrakterní multiorgánové selhání. Jsou zohledňovány i psychosociální faktory, jako opakované pokusy o sebevraždu pacientů se závažnými psychickými problémy a závislost na návykových látkách, alkoholizmus.
Pro výběr vhodných kandidátů k TJ je nutné mít k dispozici prognostický model, který dokáže včas a s maximální přesností předpovědět výsledky. Doposud bylo sice zvažováno mnoho klinických a laboratorních parametrů, které předpovídají výsledky u pacientů s ASJ, ale z hlediska přesnosti, použitelnosti a snadnosti vyhodnocení není prakticky žádný z nich modelem optimálním.
Nejčastěji jsou k hodnocení prognózy a k indikaci k TJ u pacientů s ASJ využívána King’s College kritéria (tab. 4), která byla vyvinuta koncem 80. let 20. století, jejichž platnost byla posléze opakovaně validována [20]. Splnění těchto kritérií znamená méně než 20% pravděpodobnost přežití bez transplantace. Další nejčastěji užívaná jsou Clichy kritéria (tab. 5), která byla původně koncipována pro ASJ na podkladě hepatitidy typu B; jsou založena na hodnocení věku, faktoru V a stupně encefalopatie u pacientů s ASJ [21]. Kritéria King’s College i Clichy umožňují identifikovat pacienty s vysokou pravděpodobností úmrtí při konzervativní terapii. Tato kritéria mají vysokou specificitu a nízkou senzitivitu, což znamená, že mnozí pacienti s ASJ mohou zemřít, aniž tato kritéria splní. Ke stanovení prognózy ASJ lze rovněž užít systém MELD (Model for End-Stage Liver Disease); prahové hodnoty MELD skóre pro ASJ a TJ ale nebyly standardizovány. Na základě konsenzu a výsledků studií je špatná prognóza spojena s dosažením MELD > 30 [22]. Ukazatelem nepříznivého vývoje ASJ je i progresivně se zmenšující objem jaterní tkáně a velký rozsah nekróz při jaterní biopsii (> 50 % nekróz). U dětí s ASJ je indikace k JT založena na hodnotách INR (INR > 4) a bilirubinu (Sbili > 300 μmol/l) bez ohledu na přítomnost jaterní encefalopatie [3].
Po zařazení na čekací listinu k TJ je třeba průběžně hodnotit stav pacientů s ohledem na vývoj onemocnění a reakci na podpůrnou léčbu. Definitivní rozhodnutí se provádí v okamžiku dostupného štěpu jater.
Při stabilizaci pacienta a známkách reparace jater a ústupu multiorgánové dysfunkce se pacient na základě multioborového konzilia zneaktivní na čekací listině, event. se z čekací listiny vyřadí [6]. Pokud se stav pacienta přes intenzivní péči progresivně zhoršuje a vyvinou se kontraindikace k výkonu, pacient je z čekací listiny vyřazen. V tomto případě je další intenzivní péče hodnocena jako nepřiměřená a je indikován přechod na péči paliativní.
Tab. 3. King’s College kritéria. Tab. 4. King’s College criteria. 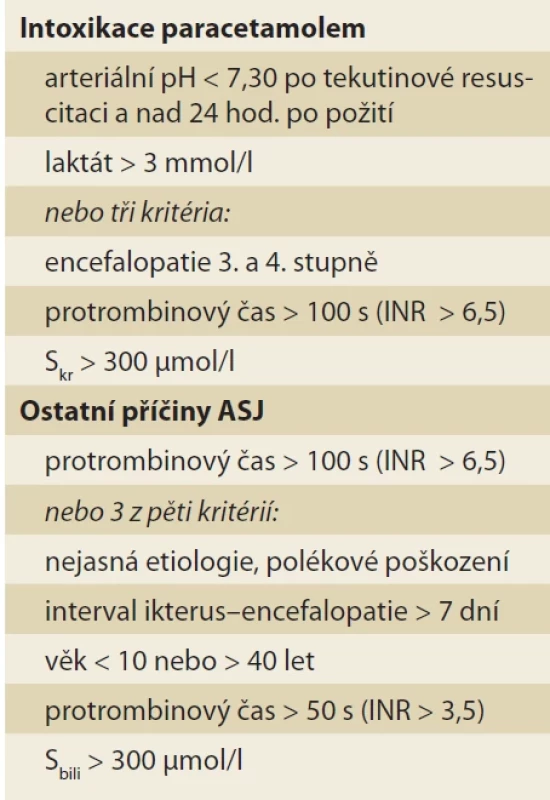
Tab. 4. Clichy kritéria. Tab. 5. Clichy criteria. 
Přežívání pacientů po transplantaci pro ASJ
Přežívání pacientů po transplantaci pro ASJ se konstantně a progresivně v čase zlepšuje. Většina pacientů se po TJ pro ASJ vrátí k normálnímu životu a práci, dochází na pravidelné kontroly a celoživotně užívá imunosupresi k zábraně rejekce transplantovaného orgánu.
Jednoleté přežití pacientů po TJ pro ASJ přesahuje 80 %, dlouhodobé přežívání je srovnatelné s výsledky elektivní TJ pro cirhózu. Důvodem horších krátkodobých výsledků je kritický stav pacienta před výkonem, multiorgánové poškození a také využití marginálních štěpů s vysokým rizikem potransplantační dysfunkce v urgentní situaci [18,23]. Nejvyšší riziko úmrtí je v prvním roce po transplantaci v souvislosti s infekcí vč. plísňové, neurologickými komplikacemi a multisystémovým orgánovým selháním. Častěji než u elektivních transplantací jsou prováděny retransplantace pro dysfunkci marginálního štěpu [24,25].
V časném potransplantačním období mohou po úspěšné TJ u některých pacientů přetrvávat abnormality orgánových funkcí, např. akutní poškození ledvin, přechodně i s nutností dialýzy, svalová slabost jako důsledek kritického stavu, zhoršená funkce gastrointestinálního traktu nebo neurologické poruchy a neuropsychické abnormality [26]. Neurologické příznaky souvisí s rozvojem mozkového edému, nitrolební hypertenze a hypoxií mozku při ASJ; neurokognitivní dysfunkce mohou být součástí širšího spektra poruch, které se běžně vyskytují u kriticky nemocných. Psychické potíže po TJ mohou souviset i se skutečností, že tito pacienti nebyli na onemocnění, které přišlo náhle a z plného zdraví, psychicky připraveni.
Závěr
Akutní selhání jater je kritický stav, který může rychle progredovat. Pro přežití pacienta je důležitá včasná diagnostika, neprodlené zavedení specifických a podpůrných terapeutických strategií a ve vybraných případech provedení urgentní TJ. Terapie ASJ je multidisciplinární záležitostí a měla by být prováděna ve specializovaných centrech. Revize prognostických kritérií a přesnější identifikace pacientů, kteří budou s vysokou pravděpodobností bez ohledu na podpůrnou terapii vyžadovat urgentní TJ, zůstává velkou výzvou do budoucna.
Zdroje
1. Lucey MR, Furuya KN, Foley DP. Liver transplantation. N Engl J Med 2023; 389 (20): 1888–1900. doi: 10.1056/NEJMra2200923.
2. Germani G, Theocharidou E, Adam R et al. Liver transplantation for acute liver failure in Europe: outcomes over 20 years from the ELTR database. J Hepatol 2012; 57 (2): 288–296. doi: 10.1016/j.jhep.2012.03.017.
3. European Association for the Study of the Liver. EASL Clinical Practical Guidelines on the management of acute (fulminant) liver failure. J Hepatol 2017; 66 (5): 1047–1081. doi: 10.1016/ j.jhep.2016.12.003.
4. Bernuau J, Benhamou JP. Classifying acute liver failure. Lancet 1993; 342 (8866): 252–253. doi: 10.1016/0140-6736 (93) 91809-z.
5. O’Grady JG, Schalm SW, Williams R. Acute liver failure: redefining the syndromes. Lancet 1993; 342 (8866): 273–275. doi: 10.1016/0140 - 6736 (93) 91818-7.
6. Seetharam A. Intensive care management of acute liver failure: considerations while awaiting liver transplantation. J Clin Transl Hepatol 2019; 7 (4): 384–391. doi: 10.14218/JCTH.2019.00032.
7. Balackmore L, Bernal W. Acute liver failure. Clin Med 2015; 15 (5): 468–472. doi: 10.7861/clin medicine.15-5-468.
8. Lee WM. Etiologies of acute liver failure. Semin Liver Dis 2008; 28 (2): 142–152. doi: 10.1055/s-2008-1073114.
9. Wong NZ, Reddy KR, Bittermann T. Acute liver failure etiology is an independent predictor of waitlist outcome but not posttransplantation survival in a national cohort. Liver Transpl 2022; 28 (1): 39–50. doi: 10.1002/lt.26187.
10. Punzalan CS, Barry CT. Acute liver failure: diagnosis and management. J Intensive Care Med 2016; 31 (10): 642–653. doi: 10.1177/0885066615609271.
11. Montrief T, Koyfman A, Long B. Acute liver failure: a review for emergency physicians. Am J Emerg Med 2019; 37 (2): 329–337. doi: 10.1016/j.ajem.2018.10.032.
12. Shingina A, Mukhtar N, Wakim-Fleming J et al. Acute liver failure guidelines. Am J Gastroenterol 2023; 118 (7): 1128–1153. doi: 10.14309/ ajg.0000000000002340.
13. Khan R, Koppe S. Modern management of acute liver failure. Gastroenterol Clin North Am 2018; 47 (2): 313–326. doi: 10.1016/j.gtc.2018.01.005.
14. Warrillow SJ, Bellomo R. Preventing cerebral oedema in acute liver failure: the case for quadruple-H therapy. Anaesth Intensive Care 2014; 42 (1): 78–88. doi: 10.1177/0310057X1404200114.
15. Vasques F, Cavazza A, Bernal W. Acute liver failure. Curr Opin Crit Care 2022; 28 (2): 198–207. doi: 10.1097/MCC.0000000000000923.
16. Katarey D, Jalan R. Update on extracorporeal liver support. Curr Opin Crit Care 2020; 26 (2): 180–185. doi: 10.1097/MCC.0000000000000708.
17. Larsen FS, Schmidt LE, Bernsmeier C et al. Highvolume plasma exchange in patients with acute liver failure: an open rando mised controlled trial. J Hepatol 2016; 64 (1): 69–78. doi: 10.1016/j.jhep.2015.08.018.
18. Tujios S, Stravitz RT, Lee WM. Management of acute liver failure: update 2022. Semin Liver Dis 2022; 42 (3): 362–378. doi: 10.1055/s-0042-1755274.
19. Castaldo ET, Chari RS. Liver transplantation for acute hepatic failure. HPB (Oxford) 2006; 8 (1): 29–34. doi: 10.1080/13651820500465741.
20. McPhail MJ, Farne H, Senvar N et al. Ability of King’s college criteria and model for end-stage liver disease scores to predict mortality of patients with acute liver failure: a meta-analysis. Clin Gastroenterol Hepatol 2016; 14 (4): 516–525. doi: 10.1016/j.cgh.2015.10.007.
21. Ichai P, Legeai C, Francoz C et al. Patients with acute liver failure listed for superurgent liver transplantation in France: reevaluation of the ClichyVillejuif criteria. Liver Transpl 2015; 21 (4): 512–523. doi: 10.1002/lt.24092.
22. Flamm SL, Yu XY, Singh S et al. American Gastroenterological Association Institute Guidelines for the diagnosis and management of acute liver failure. Gastroenterology 2017; 152 (3): 644–647. doi: 10.1053/j.gastro.2016.12.026.
23. Bernal W, Hyyryainen A, Gera A et al. Lessons from look-back in acute liver failure? A single centre experience of 3300 patients. J Hepatol 2013; 9 (1): 74–80. doi: 10.1016/j.jhep.2013.02.010.
24. Arora H, Thekkekandam J, Tesche L et al. Long-term survival after 67 hours of anhepatic state due to primary liver allograft nonfunction. Liver Transpl 2010; 16 (12): 1428–1433. doi: 10.1002/lt.22166.
25. European Association for the Study of the Liver. EASL Clinical Practice Guidelines: liver transplantation. J Hepatol 2016; 64 (2): 433–485. doi: 10.1016/j.jhep.2015.10.006.
26. Anand AC, Singh P. Neurological recovery after recovery from acute liver failure: is it complete? J Clin Exp Hepatol 2019; 9 (1): 99–108. doi: 10.1016/j.jceh.2018.06.005.
27. Bernal W, Wendon J. Acute liver failure. N Engl J Med 2013; 369 (26): 2525–2534. doi: 10.1056/NEJMra1208937.
ORCID autorky
E. Kieslichová 0000-0002-3930-623X.
Doručeno/Submitted: 28. 2. 2024Přijato/Accepted: 13. 3. 2024doc. MUDr. Eva Kieslichová, Ph.D.Klinika anesteziologie, resuscitace a intenzivní péčeInstitut klinické a experimentální medicínyVídeňská 1958/914000 Praha 4evki@ikem.czŠtítky
Dětská gastroenterologie Gastroenterologie a hepatologie Chirurgie všeobecná
Článek vyšel v časopiseGastroenterologie a hepatologie
Nejčtenější tento týden
2024 Číslo 2- Efekt itopridu na motilitu jícnu a funkci dolního jícnového svěrače
- Itoprid v léčbě funkční dyspepsie
- Farmakokinetika a tolerance pantoprazolu v dětském věku
- Vliv podávání prokinetik na riziko syndromu bakteriálního přerůstání u pacientů užívajících inhibitory protonové pumpy
- Strava bohatá na arginin a prolin slibuje urychlení hojení ran u diabetických pacientů
-
Všechny články tohoto čísla
- Transplantace jater pro ACLF
- Transplantace jater pro chronickou hepatitidu C – význam protivirové léčby v roce 2024
- Transplantace jater pro cholestatická onemocnění
- Transplantace jater pro hepatocelulární karcinom
- Transplantace jater pro deficit alfa-1-antitrypsinu
- Cesta pacienta s cirhózou od registrácie do transplantačnému programu pečene, analýza 996 pacientov z registra RH7 na Slovensku
- Diagnostika alkoholovej choroby pečene u gastroenterológa
- Izoniazidom navodené poškodenie pečene sprevádzané ikterom
- Robotická pankreatická chirurgie v České republice – první zkušenosti
- První zkušenosti s filgotinibem ve vyšší linii léčby u pacientů s ulcerózní kolitidou
- Erratum
- Výběry z mezinárodních časopisů
- Odkaz profesora Friče poneseme dál
- Kreditovaný autodidaktický test: Hepatologie
- Editorial
- Úvodní slovo
- Vývoj indikací k transplantaci jater
- Transplantace jater pro akutní selhání jater
- Gastroenterologie a hepatologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Diagnostika alkoholovej choroby pečene u gastroenterológa
- Transplantace jater pro akutní selhání jater
- Robotická pankreatická chirurgie v České republice – první zkušenosti
- Izoniazidom navodené poškodenie pečene sprevádzané ikterom
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Revma Focus: Spondyloartritidy
nový kurz
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Autoři: prof. MUDr. Pavel Horák, CSc., doc. MUDr. Ludmila Brunerová, Ph.D., doc. MUDr. Václav Vyskočil, Ph.D., prim. MUDr. Richard Pikner, Ph.D., MUDr. Olga Růžičková, MUDr. Jan Rosa, prof. MUDr. Vladimír Palička, CSc., Dr.h.c.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



