-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Biologická léčba psoriatické artritidy
Biological treatment of psoriatic arthritis
Psoriatic arthritis (PsA) is a heterogeneous disease affecting, besides synovial joints, also the entheses, the soft tissues of the whole finger (dactylitis) and the axial skeleton. Currently the classification criteria CASPAR are used to diagnose PsA. In a large number of patients the disease leads to irreversible joint damage (X-ray, respectively clinical) which significantly reduces life quality and limits the patient in his/her everyday activities and also considerably limits their work capacity. There is evidence showing that early commencement of treatment and treat to target principle can significantly reduce this negative development. In recent time the knowledge of the disease pathogenesis has been extending and at the same time new drugs appear that act on the critical pathogenetic processes in a targeted way. These are biological drugs from the group of TNFα inhibitors and, most recently, also inhibitors of Th17 – IL17 pathway. Together with that is further specified the treatment strategy and the way of its monitoring. These new findings have led to the update of recommendations for the treatment and monitoring of psoriatic arthritis by the Czech Society for Rheumatology.
Key words:
biological drugs – conventional synthetic disease-modifying antirheumatic drugs – early treatment – psoriatic arthritis – targeted synthetic disease modifying drugs – treat to target
Autoři: Jiří Štolfa
Působiště autorů: Revmatologický ústav, Praha
Vyšlo v časopise: Vnitř Lék 2018; 64(2): 127-135
Kategorie: Přehledné referáty
Souhrn
Psoriatická artritida (PsA) je heterogenní onemocnění postihující mimo kloubní synovialis i enteze, měkké tkáně celého prstu (daktylitida) a axiální skelet. Pro diagnózu PsA se v současné době používají klasifikační kritéria CASPAR. Onemocnění vede u velké části pacientů k nevratnému kloubnímu poškození (RTG, resp. klinickému), které výrazně zhoršuje kvalitu života a limituje pacienta v běžných aktivitách denního života a výrazně i limituje pracovní schopnost. Jsou doklady pro to, že časné zahájení léčby a léčba k cíli jsou schopny výrazně tento negativní vývoj omezit. V poslední době se prohlubují znalosti o patogenezi onemocnění a současně se objevují i nové léky, které cíleně zasahují do klíčových patogenetických dějů. Jedná se o biologické léky ze skupiny inhibitorů TNFα a v poslední době i inhibitory cesty Th17 – IL17. Současně se upřesňuje i strategie léčby a způsob její monitorace. Tyto nové poznatky vedly k aktualizaci doporučení pro léčbu a monitoraci psoriatické artritidy Českou revmatologickou společností.
Klíčová slova:
biologické léky – cílené syntetické chorobu modifikující léky – časná léčba – konvenční syntetické chorobu modifikující léky – léčba k cíli – psoriatická artritidaÚvod
Psoriatická artritida (PsA) je heterogenní onemocnění, které sdílí některé charakteristické klinické rysy (psoriáza, entezitida, sakroiliitida, spondylitida, uveitida), genetické pozadí a rodinnou anamnézu s větší skupinou spondylartritid (SpA), mezi které patří dále ankylozující spondylitida (Bechtěrevova choroba), reaktivní artritidy a enteropatické artritidy.
Psoriatická artritida zahrnuje více klinických manifestací než jenom postižení kloubů (artritida) a kůže (psoriáza). Týká se to entezí (entezitida), difuzního zánětu celého prstu (daktylitida) a axiálního skeletu (sakroiliitida/spondylitida). Proto by bylo výstižnější hovořit spíše o „psoriatické nemoci“ než jen o „psoriatické artritidě“.
V souvislosti s touto heterogenitou vyvstává otázka klasifikačních kritérií pro PsA. Dosud používaná diagnostická kritéria dle Molla a Wrighta z roku 1971 [1] nepostihují v plné šíři klinický obraz PsA. Od té doby byla vyvinuta řada dalších klasifikačních kritérií, která se však neujala. Nová klasifikační kritéria CASPAR (ClASsification criteria for Psoriatic ARthritis), tab. 1, umožňují stanovení diagnózy jak časné, tak etablované psoriatické artritidy s vysokou specificitou a senzitivitou. Na rozdíl od předchozích zahrnují i jiné manifestace než artritidu [2].
Tab. 1. Klasifikační kritéria CASPAR (ClASsification criteria for Psoriatic ARthritis) 
Chceme-li tedy hodnotit psoriatickou artritidu komplexně, je třeba do tohoto hodnocení zahrnout nejen artritidu a psoriázu, ale i uvedené další projevy, tj. entezitidy, daktylitidy a axiální postižení.
Léčba a farmakologické možnosti
Od toho se musí odvíjet i léčebná strategie, která musí přihlížet k těmto různým klinickým manifestacím a jejich kombinacích s vědomím, že ne všechny odpovídají stejně na stejné léky. Onemocnění významně zhoršuje kvalitu života v důsledku bolesti (způsobené nejen artritidou, ale i entezitidou, která může v klinickém obrazu i dominovat), funkčního omezení, kožního postižení, které kromě kosmetického dopadu a s tím souvisejících emočních problémů může pacienta obtěžovat i úporným svěděním a systémovou odpovědí na onemocnění (únava, nevýkonnost, deprese). Nezanedbatelné jsou i nežádoucí účinky léčby.
Cílem léčby je tedy kromě odstranění, resp. minimalizace subjektivní symptomatologie zejména prevence vývoje ireverzibilního kloubního poškození s příslušnými funkčními dopady. V terapeutických úvahách je nutno zohlednit i komorbidity, které toto onemocnění často doprovázejí. Jedná se zejména o obezitu, metabolický syndrom a kardiovaskulární onemocnění. V poslední době se zdůrazňuje princip „sdíleného rozhodnutí“ o léčbě. Do tohoto procesu by měli být zahrnuti kromě revmatologa i ostatní relevantní odborníci, a zejména také sám pacient.
Léčbu psoriatické artritidy (psoriatické nemoci) lze rozdělit do 3 úrovní:
- úroveň – nesteroidní antirevmatika (NSA), intraartikulární glukokortikoidy (GK)
- úroveň – konvenční syntetické chorobu modifikující léky (csDMARDs)
- úroveň – biologická farmaka (bDMARDs)
V rámci biologických farmak přicházejí na trh nová farmaka s odlišným mechanizmem účinku než je inhibice TNFα (TNFi) – inhibitory osy IL12/23-IL17 (ustekinumab, sekukinumab). Nově jsou vyvíjena farmaka s „malou molekulou“, cílená na určité komponenty imunopatologického řetězce (intracelulární přenašeče) pro perorální použití – cílená, syntetická chorobu modifikující farmaka (tsDMARDs) – apremilast, tofacitinib.
Současně se etabluje nová strategie léčby, stojící na časné léčbě a léčbě k cíli.
Nesteroidní antirevmatika
Nesteroidní antirevmatika (NSA) jsou lékem první volby u aktivní PsA. Není nezbytné podávat NSA paušálně všem pacientům, v některých případech lze vystačit s prostými analgetiky, někteří pacienti nevyžadují žádnou symptomatickou terapii. Koxiby jsou v této indikaci stejně účinné jako neselektivní NSA. Vždy je třeba mít na paměti, že NSA nemají žádný chorobu modifikující efekt a že jejich použití v monoterapii je možné pouze u lehkých, nedestruktivních forem onemocnění bez výraznějšího kožního postižení (které mohou potenciálně i zhoršit).
Glukokortikoidy (GK)
Intraartikulární aplikace glukokortikoidů (GK) je užitečná u lokalizovaných forem (oligoartritida/monoartritida, entezitida, daktylitida) a u akutních vzplanutí jinak dobře kontrolovaných polyartikulárních forem. V případě daktylitid se kortikoid aplikuje do šlachové pochvy, případně do okolí šlachy, optimálně pod ultrasonografickou kontrolou.
Systémové podávání GK je spojeno s rizikem vzplanutí kožního syndromu při jejich detrakci, i když pro to není opora v klinických studiích. Současně chybí doklady o účinnosti GK z klinických studií u psoriatické artritidy. Přesto v registrech pacientů s PsA užívá značná část pacientů systémové GK (např. v německém registru 30 % pacientů). Systémové podávání glukokortikoidů by mělo být vyhrazeno jen pro těžké, zpravidla polyartikulární relapsy onemocnění, v nízké dávce, po co nejkratší dobu.
Chorobu modifikující léky
Chorobu modifikující léky (csDMARDs) jsou indikovány tam, kde nebylo dosaženo léčebného cíle postupem na první úrovni léčby (NSA, resp. intraartikulární GK). Lékem 1. volby je při nepřítomnosti kontraindikací či intolerance metotrexát. Alternativou jsou leflunomid, sulfasalazin nebo cyklosporin A.
V přítomnosti negativních prognostických markerů (tab. 2) nebo závažného kožního syndromu (tab. 3) je možné tuto úroveň vynechat a zavést léčbu csDMARDs ihned.
Tab. 2. Nepříznivé prognostické markery 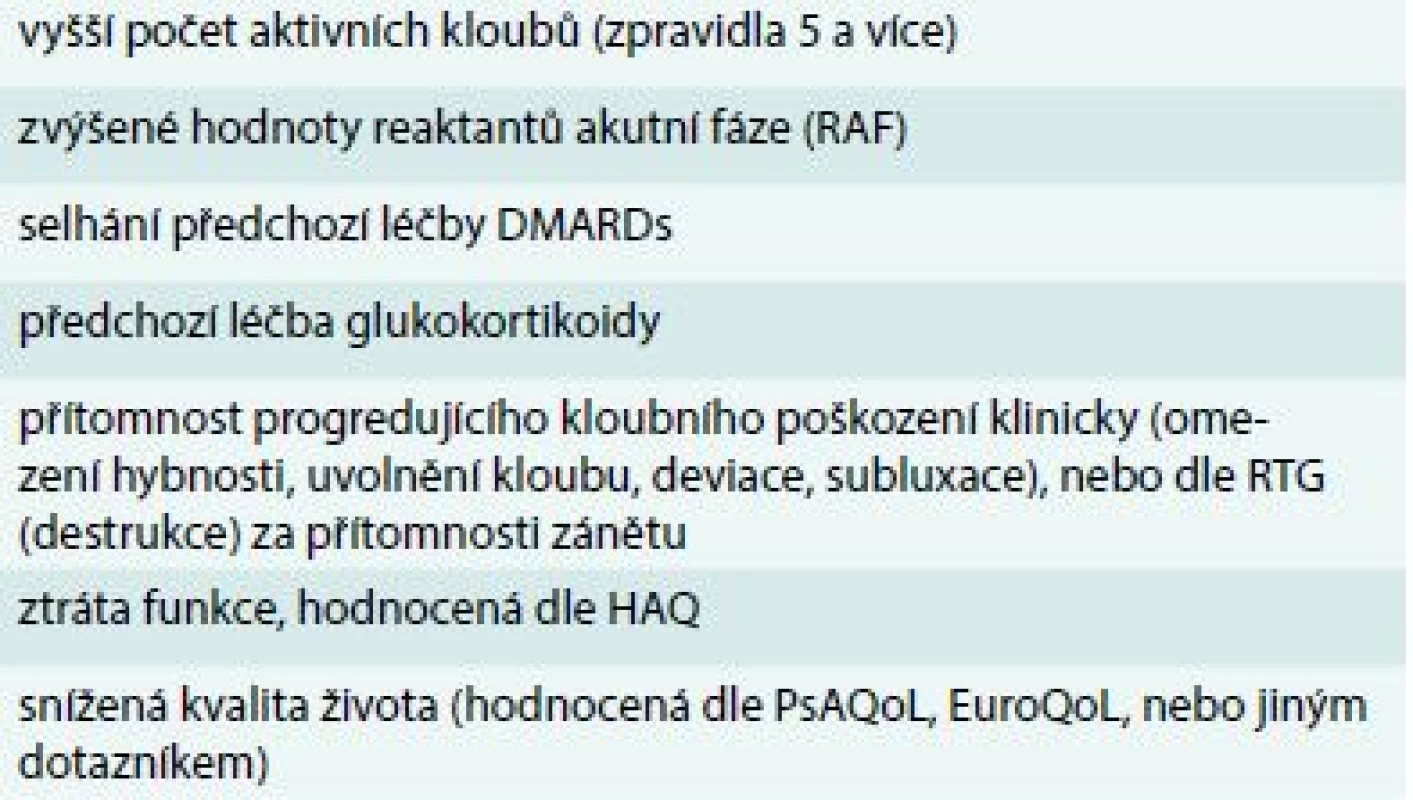
Tab. 3. Globální hodnocení psoriázy lékařem (GHPL) 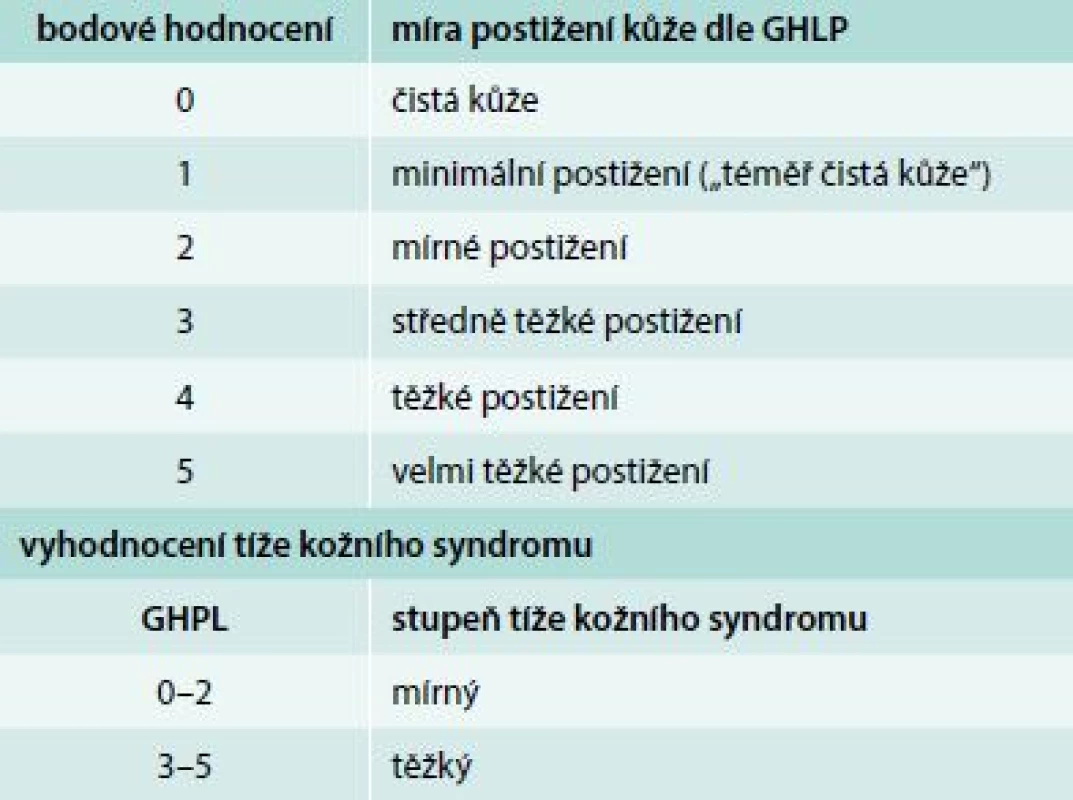
Biologická léčba – anti-TNFα
V současné době jsou pro léčbu PsA schváleny a pojišťovnami kategorizovány všechny inhibitory TNFα (anti-TNFα), tj. infliximab, etanercept, adalimumab, golimumab a certolizumab.
Obecně je biologická léčba anti-TNFα indikována v případě selhání léčby nižší úrovní, tedy zpravidla konvenčními syntetickými DMARDs v průběhu 3–6 měsíců (dle farmakodynamického profilu léku). Selháním léčby se rozumí nedosažení léčebného cíle, tj. remise, nebo stavu „minimální aktivity onemocnění“ (minimal disease activity – MDA), tab. 4.
Tab. 4. Minimální aktivita onemocnění 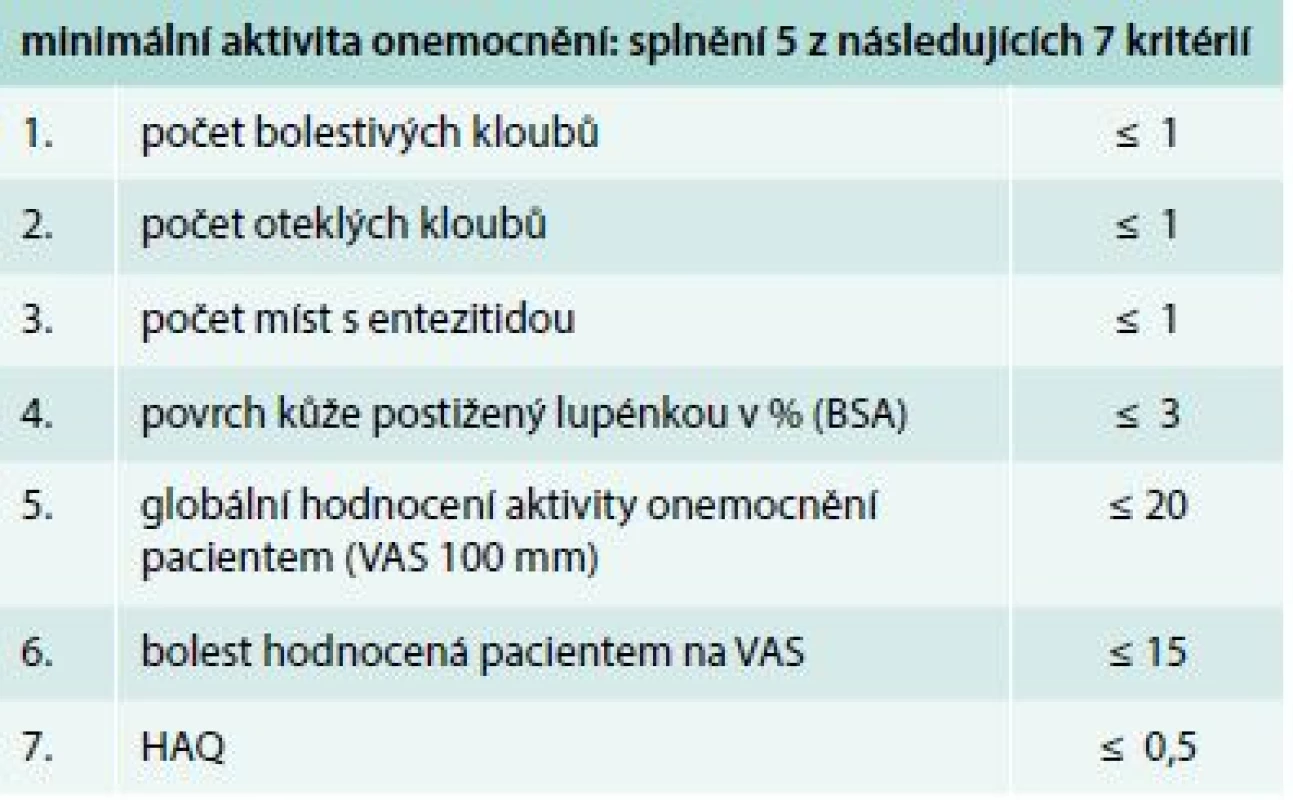
BSA – Body Surface Area HAQ – Health Assessment Questionaire VAS – vizuální analogová stupnice Nebyly prokázány rozdíly v účinnosti mezi jednotlivými inhibitory TNFα (TNFi), i když studie srovnávající jednotlivé preparáty přímo chybějí. Nejsou žádné doklady o vyšší účinnosti TNF inhibitorů (TNFi) v kombinaci s csDMARDs ve srovnání s TNFi v monoterapii.
TNFi jsou účinné i u entezitid a daktylitid. U těchto pacientů může být léčba TNFi indikována i bez předchozího léčebného pokusu csDMARDs, vzhledem k tomu, že chybí doklady o jejich účinnosti v těchto situacích [3]. Předpokladem pro takový postup je ale selhání nespecifické protizánětlivé léčby (NSA) a alespoň 2 lokálních injekcí glukokortikoidu a přetrvávající těžká entezitida/daktylitida. V současné době není shoda v definici závažné/těžké entezitidy/daktylitidy. Pro potřebu českých národních „doporučení“ definujeme závažnou/těžkou daktylitidu jako přítomnost 3 míst s entezitidou, resp. 3 prstů postižených daktylitidou a významné funkční omezení [4], doplněné o sonografickou verifikaci.
U pacientů s predominantním aktivním postižením axiálního skeletu je indikována biologická léčba bez předchozího pokusu s csDMARDs. Aktivním axiálním postižením se zde rozumí hodnota BASDAI (Bath Ankylosing Spondylitis Disease Activity Index) ≥ 40 mm/VAS (vizuální analogová škála) 100 mm a hodnota ASQoL (Ankylosing Spondylitis Quality of Life) > 6.
Infliximab
Infliximab je chimerická monoklonální protilátka proti tumory nekrotizujícímu faktoru (tumour necrosis factor α – TNFα). Molekula infliximabu je tvořena ze 75 % humánní a z 25 % myší komponentou (variabilní část imunoglobulinové molekuly – Fab). Váže se jak na solubilní, tak na transmembránovou formu TNFα v pikomolárních koncentracích. Tento komplex váže komplement a vede k lýze buňky [5]. Infliximab (na rozdíl od etenarceptu) neváže TNFβ (lymfotoxin). Eliminační poločas infliximabu je kolem 10 dní.
Účinnost infliximabu byla prokázána pro léčbu psoriázy [6,7], a to i u pacientů, kteří neodpověděli dostatečně na léčbu etanerceptem [8]. Je účinný ve srovnání s placebem i v léčbě nehtové psoriázy, a to projevů vycházejících jak z matrix, tak z nehtového lůžka [6]. Stejně účinně ovlivňuje i psoriatickou artritidu bez ohledu na současné užívání metotrexátu [6,9], včetně jejích extraartikulárních projevů jako je daktylitida nebo entezitida [6,9]. Infliximab signifikantně inhibuje i progresi RTG poškození [10]. S tím souvisí i signifikantní zlepšení funkčního omezení hodnoceného dle HAQ a SF-36 a kvality života [6,9].
Podává se v nitrožilních infuzích v dávce 3–5 mg/kg hmotnosti v 6–8 týdenních intervalech. Na úvod léčby se podávají tyto infuze v týdnech 0, 2 a 6. Kombinace s metotrexátem je vhodná vzhledem k omezení tvorby antichimérických protilátek (HACA).
Etanercept
Etanercept je solubilní, dimerický fúzovaný protein, sestávající ze dvou extracelulárních částí humánního receptoru pro TNFα p75 a konstantní části humánního imunoglobulinu IgG1.
Po parenterálním podání váže volný TNFα, a tím blokuje jeho interakci s membránovým receptorem, a oslabuje tak jeho prozánětlivý efekt. Komplex TNFα-etanercept neváže komplement, nevede proto k lýze buňky [5]. Eliminační poločas etanerceptu je kolem 4 dní.
Klinická hodnocení prokazují jeho účinnost u všech klinických manifestací, včetně periferních kloubů, entezitid a daktylitid [11], zpomaluje i RTG progresi [12,13].
Metaanalýza klinických studií ukázala poněkud nižší účinnost etanerceptu u psoriázy ve srovnání s adalimumabem, golimumabem a infliximabem [14]. Je účinný i u nehtové psoriázy a Výbor národní nadace pro psoriázu (National Psoriasis Foundation) jej doporučil i k léčbě izolovaného postižení nehtů [15].
U PsA se podává v subkutánních injekcích 50 mg 1krát týdně, nebo 25 mg 2krát týdně.
Adalimumab
Adalimumab je rekombinantní humánní monoklonální protilátka IgG1 specifická proti TNFα. Váže se na TNFα s vysokou afinitou a specifitou, a tím neutralizuje biologickou funkci solubilního i membránově vázaného TNFα blokádou interakce s oběma buněčnými receptory p55 a p75. Neváže se na TNFβ (lymfotoxin) [16]. Eliminační poločas adalimumabu je kolem 14 dní.
Klinická hodnocení prokazují účinnost prakticky u všech manifestací PsA, tedy u periferní artritidy, u kožního postižení, ale i u entezitid, daktylitid [16], a zejména je schopen zpomalit RTG progresi [17]. Současně významně zlepšuje i funkční důsledky onemocnění (měřeno indexy HAQ – Health Assessment Questionaire a FACIT – Functional Assessment of Chronic Illness Therapy), kvalitu života (Dermatology Life Quality Index – DLQI) a SF-36 [17]. Nepřímé srovnání účinnosti adalimumabu s jinými TNF inhibitory (infliximab, etanercept, golimumab) neukázalo žádné rozdíly v účinnosti ani v bezpečnostním profilu [18,19]. Účinnost adalimumabu zůstává zachována i po přechodu z jiného TNFi, i když účinnost je numericky poněkud nižší [20,21]. Klinické a observační studie prokázaly dobrou účinnost i u psoriatického postižení nehtů. Na základě těchto studií jej Výbor národní nadace pro psoriázu (National Psoriasis Foundation) doporučil mimo jiné i k léčbě izolovaného postižení nehtů [15].
Podává se v subkutánních injekcích v dávce 40 mg 1krát za 2 týdny. Podobně jako u etanerceptu, lze jej podávat samostatně, bez metotrexátu, ale kombinované podávání může v některých případech potencovat jeho účinnost [22].
Golimumab
Jedná se o plně humánní monoklonální protilátku proti TNFα. Váže se jak na solubilní, tak na transmembránovou formu TNFα, váže komplement a vede k lýze buňky [5]. Eliminační poločas golimumabu je 14 dní.
Studie fáze 3 ukázaly přetrvávající zlepšení všech sledovaných parametrů kožních, včetně nehtové psoriázy [23], kloubních [23,24] a entezitid [25]. Daktylitida byla příznivě ovlivněna ve srovnání s placebem pouze vyšší dávkou – 100 mg [25]. Zlepšuje kvalitu života, zvyšuje produktivitu a inhibuje rentgenovou progresi [24,25].
Podává se subkutánně 1krát měsíčně v dávce 50 mg.
Certolizumab
Pegylovaný Fab fragment monoklonální protilátky proti TNFα. Váže se na TNFα a zabraňuje tak jeho vazbě na membránový receptor. Protože neobsahuje Fc oblast protilátky, neváže komplement, ani nenavozuje protilátkami zprostředkovanou, cytotoxicitu in vitro. Eliminační poločas certolizumabu je 14 dní.
Jeho účinnost je podobná jako u infliximabu a adalimumabu.
V klinických studiích byla prokázána jeho účinnost v léčbě kožní i nehtové psoriázy [27], stejně tak jako v léčbě psoriatické artritidy [26,28], i entezitidy a daktylitidy [29]. Podobně jako ostatní inhibitory TNFα účinně inhibuje RTG progresi [30]. Významně zlepšuje i funkční parametry, kvalitu života a pracovní produktivitu [31,32]. Jeho účinnost zůstává zachována i u pacientů před tím léčených jinými inhibitory TNFα [29].
Podává se subkutánně v iniciální dávce 400 mg v týdnech 0; 2 a 4 a dále v dávce 200 mg za 2 týdny.
Nová farmaka k léčbě psoriatické artritidy
V současné době jsou schváleny a hrazeny všechny inhibitory TNFα (infliximab, etanercept, adalimumab, golimumab, certolizumab).
V posledních letech se ukazuje, že mimo TNFα mají v genezi psoriázy, PsA a ostatních chorobných jednotek v rámci spondylartritid (SpA), nepochybně význam i jiné složky imunopatogeneze. Pozornost se v současné době soustřeďuje zejména na interleukin 12/23 (IL12/23), na interleukin 17 (IL17) a na tzv. malé molekuly, které modulují postreceptorové, transdukční děje (inhibitory JAK a apremilast). Tato farmaka jsou vyráběna synteticky a používá se pro ně označení cílené (targeted) syntetické (synthetic) DMARDs – tsDMARDs.
Modulace interleukinů 12/23
Nadměrná produkce IL23 je jedním z hnacích patogenetických mechanizmů v celé skupině SpA a současně je známa vyšší senzitivita na jeho působení u psoriázy, ale také u AS a u idiopatických střevních zánětů.
Ustekinumab
Ustekinumab – plně humánní monoklonální protilátka IgG1κ se specifickou afinitou k podjednotce p40 cytokinů IL12 a IL23, kterým tak brání navázat se na receptory exprimované na povrchu imunitních buněk, je jedním z prvních biologických léků této skupiny. Eliminační poločas se pohybuje mezi 15 a 45 dny.
Ustekinumab signifikantně zlepšuje psoriázu hodnocenou dle indexu PASI (Psoriasis Area and Severity Index). Ve studii ACCEPT – Active Comparator (CNTO1275/Enbrel) Psoriasis Trial, která porovnávala ustekinumab s etanerceptem, byla numericky lepší odpověď u obou dávek ustekinumabu (45 mg, resp. 90 mg) dle PASI75 [33].
Účinnost ustekinumabu u PsA byla prokázána ve 2 klinických studiích fáze 3, PSUMMIT I a II. Ve studii PSUMMIT I (ustekinumab 90 mg, resp. 45 mg po 12 týdnech vs placebo) bylo ve 24. týdnu dosaženo statisticky významně lepší odpovědi dle ACR20, ACR50 – kritéria American College of Rheumatology, stejně jako u kožní odpovědi dle PASI75. Mimo to se významně zlepšily i ostatní manifestace psoriatické nemoci, jako daktylitidy a entezitidy [34]. Tento efekt přetrvával i po 1 roce.
Do studie PSUMMIT II byli zařazeni i pacienti s předchozí expozicí TNFi (58 %) a dále byli stratifikování dle současného užívání metotrexátu při zahájení studie. Odpověď jak kloubní (dle ACR20), tak kožní (dle PASI) byla obdobná jako ve studii PSUMMIT I, ukázalo se ale, že pacienti s předchozí expozicí TNFi měli numericky horší odpověď (35,6 % pro obě dávky vs 14,5 % u placeba, ve srovnání s TNFi „naivními“ pacienty – 43,8 % vs 20,2 %). Odpověď se dále zhoršila u pacientů se 2 a více TNFi. Komedikace metotrexátem neměla žádný vliv na odpověď [35].
Po sloučení obou studií bylo propočítáno relativní riziko (RR) pro ACR20 proti placebu s výsledkem 2,17 (95% CI 1,71–2,76) pro dávku 90 mg, resp. 1,95 (95% CI 1,52–2,50) pro dávku 45 mg [36]. Rovněž se zpomalila RTG progrese [37]. Nevyskytl se žádný závažný nežádoucí účinek, pro který by pacient musel být ukončen ve studii [36]. V malé, otevřené studii ECLIPSA, která porovnávala ustekinumab s celou skupinou inhibitorů TNFα, byla signifikantně lepší odpověď u entezitid hodnocená dle skóre SPARCC (Spondyloarthritis Research Consortium of Canada): 71 % pacientů ve skupině užívající ustekinumab dosáhlo úplného vymizení entezitid (skóre 0) ve srovnání s 55 % ve skupině užívající inhibitory TNFα [38]. Signifikantně zlepšuje i funkci hodnocenou dle HAQ a kvalitu života [39].
Ustekinumab (STELARA) je v ČR registrovaný pro použití u psoriázy i u PsA, kategorizován je zatím pouze pro použití u psoriázy.
Podává se v subkutánních injekcích v iniciální dávce 45 mg v týdnu 0 a 4 a následně 45 mg po 12 týdnech. U pacientů se středně těžkou a těžkou psoriázou se podává v dávce 90 mg ve stejném schématu.
Inhibice interleukinu 17
IL 17 je prozánětlivý cytokin, který hraje rovněž významnou roli v patogenezi psoriázy a psoriatické artritidy, podobně jako v jiných imunitně zprostředkovaných chronických zánětlivých onemocněních. Zvýšená exprese IL17 byla nalezena jak v synovialis kloubů u pacientů s PsA, tak v psoriatických lézích. Inhibice tohoto cytokinu tak představuje relevantní cíl léčby PsA [40].
Sekukinumab
Nedávno registrovaný je sekukinumab – plně humánní monoklonální protilátka proti IL17A.
Sekukinumab je první inhibitor IL17A s prokázanou účinností u psoriatické artritidy. Byla prokázána ve studiích FUTURE 1 a FUTURE 2 u více než 1 000 pacientů. V těchto studiích kontrolovaných placebem signifikantně zlepšil všechny domény „psoriatické nemoci“ včetně kožních, kloubních i extraartikulárních manifestací (entezitidy, daktylitidy). U více než 80 % pacientů nebyla pozorována žádná RTG progrese. Sekukinumab byl účinným bez ohledu na současnou léčbu metotrexátem nebo předchozí léčbu inhibitory TNFα [41].
V obou studiích (FUTURE 1 a FUTURE 2) dostávali pacienti sekukinumab po 4 týdnech v dávkách 300 mg, 150 mg, nebo 75 mg. Metaanalýza obou studií určila RR (risk ratio) pro ACR20 3,31 (95% CI 2,04–5,36), 5,82 (95% CI 1,56–21,71), a 4,47 (95% CI 0,66–30,26) [36].
V randomizované srovnávací studii FIXTURE byl sekukinumab účinnější než etanercept [42].
Pokud se jedná o bezpečnost, nebyl žádný rozdíl v ukončení studie pro nežádoucí účinky, resp. závažné nežádoucí účinky ve skupině sekukinumabu oproti placebu. Vyskytly se případy kandidózy ve skupině sekukinumabu (2 % ve FUTURE 1, resp. 5 % ve FUTURE 2) ve srovnání se skupinou užívající placebo, v níž se kandidóza nevyskytla. Nevedly ale k přerušení studie [36].
Podává se subkutánně v dávce 150 mg s iniciálním podáním v týdnech 0, 1, 2 a 3, následovaná měsíční udržovací dávkou od týdne 4. U pacientů se současně přítomnou středně těžkou až těžkou ložiskovou psoriázou nebo u pacientů nedostatečně odpovídajících na anti-TNFα (IR), je doporučená dávka 300 mg se stejným schématem. Každá dávka 300 mg je podána ve 2 dílčích subkutánních injekcích po 150 mg.
Ixekizumab
V současné době probíhá studie fáze 3 s podobným preparátem – ixekizumabem – monoklonální, humanizovanou protilátkou proti IL17A. Předběžné výsledky ukazují na dobrou účinnost u PsA, s podobnou účinností jako v kontrolní větvi s adalimumabem [43].
Brodalumab
Studie s blokátorem receptoru pro IL17 (brodalumab) byla pozastavena pro zvýšený výskyt depresí.
Apremilast
Apremilast je specifický inhibitor fosfodiesterázy 4. Jedná se o novou, malou molekulu pro perorální použití. Apremilast moduluje expresi prozánětlivých cytokinů prostřednictvím zvýšené hladiny intracelulárního cAMP s následným snížením hladin TNFα, IL12 a IL23 [44]. Ve studii fáze 2 prokázal účinnost proti placebu v dávce 20 mg 2krát denně, resp. 40 mg 1krát denně, hodnoceno dle ACR20. Nejčastějšími nežádoucími účinky byly průjem, bolesti hlavy, nauzea, únava a katary horních cest dýchacích [45]. V současné době probíhají klinické studie fáze 3 u psoriázy i psoriatické artritidy. V rámci programu PALACE (The Psoriatic Arthritis Long-term Assessment of Clinical Efficacy) probíhají 4 studie (PALACE 1; 2; 3; 4). Předběžné výsledky studie PALACE 1 (23,6 % pacientů bylo před tím léčeno TNFi, u 9,3 % z nich šlo o selhání léčby) potvrdily účinnost i u pacientů s PsA, kteří byli v minulosti léčeni TNFi, i když odpověď dle ACR20 byla poněkud nižší [46,47]. Současné podávání metotrexátu nezvyšuje účinnost.
Metaanalýza těchto studií ukázala RR odpovědi dle ACR20 oproti placebu 1,98 (95% CI 1,64–2,38) pro dávku 2krát 30 mg, resp. 1,70 (95% CI 1,40–2,06) pro dávku 2krát 20 mg. Dobrá odpověď byla i pro kožní postižení a entezitidy, nebyla však zaznamenána významná odpověď pro daktylitidy [36].
Z výsledků dosavadních studií vyplývá, že účinnost apremilastu u psoriázy a psoriatické artritidy je relativně nižší. Zdá se tedy, že bude vhodný u pacientů s dominantním kloubním postižením, s mírnou až střední formou a mírnou psoriázou a po selhání bDMARD 1 linie (TNFi). Významný je i jeho příznivý bezpečnostní profil.
Inhibitory JAK
Tofacitinib
Janusovy kinázy (JAK) jsou intracelulární tyrozinové kinázy, sloužící jako intracelulární signální molekuly pro různé prozánětlivé molekuly (včetně IL23), které jsou nezbytné pro aktivaci a plnou funkci T-lymfocytů.
Tofacitinib je inhibitor JAK1 a JAK3, do menší míry i JAK2 [48]. Jedná se o malou molekulu, určenou pro perorální podání. Tofacitinib mimo jiné suprimuje expresi receptoru pro IL23, a tím ovlivňuje diferenciaci Th17 buněk. Současně interferuje se signalizací IL6 a IFNγ [49]. Studie u RA ukázaly dobré výsledky v monoterapii i v kombinaci s jinými DMARDs. Účinnost byla prokázána i u psoriázy ve studii fáze 2 [50]; studie fáze 3 probíhá. U psoriatické artritidy probíhá multicentrická randomizovaná studie fáze 3 s tofacitinibem v dávce 5 mg, resp. 10 mg 2krát denně kontrolovaná placebem. Určité riziko léčby představují infekce, malignity, hyperlipidemie, leukopenie a anémie.
Strategie léčby
Strategie léčby vychází z časného záchytu onemocnění a zahájení léčby, tak aby se zabránilo nevratnému poškození klouby. Druhým pilířem léčby je „léčba k cíli“. V současné době se pokládá za racionální cíl kromě remise, která není vždy dosažitelná, dosažení alespoň „minimální aktivity onemocnění“ (MDA), tab. 4.
Problémem léčby PsA je, že onemocnění postihuje různé tkáně pohybového aparátu – kromě kloubů a kůže i úpony (entezitidy), měkké tkáně celého prstu (daktylitidy), axiální skelet (sakroiliitida/spondylitida) a nehty, a proto musí být léčba individualizována dle dominantního postižení.
Česká revmatologická společnost publikovala v roce 2017 Doporučení pro léčbu psoriatické artritidy [51]. V nich specifikovala i indikace pro zahájení biologické léčby (tab. 5, 6, 7 a 8). Biologická a cílená syntetická farmaka schválená pro léčbu psoriatické artritidy jsou uvedena v tab. 9.
Tab. 5. Indikace biologické léčby u postižení periferních kloubů u PsA 
Tab. 6. Indikace biologické léčby u izolovaných entezitid 
Tab. 7. Indikace biologické léčby u izolovaných daktylitid 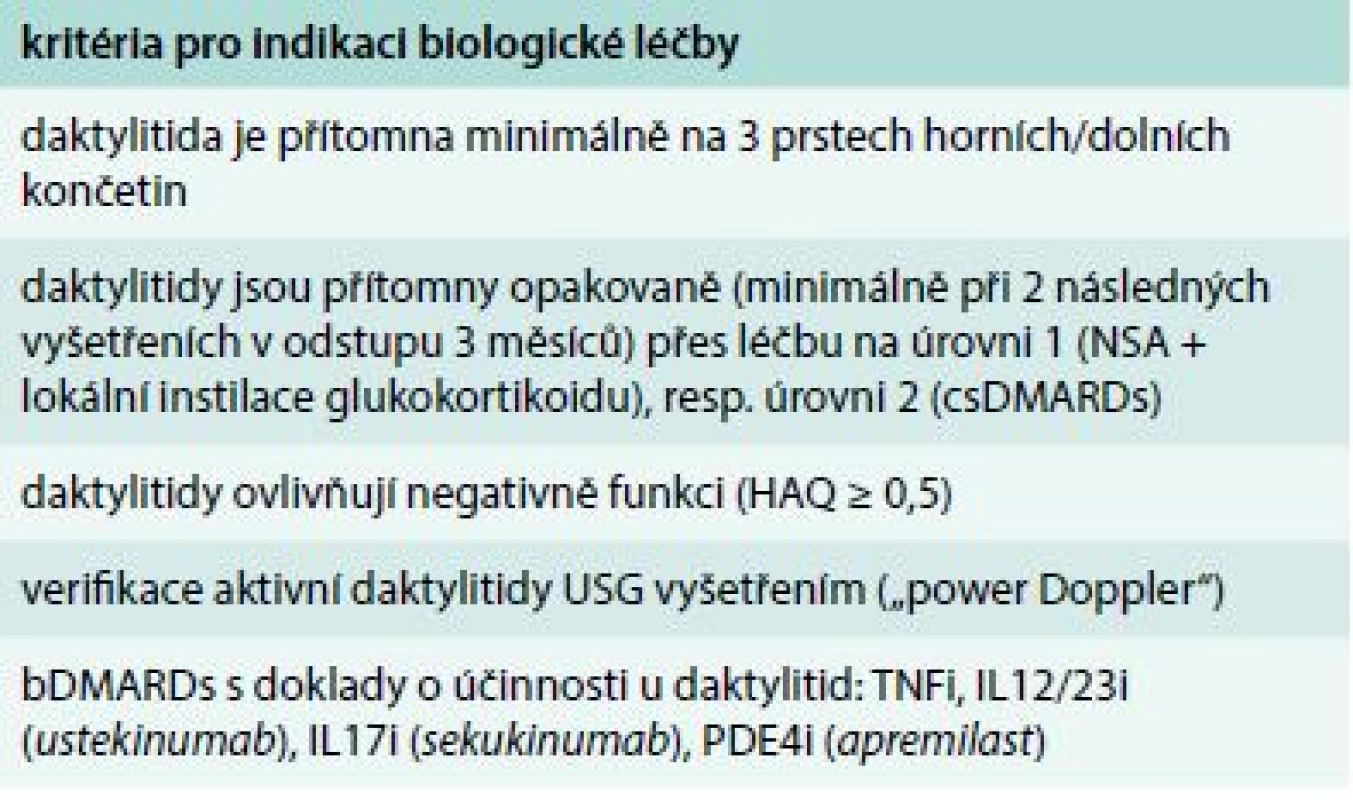
Tab. 8. Indikace biologické léčby u izolovaných axiálních forem PsA 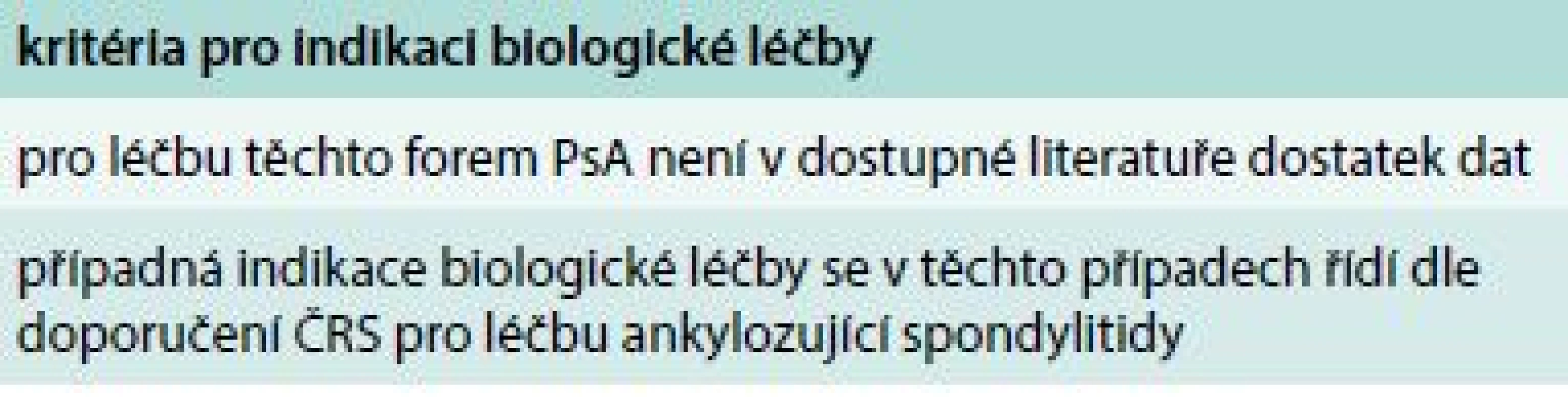
Tab. 9. Biologická farmaka schválená pro léčbu psoriatické artritidy 
Závěr
Léčba psoriatické artritidy prodělala v posledních letech výrazný posun. Jednak byly vyvinuty nové biologické léky s odlišným mechanizmem účinku (než je inhibice TNFα) – ustekinumab a sekukinumab, a cílené syntetické léky pro perorální použití – apremilast a tofacitinib. Kromě tofacitinibu již byli schváleny pro použití u psoriatické artritidy, dosud ale nebyla stanovena úhrada.
Další vývoj bude směřovat k hlubšímu poznání patogeneze onemocnění, vývoji nových léků a upřesnění strategie léčby.
Od těchto opatření lze očekávat lepší výsledky léčby i zlepšení kvality života a zachování pracovní schopnosti.
Tato práce vznikla za podpory Výzkumných záměrů MZ ČR č. 000 000 23728.
Doručeno do redakce 4. 10. 2017
Přijato po recenzi 19. 11. 2017
prim. MUDr. Jiří Štolfa, Ph.D.
Revmatologický ústav, Praha
Zdroje
1. Wright V, Moll JM. Psoriatic arthritis. Bull Rheum Dis 1971; 21(5): 627–632.
2. Taylor W, Gladman D, Helliwell P et al. Classification criteria for psoriatic arthritis: development of new criteria from a large international study. Arthritis Rheumatol 2006; 54(8): 2665–2673. Dostupné z DOI: <http://dx.doi.org/10.1002/art.21972>.
3. Ash Z, Gaujoux-Viala C, Gossec L, et al. A systematic literature review of drug therapies for the treatment of psoriatic arthritis: current evidence and meta-analysis informing the EULAR recommendations for the management of psoriatic arthritis. Ann Rheum Dis 2012; 71(3): 319–326. Dostupné z DOI: <http://dx.doi.org/10.1136/ard.2011.150995>.
4. Mumtaz A, Gallagher P, Kirby B et al. Development of a preliminary composite disease activity index in psoriatic arthritis. Ann Rheum Dis 2011; 70(2) :272–277. Dostupné z DOI: <http://dx.doi.org/10.1136/ard.2010.129379>.
5. Braun J, Sieper J. Role of novel biological therapies in psoriatic arthritis. Therapy review. Biodrugs 2003; 17(3): 187–199.
6. Antoni CE, Kavanaugh A, Kirkham B et al. Sustained benefits of infliximab therapy for dermatologic and articular manifestations of psoriatic arthritis: results from the infliximab multinational psoriatic arthritis controlled trial (IMPACT). Arthritis Rheumatol 2005; 52(4): 1227–1236. Dostupné z DOI: <http://dx.doi.org/10.1002/art.20967>. Erratum in Arthritis Rheumatol. 2005; 52(9): 2951.
7. Reich K, Nestle FO, Papp K et al. Infliximab induction and maintenance therapy for moderate-to-severe psoriasis: a phase III, multicentre, double-blindtrial. Lancet 2005; 366(9494): 1367–1374.
8. Gottlieb AB, Kalb RE, Blauvelt A et al. The efficacy and safety of infliximab inpatients with plaque psoriasis who had an inadequate response to etanercept: results of a prospective, multicenter, open-label study. J Am Acad Dermatol 2012; 67(4): 642–650. Dostupné z DOI: <http://dx.doi.org/10.1016/j.jaad.2011.10.020>.
9. Kavanaugh A, Krueger GG, Beutler A et al. Infliximab maintains a high degree of clinical response in patients with active psoriatic arthritis through 1 year of treatment: results from the IMPACT 2 trial. Ann Rheum Dis 2007; 66(4): 498–505. Dostupné z DOI: <http://dx.doi.org/10.1136/ard.2006.058339>.
10. van der Heijde D, Kavanaugh A, Gladman DD et al. Infliximab inhibits progression of radiographic damage in patients with active psoriatic arthritis through 1 year of treatment: results from the induction and maintenance psoriatic arthritis clinical trial 2. Arthritis Rheumatol 2007; 56(8): 2698–2707. Dostupné z DOI: <http://dx.doi.org/10.1002/art.22805>.
11. Sterry W, Ortonne JP, Kirkham B et al. Comparison of two etanercept regimens for treatment of psoriasis and psoriatic arthritis: PRESTA randomised double blind multicentre trial. BMJ 2010; 340: c147. Dostupné z DOI: <http://dx.doi.org/10.1136/bmj.c147>.
12. Mease PJ, Kivitz AJ, Burch FX et al. Etanercept treatment of psoriatic arthritis: safety, efficacy, and effect on disease progression. Arthritis Rheumatol 2004; 50(7): 2264–2272. Dostupné z DOI: <http://dx.doi.org/10.1002/art.20335>.
13. Mease PJ, Kivitz AJ, Burch FX et al. Continued inhibition of radiographic progression inpatients with psoriatic arthritis following 2 years of treatment with etanercept. J Rheumatol 2006; 33(4): 712–721.
14. Ash Z, Gaujoux-Viala C, Gossec L et al. A systematic literature review of drug therapies for the treatment of psoriatic arthritis: current evidence and meta-analysis informing the EULAR recommendations for the management of psoriatic arthritis. Ann Rheum Dis 2012; 71(3):319–326. Dostupné z DOI: <http://dx.doi.org/10.1136/ard.2011.150995>.
15. Crowley JJ, Weinberg JM, Wu JJ et al. Treatment of nail psoriasis: best practice recommendations from the medical board of the national psoriasis foundation. JAMA Dermatol 2015; 151(1): 87–94. Dostupné z DOI: <http://dx.doi.org/10.1001/jamadermatol.2014.2983>.
16. Baker DE. Adalimumab: Human recombinant imunoglobulin G1 anti-tumour necrosis factor monoclonal antibody. Rev Gastroenterol Disord 2004; 48(4): 196–210.
17. Gladman DD, Mease PJ, Cifaldi MA et al. Adalimumab improves joint-related and skin related functional impairment in patients with psoriatic arthritis: patient-reported outcomes of the adalimumab effectiveness in psoriatic arthritis trial. Ann Rheum Dis 2007; 66(2): 163–168. Dostupné z DOI: <http://dx.doi.org/10.1136/ard.2006.057901>.
18. Fenix-Caballero S, Alegre-del Rey EJ, Castano-Lara R et al. Direct and indirect comparison of the efficacy and safety of adalimumab, etanercept, infliximab and golimumab in Psoriatic arthritis. J Clin Pharm Ther 2013; 38(4): 286–293. Dostupné z DOI: <http://dx.doi.org/10.1111/jcpt.12045>.
19. Thorlund K, Druyts E, Avina-Zubieta JA et al. Anti-tumor necrosis factor (TNF) drugs for the treatment of Psoriatic arthritis: an indirect comparison meta-analysis. Biologics 2012; 6 : 417–427. Dostupné z DOI: <http://dx.doi.org/10.2147/BTT.S37606>. Erratum in Biologics 2014; 8 : 57–58.
20. Fagerli KM, Lie E, van der Heijde D et al. Switching between TNF inhibitors in psoriatic arthritis: data from the NOR-DMARD study. Ann Rheum Dis 2013; 72(11): 1840–1844. Dostupné z DOI: <http://dx.doi.org/10.1136/annrheumdis-2012–203018>.
21. Glintborg B, Ostergaard M, Krogh NS et al. Clinical response, drug survival, and predictors thereof among 548 patients with psoriatic arthritis who switched tumor necrosis factor alpha inhibitor therapy: results from the Danish Nationwide DANBIO registry. Arthritis Rheumatol 2013; 65(5): 1213–1223. Dostupné z DOI: <http://dx.doi.org/10.1002/art.37876>.
22. Braun J, Sieper J. Role of novel biological therapies in psoriatic arthritis. Therapy review. Biodrugs 2003; 17(3): 187–199.
23. Kavanaugh A, McInnes I, Mease P et al. Golimumab, a new human tumor necrosis factor alpha antibody, administered every 4 weeks as a subcutaneous injection in psoriatic arthritis: 24-week efficacy and safety results of a randomized, placebo-controlled study. Arthritis Rheumatol 2009; 60(4): 976–986. Dostupné z DOI: <http://dx.doi.org/10.1002/art.24403>. Erratum in Arthritis Rheumatol 2010; 62(8): 2555.
24. Kavanaugh A, McInnes IB, Mease P et al. Clinical efficacy, radiographic and safety findings through 5 years of subcutaneous golimumab treatment in patients with active psoriatic arthritis: results from a long-term extension of a randomised, placebo-controlled trial (the GO-REVEAL study). Ann Rheum Dis 2014; 73(9):1689–1694. Dostupné z DOI: <http://dx.doi.org/10.1136/annrheumdis-2013–204902>.
25. Kavanaugh A, Mease P. Treatment of psoriatic arthritis with tumor necrosis factor inhibitors: longer-term outcomes including enthesitis and dactylitis with golimumab treatment in the long term extension of a randomized, placebo-controlled study (GO-REVEAL). J Rheumatol Suppl 2012; 89 : 90–93. Dostupné z DOI: <http://dx.doi.org/10.3899/jrheum.120254>.
26. Rozenblit M, Lebwohl M. New biologics for psoriasis and psoriatic arthritis. Dermatol Ther 2009; 22(1): 56–60. Dostupné z DOI: <http://dx.doi.org/10.1111/j.1529–8019.2008.01216.x>.
27. Reich K, Ortonne JP, Gottlieb AB et al Successful treatment of moderate to severe plaque psoriasis with the PEGylated Fab’ certolizumab pegol: results of a phase II randomized, placebo-controlled trial with a re-treatment extension. Br J Dermatol 2012; 167(1): 180–190. Dostupné z DOI: <http://dx.doi.org/10.1111/j.1365–2133.2012.10941.x>.
28. Mease PJ, Fleischmann R, Wollenhaupt J et al. Effect of certolizumab pegol over 48 weeks on signs and symptoms in patients with Psoriatic arthritis with and without prior tumor necrosis factor inhibitor exposure. Rheumatology 2014; 53(Suppl 1): i137-i138. Dostupné z DOI: <https://doi.org/10.1093/rheumatology/keu115.004>.
29. Mease PJ, Fleischmann R, Deodhar AA et al. Effect of certolizumab pegol on signsand symptoms in patients with psoriatic arthritis: 24-week results of a phase 3 double-blind randomised placebo-controlled study(RAPID-PsA). Ann Rheum Dis 2014; 73(1): 48–55. Dostupné z DOI: <http://dx.doi.org/10.1136/annrheumdis-2013–203696>.
30. van der Heijde D, Fleischmann R, Wollenhaupt J et al. Effect of different imputation approaches on the evaluation of radiographic progression in patients with psoriatic arthritis: results of the RAPID-PsA 24-week phase III double-blind randomised placebo-controlled study of certolizumab pegol. Ann Rheum Dis 2014; 73(1): 233–237. Dostupné z DOI: <http://dx.doi.org/10.1136/annrheumdis-2013–203697>.
31. Gladman D, Fleischmann R, Coteur G et al. Effect of certolizumab pegol on multiple facets of Psoriatic arthritis as reported by patients: 24-week patient-reported outcome results of a phase III, multicenter study. Arthritis Care Res 2014; 66(7): 1085–1092. Dostupné z DOI: <http://dx.doi.org/10.1002/acr.22256>.
32. Kavanaugh A, Gladman D, van der Heijde D et al. Improvements in productivity at paid work and within the household, and increased participation in daily activities after 24 weeks of certolizumab pegol treatment of patients with psoriatic arthritis: results of a phase 3 double-blind randomised placebo-controlled study. Ann Rheum Dis 2015; 74(1): 44–51. Dostupné z DOI: <http://dx.doi.org/10.1136/annrheumdis-2014–205198>.
33. Young MS, Horn EJ, Cather JC. The ACCEPT study: ustekinumab versus etanercept in moderate-to-severe psoriasis patients. Expert Rev Clin Immunol 2011; 7(1): 9–13. Dostupné z DOI: <http://dx.doi.org/10.1586/eci.10.92>.
34. Ritchlin CT, Gottlieb AB, McInnes IB et al. Ustekinumab in active psoriatic arthritis including patients previously treated with anti-TNF agents: results of a phase 3, multicenter, double blind, placebo-controlled study [abstract 2557]. Arthritis Rheumatol 2012; 64(10 Suppl): S1080-S1081. Dostupné z DOI: <http://dx.doi.10.1002/art.37735>.
35. Ritchlin C, Rahman P, Kavanaugh A et al. [PSUMMIT 2 Study Group]. Efficacy and safety of the anti-IL-12/23 p40 monoclonal antibody, ustekinumab, in patients with active psoriatic arthritis despite conventional non-biological and biological anti-tumour necrosis factor therapy: 6-month and 1-year results of the phase 3, multicentre, double-blind, placebo-controlled, randomised PSUMMIT 2 trial. Ann Rheum Dis 2014; 73(6): 990–999. Dostupné z DOI: <http://dx.doi.org/10.1136/annrheumdis-2013–204655>.
36. Ramiro S, Smolen JS, Landewé R et al. Pharmacological treatment of psoriatic arthritis: a systematic literature review for the 2015 update of the EULAR recommendations for the management of psoriatic arthritis. Ann Rheum Dis 2016; 75(3): 490–498. Dostupné z DOI: <http://dx.doi.org/10.1136/annrheumdis-2015–208466>.
37. Kavanaugh A, Ritchlin C, Rahman P et al. Ustekinumab, an anti-IL-12/23 p40 monoclonal antibody, inhibits radiographic progression in patients with active psoriatic arthritis: results of an integrated analysis of radiographic data from the phase 3, multicentre, randomised, double-blind, placebo-controlled PSUMMIT-1 and PSUMMIT-2trials. Ann Rheum Dis 2014; 73(6): 1000–1006. Dostupné z DOI: <http://dx.doi.org/10.1136/annrheumdis-2013–204741>.
38. Araujo E, Englbrecht M, Hoepken S et al. Ustekinumab is superior to TNF inhibitor treatment in resolving enthesitis in PSA patients with active enthesitis – results from the enthesial clearance in psoriatic arthritis (ECLIPSA) study. An Revm Dis 2017; 76(Suppl 2): 142. Dostupné z DOI: <http://dx.doi. 10.1136/annrheumdis-2017-eular.5398 >.
39. Kavanaugh A, Menter A, Mendelsohn A et al. Effect of ustekinumab on physical function and health-related quality of life in patients with psoriatic arthritis: a randomized, placebo-controlled, phase II trial. Curr Med Res Opin 2010; 26(10): 2385–2392. Dostupné z DOI: <http://dx.doi.org/10.1185/03007995.2010.515804>.
40. Noordenbos T, Yeremenko N, Gofita I et al. Interleukin-17-positive mast cells contribute to synovial inflammation in spondylarthritis. Arthritis Rheumatol 2012; 64(1): 99–109. Dostupné z DOI: <http://dx.doi.org/10.1002/art.33396>.
41. Philip Mease P, McInnes IB. Secukinumab: A New Treatment Option for Psoriatic Arthritis. Rheumatol Ther 2016; 3(1): 5–29. Dostupné z DOI: <http://dx.doi.org/10.1007/s40744–016–0031–5>.
42. Langley RG, Elewski BE, Lebwohl M et al. Secukinumab in plaque psoriasis – results of two phase 3 trials. N Engl J Med 2014; 371(4): 326–338. Dostupné z DOI: <http://dx.doi.org/10.1056/NEJMoa1314258>.
43. Mease PJ, van der Heijde D, Ritchlin CT et al. A Randomized, double-blind, active - and placebo-controlled phase 3 study of efficacy and safety of ixekizumab, adalimumab, and placebo therapy in patients naïve to biologic disease modifying anti-rheumatic drugs with active psoriatic arthritis. 2015 ACR/ARHP Annual Meeting. ABSTRACT NUMBER: 977. Arthritis Rheumatol 2015; 67(Suppl 10). Dostupné z WWW: <http://acrabstracts.org/abstract/a-randomized-double-blind-active-and-placebo-controlled-phase-3-study-of-efficacy-and-safety-of-ixekizumab-adalimumab-and-placebo-therapy-in-patients-naive-to-biologic-disease-modifying-anti/>.
44. Schafer PH, Parton A, Gandhi AK et al. Apremilast, a cAMP phosphodiesterase-4 inhibitor, demonstrates anti-inflammatory activity in vitro and in a model of psoriasis. Br J Parmacol 2010; 159(4): 842–855. Dostupné z DOI: <http://dx.doi.org/10.1111/j.1476–5381.2009.00559.x>.
45. Schett G, Wollenhaupt J, Papp K et al. Oral apremilast in the treatment of active psoriatic arthritis: results of a multicenter, randomized, double-blind, placebo-controlled study. Arthritis Rheumatol 2012; 64(10): 3156–3167. Dostupné z DOI: <http://dx.doi.org/10.1002/art.34627>.
46. Kavanaugh A, Mease PJ, Gomez-Reino JJ et al. Apremilast, an oral phosphodiesterase 4 inhibitor, in patients with psoriatic arthritis: results of a phase 3, randomized, controlled trial [abstract L13]. Arthritis Rheumatol 2012; 64(Suppl 10): 4172–4173. Dostupné z DOI: <http://dx.doi.10.1002/art.37735>.
47. Celgene International Sarl. Apremilast achieves statistical significance for the primary endpoint of the first phase III study (PALACE-1) in patients with psoriatic arthritis. [Press release]. 2012. Dostupné z WWW: <http://ir.celgene.com/releasedetail.cfm?releaseid=795226>.
48. Fleischman R, Kremer J, Cush J et al. Placebo-controlled trial of tofacitinib monotherapy in rheumatoid arthritis. N Engl J Med 2012; 367(6): 495–507.
49. Ghoreshi K, Laurence A, O´Shia JJ. Janus kinases in immune cell signaling. Immunol Rev 2009; 228(1): 273–287. Dostupné z DOI: <http://dx.doi.org/10.1111/j.1600–065X.2008.00754.x>.
50. Papp KA, Menter A, Strober B et al. Efficacy and safety of tofacitinib, an oral Janus kinase inhibitor, in the treatment of psoriasis: a phase 2b randomized placebo-controlled dose ranging study. Br J Dermatol 2012; 167(3): 668–677. Dostupné z DOI: <http://dx.doi.org/10.1111/j.1365–2133.2012.11168.x>.
51. Štolfa J, Vencovský, J, Pavelka K. Doporučené léčebné postupy pro psoriatickou artritidu. Čes Revmatol 2016; 24(4): 142–152.
Štítky
Diabetologie Endokrinologie Interní lékařství
Článek vyšel v časopiseVnitřní lékařství
Nejčtenější tento týden
2018 Číslo 2- Není statin jako statin aneb praktický přehled rozdílů jednotlivých molekul
- Magnosolv a jeho využití v neurologii
- Moje zkušenosti s Magnosolvem podávaným pacientům jako profylaxe migrény a u pacientů s diagnostikovanou spazmofilní tetanií i při normomagnezémii - MUDr. Dana Pecharová, neurolog
- S prof. Vladimírem Paličkou o racionální suplementaci kalcia a vitaminu D v každodenní praxi
-
Všechny články tohoto čísla
- Axiální spondylartritida
- Využitie MRI vyšetrenia pri diagnostike axiálnej spondylartritídy
- Biologická léčba psoriatické artritidy
- Život ohrožující projevy systémového lupusu a antifosfolipidového syndromu ve vnitřním lékařství
- Systémová sklerodermie v roce 2017
- Idiopatické zánětlivé myopatie
- Nové trendy v monitorování a léčbě ANCA asociovaných vaskulitid
- Difuzní alveolární hemoragie – akutní, život ohrožující stav v revmatologii
- Polymyalgia rheumatica
- Léčba k cíli u dnavé artritidy
- Nutraceutika v terapii gonartrózy: pohled ortopeda
- Osteoporóza a kvalita kostní hmoty
- Léčba chronické bolesti u zánětlivých revmatických onemocnění
- Revmatologie a vnitřní lékařství
- Revmatoidní artritida
- Vnitřní lékařství
- Archiv čísel
- Aktuální číslo
- Pouze online
- Informace o časopisu
Nejčtenější v tomto čísle- Axiální spondylartritida
- Využitie MRI vyšetrenia pri diagnostike axiálnej spondylartritídy
- Idiopatické zánětlivé myopatie
- Difuzní alveolární hemoragie – akutní, život ohrožující stav v revmatologii
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



