-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Tirzepatid – přichází nové antidiabetikum a antiobezitikum se širokými perspektivami
Autoři: Štěpán Svačina
Působiště autorů: 3. interní klinika 1. LF UK a VFN v Praze
Vyšlo v časopise: Svět praktické medicíny, 6, 2024, č. 2, s. 77-81
Kategorie: Medicína v ČR: Lékový profil
Souhrn
Injekční inkretinová analoga jsou v diabetologii používána již přes 15 let a v obezitologii 5 let. Již několik roků jsou vyvíjeny peptidové molekuly, které mají vlastnosti více střevních peptidů najednou. Prvním v USA a nyní i v Evropě dostupným lékem je tirzepatid – analog dvou hormonů (tzv. twincretin) glukagon like peptidu-1 (GLP-1) a glukózo-dependentního inzulinotropního polypeptidu (GIP). Řada studií programu SURPASS i SURMOUNT ukázala vynikající pozitivní efekt při léčbě diabetu 2. typu i obezity. To ukazuje obrovskou perspektivu molekul s vlastnostmi více střevních peptidů v medicíně. Zkušenosti s podáváním léku již máme a od léta bude pravděpodobně dostupný na úhradu pacientem v obezitologii i diabetologii. O úhradě zejména pro diabetiky 2. typu se jedná.
Existence střevních peptidů (tzv. inkretinů) je známa již 50 let [podrobně v 1]. Prvním u nás dostupným lékem byl exenatid – analog GLP-1 podávaný v injekci 2× denně od roku 2008. Postupně byla vyvíjena inkretinová analoga aplikovaná jednou denně a jedenkrát týdně. Dnes mají lékaři v ČR z této skupiny na výběr injekční antidiabetika exenatid, liraglutid, lixisenatid, dulaglutid a semaglutid. Komplexně ovlivňují nejen diabetes 2. typu, ale výrazně zlepšují i kardiovaskulární prognózu pacientů.
Od roku 2018 je první z těchto léků liraglutid využíván i v obezitologii a schváleno je i využití semaglutidu (momentálně v ČR nedostupný) pro léčbu obezity [podrobně v 2] . Jedna syntetická molekula peptidu může mít vlastnosti dvou i více inkretinů. Ve vývoji je několik variant léků s vlastností dvou různých inkretinů, a dokonce i léky s vlastností tří různých inkretinových molekul. První z léků, který vstoupil do diabetologické a obezitologické praxe, je tirzepatid.3
Indikace tirzepatidu
Tirzepatid byl schválen jako antidiabetikum pod názvem Mounjaro v USA v květnu 2022 a v EU v září 2022. V současné době je tirzepatid schválený spolu s dietou a fyzickou aktivitou k léčbě dospělých s diabetem 2. typu, který není uspokojivě kontrolován. Může být používán samostatně u pacientů, kteří nemohou užívat metformin, nebo jako „přídavek“ k jiným antidiabetikům.
Tirzepatid je také schválen v Evropě i v USA jako antiobezitikum u nediabetiků – používá se spolu s dietou a fyzickou aktivitou, aby pomohl redukovat hmotnost a udržet ji pod kontrolou. Používá se u osob, které trpí obezitou (BMI 30 kg/m2 nebo více), nebo u osob s nadváhou (BMI mezi 27 a 30 kg/ m2), pokud mají zdravotní problémy související s hmotností –tj. za přítomnosti alespoň jednoho komorbidního stavu souvisejícího s hmotností (např. hypertenze, dyslipidemie, obstrukční spánková apnoe, kardiovaskulární onemocnění, prediabetes nebo diabetes mellitus 2. typu).
Mechanismus účinku
Mechanismus účinku GLP-1 analog je všeobecně znám [podrobně v 1, 2] a zahrnuje centrální efekty, efekt na vyprazdňování žaludku i efekt metabolický ovlivňující zejména sekreci inzulinu a glukagonu. Na obrázku 14 je pro srovnání uveden fyziologický efekt GLP-1 a GIP. Na první pohled je vidět, že přidání vlastnosti dalšího peptidu rozšiřuje počet efektů v organismu a činí z tirzepatidu nadějný lék nejen pro léčbu diabetu 2. typu, ale i pro léčbu obezity. Proto byly sestaveny dva programy studií SURPASS a SURMOUNT [přehledně výsledky v 5], a jak je zmíněno v závěru, probíhají studie zaměřené i na další onemocnění [podrobně v 5].
Tirzepatid jako antidiabetikum
Studie SURPASS-1
Antidiabetický efekt byl samozřejmě nejprve prokázán na zvířatech a ve studiích fáze II. Velká studie SURPASS-1 srovnávala tirzepatid s placebem,6 a tedy exaktně prokázala antidiabetický efekt u pacientů neovlivněných jinými léky. Studie fáze III byla provedena u diabetiků nedostatečně kompenzovaných režimovými opatřeními v letech 2019 – 20 u 478 pacientů rozdělených do čtyř skupin: 1× týdně s. c. placebo nebo tirzepatid (5, 10 nebo 15 mg). Šlo o diabetiky, které běžně vidíme i v našich ordinacích – průměrný HbA1c 7,9 % [63 mmol/mol], věk 54,1 let, trvání diabetu 4,7 let a BMI 31,9 kg/m2. Průměrný pokles HbA1c činil 1,87 % (20 mmol/mol), 1,89 % (21 mmol/ mol) a 2,07 % (23 mmol/ mol) podle dávky tirzepatidu. U placeba došlo k vzestupu +0,04 % (+0,4 mmol/mol). Pokles hmotnosti činil 7,0 až 9,5 kg v průměru podle dávky tirzepatidu. Nebyly zaznamenány hypoglykemie a nejčastějším vedlejším účinkem byla nauzea ve frekvenci podobné jako při užití jiných inkretinových analog.
Obr. 1. Účinky glukagon like peptidu-1 (GLP-1) a gastrického inhibičního peptidu (GIP). 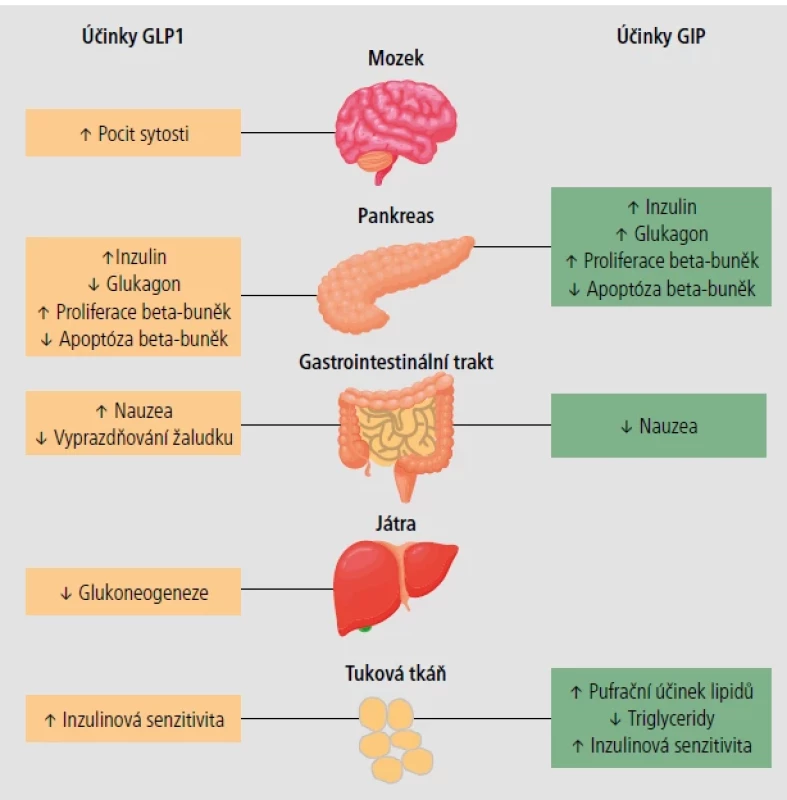
[Upraveno podle: Andraos J, Muhar H, Smith SR. Beyond glycemia: Comparing tirzepatide to GLP-1 analogues. Rev Endocr Metab Disord 2023;24(6):1089–1101.] Studie SURPASS-2
Výsledky studie SURPASS-2,7 která srovnávala tirzepatid se semaglutidem, přinášíme i graficky na obrázcích 2 a 3.8 Semaglutid je dnes velmi běžně používaný analog GLP-1 podávaný 1× týdně, a proto přímé srovnání vývoje glykovaného hemoglobinu HbA1c a hmotnosti v této studii je tak vý znamné. Ve 40týdenní studii bylo sledováno 1879 pacientů rozdělených náhodně znovu 1 : 1 : 1 : 1 k podání tirzepatidu 5 mg, 10 mg nebo 15 mg a semaglutidu 1 mg. To je u nás běžně užívaná dávka. Výchozí hladina glykovaného hemoglobinu činila v průměru 8,28 %, průměrný věk pacientů byl 56,6 let a hmotnost v průměru 93,7 kg. Uspořádání studie bylo tedy podobné jako u studie SURPASS-1. Primárním cílem bylo sledování změn hladin glykovaného hemoglobinu, které zaznamenaly pokles (−2,01 %, −2,24 % a −2,30 %) podle dávky tirzepatidu a −1,86 % po semaglutidu. Rozdíl hmotnosti ve srovnání s poklesem po semaglutidu byl v průměru −1,9 kg, −3,6 kg a −5,5 kg po 5, 10, resp. 15 mg tirzepatidu. Tirzepatid byl v testování noninferiorní a superiorní k podání semaglutidu. Vedlejší účinky byly podobné jako ve studii SURPASS-1.
Obr. 2. Změny hladin glykovaného hemoglobinu ve studii SURPASS-2. 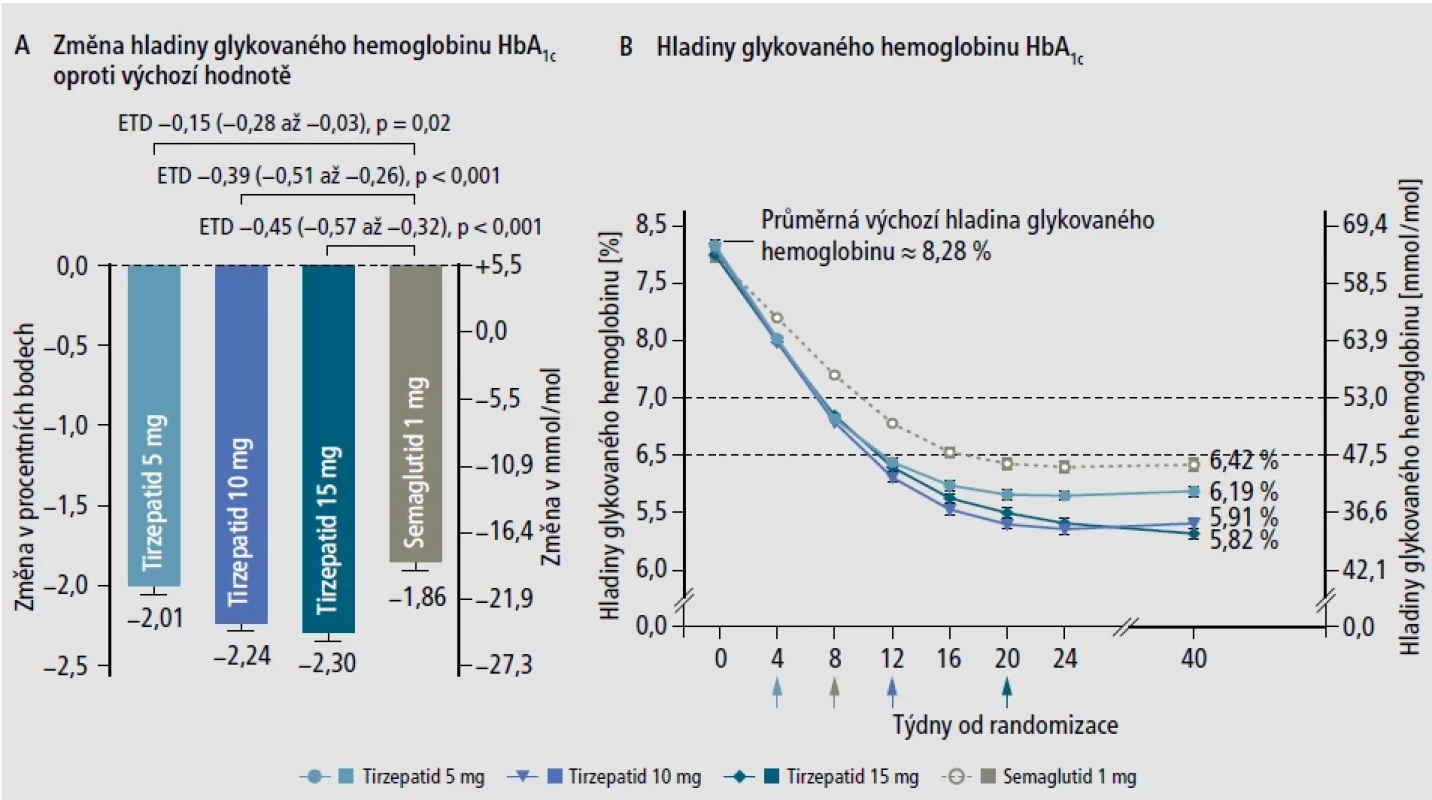
[Upraveno podle: McCormick LM, Hoole SP, White PA, et al. Pre-treatment with glucagon-like peptide-1 protects against ischemic left ventricular dysfunction and stunning without a detected difference in myocardial substrate utilization. JACC Cardiovascular Interventions 2015;8:292–301.] Studie SURPASS-3
Ve studii SURPASS-3 byl tirzepatid srovnán s titrovanou dávkou inzulinu degludek u pacientů nedostatečně kompenzovaných metforminem nebo metforminem a gliflozinem.9 Tirzepatid byl navyšován podle efektu vždy po 4 týdnech o dávku 2,5 mg. Inzulin degludek byl iniciálně podán v dávce 10 jednotek denně a byl titrován až do poklesu glykemie pod 5,0 mmol/l po dobu 52 týdnů. Primárním cílem bylo prokázání non-inferiority pro tirzepatid 10 mg nebo 15 mg nebo obou versus inzulin degludek ve změně HbA1c v 52. týdnu. Redukce HbA1c činila 1,93 % v případě tirzepatidu 5 mg, 2,20 % po tirzepatidu 10 mg, 2,37 % po tirzepatidu 15 mg a 1,34 % po použití inzulinu degludek. Průměrná změna hmotnosti po tirzepatidu činila −7,5 až −12,9 kg podle dávky tirzepatidu (tedy došlo k úbytku hmotnosti) a naopak po inzulinu činila +2,3 kg (tedy došlo k nárůstu hmotnosti). Závěrem studie bylo konstatováno, že tirzepatid u diabetes mellitus 2. typu v dávce 5, 10 a 15 mg byl superiorní vůči degludeku v redukci HbA1c a hmotnosti i výskytu hypoglykemií.
Studie SURPASS-4
Ve studii SURPASS-4 byl tirzepatid srovnán se speciálním zřetelem na kardiovaskulární bezpečnost.10 Byl srovnáván s inzulinem glarginem u vysoce kardiovaskulárně rizikové skupiny diabetiků 2. typu. Zařazeni byli diabetici léčení metforminem, sulfonylureou nebo inhibitory SGLT2 s bazálním HbA1c 7,5–10,5 % (58–91 mmol/mol), BMI nad 25 kg/m2 a přítomným kardiovaskulárním onemocněním nebo v definovaném vysokém kardiovaskulárním riziku. Podáván byl tirzepatid (10 mg nebo 15 mg) a inzulin glargin byl titrován ke glykemii pod 100 mg/dl. Primárním cílem byl průkaz non-inferiority v HbA1c a sledován byl také výskyt kardiovaskulárních příhod. Do 52. týdne došlo k poklesu HbA1c – po tirzepatidu změna činila −2,43 %, resp. −2,58 % versus změna −1,44 % po glarginu. Byla tedy prokázána non-inferiorita vůči glarginu. Výskyt příhod MACE-4 (KV úmrtí, infarkt myokardu, iktus, hospitalizace pro anginu pectoris) byl zjištěn u 35 pacientů po tirzepatidu (riziko 0,74[0,51–1,08]), kdy po glarginu došlo k 60 příhodám. Tirzepatid tudíž nesignifikantně snížil výskyt MACE, a kardiovaskulárně je tedy pravděpodobně minimálně bezpečný.
Studie SURPASS-5
Ve studii SURPASS-5 byl tirzepatid přidáván k inzulinu glargin u pacientů nedostatečně kompenzovaných na glarginu a metforminu nebo glarginu samotném.11 Ve studii v poměru 1 : 1 : 1 : 1 byl přidán tirzepatid v dávce 5, 10 nebo 15 mg, v poslední větvi studie bylo místo tirzepatidu přidáváno placebo. Změna HbA1c ve 40. týdnu činila −2,11 % po tirzepatidu 5 mg, −2,40 % po tirzepatidu 10 mg a −2,34 % po tirzepatidu 15 mg vs. −0,86 % po placebu, a znamenala tedy pokles glykovaného hemoglobinu. U hmotnosti byly zaznamenány následující úbytky: −5,4 kg po tirzepatidu 5 mg, −7,5 kg po tirzepatidu 10 mg, −8,8 kg po tirzepatidu 15 mg a naopak nárůst +1,6 kg po placebu. Studie tedy ukazuje, že dnes běžně užívané kombinace s analogy GLP - 1, která jsou přidávána k nedostatečně působícímu dlouho dobému inzulinovému analogu, mohou být v budoucnu podobně efektivní i v kombinaci tirzepatid–inzulin.
Obr. 3. Změny tělesné hmotnosti ve studii SURPASS-2. 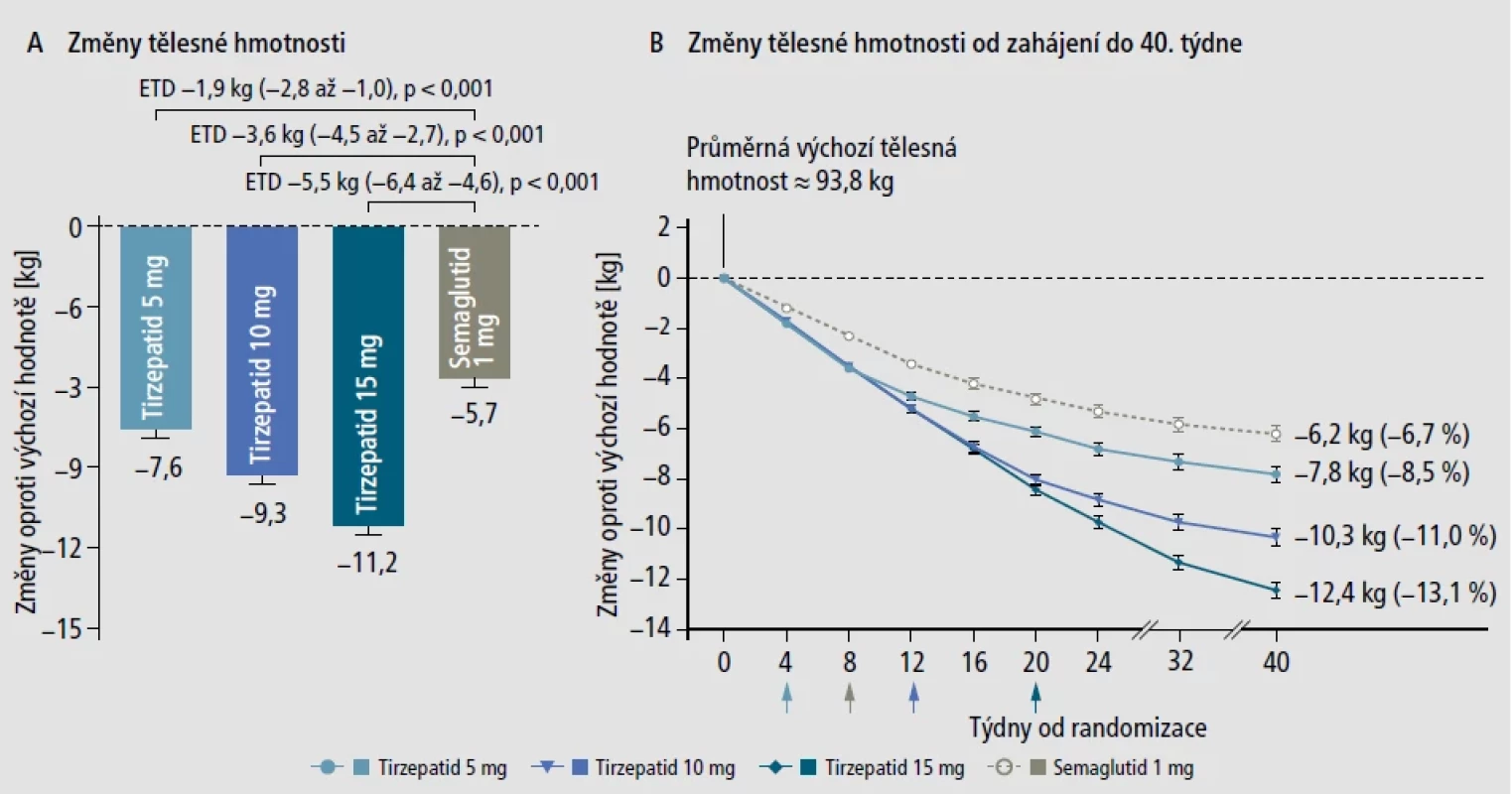
[Upraveno podle: McCormick LM, Hoole SP, White PA, et al. Pre-treatment with glucagon-like peptide-1 protects against ischemic left ventricular dysfunction and stunning without a detected difference in myocardial substrate utilization. JACC Cardiovascular Interventions 2015;8:292–301.] Obr. 4. Procentuální změna tělesné hmotnosti za 88 týdnů. Zobrazeny jsou pozorované průměrné hodnoty z úplného analytického souboru. Chybové úsečky představují 95% CI pro průměr. Přerušovaná svislá čára v týdnu 36 představuje bod randomizace. Analýza kovariance pomocí úplného analytického souboru s hybridními imputačními středními hodnotami nejmenších čtverců v týdnu 88 je také zobrazena vpravo. 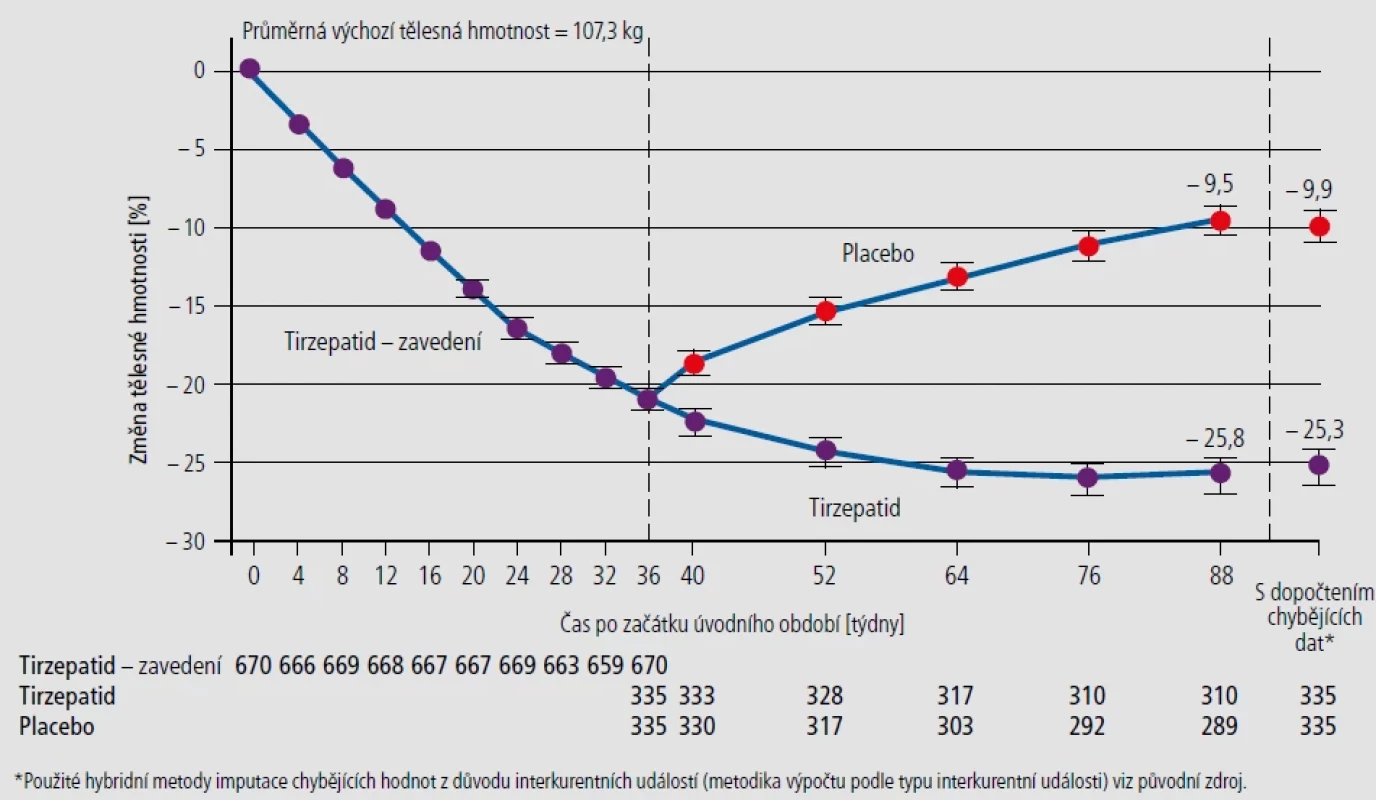
[Upraveno podle: Aronne LJ, Sattar N, Horn DB, et al. Continued treatment with tirzepatide for maintenance of weight reduction in adults with obesity: The SURMOUNT-4 randomized clinical trial. JAMA 2024;331(1):38–48.] Tirzepatid jako antiobezitikum
Prakticky do všech médií celého světa pronikly neuvěřitelné výsledky studie SURMOUNT-1. Jednalo se o dvojitě zaslepenou studii fáze III,12 kdy 2539 dospělých s BMI vyšším než 30 kg/m2 nebo s BMI 27–30 kg/m2 s jednou komplikací obezity bylo rozděleno do skupin k podání tirzepatidu (5 mg, 10 mg nebo 15 mg) nebo placeba po dobu 72 týdnů s možností eskalace dávky v posledních 20 týdnech. Počáteční průměrná hmotnost činila 104,8 kg při průměrném BMI 38,0 kg/ m2. Po podání tirzepatidu došlo ke změně hmotnosti o −16,0 %, −21,4 % a −22,5 % v závislosti na dávce tirzepatidu a −2,4 % po placebu. Po nejvyšší dávce tirzepatidu tedy pacienti redukovali o neuvěřitelných 24 kilogramů, a to překvapilo celý svět.
Často kladenou otázkou je, zda antiobezitika budou užívána dlouhodobě jako hypolipidemika, antihypertenziva či anti - diabetika. Studie SURMOUNT-4 (Obr. 4)13 a citace ukazuje, co se stane u pacientů, kteří do 36. týdne studie zhubli v průměru 20 % hmotnosti. Hmotnost bezprostředně výrazně stoupá po vysazení a u pacientů aplikujících původní dávku dále hmotnost klesá, resp. po necelých dvou letech při stejné dávce začíná stagnovat. Perspektiva použití antiobezitik je tedy velmi dlouhá a snad i trvalá.
Závěr – perspektivy užití tirzepatidu
Tirzepatid 1× týdně s. c. je v Evropě již schválen jako prakticky nejúčinnější antidiabetikum, a to i ve srovnání se semaglutidem i inzulinem. Velmi zajímavý je přehled studií, které s tirzepatidem probíhají.5 Týkají se nealkoholické steatohepatitidy, dále srovnání s dulaglutidem ve výskytu kardiovaskulárních příhod nebo jsou to studie u dětí a adolescentů s diabetem 2. typu.
Studie SURPASS-6 srovnává pacienty nedostatečně kompenzované glarginem ve dvou větvích s přidáním tirzepatidu nebo intenzifikované terapie inzulinem lispro 3× denně. Může prokázat výhody přidání tirzepatidu k inzulinu před intenzifikací inzulinové léčby. Studie SUR MOUNT-2 je zaměřena na obézní diabetiky 2. typu. Studie SURMOUNT-3 je zaměřena na přidání tirzepatidu po intenzivním redukčním programu s již značnou redukcí hmotnosti. To připomíná studie s liraglutidem a kombinací naltrexon–bupropion u pacientů, kteří redukovali režimově a úbytek se zastavil.2 Studie SURMOUNT-CN je prováděna v Číně a je zaměřena na obézní bez diabetu s komorbiditami a podobná studie je prováděná v Japonsku. Studie SUMMIT je zaměřena na pacienty se srdečním selháním se zachovanou ejekční frakcí. Studie SURPASS-EARLY je zaměřená na léčbu pacientů s čerstvě zjištěným diabetem 2. typu.
Tirzepatid je aktuálně nejperspektivnější lék v diabetologii i obezitologii a je možné, že zásadně ovlivní i léčbu dalších komorbidit obezity a diabetu. Již přehledy o současných studiích ukázaly zajímavý efekt na lipidy a krevní tlak [5, graficky převzato v 14].
Pro tirzepatid, který je prvním zástupcem v nové skupině antidiabetik, se začíná v angličtině používat název twincretin nebo název lék s duálním inkretinovým mechanismem a bude zajímavé, jak se bude tato skupina naplňovat v příštích letech dalšími léky.
Zdroje
1. Svačina Š. Antidiabetika – historie, současnost a budoucnost. 1. vyd. Praha: Axonite, 2016.
2. Svačina Š. Antiobezitika – vývoj, současnost a perspektivy. 1. vyd. Praha: Grada Publishing, 2022.
3. Svačina Š. Tirzepatid jako posel budoucnosti – nové antidiabetikum se širokými perspektivami. Aktuální medicína 2023;7(1):43–48.
4. Andraos J, Muhar H, Smith SR. Beyond glycemia: Comparing tirzepatide to GLP-1 analogues. Rev Endocr Metab Disord 2023;24(6): 1089–1101.
5. Forzano I, et al. Tirzepatide: a systematic update. Int J Mol Sci 2022; 23(23):14631.
6. Rosenstock J, et al. Efficacy and safety of a novel dual GIP and GLP-1 receptor agonist tirzepatide in patients with type 2 diabetes (SURPASS-1): a double-blind, randomised, phase 3 trial. Lancet 2021;398(10295): 143–155.
7. Frías JP, et al. Tirzepatide versus semaglutide once weekly in patients with type 2 diabetes (SURPASS-2 study). N Engl J Med 2021;385(6): 503–515.
8. McCormick LM, Hoole SP, White PA, et al. Pre-treatment with glucagon-like peptide-1 protects against ischemic left ventricular dysfunction and
stunning without a detected difference in myocardial substrate utilization. JACC Cardiovascular Interventions 2015;8 : 292–301.9. Ludvik B, et al. Once-weekly tirzepatide versus once-daily insulin degludec as add-on to metformin with or without SGLT2 inhibitors in patients with type 2 diabetes (SURPASS-3): a randomised, open-label, parallel-group, phase 3 trial. Lancet 2021;398(10300):583–598.
10. Del Prato S, et al. Tirzepatide versus insulin glargine in type 2 diabetes and increased cardiovascular risk (SURPASS-4): a randomised, open-label, parallel-group, multicentre, phase 3 trial. JAMA 2022;327(6):534–545.
11. Dahl D, et al. Effect of subcutaneous tirzepatide vs placebo added to titrated insulin glargine on glycemic control in patients with type 2 diabetes: the SURPASS-5 randomized clinical trial. JAMA 2022;327(6): 534–545.
12. Jastreboff AM, et al. Tirzepatide once weekly for the treatment of obesity. SURMOUNT-1 Study. N Engl J Med 2022;387(3):205–216.
13. Aronne LJ, Sattar N, Horn DB, et al. Continued treatment with tirzepatide for maintenance of weight reduction in adults with obesity: The SURMOUNT-4 randomized clinical trial. JAMA 2024;331(1):38–48.
14. Svačina Š. Farmakologická léčba obezity a snížení TK. In: Widimský J. ed. Arteriální hypertenze – současné klinické trendy. XXI. symposium – sborník přednášek. 1. vyd. Praha: Triton, 2023.
Štítky
Praktické lékařství pro děti a dorost Praktické lékařství pro dospělé
Článek vyšel v časopiseSvět praktické medicíny
Nejčtenější tento týden
- Na inkontinenční pomůcky nově dosáhne více pacientů
- EGb 761: extrakt z Ginkgo biloby s definovaným složením
- Naděje budí časná diagnostika Parkinsonovy choroby založená na pachu kůže
- Pacient se bude cítit komfortně pouze při správně zvolené absorpční pomůcce
- Úloha praktického lékaře v péči o inkontinentní pacienty
-
Všechny články tohoto čísla
- Úvodní slovo
- Pokud začnete na začátku předvýjezdového poradenství probírat cokoliv jiného než vakcíny, obvykle vás klient zarazí a řekne, ale já jsem tady kvůli očkování!
- Nové registrace EMA
- Léčba a prevence HIV infekce: doporučení z panelu Mezinárodní antivirové společnosti – USA
- Komentář k článku Léčba a prevence HIV infekce: doporučení z panelu Mezinárodní antivirové společnosti – USA
- Pruritus: diagnostika a léčba
- Komentář k článku Pruritus: diagnostika a léčba
- Terapie psoriázy u seniorů
- Bimekizumab – účinná moderní léčba psoriázy
- Alopecie – jak poznat a léčit jednotlivé typy alopetických onemocnění?
- Hidradenitis suppurativa: klinický obraz, diagnostika a léčba
- Maligní melanom, i přes moderní léčbu stále obávaná diagnóza
- Rizikové faktory a profylaxe recidivujícího erysipelu a celulitidy
- Efekt antikoagulační léčby u obtížně se hojících bércových ulcerací
- Antacida ve fixní kombinaci s Opuntiae extractum u gastroezofageálního refluxu
- V tom, co můžeme pacientům nabídnout, jdeme stále dopředu
- Karbapenem šetřící strategie začíná již v laboratoři
- Přidání extraktu EGb 761 ke kognitivům je účinnější než monoterapie
- Tirzepatid – přichází nové antidiabetikum a antiobezitikum se širokými perspektivami
- V péči o onkologické pacienty je stále co zlepšovat
- Znalostní test: 2 kredity ČLK
- Svět praktické medicíny
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Tirzepatid – přichází nové antidiabetikum a antiobezitikum se širokými perspektivami
- Rizikové faktory a profylaxe recidivujícího erysipelu a celulitidy
- Maligní melanom, i přes moderní léčbu stále obávaná diagnóza
- Alopecie – jak poznat a léčit jednotlivé typy alopetických onemocnění?
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



