-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
TDM digoxinu v klinické praxi
TDM of digoxin in clinical practice
Introduction:
Digoxin is a positive inotropic drug frequently prescribed in the treatment of chronic congestive cardiac failure. Recent evidence suggests that a lower therapeutic range of 0.5 – 0.9 ng/ mL is associated with reduced mortality. With complex pharmacokinetic profile and narrow therapeutic index, its use in managing patients with heart failure can present a challenge to clinicians.Aim:
To show the advantages of therapeutic drug monitoring for dosing of digoxin.Method:
Bayesian analysis was used to predict the long‑term serum concentration – time profiles of digoxin, using the MW ‑ Pharm 3.30 software. The serum levels of digoxin were determined by MEIA.Results:
Three case reports are presented showing a prediction of steady ‑ state digoxin level three days after the start of administration, drug‑drug interaction between digoxin and spironolactone/ carvedilol and an example of long‑term patient non‑compliance.Conclusion:
Therapeutic drug monitoring is very useful for prediction of serum levels of digoxin alone and in combination with different interacting drugs. It helps to understand compliance ‑ influencing factors and to improve interventional strategies to increase digoxin compliance.Keywords:
chronic heart failure – digoxin – therapeutic drug monitoring – compliance – drug‑drug interactions
Autoři: M. Grundmann 1; I. Kacířová 1,2
Působiště autorů: Ústav klinické farmakologie, LF OU, Ostrava 1; Oddělení klinické farmakologie, Ústav laboratorní dia gnostiky, FN Ostrava 2
Vyšlo v časopise: Kardiol Rev Int Med 2015, 17(1): 65-69
Kategorie: Interní medicína
Souhrn
Úvod:
Digoxin je pozitivně inotropní léčivo, které je stále často používáno k léčbě chronického srdečního selhání. Nedávné analýzy ukázaly, že digoxin v nízkém terapeutickém rozmezí 0,5 – 0,9 ng/ ml snižuje mortalitu pacientů. Úzké terapeutické rozmezí digoxinu a jeho farmakokinetický profil vyžadují od klinika nový přístup v terapii srdečního selhání.Cíl:
Ukázat výhody terapeutického monitorování hladin léčiv pro dávkování digoxinu.Metoda:
Pro farmakokinetickou analýzu bylo použito Bayesianské analýzy za pomocí software MW ‑ Pharm 3.30. Koncentrace digoxinu byla stanovena imunochemicky metodou MEIA.Výsledky:
Jsou prezentovány tři kazuistiky, které ukazují: 1. tři dny po nasazení predikci hladiny digoxinu v ustáleném stavu, 2. lékovou interakci digoxinu v kombinaci se spironolaktonem a karvedilolem a 3. příklad dlouhodobé non‑compliance u pacienta.Závěr:
Terapeutické monitorování hladin léčiv je velice užitečnou metodou k predikci koncentrace digoxinu jak samotně užívaného, tak v kombinaci s různými interagujícími léčivy. Pomáhá lépe porozumět faktorům ovlivňujícím compliance a umožňuje zlepšit compliance pacienta.Klíčová slova:
chronické srdeční selhání – digoxin – terapeutické monitorování hladin léčiv – compliance – lékové interakceÚvod
V doporučeních Evropské kardiologické společnosti i České kardiologické společnosti pro léčbu chronického srdečního selhání je v algoritmu uveden digoxin na 5. místě za ACE inhibitory, antagonisty AT1 receptorů, betablokátory, antagonisty aldosteronových receptorů a diuretiky [1,2]. Digoxin je nejstarší a nejlacinější lék užívaný v léčbě srdečního selhání. V posledních letech bylo provedeno 13 randomizovaných studií (7 896 pacientů) s end pointem mortality, hospitalizace a klinického stavu [3]. Metaanalýza z osmi studií, která zahrnovala mortalitní data, prokázala, že digoxin mortalitu neovlivňuje. Tyto výsledky byly získány převážně z DIG studie, kde však byl prokázán signifikantně významný pozitivní efekt týkající se kvality života. Čtyři studie zahrnovaly data týkající se hospitalizace pro zhoršení srdečního selhání, kde digoxin signifikantně snižoval relativní riziko o 23,4 %. Dvanáct studií prezentovalo data kardiálních symptomů a výsledky u pacientů léčených digoxinem byly lepší ve srovnání s placebem [4].
Význam koncentrace digoxinu v séru
V roce 2003 byly zveřejněny výsledky post‑hoc analýzy studie DIG v závislosti na dosažených hladinách digoxinu. Rathore et al [5] rozdělili pacienty podle dosažených koncentrací digoxinu v séru do tří skupin: 0,5 – 0,8 ng/ ml, 0,9 – 1,1 ng/ ml a ≥ 1,2 ng/ ml. Nejnižší koncentrace snižovaly mortalitu, zatímco výsledky prostřední koncentrace se nelišily od placeba a sérové koncentrace ≥ 1,2 ng/ ml signifikantně zvyšovaly celkovou i kardiovaskulární mortalitu o 11,8 %. Další reanalýzu provedli Ahmed et al [6], kteří zjistili, že digoxin v rozmezí 0,5 – 0,9 ng/ ml významně snižoval jednoroční mortalitu a hospitalizaci pacientů s chronickým srdečním selháním, kteří byli léčeni ACE inhibitory a diuretiky. Autoři popsali, že ve studii DIG byl medián dávky digoxinu 0,25 mg s rozptylem 0,125 – 0,5 mg/ den. 11 % pacientů dostávalo 0,375 mg digoxinu za den a 1 % pacientů 0,5 mg/ den, z čehož vyplynulo množství hospitalizací z důvodu digoxinové toxicity.
Účinky digoxinu
Digoxin inhibuje Na+/ K+ ATPázu v buněčné membráně, čímž dochází ke zvýšení nitrobuněčného obsahu sodíku a výměnným mechanizmem druhotně k vzestupu nitrobuněčného obsahu vápníku a jeho vazbě na kontraktilní proteiny myofibril. Výsledkem jsou změny hemodynamiky u srdečního selhání (zvýšený srdeční výdej, zvýšení ejekční frakce levé komory), neurohumorální účinky (vagomimetický účinek, snížení sérové koncentrace noradrenalinu, snížená aktivace systému renin‑angiotenzin, přímý sympatolytický efekt, zlepšená senzitivita baroreceptorů, zvýšené vylučování ANP a BNP) a elektrofyziologické účinky (negativně chronotropní a dromotropní účinek). Inhibiční účinek digoxinu na neurohormony při srdečním selhání se projevuje při nízkých koncentracích digoxinu [7,8].
Dávkování digoxinu
Z předchozích studií vyplývá, že cílem terapie chronického srdečního selhání digoxinem jsou nízké koncentrace v séru mezi 0,5 a 0,9 ng/ ml. Tyto koncentrace závisí na dávce, věku pacienta, pohlaví, hmotnosti, funkci ledvin a současné medikaci. Protože se u digoxinu jedná o dlouhodobý efekt a výsledek, nemůže se dávkování řídit pouze klinickým stavem, ale také využitím terapeutického monitorování hladin léčiv (TDM), které se skládá z: 1. analýzy koncentrace léčiva v séru, 2. interpretace dosažené koncentrace s využitím farmakokinetické analýzy a 3. zpětné vazby s klinikem [9]. Bohužel TDM jako jedna ze základních metod oboru klinické farmakologie není v dostatečné míře nabízena ani požadována [10].
Cíl práce
Cílem práce je ukázat na příkladu kazuistik výhodnost TDM při dávkování digoxinu při úpravě dávek při současné kombinaci s jinými léčivy i analýze non‑compliance i chyb lékaře.
Metoda
Digoxin byl stanovován imunoanalytickou metodou MEIA na přístroji AxSym Abbott, farmakokinecká analýza prováděna pomocí software MW ‑ Pharm 3.30 MediWare. Digoxin byl odebírán před podáním následující dávky, tedy jako tzv. trough = údolní hladina, a současně s vyplněnou žádankou zaslán na Oddělení klinické farmakologie (OKF) FN Ostrava (http:/ / www.fno.cz/ oddeleni ‑ klinicke ‑ farmakologie/ ke ‑ stazeni). Pro správné provedení farmakokinetické analýzy je potřeba vyplnit některé základní údaje, jako jsou hmotnost (alespoň přibližná), sérový kreatinin, kalium, dávková anamnéza (dávka digoxinu, cesta podání, délka podávání digoxinu – zda se jedná o odběr krátce po nasazení či v ustáleném stavu), ostatní léková anamnéza a odběrový čas (před podáním nebo v případě podezření z intoxikace kdykoli po podání dávky). Doporučení optimální dávky jsou mimo FN Ostrava posílána následující pracovní den (v rámci FNO nemocničním laboratorním systémem již v den odběru), při analýze hladin digoxinu nad horní hranicí terapeutického rozmezí jsou navíc ihned po interpretaci telefonována nemocničním i mimonemocničním žadatelům. Na našem pracovišti používáme při provádění TDM digoxinu terapeutické rozmezí 0,5 – 1,2 ng/ ml.
Výsledky
Kazuistika č. 1: Predikce dávky digoxinu pro dosažení optimální koncentrace tři dny po nasazení (obr. 1a, 1b).
Obr. 1. a. Dvaadevadesátiletá žena byla přijata na kardiovaskulární oddělení s diagnózami ICHS chron., stp. CABG, chronické srdeční selhání, diabetes mellitus II. typu a hyperurikemie pro zhoršení stavu. 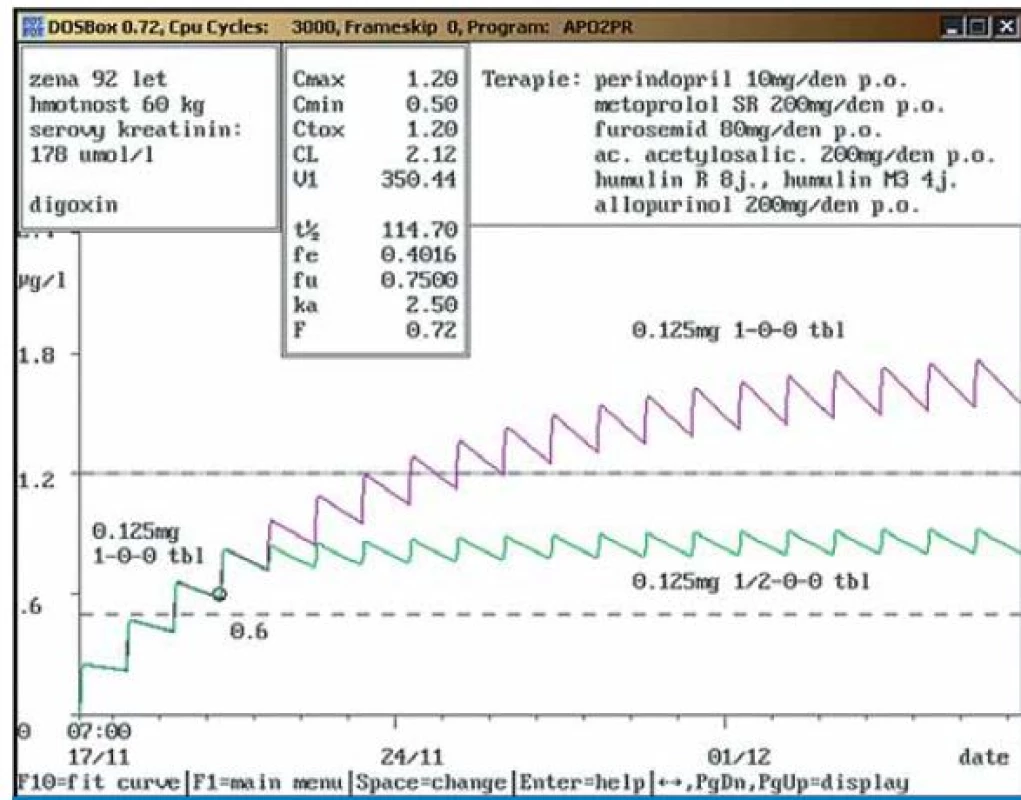
K dosavadní terapii ACEI, betablokátor a diuretikum byl přidán digoxin v dávce 0,125 mg/den. 3. den po nasazení byla změřena koncentrace digoxinu v séru – 0,6 ng/ml. S použitím software MW-Pharm 3.30 byla provedena farmakokinetická analýza a predikce ukázala, že při užívání nastavené dávky by se při steady-state dosáhlo koncentrace kolem 1,6 ng/ml, tedy koncentrace, u které bylo popsáno zvýšené riziko mortality. Proto na základě PK modelace bylo doporučeno podávání digoxinu v dávce 0,125 mg ½ tbl denně a na obrázku byla znázorněna predikce hladiny mezi 0,8–0,9 ng/ml. Kontrola byla doporučena za týden vzhledem k hospitalizaci. Obr. 1b. Kontrolní vyšetření koncentrace digoxinu po jednotýdenní změně dávky digoxinu na 0,125 mg ½-0-0 tbl při nezměněné další terapii a stejných ledvinových funkcích ukázalo správnou predikci. 
Změřená koncentrace digoxinu byla 0,8 ng/ml a pacientka byla propuštěna do péče praktického lékaře s doporučením další kontroly koncentrace digoxinu dle klinického stavu, a to zejména v případě změny renálních funkcí. Kazuistika č. 2: Intoxikace digoxinem v důsledku lékové interakce se současným podáváním karvedilolu a spironolaktonu (obr. 2a, 2b).
Obr. 2. a. Jedenasedmdesátiletý muž byl přijat na kardiovaskulární oddělení s diagnózami ICHS chron., stp. CABG, chronické srdeční selhání s fibrilací síní, hyperlipoproteinemie a hyperurikemie. 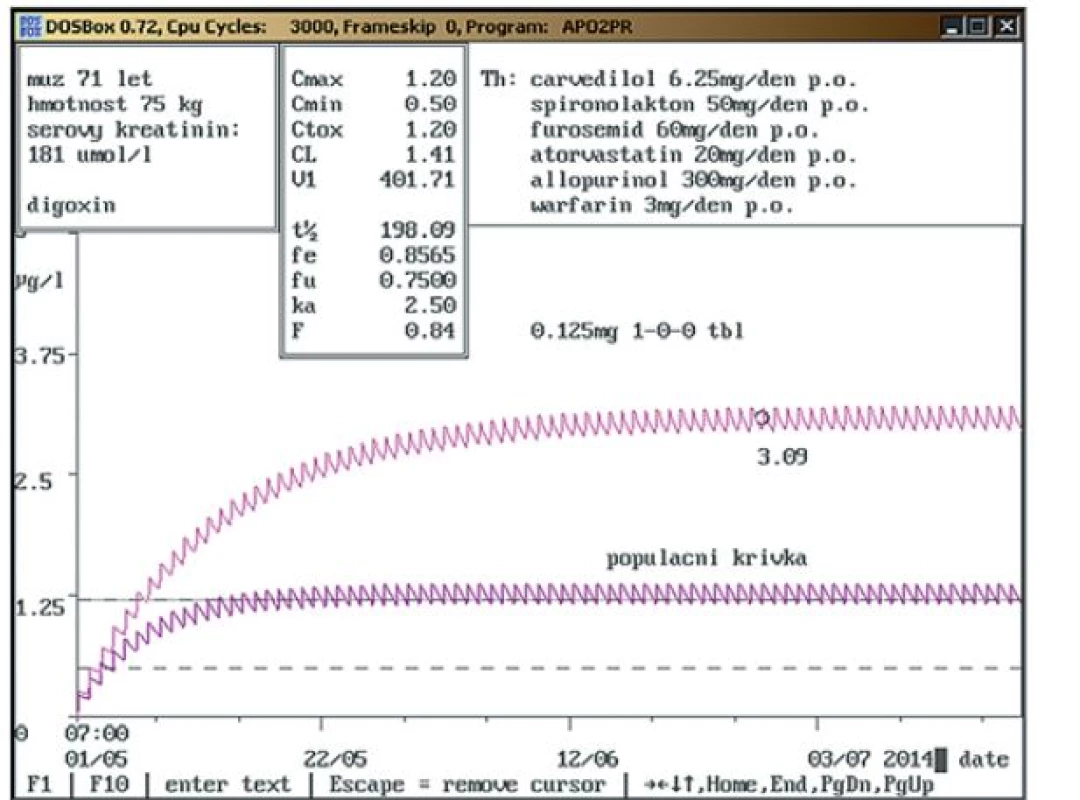
Stěžoval si na nechutenství, nauzeu a pokles hmotnosti o 3–4 kg za posledních 14 dní. Při vstupním vyšetření byly patrné markantní známky gynekomastie. Stanovená koncentrace digoxinu 3,09 ng/ml je považována za koncentraci toxickou, ale na základě farmakokinetické analýzy její hodnota výrazně převyšovala koncentraci, kterou by dotyčný pacient měl mít na základě populační farmakokinetiky pro jeho věk, hmotnost a renální funkce (viz populační křivka). Poněvadž pacient byl léčen mimo jiné karvedilolem a spironolaktonem, které jsou známé jako léčiva výrazně zvyšující hladinu digoxinu, rozdíl mezi naměřenou a očekávanou koncentrací je kvantifikací této lékové interakce způsobující snížené vylučování digoxinu. To v tomto případě činí cca 160 %. Obr. 2b. Na základě farmakokinetické analýzy bylo doporučeno digoxin vysadit na týden s průběžnou kontrolou za 3 dny s cílem dosažení koncentrace pod 1,0 ng/ml po následném snížení dávky digoxinu na 0,125 mg ½ tbl denně. 
Průběžná kontrola ukázala správnost predikce a po 3 dnech snížení koncentrace digoxinu na 2,08 ng/ml byl digoxinu vysazen další 4 dny a opětovně nasazen ve snížené doporučované dávce s kontrolním stanovením koncentrace 0,96 ng/ml po 4 dnech užívání. Pacient dostal opět chuť k jídlu a s poklesem koncentrace digoxinu se postupně upravovala i renální funkce. Gynekomastii je možno vysvětlit vlivem spironolaktonu a digoxinu. Kazuistika č. 3: Non ‑ compliance pacienta po propuštění a v průběhu ambulantní péče (obr. 3a – 3e).
Obr. 3. a. Jedenaosmdesátiletý pacient byl přijat na plicní oddělení pro CHOPN a s dalšími diagnózami chronické srdeční selhání s fibrilací síní, ICHS chron., hyperplazie prostaty. 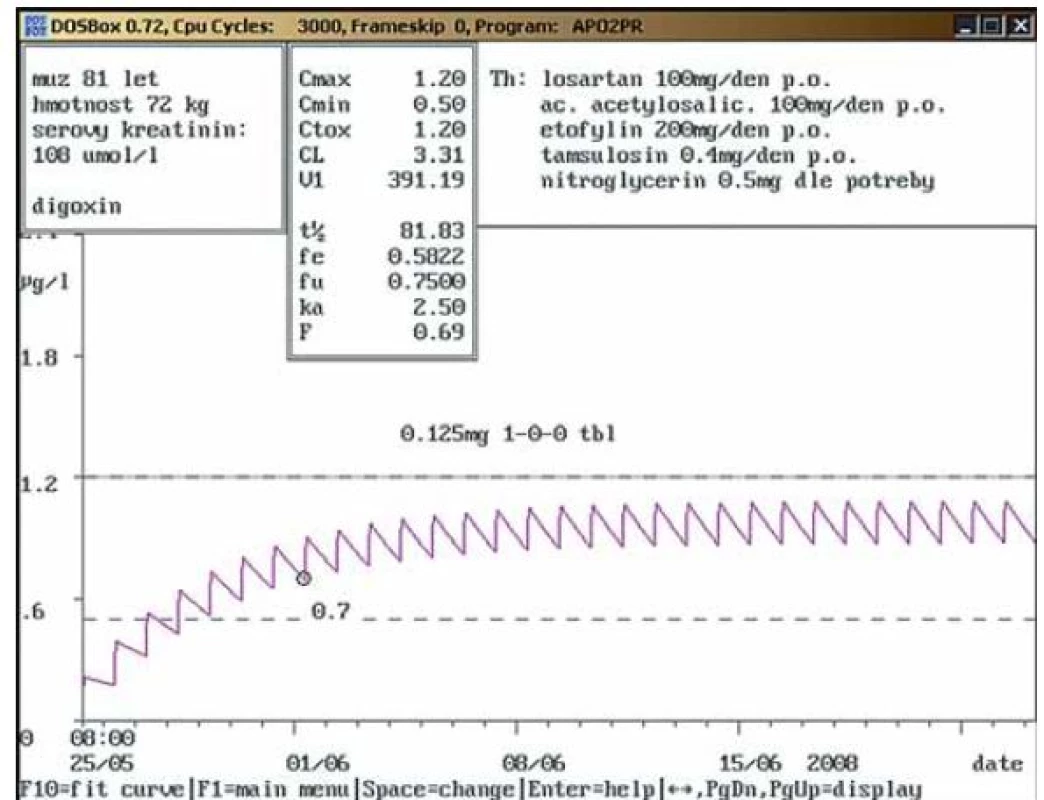
Během hospitalizace byl přidán digoxin v dávce 0,125 mg p.o. a za 7 dnů byla změřena koncentrace a provedena farmakokinetická analýza. Z ní vyplynulo, že při dosažení steady-state bude minimální koncentrace okolo 0,9 ng/ml a bylo doporučeno pokračovat v podávání stejné dávky i po propuštění s následnou kontrolou koncentrace digoxinu v séru v ambulanci. Obr. 3b. K ambulantní kontrole koncentrace digoxinu při dávkování 0,125 mg/den dochází zhruba za 5 měsíců. 
Změřená koncentrace 0,14 ng/ml naprosto neodpovídá predikované koncentraci podle populační křivky, diagnostikována non-compliance a doporučeno podávání původní dávky 0,125 mg/den s následnou kontrolou koncentrace za měsíc. Obr. 3c. Ke kontrole přichází vzorek pacienta za 9 měsíců, v žádance uvedeno, že užívá digoxin 0,125 mg 1× denně. 
Farmakokinetická analýza změřené koncentrace digoxinu 1,16 ng/ml ukázala, že pacient užívá původně doporučenou dávku 0,125 mg a nikoliv dvojnásobnou dávku, která mu byla ordinována ošetřujícím lékařem. Jedná se tedy opět o non-compliance vzhledem k ordinaci ambulantního lékaře. Poněvadž populační křivka pro zvýšenou dávku ukázala hladiny kolem 2,0 ng/ml, což jsou hladiny toxické, opět doporučeno podávání dávky 0,125 mg 1× denně. Obr. 3d. Navzdory našemu doporučení ošetřující lékař přesvědčil pacienta, aby užíval zvýšenou dávku 0,125 mg 2× denně a pacient přichází zhruba po roce na kontrolu s hladinou 2,18 ng/ml. 
Farmakokinetická analýza ukázala, že pacient je poprvé během 2 let compliantní, avšak změřená hladina je v toxickém rozmezí asi tak, jak byla při minulém vyšetření predikována. Doporučeno digoxin na 2 dny vysadit a pokračovat v původně doporučované dávce 0,125 mg 1x denně. Obr. 3e. Po dalším roce je poslán vzorek pacienta ke kontrole koncentrace digoxinu při dávkování 0,125 mg 1× denně a po 3 letech je dosaženo původně predikované koncentrace digoxinu 0,9 ng/ml, pacient je compliantní a i lékař akceptoval konečně naše doporučení. Další medikace se během 3 let našeho sledování neměnila. 
Diskuze
Velkou výhodou TDM je využití tzv. Bayesianského principu, kdy na základě jedné hladiny a dalších individuálních parametrů pacienta můžeme predikovat, jaká bude hladina digoxinu po dosažení ustáleného stavu, což by mohlo trvat při renální insuficienci i tři týdny. To umožňuje již krátce po nasazení terapie predikovat, jaké koncentrace digoxinu bude dosaženo při dlouhodobé terapii. Individuální výpočet farmakokinetických parametrů ukazuje, že při stejných dávkách mohou být u stejně starých pacientů různé koncentrace, např. u 75letého pacienta možno podávat dávku 0,25 mg, i když je v guidelines doporučena dávka 0,125 mg [9]. Současné podávání některých léčiv, jako jsou amiodaron, spironolakton, verapamil, chinidin, klaritromycin, erytromycin, itrakonazol, alprazolam a jiné, zvyšují koncentraci digoxinu v séru v důsledku inhibice MDR1 - trasportéru (P ‑ glykoproteinu) [11,12]. V kazuistice č. 2 je uveden vliv spironolaktonu a karvedilolu na koncentraci digoxinu, která je toxická a výrazně se liší od populační křivky. Pouze Bayesianský princip výpočtu farmakokinetických parametrů na základě dosažené hladiny umožňuje jednak úpravu dávky a jednak vysvětlení vysoké koncentrace. Farmakokinetický servis umožňuje výrazné snížení toxických koncentrací. Ve FN Ostrava byly toxické koncentrace zjištěny u 3 % pacientů, zatímco ve Fakultní Thomayerově nemocnici v Praze, kde není prováděn farmakokinetický servis, ale jen měření hladin, u 8 % pacientů [13,14].
Non ‑ compliance pacientů je jedním z hlavních problémů léčby nejen u srdečního selhání a fibrilace síní. Může vést buď k intoxikaci, nebo k selhání terapeutického efektu [15 – 17]. Informace o compliance digoxinu je jedním z důležitých faktorů pro účinné léčení, avšak takové údaje jsou řídké. První systematické review a metaanalýzy prospektivních observačních studií, které studovaly non‑compliance digoxinu v reálné praxi, provedli Kongkaew et al [18]. Bylo nalezeno osm studií, které sledovaly prevalenci non‑compliance digoxinu u ambulantních pacientů. Medián prevalence digoxinové non‑compliance činil 43,07 %, z toho šest studií popisovalo předávkování a pět poddávkování. Další tři studie analyzovaly non‑compliance digoxinu po propuštění z nemocnice, průměrná prevalence byla 25,1 %. Jedna studie sledovala non‑compliance digoxinu u hospitalizovaných pacientů, i tam byla nalezena non‑compliance v 4,51 %. Tento přehled a metaanalýzy ukazují, že non‑compliance je signifikantní přetrvávající problém, který limituje efektivní použití digoxinu u pacientů se srdečním selháním a/ nebo fibrilací síní. Co se týká metod stanovení compliance, bylo použito počítání tablet, pohovor s pacientem a stanovení koncentrace digoxinu v séru. V našem sdělení předkládáme možnost využití TDM digoxinu s farmakokinetickou analýzou k diagnostice a kontrole non‑compliance. Farmakokinetická analýza pomocí software MW Pharm 3.30 umožňuje diagnostiku úplné nebo částečné non‑compliance jak ve smyslu poddávkování, tak i ve smyslu předávkování u ambulantních pacientů, jak jsme ukázali v předchozí práci [9]. Prezentovaný případ non‑compliance v tomto sdělení ukazuje na celou řadu problémů a chyb jak ze strany pacienta, tak ze strany lékaře. Pacientovi je na základě farmakokinetické analýzy doporučeno dávkování 0,125 mg za den a kontrola do jednoho měsíce. Kontrola je provedena až za pět měsíců a výsledek ukázal non‑compliance pacienta, který je možno zařadit mezi 25 % non‑compliance u propuštěných pacientů [18]. Další chyba provází kontrolu za osm měsíců. Lékař neakceptuje naše doporučení a zvyšuje dvojnásobně dávku. Pacientova non‑compliance v tomto případě je jeho ochrana před intoxikací. Lékař opět neakceptuje naše doporučení a pacient je poprvé compliantní, ovšem s námi predikovanou intoxikací. Teprve za další rok prokazuje pacient compliance a koncentrace digoxinu je poprvé v námi predikovaném terapeutickém rozmezí. Můžeme popsat tři základní chyby – non‑compliance pacienta, chybné doporučení ošetřujícího lékaře nerespektující naše doporučení s farmakokinetickou analýzou a dlouhé intervaly mezi jednotlivými kontrolami. V přehledu je též zmiňována non‑compliance při hospitalizaci, takovýto příklad jsme publikovali již dříve [9]. S použitím farmakokinetické analýzy jsme prokázali „samoléčení“ pacientky digoxinem uloženým v nemocničním stolku.
Závěr
Digoxin má stále místo v léčbě chronického srdečního selhání, ale jeho benefiční účinek se objevuje při nízkých koncentracích v séru v rozmezí 0,5 – 0,9 ng/ ml. Existuje mnoho proměnných, které ovlivňují koncentrace digoxinu, jako jsou dávka, věk, hmotnost, funkce ledvin, lékové interakce. K dosažení terapeutického optima pomáhá terapeutické monitorování hladin léčiv, které umožňuje na základě individuálního výpočtu farmakokinetických parametrů predikci hladin i vysvětlení různých typů non‑compliance a lékových interakcí. TDM digoxinu by mělo být součástí guidelines České kardiologické společnosti.
Doručeno do redakce: 26. 1. 2015
Přijato po recenzi: 6. 2. 2015
doc. MU Dr. Milan Grundmann, CSc.
www.osu.cz
milan.grundmann@osu.cz
Zdroje
1. McMurray JJ, Adamopoulos S, Anker SD et al. ESC Committee for Practice Guidelines. ESC guidelines for the diagnosis and treatment of acute and chronic heart failure 2012: The Task Force for the Diagnosis and Treatment of Acute and Chronic Heart Failure 2012 of the European Society of Cardiology. Developed in collaboration with the Heart Failure Association (HFA) of the ESC. Eur J Heart Fail 2012; 14 : 803 – 869. doi: 10.1093/ eurjhf/ hfs105.
2. Špinar J, Vítovec J, Hradec J et al. Doporučený postup České kardiologické společnosti pro diagnostiku a léčbu chronického srdečního selhání 2011. Cor Vasa 2012; 54 : 113 – 134.
3. Hood WB Jr, Dans AL, Guyatt GH et al. Digitalis for treatment of heart failure in patients in sinus rhythm. Cochrane Database Syst Rev 2014; 4: CD002901. doi: 10.1002/ 14651858.CD002901.pub3.
4. The Digitalis Investigation Group. The effect of digoxin on mortality and morbidity in patients with heart failure. N Engl J Med 1997; 336 : 525 – 533.
5. Rathore SS, Curtis JP, Wang Y et al. Association of serum digoxin concentration and outcomes in patients with heart failure. JAMA 2003; 289 : 871 – 878.
6. Ahmed A, Waagstein F, Pitt B et al. Effectiveness of digoxin in reducing one‑year mortality in chronic heart failure in the Digitalis Investigation Group trial. Am J Cardiol 2009; 103 : 82 – 87. doi: 10.1016/ j.amjcard.2008.06.068.
7. Gheorghiade M, van Veldhuisen DJ, Colucci WS. Contemporary use of digoxin in the management of cardiovascular disorders. Circulation 2006; 113 : 2556 – 2564.
8. Gheorghiade M, Ferguson D. Digoxin. A neurohormonal modulator in heart failure? Circulation 1991; 84 : 2181 – 2186.
9. Grundmann M, Kacířová I. Význam TDM, fenotypizace a genotypizace pro správné dávkování léčiv. Čas Lék čes 2010; 149 : 482 – 487.
10. Grundmann M. 30 let klinické farmakologie ve zdravotnických zařízeních České republiky. Klin Farmakol Farm 2008; 22 : 127 – 129.
11. Kakumoto M, Takara K, Sakaeda T et al. MDR1 – mediated interaction of digoxin with antiarrhythmic or antianginal drugs. Biol Pharm Bull 2002; 25 : 1604 – 1607.
12. Ehle M, Patel C, Giugliano RP. Digoxin: clinical highlights: a review of digoxin and its use in contemporary medicine. Crit Pathw Cardiol 2011; 10 : 93 – 98. doi: 10.1097/ HPC.0b013e318221e7dd.
13. Alušík Š, Paluch Z, Lejsková M et al. Neuropsychiatrické projevy u intoxikace digoxinem. Klin Farmakol Farm 2009; 23 : 162 – 165.
14. Kacířova I, Grundmann M, Halvová P. TDM of digoxin and theophylline as an indicator of the quality of medical care in University Hospital Ostrava – results of the 5‑years monitoring. Abstract of IATDMCT European Therapeutic Drug Monitoring ‑ Personalised Pharmacotherapy Conference 2014; S101.
15. Cline CM, Bjorck ‑ Linne AK, Israelsson BY et al. Non ‑ compliance and knowledge of prescribed medication in elderly patients with heart failure. Eur J Heart Fail 1999; 1 : 145 – 149.
16. Goodyer LI, Miskelly F, Milligan P. Does encouraging good compliance improve patients’ clinical condition in heart failure? Br J Clin Pract 1995; 49 : 173 – 176.
17. van der Wal MH, Jaarsma T, van Veldhuisen DJ. Non ‑ compliance in patients with heart failure; how can we manage it? Eur J Heart Fail 2005; 7 : 5 – 17.
18. Kongkaew C, Sakunrag I, Jianmongkol P. Non ‑ compliance with digoxin in patients with heart failure and/ or atrial fibrillation: a systematic review and meta‑analysis of observational studies. Arch Cardiovasc Dis 2012; 105 : 507 – 516. doi: 10.1016/ j.acvd.2012.06.004.
Štítky
Dětská kardiologie Interní lékařství Kardiochirurgie Kardiologie
Článek Genetika kardiomyopatií
Článek vyšel v časopiseKardiologická revue – Interní medicína
Nejčtenější tento týden
2015 Číslo 1- Riziko rozvoje závažné infekce po císařském řezu lze snížit provedením antiseptického výplachu vaginy
- Spolehlivý systém skórování jizev k hodnocení fotografií popálenin
- Intermitentní hladovění v prevenci a léčbě (nejen) civilizačních chorob
- Stárnutí populace: problém, či výzva pro české zdravotnictví a medicínu?
- Nedostatečné dávkování enoxaparinu je u pacientů po ortopedickém výkonu časté a zvyšuje riziko tromboembolické nemoci
-
Všechny články tohoto čísla
- Vyšetření cerebrovaskulární rezervy u asymptomatických pacientů s významnou stenózou vnitřní karotické tepny
- Genetika kardiomyopatií
- Katetrizační léčba chronické stabilní ischemické choroby srdeční v současnosti
- Katetrizační uzávěr foramen ovale patens u potápěčů
- Katetrizační léčba fibrilace síní
- Srdeční resynchronizační terapie – kdy a u koho ji v současnosti indikovat?
- Není perikarditida jako perikarditida – kazuistika
- Studie Pegasus – duální antiagregace (ASA + ticagrelor) dlouhodobě po infarktu myokardu
- Nové studie dávají naději na zlepšení terapie aterosklerózy
-
Hlavolamy 2015
Propojení kardiologie a diabetologie - Vyhlášení výsledků autorské soutěže O nejlepší kazuistiku v roce 2014
- Vývoj a úkoly klinické farmakologie ve zdravotnické péči v ČR
- TDM antibiotik v klinické praxi
- prof. MUDr. Josef Veselka, CSc., FESC, FSCAI, FICA (*23. 3. 1965)
- TDM digoxinu v klinické praxi
- Patofyziologie a diagnóza obstrukce u hypertrofické kardiomyopatie
- Lékové interakce a současná klinická praxe
- Přímá perorální antikoagulancia – perspektivy terapeutického monitorování
- Klinická farmakologie antirevmatik
- Specifika klinických hodnocení léčiv časných fází I a II
- Význam TDM metotrexátu při terapii psoriázy
- Kardiologická revue – Interní medicína
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- TDM digoxinu v klinické praxi
- Lékové interakce a současná klinická praxe
- Srdeční resynchronizační terapie – kdy a u koho ji v současnosti indikovat?
- TDM antibiotik v klinické praxi
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



