-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Palopegteriparatid – postavenie v liečbe hypoparatyreózy
The role of palopegteriparatide in the treatment of hypoparathyroidism
Hypoparathyroidism is a rare endocrine disorder characterized by insufficient secretion of parathyroid hormone, leading to hypocalcemia and its severe clinical consequences. While there are various etiological forms, the most common cause is post-surgical removal of the parathyroid glands, such as after total thyroidectomy. Diagnosis is based on low parathyroid hormone levels combined with hypocalcemia and other biochemical changes. Clinical manifestations range from mild neurological symptoms to life-threatening complications such as laryngospasms and cardiac arrhythmias. Long-term complications include nephrolithiasis, renal insufficiency, and alterations in bone remodeling. The standard treatment consists of active vitamin D and oral calcium supplementation; however, this therapy does not always adequately regulate calcium metabolism without the risk of hypercalciuria and nephropathy. Newly developed treatment options, such as palopegteriparatide (TransCon PTH), represent a potential breakthrough in hypoparathyroidism management. This innovative form of parathyroid hormone has a prolonged effect, enabling calcium stabilization while minimizing the need for calcium and vitamin D supplementation. Clinical studies demonstrate significant improvements in patients’ quality of life and a reduction in complication rates. Although palopegteriparatide shows high efficacy and a favorable safety profile, its availability in Slovakia and Czechia remains limited. Its approval and inclusion in therapeutic options could significantly change the approach to hypoparathyroidism treatment and improve patient outcomes.
Keywords:
hypoparathyroidism, standard therapy, complications, palopegteriparatide.
Autoři: Králik Roman; Pavúková Simona; Payer Juraj; Kužma Martin
Působiště autorů: V. interná klinika LF UK a UNB, Bratislava
Vyšlo v časopise: Clinical Osteology 2025; 30(1): 42-45
Kategorie: Přehledové články
Souhrn
Hypoparatyreóza je vzácne endokrinologické ochorenie charakterizované nedostatočnou sekréciou parathormónu, ktorá vedie k hypokalciémii a jej závažným klinickým dôsledkom. Hoci existuje viacero etiologických foriem, najčastejšie vzniká po chirurgickom odstránení prištítnych teliesok, napríklad pri totálnej tyreoidektómii. Diagnostika je založená na nízkej koncentrácii parathormónu v kombinácii s hypokalciémiou a ďalšími biochemickými zmenami. Klinické prejavy sú rôznorodé – od miernych neurologických symptómov až po život ohrozujúce komplikácie, ako sú laryngospazmy či srdcové arytmie. Dlhodobé komplikácie zahŕňajú nefrolitiázu, renálnu insuficienciu a zmeny v kostnej remodelácii. Štandardná liečba spočíva v substitúcii aktívneho vitamínu D a perorálneho kalcia, avšak táto terapia nie vždy dokáže dostatočne regulovať metabolizmus vápnika bez rizika hyperkalciúrie a renálneho poškodenia. Novo vyvíjané liečebné možnosti, ako je palopegteriparatid (TransCon PTH), predstavujú potenciálny prelom v manažmente hypoparatyreózy. Ide o inovatívnu formu parathormónu s dlhodobým účinkom, ktorá umožňuje stabilizáciu kalciémie pri minimalizácii potreby suplementácie kalcia a vitamínu D. Klinické štúdie ukazujú významné zlepšenie kvality života pacientov a redukciu výskytu komplikácií. Hoci palopegteriparatid vykazuje vysokú účinnosť a bezpečnostný profil, jeho dostupnosť na Slovensku a v Českej republike je zatiaľ obmedzená. Jeho schválenie a zaradenie do terapeutických možností by mohlo zásadne zmeniť prístup k liečbe hypoparatyreózy a zlepšiť prognózu pacientov.
Klíčová slova:
hypoparatyreóza, štandardná terapia, komplikácie, palopegteriparatid.
Úvod
Hypoparatyreóza patrí k vzácnym ochoreniam, odhaduje sa, že jej prevalencia v Európskej únii je 3,2/10 000 obyvateľov (1). Podľa etiológie sa delí na dve hlavné skupiny: chirurgickú a nechirurgickú. Drvivú väčšinu prípadov predstavuje chirurgická, ktorá sa najčastejšie vyskytuje po totálnej tyreoidektómii. Spektrum nechirurgickej hypoparatyreózy je široké, patrí sem napríklad autoimunitný polyglandulárny syndróm, izolovaná autoimunitná hypoparatyreóza, infiltratívne ochorenia, napr. granulomatózne choroby, sarkoidóza a iné. Býva tiež geneticky podmienená, napr. pri DiGeorgeovom syndróme, autozomálne dominantnej hypokalciémii a mnohých ďalších (2, 3, 4, 5).
Diagnostika sa zakladá na preukázaní nízkej koncentrácie parathormónu súbežne s hypokalciémiou, hyperkalciúriou, hypofosfatúriou a hyperfostatémiou. Deficit parathormónu a vápnika by mal byť stanovený minimálne dvakrát po sebe s odstupom aspoň dvoch týždňov. Dôležité je vylúčiť hypomagneziémiu, ktorá môže viesť k funkčnej hypoparatyreóze. Koncentrácie vitamínu D bývajú nízke, prípadne v norme (2).
Klinické prejavy a komplikácie
Koncentrácia vápnika v sére ovplyvňuje všetky orgánové systémy v ľudskom tele, preto je klinický obraz tohto ochorenia rozsiahly. Najčastejšie sa hypokalciémia prejavuje formou tetánie, parestézií či svalových zášklbov (Chvostekov a Trousseaov príznak). V závažnejších prípadoch môže vyústiť do epileptických záchvatov či kómy. Život ohrozujúci býva laryngospazmus a bronchospazmus. EKG vykazuje napríklad bradykardiu alebo predĺženie QT intervalu, čo môže vyvolať komorovú tachykardiu či fibriláciu. Známe sú tiež prípady srdcového zlyhania či kardiomyopatie zapríčinené hypokalciémiou (6, 7, 8, 9). Pacienti sa často sťažujú aj na rôzne psychické zmeny, ako napríklad zhoršenie kognitívnych funkcií, únava, znížená koncentrácia, anxieta a depresia (10, 11).
Dobre známe sú aj komplikácie hypoparatyreózy, ktoré sa rozvíjajú chronicky a úzko súvisia s jej štandardnou terapiou. Najčastejšie býva postihnutý uropoetický systém. Nefrolitiáza a nefrokalcinóza sa vyskytujú až v 35 % prípadov (12). Vyvoláva ich výrazná kalciúria podmienená základným ochorením spolu s vysokými dávkami pri suplementácii kalcia. Rozvoj renálnej insuficiencie býva častejšie pozorovaný u pacientov s hypoparatyreózou než v bežnej populácii (incidencia okolo 41 %), rovnako aj progresia do „end-stage“ renálneho zlyhania (13, 14, 15). Kosti pacientov s hypoparatyreózou tiež vykazujú zmeny v porovnaní s bežnou populáciou. Pozorujeme u nich zníženú remodeláciu kostnej hmoty, vyššie hodnoty kostnej denzity a nižšie hodnoty trabekulárneho kostného skóre. Tieto zmeny sa spájajú s vyššou náchylnosťou kostí na fraktúry v porovnaní s bežnou populáciou (16, 17, 18).
Štandardná liečba hypoparatyreózy
Väčšina endokrinopatií s hormonálnym deficitom býva liečených hormonálnou substitúciou. Hypoparatyreóza z tohto hľadiska patrí k výnimkám, pri ktorých podávanie chýbajúceho hormónu netvorí základ terapie. V súčasnosti sa naďalej považuje za štandard v liečbe hypoparatyreózy substitúcia vitamínu D a kalcia. Dávkovanie jednotlivých preparátov je vysoko individuálne a často ho treba upravovať. Spravidla by dávky kalcia nemali presiahnuť 2 g/deň, horná hranica alfakalcidiolu je 3 µg/deň, v prípade kalcitriolu najviac 1,5 µg/deň. Hlavným cieľom terapie je zlepšiť kvalitu života pacientov minimalizovaním výskytu symptómov z hypokalciémie. Odporúča sa udržiavať koncentrácie sérového kalcia v dolnom pásme normy. Súčasne sa snažíme predísť rozvoju komplikácií spomenutých vyššie. Predovšetkým monitorujeme kalciúriu, renálne parametre, pravidelne kontrolujeme prítomnosť nefrolitiázy/kalcinózy a kalcifikácií na iných miestach (19, 20). Napriek maximálnemu úsiliu je manažment týchto pacientov náročný. Často dochádza k prekračovaniu odporúčaných dávok kalcia a vitamínu D v snahe o minimalizáciu príznakov z hypokalciémie, čo vedie k vzniku nežiaducich účinkov.
Palopegteriparatid
TransCon PTH (1-34), známy aj ako palopegteriparatid, predstavuje novú možnosť liečby hypoparatyreózy. Ide o prekurzor zložený z inaktívneho parathormónu, metoxypolyetylénglykolového nosiča a TransCon linkera. Po jeho aplikácii dochádza vo fyziologických podmienkach k štiepeniu tejto molekuly a uvoľneniu aktívnej formy parathormónu, ktorá sa viaže na receptory v cieľových tkanivách, ako sú kosť, obličky a črevo. Touto cestou sa zabezpečuje pôsobenie nedostatkového hormónu a úprava kalciémie. V porovnaní s ostatnými preparátmi parathormónu má TransCon PTH výhodu dlhodobého účinku v ľudskom organizme – až 24 hodín. Predchádzajúce preparáty pôsobili len 12 až 16 hodín.
Indikácie na liečbu
Slovenská endokrinologická spoločnosť vydala v roku 2024 konsenzus, v ktorom bol definovaný pacient vhodný na substitučnú liečbu parathormónom pri hypoparatyreóze. Zohľadnili sa viaceré kritériá a parametre, ako dávkovanie štandardnej terapie, rozvoj výraznej hyperkalciúrie, renálnej insuficiencie a ďalšie. Prehľad týchto kritérií uvádza tabuľka 1. Podotýkame, že ak pacient spĺňa ktorékoľvek z týchto kritérií, je vhodným kandidátom na liečbu parathormónom. Tabuľka 1 obsahuje aj kontraindikácie liečby parathormónom.
Spôsob podávania a dávkovanie
Palopegteriparatid sa podáva výlučne subkutánne raz denne injekčnou formou. Počiatočná dávka je 18 µg denne s postupnou titráciou až do maximálnej dennej dávky 60 µg. Pred prvým podaním PTH(1-34) sa musí upraviť dávka aktívneho vitamínu D a preparátov kalcia podľa aktuálnej kalciémie. Ak sú hodnoty sérového kalcia ≥ 2,07 mmol/l, ukončíme podávanie vitamínu D a ponecháme suplementy kalcia. V prípade kalciémie < 2,07 mmol/l redukujeme dávku vitamínu D aspoň o polovicu a kalciové suplementy ponecháme.
Titrácia dávky prebieha v krokoch po 3 μg/deň. Interval medzi zvyšovaním dávkovania je minimálne 7 dní pri sledovaní koncentrácie vápnika v sére. Cieľom je dosiahnuť udržiavaciu dávku, ktorá zabezpečí udržanie kalciémie v medziach normy, bez nutnosti podávania vitamínu D či suplementov kalcia. Pri vynechaní dávky podáme liek čo najskôr v prípade, ak neuplynulo viac ako 12 hodín. Ak bol tento časový interval prekročený, nasledujúcu dávku podáme podľa klasického harmonogramu. Dávkovanie nie je potrebné upraviť na základe veku (bezpečnosť a účinnosť u detí do 18 rokov nebola stanovená). Pacienti s renálnou insuficienciou s glomerulárnou filtráciou ≥ 30 ml/min nemusia meniť dávkovanie. Štúdie u pacientov s nižšou filtráciou doteraz neprebehli.
Tab. 1. Indikácie a kontraindikácie liečby parathormónom podľa konsenzu Slovenskej endokrinologickej spoločnosti z roku 2024 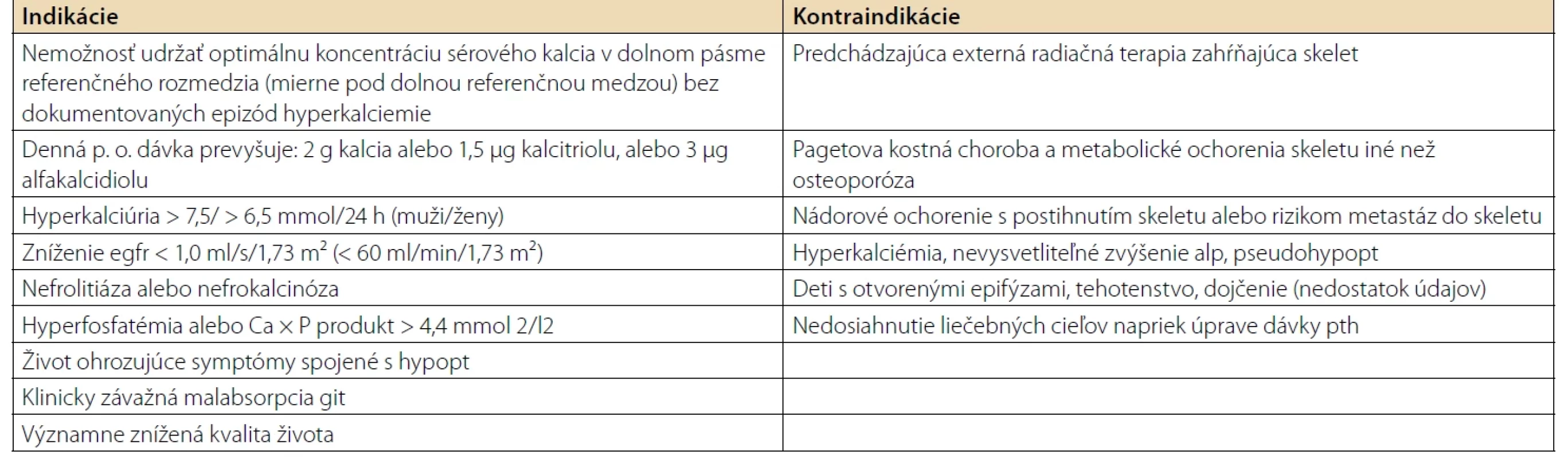
Účinnosť a bezpečnosť palopegteriparatidu
Dve veľké randomizované zaslepené štúdie, konkrétne PaTHway a PaTH Forward, sa zaoberali vlastnosťami TransCon PTH(1-34) a sledovali jeho účinnosť v období od 4 do 52 týždňov. Výsledky získané týmito štúdiami naznačujú, že ide nielen o vysokoúčinný, ale aj bezpečný liek pre pacientov s hypoparatyreózou.
Kvalitu života je náročné objektivizovať, no nespochybniteľne predstavuje zásadný pilier liečby vo všetkých medicínskych špecializáciách. Štandardne sa posudzuje pomocou dotazníkov. V prípade uvedených štúdií boli využité HPES (špecifický pre hypoparatyreózu) a SF-36 (nešpecifický pre hypoparatyreózu). V oboch dotazníkoch uvádzali pacienti štatisticky významné zlepšenie kvality života po fyzickej aj psychickej stránke v porovnaní s placebom. Zmierňovali sa príznaky z hypokalciémie, zlepšilo sa každodenné fungovanie pacientov (21, 22, 23).
Posúdenie udržania normokalciémie a nezávislosti od preparátov kalcia a vitamínu D je jedným z hlavných cieľov liečby parathormónom. Palopegteriparatid sa ukázal v tomto parametri ako veľmi efektívny. V štúdii PaTH Forward dosiahlo v 26. týždni úplnú nezávislosť od preparátov kalcia a vitamínu D 76 % pacientov, nezávislosť od vitamínu D a redukciu suplementov kalcia nad 500 mg/deň zaznamenalo až 91 % všetkých pacientov. Podobné výsledky boli zdokumentované v štúdii PaTHway. Po 26 týždňoch dosiahlo 79 % všetkých pacientov primárny cieľ (nezávislosť od štandardnej terapie a zároveň nevyžadovali navýšenie palopegteriparatidu v posledných 4 týždňoch štúdie). Na porovnanie, iba 5 % pacientov na placebe dosiahlo tento cieľ. Celkovo až 93 % pacientov dokázalo vysadiť konvenčnú terapiu. V 52. týždni cieľové hodnoty kalcia dosahovalo 81 % pacientov a až 95 % bolo nezávislých od preparátov kalcia či vitamínu D. Zaujímavý je aj údaj o celkovom počte tabliet suplementov vitamínu D a kalcia na deň. Z pôvodných priemerných 6,7 klesol denný počet tabliet na 0,5. Placebo skupina mala vstupne identickú dennú spotrebu tabliet, na konci sledovaného obdobia 5,4 denne (21, 22, 23).
Významný bol aj vplyv na úpravu kalciúrie. Do fyziologického rozpätia sa dostalo takmer 61 % pacientov na TransCon PTH v porovnaní s približne 29 % v skupine na placebe. Celkové hodnoty 24-hodinovej kalciúrie klesli z priemerných 415 mg/deň na začiatku štúdie, na 178 mg/deň na jej konci. Koncentrácie kalcia, fosfátu a kalciofosfátového súčinu boli v medziach normy počas trvania štúdií. Zároveň sa znížila frekvencia výskytu hypokalciémie v porovnaní s hodnotami pred začiatkom liečby TransCon PTH. Pozorovala sa aj úprava kostného obratu, hodnotená na základe normalizácie anabolického markera P1NP a resorpčného markera CTx (21, 22, 23).
Počas trvania štúdií nebol zaznamenaný žiadny závažný nežiaduci účinok palopegteriparatidu, ktorý by viedol k ukončeniu terapie alebos k úmrtiu pacienta. K najčastejším nežiaducim účinkom patrili reakcie v mieste vpichu (31 %), bolesti hlavy (16,9 %), hyperkalciémia (9,8 %), nauzea (8,5 %), únava (6,8 %), hypertenzia (6,8 %) (21, 22, 23).
Záver
Hypoparatyreóza patrí k vzácnym ochoreniam, napriek tomu výrazne ovplyvňuje kvalitu života pacientov, morbiditu a mortalitu. Zaraďuje sa k úzkej skupine endokrinopatií, ktoré sa štandardne neliečia substitúciou chýbajúceho hormónu. Palopegteriparatid sa javí ako sľubná liečba hypoparatyreózy – je účinný a bezpečný, znižuje výskyt komplikácií spojených so samotným ochorením, ale aj so štandardnou liečbou. Najväčšou nevýhodou palopegteriparatidu je však jeho nedostupnosť na Slovensku a v Českej republike. Momentálne sa usilujeme o schválenie jeho podávania našim pacientov, čo by mohlo výrazne zlepšiť kvalitu ich života.
Zdroje
1. Karpf D, et al. Prevalence of hypoparathyroidism in the EU: a systematic review and meta-analysis. Endocrine abstracts. 2020.
2. Siraj N, Hakami Y, Khan A. Medical hypoparathyroidism. Endocrinol Metab Clin North Am. 2018;47(4):797-808.
3. Hannan FM, Babinsky VN, Thakker RV. Disorders of the calcium-sensing receptor and partner proteins: insights into the molecular basis of calcium homeostasis. J Mol Endocrinol. 2016;57(3):R127-R142.
4. El-Hattab AW, Adesina AM, Jones J, Scaglia F. MELAS syndrome: clinical manifestations, pathogenesis, and treatment options. Mol Genet Metab. 2015;116(1-2):4-12.
5. Abraham MB, Li D, Tang D, et al. Short-stature and hypoparathyroidism in a child with Kenny-Caffey syndrome type 2 due to a novel mutation in FAM111A gene. Int J Pediatr Endocrinol. 2017;2017 : 1.
6. Silva BC. Skeletal and nonskeletal consequences of hypoparathyroidism. Arch Endocrinol Metab 2022. doi: 10.20945/2359-3997000000553.
7. Vadiveloo T, Donnan PT, Leese CJ, Abraham KJ, Leese GP. Increased mortality and morbidity in patients with chronic hypoparathyroidism: a population-based study. Clin Endocrinol. 2019;90 : 285-292.
8. Cusano NE, Bilezikian JP. Signs and Symptoms of Hypoparathyroidism. Endocrinol Metab Clin North Am. 2018;47(4):759-770.
9. Saini N, Mishra S, Banerjee S, Rajput R. Hypocalcemic cardiomyopathy: a rare presenting manifestation of hypoparathyroidism. BMJ Case Rep. 2019;12.
10. Brod M, Waldman LT, Smith A, Karpf D. Assessing the Patient Experience of Hypoparathyroidism Symptoms: Development of the Hypoparathyroidism Patient Experience Scale-Symptom (HPES-Symptom) Patient. 2020.
11. Brod M, Waldman LT, Smith A, Karpf D. Living with hypoparathyroidism: development of the Hypoparathyroidism Patient Experience Scale-Impact (HPES-Impact) Qual Life Res. 2021.
12. Hadker N, Egan J, Sanders J, et al. Understanding the burden of illness associated with hypoparathyroidism reported among patients in the PARADOX study. Endocr Pract.2014;20(7):671-679.
13. Meola A, Vignali E, Matrone A, Cetani F, Marcocci C. Efficacy and safety of long-term management of patients with chronic post-surgical hypoparathyroidism. J Endocrinol Investig. 2018;41(10):1221-1226.
14. Underbjerg L, Sikjaer T, Mosekilde L, Rejnmark L. Cardiovascular and renal complications to postsurgical hypoparathyroidism: a Danish nationwide controlled historic follow-up study. J Bone Miner Res. 2013;28(11):2277-2285.
15. Underbjerg L, Sikjaer T, Mosekilde L, Rejnmark L. The epidemiology of nonsurgical hypoparathyroidism in Denmark: a nationwide case finding study. J Bone Miner Res. 2015;30(9):1738-1744.
16. Silva BC. Skeletal and nonskeletal consequences of hypoparathyroidism. Arch Endocrinol Metab. 2022. doi: 10.20945/2359-3997000000553.
17. Rubin MR. Skeletal Manifestations of Hypoparathyroidism. Bone 2019;120 : 548-555.
18. Cipriani C, Minisola S, Bilezikian JP, Diacinti D, Colangelo L, Piazzolla V, et al. Vertebral Fracture Assessment in Postmenopausal Women With Postsurgical Hypoparathyroidism. J Clin Endocrinol Metab. 2021;106(5):1303-1311.
19. Kršek M, et al. Doporučený postup české endokrinologické společnosti pro diagnostiku a léčbu primární hyperparatyreózy a hypoparatyreózy. Vnitř Lék. 2021;67(Suppl. A).
20. Lazúrová I, Payer J, et al. Štandardné diagnostické a terapeutické postupy v endokrinológii. II. vyd. Vienala: Košice 2014. ISBN: 978-80-8126-089-6.
21. Khan AA, et al. Efficacy and Safety of Parathyroid Hormone Replacement With TransCon PTH in Hypoparathyroidism: 26-Week Results From the Phase 3 PaTHway Trial. J Bone Miner Res. 2023 Jan;38(1):14-25. doi: 10.1002/jbmr.4726. Epub 2022 Nov 12. PMID: 36271471; PMCID: PMC10099823.
22. Khan AA, et al. PaTH Forward: A Randomized, Double-Blind, Placebo-Controlled Phase 2 Trial of TransCon PTH in Adult Hypoparathyroidism. J Clin Endocrinol Metab. 2022 Jan 1;107(1):e372-e385. doi: 10.1210/clinem/dgab577. PMID: 34347093; PMCID: PMC8684498.
23. Clarke BL, et al. Efficacy and Safety of TransCon PTH in Adults with Hypoparathyroidism: 52-Week Results From the Phase 3 PaTHway Trial. J Clin Endocrinol Metab. 2024 Oct 8; dgae693. doi: 10.1210/clinem/dgae693. Epub ahead of print. Erratum in: J Clin Endocrinol Metab. 2025 Feb 04:dgaf048. doi: 10.1210/clinem/dgaf048. PMID: 39376010.
Štítky
Biochemie Dětská gynekologie Dětská radiologie Dětská revmatologie Endokrinologie Gynekologie a porodnictví Interní lékařství Ortopedie Praktické lékařství pro dospělé Radiodiagnostika Rehabilitační a fyzikální medicína Revmatologie Traumatologie Osteologie
Článek Několik slov úvodemČlánek Sekundární osteoporóza
Článek vyšel v časopiseClinical Osteology
Nejčtenější tento týden
2025 Číslo 1- Aktuální doporučení pro diagnostiku von Willebrandovy choroby
- Naděje budí časná diagnostika Parkinsonovy choroby založená na pachu kůže
- Na inkontinenční pomůcky nově dosáhne více pacientů
- Postabortivní syndrom – symptomy, dopady a možnosti léčby
-
Všechny články tohoto čísla
- Od beznaděje k výsledkům: klinické zkušenosti a efektivní strategie při léčbě kalcifylaxe
- Vitamin D – aktuální přehled problematiky a specifika v nefrologické praxi
- Několik slov úvodem
- Vybrané příběhy z osteonefrologie – úvod do problematiky
- Predikcia osteoporotických zlomenín na základe intenzity signálu MR?
- Palopegteriparatid – postavenie v liečbe hypoparatyreózy
- Hypofosfatázia – štandardný diagnostický a terapeutický postup
- Sekundární osteoporóza
- Kompletně nový přístup k problematice onemocnění kostního systému u pacientů s chronickým onemocněním ledvin (CKD--MBD) – jaká KDIGO doporučení pro praxi můžeme očekávat? Komentář k textu kritické konference KDIGO 2025
- Výber z najnovších vedeckých informácií v osteológii
- Clinical Osteology
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Vitamin D – aktuální přehled problematiky a specifika v nefrologické praxi
- Sekundární osteoporóza
- Kompletně nový přístup k problematice onemocnění kostního systému u pacientů s chronickým onemocněním ledvin (CKD--MBD) – jaká KDIGO doporučení pro praxi můžeme očekávat? Komentář k textu kritické konference KDIGO 2025
- Od beznaděje k výsledkům: klinické zkušenosti a efektivní strategie při léčbě kalcifylaxe
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Revma Focus: Spondyloartritidy
nový kurz
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Autoři: prof. MUDr. Pavel Horák, CSc., doc. MUDr. Ludmila Brunerová, Ph.D., doc. MUDr. Václav Vyskočil, Ph.D., prim. MUDr. Richard Pikner, Ph.D., MUDr. Olga Růžičková, MUDr. Jan Rosa, prof. MUDr. Vladimír Palička, CSc., Dr.h.c.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



