-
Články
Top novinky
Reklama- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
Top novinky
Reklama- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Top novinky
ReklamaAnální karcinom a jeho screening
Anal Cancer and Its Screening
Anal cancer is a tumour with a low prevalence but high morbidity. Due to the rarity of this tumour, therefore, its screening has not been considered until recently. However, in recent decades there has been an increase in the number of cases, especially in the population of HIV-positive men having sex with men. Since the most cases of anal cancer are squamous cell carcinomas associated with human papillomavirus (HPV) infection, as in the case of cervical cancer, there is the possibility of secondary prevention through appropriate screening. The basis of current screening examinations are digital anorectal examination, cytological examination and anoscopy. Early detection of treatable forms is important, also based on the fact that due to cultural changes and the prevalence of risk factors, an increase in the incidence of this tumour can be expected. However, education and motivation of at-risk groups of patients are necessary to increase the effectiveness of the screening, mainly by raising awareness of anal cancer and the role of risky sexual behavior and HPV infection.
Keywords:
cytology – HPV – screening – HIV – anal cancer – MSM – anoscopy
Autoři: F. Rob 1; J. Němcová 2,3,4; J. Šmahelová 5; J. Marx 6; O. Ondič 2,3,4
Působiště autorů: Dermatovenerologická klinika 2. LF UK a Fakultní nemocnice Bulovka, Praha, pověřený přednosta MUDr. Filip Rob, Ph. D. 1; Biomedicínské centrum Lékařské fakulty v Plzni, Plzeň, prof. MUDr. Milan Štengl, Ph. D. 2; Šiklův patologický ústav, Fakultní nemocnice v Plzni, Plzeň, prof. MUDr. Michal Michal 3; Bioptická laboratoř s. r. o., Plzeň, prof. MUDr. Alena Skálová, CSc. 4; Národní referenční laboratoř pro papillomaviry a polyomaviry, Ústav hematologie a krevní transfuze, Praha, prof. MUDr. Petr Cetkovský, Ph. D., MBA 5; Chirurgická klinika 1. LF UK a Fakultní nemocnice Bulovka, Praha, doc. MUDr. Jan Fanta, DrSc. 6
Vyšlo v časopise: Čes-slov Derm, 97, 2022, No. 1, p. 3-15
Kategorie: Souborné referáty (doškolování lékařů)
Souhrn
Anální karcinom je nádor s nízkou prevalencí, ale vysokou morbiditou. Díky vzácnosti tohoto nádoru proto nebylo donedávna ani uvažováno o jeho screeningu. V posledních dekádách však dochází k nárůstu počtu případů hlavně v populaci HIV pozitivních mužů majících sex s muži. Vzhledem k tomu, že většina případů análního karcinomu jsou dlaždicobuněčné karcinomy asociované s infekcí lidskými papilomaviry (HPV), máme obdobně jako v případě karcinomu děložního hrdla i v případě análního karcinomu možnost sekundární prevence pomocí vhodného screeningu. Základem současných screeningových vyšetření je digitální anorektální vyšetření, cytologické vyšetření a anoskopie. Včasné zachycení léčitelných forem je důležité i vzhledem k tomu, že díky kulturním změnám a prevalenci rizikových faktorů lze v budoucnu předpokládat nadále zvyšování incidence tohoto nádoru. Ke zvýšení efektivity screeningu je však nutná taktéž edukace a motivace rizikových skupin pacientů, hlavně rozšiřováním povědomí o análním karcinomu a roli rizikového sexuálního chování a HPV infekce.
Klíčová slova:
cytologie – HPV – screening – HIV – anální karcinom – MSM – anoskopie
ÚVOD
Anální karcinom je nádor s nízkou prevalencí, ale vysokou morbiditou. Díky vzácnosti tohoto nádoru proto nebylo donedávna ani uvažováno o jeho screeningu. V posledních dekádách však dochází k nárůstu počtu případů hlavně v populaci HIV pozitivních mužů majících sex s muži (MSM). Vzhledem k tomu, že většina případů análního karcinomu jsou dlaždicobuněčné karcinomy asociované s infekcí lidskými papilomaviry (HPV), máme obdobně jako v případě karcinomu děložního hrdla i v případě análního karcinomu možnost sekundární prevence pomocí vhodného screeningu. Díky anatomické lokalitě, která je obtížně samovyšetřitelná a pro mnohé pacienty velmi citlivá, dochází často ke zpoždění správné diagnózy o mnoho let, kdy se již pacient nachází ve stadiích onemocnění, která nejsou léčitelná. Díky tomu, že máme poměrně jasně definovanou rizikovou populaci, je možné správnou primární prevencí i včasným screeningem přednádorových stavů předejít velkému počtu těchto karcinomů. Současně lze očekávat, že vzhledem ke kulturním změnám a prevalenci rizikových faktorů se bude nadále výskyt análního karcinomu zvyšovat. Výrazným problémem je pozdní diagnostika, kdy téměř polovina pacientů přichází s již velmi pokročilým onemocněním ve stadiu diseminace. Tento trend výrazně zhoršuje prognózu pacientů, neboť v časných stadiích anální karcinom může být resekabilní a velmi dobře reaguje na kombinovanou chemoradioterapii, zatímco v pozdějích stadiích vyžaduje obtížné chirurgické operace s trvalou kolostomií zatížené vysokou morbiditou a negativním dopadem na kvalitu života [1].
EPIDEMIOLOGIE
Anální karcinom patří mezi vzácné nádory, tvoří pouze kolem 1,5 % gastrointestinálních malignit. V České republice (ČR) se jeho incidence dlouhodobě pohybuje mezi 0,6–1 případem na 100 tisíc obyvatel, s mortalitou kolem 0,2–0,4 případů na 100 tisíc obyvatel [20]. V posledních desetiletích však výskyt rakoviny konečníku vykazuje celosvětově rostoucí trend, což je možné pozorovat i na datech z ČR (obr. 1). Velké studie v USA prokázaly téměř dvojnásobný nárůst v incidenci mezi roky 1975 a 2000 nejen u mužů, ale také u žen. V minulosti se anální karcinom vyskytoval hlavně u mužů a žen kolem 7. decenia, v posledních letech však přibývá hlavně u mladších mužských pacientů s HIV infekcí [40]. Několik epidemiologických studií prokázalo, že incidence análního karcinomu mezi HIV pozitivními muži majícími sex s muži (MSM) přesahuje 130 případů na 100 tisíc obyvatel. Recentně provedená metaanalýza na podkladě několika desítek epidemiologických studií potvrdila nejvyšší riziko u HIV pozitivních MSM (85 případů na 100 tisíc obyvatel), mezi další rizikové skupiny patří heterosexuální osoby s HIV infekcí (32 případů na 100 tisíc obyvatel), HIV negativní MSM (19 případů na 100 tisíc obyvatel), ženy s HPV asociovanými karcinomy či prekancerózami (9 případů na 100 tisíc obyvatel) či pacienti po transplantaci solidních orgánů (13 případů na 100 tisíc obyvatel) [12]. Z těchto dat je patrné, že existují výrazné rozdíly u specifických populací a zatímco v běžné populaci případný screening onemocnění není smysluplný, u HIV pozitivních MSM je nutné ho provádět.
Obr. 1. Incidence a mortalita análního karcinomu v České republice v letech 2000–2018
(zdroj: www.svod.cz)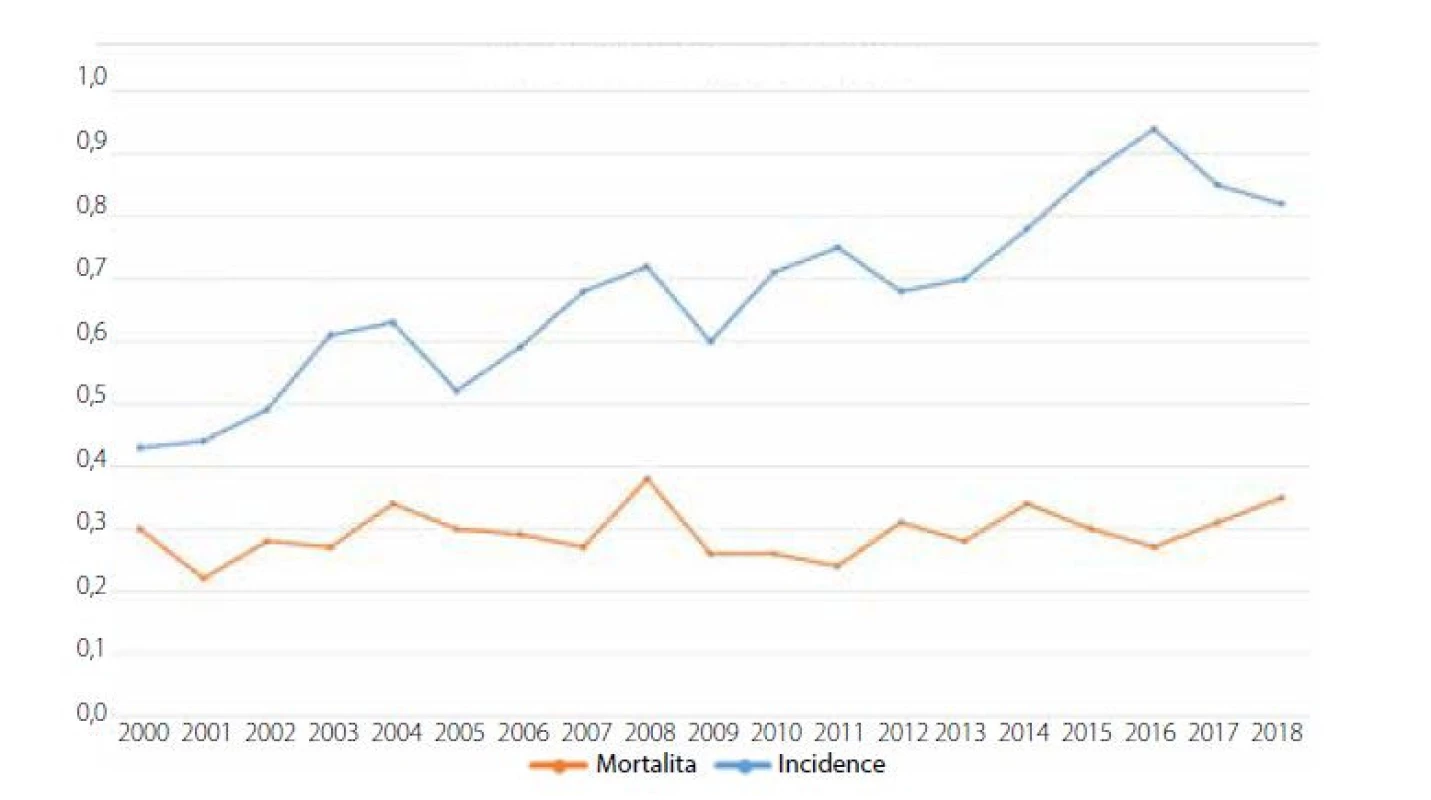
MALIGNÍ NÁDORY ANÁLNÍ OBLASTI
Anální karcinomy tvoří heterogenní soubor malignit, které se svým patologickým chováním až na výjimky chovají jako dlaždicobuněčné karcinomy (děložní hrdlo, orofaryng). Vzácnější typy nádorů, jako je perianální skvamózní karcinom, mají spíše průběh jako rakovina vulvy či penisu. Dlaždicobuněčné karcinomy tvoří kolem 90 % všech případů análních karcinomů, zbylých 10 % případů tvoří adenokarcinomy, bazocelulární karcinomy, vzácně melanomy, lymfomy či nediferencované tumory [54].
Dlaždicobuněčný/ spinocelulární karcinom
Dlaždicobuněčné karcinomy vznikají, jak název napovídá, z buněk dlaždicobuněčného epitelu, které jsou přítomné jak v análním kanálu, tak na kůži jeho okraje (typicky však v oblasti přechodového epitelu – transformační zóny). Dlaždicobuněčné karcinomy v oblasti perianální kůže jsou obdobné spinocelulárním karcinomům na jiných částech těla a i jejich terapie je shodná.
Adenokarcinom
Adenokarcinom vzniká v buňkách, které lemují horní část konečníku v oblasti rekta. Méně často může vycházet ze žlázových buněk pod anální sliznicí, které uvolňují sekret do análního kanálu. Adenokarcinomy mohou také vznikat v apokrinních žlázách. Specifickou jednotkou je Pagetova choroba, což je typ karcinomu apokrinních žláz, který se šíří povrchovou vrstvou kůže. Pagetova choroba může postihnout kůži kdekoli v těle, ale nejčastěji postihuje kůži perianální oblasti, vulvy nebo prsu [33].
Bazocelulární karcinom
Bazocelulární karcinomy jsou mnohem častější v oblastech pokožky vystavených slunci, jako je obličej a ruce. Vzácně se může objevit v oblasti perianální kůže. Terapie je obdobná jako u jiných lokalizací bazocelulárních karcinomů, tedy chirurgická excize [42].
Melanom
Melanomy v anální oblasti jsou vzácné, ale vzhledem k přítomnosti melanocytů jak v oblasti perianální kůže, tak ve sliznici análního kanálu, je nutné v této oblasti pomýšlet i na tuto diagnózu. Tvoří však méně než 1 % nádorů v této anatomické lokalizaci. Pokud je melanom diagnostikován v počátečním stadiu, lze ho odstranit chirurgickým výkonem a výhled na dlouhodobé přežití je velmi dobrý, nicméně protože anální melanomy jsou těžko viditelné, většina je nalezena v pokročilé fázi onemocnění, kdy již resekce celého nádoru není možná, či jsou přítomné metastázy [58].
BENIGNÍ AFEKCE V OBLASTI ANU
V anální oblasti se častěji vyskytují benigní léze, které je nutné mít na paměti v rámci diferenciální diagnostiky. Nejčastěji můžeme pozorovat polypy, což jsou malé pendulující výchlipky sliznice s rozdílnou etiologií vzniku (zánětlivé polypy, lymfoidní polypy a fibroepiteliální polypy). Jedná se o benigní útvary, které mohou obtěžovat mechanicky. Z ostatních běžných afekcí mohou být obdobného vzhledu fibromy. Anogenitální bradavice způsobené nízkorizikovou HPV infekcí (převážně typy HPV6 a HPV11) mají charakter pendulujících měkkých papul růžové barvy či barvy kůže. Zpravidla bývá přítomno více bradavic, které mohou zasahovat i do oblasti análního kanálu (obr. 2). V rámci diferenciální diagnostiky genitálních bradavic se zvláště u MSM můžeme setkat s condylomata lata (obr. 3), projevem sekundární syfilis, který je charakteristický široce přisedlými často macerovanými či erodovanými papulami až plaky [73].
Obr. 2. Perianální condylomata acuminata
(archiv Dermatovenerologické kliniky 2. LF UK a FN Bulovka)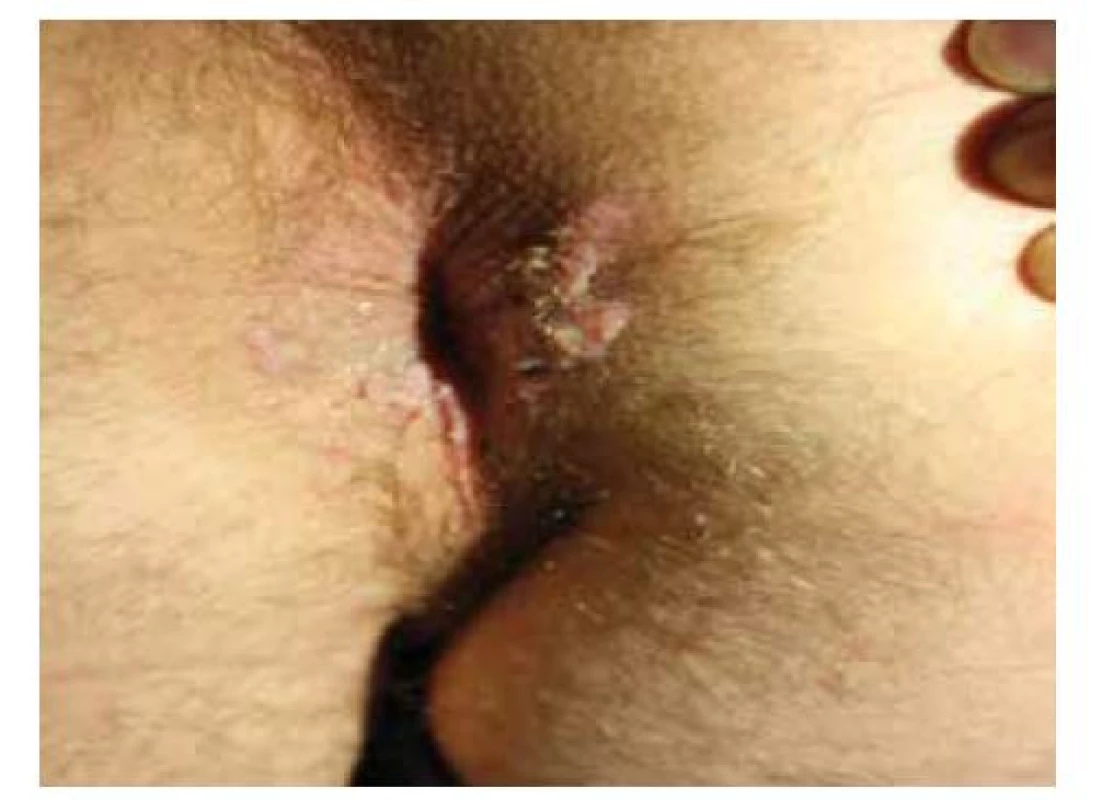
Obr. 3. Perianální condylomata lata
(archiv Dermatovenerologické kliniky 2. LF UK a FN Bulovka)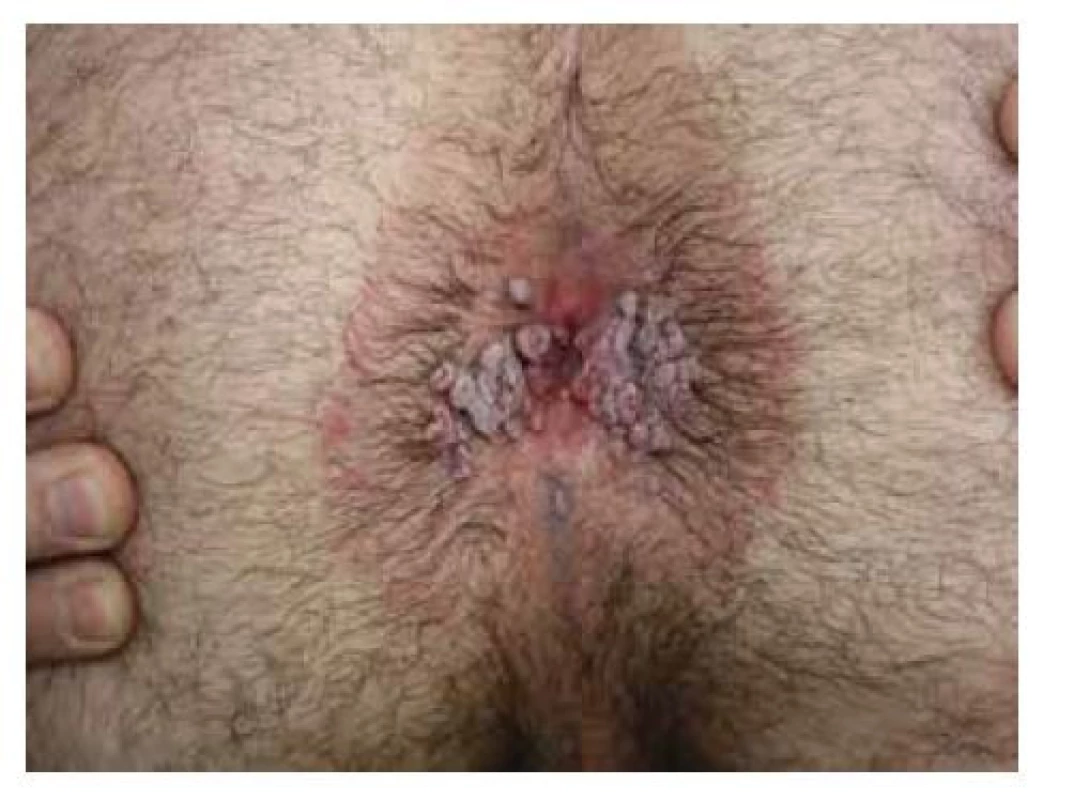
KLINICKÝ OBRAZ A SYMPTOMY
Klinicky se anální karcinom může manifestovat jako exofyticky rostoucí nehomogenní masa nebo nehojící se vřed. Anální karcinom se často projevuje krvácením, ale tento symptom bývá mylně zaměněn za krvácení z hemoroidů. Mezi ostatní časté symptomy patří bolestivost, pruritus ani, výtok, časté nucení na stolici, ztenčení stolice (tužkovitá stolice), inkontinence stolice či rozvoj píštělí. Většina z těchto symptomů je však již známkou pokročilého onemocnění [49].
Podobnost análního karcinomu s karcinomem děložního hrdla
Mezi dlaždicobuněčnými nádory děložního hrdla a anu existuje mnoho podobností. Oba typy nádorů jsou v převážné většině případů způsobeny perzistentní infekcí vysocerizikovými (HR) typy HPV a vyskytují se v transformační zóně epitelu (cervix, anální kanál). Transformační zóny v oblasti děložního hrdla a anu jsou typické epitelem s vysokou replikační aktivitou, který je díky tomu velmi náchylný ke genetickým změnám. K dalšímu ovlivnění buněčného dělení, opravných mechanismů syntézy DNA a navození nestabilního stavu v buňkách dochází po infekci HPV, což může vést k rozvoji malignit. Současně u obou onemocnění hraje výraznou roli imunosuprese, která usnadňuje ustavení perzistentní HPV infekce [28, 32]. Obdobně jako u karcinomu děložního hrdla je většina nádorů způsobena infekcí onkogenním typem HPV16 [28]. U obou typů nádorů je taktéž výrazný rozdíl v prognóze pacientů při včasné diagnostice oproti pozdnímu zachycení nádoru. U brzkých stadií rakoviny konečníku je 5leté přežití u více než 80 % pacientů, v případě pozdních stadií u méně než 30 % [32]. V případě obou těchto nádorových onemocnění je tedy zásadním cílem zamezit infekci rizikovými HPV pomocí vakcinace nejenom u dívek, ale také chlapců.
RIZIKOVÉ FAKTORY
V současnosti jsou známé rizikové faktory asociované s vyšším rizikem análního karcinomu (tab. 1).
Tab. 1. Rizikové faktory pro anální karcinom 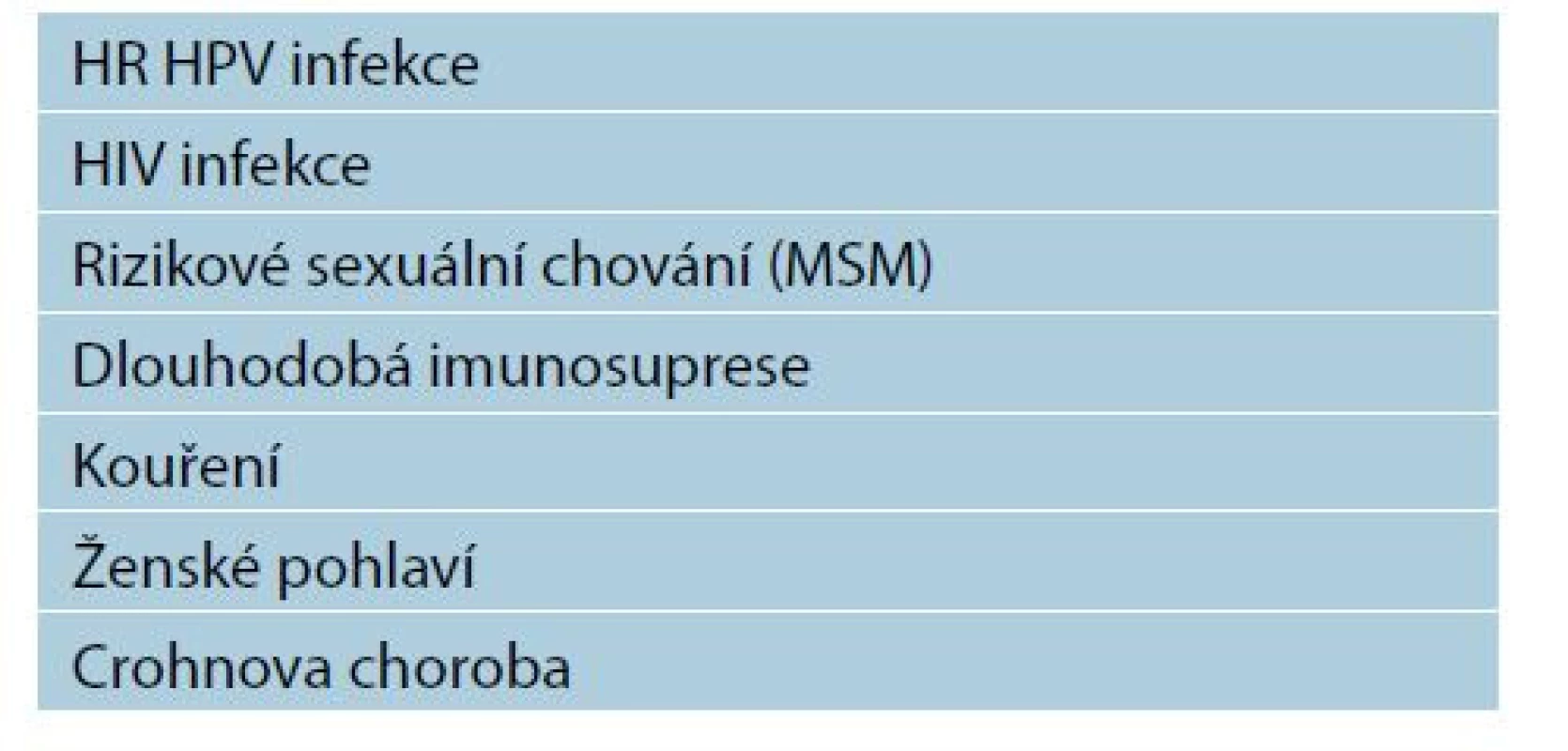
HPV infekce
Četné studie ukazují, že většina dlaždicobuněčných análních nádorů je spojena s infekcí HR HPV, stejnými viry, které způsobují karcinom cervixu a vulvy, penisu a orofaryngu [19, 28]. Dále bylo prokázáno, že ženy s anamnézou karcinomu či prekancerózy děložního hrdla mají i zvýšené riziko rakoviny konečníku [62].
HPV jsou velkou rodinou dvouvláknových malých DNA virů s transformačním potenciálem, které infikují buňky bazální vrstvy dlaždicobuněčného epitelu. V současnosti je popsáno více než 200 typů HPV. Kromě nejčastěji detekovaného typu HPV16 jsou s análním karcinomem etiologicky spojeny i některé další HR typy, HPV18, HPV31, HPV33 a HPV45 [26, 27].
V oblasti análního kanálu je HPV infekce u žen téměř stejně častá jako v genitální oblasti [26]. V mužské populaci se prevalence anální HPV infekce výrazně liší podle sexuální orientace. Zatímco u heterosexuálních mužů se pohybuje kolem 25 %, ve skupině MSM je prevalence mezi 70–90 % [24, 44].
K přenosu HPV z jedné osoby na druhou či k autoinokulaci dochází přímým kontaktem s kůží či sliznicí z infikované oblasti těla. Nejčastěji se tedy virus přenáší během sexu, a to nejenom vaginálního, ale také análního a orálního. Ačkoliv je HPV infekce častá a k infekci dojde během života u většiny sexuálně aktivní populace, klinické projevy se objeví vzácně, neboť většina těchto infekcí je úspěšně odstraněna imunitním systémem. Vzhledem k tomu, že životní cyklus HPV probíhá v keratinocytech, je pro indukci efektorové T-buněčné odpovědi zásadní prezentace virových antigenů Langerhansovými buňkami. Při odstraňování infikovaných buněk specifickými CD4+ pomocnými Th1 lymfocyty nedochází, jako u jiných infekcí, k masivní apoptóze či buněčné smrti infikované buňky. HPV jsou schopny účinně unikat imunitnímu dozoru a navodit latentní infekci v bazálních buňkách epitelu. Tuto teorii potvrzují nálezy perzistujícího genomu viru v bazálních buňkách i po letech od regrese léze [36]. Vlivem imunosuprese či změn hormonálních hladin může dojít k reaktivaci viru, která opět spustí replikační cyklus viru. Průměrná doba clearance HPV infekce se pohybuje mezi 6–8 měsíci, pro HPV16 je průměrná doba delší než jeden rok [22].
Pokud imunitní aparát není schopen virovou infekci účinně potlačit, zvyšuje se pravděpodobnost perzistentní infekce. Ta v případě HR HPV může vést k imortalizaci a následné transformaci hostitelských buněk, k selekci maligního klonu a vzniku intraepiteliálních neoplazií s následnou progresí do invazivního karcinomu [39]. Ani přes intenzivní výzkum však zatím není jasné, jak často přechází aktivní infekce do perzistentní a jak dlouho může HPV infekce perzistovat [25]. Lze tedy shrnout, že perzistence viru je způsobena především selháním imunitní odpovědi.
HIV infekce
Několika studiemi bylo potvrzeno, že HIV infekce je nezávislým rizikovým faktorem análního karcinomu. Vzhledem k rostoucímu počtu HIV pozitivních MSM se mluví o „epidemii“ análního karcinomu v této specifické populaci. Jen přítomnost HIV infekce zvyšuje celoživotní riziko análního karcinomu 30krát a 5letou mortalitu 4krát [13]. V případě HIV infekce se riziko zvyšuje s horším imunologickým stavem pacienta, zvláště při počtu CD4+ buněk pod 200 buněk/mm3. Zatímco v případě mnoha onemocnění asociovaných s pokročilou HIV infekcí (AIDS), kde je antiretrovirová léčba protektivním faktorem, nemá ani účinná terapie HIV pozitivní efekt na výskyt análního karcinomu [7].
Sexuální chování
Rizikové sexuální chování je významným faktorem pro získání HPV i HIV infekce, a v důsledku toho i výskytu análního karcinomu (obdobně jako pro karcinom děložního hrdla u žen). Typickými rizikovými faktory jsou dřívější zahájení sexuálního života, vyšší počet sexuálních partnerů a styky s partnerem, který v průběhu života měl vyšší počet sexuálních kontaktů. Významným rizikovým faktorem pro anální karcinom jsou receptivní anální styky, a to nejenom u mužů, ale také u žen, hlavně do 30 let života, což výrazně zvyšuje riziko získání HPV infekce v této oblasti se všemi nepříznivými důsledky [66].
Kouření
Kouření je nezávislým rizikovým faktorem pro anální karcinom [16]. Studie provedená na vzorcích análního epitelu kuřáků a celoživotních nekuřáků prokázala, že látky vznikající při kouření tabáku v těle působí změny v genomu análního epitelu [48]. Přestat s kouřením je smysluplné, neboť se toto riziko částečně snižuje [4].
Dlouhodobá imunosuprese
Obdobně jako u ostatních HPV asociovaných malignit, i v případě análního karcinomu dlouhodobá imunosuprese, např. u pacientů po transplantaci, zvyšuje riziko jeho vzniku. U pacientů po transplantaci jater či ledvin je 30–100krát vyšší oproti běžné populaci [2, 47].
Pohlaví
V minulosti převažovaly případy análního karcinomu u žen, hlavně díky poměrně jednoduchému přenosu HPV infekce z oblasti genitálu do anální oblasti. Studie provedená na ženách s těžkou dysplazií děložního hrdla prokázala známky rizikové HPV infekce u více než 50 % pacientek v této skupině [30]. V posledních dvou dekádách je anální karcinom častější u mužů, hlavně v populaci MSM [69].
Crohnova choroba
Chronický zánět v perianální oblasti způsobený Crohnovou chorobou a jejími komplikacemi je významným rizikovým faktorem pro rozvoj análního karcinomu. U pacientů s Crohnovou chorobu tvoří anální karcinom 14 % ze všech kolorektálních karcinomů, zatímco v běžné populaci bez Crohnovy choroby je to 1,4 % [59].
Anální intraepiteliální neoplazie
Obdobně jako cervikální intraepiteliální neoplazie (CIN) v případě karcinomu cervixu jsou anální intraepiteliální neoplazie (AIN) prekurzory invazivního karcinomu anu a hodnotí dysplastické změny v epitelu análního kanálu [51]. Podle starší terminologie existují 3 stupně těchto dysplazií – mírná, střední a těžká. Vzhledem k biologickému chování jednotlivých lézí je v současnosti pro středně těžkou a těžkou dysplazii využíván pojem high-grade skvamózní intraepiteliální léze (HSIL) nebo high-grade anální intraepiteliální neoplazie (HGAIN), neboť jsou asociovány s vyšším rizikem progrese do análního karcinomu [55].
Základním léčebným postupem u mírné dysplazie (low-grade skvamózní intraepiteliální léze – LSIL) je dispenzarizace, v případě HSIL je doporučován odběr biopsie a případná léčba, která je uvedena dále v textu [1].
Progrese análních prekanceróz do karcinomu
Rychlost a pravděpodobnost progrese prekanceróz do invazivního karcinomu není zcela známa. Kazuistické práce v minulosti zdokumentovaly přechod análních mírně dysplastických lézí, přes závažné dysplazie až do análního karcinomu (obr. 4 a 5). Starší práce uváděly progresi prekanceróz do invazivního karcinomu do 10 % případů [37]. Novější data však naznačují, že zvláště u imunokompromitovaných pacientů se riziko pohybuje mezi 13–50 %. Na podkladě těchto dat někteří autoři odhadují riziko progrese AIN po invazivní karcinom přibližně 10 % za 5 let [32]. Rychlost progrese však velmi pravděpodobně závisí na mnoha faktorech, a proto je tato data nutné interpretovat opatrně. Recentní práce provedené na HIV pozitivních MSM ukazují rychle se zvyšující zastoupení těžkých dysplazií ve sledované kohortě o více než 10 % ročně [57].
Obr. 4. Anální karcinom
(archiv Chirurgické kliniky 2. LF UK a FN Motol)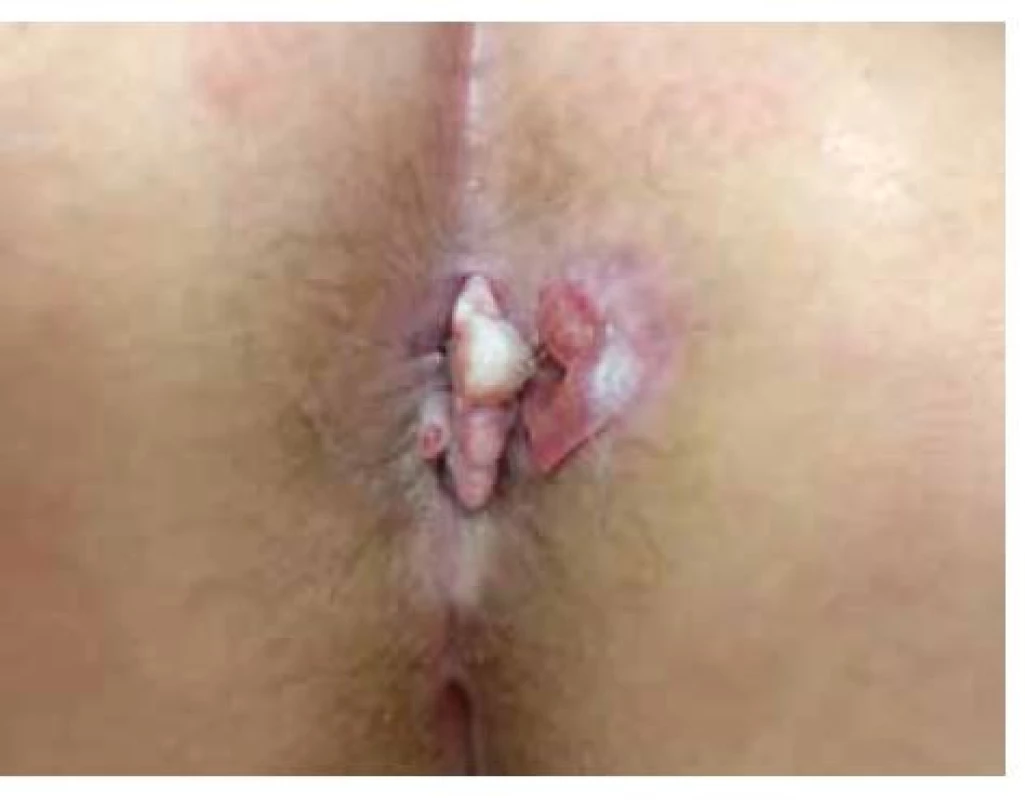
Obr. 5. Anální karcinom
(archiv Chirurgické kliniky 2. LF UK a FN Motol)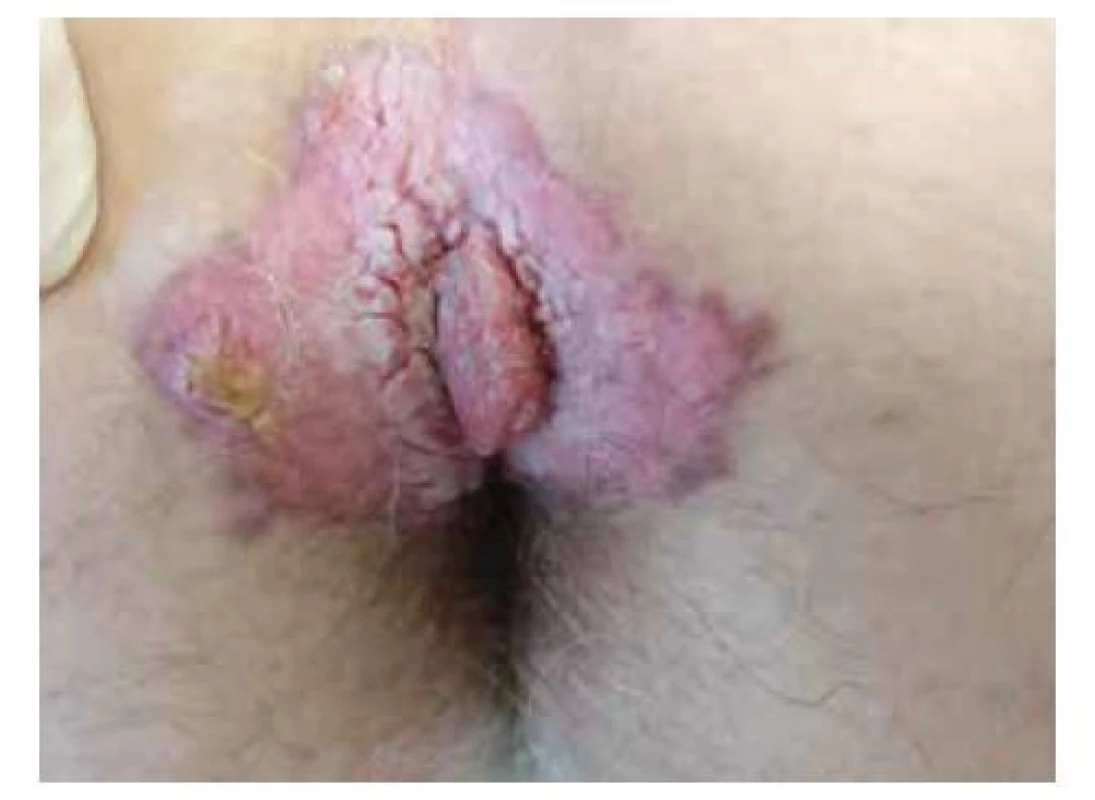
SCREENINGOVÁ VYŠETŘENÍ ANÁLNÍHO KARCINOMU
Cílem screeningu análního karcinomu je provádět pravidelné vyšetření u vybraných skupin populace s výrazně vyšším rizikem pro vznik tohoto nádoru, tedy hlavně HIV pozitivních mužů majících sex s muži.
Digital anorectal exam (DARE)
Digitální anorektální vyšetření (DARE) je v současnosti považováno za jedno ze základních vyšetření pro screening análního karcinomu, ačkoliv jeho senzitivita ani specificita zatím nebyly prokázány [45]. DARE je však bezpečné a rychlé vyšetření, které nevyžaduje speciální instrumentárium a může společně s vizuální aspekcí perianální krajiny a anoskopií sloužit jako vhodný základ screeningu análního karcinomu [3].
Lékař provádí DARE pomocí prstu (zpravidla ukazováku), který zasune přiblizně 5 cm za anální okraj a následně provede v rozsahu 360° palpaci kanálu a distálního konečníku. Účelem DARE je detekovat abnormality perianální, análního kanálu, distálního konečníku a u žen rektovaginálního septa. Procedura je rychlá, obvykle netrvá déle než 1 minutu a pro pacienty zpravidla představuje pouze lehký diskomfort. Díky stále častějšímu užívání této metody byly publikovány podrobné pokyny, standardy a metriky pro zajištění kvality DARE v rámci screeningu análního karcinomu, které patří k základnímu vyšetření [45].
Anální cytologie
Anální cytologie je často primárním nástrojem screeningu análního karcinomu. Obdobně jako je tomu v případě cytologického screeningu karcinomu děložního hrdla, anální cytologie využívá skutečnosti, že lze detekovat HPV virem indukované transformační změny epitelu v odloučených buňkách, které se získají stěrem anální sliznice. Stěr pro anální cytologii se provádí nejčastěji pomocí dakronového tampónu nebo speciálního kartáčku pro odběr anální cytologie, následně se buňky uvolní do tekutého media (cytologie na tenké vrstvě – LBC – liquid-based cytology) nebo jsou natřeny na cytologické sklíčko a po obarvení jsou odečteny cytoscreenerem a/nebo patologem. Nálezy v anální cytologii jsou klasifikovány zhruba jako v cervikálním cytologickém screeningu pomocí systému Bethesda: NILM (bez intraepiteliální léze a malignity), ASC-US (atypické dlaždicové buňky nejistého významu), LSIL (low-grade/mírná dysplazie dlaždicového epitelu, ASC-H (atypické dlaždicové buňky – nelze vyloučit těžkou dysplazii), HSIL (high-grade/těžká dysplazie dlaždicového epitelu) a karcinom [61]. Citlivost anální cytologie pro detekci těžkých lézí se pohybuje u různých studií od 69 % do 93 %, ale specificita je nižší, a to mezi 32–59 % [32]. Stupeň dysplazie určený pomocí anální cytologie může být poměrně často nepřesný, proto je jako rizikový nález brán již cytologický nález ASC-US [5].
Obr. 6. NILM (negativní pro intraepiteliální lézi a malignitu) – obecně jsou anální cytologické LBC (liquid-based cytology) nátěry méně buněčné než cervikální LBC
Keratotické šupinky (šipky) jsou často hojně přítomny.
(barvení podle Papanicolaou, zvětšení 200x)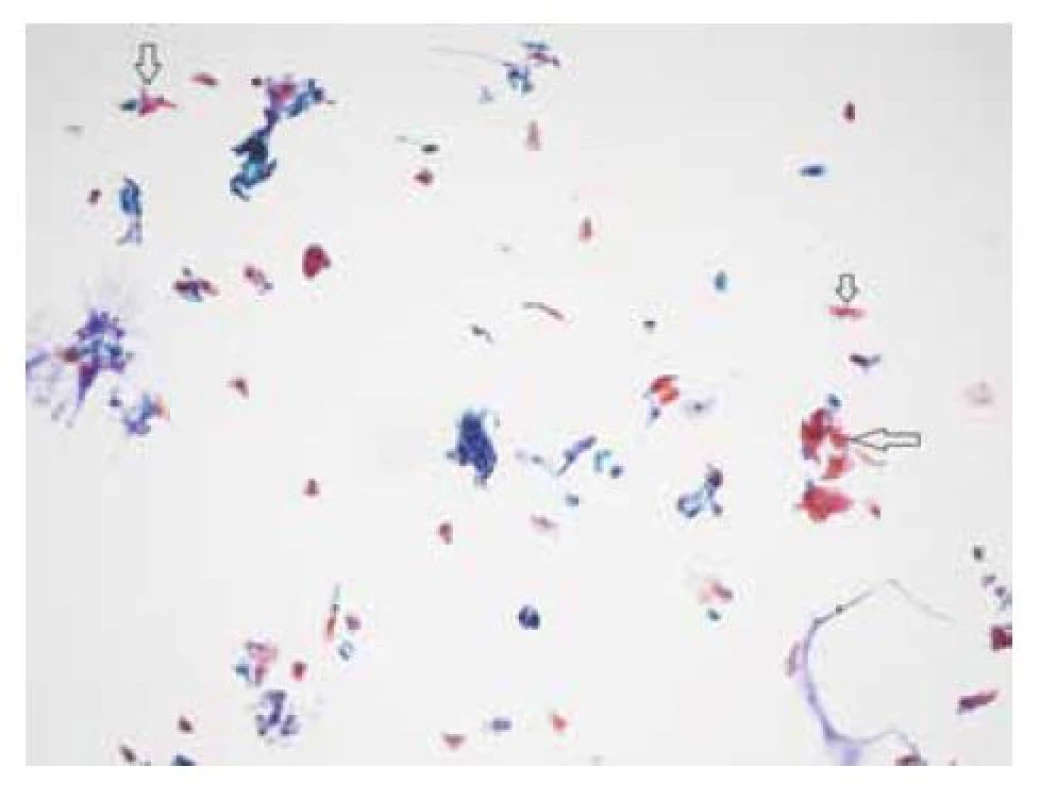
Obr. 7. LSIL (low-grade skvamózní intraepiteliální léze) – anální cytologické nátěry LBC (liquid-based cytology) diagnostikované jako LSIL obsahují velké dysplastické buňky skvamózního původu vykazující znaky odpovídající infekci HPV (šipky)
(barvení podle Papanicolaou, zvětšení 400x)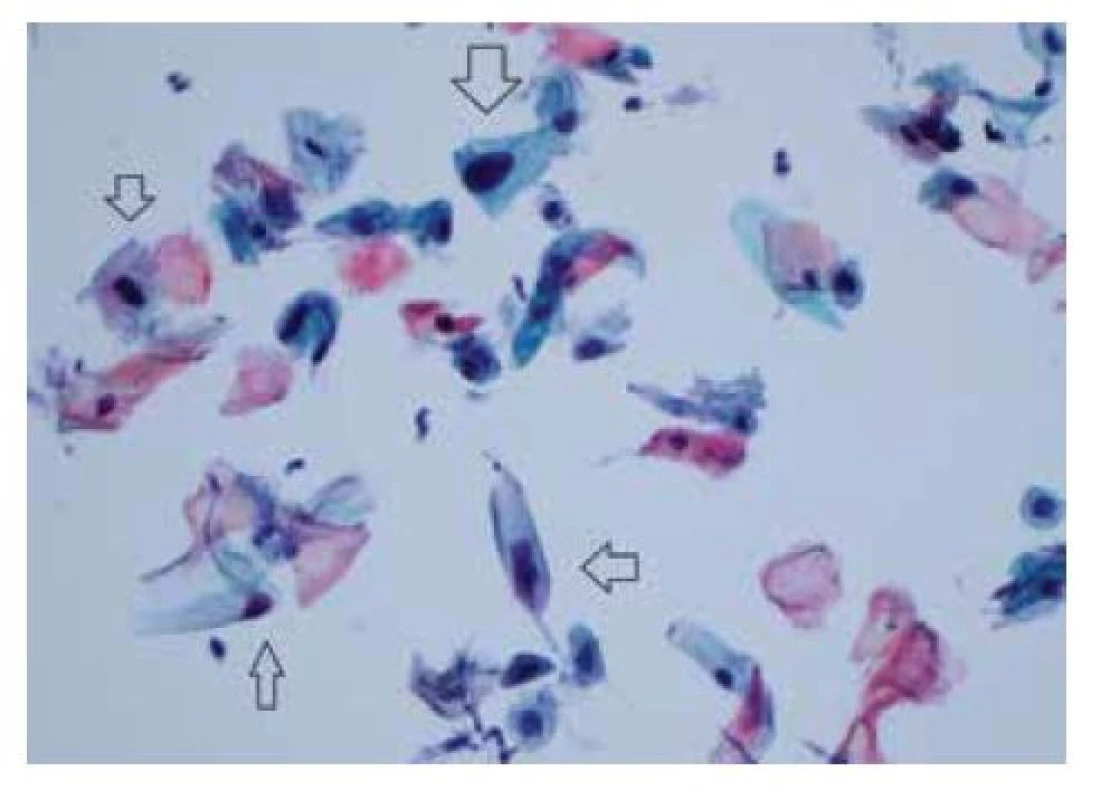
Obr. 8. HSIL (high-grade skvamózní intraepiteliální léze) – vzácné malé dysplastické buňky (šipky) skvamózního původu s vysokým nukleocytoplazmatickým poměrem a tmavým nepravidelným jádrem
(barvení podle Papanicolaou, zvětšení 400x)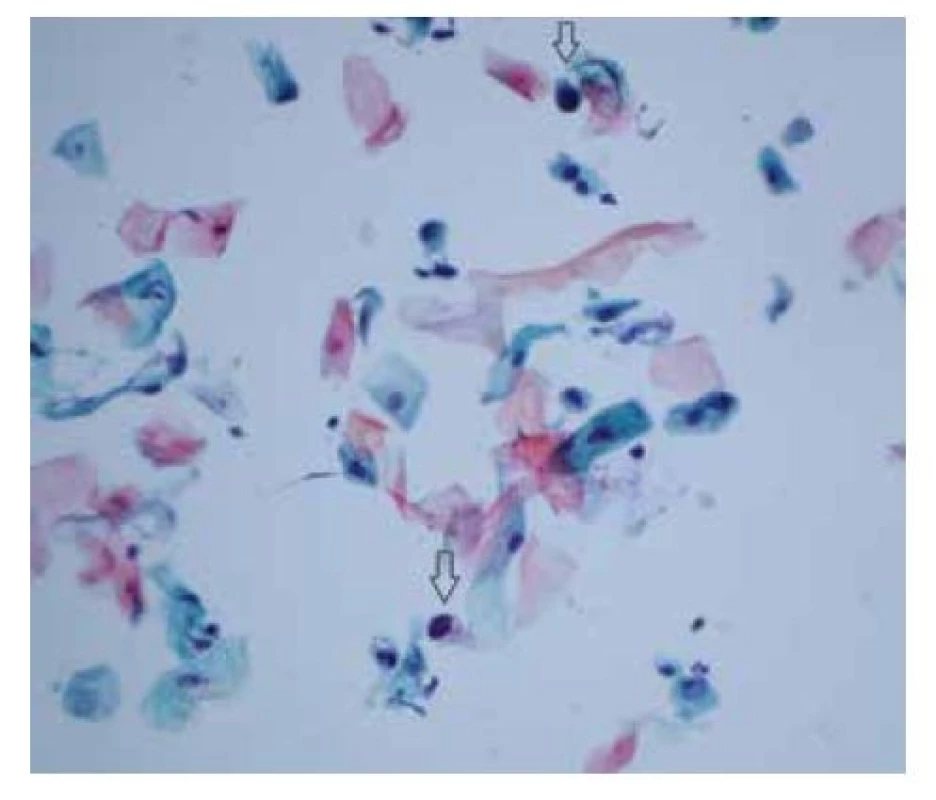
HPV testace
Nižší citlivost a specificita anální cytologie pro detekci análního karcinomu a těžkých prekanceróz by mohly být kompenzovány doplněním o testování dalšího biomarkeru, ideálně z jediného odběru buněk do tekutého média (LBC). Cervikální cytologii takto doplňuje HR-HPV test detekující 12–14 vysoce rizikových HPV typů, které jsou zodpovědné za 99 % cervikálních dlaždicobuněčných karcinomů. V případě screeningu análního karcinomu u vysoce rizikové populace je však využití HR-HPV testu omezené díky vysoké prevalenci HR-HPV v análním stěru. Specificita HR-HPV DNA testu je tedy velmi nízká, kolem 23 % při citlivosti detekce těžkých análních prekanceróz 95 % [11]. Vyšší potenciál pro využití ve screeningu análního karcinomu mají spíše HPV testy detekující nižší počet HR-HPV typů, zejména HPV16 a HPV18, nebo testy detekující transkripční aktivitu HR-HPV onkogenů E6/E7, tedy testy založené na detekci specifické HPV mRNA [41].
Metylace DNA
Velmi slibně se pro použití ve screeningu análního karcinomu jeví jiný typ biomarkeru, a to metylace DNA. Metylace patří mezi epigenetické modifikace DNA. Jejím principem je vazba metylové skupiny na DNA v oblasti tzv. CpG ostrůvků za pomoci enzymů metyltransferáz, což ovlivňuje přepis konkrétního genu do cílového proteinu. Vyšší míra metylace určitých lidských i HPV genů je spojena s těžkou prekancerózou a karcinomem děložního hrdla a může být klinicky využívána pro stratifikaci rizika HR-HPV pozitivních žen ve screeningu [18, 34]. Díky analogii v patogenezi cervikálního a análního karcinomu se předpokládá podobný metylační vzorec i u těžkých análních prekanceróz a karcinomů, což bylo na několika studiích prokázáno [35]. Přínos analýzy metylace DNA ve screeningu análního karcinomu je však nutné ověřit také klinickými daty [68].
Anoskopie a anoskopie s vysokým rozlišením
Anoskopické vyšetření je ekvivalentem kolposkopického vyšetření u žen. Běžná anoskopie má však nízkou senzitivitu a její využití pro screening análního karcinomu není vhodné. Z toho důvodu je doporučováno vyšetření anoskopií s vysokým rozlišením (high-resolution anoscopy – HRA), díky kterému je možné zkoumat celý anální kanál a perianální kůži pod pečlivou vizuální kontrolou [17]. Díky tomu je možné odebrat opravdu cílenou biopsii ze suspektního ložiska pod vizuální kontrolou. K lepšímu zviditelnění rychle rostoucích buněk lze užít 5% roztok kyseliny octové, který způsobí dočasné zbělání těchto oblastí. Možnost vizualizace análního kanálu pomocí HRA efektivně doplňuje limitace cytologického či HPV testování. V současnosti je HRA doporučována všem pacientům ve screeningu s abnormální cytologií [32]. Longitudinální studie asymptomatických MSM, kteří byli v průměru sledováni po 4 roky, prokázala, že HRA odhalila high-grade dysplaie u 11 % pacientů s normálními cytologickými nálezy [17]. Základní bariérou výraznějšího užití HRA je její dostupnost i přesto, že nákladová efektivita tohoto vyšetření byla prokázána [29]. Nutnost přístrojového vybavení je pouze částí problému, velmi důležitý je i trénink a zkušenost lékařů, kteří vyšetření provádějí. Vyšší úspěšnost správné diagnostiky rizikových lézí je dosažena u lékařů, kteří mají provedených několik stovek HRA vyšetření [50]. Z těchto všech důvodů je proto v současnosti HRA využívána až jako screeningový nástroj druhé linie u pacientů s abnormální cytologii či HPV testy. V ČR možnosti tohoto vyšetření v současnosti prakticky neexistují. Na základě zkušeností autorů této publikace a nedostupnosti HRA byl vytvořen návrh screeningu análního karcinomu u rizikových populací, který je součástí této publikace.
Bariéry screeningu análního karcinomu
Kromě nedostupnosti vyšetření a omezeného počtu center nabízející tento screening, který byl již v tomto textu diskutován, existují četné bariéry i na straně pacientů. Jedním ze základních úskalí všech screeningových programů je adherence pacientů se screeningem. Podle dosud provedených studií je právě compliance se screeningem análního karcinomu velkým problémem zvláště u HIV pozitivních MSM [64]. V současnosti jsou doporučovány notifikace (e-mail, telefon) pro pacienty, kteří mají mít screeningovou návštěvu. V praxi však takovéto upozorňování pacientů naráží na omezený počet administrativního personálu, který by se této aktivitě mohl věnovat [31].
Pacienti se taktéž často obávají bolestivosti či diskomfortu při vyšetření, a mohou proto screening či jeho opakování odmítnout. Studie zaměřující se na pozitivní prediktory u pacientů, kteří pravidelně dochází na screening análního karcinomu, zjistila, že vyšší compliance mají edukovaní pacienti, pacienti se subjektivními obtížemi a diagnózu HSIL [65].
Dalším výrazným problémem je stále poměrně nízké povědomí o HPV infekci a její rizikovosti mezi HIV pozitivními MSM. Studie zabývající se touto problematikou zjistila, že 35 % MSM nikdy neslyšelo o HPV infekci a jen 43 % vědělo, že HPV infekce může probíhat asymptomaticky. Zatímco 46 % respondentů vědělo, že HPV způsobuje genitální bradavice, méně než 20 % mělo povědomí, že taktéž způsobuje rakovinu penisu, anu a orofaryngu. Obdobně méně než polovina respondentů věděla, že existuje vakcína proti HPV infekci a případný zájem o očkování měla méně než polovina z těchto pacientů [6]. Z těchto dat vyplývá, že existují velké mezery v edukaci rizikových skupin pacientů nejen stran análního karcinomu, ale také HPV infekce.
LÉČBA ANÁLNÍ INTRAEPITELIÁLNÍ NEOPLAZIE
V součanosti existuje poměrně velké spektrum možností terapie AIN. Studie o účinnosti a bezpečnosti jednotlivých léčebných modalit jsou však zpravidla založeny na nízkých počtech nižších desítek pacientů, a proto je jejich výpovědní hodnota omezená [8].
Imiquimod – je aplikován ve formě 5% krému, jedná se o imunomodulační terapii, která aktivuje produkci cytokinů ve virem zasažených buňkách. Jedná se off - -label terapii, která je však běžně využívána. Účinnost imiquimodu na léze AIN se podle recentně provedené metaanalýzy pohybuje mezi 14–86 %. Riziko rekurencí je však vysoké a pohybuje se mezi 39–71 % během 3 let. Mezi nežádoucí účinky léčby patří svědění, bolestivost či krvácení v místě aplikace. Nicméně compliance s léčbou bývá vysoká, kolem 80–100 % [8, 21].
5-fluoruracil – je analogem pyrimidinu, který inhibuje thymidylát syntetázu – enzym podílející se na syntéze thymidinu, který je součástí DNA. Obdobně jako u imiquimodu je i jeho užití na léze AIN off-label, neboť je indikováno na bazocelulární karcinomy a aktinické keratózy. Na základě 4 klinických studií je kompletního odstranění AIN dosaženo u 9–86 % pacientů. Klinická studie však prokázala výrazné snížení virové nálože HPV16 i u pacientů, kteří nedosáhli úplného odstranění lézí. Recidivy se objevují u 9–58 % pacientů v průběhu jednoho roku. Vedlejší účinky terapie v anální oblasti jsou časté a postihují až 85 % pacientů, typicky mezi ně patří anální diskomfort, bolestivost a krvácení [52, 60].
Cidofovir – je analogem cytidinového nukleotidu, u něhož se prokázala in vitro účinnost na odstranění HPV infekce. Současné poznání je však stále omezené a existují pouze dvě studie, v nichž kompletního odstranění AIN bylo dosaženo u 59 % pacientů, recidiva se objevila pouze u 18 % pacientů. Vedlejší účinky terapie (pálení, bolestivost, krvácení) udávalo 97 % pacientů, vzhledem k tomu není v současnosti tato terapie doporučována v první ani druhé linii [8, 56].
Trichloroctová kyselina – je využívána v 80–85% koncentraci k naleptání vrchních vrstev kůže. Podle dostupných studií se účinnost na úplné odstranění lézí pohybuje mezi 28–72 %, s recidivami u 15–28 % pacientů v prvním půl roce po léčbě. Vedlejší účinky jsou obdobné jako u ostatních lokálních terapií a zahrnují svědění, bolestivost a krvácení postižené oblasti [14].
Chirurgická excize – se využívala hlavně v minulosti, než byly dostupné lokální preparáty k léčbě AIN. V současnosti se od ní upouští vzhledem k riziku vzniku anální stenózy či špatné sexuální funkce. Studie zkoumající účinnost chirurgické excize prokázaly recidivu u 18–30 % high-grade AIN. Důležitým výsledkem je také to, že kompletního odstranění lézí (AIN nezasahujících do okrajů resekátu) bylo dosaženo pouze u 14 % pacientů [9, 72].
Elektrokauterizace – při elektroktrokauterizaci se využívá k odstranění suspektních lézí diatermie. Úplného zhojení lézí bylo podle šesti klinických studií dosaženo u 22–78 % pacientů s high-grade AIN. Recidiva lokální se objevuje u přibližně 39 % ošetřených lézí, podle dosud provedených studií je riziko recidivy výrazně nižší u HIV negativních oproti HIV pozitivním pacientům. Vedlejší účinky jsou časté a patří mezi ně bolestivost, krvácení, vznik anální stenózy či infekce. Vzhledem k bolestivosti je většina výkonů prováděna v lokální anestezii, některými autory je proto navrhováno provádění elektrokauterizace v sedaci či celkové anestezii, což by umožňovalo lepší zobrazení a přístup k suspektním lézím. Ve studii srovnávající toleranci elektrokauterizace oproti 5-fluoruracilu, udávali pacienti po půl roce od léčby vyšší kvalitu života a lepší sexuální funkci při léčbě 5-fluoruracilem [10, 38].
Infračervená koagulace – je novější metodou, která využívá aplikaci sondy do análního kanálu, která směruje krátké výboje infračerveného světla do ošetřovaných oblastí. V současnosti existuje šest studií zkoumající účinnost této metody na AIN. Úplného odstranění lézí bylo dosaženo u 3–71 % pacientů. Obdobně jako ostatní ablativní metody patří mezi nežádoucí účinky terapie bolestivost, krvácení, ale méně často oproti elektrokauterizaci či chirurgické excizi [8, 15].
Radiofrekvenční ablace – je metodou využívanou hlavně u endoskopických výkonů, využívá více elektrod k zajištění radiofrekvenční energie, která způsobuje koagulaci tkáně při vysokých teplotách. V současnosti dvě recentní studie na terapii AIN, jež se zaměřovaly pouze na recidivu, která se pohybovala mezi 0–14 % v jednom roce po opakovaném ošetření. Vzhledem k omezeným znalostem není tedy vhodné tuto terapii využívat v první či druhé linii léčby [23].
Fotodynamická terapie – využívá fotodynamického senzibilizátoru lokálně či systémově aplikovaného, který je aktivován UV zářením. Dvě studie prokázaly úplnou odpověď na terapii u 27–40 % pacientů s recidivami u 20 % pacientů. Mezi nežádoucími účinky bylo svědění, bolestivost a krvácení v ošetřované oblasti [67, 70].
HPV vakcinace – představuje profylaktický přístup zabránění HPV infekce u naivních osob před expozicí viru. Několik menších nezaslepených studií zpočátku poukazovalo na regresi lézí či nižší riziko rekurence po očkování kvadrivalentní vakcínou u pacientů s high-grade AIN [46]. Velká randomizovaná, placebem kontrolovaná studie však neprokázala žádný benefit kvadrivalentní vakcinace u pacientů s AIN v průběhu 3,5 roku sledování [63]. Z toho důvodu nelze očekávat terapeutický přínos HPV vakcinace u pacientů s AIN na jejich současné léze či jejich recidivu [71].
DIAGNOSTIKA ANÁLNÍHO KARCINOMU
Případnou diagnostiku samotného análního karcinomu již provádí zpravidla chirurg (proktolog). Vzhledem k tomu, že neexistují typické diagnostické znaky pro anální karcinom, zůstává základem histologická verifikace bioptickým vyšetřením, následována stagingem pomocí zobrazovacích metod. Základním vyšetřením je endoanální ultrazvukové vyšetření, které může pomoci objasnit hloubku invaze nádoru do oblasti análního svěrače, naopak je však velmi limitující pro zobrazení postižených lymfatických uzlin. Klasickým stagingovým vyšetřením je CT vyšetření a MRI. Výhodou MRI je detailnější zobrazení postižené tkáně s dobrou vizualizací lymfatických uzlin. PET/CT je využíváno hlavně v případě pokročilého onemocnění k vizualizaci možných vzdálených metastáz [49].
LÉČBA ANÁLNÍHO KARCINOMU
Primárním cílem léčby je dosáhnout vyléčení pomocí lokální kontroly onemocnění se zachováním funkce análního svěrače s co možná nejlepší dosažitelnou kvalitou života. Na volbě nejvhodnější terapie by se měl podílet multidisciplinární tým obsahující onkologa, chirurga (proktologa), radiologa a patologa. Současná terapeutická doporučení se výrazně liší u karcinomů v oblasti análního kanálu, kde je první volbou chemoradioterapie, zatímco v případě menších karcinomů v oblasti análního okraje je první volbou excize nádoru [49].
Chirurgické radikální odstranění análních karcinomů bylo základem terapie do poloviny 80. let minulého století, výsledky studií však následně potvrdili lepší efektivitu kombinované chemoradioterapie, a proto byla chirurgie jako primární terapeutické metoda (až na nádory v oblasti análního okraje) opuštěna. Hlavním důvodem bylo časté porušení funkce análního svěrače, které vedlo k výrazně negativnímu vlivu na kvalitu života pacientů [49].
Chemoradioterapie kombinuje systémové podání 5-fluoruracilu a jiných cytotoxických léků (mitomycin C, cisplastina) s radioterapií. Tato léčba prokázala v klinických studiích kompletní regresi tumorů v 80–90 % případů a nabízí pacientům možnost zachování funkce análního svěrače. Vzhledem k hematologické toxicitě této léčby je nutné vyšetření krevního obrazu před a během terapie, kožní nežádoucí účinky terapie jsou taktéž časté [43].
Brachyterapie je vysoce konformní léčba, která je schopna dodat vysokou dávku záření primárnímu tumoru, šetřící okolní normální tkáně, kontralaterální sliznici a svěrač. Současné znalosti s intersticiální implantací iridia u análního karcinomu jsou stále velmi omezené, proto se v monoterapii nedoporučuje, ale může být použitelná jako stimulační prostředek po reakci na chemoradioterapii [53].
U pacientů s lokálně perzistentním, progresivním nebo rekurentním onemocněním je třeba zvážit radikální chirurgické řešení. Jen velmi malá část pacientů může být v této fázi léčena lokální resekcí. U většiny pacientů je vyžadována alespoň abdomino-perineální excize, protože dosažení negativního resekčního okraje se jeví jako klíčové. U některých pacientů je nutná exenterace pánevní oblasti a takto komplikovaný chirurgický výkon by měl být přednostně prováděn v institucích se zkušenostmi s multiviscerálními resekcemi [49].
Nicméně je nutné si uvědomit, že vzhledem k poměrně vzácnému výskytu análního karcinomu je počet randomizovaných klinických studií různých terapií análního karcinomu stále omezený.
ZÁVĚR
Vzhledem ke stárnutí populace, zvyšujícímu se počtu HIV pozitivních pacientů a prodlužování délky jejich života, lze nadále očekávat nárůst případů análního karcinomu celosvětově. Implementace screeningových programů v nejvíce rizikových populacích, jako jsou HIV pozitivní MSM je proto nezbytná. Ačkoliv efektivní vyšetřovací metody screeningu análního karcinomu jako HRA existují, v praxi extrémní nedostupnost tohoto vyšetření tento způsob screeningu v současnosti prakticky znemožňuje. Základem screeningu tedy nadále zůstává pravidelné cytologické vyšetření. Zda další vyšetřovací metody, jako je digitální anorektální vyšetření, HPV testování či metylace DNA, jsou vhodnými metodami pro triáž rizikových pacientů, stále není jasné. Nedílnou součástí screeningového algoritmu musí být úzká spolupráce infektologů, dermatovenerologů a chirurgů pečujících o tyto rizikové pacienty (obr. 9). Ke zvýšení efektivity screeningu je však nutná taktéž edukace a motivace rizikových skupin pacientů, hlavně rozšiřováním povědomí o análním karcinomu a roli HPV infekce.
Obr. 9. Návrh screeningu análního karcinomu v České republice 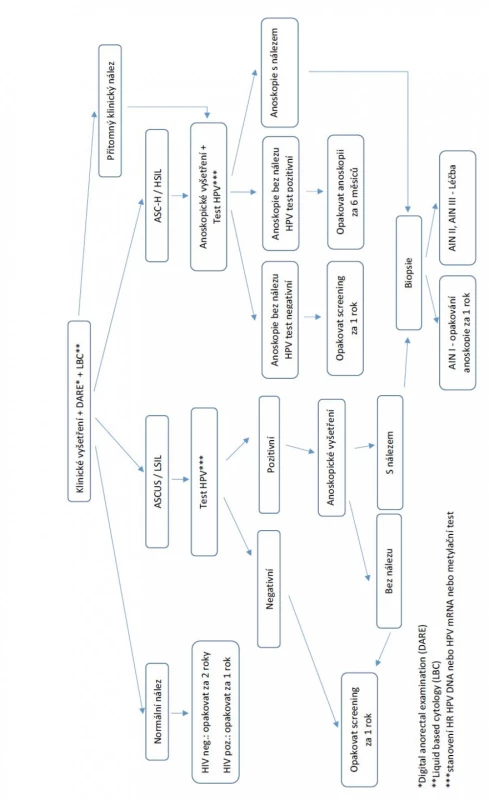
Prohlášení o střetu zájmů
Autoři v souvislosti s tématem práce v posledních 12 měsících nespolupracovali s žádnou farmaceutickou firmou.
Podpora: Grantem AZV ČR 17-31777A.
Do redakce došlo dne 2. 12. 2021.
Adresa pro korespondenci:
MUDr. Filip Rob, Ph.D.
Dermatovenerologická klinika 2. LF UK a FNB
Budínova 2/81
180 81 Praha 8
e-mail: filip.rob@bulovka.cz
Zdroje
1. ALAM, N. N., WHITE, D. A., NARANG, S. K. et al. Systematic review of guidelines for the assessment and management of high‐grade anal intraepithelial neoplasia (AIN II/III). Colorectal Dis, 2016, 18, p. 135–146.
2. ALBRIGHT, J. B., BONATTI, H., STAUFFER, J. et al. Colorectal and anal neoplasms following liver transplantation. Colorectal Dis, 2010, 12, p. 657–666.
3. ALBUQUERQUE, A., NATHAN, M., CAPPELLO, C. et al. Anal cancer and precancerous lesions: a call for improvement. Lancet Gastroenterol Hepatol, 2021, 6, p. 327–334.
4. BERTISCH, B., FRANCESCHI, S., LISE, M. Risk factors for anal cancer in persons infected with HIV: a nested case-control study in the Swiss HIV Cohort Study. Am J Epidemiol, 2013, 178, p. 877–884.
5. BETACOURT, E. M., WAHBAH, M. M., BEEN, L. C. et al. Anal cytology as a predictor of anal intraepithelial neoplasia in HIV-positive men and women. Diagn Cytopathol, 2013, 41, p. 697–702.
6. BJEKIC, M., SIPETIC-GRUJICIC, S., DUNIC, I. et al. Human papillomavirus and anal carcinoma knowledge in men who have sex with men in Belgrade, Serbia. Int J Dermatol, 2016, 55, p. 1082–1087.
7. BLASER, N., BERTISCH, B., KOUYOS, R. D. et al. Impact of screening and antiretroviral therapy on anal cancer incidence in HIV-positive MSM. Aids, 2017, 31, p. 1859–1866.
8. BROGDEN, D. R., WALSH, U., PELLINO, G. et al. Evaluating the efficacy of treatment options for anal intraepithelial neoplasia: a systematic review. Int J Colorect Dis, 2021, 36, p. 213–226.
9. BROWN, S. R., SKINNER, P., TIDY, J. et al. Outcome after surgical resection for high-grade anal intraepithelial neoplasia (Bowen’s disease). Br J Surg, 1999, 86, p. 1063–1066.
10. BURGOS, J., CURRAN, A., LANDOLFI, S. et al. The effectiveness of electrocautery ablation for the treatment of high-grade anal intraepithelial neoplasia in HIV-infected men who have sex with men. HIV Med, 2016, 17, p. 524–531.
11. CLARKE, M. A., WENTZENSEN, N. Strategies for screening and early detection of anal cancers: A narrative and systematic review and meta-analysis of cytology, HPV testing, and other biomarkers. Cancer Cytopathol, 2018, 126, p. 447–460.
12. CLIFFORD, G. M., GEORGES, D., SHIELS, M. S. et al. A meta‐analysis of anal cancer incidence by risk group: Toward a unified anal cancer risk scale. Int J Cancer, 2021, 148, p. 38–47.
13. COLÓN-LOPÉZ, V., SHIELS, M. S., MACHIN, M. et al. Anal cancer risk among people with HIV infection in the United States. J Clin Oncol, 2018, 36, p. 68.
14. CRANSTON, R. D., BAKER, J. R., LIU, Y. et al. Topical application of trichloroacetic acid is efficacious for the treatment of internal anal high-grade squamous intraepithelial lesions in HIV-positive men. Sex Transm Dis, 2014, 41, p. 420–426.
15. CRANSTON, R. D., HIRSCHOWITZ, S. L., CORTINA, G. et al. A retrospective clinical study of the treatment of high-grade anal dysplasia by infrared coagulation in a population of HIV-positive men who have sex with men. Int J STD AIDS, 2008, 19, p. 118–120.
16. DALING, J. R., MADELEINE, M. M., JOHNSON, L. G. et al. Human papillomavirus, smoking, and sexual practices in the etiology of anal cancer. Cancer, 2014, 101, p. 270–280.
17. DALLA PRIA, A., ALFA-WALI, M., FOX, P. et al. High-resolution anoscopy screening of HIV-positive MSM: longitudinal results from a pilot study. Aids, 2014, 28, p. 861–867.
18. DE STROOPER, L. M. A., VERHOEF, V. M. J., BERKHOF, J. et al. Validation of the FAM19A4/mir124-2 DNA methylation test for both lavage - and brushbased self-samples to detect cervical (pre)cancer in HPV-positive women. Gynecol Oncol, 2016, 141, p. 341–347.
19. DONA, M. G., BENEVOLO, M., LATINI, A. et al. Anal cytological lesions and HPV infection in individuals at increased risk for anal cancer. Cancer Cytopathol, 2018, 126, p. 461–470.
20. Epidemiologie zhoubných nádorů v České republice (online) (18.9.2021). Dostupné na www: https:// www.svod.cz/.
21. FOX, P. A., NATHAN, M., FRANCIS, N. et al. A double-blind, randomized controlled trial of the use of imiquimod cream for the treatment of anal canal highgrade anal intraepithelial neoplasia in HIV-positive MSM on HAART, with long-term follow-up data including the use of open-label imiquimod. Aids, 2006, 24, p. 2331–2335.
22. GIULIANO, A. R., LEE, J. H., FULP, W. et al. Incidence and clearance of genital human papillomavirus infection in men (HIM): a cohort study. Lancet, 2011, 377, p. 932–940.
23. GOLDSTONE, R. N., HASAN, S. R., DRURY, S. et al. A trial of radiofrequency ablation for anal intraepithelial neoplasia. Int J Color Dis, 2017, 32, p. 357–365.
24. GOLDSTONE, S., PALEFSKY, J. M., GIULIANO, A. R. et al. Prevalence of and risk factors for human papillomavirus (HPV) infection among HIV-seronegative men who have sex with men. J Infect Dis, 2011, 203, p. 66–74.
25. GRAVITT, P. E. The known unknowns of HPV natural history. J Clin Invest, 2011, 121, p. 4593–4599.
26. HERNANDEZ, B. Y., MCDUFFIE, K., ZHU, X. et al. Anal human papillomavirus infection in women and its relationship with cervical infection. Cancer Epidem Biomarkers Prev, 2005, 14, p. 2550–2556.
27. HOOTS, B. E., PALEFSKY, J. M., PIMENTA, J. M. et al. Human papillomavirus type distribution in anal cancer and anal intraepithelial lesions. Int J Cancer, 2009, 124, p. 2375–2383.
28. KRZOWSKA-FIRYCH, J., LUCAS, G., LUCAS, C. et al. An overview of Human Papillomavirus (HPV) as an etiological factor of the anal cancer. J Infect Pub Health, 2019, 12, p. 1-6.
29. LAM, J. M. C., HOCH, J. S., TINMOUTH, J. et al. Costeffectiveness of screening for anal precancers in HIV-positive men. Aids, 2011, 25, p. 635–642.
30. LAMMÉ, J., PATTARATORNKOSOHN, T., MERCADO - ABADIE, J. et al. Concurrent anal human papillomavirus and abnormal anal cytology in women with known cervical dysplasia. Obstet Gynecol, 2014, 124, p. 242–248.
31. LANDSTRA, J. M. B., CIARROCHI, J., DEANE, F. P. Psychosocial aspects of anal cancer screening: a review and recommendations. Sex health, 2012, 9, p. 620–627.
32. LEEDS, I. L., FANG, S. H. Anal cancer and intraepithelial neoplasia screening: a review. World J Gastrointest Surg, 2016, 39, p. 41.
33. LEWIS, G. D., HAQUE, W., BUTLER, E. B. et al. Survival outcomes and patterns of management for anal adenocarcinoma. Ann Surg Oncol, 2019, 26, p. 1351–1357.
34. LORINCZ, A. T., BRENTNALL, A. R., SCIBIOR-BENTKOWSKA, D. et al. Validation of a DNA methylation HPV triage classifier in a screening sample. Int J Cancer, 2016, 138, p. 2745–2751.
35. LORINCZ, A. T., NATHAN, M., REUTER, C. et al. Methylation of HPV and a tumor suppressor gene reveals anal cancer and precursor lesions. Oncotarget, 2017, 8, p. 50510–50520.
36. MAGLENNON, G. A., MCINTOSH, P., DOORBAR, J. Persistence of viral DNA in the epithelial basal layer suggests a model for papillomavirus latency following immune regression. Virology, 2011, 414, p. 153–163.
37. MARFING, T. E., ABEL, M. E., GALLAGHER, D. M. Perianal Bowen‘s disease and associated malignancies. Results of a survey. Dis Colon Rectum, 1987, 30, p. 782–785.
38. MARKS, D. K., GOLDSTONE, S. E. Electrocautery ablation of highgrade anal squamous intraepithelial lesions in HIV-negative and HIV-positive men who have sex with men. J Acquir Immune Defic Syndr, 2012, 59, p. 259–265.
39. MONNIER-BENOIT, S., MAUNY, F., RIETHMULLER, D. et al. Immunohistochemical analysis of CD4+ and CD8+ T-cell subsets in high risk human papillomavirus-associated pre-malignant and malignant lesions of the uterine cervix. Gynecologic Oncol, 2006, 102, p. 22–31.
40. NELSON, R. A., LEVINE, A. M., BERNSTEIN, L. et al. Changing patterns of anal canal carcinoma in the United States. J Clin Oncol, 2013, 31, p. 1569–1575.
41. NEMCOVA, J., CERNA, K., ROB, F. et al. Prevalence of high-risk human papillomavirus DNA and mRNA and its association with abnormal anal cytology in the Czech male anal cancer screening cohort. Diagn Cytopathol, 2021, 49, p. 1188–1195.
42. NIELSEN, O. V., JENSEN, S. L. Basal cell carcinoma of the anus – a clinical study of 34 cases. J Br Surg, 1981, 68, p. 856–857.
43. NIGRO, N. D., VAITKEVICIUS, V. K., CONSIDINE, B. Combined therapy for cancer of the anal canal: a preliminary report. Dis Colon Rectum, 1974, 17, p. 354–356.
44. NYITRAY, A. G., NIELSON, C. M., HARRIS, R. B. et al. Prevalence of and risk factors for anal human papillomavirus infection in heterosexual men. J Infect Dis, 2008, 197, p. 1676–1684.
45. NYITRAY, A. G., D SOUZA, G., STIER, E. A. et al. The utility of digital anal rectal examinations in a public health screening program for anal cancer. J Low Genit Tract Dis, 2020, 24, p. 192.
46. PALEFSKY, J. M., BERRY, J. M., JAY, N. et al. A trial of SGN-00101 (HspE7) to treat highgrade anal intraepithelial neoplasia in HIV-positive individuals. Aids, 2006, 20, p. 1151–1155.
47. PATEL, H. S., SILVER, A. R., NORTHOVER, J. M. Anal cancer in renal transplant patients. Int J Colorect Dis, 2007, 22, p. 1–5.
48. PHILLIPS, D. H., HEWER, A., SCHOLEFIELD, J. H. et al. Smoking-related DNA adducts in anal epithelium. Mutat Res, 2004, 560, p. 167–172.
49. RAO, S., GUREN, M. G., KHAN, K. et al. Anal cancer: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann Oncol, 2021, 32, p. 1087–1100.
50. RICHEL, O., PRINS, J. M., DE VRIES, H. J. Screening for anal cancer precursors: what is the learning curve for high-resolution anoscopy? Aids, 2014, 28, p. 1376–1377.
51. ROBERTS, J. R., SIEKAS, L. L., KAZ, A. M. Anal intraepithelial neoplasia: A review of diagnosis and management. World J Gastrointest Oncol, 2007, 9, p. 50.
52. RICHEL, O., WIELAND, U., DE VRIES, H. J. et al. Topical 5-fluorouracil treatment of anal intraepithelial neoplasia in human immunodeficiency virus-positive men. Br J Dermatol, 2010, 163, p. 1301–1307.
53. SAARILAHTI, K., ARPONEN, P., VAALAVIRTA, L. et al. The effect of intensity-modulated radiotherapy and high dose rate brachytherapy on acute and late radiotherapy-related adverse events following chemoradiotherapy of anal cancer. Radiotherapy and Oncology, 2008, 87, p. 383–390.
54. SALATI, S. A., AL KADI, A. Anal cancer–a review. Int J Health Sci, 2012, 6, p. 206.
55. SCHOLEFIELD, J. H., CASTLE, M. T., WATSON, N. F. S. Malignant transformation of high-grade anal intraepithelial neoplasia. J Br Surg, 2005, 92, p. 1133–1136.
56. SENDAGORTA, E., BeERNARDINO, J. I., ALVAREZ - GALLEGO, M. et al. Topical cidofovir to treat high-grade anal intraepithelial neoplasia in HIV-infected patients: a pilot clinical trial. Aids, 2016, 30, p. 75–82.
57. SIMARD, E. P., WATSON, M., SARAIYA, M. et al. Trends in the occurrence of high-grade anal intraepithelial neoplasia in San Francisco: 2000–2009. Cancer, 2013, 119, p. 3539–3545.
58. SINGER, M., MUTCH, M. G. Anal melanoma. Clin Colon Rectal Surg, 2006, 19, p.78–87.
59. SJODAHL, R. I., MYRELID, P., SODERHOLM, J. D. Anal and rectal cancer in Crohn‘s disease. Colorect Dis, 2003, 5, p. 490–495.
60. SNYDER, S. M., SIEKAS, L., ABOULAFIA, D. M. Initial experience with topical fluorouracil for treatment of HIV-associated anal intraepithelial neoplasia. J Int Assoc Phys AIDS Care, 2011, 10, p. 83–88.
61. SOLOMON, D., DAVEY, D., KURMAN, R. et al. The 2001 Bethesda System: terminology for reporting results of cervical cytology. JAMA, 2002, 287, p. 2114–2119.
62. STIER, E. A., CHIAO, E. Y. Anal cancer and anal cancer precursors in women with a history of HPV-related dysplasia and cancer. Semin Colon Rect Surger, 2017, 28, p. 97–101.
63. SWEDISH, K. A., FACTOR, S. H., GOLDSTONE, S. E. Prevention of recurrent high-grade anal neoplasia with quadrivalent human papillomavirus vaccination of men who have sex with men: a nonconcurrent cohort study. Clin Infect Dis, 2012, 54, p. 891–898.
64. TINMOUTH, J., RABOUD, J., ALI, M. et al. The psychological impact of being screened for anal cancer in HIV-infected men who have sex with men. Dis Colon Rect, 2011, 54, p. 352–359.
65. TRUESDALE, M. D., GOLDSTONE, S. E. The fear factor: drivers and barriers to follow-up screening for human papillomavirus-related anal cancer in men who have sex with men. Int J STD & AIDS, 2010, 21, p. 482–488.
66. URONIS, H. E., BENDELL, J. C. Anal cancer: an overview. Oncologist, 2007, 12, p. 524–534.
67. VAN DER SNOEK, E. M., DEN HOLLANDER, J. C., AANS, J. B. et al. Photodynamic therapy with systemic meta-tetrahydroxyphenylchlorin in the treatment of anal intraepithelial neoplasia, grade 3. Lasers Surg Med, 2012, 44, p. 637–644.
68. VAN DER ZEE, R. P., RICHEL, O., VAN NOESEL, C. J. M. et al. Host Cell Deoxyribonucleic Acid Methylation Markers for the Detection of High-grade Anal Intraepithelial Neoplasia and Anal Cancer. Clin Infect Dis, 2019, 68, p. 1110–1117.
69. WEIS, S. E., VECINO, I., POGODA, J. M. et al. Prevalence of anal intraepithelial neoplasia defined by anal cytology screening and high-resolution anoscopy in a primary care population of HIVinfected men and women. Dis Colon Rectum, 2011, 54, p. 433–441.
70. WELBOURN, H., DUTHIE, G., POWELL, J. et al. Can photodynamic therapy be the preferred treatment option for anal intraepithelial neoplasia? Initial results of a pilot study. Photodiagn Photodyn Ther, 2014, 11, p. 20–21.
71. WILKIN, T. J., CHEN, H., CESPEDES, M. S. et al. A randomized, placebo-controlled trial of the quadrivalent human papillomavirus vaccine in human immunodeficiency virus-infected adults aged 27 years or older: AIDS Clinical Trials Group Protocol A5298. Clin Infect Dis, 2018, 67, p. 1339 – 1346.
72. WILLEMS, N., LIBOIS, A., NKUIZE, M. et al. Treatment of anal dysplasia in HIV-positive men who have sex with men in a large AIDS reference centre. Acta Clin Belg, 2017, 72, p. 29–35.
73. ZÁKOUCKÁ, H. Sexuálně přenosné infekce – moderní přístup k diagnostice – část I. Dermatol. Praxi, 2020, 14(1), p. 10–16.
Štítky
Dermatologie Dětská dermatologie
Článek vyšel v časopiseČesko-slovenská dermatologie
Nejčtenější tento týden
2022 Číslo 1- Takrolimus v terapii atopické dermatitidy a analýza jeho nákladové efektivity ve srovnání s kortikosteroidní léčbou
- Daivobet gel – lékový profil
- Fixní kombinace kalcipotriol/betamethason v topické léčbě psoriázy
- Psoriáza a kouření – vzájemně se potencující rizika?
Nejčtenější v tomto čísle- Diskoidní lupus erythematosus víček. Popis případu
- Anální karcinom a jeho screening
- Lineární hyperpigmentace levé pektorální krajiny a linea alba. Stručný přehled
- Síťovitá makula
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Revma Focus: Spondyloartritidy
nový kurz
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Autoři: prof. MUDr. Pavel Horák, CSc., doc. MUDr. Ludmila Brunerová, Ph.D., doc. MUDr. Václav Vyskočil, Ph.D., prim. MUDr. Richard Pikner, Ph.D., MUDr. Olga Růžičková, MUDr. Jan Rosa, prof. MUDr. Vladimír Palička, CSc., Dr.h.c.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



