-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Srovnání lidského choriového gonadotropinu (Pregnyl 10 000 IU i.m.) s GnRH agonistou (triptorelin 0,2 mg s.c.) pro maturaci oocytů u stejných dárkyň vajíček – klinické a embryologické charakteristiky
Comparison of human chorionic gonadotropin (Pregnyl 10 000 IU i.m.) versus GnRH agonist (triptorelin 0,2 mg s.c.) for final oocytes maturation in the same egg donors – clinical and embryological characteristics
Objective:
To compare clinical and embryological characteristics in donor cycles triggered for final oocytes maturation with Pregnyl 10 000 IU i.m. versus triptorelin 0.2 mg s.c. in the same patients in two sequential stimulation cycles. The aim of the study is to decrease the risk of the development of ovarian hyperstimulation syndrome (OHSS) at high response donors by the replacement of Pregnyl 10 000 IU i.m. vs. triptorelin 0.2 mg s.c. The administration of a single dose of gonadotropin-releasing hormone agonist (triptorelin 0.2 mg s.c.) induces release of LH from the pituitary gland similarly to a spontaneous LH surge.Subject:
Prospective cross-over trial.Setting:
Sanatorium Pronatal, Praha.Subject and method:
From August 2009 to July 2010 we analysed 24 stimulation cycles in 12 egg donors treated with GnRH antagonist protocol with recombinant FSH (follitropin beta). We identified patients with more than 15 follicles during examination by transvaginal ultrasound. When at least 3 leading follicles reached 17 mm in diameter we administrated Pregnyl 10 000 IU i.m. for final oocytes maturation and triptorelin 0.2 mg s.c in the subsequent treatment cycle.Results:
The primary outcome measure was number of oocytes, proportion mature oocytes and fertilized oocytes. The secondary outcome were duration of FSH stimulation, total dose of gonadotropins and mean daily dose of gonadotropins. Data was analysed by paired t-test. We retrieved 17,2 ± 8,6 vs. 15,8 ± 5,3 (ns) oocytes, 12,6 ± 7,3 vs. 13,0 ± 5,4 (ns) metaphase II oocytes, proportion of metaphase II oocytes (%) was 73 vs. 83 (ns), number of fertilized oocytes 11,5 ± 6,7 vs. 11,7 ± 4,5 (ns), fertilization rate (%) 91 vs. 90 (ns) in Pregnyl’s vs. triptorelin’s group, resp. Duration of FSH stimulation (days) 12,2 ± 0,8 vs. 12,4 ± 0,7 (ns), total dose of gonadotropins (IU) 1744 ± 277 vs. 1740 ± 276 (ns), mean daily dose of gonadotropins (IU) 238 ± 43 vs. 221 ± 36 (ns), were not statistically different in both groups.Conclusions:
Number of mature oocytes and subsequent embryonic cleavage is comparable to standard hCG treatment. There are no differences in clinical and embryological characteristics in both groups. Only one patient with administration of Pregnyl 10 000 IU i.m. was treated for OHSS grade II by vaginal paracentesis. Administration of triptorelin 0,2 mg s.c. is a safe and effective approach to achieve mature oocytes in egg donation programme, where we do not take care of implantation, which has got some limitations based on several studies.Key words:
egg donation, in vitro fertilization, ICSI, hCG, Pregnyl, GnRH agonist, triptorelin, oocyte maturation.
Autoři: R. Středa 1,2,3,4; Tonko Mardešič 1,2; V. Sobotka 1,2; D. Koryntová 2; L. Hybnerová 2; M. Jindra 2; V. Paseková 1; J. Slámová 1; M. Števíková 1; J. Vobořil 1; L. Jelínková 1; Š. Vilímová 1; J. Ichová 1; J. Mádrová 1; H. Teršová 1; M. Mašata 1; J. Sobotková 3,4
Působiště autorů: Sanatorium Pronatal, Praha, vedoucí lékař doc. MUDr. T. Mardešič, CSc. 1; Pronatal Plus s. r. o., Praha, vedoucí lékařka MUDr. D. Koryntová, CSc. 2; Porodnicko-gynekologická klinika, Pardubická krajská nemocnice a. s., přednosta doc. MUDr. M. Košťál, CSc. 3; Fakulta zdravotnických studií, Univerzita Pardubice 4
Vyšlo v časopise: Ceska Gynekol 2011; 76(2): 113-118
Souhrn
Cíl:
Srovnat klinické a embryologické charakteristiky v cyklech darovaných vajíček s maturací oocytů po aplikaci lidského choriového gonadotropinu (hCG) Pregnyl 10 000 IU i.m. vs. triptorelin 0,2 mg s.c. u stejných žen ve dvou následných stimulačních cyklech. Cílem studie je snížit riziko rozvoje ovariálního hyperstimulačního syndromu (OHSS) u dárkyň vajíček s velkou ovariální odpovědí náhradou Pregnylu 10 000 IU i.m. triptorelinem 0,2 mg s.c. Podání jedné dávky GnRH agonisty (triptorelin 0,2 mg s.c.) indukuje uvolnění LH z hypofýzy podobně jako spontánní LH vrchol.Typ studie:
Prospektivní cross-over studie.Název a sídlo pracoviště:
Sanatorium Pronatal, Praha.Předmět a metoda:
Od srpna 2009 do července 2010 jsme analyzovali 24 stimulačních cyklů u 12 dárkyň vajíček připravovaných GnRH antagonistickým protokolem s rekombinantním FSH (follitropin beta). Identifikovali jsme dárkyně s více než 15 folikuly u ultrazvukového vyšetření, a pokud alespoň 3 folikuly dosáhly 17 mm v průměru, aplikovali jsme pro maturaci oocytů Pregnyl 10 000 IU i.m. a v následném cyklu triptorelin 0,2 mg s.c.Výsledky:
Primárním cílem byl počet oocytů, zastoupení zralých (MII) oocytů, počet a zastoupení fertilizovaných oocytů. Sekundárním cílem bylo trvání FSH stimulace, celková dávka gonadotropinů a průměrná denní dávka gonadotropinů. Data jsme analyzovali párovým t-testem. Získali jsme 17,2 ± 8,6 vs. 15,8 ± 5,3 (ns) vajíček, 12,6 ± 7,3 vs. 13,0 ± 5,4 (ns) oocytů v metafázi II. zracího dělení (MII), zastoupení M II oocytů (%) bylo 73 vs. 83 (ns), počet fertilizovaných oocytů 11,5 ± 6,7 vs. 11,7 ± 4,5 (ns), fertilization rate (%) 91 vs. 90 (ns) ve skupině Pregnyl vs. triptorelin, resp. Trvání FSH stimulace (dny) 12,2 ± 0,8 vs. 12,4 ± 0,7 (ns), celková dávka gonadotropinů (IU) 1744 ± 277 vs. 1740 ± 276 (ns), průměrná denní dávka gonadotropinů (IU) 238 ± 43 vs. 221 ± 36 (ns), nebyla statisticky odlišná u obou skupin.Závěr:
Počet zralých (MII) oocytů a následně embryologický vývoj je srovnatelný se skupinou Pregnyl. Neprokázali jsme odlišnosti ani v klinických, ani v embryologických charakteristikách při porovnání obou souborů. Pouze 1 pacientka s Pregnylem podstoupila ambulantně paracentézu pro OHSS II. st. Aplikace triptorelinu 0,2 mg s.c. je bezpečný a účinný přístup k dosažení zralých oocytů v programu darování vajíček, kde náš zájem není zaměřen na implantaci, kde na základě několika studií existují jistá omezení.Klíčová slova:
darování vajíček, mimotělní oplodnění, ICSI, hCG, Pregnyl, GnRH agonista, triptorelin, maturace oocytů.ÚVOD
Na celém světě v souvislosti s léčbou neplodnosti vzrůstá potřeba darovaných vajíček [15, 16]. Indikací pro program darování oocytu jsou genetická onemocnění (např. Turnerův syndrom), ageneze vaječníku, syndrom předčasného ovariálního selhání, stav po chirurgických zákrocích na vaječníku (např. endometrióza), úplné odstranění vaječníku (např. pro cystu nebo tumor) nebo pokročilý reprodukční věk. Receptivitu endometria pro implantaci embrya zajišťujeme hormonální substituční léčbou i u žen nad 40 let [18]. Hormonální stimulaci dárkyně realizujeme v časovém souladu s hormonální přípravou sliznice příjemkyně. Po odběru vajíček dárkyně a oplození vajíček spermiemi partnera příjemkyně metodou ICSI probíhá v laboratorních podmínkách kontrola vývoje embryí a výběr embryí k transferu v rámci prodloužené kultivace (4.–5. den, stadium moruly nebo blastocysty). Správně realizovaný program nabízí poté příjemkyním při transferu 2 blastocyst očekávanou úspěšnost 50–60 %. Hormonální suplementace příjemkyně probíhá i dále v těhotenství do ukončení prvního trimestru.
Přes snahu o minimální stimulaci dárkyně zůstává reálným rizikem rozvoj ovariálního hyperstimulačního syndromu (OHSS). Cílem naší práce je minimalizovat toto riziko u dárkyň s velkou ovariální odpovědí (více než 15 folikulů) náhradou Pregnylu 10 000 IU i.m. triptorelinem 0,2 mg s.c. Podání jedné dávky GnRH agonisty (triptorelin 0,2 mg s.c.) indukuje uvolnění LH z hypofýzy podobně jako spontánní LH vrchol a vede k maturaci oocytů (dokončení I. zracího dělení a zástava vývoje oocytů v metafázi II. zracího dělení). Cílem studie je srovnat klinické a embryologické charakteristiky v cyklech darovaných vajíček s maturací oocytů po aplikaci Pregnylu 10 000 IU i.m. vs. triptorelin 0,2 mg s.c. u stejných žen ve dvou následných stimulačních cyklech.
CÍL STUDIE
Primárním cílem je počet oocytů, zastoupení zralých (MII) oocytů, počet a zastoupení fertilizovaných oocytů.
Sekundárním cílem je trvání FSH stimulace, celková spotřeba FSH a průměrná denní dávka FSH.
TYP STUDIE A STATISTICKÁ ANALÝZA
Realizovali jsme prospektivní cross-over studii. Data jsme analyzovali párovým t-testem. Hladina významnosti alfa 0,05 (p<0,05) je považována za statisticky významnou. Statisticky nevýznamná data – ns.
MATERIÁL A METODA
Od srpna 2009 do července 2010 jsme analyzovali 24 stimulačních cyklů u 12 dárkyň vajíček připravovaných GnRH antagonistickým protokolem s rekombinantním FSH (folitropin beta).
Vstupní kritéria
- Způsobilost pro darování vajíček podle zákona č. 422/2008 Sb. (genetické vyšetření, věk 18 až 35 let, informovaný souhlas, vyloučení všech sexuálně přenosných chorob aj.).
- Anamnesticky již realizovaný cyklus darování oocytů s aplikací Pregnylu 10 000 IU i.m.
- 15 a více folikulů při ultrazvukovém vyšetření.
Průběh studie
- Vysvětlili jsme cíle a metodu studie, podepsali jsme informovaný souhlas.
- Definovali jsme skupinu dárkyň A, která měla na dřívější ovariální stimulaci s aplikací Pregnylu 10 000 IU tvorbu 15 a více folikulů.
- Ultrazvukovým vyšetřením před aplikací gonadotropinů jsme vyloučili ovariální cysty.
- Určili jsme počáteční dávku FSH na základě antral follicle count (AFC), velikosti vaječníků a znalosti odpovědi na předchozí ovariální stimulaci (150–300 IU denně, obvykle 225 IU).
- Folikulární vývoj jsme monitorovali ultrazvukovým vyšetřením 7. a 9. den menstruačního cyklu.
- Při průkazu 15 a více folikulů jsme dárkyně zařadili do skupiny B triptorelin 0,2 mg s.c.
- Triptorelin 0,2 mg s.c. jsme aplikovali při dosažení průměru 17 mm u nejméně 3 folikulů.
- Odběr oocytů za 36 hod, intracytoplazmatická injekce spermií do vajíčka (ICSI).
- Hodnocení fertilizace.
VÝSLEDKY
Embryologické charakteristiky a charakteristiky cyklů jsou uspořádány v tabulkách 1 a 2.
Tab. 1. Embryologické charakteristiky 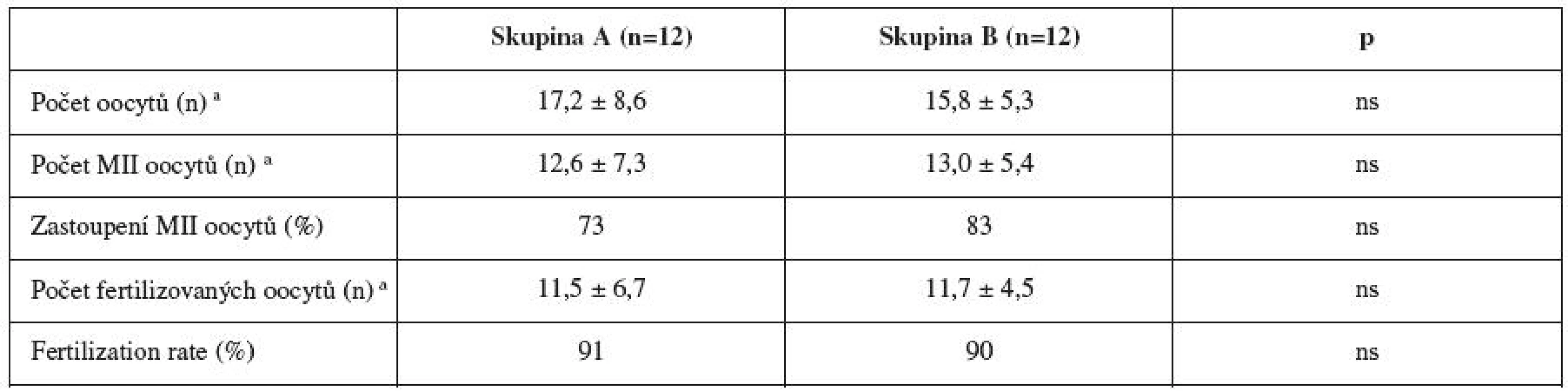
a Výsledky jsou vyjádřeny jako průměr ± SD, párový t-test Tab. 2. Charakteristiky cyklů 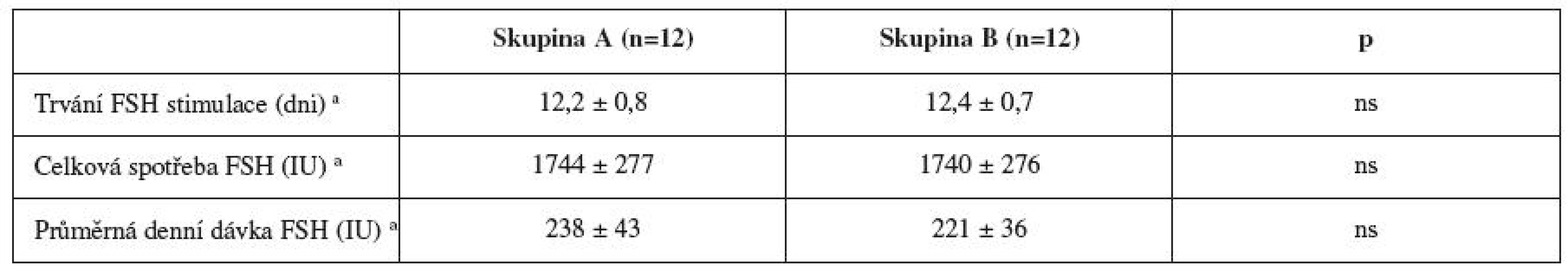
a Výsledky jsou vyjádřeny jako průměr ± SD, párový t-test Grafické znázornění výsledků přinášejí grafy 1–6.
Graf 2. Zastoupení M II oocytů 
Graf 3. Počet fertilizovaných oocytů 
Graf 5. Celková dávka gonadotropinů 
Graf 6. Průměrná denní dávka gonadotropinů 
Neprokázali jsme odlišnosti při porovnání charakteristik obou skupin.
OHSS I. stupně jsme zaznamenali jen u jedné dárkyně po aplikaci Pregnylu 10 000 IU i.m. Klidový a pitný režim společně s ambulantní paracentézou vedl k vyřešení komplikace. V následném cyklu s aplikací triptorelinu 0,2 mg s.c. se v souladu s literálními údaji OHSS již neprojevil.
DISKUSE
Aplikace lidského choriového gonadotropinu (hCG) ke konečnému dozrání vajíček je stále standardem pro ukončení indukce ovulace [7]. Je charakterizována delším biologickým poločasem hormonu (> 24 hod versus 60 min pro LH), pevnější a delší vazbou na granulózové buňky folikulů oproti endogennímu ovulačnímu LH vrcholu [9, 12]. Takto navozený dlouhotrvající luteotropní efekt (vývoj mnohočetných žlutých tělísek a dosažení vysokých hladin estradiolu a progesteronu) dále vede k uvolnění mediátorů (např. VEGF, IL-2 apod.) a ke komplexnímu účinku na organismus (např. zvýšení permeability cév apod.), který může být příčinou rozvoje OHSS.
Aplikace bolusu GnRH agonisty indukuje uvolnění LH z hypofýzy podobně jako spontánní LH vrchol. Hladiny LH v průběhu dvou hodin prudce stoupají, čtyři hodiny dosahují maxima a dále klesají, hladina FSH mají podobný průběh [12, 13]. Kol et al. [13] prokázal významně nízkou hladinu progesteronu v porovnání s aplikaci hCG, a tím luteolytický účinek.
GnRH agonista triptorelin je léčivý přípravek, který vznikl náhradou aminokyseliny Gly na pozici 6 Trp přirozeného hormonu [9]. Při použití aplikace triptorelinu 0,2 mg s.c. Kol et al. [13] prokázal 100% spolehlivost konečné maturace oocytů u 1200 žen bez zaznamenání případu ovariálního hyperstimulačního syndromu.
GnRH antagonistický protokol zajišťuje kvalitu vajíček prevencí předčasného uvolnění LH, čehož se dosahuje kompetitivní vazbou GnRH antagonisty na receptory hypofýzy. Tento protokol, byť v kombinaci hCG, významně snižuje riziko rozvoje OHSS v porovnání s dlouhým GnRH agonistickým protokolem [9, 10, 20]. Přes účinek GnRH antagonisty zůstává hypofýza citlivá na podání GnRH agonisty v obvyklých dávkách. Byl prokázán spolehlivý účinek GnRH agonisty na uvolnění LH i v tomto protokolu a dosažení konečné maturace ooocytů [7, 12] a díky již zmíněnému luteolytickému účinku předchází rozvoji OHSS [13]. Itskovitz [12] v roce 2000 studoval 8 žen s více než 20 folikuly (vysoce riziková skupina z rozvoje OHSS), u kterých podal triptorelin 0,2 mg s.c. a měřil hladiny LH, FSH, progesteronu a estradiolu před aplikací, za 0,5, 1, 2, 4, 8 hodin a v den punkce folikulů. Prokázal tak sérové hladiny LH (IU/l) 2,4, 12,7, 14,3, 73,7, 219, 71 a 7,9 resp.; FSH (IU/l) 5,4, 5,6, 5,7, 8,1, 18,6, 16,4 a 5,7 resp., progesteronu (ng/ml) 1, 1,2, 1,4, 2,2, 4,5, 8,7 a 9,7 resp., estradiolu (pg/ml) 4775, 4630, 4505, 5080, 5540, 6000 a 2375 resp. Získal průměrně 23,4 ± 15,4 oocytů a 83 % oocytů bylo ve fázi MII. Itskovitz potvrdil, že jednorázová aplikace triptorelinu 0,2 mg vede k adekvátnímu uvolnění LH v GnRH antagonistickém protokolu.
Fauser [7] v roce 2002 publikoval výsledky studie, kdy u GnRH antagonistického protokolu randomizovaně podal hCG, triptorelin 0,2 mg a další GnRH analog leuprorelin ve skupinách 17, 15 a 15 žen resp. U triptorelinu 0,2 mg potvrdil LH vrchol 130 ± 60 IU/l dosažený po 4 hodinách vs. od 0,9 do 107 ± 55 u leuprorelinu (p< 0,001). Oproti tomu byl ve skupině hCG nárůst hormonu postupný, vysoká hladina byla prokázána ještě 10 dní po aplikaci a návrat k hladinám 5 ± 1,6 IU/l až 1 týden po embryotransferu. Počet oocytů byl 9,8 ± 5,4, 8,7 ± 4,5 a 8,3 ± 3,3 resp., zastoupení MII oocytů 72, 85 a 86 % a fertilizace 61, 62 a 56 % resp.
Griesinger v metaanalýze [11] v roce 2006 shrnuje uplatnění aplikace GnRH agonisty k dosažení konečné maturace oocytů v GnRH antagonistickém protokolu. Studoval v souhrnu 275 randomizovaných subjektů a potvrdil statisticky nevýznamné rozdíly mezi oběma skupinami v počtu vajíček, zastoupení MII oocytů, fertilization rate a kvalitě embryí.
V programu darování vajíček i v programu léčby neplodnosti metodou IVF/ICSI se právě aplikace triptorelinu 0,2 mg s.c. stala dominantně používaným postupem (2 ze 3 randomizovaných studií v programu darování vajíček [8, 17, 19] a 4 z 5 randomizovaných studií v programu léčby neplodnosti metodou IVF/ICSI [1, 2, 6, 7, 14]).
V roce 2007 v rozsáhlé retrospektivní studii [3] Bodri et al. shrnul své zkušenosti u 1170 dárkyň vajíček. Porovnával aplikaci rekombinantního lidského choriového gonadotropinu (rhCG) vs. triptorelinu 0,2 mg, oba s.c. Zastoupení MII oocytů bylo srovnatelné, ale prokázal se statistický rozdíl ve fertilization rate 65 % vs. 69 %, resp. - vyšší po aplikaci GnRH analoga. Incidence OHSS středního/těžkého průběhu byl 1,26 % (13 žen z 1031) vs. 0 % (0 žen z 1046), resp. vyšší po aplikaci rhCG. Výsledky těhotenského indexu u příjemkyň byly srovnatelné.
První randomizovanou studii porovnávající aplikaci rhCG a triptorelinu 0,2 mg přinesl Galindo [8] v roce 2009. V souborech 106 žen prokázal 8,0 ± 4,6 vs. 7,5 ± 4,1 MII oocytů, zastoupení MII oocytů 67 vs. 67 %, fertilization rate 67 % vs. 71 % i klinická těhotenství - vše srovnatelné. OHSS byl pozorován u 9 žen po aplikaci rhCG vs. 0 žen resp.
Další randomizovanou práci publikoval Melo [17] také v roce 2009. Srovnával embryologické charakteristiky a riziko vzniku OHSS u 100 dárkyň v každé skupině (rhCG a triptorelin 0,2 mg). Embryologické charakteristiky byly u obou skupiny shodné, riziko OHSS bylo prokázáno po aplikaci rhCG vs. triptorelin 0,2 mg.
Porovnání účinku hCG a leuprolidu acetátu u 44 stejných dárkyň ve dvou následných stimulačních cyklech v randomizované studii publikoval Sismanogolu [19]. Prokázal délku aplikace FSH 10 ± 1 den vs. 10 ± 0,8 dne, počet oocytů 36 ± 11 vs. 38 ± 14, zastoupení MII oocytů 79 % vs. 81 %, fertilization rate 73 vs. 75 % - výsledky statisticky shodné pro obě skupiny. Dále sledoval projev OHSS středního stupně u 3 žen (6,8 %) vs. 0 (0 %), resp. - vyšší riziko OHSS ve skupině hCG.
V prevenci rozvoje OHSS Brodi [4] v roce 2010 publikoval své zkušenosti s aplikací triptorelinu 0,2 mg u 102 dárkyň s vysokým rizikem rozvoje OHSS (více než 20 folikulů, E2 ≥ 4000 pg/ml a s více než 20 získanými oocyty). Průměrný počet punktovaných folikulů byl 25 ± 6, počet MII oocytů 19 ± 7, průměrná dávka FSH 203 ± 35, délka aplikace FSH 10 ± 1 den a celková spotřeba FSH 1983 ± 476 IU. U žádné dárkyně ve studii nebyl prokázán rozvoj OHSS.
Omezení pilotní fáze studie je dáno velikostí souboru. Na základě této velikosti souboru není statistické hodnocení výsledků signifikantně významné.
ZÁVĚR
Počet zralých (MII) oocytů a následně embryologický vývoj je srovnatelný se skupinou Pregnyl.
Neprokázali jsme odlišnosti ani v embryologických, ani v klinických charakteristikách při porovnání obou souborů.
Pouze 1 pacientka s Pregnylem podstoupila ambulantně paracentézu pro OHSS II. st.
Aplikace triptorelinu 0,2 mg s.c. je bezpečný a účinný přístup k získání zralých oocytů v programu darování vajíček, kde náš zájem není zaměřen na implantaci, kde na základě několika studií existují jistá omezení.
MUDr. Robert Středa
Sanatorium Pronatal
Na Dlouhé mezi 4/12
147 00 Praha-Hodkovičky
rstreda@seznam.cz
Zdroje
1. Acevedo, B., Gomez-Palomares, JL., Ricciarelli, E., Hernandez, ER. Triggering ovulation with gonadotropin-releasing hormone agonists does not compromise embryo implantation rates. Fertil Steril, 2006, 86, p. 1682-1687.
2. Beckers, NG., Macklon, NS., Eijkemans, MJ., et al. Nonsupplemented luteal phase characteristics after the administration of recombinant human chorionic gonadotropin, recombinant luteinizing hormone, or gonadotropin-releasing hormone (GnRH) agonist to induce final oocyte maturation in in vitro fertilization patients after ovarian stimulation with recombinant follicle-stimulating hormone and GnRH antagonist cotreatment. J Clin Endocrinol Metab, 2003, 88, p. 4186-4192.
3. Bodri, D., Guillen, JJ., Galindo, A., et al. Triggering with human chorionic gonadotropin or a gonadotropin-releasing hormone agonist in gonadotropin-releasing hormone antagonist-treated oocyte donor cycles: findings of a large retrospective cohort study. Fertil Steril, 2009, 91, p. 365-371.
4. Bodri, D., Guillen, JJ., Trullenque, M., et al. Early ovarian hyperstimulation syndrome is completely prevented by gonadotropin releasing-hormone agonist triggering in high-risk oocyte donor cycles: a prospective, luteal-phase follow-up study. Fertil Steril, 2010, 93, p. 2418-2420.
5. Brinsden, PR. A textbook of in vitro fertilization and assisted reproduction. New York: Parthenon Publishing, 1999, p. 257-265.
6. Engmann, L., DiLuigi, A., Schmidt, D., et al. The use of gonadotropin-releasing hormone (GnRH) agonist to induce oocyte maturation after cotreatment with GnRH antagonist in high-risk patients undergoing in vitro fertilization prevents the risk of ovarian hyperstimulation syndrome: a prospective randomized controlled study. Fertil Steril, 2008, 89, p. 84-91.
7. Fauser, BC., de Jong, D., Olivennes, F., et al. Endocrine profiles after triggering of final oocyte maturation with GnRH agonist after cotreatment with the GnRH antagonist ganirelix during ovarian hyperstimulation for in vitro fertilization. J Clin Endocrinol Metab, 2002, 87, p. 709-715.
8. Galindo, A., Bodri, D., Guillen, JJ., et al. Triggering with HCG or GnRH agonist in GnRH antagonist treated oocyte donation cycles: a randomised clinical trial. Gynecol Endocrinol, 2009, 25, p. 60-66.
9. Gardner, DK., Weissman, A., Howles, CM., Shoham, Z. Textbook of assisted reproductive techniques, 1st edition, London: Martin Dunitz, 2001, p. 484-491, 645-654.
10. Griesinger, G., Felberbaum, R., Diedrich, K. GnRH-antagonists in reproductive medicine. Arch Gynecol Obstet, 2005, 273, p. 71-78.
11. Griesinger, G., Diedrich, K., Devroey, P., Kolibianakis, EM. GnRH agonist for triggering final oocyte maturation in the GnRH antagonist ovarian hyperstimulation protocol: a systematic review and meta-analysis. Hum Reprod Update, 2006, 12, p. 159-168.
12. Itskovitz-Eldor, J., Kol, S., Mannaerts, B. Use of a single bolus of GnRH agonist triptorelin to trigger ovulation after GnRH antagonist ganirelix treatment in women undergoing ovarian stimulation for assisted reproduction, with special reference to the prevention of ovarian hyperstimulation syndrome: preliminary report: short communication. Hum Reprod, 2000, 15, p. 1965‑1968.
13. Kol, S. Luteolysis induced by a gonadotropin-releasing hormone agonist is the key to prevention of ovarian hyperstimulation syndrome. Fertil Steril, 2004, 81, p. 1-5.
14. Kolibianakis, EM., Schultze-Mosgau, A., Schroer, A., et al. A lower ongoing pregnancy rate can be expected when GnRH agonist is used for triggering final oocyte maturation instead of HCG in patients undergoing IVF with GnRH antagonists. Hum Reprod, 2005, 20, p. 2887-2892.
15. Koryntova, D., Jelinkova, L., Rezabek, K., Zivny, J. Asistovaná reprodukce - současný stav a perspektivy. Čes Gynekol, 1999, 64, s. 383-388.
16. Mardesic, T. Indikace a výsledky léčby sterility metodami asistované reprodukce. Mod Gynek Porod 2002, 11, s. 565-571.
17. Melo, M., Busso, CE., Bellver, J., et al. GnRH agonist versus recombinant hCG in an oocyte donation programme: a randomized, prospective, controlled, assessor-blind study. Reprod Biomed Online, 2009, 19, p. 486-492.
18. Sauer, MV., Paulson, RJ., Lobo, RA. A preliminary report on oocyte donation extending reproductive potential to women over 40. N Engl J Med, 1990, 323, p. 1157-1160.
19. Sismanoglu, A., Tekin, HI., Erden, HF., et al. Ovulation triggering with GnRH agonist vs. hCG in the same egg donor population undergoing donor oocyte cycles with GnRH antagonist: a prospective randomized cross-over trial. J Assist Reprod Genet, 2009, 26, p. 251-256.
20. Tarlatzis, BC., Fauser, BC., Kolibianakis, EM., et al. GnRH antagonists in ovarian stimulation for IVF. Hum Reprod Update, 2006, 12, p. 333-340.
Štítky
Dětská gynekologie Gynekologie a porodnictví Reprodukční medicína
Článek Možnosti a výsledky preimplantační genetické diagnostiky (PGD) u párů s chromozomální translokacíČlánek Prokázané klinické účinky rekombinantních gonadotropinů v porovnání s urinárními v indukci ovulaceČlánek EditorialČlánek Děložní myomy a jejich léčbaČlánek Screening kolorektálního karcinomu v ordinaci praktického gynekologa – který test je ten pravý?
Článek vyšel v časopiseČeská gynekologie
Nejčtenější tento týden
2011 Číslo 2- Aktuální doporučení pro diagnostiku von Willebrandovy choroby
- Postabortivní syndrom – symptomy, dopady a možnosti léčby
- Trombóza portální žíly jako komplikace infekce COVID-19 – kazuistika
- Romosozumab zlepšuje kostní mikroarchitekturu u postmenopauzálních žen s osteoporózou
- S MUDr. Janem Rosou o problematice osteoporózy u revmatologických pacientů: Kdy začít s osteoanaboliky a jak minimalizovat selhání léčby?
-
Všechny články tohoto čísla
- Možnosti a výsledky preimplantační genetické diagnostiky (PGD) u párů s chromozomální translokací
- Luteální podpora v programu IVF/ET
- Prokázané klinické účinky rekombinantních gonadotropinů v porovnání s urinárními v indukci ovulace
- Srovnání lidského choriového gonadotropinu (Pregnyl 10 000 IU i.m.) s GnRH agonistou (triptorelin 0,2 mg s.c.) pro maturaci oocytů u stejných dárkyň vajíček – klinické a embryologické charakteristiky
- Prodloužená kultivace embryí při IVF nezvyšuje naději na otěhotnění
- Do jaké míry je rozvoj ovariálního hyperstimulačního syndromu v přímé souvislosti se syndromem polycystických ovarií u IVF pacientek podstupujících řízenou hyperstimulaci ovarií?
- Využití a význam 3D ultrasonografického vyšetření v asistované reprodukci
- Vybrané markery v skorej predikcii preeklampsie
- Význam konzultace při výběru kombinované hormonální antikoncepce – výsledky projektu CHOICE (Contraception Health Research Of Informed Choice Experience) v České a Slovenské republice
- Prevalence žen s hyperaktivním močovým měchýřem v České republice
- Děložní myomy a jejich léčba
- Screening kolorektálního karcinomu v ordinaci praktického gynekologa – který test je ten pravý?
- Spontánna ruptúra uterinných ciev počas gravidity u pacientky s predchádzajúcou endometriózou
- Zemřel prof. MUDr. Otakar Nyklíček, DrSc. FIAC (em.)
- Reprodukční imunologie ve světě
- XXXIX. globální kongres minimálně invazivní gynekologie Las Vegas, USA
- CELOSTÁTNÍ KONFERENCE Sdružení soukromých gynekologů ČR a České gynekologické a porodnické společnosti ČLS JEP
- Editorial
- Snížená plodnost a současné možnosti vyšetřování v reprodukční imunologii
- Onkofertilita – nový směr reprodukční medicíny
- Česká gynekologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Prodloužená kultivace embryí při IVF nezvyšuje naději na otěhotnění
- Děložní myomy a jejich léčba
- Luteální podpora v programu IVF/ET
- Snížená plodnost a současné možnosti vyšetřování v reprodukční imunologii
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání





